Efeitos do tratamento com Hidrogel na cicatrização de úlceras
venosas de membros inferiores: Revisão Sistemática
Cibele Teresinha Dias Ribeiro
Natal
PROGRAMA DE PÓS-GRADUAÇÃO EM FISIOTERAPIA
Efeitos do tratamento com Hidrogel na cicatrização de úlceras
venosas de membros inferiores: Revisão Sistemática
Cibele Teresinha Dias Ribeiro
Dissertação apresentada à Universidade
Federal do Rio Grande do Norte –
Programa de pós-graduação em
Fisioterapia, para a obtenção do
título de Mestre em Fisioterapia.
Orientador: Guilherme A. F. Fregonezi
Universidade Federal do Paraná
Sistema de Bibliotecas
Ribeiro, Cibele Teresinha Dias
Efeitos do tratamento com Hidrogel na cicatrização de úlceras venosas de
membros inferiores: revisão sistemática. / Cibele Teresinha Dias Ribeiro. –
Natal, 2014.
96f: il.; 30cm.
Orientador: Guilherme Augusto de Freitas Fregonezi
Dissertação (Mestrado) – Programa de Pós-Graduação em Fisioterapia.
Centro de Ciências da Saúde. Universidade Federal do Rio Grande do Norte.
1. Úlcera venosa. 2. Insuficiência venosa. 3.
Hidrogel. I. Título II.
Fregonezi, Guilherme Augusto de Freitas. III Universidade Federal do Rio
Grande do Norte. Centro de Ciências da Saúde. Programa de
Pós-Graduação em Fisioterapia.
iii
PROGRAMA DE PÓS-GRADUAÇÃO EM FISIOTERAPIA
Coordenador do Programa de Pós-Graduação em Fisioterapia:
iv
Efeitos do tratamento com Hidrogel na cicatrização de úlceras
venosas de membros inferiores: Revisão Sistemática
BANCA EXAMINADORA
Prof. Dr. Guilherme Augusto Freitas Fregonezi Presidente - UFRN
Prof. Drª Selma Sousa Bruno UFRN – Membro Interno
Prof. Drª Andrea Lemos Bezerra de Oliveira UFPE – Membro externo
Ao meu esposo, Fernando e a minha filha Bianca.
vi
Inicialmente quero agradecer a Deus e a minha família por me amparar nos
momentos difíceis, me dar força interior para superar as dificuldades, me mostrar o
caminho certo nas horas incertas e me suprir em todas as minhas necessidades.
Aos meus pais, pela educação, pelos valores, pelo que sou hoje. Ao meu pai, que
tenho certeza estar comemorando comigo mais esta vitória. De onde você estiver,
pai, agradeço tudo o que fez por mim e por ter mostrado a todos que viver vale a
pena e temos que lutar até os últimos segundos de nossas vidas pelo e por quem
mais amamos!! A minha mãe, amor incondicional, por sempre me apoiar, ajudar em
todos os momentos e estar presente nos momentos mais especiais e importantes da
minha vida. A todos os familiares, em especial a minhas irmãs, Danielle e Franciele,
as quais sempre estiveram ao meu lado, me apoiando e que, apesar da distância,
nossa união e cumplicidade sempre estiveram presentes. A minha tia Solange, que
teve uma participação especial na minha educação como minha professora também.
Ao meu professor mais especial, esposo, companheiro, amigo, meu “porto
seguro”, Fernando Dias, obrigada por tudo! Agradeço por toda a sua paciência em
sempre estar pronto a passar o seu conhecimento de maneira clara e com
entusiasmo. Você é um exemplo de professor e pesquisador. São admiráveis a sua
dedicação ao ensino e a forma como contagia a todos a também querer aprender
cada vez mais. E a minha filha Bianca, que é a razão da minha vida.
Agradeço ao Professor Guilherme Fregonezi, pela orientação. Obrigada pelas
oportunidades oferecidas pelo senhor antes mesmo de iniciar o mestrado e pelos
ensinamentos que foram fundamentais durante todo esse tempo.
vii
essenciais para a realização desta revisão, pois sempre responderam aos meus
e-mails prontamente, resolvendo minhas dúvidas e enviando sugestões.
A todos os colegas de mestrado, principalmente a Fernando Macedo, que nos
deixou tão inesperadamente, mas que tive a oportunidade de conhecer melhor no
laboratório 6, ajudando-o nos pilotos do projeto por ele desenvolvido. Que você
esteja em paz!
A todos os amigos que faziam e ainda fazem parte do laboratório 6, pelo
convívio e aprendizagem.
As pessoas especiais que sempre serão lembradas durante o período no qual
vivi em Natal: à professora e amiga Vanessa Resqueti, pela amizade, por todos os
momentos juntas, principalmente os de convívio familiar; à Diana Freitas e Gabriela
Chaves, por compartilharmos sempre dúvidas dos nossos trabalhos e pelos ótimos
momentos que vivenciamos no departamento; à Jaqueline Andruchak, pela amizade;
à professora Ana Raquel, uma das primeiras pessoas a qual conheci em Natal e
que sempre me apoiou na realização desse mestrado além de ter convivido com ela
em muitos momentos em família.
Aos funcionários do departamento de Fisioterapia da UFRN, principalmente a
Edriene e a D. Eudione, por sempre estarem dispostas a me ajudar, servindo como
“babás” para que eu conseguisse participar de cursos e aulas.
viii
Dedicatória v
Agradecimentos vi
Listas
Lista
de
abreviaturas
x
Lista
de
figuras
xi
Lista
de
gráficos
xii
Resumo
xiii
Abstract
xiv
1
INTRODUÇÃO
1
1.1 Doença venosa
crônica
2
1.2 Úlceras venosas
5
1.2.1 Processo de cicatrização de uma úlcera
7
1.2.2 Curativos de carboximetilcelulose
8
1.3 Justificativa
11
1.4
Objetivos
12
1.4.1
Objetivo
principal
12
1.4.2
Objetivos
secundários
12
2
MATERIAIS
E
MÉTODOS
13
2.1
Caracterização
da
pesquisa
14
2.2 Etapas de uma revisão pela Colaboração Cochrane
14
2.3 Critérios para considerar os estudos para a revisão
17
ix
3.1.2
Estudos
incluídos
40
3.2 Risco de viés
dos
estudos
incluídos
41
3.3 Efeitos do hidrogel
44
3.3.1 Comparação entre hidrogel, Quitosana, e gaze com solução sali-
na (He e col. 2008) 44
3.3.2 Comparação entre hidrogel, Intrasite, e gel de alginato (de la
Brassine e col. 2006) 46
3.3.3 Comparação entre hidrogel, Intrasite, e mel de Manuka (Gethin e
col. 2008) 47
3.3.4 Comparação entre hidrogel e hidrocolóide (Grotewohl, 1994) 48
4 DISCUSSÃO
50
5 CONSIDERAÇÕES FINAIS E CONCLUSÃO
53
6
REFERÊNCIAS
BIBLIOGRÁFICAS
55
ANEXOS
61
ANEXO 1: Protocolo publicado-Hydrocolloid for healing venous leg ulcer 62
ANEXO 2: Estudos excluídos e justificativas para exclusão 80
ANEXO 3: Características dos estudos incluídos 87
x
IC- Intervalo de Confiança
ITB- Índice Tornozelo-Braquial
IVC- Insuficiência Venosa Crônica
NPF- Nurse Prescriber´s Formulary
RevMan- Review Manager
RR- Risco Relativo
xi
Colaboração Cochrane.
Figura 2: Diagrama com o resultado da seleção dos estudos.
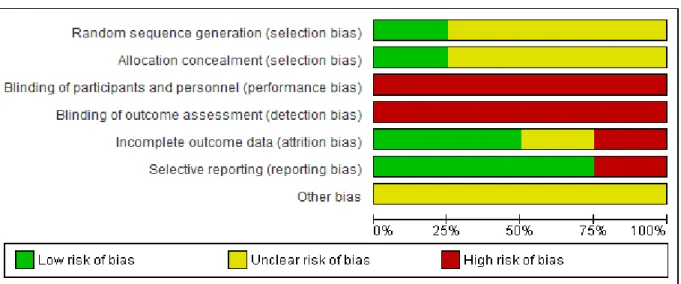
Figura 3: Avaliação do risco de viés de todos os estudos incluídos na revisão
xii
Gráfico 1: Forest plot representando a comparação do hidrogel com gaze com
solução salina para o desfecho cicatrização completa das úlceras.
Gráfico 2: Forest plot representando a comparação do hidrogel com o gel de alginato
para o desfecho porcentagem de redução da úlcera em 4 semanas de tratamento.
Gráfico 3: Forest plot representando a comparação do hidrogel com o mel de
Manuka para o desfecho cicatrização completa das úlceras.
xiii
acometer a população idosa e ser a principal responsável pelas úlceras de membros
inferiores nesta população. O uso de adesivos no cuidado de uma úlcera venosa é
parte fundamental no tratamento para a cicatrização, no entanto, as evidências para
auxiliar na escolha do melhor adesivo são escassas. O objetivo principal do estudo
foi avaliar a eficácia do tratamento com o hidrogel na cicatrização de úlceras
venosas mediante métodos de busca, síntese de informação e análise estatística
através de uma revisão sistemática com meta-análise. Foram selecionados estudos
controlados randomizados nas seguintes bases de dados: CENTRAL; DARE; NHS
EED; MEDLINE; EMBASE; CINAHL. Além dessas bases foram consultados três
websites para identificar estudos em andamento: ClinicalTrials.gov, OMS ICTRP e
ISRCTN
. Os desfechos primários analisados foram:
cicatrização completa das
úlceras e incidência de infecção das úlceras e os secundários foram: alterações no
tamanho da úlcera, tempo de cicatrização das úlceras, recorrência das úlceras,
qualidade de vida dos participantes, dor e custos do tratamento.
Quatro estudos
estão atualmente incluídos na revisão com um total de 250 pacientes.
O uso do
hidrogel parece ser superior ao curativo convencional, gaze embebida em salina,
para a cicatrização de úlceras venosas de membros inferiores; 16/30 pacientes
apresentaram cicatrização completa das úlceras (RR 5,33, 95%CI [1,73,16,42]). O
gel de alginato demonstrou ser mais efetivo quando comparado ao hidrogel quanto à
redução da área da úlcera; 61,2% (
±
26,2%) com o alginato e 19,4% (
± 24,3%) com
o hidrogel ao final das quatro semanas de tratamento.
O mel de Manuka demonstrou
ser similar ao hidrogel em relação à porcentagem de redução da área. Esta revisão
mostrou que não
existem evidências disponíveis a respeito da eficácia do hidrogel
em relação aos outros tipos de curativo na cicatrização de úlceras venosas de
membros inferiores, demonstrando assim a necessidade de futuras pesquisas para
auxiliar os profissionais da saúde na escolha do adesivo correto.
xiv
affects the elderly population and primarily is responsible for leg ulcers in this
population. The use of dressings in the care of a venous ulcer is a fundamental part
of the treatment for healing, however, evidence to assist in choosing the best
dressing is scarce. The main objective of this study was to evaluate the effectiveness
of treatment with hydrogel in the healing of venous ulcers using search methods,
synthesis of information and statistical research through a systematic review and
meta-analysis. Randomized controlled trials were selected in the following
databases:
CENTRAL; DARE; NHS EED; MEDLINE; EMBASE; CINAHL.
Beyond
these databases three websites were consulted to identify ongoing studies:
ClinicalTrials.gov, OMS ICTRP e ISRCTN
. The primary outcomes were analyzed:
complete wound healing, incidence of wound infection and the secondary were:
changes in ulcer size, time to ulcer healing, recurrence of ulcer, quality of life of
participants, pain and costs of treatment. Four studies are currently included in the
review with a total of 250 participants. The use of hydrogel appears to be superior to
conventional dressing, gauze soaked in saline, for the healing of venous leg ulcers;
16/30 patients showed complete healing of ulcers (RR 5,33, 95%CI [1,73,16,42]).
The alginate gel was shown to be more effective when compared to the hydrogel
dressing in reduction of the wound area; 61,2% (
±
26,2%) with alginate e 19,4% (
±
24,3%) with hydrogel at the end of four weeks of treatment.
Manuka honey has
shown to be similar to the hydrogel dressings in percentage of area reduction. This
review demonstrated that there
is no evidence available about the effectiveness of
the hydrogel compared to other types of dressings on the healing of venous leg
ulcers of the lower limbs
, thus demonstrating the need of future studies to
assist
health professionals in choosing the correct dressing
.
Keywords: chronic venous insufficiency, venous ulcers, hydrogel dressings,
As úlceras venosas de membros inferiores são frequentes e recorrentes, em
especial, em idosos. É uma ferida complexa associada a um custo considerável para
os pacientes e para saúde pública. O uso de adesivos no cuidado de uma úlcera
venosa é parte fundamental no tratamento para a cicatrização, no entanto, as
evidências para auxiliar a escolha do melhor adesivo são escassas. Atualmente
buscam-se intervenções terapêuticas que possam acelerar o processo de
cicatrização das feridas diminuindo assim, a morbidade, as complicações e os
gastos oriundos da doença.
O presente estudo trata-se de uma revisão sistemática com o objetivo de
sintetizar o resultado de pesquisas selecionadas sobre a eficácia do tratamento do
hidrogel na cicatrização de úlceras venosas mediante métodos de busca, síntese de
informação e análise estatística através de uma revisão sistemática com
meta-análise.
1.1 Doença Venosa Crônica
A doença venosa crônica (DVC) destaca-se entre as doenças crônicas que
acometem a população idosa e é a principal responsável pelas úlceras de membros
inferiores nesta população
1;2. A DVC refere-se a uma doença que afeta o
funcionamento do sistema venoso dos membros inferiores decorrentes de uma
hipertensão venosa de longa duração, causada por insuficiência valvular com ou
sem obstrução do fluxo venoso podendo afetar o sistema venoso superficial, sistema
venoso profundo, ou ambos
3. Essa condição abrange uma série de apresentações
clínicas que podem variar de telangiectasias a úlceras abertas.
A classificação da DVC dos membros inferiores surgiu a partir de um
consenso estabelecido por um comitê de especialistas de vários países
4e
posteriormente ela foi revisada e atualizada por alguns autores do mesmo comitê
5.
Ela é classificada segundo a classificação Clinical-Etiology-Anatomy-Patophysiology
(CEAP) onde C refere-se aos sinais clínicos da doença; E à etiologia; A refere-se à
localização anatômica da doença e P à fisiopatologia. Todas as formas de
apresentação clínica da DVC estão divididas em sete categorias que variam de
acordo com a gravidade, sendo C0 a ausência de sinais; C1 telangiectasias e/ou
dos membros; C4b lipodermatosclerose e/ou atrofia branca; C5 úlcera venosa
cicatrizada e C6 úlcera venosa ativa.
Em relação à etiologia, a DVC divide-se em três classes: congênita (Ec),
primária (Ep), secundária (Es) ou sem causa venosa identificável (Em). No que diz
respeito à anatomia venosa do membro inferior, esta se divide em três sistemas:
superficial (As), profundo (Ad), perfurante (Ap) e local venoso não identificável (An).
Por fim, em termos fisiopatológicos, a DVC poderá resultar de um refluxo (Pr), de
uma obstrução (Po), de ambos os processos (refluxo e obstrução – Pr,o) e
patofisiologia não identificada (Pn)
5.
Tendo como base a classificação CEAP, a doença venosa crônica é definida
como qualquer forma de doença venosa desde C0 a C6. Existe uma sobreposição
de termos, pois alguns autores consideram o termo insuficiência venosa crônica
(IVC) como sinônimo de DVC abrangendo assim todas as classes da doença. Por
outro lado, alguns consideram IVC apenas casos avançados da doença como
aqueles pacientes que apresentam edema (C3), alterações subcutâneas (como
lipodermatoesclerose C4b) e úlcera venosa (C5-C6)
6.
A prevalência da IVC tende a aumentar com a idade
7. Um único estudo
realizado no Brasil, interior de São Paulo, sobre alterações venosas de membros
inferiores estimou a prevalência de varizes em 39,5% e de formas mais graves da
IVC, no caso as úlceras abertas ou cicatrizadas em 1,5%
8.
Nos Estados Unidos estima-se que aproximadamente 2,5 milhões de pessoas
tenham IVC, das quais 20% chegam a desenvolver úlcera venosa
9. Uma revisão
com 11 estudos de prevalência realizados na Austrália e Europa estimou a
prevalência de úlceras venosas de membros inferiores em 0,1% a 0,3% na
população adulta
10. Os dados epidemiológicos têm consistentemente sugerido que
a prevalência aumenta com a idade e é maior entre as mulheres
11-14. Tem sido
estimado que a incidência de úlceras venosas na terceira idade seja de 0,76/100
pessoas por ano em homens e de 1,42/100 pessoas por ano em mulheres
13.
As úlceras venosas estão associadas a um custo considerável para o
saúde pública por ser progressiva e apresentar propensão à recorrência
15. Duas
revisões sistemáticas sobre qualidade de vida em pacientes com úlceras de perna
reportaram que a presença de ulceração na perna estava associada com dor,
restrição às atividades de trabalho e lazer, mobilidade reduzida, perturbação do
sono, redução do bem-estar psicológico e isolamento social
16;17O custo do tratamento de uma úlcera de perna não cicatrizada no Reino
Unido foi estimado em cerca de EUR 1,3 mil por ano (valores calculados em 2001)
18.
Um estudo realizado na Alemanha revelou que o custo médio por ano com um
paciente com uma úlcera venosa crônica é de EUR 9569 dos quais 92% estão
relacionados a custos diretos como gastos com exames, curativos, taxas médicas e
8% estão relacionados a custos indiretos como perda da produtividade no trabalho
19.
Um estudo de coorte realizado no USA registrou que os custos diretos com um
paciente com uma úlcera venosa de membros inferiores seria em media $2400 por
mês (valor estimado em 1997)
20.
Como descrito, a IVC provém da disfunção do sistema venoso dos membros
inferiores decorrentes de uma hipertensão venosa de longa duração. Os fatores
predisponentes da hipertensão venosa incluem história de trombose venosa
profunda (TVP), tromboflebite, trauma na perna, artrite, obesidade, gravidez e vida
sedentária. Esses fatores podem resultar em danos às válvulas nas veias das
pernas
21;22. Em condições normais, o fluxo de sangue nos vasos venosos ocorre em
uma única direção, das veias do sistema superficial para as veias do sistema
profundo, orientado pelas inúmeras válvulas contidas no interior das veias desses
sistemas e auxiliado pela musculatura dos membros inferiores especialmente das
pernas e dessas desembocando no átrio direito. Esse mecanismo faz com que a
pressão venosa, que em posição ortostática pode atingir valores de até 80mmHg a
90mmHg seja reduzida para 30 mmHg em resposta a ação valvular e à contração
muscular; portanto, uma falha no funcionamento dessas válvulas pode desencadear
a hipertensão venosa
21;23.
Durante a progressão da insuficiência venosa, observam-se alterações da
microcirculação representadas pela diminuição do número de capilares associado às
alterações morfológicas dos capilares remanescentes que se tornam contorcidos,
O
2local
24-26. Uma teoria importante e provavelmente mais aceita atualmente para a
fisiopatologia da ulceração venosa é a teoria do encarceramento dos leucócitos
26;27.
A estase venosa favorece a marginalização dos leucócitos e a interação
endotélio-leucocitária, com consequente infiltração leucocitária e produção de citocinas e
substâncias químicas por parte destes. Estes fatores contribuirão para a lesão
tissular (semelhante ao que ocorre na inflamação crônica)
27;28.
1.2
Úlceras venosas
A complicação mais importante da IVC é a úlcera venosa representando
cerca de 70% de todas as úlceras de perna.
Elas
apresentam-se como feridas
abertas, geralmente irregulares e superficiais nos membros inferiores, predominando
no terço inferior da perna e caracteristicamente tendem a se cronificar, serem
recidivantes e apresentarem cicatrização lenta, especialmente quando não tratadas
prontamente e adequadamente. Estão associadas à hipertensão venosa sustentada
e alterações da microcirculação decorrentes de insuficiência venosa crônica
26-28;29.
Essa condição causa problemas físicos, psicológicos e financeiros que
impactam a qualidade de vida dos pacientes. O impacto das úlceras venosas na
rotina diária dos pacientes tem sido descrito em vários estudos quantitativos e
qualitativos. Os maiores problemas reportados pelos pacientes são: dor, imobilidade,
distúrbios do sono, falta de energia, limitações nas atividades de trabalho e lazer,
preocupações, frustações e falta de autoestima
16;17.
A duração de uma úlcera venosa pode variar de algumas semanas a mais de
10 anos e em algumas pessoas elas nunca cicatrizam
14;30;31. O tamanho da úlcera
bem como a sua duração (tempo maior que 18 meses) são fatores que contribuem
para o risco de uma úlcera não cicatrizar
32. Outros fatores também estão associados
a um atraso da cicatrização das úlceras, como: lipodermatoesclerose, evidência de
trombose venosa profunda, tromboflebite superficial e baixa mobilidade do
tornozelo
33.
Margolis
et al
.
34mostraram, através de um estudo de coorte com 260
pacientes que apresentavam úlcera venosa e foram tratados por um período de 2
insucesso da cicatrização de uma úlcera com 24 semanas de duração que foram:
tamanho inicial da ferida, duração da ferida no início do tratamento, história de
ligadura venosa, história de cirurgia para colocação de prótese de joelho ou quadril,
ITB (índice tornozelo-braquial) <0,8, ferida coberta com fibrina em uma área >50%
no início do tratamento.
O diagnóstico da úlcera venosa é basicamente clínico realizado através da
anamnese e do exame clínico. Na anamnese deve-se observar: queixa e a duração
dos sintomas; doenças anteriores como a trombose venosa; traumatismos prévios
dos membros e a existência de doença varicosa e principalmente a aparência e
localização da úlcera. Os sintomas incluem sensação de peso nas pernas e dor nos
membros inferiores principalmente ao final do dia
35. O diagnóstico clínico juntamente
com os exames complementares tem como objetivo estabelecer as possíveis causas
da IVC, se ela ocorre por obstrução do retorno venoso, por refluxo ou por ambos.
Dentre os exames complementares existentes os mais usados são: o Doppler de
ondas contínuas, o eco-Doppler venoso e a pletismografia venosa
35;36. Todo
paciente que apresenta uma úlcera precisa realizar o índice tornozelo-braquial (ITB)
para investigar a presença de doença arterial obstrutiva periférica. É um teste não
invasivo, de baixo custo, determinado pelo Doppler vascular que é calculado através
da maior pressão sistólica aferida no tornozelo aferida nas artérias tibial posterior ou
pediosa dividida pela maior pressão sistólica aferida no membro superior utilizando a
artéria braquial. Índices iguais ou menores que 0,9 caracterizam o diagnóstico de
doença arterial periférica
37. Índices maiores que 0,8 são geralmente usados para
afastar a coexistência de doença arterial periférica como causa da úlcera levando ao
diagnóstico de úlcera devido a insuficiência venosa
38.
Devido às características de cronicidade e alta reincidência das úlceras
venosas, atualmente buscam-se intervenções terapêuticas que possam acelerar o
processo de cicatrização das feridas diminuindo assim, a morbidade, as
complicações e os gastos oriundos da doença. Embora o uso de compressão por
enfaixamento e cuidados com a ferida seja o tratamento padrão
1;39, o uso de
agentes físicos como o ultrassom
40;41, o laser associado à outras terapias como led
para a aceleração da cicatrização das feridas além do tratamento promovido pela
Fisioterapia através dos exercícios físicos
44.De acordo com as Diretrizes sobre Diagnóstico, Prevenção e Tratamento da
Doença Venosa Crônica da Sociedade Brasileira de Angiologia e Cirurgia Vascular
(SBACV)
36, durante o tratamento de uma úlcera venosa é necessário aliar a terapia
compressiva com a elevação do membro durante o repouso. Para o tratamento de
uma úlcera venosa são necessárias medidas que almejem a rápida cicatrização da
úlcera através de cuidados básicos de limpeza do local afetado, uso de curativos,
terapia compressiva, uso de agentes físicos, exercícios.
1.2.1
Processo de cicatrização de uma úlcera
O processo de cicatrização envolve vários fenômenos entre os mais
importantes estão os bioquímicos e fisiológicos que podem atuar de forma
harmoniosa para garantir a reconstituição tecidual. A cicatrização depende de vários
fatores locais e gerais, como: localização anatômica, tipo de pele, raça, idade, etc.
O processo de cicatrização das úlceras envolve três estágios. Inicialmente
existe o estágio inflamatório, que é precedido por uma fase de coagulação que se
inicia após o surgimento da ferida. Esta fase depende da atividade plaquetária e da
cascata de coagulação. Ocorre uma série de liberação de produtos como,
substâncias vasoativas, proteínas adesivas, fatores de crescimento e proteases que
são liberadas e estabelecem o desenvolvimento de outras fases. A formação do
coágulo serve não apenas para coaptar as bordas da ferida, mas também para
cruzar a fibronectina, oferecendo uma matriz provisória, em que os fibroblastos,
células endoteliais e queratinócitos possam ingressar na ferida
45.
No estágio inflamatório o macrófago aparece como a célula mais importante,
pois ele fagocita as bactérias, desbrida corpos estranhos e direciona o
desenvolvimento do tecido de granulação. A fase de proliferação é responsável pelo
fechamento da lesão e finalizando o processo ocorre a etapa de reparo tecidual em
um estágio de remodelamento
45;46.
Todo o processo de cicatrização depende da proliferação de fibroblastos e da
encontrados em abundância no tecido de granulação, sendo o colágeno tipo III em
maior quantidade nas bordas da lesão dérmica
47. A resposta inicial
imunohistoquímica para a cicatrização tecidual depende basicamente da presença
de ambos os tipos de colágeno. No entanto são vários os fatores que influenciam o
processo de cicatrização, retardando o mesmo e tornando as feridas crônicas. Entre
eles interferem a idade, o estado nutricional do paciente e a existência de doenças
como a diabetes
45.
Phillips e colaboradores
48citaram em seu estudo que a área da úlcera bem
como sua duração é preditora significativa da cicatrização completa e do tempo para
cicatrização total em uma úlcera. O percentual de cicatrização e a área da úlcera na
terceira semana são bons preditores de uma cicatrização completa da úlcera.
1.2.2
Curativos de carboximetilcelulose
Os curativos em geral são aplicados nas feridas diretamente ou sobre outro
adesivo ou bandagem. O ambiente ideal para a cicatrização é aquele no qual a
ferida é mantida coberta e úmida. Existem vários tipos de adesivos que promovem
esse meio úmido com o objetivo de reepitelização da ferida, promover conforto ao
paciente, controlar o exudato da ferida, prevenir que as bandagens não
permaneçam em contato direto com a ferida, minimizar o número de trocas dos
adesivos e o risco de maceração
49.
De acordo com a
Nurse Prescriber´s Formulary (NPF)
49, o adesivo apropriado
para o tratamento das feridas não depende somente do tipo de ferida, mas do
estágio em que se encontra o processo de cicatrização da mesma. A NPF classifica
os adesivos em quatro categorias:
Básicos
: Esta categoria é subdividida em adesivos absorventes e adesivos de baixa
aderência. Os de baixa aderência são compostos de algodão e podem ser
colocados diretamente em contato com a ferida. Eles podem conter algum
medicamento como a clorexidina ou não apresentar medicamento como a gaze de
parafina. Os adesivos absorventes são aplicados diretamente na ferida e podem ser
usados como uma camada secundária a um tratamento com feridas com muito
Avançados -
Esta categoria é composta por oito tipos de adesivos:
- Adesivos de Hidrogel: será descrito com mais detalhes abaixo por ser o
adesivo utilizado como tratamento proposto pela revisão.
- Adesivos de Hidrocolóide: são geralmente compostos por uma matriz
absorvente de hidrocolóide sobre uma película permeável ao vapor ou espuma de
apoio, exemplo: Granuflex (ConvaTec).
- Adesivos de alginato: esses adesivos são altamente absorventes e possuem
em sua composição alginato de cálcio ou alginato de cálcio de sódio que podem ser
combinados com o colágeno. O alginato forma um gel quando em contato com a
superfície da ferida. Esse gel pode ser retirado no momento da troca do adesivo ou
lavado com solução salina estéril, exemplo: Curasorb (Covidien).
- Adesivos de espuma: esses adesivos contém espuma de poliuretano
hidrofílica e são designados para absorver o exudato da ferida e manter a superfície
da mesma úmida. Existem vários tipos, algumas, por exemplo, contém material
absorvente adicional como a viscose e fibras de acrilato, exemplo: Allevyn (Smith &
Nephew).
- Adesivos macios de polímero: são compostos de um polímero de silicone
macio mantidos em uma camada não aderente. Eles são moderadamente
absorventes, exemplo: Urgotul (Urgo).
- Adesivos de membrana e filmes permeáveis: esses adesivos são
permeáveis ao vapor de água e oxigênio, mas não são permeáveis a água no
estado líquido ou micro-organismos, exemplo: Opsite (Smith & Nephew).
- Adesivos de efeito capilar: esses adesivos contem um núcleo absorvente de
fibras hidrofílicas mantidas entre duas camadas de contato de baixa aderência,
exemplo: Vacutx (Protex).
- Adesivos de absorção de odores: esses adesivos contem carvão na sua
frequentemente com um adesivo secundário para melhorar a absorção, exemplo:
CarboFLEX (ConvaTec).
Anti-microbial -
Existem três tipos nessa subdivisão:
- Adesivos impregnados com mel: esses adesivos contém mel de pureza
médica com propriedades anti-inflamatórias e anti-microbiais. Podem ser usados em
feridas agudas e crônicas, exemplo: Medihoney (Medihoney).
- Adesivos impregnados com prata: eles são usados para tratar feridas
infectadas, exemplo: Acticoat (Smith & Nephew).
- Adesivos impregnados com iodo:
esses adesivos liberam iodo livre no qual
pode agir como um antiséptico para a ferida quando esta é exposta ao exudato,
exemplo: Iodozyme (Insense).
Existem ainda outros tipos de adesivos antimicrobiais compostos de gaze ou
adesivos de baixa aderência impregnados com solução oleosa que apresentam
propriedades antimicrobiais.
Adesivos especializados
- Nessa categoria existem dois tipos:
- Adesivos de silicone para queloides: esses adesivos reduzem ou previnem a
cicatriz hipertrófica ou queloides, exemplo: Cica-Care (Smith & Nephew).
- Adesivos de matriz moduladora de proteinase: eles alteram a atividade de
enzimas proteolíticas em feridas crônicas, exemplo: Promogran (Systagenix).
O hidrogel utilizado como curativo primário (curativo usado em contato direto
com a ferida)
é um adesivo que pode apresentar-se sob a forma de gel transparente,
amorfo ou placa. As placas são geralmente compostas por água, propileno glicol e
carboximetilcelulose ou água e polivinilpirridona. A NPF
49descreve os hidrogéis
como adesivos compostos de polímeros de amido possuindo até 96% de água.
Os hidrogéis bem como os adesivos em geral, têm como objetivo proteger a
ferida promovendo um ambiente úmido visando a cicatrização da mesma. Eles são
com muito exudato, pois, o excesso de hidratação pode provocar a maceração do
tecido ao redor da ferida. É necessário um curativo secundário (usado sobre o
curativo primário; não aderente) para cobrir a ferida (NPF). As trocas deste tipo de
curativo não necessitam ser diárias, porém dependem do curativo secundário e
podem ocorrer entre um período de cinco a sete dias. Elas devem ser feitas quando
for observado um extravasamento de exsudato para fora do curativo
45.
Além da vantagem da manutenção do meio úmido, os hidrogéis favorecem a
angiogênese e promovem o desbridamento autolítico. Esse último processo é
responsável pela digestão das células mortas através de enzimas sendo favorecido
pela manutenção do meio úmido
50. Outra vantagem dos curativos de hidrogéis é que
eles protegem as terminações nervosas reduzindo assim a dor dos pacientes
51e
causando menos desconforto durante as trocas.
1.3
Justificativa
O uso de curativos no cuidado de uma úlcera venosa é parte fundamental no
tratamento para a cicatrização. Existem muitos tipos disponíveis no mercado e os
custos variam consideravelmente. Para a escolha correta do uso do curativo para
cada paciente deve-se levar em consideração além do tipo da ferida e suas
características o estágio de cicatrização.
No entanto, a base de evidências para guiar qual o curativo correto para o
tratamento ideal da úlcera é escassa. São necessárias orientações para ajudar os
profissionais de saúde a tomar decisões a respeito do melhor curativo disponível
para o tratamento visando uma rápida cicatrização da úlcera.
Além disso, apesar do uso de diversos curativos ainda existe carência de
análises sistemáticas que avaliem a efetividade do uso destes na cicatrização de
úlceras venosas, incluindo o uso de hidrogel e adesivos de carboximetilcelulose
(hidrocolóides) embora estes sejam amplamente utilizados na rotina clínica.
Portanto, este estudo propôs avaliar a evidência clínica sobre a efetividade do
tratamento do hidrogel para a cicatrização de úlceras venosas através de uma
revisão sistemática. Além disso, a fisioterapia aplicada às doenças vasculares
em contato com pacientes acometidos por úlceras de pele; portanto necessitando
conhecer a indicação e a efetividade destes curativos.
1.4
Objetivos
1.4.1
Objetivo principal
Avaliar o resultado de estudos sobre a eficácia do hidrogel comparado com
outros tratamentos e outros adesivos para a cicatrização de úlceras venosas.
1.4.2
Objetivos secundários
- Selecionar, avaliar e incluir os ensaios clínicos controlados e randomizados
no qual apresentem os efeitos dos tratamentos de hidrogel para a cicatrização de
úlceras venosas comparados com outros nas alterações do tamanho da úlcera,
tempo até a cicatrização bem como sua recorrência;
- Avaliar a eficácia do tratamento de hidrogel na melhora da qualidade de vida
e da dor;
- Avaliar os custos do tratamento das úlceras venosas.
2.1 Caracterização da pesquisa
O presente estudo trata-se de uma revisão sistemática com metanálise
desenvolvida em parceria com a Colaboração Cochrane (The Cochrane
Collaboration). A revisão seguiu as recomendações para realização de revisões
sistemáticas e meta-análise propostas pelo
Cochrane Handbook for Systematic
Reviews of Interventions
disponível no site da Colaboração Cochrane
52.
2.2 Etapas de uma revisão pela Colaboração Cochrane
A Colaboração Cochrane, fundada em 1992 no Reino Unido é uma
organização internacional sem fins lucrativos cujos objetivos são preparar, manter e
assegurar o acesso a revisões sistemáticas sobre efeitos de intervenções na área da
saúde. A estrutura organizacional da Colaboração Cochrane divide-se em: rede de
consumidores, centros, comitê diretor, campos, grupos de metodologia e grupos de
revisão. Os grupos de revisão, por sua vez, estão divididos nas diversas áreas da
saúde. A presente revisão faz parte do “Grupo de Feridas” (Wounds Group), com
sede localizada na cidade North Yorkshire, York, United Kindom.
Para iniciar uma revisão sistemática pela Colaboração Cochrane é necessário
inicialmente contatar o (a) coordenador (a) do grupo de interesse a fim de discutir
possíveis títulos para a revisão, os quais não entrem em choque com outros títulos
já existentes nos grupos de revisões e assegurar a viabilidade da revisão proposta.
O site da Colaboração Cochrane disponibiliza todas as informações e dados do
corpo editorial e coordenadores de cada grupo, além das revisões já existentes.
Após checar a viabilidade do tema sugerido, é então necessário preencher o
formulário de registro do título ou o formulário de atualização, os quais contém uma
breve descrição sobre a revisão, bem como algumas informações dos autores. O
formulário é então submetido ao corpo editorial do grupo o qual é responsável pelo
aceite da revisão sugerida.
Para iniciar a presente revisão, os autores contataram a coordenadora do
Grupo de Feridas e enviaram uma proposta de titulo. O grupo então sugeriu dividir
uma revisão já publicada
53e que precisava ser atualizada em quatro outras revisões.
registro de dois títulos sugeridos no qual foi aprovado pelos editores do grupo.
Todas as etapas a seguir foram realizadas de acordo com o
Cochrane Handbook for
Systematic Reviews of Interventions
52fornecido pela Colaboração Cochrane.
Devido ao tempo necessário para desenvolvimento de uma revisão
sistemática e alguns atrasos durante o desenvolvimento do estudo, o resultado de
uma das revisões está sendo apresentado aqui nesta dissertação
54(Hidrogel
dressings for venous leg ulcers) e a outra revisão ainda se encontra em andamento
55(Anexo 1).
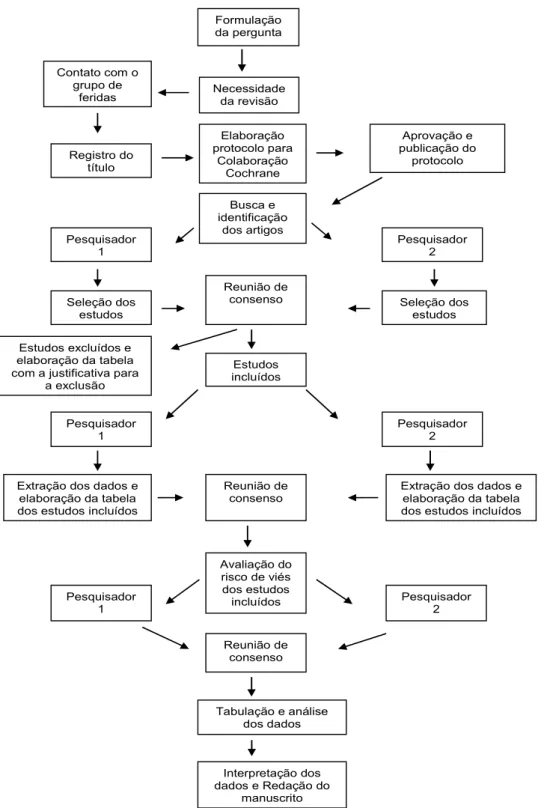
A Colaboração Cochrane recomenda que a revisão sistemática seja efetuada
em sete passos: formulação da pergunta; localização e seleção dos estudos;
avaliação crítica dos estudos; coleta de dados; análise e apresentação dos dados e
aprimoramento e atualização da revisão
52. Segue abaixo o fluxograma completo com
todas as etapas para a realização da revisão sistemática pela Colaboração
Formulação da pergunta Necessidade da revisão Contato com o
grupo de feridas Registro do título Elaboração protocolo para Colaboração Cochrane Aprovação e publicação do protocolo Busca e identificação dos artigos Pesquisador 1 Pesquisador 2 Seleção dos estudos Seleção dos estudos Reunião de consenso Estudos incluídos Estudos excluídos e
elaboração da tabela com a justificativa para
a exclusão
Pesquisador 1
Pesquisador 2
Extração dos dados e elaboração da tabela dos estudos incluídos
Extração dos dados e elaboração da tabela dos estudos incluídos Reunião de
consenso
Avaliação do risco de viés dos estudos incluídos Pesquisador 1 Pesquisador 2 Reunião de consenso
Tabulação e análise dos dados
Interpretação dos dados e Redação do
manuscrito
Figura 1
:
Fluxograma da estratégia de elaboração de uma revisão sistemática pela
2.3 Critérios para considerar os estudos para a revisão
Os seguintes critérios foram considerados para a inclusão dos estudos na
revisão: tipos de estudos; tipos de participantes; tipos de intervenções; tipos de
desfecho (primários e secundários); métodos de busca para identificação dos
estudos (busca eletrônica e outras fontes de pesquisa). Para a coleta e análise dos
dados foi considerada a avaliação do risco de viés; mensuração do efeito do
tratamento; dados incompletos ou ausentes; avaliação da heterogeneidade; análise
de subgrupo e análise de sensibilidade.
Foram incluídos estudos controlados randomizados que apresentassem os
efeitos do hidrogel na cicatrização de úlceras venosas de membros inferiores em
pacientes de qualquer idade. Os desfechos primários analisados foram: cicatrização
completa da ferida medida pelo número de úlceras completamente cicatrizadas
durante a duração de cada estudo e a incidência de infecção na ferida. Os
desfechos secundários foram: mudanças no tamanho da úlcera medidas pela
redução no seu tamanho original expresso em valores absolutos (cm
²
) ou relativos
(%); tempo de cicatrização da úlcera; recorrência da úlcera; qualidade de vida
avaliada através de questionários genéricos padronizados como o SF-36, SF-12 ou
SF-6; dor avaliada no momento da troca do adesivo ou durante o tratamento através
de instrumentos validados como questionários ou escala visual analógica; e custos.
Foram pesquisados estudos nas seguintes bases de dados eletrônicas: CENTRAL
2013, Issue 8; DARE 2013, Issue 8; NHS EED 2013, Issue 8; MEDLINE (1948 a
agosto de 2013); EMBASE (1980 a setembro de 2013); CINAHL (1982 a agosto de
2013). Além dessas bases foi consultado 3 websites para identificar estudos em
andamento: ClinicalTrials.gov, OMS ICTRP e ISRCTN. A busca de artigos foi
realizada pela própria equipe do grupo de revisão de acordo com o protocolo
pré-estabelecido (Wounds group). No entanto a escolha dos descritores e a decisão de
quais estudos entrariam para a revisão foi função dos autores.
Foi utilizado o software Review Manager (RevMan) versão 5.2 disponível para
download no site da Colaboração Cochrane para a combinação e análise dos dados.
Os seguintes dados foram extraídos dos estudos e inseridos no RevMan de maneira
método de randomização e sigilo de alocação, mascaramento dos participantes e
dos avaliadores, desistências e exclusões, entre outros. Foram extraídos também
descrição dos participantes, como: amostra total, idade, tipo e duração da úlcera,
critérios de inclusão e exclusão. Na descrição da intervenção foi extraído o tipo de
adesivo usado como tratamento, duração do tratamento e a descrição dos
resultados.
Na intenção de evitar a possibilidade de viés, aumentando assim a qualidade
dos resultados, foi utilizada uma tabela para avaliação do risco de viés (The
Cochrane Collaboration´s tool for assessing risk of bias) fornecida pela Colaboração
Cochrane, no qual inclui os seguintes itens: sequência de randomização (random
sequence generation), sigilo de alocação (allocation concealment), mascaramento
dos participantes e dos avaliadores (blinding of participantes and personnel),
mascaramento dos avaliadores envolvidos com a análise dos desfechos de cada
estudo (blinding of outcome assessment), descrição seletiva do desfecho (selective
reporting) e outros vieses (other bias). Cada item recebeu uma das seguintes
classificações: “alto risco de viés”, “baixo risco de viés” ou “risco incerto de viés” de
acordo com o Handbook for Systematic Reviews of Interventions da Colaboração
Cochrane. A avaliação do risco de viés foi realizada de maneira independente por
dois autores.
Para a análise estatística foi utilizado o software RevMan 5.2 onde a
mensuração do efeito do tratamento foi analisada através das variáveis contínuas
que foram expressas como diferença de média com um intervalo de confiança (IC)
de 95% e das variáveis dicotômicas foram expressas através da estimativa do risco
relativo (RR) também com um intervalo de confiança de 95%.
Todos os critérios citados acima estão descritos detalhadamente na seção de
Os resultados estão divididos em duas partes: na primeira encontra-se o
protocolo publicado na base de dados da Colaboração Cochrane e em seguida a
análise dos dados e discussão descritiva dos resultados que ainda não foram
Hydrogel dressings for venous leg ulcers (Protocol)
Ribeiro CTD, Dias FAL, Fregonezi GAF
This is a reprint of a Cochrane protocol, prepared and maintained by The Cochrane Collaboration and published inThe Cochrane Library2013, Issue 9
http://www.thecochranelibrary.com
Hydrogel dressings for venous leg ulcers (Protocol)
T A B L E O F C O N T E N T S
1 HEADER . . . .
1
ABSTRACT . . . .
1
BACKGROUND . . . .
3
OBJECTIVES . . . .
3 METHODS . . . .
6
ACKNOWLEDGEMENTS . . . .
7 REFERENCES . . . .
9
APPENDICES . . . .
15
CONTRIBUTIONS OF AUTHORS . . . .
15 DECLARATIONS OF INTEREST . . . .
15 SOURCES OF SUPPORT . . . .
i Hydrogel dressings for venous leg ulcers (Protocol)
[Intervention Protocol]
Hydrogel dressings for venous leg ulcers
Cibele TD Ribeiro1, Fernando AL Dias2, Guilherme AF Fregonezi3
1Graduate Program in Physiotherapy, Federal University of Rio Grande do Norte, Natal, Brazil.2Department of Physiology, Federal
University of Paraná, Curitiba, Brazil.3Department of Physical Therapy, Federal University of Rio Grande do Norte, Natal, Brazil
Contact address: Guilherme AF Fregonezi, Department of Physical Therapy, Federal University of Rio Grande do Norte, Avenida Senador Salgado Filho, 3000, Lagoa Nova, Natal, Rio Grande do Norte, 59078-470, Brazil.fregonezi@ufrnet.br.
Editorial group:Cochrane Wounds Group.
Publication status and date:New, published in Issue 9, 2013.
Citation: Ribeiro CTD, Dias FAL, Fregonezi GAF. Hydrogel dressings for venous leg ulcers.Cochrane Database of Systematic Reviews
2013, Issue 9. Art. No.: CD010738. DOI: 10.1002/14651858.CD010738.
Copyright © 2013 The Cochrane Collaboration. Published by John Wiley & Sons, Ltd.
A B S T R A C T
This is the protocol for a review and there is no abstract. The objectives are as follows:
To assess the effects of hydrogel wound dressings for healing venous leg ulcers in people in any care setting.
B A C K G R O U N D
A glossary of medical terms is available inAppendix 1.
Description of the condition
Venous leg ulcers (VLU) present as open wounds generally irregu-lar and shallow or sores on the lower limb. They are associated with sustained venous hypertension and microcirculatory alterations resulting from chronic venous insufficiency (Grey 2006;Wollina 2006).This condition has psychological and financial impact and also impacts on the physical functioning of affected patients. The impact of leg ulcers on patient’s daily life is described in many quantitative and qualitative studies. The major problems reported from the patients are: pain, immobility, sleep disturbance, lack of energy, limitations in work and leisure activities, worry, frustra-tion and lack of self-esteem (Herber 2007;Persoon 2004). Thus, venous leg ulcers will ultimately impact quality of life. Venous leg ulceration is a chronic health problem that can take years to heal completely, and, as it has a high rate of recurrence, often requires life-long treatment (Margolis 2002;Van Hecke 2011). Wound
size and wound duration (greater than 18 months) were major contributors to a risk of not healing (Margolis 2004). Addition-aly, the presence of lipodermatosclerosis, evidence of deep vein thrombosis, superficial thrombophlebitis or poor ankle mobility were individually associated with delayed healing (Lantis 2013). The incidence of venous ulceration rises with increasing age (De Araujo 2003; Wipke-Tevis 2000). The primary risk factors are aging, gender (more common in women), obesity, previous leg injuries, deep venous thrombosis (clots in veins) and phlebitis (in-flammation of veins) (Collins 2010). Insufficiency of the superfi-cial, perforating or deep veins of the leg is also a risk factor for leg ulceration (Valencia 2001). Venous leg ulcers have been estimated to afflict between 0.2% and 1% of the total population and be-tween 1% and 3% of the elderly population in the United States (USA) and Europe (Margolis 2002).The estimated incidence of venous leg ulcers in the elderly (i.e. aged 65 years or older) per 100 person-years is around 0.76 for males and 1.42 for females (Margolis 2002). The estimated prevalence of venous leg ulcers ranges between 0.6 and 1.9 per cent in the adult population of the UK, USA, and Europe (Briggs 2003). Epidemiological studies estimate that venous leg ulcers affect 1 million people in the USA,
1 Hydrogel dressings for venous leg ulcers (Protocol)
accounting for 70 to 80 per cent of all ulcers of the lower limbs (De Araujo 2003). A cohort study calculated that direct medical care costs attributable to a VLU averaged $2400 (in 1997 value US dollars) per month (Olin 1999). Up to 10 per cent of the pop-ulation in Europe and North America has valvular incompetence, with 0.2 per cent developing venous ulceration. Venous ulceration represents the most prevalent form of difficult-to-heal wounds, and treating these problematic wounds requires significant health-care resources. Recent data from Germany revealed that the mean total cost per year for a patient with chronic venous leg ulceration was EUR 9569, of which 92% was estimated to be direct costs (non drug treatment, inpatients costs and outpatient care) and 8% indirect costs (inability to work) (Purwins 2010).
The physiopathology of venous ulcers starts as a macrovascular problem due to valve incompetence. Aetiological (causative) fac-tors such as venous thrombosis could cause valve insufficiency that results in venous stasis and reflux, which are the predominant fac-tors in chronic venous insufficiency (Raju 2010). In the normal venous system, pressure decreases during exercise as a result of the action of the muscles pumping the blood vessels. In a system where the valves are incompetent, the venous pressure remains high (Grey 2006). Sustained venous hypertension will ultimately lead to microcirculatory dysfunction and cause alterations in skin perfusion, which can then lead to ulceration.
Alterations in the microcirculation are described as a decrease in the capillary density, which can also be reduced by dilation, tor-tuosity and convolution of the remaining capillaries (Howlader 2003;Incandela 2001;Junger 2000). This impacts the nutrition and clearance of by-products in the tissue, leading to skin changes observed in the form of swelling, eczema, hyperpigmentation (skin coloration), lipodermatosclerosis (hard, tight skin) and, ultimately, tissue ulceration. Part of the pathway leading to tissue damage and ulceration is due to leucocyte interaction with endothelial cell-surface binding molecules that facilitate their migration into tis-sue. Once leucocytes are in the tissue they become active and pro-duce a series of molecules that lead to tissue damage (Smith 2006;
Wollina 2006).
The diagnosis of venous ulceration is usually based on clinical ex-amination. Additional tests such as colour duplex ultrasonography (measurement of blood flow in the veins and arteries of the leg), plethysmography (measures variations in the size or volume of a limb), venography ( x-ray test that provides an image of the leg veins) and ankle brachial pressure index (ABPI- provides the ratio of systolic blood pressure at the ankle to that in the arm) (Cochrane Wounds Group Glossary;The Free Medical Dictionary) may be helpful if the diagnosis is unclear (Collins 2010;Robson 2006). All patient that present an ulcer should be screened for peripheral arterial disease (PAD) by Doppler measurement of ABPI. An in-dex equal or lower than 0.9 is the diagnosis criterion for periph-eral arterial disease (Rooke 2011); however, ABPI measurement greater than 0.8 is generally used to exclude peripheral arterial dis-ease as the cause of a leg ulceration, leaving the most likely
diag-nosis venous ulceration (RCN 2006). Venous ulcers are generally irregular and shallow, and often occur over bony prominences, particularly in the gaiter area (over the medial malleolus). Skin al-terations surrounding the ulcer such as hyperpigmentation, lipo-dermatosclerosis and fibrosis are usually present (Collins 2010). Frequent symptoms for venous ulceration include pain, odour and drainage from the wound (Valencia 2001). Arterial ulcers can be distinguished from venous ulcers because the former typically have round and well-demarcated borders and the presence of necrotic tissue in the wound bed. Physical symptoms of arterial leg ulcers include: loss of leg hair; atrophic skin (wasting of skin); cold feet; absence of, or decrease in, arterial pulses; and symptoms such as intermittent claudication (pain on walking that goes away with rest). Neuropathic ulcers are more common in, but are not lim-ited to, patients with diabetes mellitus. These differ from venous leg ulcers in having defined borders, they are usually deeper than venous ulcers and are associated with foot numbness, burning and paraesthesia (sensation of “pins and needles”) (Valencia 2001). The standard treatment for venous leg ulcer is compression ther-apy. It has been shown that compression increases the heal-ing rates of venous leg ulcers compared with no compression (O’Meara 2009). This treatment is often applied with other inter-ventions, such as debridement (Tang 2012), topical agents (Briggs 2012;Robson 2006), physical agents (Aziz 2011;Cullum 2010;
Flemming 1999), dressings (Palfreyman 2007).
Description of the intervention
The optimal wound healing environment is one where the wound is kept covered and moist, rather than left open to the air. Standard treatment for venous leg ulcers should include therapeutic com-pression (may be applied by bandages) in addition to a dressing, except when otherwise indicated (O’Meara 2009;Robson 2006). Dressings are applied underneath bandages or stockings with the aim of protecting the wound and providing a moist environment to aid healing. Nowadays, several types of dressing seek to achieve a moist environment, the aim of which is to promote re-epithelial-isation of the wound, providing comfort, controlling exudate and helping to prevent bandages and stockings adhering to the wound bed. The ideal conditions required for wound healing in terms of dressing application have been explained as follows: maintenance of a moist wound environment without risk of maceration; avoid-ance of toxic chemicals, particles or fibres in the dressing fabric; minimisation of number of dressing changes; and maintenance of an optimum pH level (NPF 2011).
The primary intervention of interest in this review is hydrogel dressings used in the treatment of venous leg ulcers. The aim of hydrogel dressings is to promote pain relief, comfort and also to favour autolytic debridement (natural enzymic removal of dead tissue) (Mandelbaum 2003). The dressings consist of a starch polymer and up to 96% water. They are supplied in two forms; flat sheets (e.g. ActiFormCool (Activa)), or amorphous
hydro-2 Hydrogel dressings for venous leg ulcers (Protocol)
gel (e.g. Aquaflo (Covidien)). Some of the hydrogels are associ-ated with alginates (e.g. Nu-Gel, Purilon Gel) (NPF 2011), which have a higher capacity for absorption and chemical debridement (Mandelbaum 2003). The advantages of hydrogel dressings are that they can be used during several phases of healing, and may pro-mote relief and comfort, however, they do require a secondary cov-ering. Hydrogel dressings also may reduce pain in painful wounds (Bradbury 2008). The interval between dressing changes varies according to the type of hydrogel dressing: amorphous hydrogel may require daily changes (Mandelbaum 2003), while hydrogel sheet dressings may last for up to seven days.
There is a broad choice of dressings available to treat wounds such as venous leg ulcers. For ease of comparison this review has classed dressings into groups according to the broad categories of the Nurse Prescribers’ Formulary 2011 (NPF 2011), that is, basic, advanced, anti-microbial and specialist wound dressings (see
Appendix 2). Dressing names, manufacturers and distributors may vary between countries.
How the intervention might work
The most appropriate dressing for wound management depends not only upon the type of wound but also on the stage of the healing process. Dressings for moist wound healing need to ensure that the wound remains moist, and free of clinical infection and excessive slough (dead tissue), but avoid peri-wound maceration (NPF 2011).
Hydrogel dressings, classified as an advanced wound dressing by the Nurse Prescribers’ Formulary, are designed to control the en-vironment for wound healing by donating fluids to dry sloughy wounds, and by facilitating autolytic debridement of necrotic tis-sue. Some hydrogel dressings also have the ability to absorb lim-ited amounts of exudate or rehydrate a wound, depending on the wound’s moisture levels (NPF 2011).
Why it is important to do this review
Chronic venous ulcer healing is a complex clinical situation that causes considerable economic impact, and adversely affects the quality of life for those who suffer from them.
Hydrogel dressings can be used to deslough wounds by promoting autolytic debridement through moisture to re-hydrate, soften and liquefy non-viable tissue present on the wound surface. There is no current up-to-date evidence to inform clinicians of the effects of hydrogel dressings in treating venous leg ulcers (Palfreyman 2007). The effect of hydrogel dressings compared with other dressings and conventional methods of care for venous ulcers needs to be established.
O B J E C T I V E S
To assess the effects of hydrogel wound dressings for healing venous leg ulcers in people in any care setting.
M E T H O D S
Criteria for considering studies for this review
Types of studies
Randomised controlled trials (RCTs), either published or unpub-lished, that have evaluated the effects of any type of hydrogel wound dressing in the treatment of venous leg ulcers irrespective of publication status or language will be included. Trials reported in abstract form only will be eligible for inclusion, provided ade-quate information is either presented in the abstract or available from the trial author. Studies using quasi-randomisation will be excluded.
Types of participants
We will include people of any age in any care setting with a di-agnosed venous leg ulcer determined either by clinical evaluation, or complementary laboratory tests (e.g. duplex ultrasonography, plethysmography and venography), or both (Collins 2010), using the definition of a positive diagnosis given by the authors. Trials that include people with wounds of other aetiology (e.g. pressure ulcers), or trials of mixed populations (venous ulcers along with arterial or diabetic ulcers) will be excluded, unless the results for the subgroup of people with venous leg ulcers are reported sep-arately or if the majority of participants (≥75% in each arm) have leg ulcers of venous aetiology. The review authors will at-tempt to contact trial authors to obtain the relevant data, if data from subgroups of people with venous leg ulcers are not reported separately. Studies of people with infected wounds will not be in-cluded, because hydrogel dressings are not indicated (prescribed) for this type of wound.Trials evaluating skin grafting are covered elsewhere and will be excluded from this review (Jones 2007).
Types of interventions
The intervention will be hydrogel dressings used as a treatment for venous leg ulcers. Comparators will be any other dressing, no dressing or another hydrogel dressing. For ease of comparison we will categorise dressings according to the Nurse Prescribers’ For-mulary (NPF 2011). We will use generic names where possible, also providing trade names and manufacturers where these are available. It is important to note, however, that manufacturers and distributors of dressings may vary from country to country, and dressing names may also differ.We will not include trials evaluat-ing hydrogel dressevaluat-ings impregnated with antimicrobial, antiseptic
3 Hydrogel dressings for venous leg ulcers (Protocol)