www.jped.com.br
ARTIGO
ORIGINAL
Effects
of
erythromycin
on
␥
-glutamyl
cysteine
synthetase
and
interleukin-1

in
hyperoxia-exposed
lung
tissue
of
premature
newborn
rats
夽
Cheng
Cai
a,∗,
Gang
Qiu
a,
Xiaohui
Gong
a,
Yihuan
Chen
ae
Huanhu
Zhao
baDepartamentodeNeonatologia,HospitaldaCrianc¸adeXangai,UniversidadeJiaoTongdeXangai,Xangai,China bCentrodePesquisaemMedicamentosTradicionaisdeGruposÉtnicosMinoritáriosChineses,UniversidadeCentral
paraNacionalidades,Pequim,China
Recebidoem8denovembrode2013;aceitoem14dejaneirode2014
KEYWORDS Erythromycin; Hyperoxia; Lunginjury; Glutathione; Interleukin-1-beta
Abstract
Objective: Toexploretheeffectoferythromycinonhyperoxia-inducedlunginjury.
Methods: One-day-oldpretermoffspringSprague-Dawley(SD)ratswererandomlydividedinto fourgroups:group1,air+sodiumchloride;group2,air+erythromycin;group3,hyperoxia+ sodiumchloride;andgroup4,hyperoxia+erythromycin.Atone,seven,and14daysof expo-sure,glutathione(GSH)andinterleukin-1beta(IL-1beta)weredetectedbydouble-antibody sandwichenzyme-linkedimmunosorbentassay(ELISA),andbicinchoninicacid(BCA)wasused todetectGSHprotein.␥-glutamine-cysteinesynthetase(␥-GCS)mRNAwasdetectedbyreverse transcription-polymerasechainreaction(RT-PCR).
Results: Comparedwithgroup1,expressionsofGSHand␥-GCSmRNAingroup3were signifi-cantlyincreasedatoneandsevendaysofexposure(p<0.05),butexpressionof␥-GCSmRNA wassignificantlyreducedat14days;expressionofIL-1betaingroup3wassignificantly incre-asedatsevendaysofexposure(p<0.05),andwassignificantlyreducedat14days.Compared withgroup3,expressionsofGSHand␥-GCSmRNAingroup4weresignificantlyincreasedat one, seven,and14 daysofexposure(p<0.05),butexpressionsofGSHshowedadownward trendat14days;expressionofIL-1betaingroup4wassignificantlyreducedatoneandseven daysofexposure(p<0.05).
Conclusions: Changesinoxidant-mediatedIL-1betaandGSHareinvolvedinthedevelopment ofhyperoxia-inducedlunginjury.Erythromycinmayup-regulatetheactivityof␥-GCS, increa-singtheexpressionofGSH,inhibitingthelevelsofoxidant-mediatedIL-1betaandalleviating hyperoxia-inducedlunginjuryviaanantioxidanteffect.
©2014SociedadeBrasileiradePediatria.PublishedbyElsevierEditoraLtda.Allrightsreserved.
DOIserefereaoartigo:http://dx.doi.org/10.1016/j.jped.2014.01.013
夽 Comocitaresteartigo:CaiC,QiuG,GongX,ChenY,ZhaoH.Effectsoferythromycinon␥-glutamylcysteinesynthetaseandinterleukin-1 inhyperoxia-exposedlungtissueofprematurenewbornrats.JPediatr(RioJ).2014;90:493---9.
∗Autorparacorrespondência.
E-mail:caicheng2004@163.com(C.Cai).
PALAVRAS-CHAVE Eritromicina; Hiperóxia; Lesãopulmonar; Glutationa; Interleucina-1beta
Efeitosdaeritromicinasobrea␥-glutamil-cisteína-sintetaseeainterleucina-1
notecidopulmonarexpostoàhiperóxiaderatosrecém-nascidosprematuros
Resumo
Objetivo: Exploraroefeitodaeritromicinasobrelesõespulmonaresinduzidasporhiperóxia.
Métodos: UmaprolederatosSprague-Dawley(SD)prematuroscomumdiadevidafoidividida aleatoriamente emquatro grupos:grupo1ar+cloretodesódio,grupo2ar+eritromicina, grupo3hiperóxia+cloretodesódioegrupo4hiperóxia+eritromicina.Comum,setee14 diasdeexposic¸ão,foramdetectadasGlutationa(GSH)eInterleucina-1beta(IL-1beta)pelo ensaioimunossorventeligadoàenzima(ELISA),eoácidobicinconinico(BCA)foiutilizadopara detectaraproteínaGSH.OmRNAda␥-glutamil-cisteina-sintetase (␥-GCS)foidetectadopor reac¸ãoemcadeiadapolimeraseviatranscriptasereversa(RT-PCR).
Resultados: Comparadasao grupo1,asexpressões domRNAdaGSHeda␥-GCSnogrupo3 aumentaramsignificativamentecomumesetediasdeexposic¸ão(p<0,05),porémaexpressão demRNAda␥-GCSdiminuiusignificativamenteaos14dias;aexpressãodeIL-1betanogrupo 3aumentousignificativamenteaos7diasdeexposic¸ão(p<0,05)ediminuiusignificativamente aos14 dias. Comparadas ao grupo3, as expressões domRNAda GSHe da␥-GCS nogrupo 4aumentaramsignificativamentecomum, setee14 diasde exposic¸ão(p<0,05), porémas expressõesdeGSHmostraramumatendênciadequedaaos14dias;aexpressãodeIL-1beta nogrupo4foireduzidasignificativamentecomumesetediasdeexposic¸ão(p<0,05).
Conclusões: As variac¸ões de IL-1 beta e GSH mediadas por oxidantes estão envolvidas no desenvolvimento de lesão pulmonar induzida por hiperóxia. A eritromicina poderáregular positivamenteaatividadeda␥-GCS,aumentandoaexpressãodeGSH,inibindoosníveis de interleucina-1betamediadaporoxidanteealiviandoalesãopulmonarinduzidaporhiperóxia pormeiodeumefeitoantioxidante.
©2014SociedadeBrasileiradePediatria.PublicadoporElsevierEditoraLtda.Todososdireitos reservados.
Introduc
¸ão
Com o rápido desenvolvimento da tecnologia de saúde materna e da perinatologia, a taxa de sobrevida de neonatos prematuros tem aumentado, principalmente em neonatos com peso muito baixo ao nascer (VLBWI).1
Entretanto, os pulmões de neonatos prematuros normal-mente são imaturos e estão em contato direto com o oxigênio,sendoumdosórgãosmaissensíveisàtoxicidadedo oxigênio.Ademais,neonatosprematurosprecisamreceber váriasterapiasdeoxigênioporumlongoperíodoapóso nas-cimento.Infelizmente,semdúvidas,issoagravaoestresse oxidativonospulmõesimaturosdeneonatosprematurose podecausarlesãopulmonaragudaecrônica.2
A lesão pulmonar induzida por hiperóxia é a principal causadedoenc¸asrespiratóriascrônicasdesdeainfânciaaté avidaadulta,e setornouumdos problemasmaisdifíceis naunidadedeterapiaintensivaneonatal.Contudo,a etio-logiaeapatogênesenãosãototalmente compreendidas.3
Atualmente, a maioria dos pesquisadores acredita que o tecidopulmonarimaturodiretamenteexpostoaoambiente hiperóxicoresultaemestresseoxidativo,quetemumpapel crucialnodesenvolvimentodelesãopulmonarinduzidapor hiperóxia.4,5Oestresseoxidativopodeperturbaroequilíbrio
entreoxidanteseantioxidanteseéumdosprincipaisfatores patogênicos.6 AGSH é umimportante antioxidante
intra-celulare possuiumpapelfundamental na manutenc¸ão da integridadeenaprevenc¸ãodedanosoxidativosnascélulas epiteliaisalveolares.7A␥-GCSéaenzimaquelimitaataxa
desínteseproteicadaGSHeregulaosníveisintracelulares daGSH.8 AIL-1beta está presentena fase inicialda
dis-plasia broncopulmonar (DBP) em neonatos prematuros e poderáterumpapelimportantenodesenvolvimentodaDBP. Contudo,apatogêneseexatadaDBPpermaneceobscurae ostratamentosclinicamenteefetivoscontinuamlimitados. Oefeitonãoantibacterianodaeritromicinaatraiu gradu-almenteaatenc¸ãodamaioriadospesquisadores.9Ela
apre-senta muitas func¸ões fisiológicas importantes, incluindo: atividade antibacteriana eficaz, efeitos anti-inflamatórios nãoespecíficosnaasma,regulac¸ãoimunológica,aderência química induzida,motilidadegastrointestinalpromovidae efeitoantitumoral.10Aeritromicinatratademaneiraefetiva
muitas doenc¸as inflamatórias infecciosas não bacterianas crônicas,algumasdasquaisapresentamreac¸õesredoxnão balanceadas.11 Entretanto, a maneira como os níveis de
expressãodeGSH,␥-GCSeIL-1betasãoafetadosnotecido pulmonarexpostoàhiperóxiacontinuaindefinida.No pre-senteestudo,exploramosoefeitodaeritromicinasobrea lesãopulmonarinduzidaporhiperóxiaemratosprematuros e estudamos osníveis deexpressão de GSH, ␥-GCSe IL-1 betaemtecidospulmonaresderatosprematuros.
Materiais
e
métodos
Modelosanimaisexperimentais12 eagrupamento
Pequim,China,forneceuRatosSDadultos(compesoentre 200-250g,incluindo100 fêmease 35machos).Oprimeiro diadegestac¸ãofoiregistradoaodetectarespermanaregião vaginalderatasfêmeaspormeiodeanálisemicroscópica. No21◦ dia degestac¸ão(período=22dias),osfetos foram retiradospormeiodeumahisterectomia.OsratosSD pre-maturoscomumdiadevidaforamdivididosaleatoriamente em quatro grupos (oito filhotes em cada grupo): o grupo 1recebeuar(21%O2)+cloretodesódio;ogrupo2recebeu ar+eritromicina;ogrupo3,hiperóxia+cloretodesódio;e ogrupo4,hiperóxia+eritromicina.Osratosnosgruposcom arforamexpostosaarambiente,enquantoosqueestavam emgruposcomhiperóxiaforamexpostosaconcentrac¸õesde O2superioresa85%edeCO2inferioresa0,5%,com tempe-raturasmantidasa25-26◦Ce60-70%deumidade,eosníveis deoxigênioe CO2nacâmaraforammonitorados continua-mentecomanalisadoresdegás.12 Naveiacaudaldosratos
prematuros,foraminjetadoscloretodesódio(0,15mL/kg) nosgrupos quereceberamcloreto desódioe eritromicina (50mg/kg)nosgruposquereceberameritromicina.Comum, sete e 14 dias de exposic¸ão, oito filhotes de cada grupo foramanestesiados e sacrificados. Aproteína foi extraída do pulmão esquerdo, e o pulmão direito foi congelado e armazenadoa-70◦CemumrefrigeradorparaRT-PCR.
O estudo foi aprovado por decisão docomitê deética egestãodebem-estardeanimaisexperimentais do hospi-tal dacrianc¸a deXangai, Universidade JiaoTong, Xangai, China.
Detecc¸ãodeGSHeIL-1betanohomogenato dotecidopulmonarpelotesteELISA
Os tecidos pulmonares foram coletados e as proteínas totais extraídasutilizando um kit de extrac¸ão de proteí-nas.Aconcentrac¸ãodeproteínasfoimensuradautilizando ométodoBradford (LaboratórioBio-Rad,CA,EUA).AGSH e a IL-1beta foramdetectadasno homogenatodo tecido pulmonarpor kitsdo testeELISAobtidos daNanjing Jian-cheng Biological Technology Co. Ltd., Nanquim, China, e daWuhanHuameiCusabio Biological TechnologyCo.Ltd., Wuhan,China,respectivamente.
Para permitir que todos os reagentes alcanc¸assem a temperaturaambienteeorganizarerotularonúmero neces-sáriodefileiras,100Ldereagentes foramadicionadosa poc¸osdeplacasdepoliestirenodoELISA,eospoc¸osforam minuciosamente lavados com tampão fosfato-salino (PBS) contendo 0,1% de Tween-20 (PBS-Tween) (Bio-Rad Labo-ratories, CA, USA) após cada etapa de incubac¸ão. Para preparartodososreagentes,incluindopadrõesdetrabalhoe amostras,100Ldospadrões,controlesouamostrasforam adicionadosaospoc¸oseincubadosporduas horasa37◦C. Apósalavagemdospoc¸os,100Ldeanticorpospoliclonais deGSH(ouIL-1beta)decabraantirratoforamadicionadosa cadapoc¸o(incubac¸ãopor30mina37◦C).Apósumaextensa lavagem,100LdeimunoglobulinaG(IgG)decoelhos anti-cabraforamadicionadosàcadapoc¸oporumahoraa37◦C. Apósaincubac¸ãodasoluc¸ãodesubstratoedasoluc¸ãode paragem, a leitura da densidadeóptica de cada poc¸o foi feitaem30minutos,utilizandoumaleitorademicroplacas ajustadapara450nm.
Detecc¸ãodeconcentrac¸õesproteicasdeGSH emhomogenatosdotecidopulmonarporácido bicinconínico(BCA)
Após o protocolo padrão para o Kit de Ensaio de Pro-teínaMicroBCA(BeijingBaitaikeBiologicalTechnologyCo., Pequim,China),asoluc¸ãodetrabalhoé:Misturarumvolume doreagenteCcom25volumesdoreagenteBe,então, adi-cionar26volumesdoreagenteAàmisturaC/B.Ovalordo pHdasoluc¸ãodetrabalhofoi11,16±0,06,medidocomum pHmetroOrion310(ThermoScientific,MA,USA).Opadrão deproteínas completamentedissolvidas (5mg/mL), 10L diluídosem100L,deformaqueaconcentrac¸ãofinalfosse 0,5mg/ml,seriaopadrãodediluic¸ãodeacordocom0,1, 2, 4, 8, 12, 16, 20L, respectivamente, para a placa de 96poc¸os, adicionarágua ultrapuraaté20L,amostrasde 10Le 200LdeBCAadicionados àsoluc¸ãode trabalho, batendogentilmentenaplacaparagarantiramisturae res-friandoasamostrasde37◦Catéatemperaturaambientepor 30-60minutos.Cadamedic¸ãofoifeitaemduplicata.Todas as absorbâncias foram corrigidas pela réplica em branco correspondente. A absorbância dasoluc¸ão em branco foi 0,048±0,006.Aabsorbânciaem562nmfoimedidaporum espectrofotômetroutilizandocuvetesdevidrocom compri-mentodopercursoópticode0,1cm.
ExpressãodemRNAda␥-GCSdetectadaporRT-PCR
O RNA total foi extraído utilizando o Sistema de Isola-mento do RNA Total RNAgent (Promega Corporation, WI, USA),deacordocomasinstruc¸õesdofabricante.Apureza e aproduc¸ão deRNA total foramdeterminadas espectro-fotometricamentecom amedic¸ão daabsorbânciade uma alíquota a 260nm e 280nm. O RNA (4g) foi transcrito reversamenteem50LdeDNAcomplementar(cDNA) utili-zandoo sistemade Transcriptase Reversa M-MLV (Jingmei Biotech Ltd, Shenzhen, China). As primeiras sequências foram projetadas pela Shanghai Biology Engineering Co., China, de acordo com a literatura: ␥-GCS, transcric¸ão: 5’-TTGGCAGCCTTCCTGATTTC-3’, transcric¸ão reversa: 5’--AACTTCTCCACAACCCTCTG-3’,tamanhodoproduto:78pb;
-actina, transcric¸ão: 5’-AAC GCAGCTCAGTAACAGTC-3’, transcric¸ãoreversa:5’-ATCCGTAAAAGCCTCTATGC-3’ tama-nho do produto: 280 pb. As misturas de reac¸ão da PCR com ␥-GCS e -actina foramsubmetidas à incubac¸ão por cinco minutos a 94◦C, seguida de 35 ciclos de 94◦C por 45 segundos, 50◦C por um minuto e 72◦C por 30 segundos.Umaextensãofinalfoirealizadaa72◦Cpordez minutos.OsprodutosdaPCRforamseparadospor eletrofo-reseemgeldeagarosea2%,tingidoscombrometodeetídio (0,5g/mL),sendoobservadosutilizandoum transilumina-dorUVeavaliadosatravésdeumsistemadeimagemcomgel GSD-8000(UVPCo.,Cambridge,ReinoUnido),aocomparar aintensidadedasfaixasdoprodutoobjetodeanálisecoma intensidadede-actinautilizadacomopadrãointerno.
Análiseestatística
0 2 4 6 8 10 12 14
14d 7d
1d
Dia
Expressão da proteína GSH
(ng/ml)
Grupo 1
Grupo 2
Grupo 3
Grupo 4
a
a
b b
b
Figura1 ExpressãodaproteínaGSHdetectadapelotesteELISAempulmõesderatosprematuros. GSH,Glutationa;ELISA,ensaioimunossorventeligadoàenzima.
ap<0,05,emcomparac¸ãoaogrupo1.
bp<0,05,emcomparac¸ãoaogrupo3.
diferenc¸asestatísticasentreosgruposforamtestadaspela análisedevariância(ANOVA)eosdadosentredoisgrupos foramanalisadosutilizadootesteq.Umvalordepinferior a0,05foiconsideradoestatisticamentesignificativo.
Resultados
EfeitodaeritromicinasobreaGSHemtecido pulmonarexpostoàhiperóxia
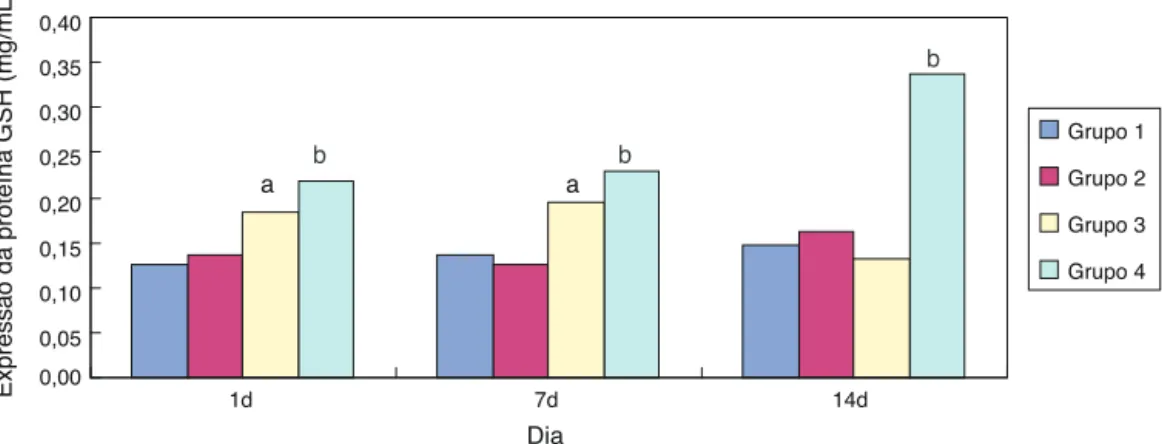
Emcomparac¸ãoao grupo1, aexpressão deGSHnogrupo 3 aumentou significativamente (p<0,05) com um e sete diasdeexposic¸ão,porémnãomostrounenhumareduc¸ão sig-nificativa(p>0,05)aos14dias.Emcomparac¸ãoaogrupo3, aexpressãodeGSHnogrupo4aumentousignificativamente comum,setee14diasdeexposic¸ão(p<0,05);atendência geraldiminuiuapós14dias(figs.1e2).
EfeitodaeritromicinasobreaIL-1betaemtecido pulmonarexpostoàhiperóxia
Em comparac¸ão ao grupo 1, a expressão de IL-1beta no grupo3aumentousignificativamente(p<0,05)aossetedias
de exposic¸ão; sua expressão diminuiu significativamente (p<0,05)aos14diasdeexposic¸ão.Emcomparac¸ãoaogrupo 3,aexpressãodeIL-1betanogrupo4diminuiu significati-vamentecomumesetediasdeexposic¸ão(p<0,05)(fig.3).
Efeitodaeritromicinasobrea␥-GCSemtecido pulmonarexpostoàhiperóxia
Emcomparac¸ãoaogrupo1,aexpressãodemRNAda␥-GCS nogrupo3aumentousignificativamente(p<0,05)comume setediasdeexposic¸ão;suaexpressãodiminuiu significativa-mente(p<0,05)aos14diasdeexposic¸ão.Emcomparac¸ão aogrupo3,aexpressãodemRNAda␥-GCSnogrupo4 dimi-nuiusignificativamentecomum,setee14diasdeexposic¸ão (p<0,05) (fig. 4). A intervenc¸ão de eritromicina regulou positivamente a atividade domRNA da␥-GCS, particular-mentenostecidospulmonaresexpostosàhiperóxia.
Discussão
Com base nas características histológicas, o desenvolvi-mento do pulmão defetos de ratos podeser divididoem
0,00 0,05 0,10 0,15 0,20 0,25 0,30 0,35 0,40
14d 7d
1d
Dia
Expressão da proteína GSH (mg/mL)
Grupo 1
Grupo 2
Grupo 3
Grupo 4
b b
b
a a
Figura2 ExpressãodaproteínaGSHdetectadaporBCAempulmõesderatosprematuros. GSH,Glutationa;BCA,ácidobicinconínico.
ap<0,05emcomparac¸ãoaogrupo1.
0 5 10 15 20 25 30
14d 7d
1d
Dia
Expressão da proteína IL-1 beta
(ng/mL)
Grupo 1
Grupo 2
Grupo 3
Grupo 4 b
b a
a a
Figura3 ExpressãodaproteínaIL-1betadetectadapelotesteELISAempulmõesderatosprematuros. IL-1beta,Interleucina-1beta;ELISA,ensaioimunossorventeligadoàenzima.
ap<0,05emcomparac¸ãoaogrupo1.
bp<0,05,emcomparac¸ãoaogrupo3.
quatro períodos: embrionário (0 ∼ 13 d), glandular (14
∼ 18 d), fase canalicular (19 ∼ 20 d) e sacular (21 ∼
22 d). O período sacular durante o desenvolvimento do pulmão humano corresponde a 28-34 semanas de idade gestacional, idade de nascimento da maioria dos neona-tos prematuros. O desenvolvimento pós-natal do pulmão dosratosédivididoemtrêsperíodos:períododeexpansão (1-4 dias após o nascimento),período alveolar (4-13 dias após o nascimento)e período de crescimentobalanceado (14-21 dias após o nascimento).Dessa forma,os diferen-tespontos detemporepresentamasdiferentesetapasde desenvolvimentopulmonaremneonatosprematurosapóso nascimento,respectivamente.
Apatogêneseeaprevenc¸ãodaDBPemneonatos prema-turosfez avanc¸ossignificativos recentemente;contudo, a patogêneseexatadaDBPcontinuaincerta,eotratamento efetivoaindaésignificativamenterestrito.13Osantibióticos
macrolídeos(AM) contêm a estrutura química decarbono 12-22 e pertencem àqueles de carbono com anel de lac-tona.AEritromicina Apodeinibirasecrec¸ãodecitocinas pró-inflamatórias, como o fatordenecrose tumoral-␣ e a IL-1beta.14Ademais,elaéumantibióticodelargoespectro
e possui atividade antibacteriana contra bactérias gram--positivasealgumasgram-negativas,bactériasanaeróbicas,
Legionella,Chlamydia,micoplasmaeRickettsia.15Aprática
clínica de longo prazo e estudos farmacológicos detalha-dosmostraram que osAM não apresentamapenas efeitos antibacterianos, mas possuem também propriedades de regulac¸ão não específicas anti-inflamatórias, antialérgicas e imunes.16 O principal papel dos antibióticos em
algu-masdoenc¸asinflamatóriaspulmonarescrônicaspoderáestar relacionadoàinibic¸ãodaexplosãooxidativadeneutrófilose aliberac¸ãodemediadoresinflamatórios.Alémdisso,osAM sãoeficazesnaprevenc¸ãoetratamentodealgumasdoenc¸as respiratórias,incluindoasma,fibrosepulmonar, panbronqui-olitedifusaealgumasdoenc¸asinflamatóriasnãoinfecciosas, comodoenc¸asdosangue,doenc¸asdepeleecâncer,eessas func¸ões não possuem relac¸ão alguma com as atividades antibacterianas.17
Aglutationaéumtripeptídeoquecontémmaterial sulfô-nico,compostodeglicina,ácidoglutâmicoecistina.A␥-GCS éaenzimaquelimitaataxadasíntesedeGSH,queregulaos níveisdeGSHintracelular.18AGSHéativadapelosistemade
oxidac¸ão/reduc¸ão in vivo, que fornece o redutor para a cistinae inibe aproduc¸ão de várias substâncias docorpo noprocessodeoxidac¸ãodasespéciesreativasdeoxigênio (ROS),inativandoaatividade daperoxidase damembrana einibindoasROS,reduzindo,assim,asROS.Amaioriados
0,00 0,05 0,10 0,15 0,20 0,25 0,30 0,35 0,40
14d 7d
1d
Dia
Expressão de mRNA da
γ
-GCS
Grupo 1
Grupo 2
Grupo 3
Grupo 4
b
b b
a
a
Figura4 ExpressãodemRNAda␥-GCSdetectadaporRT-PCRempulmõesderatosprematuros.
␥-GCS,␥-glutamil-cisteina-sintetase;RT-PCR,reac¸ãoemcadeiadapolimeraseviatranscriptasereversa.
ap<0,05,emcomparac¸ãoaogrupo1.
pesquisadoresreconheceuqueasROScausadasporestresse oxidativopossuemumpapelimportantenodesenvolvimento dalesãopulmonarinduzidaporhiperóxia.19Diversosestudos
identificaramqueexperimentosinvivoein vitromostram que, como um importante antioxidante, a GSH desempe-nhouumpapeldedestaquenamanutenc¸ãodaintegridade dascélulasepiteliaisdasviasaéreas,resistindoàlesãoeà inflamac¸ãopulmonares.20
Nopresenteestudo,emcomparac¸ãoaogrupoexpostoa ar+cloretodesódio,aexpressãodeGSH nostecidos pul-monaresderatosprematurosaumentousignificativamente apósaintervenc¸ãocomeritromicinanosdias1,7e 14no grupoexpostoaeritromicina+cloretodesódio(p<0,05). Suaexpressãoaumentousignificativamentenodia1enodia 7apósaexposic¸ãoàhiperóxianogrupoexpostoà hiperó-xia+cloretodesódio,ediminuiusignificativamentenodia 14.AexpressãodeGSHnogrupoexpostoahiperóxia+ eri-tromicinaaumentou significativamenteapósaintervenc¸ão comexposic¸ãoàhiperóxiaeeritromicinanosdias1,7e14, porémapresentouumatendênciadequedasignificativano dia14.Adetecc¸ãodaexpressãodeGSHporBCAconfirmouos resultadosdoELISA.Apósaexposic¸ãoàhiperóxianosdias1e 7,aexpressãodeGSHaumentousignificativamente.Ocorpo podeapresentaralgummecanismodeautoprotec¸ãoepode resistiraumalesãocausadaporhiperóxia.ConformeasROS intracelularesaumentam,osgrupossulfúricosdecisteínana GSHapresentamumaforteatividadedeafinidadeepodem serutilizadoscomoalvoseletrofílicosquesecombinamcom asROS. Eles tambémpossuem umafunc¸ão na eliminac¸ão dasROS e na peroxidac¸ão lipídica, evitando, assim, dano na membrana da célula alveolar.Contudo, a exposic¸ão à hiperóxia fez com que a proteína GSH nas células epite-liais alveolares fosse gravemente danificada por estresse oxidativonodia 14,eaexpressãodeGSH nãoapresentou diminuic¸ãosignificativa.
A␥-glutamil-cisteina-sintetase éa enzimaque limitaa taxadesínteseproteicadaGSH,queregulaosníveis intrace-lularesdaGSH.21Esteestudomostrouqueaintervenc¸ãode
eritromicina pode inibir a regulac¸ão positiva dos níveis de proteína da GCS nos tecidos pulmonares por meio da exposic¸ãoàhiperóxianosdias1e7(p<0,05).Aintervenc¸ão da eritromicina não apresentou influência óbvia sobre a exposic¸ão à hiperóxia no dia 14, porém a expressão de mRNAda␥-GCSaumentousignificativamentenosdias7e14 (p<0,05),oquepodeestarrelacionadoàsproteínas regu-latórias relevantes após a transcric¸ão de mRNA da␥-GCS devido ao dano por exposic¸ão à hiperóxia, resultando na inibic¸ão,pelaeritromicina,daregulac¸ãopositivadosníveis deproteínadaGCSpormeiodeexposic¸ãoàhiperóxia.
Reac¸ões infecciosas e inflamatórias são fatores funda-mentaisna patogênese da DBP em neonatos prematuros, fatoconfirmadopor meiodeestudosclínicos eanimais.22
Foi relatado que a IL-1 beta, como uma citocina pró--inflamatória, possui uma posic¸ão central na patogênese daDBPe umimportante papel patogênicoem lesões pul-monaresagudase crônicas em neonatosprematuros.23 No
presente estudo, descobrimos que, em comparac¸ão aos gruposexpostosaar,aexpressãodaIL-1betanotecido pul-monarderatosprematurosdosgruposexpostosàhiperóxia aumentousignificativamentenodia7ediminuiunodia14. Ademais,comparadaaosgruposexpostosacloretodesódio, aexpressãodaIL-1betadiminuiusignificativamentenos
gru-posexpostosàeritromicinanosdias1e7.Poroutrolado,a expressão de GSH nostecidos pulmonares aumentou após aintervenc¸ãodaeritromicinanosdias1,7e14.Esses resul-tadosmostraramqueoprincipalpapeldaeritromicinapode estarrelacionadoàinibic¸ãodaexplosãooxidativade neutró-filose àliberac¸ãodemediadoresinflamatórios.Assim,um dosprincipaismecanismosdosAMaotrataraDBPem neo-natosprematurospodeserainibic¸ãodaexplosãooxidativa deneutrófilosealiberac¸ãodemediadoresinflamatórios.
Em resumo, a eritromicina pode inibir o surto oxida-tivodegranulócitos neutrosnotecidopulmonar,melhorar a func¸ão antioxidante daGSH, inibira liberac¸ão da cito-cinainflamatóriaIL-1betae,porisso,possuiumimportante papelnareduc¸ãodoestresseoxidativonodesenvolvimento de lesão pulmonar induzida por hiperóxia, o que poderá estabelecerumanovabaseteóricaparaotratamentoclínico delesãopulmonarinduzidaporhiperóxia.
Financiamento
EstetrabalhofoifinanciadopeloComitêdeCiênciae Tec-nologiadeXangai(NúmerodoProjeto:134119a0500).
Conflitos
de
interesse
Osautoresdeclaramnãohaverconflitosdeinteresse.
Referências
1.JobeAJ.ThenewBPD:anarrestoflungdevelopment.Pediatr Res.1999;46:641---3.
2.JobeAH.Thenewbronchopulmonarydysplasia.CurrOpin Pedi-atr.2011;23:167---72.
3.FarstadT,BratlidD,MedbøS,MarkestadT,NorwegianExtreme PrematurityStudyGroup.Bronchopulmonarydysplasia- preva-lence,severityand predictivefactorsina nationalcohortof extremelyprematureinfants.ActaPaediatr.2011;100:53---8. 4.SaugstadOD.Bronchopulmonarydysplasia-oxidativestressand
antioxidants.SeminNeonatol.2003;8:39---49.
5.FernandesLV,GoulartAL, SantosAM,BarrosMC,GuerraCC, KopelmanBI.Neurodevelopmentalassessmentofverylowbirth weightpreterminfantsatcorrectedageof18-24 monthsby BayleyIIIscales.JPediatr(RioJ).2012;88:471---8.
6.DundarozR, Erenberk U, TurelO, DemirAD, OzkayaE, Erel O. Oxidativeand antioxidative statusof childrenwithacute bronchiolitis.JPediatr(RioJ).2013;89:407---11.
7.Hassanin KM, Abd El-Kawi SH, Hashem KS. The prospective protectiveeffectofseleniumnanoparticlesagainst chromium--inducedoxidative and cellular damage inratthyroid. IntJ Nanomedicine.2013;8:1713---20.
8.Kim BY, Kwak SY, Yang JS, Han YH. Phosphorylation and stabilizationofc-MycbyNEMOrenderscellsresistantto ioni-zing radiation through up-regulation of ␥-GCS. Oncol Rep. 2011;26:1587---93.
9.Swords WE,Rubin BK.Macrolide antibiotics,bacterial popu-lations and inflammatory airway disease. Neth J Med. 2003;61:242---8.
10.Amado-RodríguezL,González-LópezA,López-AlonsoI,Aguirre A,AstudilloA,Batalla-SolísE,etal.Anti-inflammatoryeffects ofclarithromycininventilator-inducedlunginjury.RespirRes. 2013;14:52.
ligaseandglutathionesynthetaseinresponsetocadmiumand nonylphenolinChironomusriparius.EnvironToxicolPharmacol. 2013;36:265---73.
12.YamJ,FrankL,RobertsRJ.Oxygentoxicity:comparisonoflung biochemicalresponsesinneonatalandadultrats.PediatrRes. 1978;12:115---9.
13.HallidayHL,EhrenkranzRA,DoyleLW.Early(<8days)postnatal corticosteroidsforpreventingchroniclungdiseaseinpreterm infants.CochraneDatabaseSystRev.2010;1:CD001146. 14.CarlsonS,MarlerL,NamSJ,SantarsieroBD,PezzutoJM,Murphy
BT.Potentialchemopreventiveactivityofanewmacrolide anti-bioticfrom a marine-derivedMicromonosporasp.Mar Drugs. 2013;11:1152---61.
15.SatoK, SugaM,Akaike T, FujiiS, Muranaka H,Doi T, etal. Therapeuticeffectoferythromycinoninfluenzavirus-induced lunginjuryinmice.AmJRespirCritCareMed.1998;157:853---7. 16.GotfriedMH.Macrolidesforthetreatmentofchronicsinusitis,
asthma,andCOPD.Chest.2004;125:52S---60S,quiz60S-61S. 17.TamaokiJ.The effects ofmacrolides oninflammatory cells.
Chest.2004;125:41S---50S,quiz51S.
18.RahmanI,vanSchadewijkAA,HiemstraPS,StolkJ,vanKrieken JH,MacNeeW,etal.Localizationofgamma-glutamylcysteine
synthetasemessengerrna expressioninlungsofsmokersand patientswithchronicobstructivepulmonarydisease.FreeRadic BiolMed.2000;28:920---5.
19.Northway Jr WH, Rosan RC, Porter DY. Pulmonary disease following respirator therapy of hyaline-membrane dise-ase. Bronchopulmonary dysplasia. N Engl J Med. 1967;276: 357---68.
20.Rahman I, MacNee W. Oxidative stress and regulation of glutathione in lung inflammation. Eur Respir J. 2000;16: 534---54.
21.ChenHH,KuoMT.Roleofglutathioneintheregulationof Cis-platin resistance in cancer chemotherapy. MetBased Drugs. 2010:2010,pii:430939.
22.RochaG.Chorioamnionitisandlunginjuryinpretermnewborns. CritCareResPract.2013;2013:890987.