www.jped.com.br
ARTIGO
ORIGINAL
Maple
syrup
urine
disease
in
Brazil:
a
panorama
of
the
last
two
decades
夽
,
夽夽
Silvani
Herber
a,
Ida
Vanessa
D.
Schwartz
b,c,d,e,f,∗,
Tatiéle
Nalin
c,f,
Cristina
Brinkmann
Oliveira
Netto
b,
José
Simon
Camelo
Junior
f,g,
Mara
Lúcia
Santos
f,h,
Erlane
Marques
Ribeiro
f,i,j,
Lavinia
Schüler-Faccini
a,b,c,e,je
Carolina
Fischinger
Moura
de
Souza
b,faProgramadePós-Graduac¸ãoemSaúdedaCrianc¸aedoAdolescente,UniversidadeFederaldoRioGrandedoSul(UFRGS),
PortoAlegre,RS,Brasil
bServic¸odeGenéticaMédica,HospitaldeClínicasdePortoAlegre,PortoAlegre,RS,Brasil
cProgramadePós-Graduac¸ãoemGenéticaeBiologiaMolecular,UniversidadeFederaldoRioGrandedoSul(UFRGS),
PortoAlegre,RS,Brasil
dLaboratórioBrain,HospitaldeClínicasdePortoAlegre,PortoAlegre,RS,Brasil
eDepartamentodeGenéticaeBiologiaMolecular,UniversidadeFederaldoRioGrandedoSul(UFRGS),PortoAlegre,RS,Brasil fRedeDXB,PortoAlegre,RS,Brasil
gDepartamentodePediatria,FaculdadedeMedicinadeRibeirãoPreto,RibeirãoPreto,SP,Brasil hHospitalPequenoPríncipe,Curitiba,PR,Brasil
iHospitalInfantilAlbertSabin,Fortaleza,CE,Brasil
jInstitutoNacionaldeGenéticaMédicaPopulacional(Inagemp),PortoAlegre,RS,Brasil
Recebidoem2deabrilde2014;aceitoem29deagostode2014
KEYWORDS Maplesyrupurine disease;
MSUD; Inbornerrors ofmetabolism; Diagnosis
Abstract
Objective: TocharacterizeasampleofBrazilianpatientswithmaplesyrupurinedisease(MSUD)
diagnosedbetween1992and2011.
Methods: In thisretrospective study,patients were identifiedthrough anational reference
laboratoryforthediagnosisofMSUDandthroughcontactwithothermedicalgeneticsservices
acrossBrazil.Datawerecollectedbymeansofachartreview.
Results: Eighty-threepatientsfrom75familieswereenrolledinthestudy(medianage,3years;
interquartilerange[IQR],0.57-7).Medianageatonsetofsymptomswas10days(IQR5-30),
DOIserefereaoartigo:http://dx.doi.org/10.1016/j.jped.2014.08.010
夽 Comocitaresteartigo:HerberS,SchwartzIV,NalinT,NettoCB,CameloJuniorJS,SantosML,etal.MaplesyrupurinediseaseinBrazil:
apanoramaofthelasttwodecades.JPediatr(RioJ).2015;91:292---8.
夽夽EstudofeitonaUniversidadeFederaldoRioGrandedoSul(UFRGS),PortoAlegre,RS,Brasil.
∗Autorparacorrespondência.
E-mail:ischwartz@hcpa.ufrgs.br(I.V.D.Schwartz).
whereasmedianageatdiagnosiswas60days(IQR29-240,p=0.001).Onlythree(3.6%)patients
werediagnosedbeforetheonsetofclinicalmanifestations.Acomparisonbetweenpatientswith
(n=12) and without (n=71) an early diagnosis shows that early diagnosis is associated
withthepresenceofpositivefamilyhistoryanddecreasedprevalenceofclinicalmanifestations
atthetimeofdiagnosis,butnotwithabetteroutcome.Overall,98.8%ofpatientshavesome
psychomotororneurodevelopmentaldelay.
Conclusion: InBrazil,patientswithMSUDareusuallydiagnosedlateandexhibitneurological
involvementandpoorsurvivalevenwithearlydiagnosis.Wesuggestthatspecificpublicpolicies
fordiagnosisandtreatmentofMSUDshouldbedevelopedandimplementedinthecountry.
©2014SociedadeBrasileiradePediatria.PublishedbyElsevierEditoraLtda.Allrightsreserved.
PALAVRAS-CHAVE Doenc¸adaurinade xaropedebordo; DXB;
Errosinatosdo metabolismo; Diagnóstico
Doenc¸adaurinadexaropedebordonoBrasil:umpanoramadasúltimasduasdécadas
Resumo
Objetivo: Caracterizarumaamostradepacientesbrasileiroscomadoenc¸adaurinadexarope
debordo(DXB)diagnosticadosentre1992e2011.
Métodos: Ospacientesforamidentificadospormeiodeumlaboratóriodereferêncianacional
paraodiagnósticodeDXBepormeiodocontatocomoutrosservic¸osdegenéticamédicano
Brasil.Osdadosforamcoletadospormeiodeumarevisãodeprontuários.
Resultados: Foramincluídosnoestudo83 pacientesde75 famílias(idademédia: trêsanos;
intervalointerquartil(IQR):0,57-7).Aidademédianosurgimentodossintomaserade10dias
(IQR:5-30),aopassoqueaidademédianodiagnósticoerade60dias(IQR:29-240;p=0,001).
Somentetrês(3,6%)pacientesforamdiagnosticadosantesdosurgimentodemanifestac¸ões
clíni-cas.Umacomparac¸ãoentrepacientescom(n=12)esem(n=71)umdiagnósticoprecocemostra
queodiagnósticoprecoceestáassociadoàpresenc¸adehistóricofamiliarpositivoeàreduc¸ãona
prevalênciademanifestac¸õesclínicasnomomentododiagnóstico,porémsemmelhorresultado.
Emgeral,98,8%dospacientestêmalgumatrasonodesenvolvimentopsicomotorouneurológico.
Conclusão: NoBrasil,ospacientescomDXBnormalmenterecebemumdiagnósticotardioe
exi-bemumenvolvimentoneurológicoebaixasobrevivência,mesmocomumdiagnósticoprecoce.
Sugerimos que políticaspúblicasespecíficas para odiagnóstico e tratamentodaDXBsejam
desenvolvidaseimplementadasnopaís.
©2014SociedadeBrasileiradePediatria.PublicadoporElsevierEditoraLtda.Todososdireitos
reservados.
Introduc
¸ão
Adoenc¸adaurinadexaropedebordo(DXB)éumadisfunc¸ão genética recessiva autossômica causada pela deficiência naatividadedocomplexoalfa-cetoácido-desidrogenasede cadeia ramificada (BCKDC). A deficiência desse complexo deenzimaslevaaníveiselevadosdeaminoácidosdecadeia ramificada (BCAA) leucina, valina e isoleucina. A leucina e seu ácido 2-oxo-isocapróico cetoanálogo são particular-mentetóxicosaosistemanervosocentral(SNC).Apesarde a incidência deDXB ao redor domundonormalmente ser estimadaem1:185.000recém-nascidos(RN),1osdados
obti-dosde examesem recém-nascidossugeremque essataxa
pode ser maior; na Alemanha, por exemplo, a incidência
estáestimadaem 1:133,000RN2e em algumas
comunida-desmenonitaseholandesasnaPensilvânia,EstadosUnidos,
ataxapodechegaraté1acada200nascidosvivos.3
Oexameneonatalpormeiodeespectrometriademassa
emtandem(MS/MS),tambémconhecidacomotriagem
neo-natal ampliada, permite o diagnóstico de DXB enquanto
o paciente ainda está assintomático, bem como o
iní-cio do tratamento precoce --- dois fatores essenciais na
melhoriado quadroclínico.3 Antes daintroduc¸ão da
tria-gem neonatalampliada, acreditava-se que a formagrave
(DXBclássica)contabilizava75-80%doscasos,4porémdados
recentessugeremqueasformasmaislevesdeDXBpodem
contabilizar até 50% dos casos diagnosticados.5 Na forma
clássica, os sintomas ocorrem primeiramente entre o 4◦
e o 7◦ dia de vida e, normalmente, incluem alterac¸ões
respiratórias,encefalopatia, um odor característico,
con-vulsõesecoma.6Nafaseaguda,énecessárioumtratamento
imediato e agressivo para reduzir os níveis de leucina, o
quedeveconsistir em umaperfusão comaltoteor de
gli-cose para estimular a secrec¸ão de insulina e suprimir o
catabolismodeproteínas.Casoissonãofuncione,poderão
ser necessárias intervenc¸ões invasivas, como diálise
peri-toneal, hemodiafiltrac¸ão ou hemodiálise. Durante a fase
de manutenc¸ão, o tratamento normalmente consiste na
restric¸ãodietéticadeBCAAesuplementac¸ãocomtiaminae
umafórmulaalimentarsemBCAA,6-8apesardeotransplante
defígadoserumaboaopc¸ão.9-11
OProgramaNacionaldeTriagemNeonatalfoi
implemen-tado em 2001 e não inclui o exame de DXB. A fórmula
pelo Sistema Único de Saúde (SUS). Adicionalmente, os
testesdelaboratório necessáriosparao diagnósticodessa
doenc¸atambémnãosãofornecidospeloSUSeestão
dispo-níveisapenasemalgunscentrosuniversitáriosselecionados
oulaboratóriosmédicosprivados.Arespeitodotransplante
defígado, nãoexiste uma rede nacional coordenada que
viseamelhorarascondic¸õesdostransplantesdefígadopara
pacientescomdisfunc¸õesmetabólicas.Porfim,nãoexistem
dadossobreaprevalênciadessadoenc¸anoBrasil.
Oobjetivodesteestudoédescreveroperfildospacientes
brasileiroscomDXB de1992 a2011deformaa contribuir
paraaconsolidac¸ãodaspolíticaspúblicasespecíficaspara
DXBnopaís.
Métodos
Esteestudo retrospectivo,multicêntrico elongitudinal foi aprovadopeloConselhodeRevisãoInstitucional.
Os pacientesforam identificados a partir dos registros doLaboratóriode ErrosInatos doMetabolismo doServic¸o de Genética Médica, servic¸o universitário que atua como centrodereferêncianacionalnodiagnósticoetratamento deerrosinatosdometabolismo,eapartirdosregistrosdo Servic¸odeInformac¸õessobreErros Inatos doMetabolismo (Siem,feitospelomesmoServic¸odeGenéticaMédica.12Esse
laboratórioprovavelmenteé responsável pelamaioria dos
diagnósticosde DXB nopaís; a propedêuticanecessária é
feitasemcustoaopacienteoumédicosolicitantee
normal-menteéfinanciadaporórgãosfinanciadoresdepesquisa.A
quantificac¸ão dosBCAAs porcromatografialíquida dealta
eficiência(CLAE)epelaanálisedeácidosorgânicosnaurina
estádisponívelnolaboratóriodesde1994;aanálise
automá-ticadeaminoácidoseMS/MStambémestádisponível,porém
adetecc¸ãodealoisoleucinajánãoé maisfeita. OSiemé
umservic¸odelinhadiretagratuito,estabelecidoem2001,
queforneceinformac¸õesamédicoseoutrosprofissionaisde
saúdeenvolvidosnodiagnósticoetratamentodepacientes
comsuspeitadeErrosInatosdoMetabolismo(EIMs)ouEIMs
confirmados.
Paraserincluídonoestudo,umpacientedeve
apresen-tar:1)aumentosignificativonosníveisdeBCAAnosangue
em maisde uma mensurac¸ão, conforme determinadopor
ummétodopadrão-ouro(quantificac¸ãodeBCAAcombase
na CLAE, noanalisador automático deaminoácidos ou na
MS/MS); e 2) diagnóstico da DXB confirmado
bioquimica-menteeestabelecidoentre1992e2011.
Os formulários de coleta de dados foram preenchidos
paracada paciente porseu médico atendente oupor um
dospesquisadoresdoestudo pormeiodeumaanálisedos
registros e gráficos disponíveis do paciente. Para
pacien-tesfalecidos,osdadosdoúltimoregistrodisponívelforam
consideradosparaadatadeinclusãonoestudo.
Definic¸ãodasvariáveisdoestudo
Foiconsideradodiagnóstico‘‘precoce’’aqueleempacientes diagnosticadosantesdo15◦diadevida.Adurac¸ãodadoenc¸a
atéodiagnósticofoidefinidacomootempodecorridoentre oiníciodas manifestac¸õesclínicase o diagnóstico bioquí-micodaDXB.Apresenc¸aeagravidadedoatrasopsicomotor enodesenvolvimentoneurológicoforamavaliadascombase
nas impressões do neurologista ou pediatra que atendeu cadapaciente.ADXBfoiclassificadaemvariantesdeacordo comoscritériosnormalmentecitadosnaliteratura.1
Análiseestatística
Foramfeitasanálisesestatísticasnoambientedesoftware 18.0doStatistical Packagefor theSocialSciences (SPSS®,
Statistics for Windows, Chicago,EUA). As variáveis foram levadasemconsiderac¸ãonaanáliseapenasseosdados esti-vessemdisponíveisparanomínimo60%daamostra.
Na análise descritiva, os dados foram expressos como frequências absolutas e relativas. As variáveis contínuas distribuídas assimetricamente foram expressas como medianas e intervalos interquartis. Foram usados o teste qui-quadrado e o teste exato de Fisher para determinar associac¸õesentreasvariáveiscategóricas.Foramusadoso testedeKruskal-Wallis e o testeUdeMann-Whitney para compararasmedianasdecaracterísticasdiferentes.Onível designificânciafoiestabelecidoem5%.
Resultados
Foramidentificados119pacientescomcomprovac¸ãoclínica oulaboratorialdaDXB(‘‘pacientescompossíveldiagnóstico daDXB’’),dosquais83atendiamaoscritériosdeinclusão. Desses, 48 estavam vivos na época do estudo, 20 vieram a óbito antesdo iníciodo estudo e 15 nãoapresentavam informac¸õescompletasdesobrevida.
Ospacientes envolvidos no estudo vieram de todasas cincoregiõesdoBrasil.Aidademédianomomentoda inclu-sãonoestudoeradetrêsanos(IQR:0,57-7anos;intervalo: 30dias-23anos).Dosparticipantes,46(55,4%)eramdosexo masculino,75(90,4%)nãoforamrelacionadose14(18,7%) apresentavam históricofamiliar deDXB.Foi relatada con-sanguinidadeem17famílias(22,7%).
Diagnóstico
A idade média no diagnóstico era de 60 dias (IQR: 29-240 dias; intervalo: sete dias-10 anos). O nível médio de leucinanodiagnóstico era de1.693mol/L(IQR: 965-2.836mol/L;faixadereferência:80-200mol/L).
1992 1 2 3 4 5 6 7 8 9
1997 2001 2002
Ano SIEM
Número de diagnósticos
2007 2011
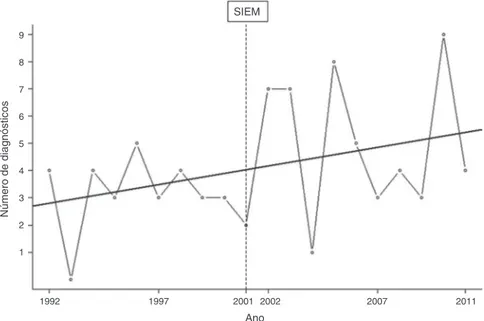
Figura1 NúmerodediagnósticosdeDXBnoBrasiletendênciade1992-2011.
OSieméumservic¸odelinhadiretagratuito,estabelecidoem2001,queforneceinformac¸õesamédicoseoutrosprofissionaisde
saúdeenvolvidosnodiagnósticoetratamentodepacientescomsuspeitaEIMsouEIMsconfirmados.
A figura 1 mostra a distribuic¸ão do número de
diag-nósticos por ano e revela uma tendência crescente em
diagnósticos durante o período do estudo. Contudo, a
comparac¸ão da idade média nodiagnóstico entre 1992 e
2001 (90 dias; IQR: 36-270; n=31) e entre 2002 e 2011
(53 dias; IQR: 20-202; n=52) não revelou diferenc¸as
estatisticamente significativas (p=0,053).O tempo médio
decorridoentreoiníciodossintomaseodiagnósticofoide
60dias(IQR:28-240)duranteaprimeiradécadadoestudo
e37dias(IQR:9-180)duranteasegundadécada(p=0,075).
ConsiderandotodosospacientescomDXBqueestavamvivos
em2011(n=48),13haviamsidodiagnosticadosentre1992
e2001e35entre2002e2011.
Somente 12 pacienteshaviam sido diagnosticados
pre-cocemente. Em três desses casos, o diagnóstico foi feito
antes do início dos sintomas como resultado de uma
tri-agem neonatal em um laboratório privado; na data de
elaborac¸ãodesterelatório,umdessespacientestemquatro
anosedesenvolvimentoneurológicoepsicomotornormale
osoutrosdoispacientes,deumeseisanos,têmatrasosleves
emoderadosnodesenvolvimentopsicomotoreneurológico,
respectivamente. A tabela 1 apresenta uma comparac¸ão
entrepacientescomesemdiagnósticoprecocedeDXB.
Manifestac¸õesclínicas
As manifestac¸ões clínicas mais comuns no momento da inclusãodospacienteseramdeatrasonodesenvolvimento psicomotoreneurológico(98,8%)esituac¸ãonutricional defi-ciente(74,7%).Doispacientesestavamacimadopeso.
A idade média no diagnóstico não foi significativa-menteassociadaàgravidadedoatrasonodesenvolvimento (n=58/83; p=0,31) nem a níveis elevados de leucina (n=57/73;p=0,961).
Dospacientes,73(88%)tinhamDXBclássica(idademédia no diagnóstico: 60 dias; IQR: 27,5-180 dias), oito (9,6%)
tinhamDXBmoderada(idademédianodiagnóstico:257dias; IQR:33,7-668 dias)edois(2,4%) tinhamDXBintermitente (idadenodiagnóstico:seis eseteanos, respectivamente). Em pacientes com a forma moderada, as manifestac¸ões clínicasmaiscomuns nodiagnósticoeram baixo apetitee anomalias respiratórias, ao passo que em pacientes com a forma intermitente essas manifestac¸ões eram convul-sõese anomalias respiratórias.Todosospacientescom as formas moderada/intermitente estavam vivos na data de elaborac¸ãodesterelatório.
Tratamento
Dospacientes,58(69,9%)estavamsendotratadospor neu-rologistas,56(67,5%)porgeneticistasmédicos,49(59,0%) porpediatras e 46 (55,4%) por nutricionistas. Outros pro-fissionaisenvolvidosnotratamentoe acompanhamentode pacientes incluíam neonatologistas, gastroenterologistas, nutricionistas,fonoaudiólogosefisioterapeutas.
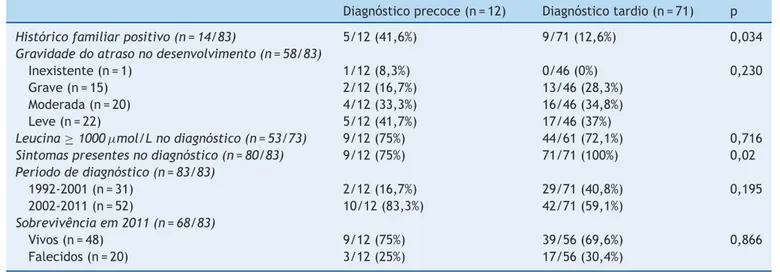
Tabela1 InfluênciadodiagnósticoprecocenocursodaDXBa
Diagnósticoprecoce(n=12) Diagnósticotardio(n=71) p
Históricofamiliarpositivo(n=14/83) 5/12(41,6%) 9/71(12,6%) 0,034
Gravidadedoatrasonodesenvolvimento(n=58/83)
Inexistente(n=1) 1/12(8,3%) 0/46(0%) 0,230
Grave(n=15) 2/12(16,7%) 13/46(28,3%)
Moderada(n=20) 4/12(33,3%) 16/46(34,8%)
Leve(n=22) 5/12(41,7%) 17/46(37%)
Leucina≥1000mol/Lnodiagnóstico(n=53/73) 9/12(75%) 44/61(72,1%) 0,716
Sintomaspresentesnodiagnóstico(n=80/83) 9/12(75%) 71/71(100%) 0,02
Períododediagnóstico(n=83/83)
1992-2001(n=31) 2/12(16,7%) 29/71(40,8%) 0,195
2002-2011(n=52) 10/12(83,3%) 42/71(59,1%)
Sobrevivênciaem2011(n=68/83)
Vivos(n=48) 9/12(75%) 39/56(69,6%) 0,866
Falecidos(n=20) 3/12(25%) 17/56(30,4%)
aDiagnósticoprecoce:diagnósticodeDXBantesdo15◦diadevida.
Óbitos
Dospacientes paraos quais osdados estavamdisponíveis (n=68),20---todoscomDXBclássica---vieramaóbitoantes doiníciodoestudo.Aidademédianoóbitoerade225dias (IQR:127,5-365dias).Nãohouveumacorrelac¸ão estatisti-camentesignificativaentreo desfechofatale osníveisde leucinanodiagnóstico(p=0,568).
Discussão
Nomelhordenossoconhecimento,esteéoprimeiroestudo a descrever o perfil de pacientes brasileiros com DXB. Apopulac¸ãoatualdoBrasilestáestimadaem190.732.694, com2.944.928nascidosvivosporano.13Portanto,
conside-randoumaincidência médiadeDXBde1:100.000nopaís,
sãoesperadosaproximadamente300novosdiagnósticosda
doenc¸aem10anos---umaestimativamuitomaisbaixa do
queaquelarealmenteincluídanoestudopelaamostra.Isso
sugerequeaDXBsejasubdiagnosticadanopaís.
A DXB atende à maioria dos critérios de Wilson e
Jungner14 para a triagem: por exemplo, existe uma fase
latente reconhecível ou sintomática precoce e um
trata-mentoaceito parapacientescom confirmac¸ãodadoenc¸a.
EmpaísesondeaDXBestáincluídanatriagemneonatal,os
pacientesnormalmentesãodiagnosticadosantesdo10◦dia
devida.3,4 Poroutro lado,empaísesonde aDXBnãoestá
incluídanosprogramaspúblicosdetriagemneonatal,como
oBrasil,odiagnósticonormalmenteépostergado,ocorreem
idadessemelhantesàquelasrelatadasemnossaamostra.15,16
ApredominânciadaDXBclássicaedepacientessintomáticos
emnossaamostrapoderiatambémserdevidaànão
inclu-sãodaDXBnosprogramaspúblicosdetriagemneonatal,já
quea literaturasugere quea triagemneonatalpermiteo
diagnósticoantecipadodasformasmais leves dadoenc¸a.5
Comoesperado,ospacientescomhistóricofamiliar
posi-tivoforam testadosantesdaqueles semhistórico familiar
deDXB;issofoidevido,provavelmente,aoaconselhamento
genéticodasfamíliasquejátinhamumfilhocomadoenc¸a
eestavam,assim,cientesdoriscoderecidivaeda
necessi-dadedeinvestigac¸ão.
Nosso estudo constatou uma tendência crescente no
númerodediagnósticosdeDXBnaúltimadécada,oque
coin-cidiucomoestabelecimentodoSiemeaimplementac¸ãode
umprogramanacional detriagemneonatalpeloMinistério
daSaúde.17Osmotivosportrásdessatendênciasão
desco-nhecidos,porémpodemrefletirumamaiorciênciadeEIMs
em geral porparte dos prestadoresde servic¸osdesaúde,
bemcomomaiorciênciademanifestac¸õesclínicasprecoces
dessas doenc¸as. Contudo, o aumento não foi
estatistica-mente significativo e não havia diferenc¸a significativana
idadenomomentododiagnósticoentreosdoisperíodos,o
quecorroboranossaconvicc¸ãodequeumapartesubstancial
depacientescomDXBcontinuaafalecersemdiagnósticoou
tratamento noBrasil.Uma situac¸ãosemelhanteocorrena
Malásia,ondeatriagemneonatalnãoincluiaDXB:o
diagnós-ticonormalmenteétardioeaDXBparecemenosprevalente
doqueoesperado.18
Atrasos psicomotor e no desenvolvimento neurológico
foramdetectados em praticamentetodos ospacientesna
amostra. Pouco maisda metade dos pacientes que
rece-beram a fórmula metabólica para DXB relataram que foi
fornecida de forma regular. Contudo,a maioria dos
paci-entes apresentou situac¸ão nutricional inadequada. Vale
ressaltarqueospacientescomDXBsempredevemser
acom-panhadosporprestadoresdecuidadosnutricionaiseapenas
metadedospacientesemnossaamostraeram
acompanha-dosporumnutricionista.19Contudo,amaioriadospacientes
que receberam a fórmula metabólica foi monitorada por
nutricionistas (dados não apresentados). Os neurologistas
eram os profissionais mais comumente responsáveis pelo
acompanhamentodos pacientes, quepoderá ser
secundá-rio à alta frequência deatraso no desenvolvimentonessa
amostra.
No Brasil, o tempo entre o diagnóstico e o
recebi-mento da fórmulametabólica é longo e variável.Quando
os pacientes foram diagnosticados no estágio agudo da
doenc¸a,duranteumainternac¸ãodevidoadescompensac¸ão
metabólica,estavamsuscetíveisaoiníciodaintroduc¸ãoda
disponível no hospital da internac¸ão, obviamente). Por
outro lado, os pacientes diagnosticados em um estágio
não agudo da doenc¸a e tratados de forma ambulatorial
estavam propensos areceber afórmula apenas
posterior-mente;naverdade,essespacientesnormalmentegarantem
oacessoàfórmulametabólicapormeiodeprocessos
judi-ciais. Novamente, vale ressaltar que o uso de fórmula
isentadeBCAAéessencial,deformaagarantiraquantidade
de proteína necessária para o crescimento e
desenvolvi-mentoadequados.1Recentemente,foramfeitosestudosem
ratos com DXB clássica e intermediária recém-induzidas
paraavaliarasconsequênciasdorápido acúmulodeBCAA
e para avaliar as possíveis opc¸ões de tratamento, como
norleucina.20
Osníveisdeleucinanodiagnósticomostraram-se
eleva-dos, com um valor médio de 1.693mol/L. Os níveis de
leucina superiores a 1.000mol/L são considerados
críti-cos, poispodemproduzir dano irretratávelouatémesmo
levaraóbito.3,21,22Contudo,nãohouveassociac¸ão
significa-tivaentrea gravidadedoatraso nodesenvolvimentoe os
níveisdeleucinanodiagnóstico.Issopodeseratribuídoao
fatodequeocontrolemetabólicodelongoprazoé
conside-radoumfatordeterminantededesenvolvimentopsicomotor
e cognitivo mais decisivo do que os níveis de leucina no
diagnóstico.22
Nesteestudo,avantagemdodiagnósticoprecoceparece
não ter sido relevante devido à falta de manejo clínico
decurtoelongoprazos.Conformerelatadoporpacientes
filipinos,15 nenhumprotocoloclínicoparaotratamentoda
DXBemestágioagudoestavadisponívelnoBrasileos
pacien-tesnãoreceberamafórmulametabólicadeformaconfiável.
Poroutrolado,emumestudodeMortonetal.4noqualos
pacientestiveramacessoàformulaeumprotocoloclínico
foiseguidonoestágioagudodadoenc¸a,oresultadogeralfoi
melhoreospacientesatingiramumdesenvolvimentomais
adequado.
Emvistadarecenteadoc¸ãodeumapolíticapública
espe-cífica para o diagnóstico e tratamento de doenc¸as raras
no Brasil,23,24 sugerimos que as seguintes etapas sejam
seguidas a fim de melhorar ainda mais a qualidade de
vida dos pacientes com DXB no país: a) expandir o
pro-grama público de triagem neonatal para incluir a DXB
entreasdoenc¸asidentificadas;b)desenvolveracapacidade
de fazer testes de aloisoleucina localmente; c) oferecer
fórmulas metabólicas específicas a todos os pacientes,
sem a necessidade de intervenc¸ão legal; d)
estabele-cer um centro nacional especializado em transplante de
fígado para doenc¸as metabólicas; e e) estabelecer uma
rede de equipes multidisciplinares que abranja médicos,
enfermeiras e nutricionistas no tratamento de erros
ina-tosdometabolismoparaodesenvolvimentodeprotocolos
nacionais para o tratamento da DXB. A criac¸ão da Rede
DXB(http://redexaropedobordo.com.br/),estabelecidaem
2010parapromoveraeducac¸ãosobreodiagnósticoe
tra-tamentodaDXB epatrocinada porumaagênciabrasileira
depesquisasepeloMinistériodaCiênciaeTecnologia,éum
dosprimeirospassoscomrelac¸ãoaesseobjetivo.
Financiamento
Coordenac¸ãodeAperfeic¸oamentodePessoaldeNível Supe-rior (Capes), Fundo de Incentivo à Pesquisa e Eventos
(Fipe-HCPA)eConselhoNacionaldeDesenvolvimento Cien-tíficoeTecnológico(CNPq)---bolsan◦
MCT/CNPq/CT-Saúde 57/2010.
Conflitos
de
interesse
Osautoresdeclaramnãohaverconflitosdeinteresse.
Agradecimentos
Aosprofissionais daRede DXB que contribuírampara este artigo,bemcomoàequipedoSetordeGenéticaMédicado HospitaldeClínicas dePortoAlegre, RS, Brasil, principal-menteaosprofissionaisenvolvidosnaanálisebiomédicade pacientescomsuspeitadedoenc¸asmetabólicas.
Referências
1.ChuangD,ShihV.Disordersofbranched-chainaminoacidand ketoacidmetabolism.In:ScriverC,BeaudetA,SlyW,ValleD, editors.Themetabolicandmolecularbasisofinheriteddisease. 7thed.NewYork:McGraw-Hill;2001.p.1971---95.
2.FingerhutR.RecallrateandpositivepredictivevalueofMSUD screeningis notinfluencedbyhydroxyproline. EurJPediatr. 2009;168:599---604.
3.SimonE,FingerhutR,BaumkötterJ,KonstantopoulouV, Ratsch-mannR,WendelU.Maplesyrupurinedisease:favourableeffect ofearlydiagnosisbynewbornscreeningontheneonatalcourse ofthedisease.JInheritMetabDis.2006;29:532---7.
4.MortonDH,StraussKA,RobinsonDL,PuffenbergerEG,Kelley RI.Diagnosisandtreatmentofmaplesyrupdisease:astudyof 36patients.Pediatrics.2002;109:999---1008.
5.Fingerhut R, Simon E, Maier EM, Hennermann JB, Wendel U. Maple syrup urine disease: newborn screening fails to discriminate between classic and variant forms. Clin Chem. 2008;54:1739---41.
6.Saudubray J, Charpentier C. Clinical phenotypes: diagno-sis/algorithms. In: Scriver CR, Beaudet AL, Sly WS, ValleD, editors.Themetabolicandmolecularbasesofinherited disea-ses.NewYork:McGraw-Hill;1995.p.327---400.
7.JouvetP,JugieM,RabierD,DesgrèsJ,HubertP,SaudubrayJM, etal.Combinednutritionalsupportandcontinuous extracorpo-realremovaltherapyinthesevereacutephaseofmaplesyrup urinedisease.IntensiveCareMed.2001;27:1798---806.
8.StraussKA,WardleyB,RobinsonD,HendricksonC,RiderNL, Puffenberger EG, et al. Classical maple syrupurine disease andbraindevelopment:principlesofmanagementandformula design.MolGenetMetab.2010;99:333---45.
9.FeierFH,MiuraIK,FonsecaEA,PortaG,PuglieseR,PortaA, etal. Successfuldomino livertransplantationinmaplesyrup urinediseaseusingarelatedlivingdonor.BrazJMedBiolRes. 2014;47:522---6.
10.Mazariegos GV, Morton DH, Sindhi R, Soltys K, Nayyar N, BondG,etal.Liver transplantationfor classicalmaplesyrup urinedisease:long-termfollow-upin37patientsand compa-rativeUnitedNetworkforOrganSharingexperience.JPediatr. 2012;160:116---21,e1.
11.SerraJD,SánchezFA,VisusFS.Enfermidadesdeorinadejarabe arce.In:SanjurjoP,BaldellouA,editors.Diagnósticoy trata-mientodelasenfermedadesmetabólicas hereditarias.3a ed. Madrid:EdicionesErgon;2010.p.487---98.
13.Brasil.MinistériodoPlanejamento,Orc¸amentoeGestão. Insti-tutoBrasileirodeGeografiaeEstatística(IBGE).In:Contagem populacional.Brasi´lia:MinistériodoPlanejamento,Orc¸amento eGestão;2010.
14.WilsonJ,JungnerG. Principlesand practiceofscreeningfor disease.Geneva:WorldHealthOrganization;1968.
15.LeeJY,ChiongMA,EstradaSC,Cutiongco-DelaPazEM,SilaoCL, PadillaCD.Maplesyrupurinedisease(MSUD)---Clinicalprofile of47Filipinopatients.JInheritMetabDis.2008;31:S281---5.
16.PangkanonS,CharoensiriwatanaW,SangtawesinV.Maplesyrup urinediseaseinThaiinfants.JMedAssocThai.2008;91:S41---4.
17.Brasil.MinistériodaSaúde.PortariaGM/MSn◦822/GMde6de junhode2001.Brasília:MinistériodaSaúde;2001.
18.YunusZM,KamaludinDA,MamatM,ChoyYS,NguL.Clinicaland biochemicalprofilesofmaplesyrupurinediseaseinMalaysian children.JIMDRep.2012;5:99---107.
19.ValadaresEG,GiannettiJG,RefoscoLF,SilvaLC,OliveiraRB, PiresRF. Leucinose: doenc¸a doxaropede bordo. In:Martins
AM,FrangipaniBJ,NichelettiC,OliveiraRB,editors.Protocolo brasileirodedietas:errosinatosdometabolismo.São Paulo: SegmentoFarma;2006.p.53---8.
20.ZinnantiWJ,LazovicJ.Interruptingthemechanismsofbrain injuryinamodelofmaplesyrupurinediseaseencephalopathy. JInheritMetabDis.2012;35:71---9.
21.Heldt K, Schwahn B, Marquardt I, Grotzke M, Wendel U. Diagnosis of MSUD bynewborn screening allows early inter-ventionwithoutextraneousdetoxification. MolGenet Metab. 2005;84:313---6.
22.HoffmannB,HelblingC,SchadewaldtP,Wendel U.Impactof longitudinalplasmaleucinelevelsontheintellectualoutcome inpatientswithclassicMSUD.PediatrRes.2006;59:17---20.
23.Brasil.MinistériodaSaúde.Portarian.◦199,de30dejaneiro de2014.Brasília:MinistériodaSaúde;2014.