PROGRAMA DE PÓS GRADUAÇÃO EM CIÊNCIAS DA SAÚDE
CONSEQUÊNCIAS DA COLECTOMIA ASSOCIADA À HEPATECTOMIA NO METABOLISMO HEPÁTICO E NA FORMA E FUNÇÃO DE HEMÁCIAS EM RATOS
MARÍLIA DANIELA FERREIRA DE CARVALHO
ii
CONSEQUÊNCIAS DA COLECTOMIA ASSOCIADA À HEPATECTOMIA NO METABOLISMO HEPÁTICO E NA FORMA E FUNÇÃO DE HEMÁCIAS EM RATOS
ORIENTADOR: Prof. Dr. ALDO DA CUNHA MEDEIROS COORIENTADOR: Prof. Dr. IRAMI ARAÚJO FILHO
NATAL/RN 2012
iii
PROGRAMA DE PÓS GRADUAÇÃO EM CIÊNCIAS DA SAÚDE
Coordenadora do Programa de Pós-Graduação em Ciências da Saúde: Prof.a Dra.: Ivonete Batista de Araújo
iv
CONSEQUÊNCIAS DA COLECTOMIA ASSOCIADA À HEPATECTOMIA NO METABOLISMO HEPÁTICO E NA FORMA E FUNÇÃO DE HEMÁCIAS EM RATOS
Aprovada em: ____/____/______
Banca Examinadora:
Presidente da Banca:
Prof. Dr. Aldo da Cunha Medeiros – UFRN
________________________________________
Membros da Banca:
Prof.ª Dra. Maria Goretti Freire de Carvalho – UnP
________________________________________
Prof. Dr. Geraldo Barroso Cavalcanti Júnior – UFRN
v
A Daniel, meu irmão, por me fazer entender com a sua ausência o essencial na vida, e por sempre ser uma referência às minhas atividades intelectuais.
vi
Ao meu orientador, Prof. Aldo da Cunha Medeiros, por ter despertado em mim a vocação de ensinar e pesquisar, por ter me dado a oportunidade de estar ao seu lado aprendendo com o seu exemplo de honestidade, determinação, ética, paciência
e cordialidade.
Ao Prof. Irami Araújo Filho, por ter me ensinado muito além da técnica cirúrgica através de seu exemplo de simplicidade e dedicação aos nossos pacientes.
À Amália Cínthia Meneses do Rêgo, pelo exemplo de mulher, mãe, professora e pesquisadora; pela orientação de toda parte laboratorial do nosso
estudo.
Ao estatístico Ítalo Medeiros Azevedo, pela orientação do nosso trabalho.
Aos meus pais, Antônio Martins e Fátima, pelo amor incondicional, principal apoio na realização dos meus sonhos e por sempre estimularem minhas atividades
intelectuais.
Ao meu marido, Ricardo Moreira, por sua dedicação, compreensão, companheirismo e incentivo constante à realização dos meus sonhos; por tornar minha vida completa
e feliz.
Às minhas irmãs, Diva e Michele, a quem tenho amor absoluto, por estarem sempre ao meu lado me apoiando, dividindo comigo os momentos mais difíceis e
felizes.
Às minhas amigas, em especial à Mônica, a quem amo como uma irmã, que sempre esteve próxima, mesmo agora distante, e sempre me motivou.
vii
“Feliz aquele que transfere o que sabe e aprende o que ensina.”
(Cora Coralina)
viii
à hepatectomia parcial, na biodistribuição do fitato-99mTcO4, na marcação e morfologia de hemácias e parâmetros metabólicos da função hepática. Dezoito ratos Wistar foram distribuídos em três grupos (seis animais cada), denominados: colectomia, colectomia+hepatectomia e sham. No primeiro grupo os animais foram submetidos a uma colectomia direita, no segundo foram submetidos ao mesmo procedimento porém associou-se uma hepatectomia esquerda e no terceiro houve apenas realização de uma laparotomia e leve manipulação de alças intestinais. No trigésimo dia pós-operatório, foi feita injeção de 0,1 mililitro intravenoso de fitato-99m
TcO4 (radioatividade 0,66 MBq) em todos os animais. Após quinze minutos, uma amostra de fígado foi colhida e pesada. O percentual de radioatividade por grama de tecido (%AIT/g) foi determinado no fígado e hemácias usando-se um contador gama automático. Dosagem sérica de alanina aminotransferase (ALT), aspartato aminotransferase (AST), fosfatase alcalina (FA), morfologia e marcação de hemácias com pertecnetato foram determinadas. O %AIT/g no fígado e nas hemácias foi menor nos animais dos grupos colectomia e colectomia+hepatectomia do que no grupo sham (p<0,05; teste de Tukey). Nenhuma diferença foi detectada comparando os grupos colectomia e colectomia + hepatectomia. A morfologia das hemácias não diferiu entre os 3 grupos. Os níveis séricos de AST, ALT e FA foram significativamente maiores no grupo colectomia+hepatectomia do que no grupo colectomia (p<0,001). Em conclusão, a colectomia associada a hepatectomia contribuiu para reduzir a captação de radiofármaco no fígado e hemácias de ratos, coincidindo com alterações na atividade enzimática do fígado.
Descritores: Colectomia. Hepatectomia. Metabolismo. Biodisponibilidade. Radiofármaco.
ix
hepatectomy on the biodistribution of the 99mTc-phytate, on metabolic parameters, as well as labeling and morphology of red blood cells. Wistar rats were distributed into three groups (each with 6), nominated as colectomy, colectomy+hepatectomy and sham. In the 30th postoperative day all rats were injected with 99mTc-phytate 0.1mL i.v. (radioactivity 0.66 MBq). After 15 minutes, liver sample was harvested and weighed. Percentage radioactivity per gram of tissue (%ATI/g) was determined using an automatic gamma-counter. Serum AST, ALT, alkaline phosphatase and red blood cells labeling were determined. The liver %ATI/g and red blood cells labeling were lower in colectomy and colectomy+hepatectomy rats than in sham rats (p <0.05), and no difference was detected comparing the colectomy and colectomy+hepatectomy groups. Red blood cells morphology did not differ among groups. Serum levels of AST, ALT and alkaline fosfatase were significantly higher in colectomy+hepatectomy than in colectomy rats (p<0.001). Hepatectomy associated with colectomy lowered the uptake of radiopharmaceutical in liver and in red blood cells in rats, coinciding with changes in liver enzymatic activity.
x PVPI- Polivinil Pirrolidona Iodo ou iodopovidona CNEM- Comissão Nacional de Energia Nuclear LIGA- Liga Norteriograndense Contra o Câncer
%AIT/g- Percentual de radioatividade por grama de tecido ALT- Alanina aminotransferase
AST- Aspartato aminotransferase FA- Fosfatase Alcalina
ANOVA- Análise de variância Tb- Tempo de meia vida biológica keV- Quiloelétron volt
99
Mo/99mTc- sistema gerador de tecnécio a partir de molibdênio 99m
Tc- 99mTecnécio
Na99mTcO4- Pertecnetato de Sódio SnCl2 - Cloreto Estanoso
CCR- Câncer colorretal
UTI- Unidade de Terapia Intensiva CEP- Comitê de Ética em Pesquisa MBq- Megabecquerel
HUOL- Hospital Universitário Onofre Lopes
xi
FIGURA 1-Retirada das amostras hepáticas ...14
FIGURA 2-Lavagem das amostras hepáticas ...14
FIGURA 3-Pesagem dos fragmentos hepáticos em balança de precisão...15
FIGURA 4-Imagem do Contador Gama...15
FIGURA 5-Fotomicrografia das hemácias nos três grupos estudados. (A) Grupo colectomia, (B) Grupo colectomia + hepatectomia e (c) Grupo Sham. 1000x...23
xii
Tabela 1- Distribuição do radioisótopo em atividade radiológica por grama de tecido em cada grupo...23 Tabela 2- Níveis séricos das enzimas hepáticas nos três grupos estudados...22
xiii 01 01 03 04 05 08 10 12 12 12 13 17 17 28 41 52 62 76 89 98 110 116 SUMÁRIO
1- INTRODUÇÃO…..……….…...
1.1-Os Radiofármacos………….……….
1.2-O Tecnécio………..……….
1.3-A Cintilografia………..……….... 1.4-Colectomia e hepatectomia………..………. 1.5-Marcação e Morfologia das hemácias...………..………. 2-JUSTIFICATIVA………..………...…….…... 3- OBJETIVO………...
3.1-Objetivos gerais………...
3.2-Objetivos específicos... 4- MÉTODO... 5-ARTIGOS PRODUZIDOS... 5.1-Metabolic and hematologic consequences of colectomy associated to
hepatectomy in rats………
5.2-Metabolism and gastric remnant changes after Roux-en-Y Gastric Bypass in
rats………...
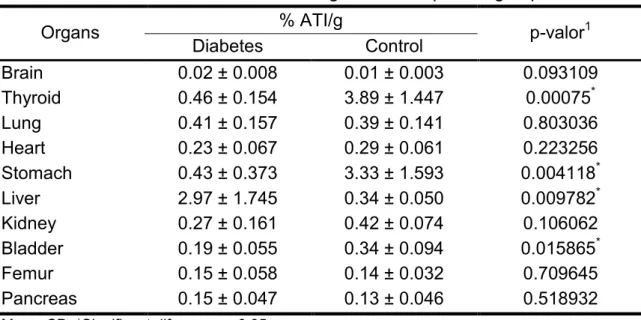
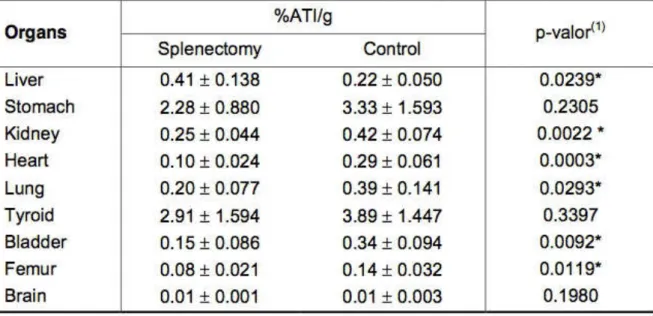
5.3-Diabetes and biodistribution of pertechnetate (Na99mTcO4) in rats……….. 5.4-Splenectomy changes the biodistribution of pertechnetate (99mTcO4-) in rats... 5.5-Bacterial translocation in rats treated with simvastatin undergoing intestinal
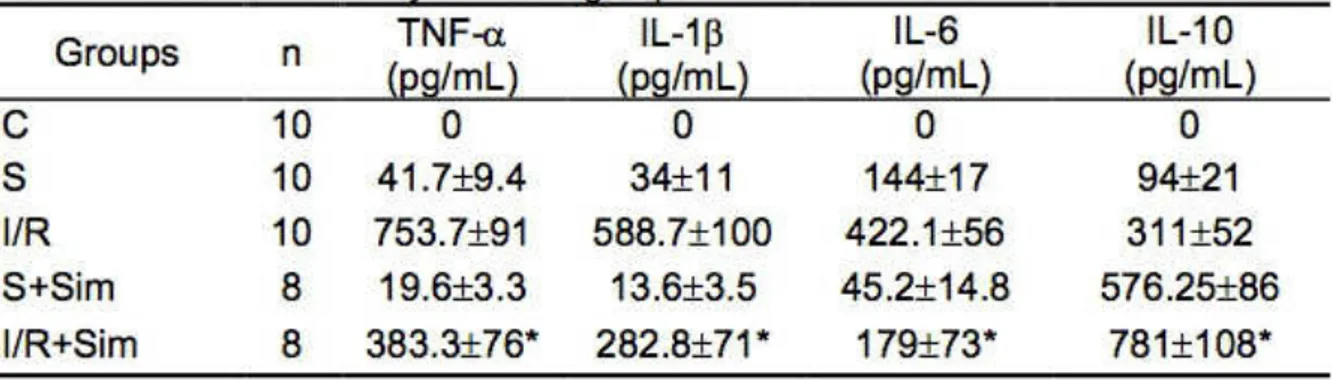
ischemia and reperfusion………..
5.6-Ileal interposition for the treatment of diabetes in rats: repercussion on beta cells
mass……….
1. INTRODUÇÃO
Ao longo dos anos os avanços na área da saúde modificaram a forma como é diagnosticada e tratada a grande maioria das doenças. Alguns métodos diagnósticos possuem grande precisão porém, não são ao todo isentos de resultados equivocados, principalmente quando se entende o paciente como um ser singular exposto a situações e experiências distintas. Já é bem estabelecido na literatura que algumas doenças, medicações, radioterapias e cirurgias podem falsear resultados de exames cintilográficos1-10, visto que estas circunstâncias podem modificar a capacidade de ligação entre os radiofármacos e as proteínas teciduais9.
Uma cirurgia de grande porte (um extenso procedimento cirúrgico relativamente difícil, envolvendo órgãos vitais) pode resultar em importantes alterações anatômicas e metabólicas e/ou complicações mutáveis e imprevisíveis4,11,12. Existem poucos trabalhos na literatura que avaliam os efeitos dessas intervenções cirúrgicas na biodistribuição de radiofármacos3.
1.1 Os radiofármacos
morfologia23. Um radiofármaco tem dois componentes: um radionuclídeo e um fármaco; a escolha de qual radiofármaco deverá ser usado é orientada pela sua predileção por determinado órgão ou por determinado componente fisiológico que se pretende ser avaliado14,24. É desejável que o radiofármaco se localize preferencialmente no órgão objeto do estudo, uma vez que a atividade de áreas não alvo podem obscurecer os detalhes estruturais da imagem do órgão alvo. As radiações do radioisótopo devem ser facilmente detectadas através de equipamentos nucleares, e a dose de radiação para o paciente deve ser mínima. Por serem usados em humanos, essas substâncias devem ser estéreis e livres de pirógenos, sendo submetidos a todas as medidas de controle de qualidade exigidas para um medicamento convencional. A diferença entre um traçador radioativo e um radiofármaco reside no fato de que o primeiro não pode ser administrado em humanos, devido à falta de controles adequados como o de esterilidade e apirogenicidade. Geralmente estas substâncias são administrados em pequena quantidade24, em dose única e não devem produzir efeitos farmacológicos. Os radiofármacos considerados ideais deverão apresentar rapidez de obtenção, fácil disponibilidade e produção, baixo custo e meia-vida suficientemente curta para diminuir a taxa de exposição do doente à radiação4,14 mas também longa o suficiente para permitir finalizar o processamento da imagem. Um radiofármaco decai com uma meia-vida definida que é caracterizada pelo radionuclídeo, denominada pela abreviação Tp ou t1/2, independente das condições físico-químicas. Quando um radiofármaco é administrado, o processo de biodistribuição se inicia e este consiste de: absorção, distribuição, metabolismo e excreção; esta última etapa pode acontecer através da eliminação fecal, urinária, transpiração ou outros mecanismos.
radiofármaco administrado por via intravenosa para a realização de cintilografia poderia7-9,25,26 gerar a possibilidade de diagnósticos equivocados, levando à repetição do exame com um aumento na dose de radiação4,5. Este fato não ocorre somente no tecido traumatizado, mas também em outros órgãos não manipulados pela intervenção cirúrgicas7. O decaimento biológico de um radiofármaco segue uma lei exponencial semelhante ao do decaimento do radionuclídeo. Assim, cada radiofármaco tem uma meia-vida biológica (Tb), sendo este o tempo necessário para que a metade dele desapareça e, por conseguinte, está relacionada com uma constante de decaimento, λb = 0.693/Tb. Portanto, em qualquer sistema biológico, a perda de um radiofármaco é devida tanto à desintegração física do radionuclídeo como pela eliminação biológica do radiofármaco. O decaimento pode ocorrer pela emissão de partículas α e β, porém estas não devem ser usadas para fins diagósticos, visto que causam danos aos tecidos, por este motivo prefere-se os raios γ. Seja qual for o modo de decaimento, para estudos de diagnóstico do radionuclídeo, este deve emitir radiação γ com uma energia entre 30 e 300 keV14. Abaixo de 30 keV os raios γ são absorvidos pelo tecido e não são captados pelo detector24.
1.2 O 99mTecnécio
O crescimento e a ampla aplicação da medicina nuclear diagnóstica tem sido impulsionada pela fácil disponibilidade do tecnécio através do sistema gerador 99
Mo/99mTc portátil e das propriedades quase ideais da radiação gama produzida por este radionuclídeo que possibilitou seu uso clínico nos mais diversos tecidos26. O 99m
são normalmente estabilizados por complexação com ligantes24. A forma química utilizada para leitura em gama câmera é o pertecnetato de sódio (Na99mTcO4), possui valência +7, e necessita de redução iônica para a marcação de substâncias, células ou órgãos em estudo. Para tal processo, a substância mais utilizada é o cloreto estanoso (SnCl2), sendo os componentes inicialmente dissolvidos em solução, liofilizados e armazenados em atmosfera de azoto ou gás inerte (diminui a oxidação do Sn2+)14.
O tecnécio é um dos radionuclídeos mais utilizados em medicina nuclear27,30, corresponde a mais de 80% do total usado4,24,26 devido se ligar a uma grande variedade de moléculas e células5,31. O Na99mTcO4 pode entrar ou sair do meio intracelular livremente, num processo de difusão passiva32. Além disso, essa substância preenche muitos dos critérios de um radionuclídeo ideal: possui radiação, custo, impacto ambiental e energia de emissão muito baixos; é de fácil uso na marcação de hemácias; tem facilidade de obtenção; possui 10% de conversão interna e uma meia vida curta (6h), o que diminui a taxa de exposição dos doentes à radiação2,11,15,24,26,33,34.
1.3 A cintilografia
As radiações gama (γ), são emissões de natureza eletromagnética, ou seja, são fótons com massa desprezível e sem carga elétrica; tais características conferem a esta radiação uma menor possibilidade de interação com a matéria quando comparada à capacidade de interação das partículas alfa (α) e beta (β). Assim, a radiação gama tem menor capacidade de ionização e alta energia, o que permite que ela percorra longas trajetórias e atravesse corpos de maior espessura. Esses fatores fizeram com que a medicina nuclear a elegesse como a radiação usada nos exames de imagem, sendo o tecnécio o isótopo radioativo mais frequentemente usado como seu emissor35.
Essas radiações partem do interior do corpo e são captadas por equipamentos, dotados de um cristal sensível, que capta cada radiação que chega produzindo uma centelha ou cintilação para formar a imagem final, daí o nome cintilografia. O aparelho que registra as radiações é chamado de gama câmara e seu componente principal é a câmara de cintilação, onde se originam informações processadas por um sistema complexo de computação que serão convertidas em imagem. Esta câmara opera no mesmo princípio de um contador de radiação gama, mas é consideravelmente mais complexa na sua construção e funcionamento35,36. A biodistribuição pode ser medida por método invasivo, envolvendo o sacrifício de
animais e quantificação da radioatividade nos órgãos e tecidos de interesse, como realizado no nosso estudo, ou por métodos não invasivos37. Esse exame pode ser realizado em diversos órgãos como coração, pulmões, ossos, rins e outros. No caso da cintilografia renal, o exame fornece imagens funcionais dos rins, ou seja, mostra como as células estão desempenhando suas funções. Devido à permanência prolongada do traçador no córtex renal, o exame fornece informações principalmente relativas à concentração do mesmo no parênquima renal, morfologia e dimensões dos rins38. Outros exemplos do uso da cintilografia com o tecnécio (99mTc-pertecnetato de sódio) é o diagnostico da mucosa gástrica ectópica (pesquisa de divertículo de Meckel) onde o pertecnetato é captado pela mucosa, além do uso na pesquisa do sangramento intestinal39-41. A sensibilidade avançada dessa técnica permite detectar alteração na função de diversos órgãos, muitas vezes superior à de outros exames36.
1.4 Colectomia e hepatectomia
décadas, testemunhamos melhorias substanciais na sobrevida de pacientes com esta neoplasia que foi resultante de um diagnóstico mais precoce, maior eficiência da quimioterapia e radioterapia, e os avanços nas técnicas cirúrgicas, melhorias na área da anestesia e cuidados pós-operatórios, principalmente em UTIs, reduzindo a morbi-mortalidade apesar da abordagem cirúrgica mais agressiva49. No entanto, a melhor promessa de cura continua sendo a excisão cirúrgica adequada do tumor43,44,50-53.
O fígado é o sítio mais frequente de metástases do CCR e estas podem ocorrer em até 60% dos pacientes43,47,52-54 porque a drenagem venosa do cólon e reto superior ocorre através da veia porta que drena diretamente para o fígado. Sabe-se que 60-70% do câncer colorretal recorrente envolve o fígado e que este é o órgão unicamente envolvido em 20-35% dos casos46-49. No momento do diagnóstico entre 15-25% dos pacientes têm metástases hepáticas clinicamente detectáveis41-44,52 e em torno de 20%-45% dos pacientes vão desenvolver metástase hepática metacrônica43,46,55, que são aquelas evidenciadas após 6 meses do diagnóstico. Porém apenas 20% dos pacientes possuem doença ressecável44,46. As recidivas após ressecção primária das lesões estão confinadas ao fígado, em aproximadamente, 50% dos casos46.
As ressecções das metástases hepáticas caracterizavam um grande desafio para os cirurgiões no passado, devido a sua alta taxa de mortalidade, mas atualmente a taxa de mortalidade é de cerca de 1-5% em importantes centros médicos46,56. Esses procedimentos se tornam cada vez mais seguros, podendo-se ressecar até 80% do parênquima hepático57. Apesar desses avanços, a taxa de ressecabilidade de metástases no momento do diagnóstico ainda é baixa, representando a baixa proporção de pacientes que podem se beneficiar de uma abordagem cirúrgica. Os principais obstáculos para a indicação da ressecção hepatica são: a doença metastática bilobar, tumores volumosos e deixar parênquima hepático residual funcional suficiente após a ressecção57.
As hepatectomias são procedimentos relacionados a grande morbi-mortalidade devido a insuficiência hepática que guarda relação com o tamanho da ressecção e
remover todos os tumores43,49. Porém, os critérios de ressecção vêm sendo contestados por diferentes grupos de pesquisadores ao longo da última década44,52; além disso, o paradigma sobre o tratamento cirúrgico das metástases colorretais sincrônicas também começou a mudar, com autores relatando bons resultados para ressecção simultânea de cólon e metástases do fígado. Os defensores de uma abordagem em dois tempos aprovam esta estratégia devido à preocupações com aumento da morbidade e mortalidade associadas à ressecção simultânea do câncer colorretal com metástases hepáticas58, porém tal fato culmina com uma abordagem mais agressiva no tratamento de metástases hepáticas colorretais45. Embora o câncer colorretal primário tenha um bom prognóstico quando ressecado com margens livres e linfonodos negativos, o diagnóstico de metástases hepáticas é o prenúncio de uma evolução pior. Até recentemente, os pacientes inicialmente considerados como não-ressecáveis foram tratados através de quimioterapia
paliativa, com baixas chances de sobrevida em cinco anos51.
Estratégias que ampliaram as indicações de ressecção hepática incluindo a quimioterapia locorregional44, embolização da veia porta, quimioterapia neoadjuvante e os procedimentos ablativos; estes últimos apesar da alta taxa de recorrência local podem ser considerados como opção terapêutica nos pacientes sem indicação de quimioterapia loco-regional59.
meses em grandes séries. Resultados de dez anos de sobrevida foram documentados em torno de 20% a 26%. Em contraste, a sobrevida mediana para não-ressecados, com metástases hepáticas colorretais, é 5-10 meses54. Porém, nem todos os pacientes possuem indicação cirúrgica e a decisão sobre ressecabilidade depende das condições do paciente, extensão da doença e da função hepática. Desse modo, apenas 10 a 20 % são candidatos à ressecção52,59. Apesar disto, as opções para tratamento não-cirúrgico do câncer colorretal metastático é muito vasta.
Se a metástase hepática é diagnosticada juntamente ao tumor primário, e é factível sua remoção, deve ser ressecada no mesmo ato operatório do tumor primário, mas caso seja evidenciada posteriormente, ela é ressecada em outro tempo cirúrgico. No presente trabalho optamos por submeter os animais a uma colectomia direita e hepatectomia esquerda simulando que esses teriam um tumor de cólon direito e metástases hepáticas apenas à esquerda (que caracterizaria uma cirurgia de grande porte) para avaliar as possíveis alterações, em modelo animal, na biodistribuição do radiofármaco e da morfologia das hemácias. Não foi objeto do nosso estudo a carcinogênese , desse modo não foi induzido câncer nestes animais, mas sim o impacto de uma cirurgia de grande porte nos parâmetros estudados. A cirurgia em questão foi escolhida por ser um procedimento cirúrgico cada vez mais indicado para o tratamento, com possibilidade curativa, de paciente com diagnóstico de adenocarcinoma de cólon com metástase hepática, visto que sua incidência é crescente ao longo das últimas décadas.
1.5 Marcação e Morfologia das hemácias
hemácias incluem: (1) o transporte transmembranar de íons de cloreto estanoso7 e pertecnetato no compartimento interno destas células, (2) redução de 99mTc (99mTcO4-) pelo SnCl2 e (3) de ligação do 99mTc reduzido para hemoglobina2. A banda-3 é o sistema de transporte do tecnécio para o interior das hemácias, e os canais de cálcio são responsáveis pelo transporte do estanho33,34,63. A literatura médica sobre o assunto em questão descreve o efeito de drogas artificiais e naturais no processo de radiomarcação de células vermelhas do sangue e proteínas plasmáticas com 99mTc. Qualquer droga pode modificar a biodisponibilidade de radiofármacos, podendo alterar a marcação de constituintes sanguíneos atuando
como agente antioxidante, modificando a estrutura da membrana ou diminuindo a eficiência do sistema de transporte transmembrana de íons estanoso e pertecnetato nas células. Neste estudo avaliamos o impacto da cirurgia de grande porte na morfologia e na marcação das hemácias61 com o tecnécio, a partir de um modelo experimental, pois sabemos que ocorrem alterações nas mesmas em situações de trauma, e quanto mais severo o trauma, mais intensas são as alterações64.
2. JUSTIFICATIVA
Já é bem estabelecido na área da medicina nuclear que determinadas
patologias, medicamentos, produtos naturais e determinados procedimentos
cirúrgicos podem alterar a biodistribuição do tecnécio e/ou fixação dos constituintes
sanguíneos7,8,9,26. Este fato não ocorre somente no tecido traumatizado, mas também em outros órgãos não submetidos a intervenções cirúrgicas7. Este estudo se propõe a avaliar se a biodistribuição de um determinado radiofármaco também sofreria influência após a realização de uma cirurgia de grande porte, em modelo murino, além de estimar se tais fatores exercem alguma alteração na função hepática, bem como sobre a morfologia e marcação das hemácias.
O radiofármaco utilizado foi o tecnécio por ser facilmente disponibilizado e ter propriedades quase ideais26. Devido ao CCR ser uma doença muito prevalente44, e
as metástases hepáticas associadas à este muito frequentes41-44; temos na cirurgia o melhor tratamento para esta doença avançada43,44,51-53. Por isso, escolhemos o procedimento cirúrgico colectomia direita com hepatectomia esquerda como representante do grupo de cirurgia de grande porte pois, além de ser cada dia mais realizado, por ser mais factível, este procedimento também revolucionou o tratamento do câncer colorretal nas últimas décadas, elevando os pacientes portadores do CCR com metástase hepática de uma situação de tratamento paliativo a uma de potencial cura.
hemácias e a biodistribuição do tecnécio podem estar alterados em órgãos importantes, assim os exames cintilográficos poderão estar sujeitos a resultados falso-positivos ou falso-negativos.
Pesquisa bibliográfica minuciosa em bases de dados eletrônicas revelou ausência de estudos nessa linha de pesquisa: alteração na biodistribuição de radiofármacos após colectomia com hepatectomia. Foram usados descritores como: metabolismo, biodistribuição, tecnécio, isótopos radioativos versus colectomia associada a hepatectomia. Desse modo, o estudo experimental teve a intenção de dar contribuição importante para o conhecimento de aspectos ainda não esclarecidos.
3. OBJETIVOS
3.1 Objetivo geral
Este trabalho objetiva avaliar se a realização de uma colectomia com hepatectomia em ratos exerce influência na biodistribuição do radiofármaco
99mTc-fitato e na função hepática.
3.2 Objetivos específicos
Avaliar se a biodistribuição do tecnécio, no fígado e hemácias de ratos, sofre alteração após um colectomia direita com hepatectomia esquerda.
Avaliar se o procedimento cirúrgico descrito altera os valores das enzimas hepáticas: TGO, TGP e FA.
Avaliar se tal intervenção cirúrgica altera a marcação e morfologia das hemácias.
4. MÉTODOS
O modelo animal escolhido para realização desta pesquisa experimental foi o rato Wistar. Os 18 animais utilizados foram fornecidos pelo biotério do Centro de Ciências da Saúde, com pesos no intervalo de 285±23 g. Foram alojados em gaiolas individuais de polipropileno e mantidos sob condições controladas de temperatura e ambiente com um ciclo claro-escuro de 12 horas. Foi permitido acesso ad libitum ao alimento na forma de ração (Labina, Purina ®) e água.
Todos os procedimentos experimentais envolvendo os animais foram
realizados de acordo com o Código de Ética para a experimentação animal e as diretrizes brasileiras para o uso científico de animais (Lei n º 11.794). O protocolo foi aprovado pelo Comitê de Ética em Pesquisa (CEP) da Universidade Federal do Rio Grande do Norte (UFRN).
No pré-operatório os animais permaneceram em jejum entre 12-18 horas. A anestesia foi realizada com injeção intraperitoneal de 0,2 ml/100 g de uma solução contendo 1 ml de cetamina (50 mg) e 1 ml de xilazina (20 mg) e então os animais foram operados sob condições assépticas após tricotomia e antissepsia com álcool 70%. Além disso, foi mantida analgesia por via subcutânea imediatamente após a cirurgia, e a cada 12 horas durante três dias com cloridrato de tramadol solução contendo 1ml (100 mg) na dose de 20 mg/kg.
Os animais foram divididos, aleatoriamente, em três grupos com seis ratos cada; o primeiro grupo chamado colectomia foi submetidos à laparotomia mediana e realizou-se uma colectomia parcial direita. Foram ressecados o ceco, 10 cm de cólon direito e 5 cm de íleo terminal. O trânsito intestinal foi reconstruído através de anastomose término-terminal ileocólica com sutura em pontos separados usando fio de polipropileno 6-0 (Ethicon®, Brasil), com auxílio um microscópio cirúrgico – aumento 10x (DFVasconcelos, São Paulo, Brasil). A laparotomia foi fechada por planos através de sutura contínua com fio mononylon 4-0 (Ethicon®, Brasil). No segundo grupo, denominado colectomia+hepatectomia, os ratos foram submetidos à colectomia parcial, com a mesma técnica descrita acima para o grupo colectomia,
intestino, sendo a parede abdominal fechada nas mesmas condições dos outros grupos.
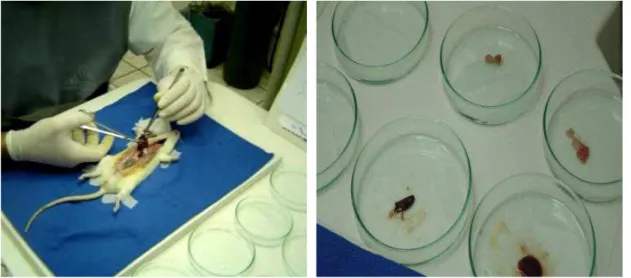
Os animais dos três grupos permaneceram em observação por 30 dias, em gaiolas individuais nas condições ambientais previamente descritas, e nesse período foram pesados semanalmente em balança digital (Filizola® São Paulo, Brasil) com sensibilidade para variação a partir de 1 grama. Após esse periodo os animais foram anestesiados e submetidos à administração de radiofármaco através da cateterização da veia femoral numa alíquota de 0,1 ml de 99mTc-fitato, correspondendo a uma atividade radioativa de 0,66 MBq. Decorridos quinze minutos da administração do radiofármaco, foi colhida amostra de 5 ml de sangue por punção cardíaca, os animais foram sacrificados com superdose de anestésico (tiopental sódico 100mg/Kg intraperitoneal) e procedeu-se a retirada de amostra do fígado para determinar a biodistribuição do fitato (Figura 1), a seguir estas foram lavadas com solução salina 0,9% (Figura 2) e pesadas em balança de precisão
(Figura 3). Um contador gama automático Wizard 1470 (Perkin-Elmer®, Finlândia)
detectou a captação radioativa hepática e das hemácias, medidas em percentual de radioatividade por grama de tecido (% ATI/g) (Figura 4).
Figura 1- Retirada das amostras hepáticas.
Toda essa fase do experimento, que utiliza radiação, seguiu as normas de radioproteção preconizados pela Comissão Nacional de Energia Nuclear (CNEM). O radiofármaco utilizado foi fornecido pelo Serviço de Medicina Nuclear da Liga Norteriograndense Contra o Câncer (LIGA) e os rejeitos radioativos foram prontamente devolvidos para a LIGA em recipiente de chumbo, para tratamento adequado.
Avaliação bioquímica
As amostras de sangue, em volumes de 3 ml, foram inseridas em tubos de ensaio sem anticoagulante, centrifugadas a 3000 rpm por 10 min e as alíquotas de plasma estocadas a -40°C até análise. Os provas de função hepática como: Aspartato aminotransferase (AST), alanina aminotransferase (ALT) e fosfatase alcalina (FA) foram medidas usando um kit comercial e dosadas em auto-analisador (Konelab, versão do software, 60i, Finlândia).
Morfologia das hemácias
A partir de amostras de sangue total foram preparadas distensões sanguíneas em lâminas, que foram coradas pelo método Leishman. As imagens das hemácias foram capturadas por câmera digital (Samsung®) usando-se microscopia óptica (Microscópio Olympus, modelo BX50, Japan, aumento 1000x,) para análise digital, após a transferência da imagem do microscópio para a tela do computador. Para
Figura 3-Pesagem em balança de precisão.
obtenção da forma das hemácias e das medidas morfométricas (relação perímetro/área) foi utilizado programa específico (Image ProPlus Software, versão 6.0).
Estatística
Os dados obtidos foram expressos em média ± desvio padrão. A comparação entre os grupos foi realizada pela análise de variância (ANOVA) e pelo teste de comparações múltiplas de Tukey, usando-se significância de 0,05.
5. ARTIGOS PRODUZIDOS
5.1. O Artigo foi publicado no periódico Acta Cirúrgica Brasileira 2011;26(6):503-07.
ISSN 1678-2674. Que possui fator de impacto 0.2486, Qualis B1 da Capes para
Área Medicina III.
Metabolic and hematologic consequences of colectomy associated
to hepatectomy in rats
1Consequências metabólicas e hematológicas da colectomia associada à
hepatectomia em ratos
Marília Daniela Ferreira CarvalhoI, Irami Araújo-FilhoII, Ítalo Medeiros AzevedoIII, Amália Cínthia Meneses RêgoIV, Aldo Cunha MedeirosV
1 Research performed at Center of Experimental Surgery, Department of Surgery, UFRN, Natal-RN,
Brazil.
I
Fellow Master Degree, Postgraduate Program of Health Sciences, UFRN, Natal, Brazil. Acquisition,
interpretation of data and collection of study informations.
II
PhD, Associate Professor, Department of Surgery, Federal University of Rio Grande do Norte
(UFRN), Natal, Brazil. Involved with technical procedures.
III
Fellow Master Degree, Department of Statistics, UFRN, Natal, Brazil.
Responsible for interpretation of data, statistical analysis.
IV
PhD, Associate Professor, Potiguar University, Natal, Brazil. Helped with technical procedures,
collection and processing of study informations
V
Chairman, Full Professor, Department of Surgery and Postgraduate Program of Health Sciences,
UFRN, Natal, Brazil. Responsible for conception, design, intellectual and scientific content of the
study.
ABSTRACT
Purpose: This study investigated the influence of partial colectomy associated with hepatectomy on the biodistribution of the 99mTc-phytate, on metabolic parameters, as
well as labeling and morphology of red blood cells. Methods: Wistar rats were
colectomy+hepatectomy and sham. In the 30th postoperative day all rats were
injected with 99mTc-phytate 0.1mL i.v. (radioactivity 0.66 MBq). After 15 minutes, liver
sample was harvested and weighed. Percentage radioactivity per gram of tissue
(%ATI/g) was determined using an automatic gamma-counter. Serum AST, ALT,
alkaline phosphatase and red blood cells labeling were determined. Results: The liver %ATI/g and red blood cells labeling were lower in colectomy and
colectomy+hepatectomy rats than in sham rats (p <0.05), and no difference was
detected comparing the colectomy and colectomy+hepatectomy groups. Red blood
cells morphology did not differ among groups. Serum levels of AST, ALT and alkaline
fosfatase were significantly higher in colectomy+hepatectomy than in colectomy rats
(p<0.001). Conclusion: Hepatectomy associated with colectomy lowered the uptake
of radiopharmaceutical in liver and in red blood cells in rats, coinciding with changes
in liver enzymatic activity.
Key words: Colectomy. Hepatectomy. Metabolism. Biological availability. Radiopharmaceutical.
RESUMO
Objetivo: Investigar a influência da colectomia associada à hepatectomia parcial, na biodistribuição do fitato-99mTcO4, na marcação e morfologia de hemácias e em
parâmetros metabólicos. Métodos: Ratos Wistar foram distribuídos em três grupos (6 animais cada), denominados: colectomia, colectomia+hepatectomia e sham. No
30º dia pós-operatório, em todos eles foi feita injeção de 0,1 mL i.v. de fitato-99mTcO4
(radioatividade 0,66 MBq). Após 15 minutos, uma amostra de fígado foi colhida e
pesada. O percentual de radioatividade por grama de tecido (%ATI/g) foi
determinado no fígado e hemácias usando-se um contador gama automático.
Dosagem sérica de AST, ALT, fosfatase alcalina, morfologia e marcação de
hemácias com pertecnetato foram determinadas. Resultados: O %ATI/g no fígado e
nas hemácias foi menor nos animais dos grupos colectomia e
colectomia+hepatectomia do que no grupo sham (p<0,05; teste de Tukey). Nenhuma
diferença foi detectada comparando os grupos colectomia e
colectomia+hepatectomia. A morfologia das hemácias não diferiu entre os 3 grupos.
Os níveis séricos de AST, ALT e fosfatase alcalina foram significativamente maiores
no grupo colectomia+hepatectomia do que no grupo colectomia (p<0,001).
captação de radiofármaco no fígado e hemácias de ratos, coincidindo com
alterações na atividade enzimática do fígado.
Descritores: Colectomia. Hepatectomia. Metabolismo. Biodisponibilidade. Radiofármaco.
INTRODUCTION
The liver is affected by metastases in 50% of patients with colorectal cancer and
metastatic disease remains the leading cause of cancer-related death. The
metastases may be single or multiple, affecting one or both hepatic lobes and are
synchronous with the primary tumor in 16 to 25% of cases, several months or years
after diagnosis1. The surgical resection of liver metastases is possible in 10 to 15%
of patients and it is considered the treatment of choice with potential for cure and
five-year survival in 22 to 65% of cases2.
One of the most widely used diagnostic tools in identifying diseases and
metabolic changes, uses radiopharmaceuticals. On nuclear medicine, pertechnetate
(99mTcO4-) is used in the diagnosis of gastric, kidney, liver, lung, intestinal, skeletal,
endocrine, heart, blood flow and postoperative disorders3. Used intravenously, this
radiopharmaceutical remains in the circulation long enough to analyse various
organic and functional parameters for the diagnosis of diseases. Gradually it comes
into equilibrium with the extracellular space, is taken up by tissues, and a small
percentage is eliminated by urinary excretion. The 99mTcO4- is used in approximately
85% of diagnosis procedures, has low cost and small environmental impact3. Some
recent studies have demonstrated significant changes in biodistribution of 99mTcO4-
on the postoperative of major surgery4-8.
In nuclear medicine, red blood cells can be labeled by 99mTcO4-, and used to
detect certain clinical disorders, digestive bleeding, blood flow, heart perfusion, etc9.
The labeling of blood constituents with 99mTcO4- has been used as a tool in
experimental studies in vitro and in vivo, in order to demonstrate the interaction
between drugs and radiopharmaceuticals18. The labeling of red blood cells involves
intracellular reaction between 99mTcO4- and hemoglobin. It is often used to evaluate
pulmonar perfusion10, digestive bleeding, liver tumors and hemodynamic disorders11.
It has been shown that changes on the morphology of red blood cells may arise in
labeling. These changes are more severe in patients with postoperative septic
complications12.
Any deviation in the uptake of radiopharmaceuticals, on vital organs and red
blood cells after surgery, can result undesirable interpretations in the results of
scintigraphic examinations, leading to mistaken diagnoses, with serious
consequences to the patients. Repetition of the exams can determine an increase of
radiation dose for patients and risk for the involved professionals.
This work is part of a research field that has been studying the consequences
of major surgery performed in organs of the digestive system. We have
demonstrated relevant postoperative metabolic disorders after massive intestinal
resection4, total gastrectomy5,6, total colectomy7 and Roux-en-Y gastric bypass8, by
using this experimental model.
Based on the above concepts, this study aimed to examine in an animal model
if colectomy associated with hepatectomy modifies liver biodistribution of 99m
Tc-phytate, metabolic parameters and labeling of red blood cells.
METHODS
Eighteen Wistar rats weighing 285±23g, were housed in polypropylene cages
and kept under controlled conditions of temperature in a clear-dark cycle of 12 hours
and allowed ad libitum access to food (Labina, Purina ®) and water. All experimental
procedures in animals were conducted according to the code of ethics for animal
experimentation of the Council for International Organization of Medical Sciences
and the Brazilian Law on the Scientific use of Animals (Law No. 11794). The protocol
was approved by the Institutional Research Ethics Committee. The anesthesia was
accomplished with intraperitonial injection of 0,2ml/100g of a solution containing 1ml
of ketamine (50mg) and 1 ml of xilazine (20 mg) and operated under aseptic
conditions. In addition, analgesia (tramadol 20 mg/kg body weight) was applied
subcutaneously immediately after surgery and every 12 hours for three days.
The animals from group colectomy underwent laparotomy and a subtotal
colectomy was performed, proceeding ileocolic anastomosis with 6-0 polypropilene
suture. Cecum, 5 cm of colon and 10 cm of ileum were resected. The laparotomy
was closed in layers with 4-0 mononylon. In the group colectomy+hepatectomy the
liver. In the group sham, we performed medium laparotomy and soft manipulation of
the intestine.
The animals were weighed weekly and remained under observation. After 30
days they were anesthetized, the femoral vein was dissected and 0.1 mL of 99m
Tc-phytate was injected i.v. (radioactivity 0.66 MBq). After 15 minutes, 5 mL of blood
were harvested by cardiac puncture and the rats were killed with an overdose of
anesthetic (sodium thiopental 100mg/Kg). A sample of liver was harvested to
examine the biodistribution of 99mTc-phytate.
After centrifugation of 2 mL of blood, red blood cells were separated for
examination of in vivo labeling with pertechnetate and morphology. The liver samples
were isolated, washed with 0.9% saline solution and weighed with a precision scale
(Bel-Mark 160-II-Italy). The detection of liver radioactive uptake was determined
using an automatic gamma counter, Wizard 1470 (PerkinElmer, Finland). The
percentage of radioactivity per gram of tissue (%ATI/g) was calculated dividing the
activity of the liver sample by the total activity administered to each animal. The
experiment with radiopharmaceutical was carried out in compliance with radiation
protection standards recommended by the Comissão Nacional de Energia Nuclear.
The radiopharmaceutical was provided by Department of Nuclear Medicine of Liga
Norte-Riograndense Contra o Câncer (LIGA) and the radioactive waste returned to
the LIGA for proper treatment.
Assay for biochemical levels
Samples of blood (3 mL) were inserted into test tubes without anticoagulant,
centrifuged to 3000 rpm by 10 min and the serum was stocked to -40°C until
analysis. Serum levels of aspartate aminotransferase (AST), alanine
aminotransferase (ALT), and alkaline phosphatase were measured using a
commercial kit on the autoanalyzer (Konelab, Software Version, 60i, Finland).
Red blood cells morphology
Blood strains were prepared on slides, them stained with Leishman. The
images of red blood cells were captured by digital camera using optical microscopy
(Olympus microscope, model BX50, Japan, 1000x,) for analysis. To take the shape
of red blood cells and the morphometric measurements we used the ImagePro Plus
Estatistics
Data were expressed as mean±sd. The comparison between groups was
performed by analysis of variance (ANOVA) and by the multiple comparison test of
Tukey, using a 0.05 significance.
RESULTS
The animals were randomly divided into three groups of six each. We
observed 8% weight loss in group colectomy+hepatectomy at the end of first week. A
progressive recovery of weight occured until day 30. In the other groups there was no
weight loss after surgery. At the end of the experiment there was no significant
difference in mean weights among groups.
Table 1 shows the results of the percentage of radioactivity per gram of tissue
(%ATI/g), found in red blood cells and liver, as well as the tests to investigate the
statistical differences among the groups colectomy, colectomy+hepatectomy and
sham.
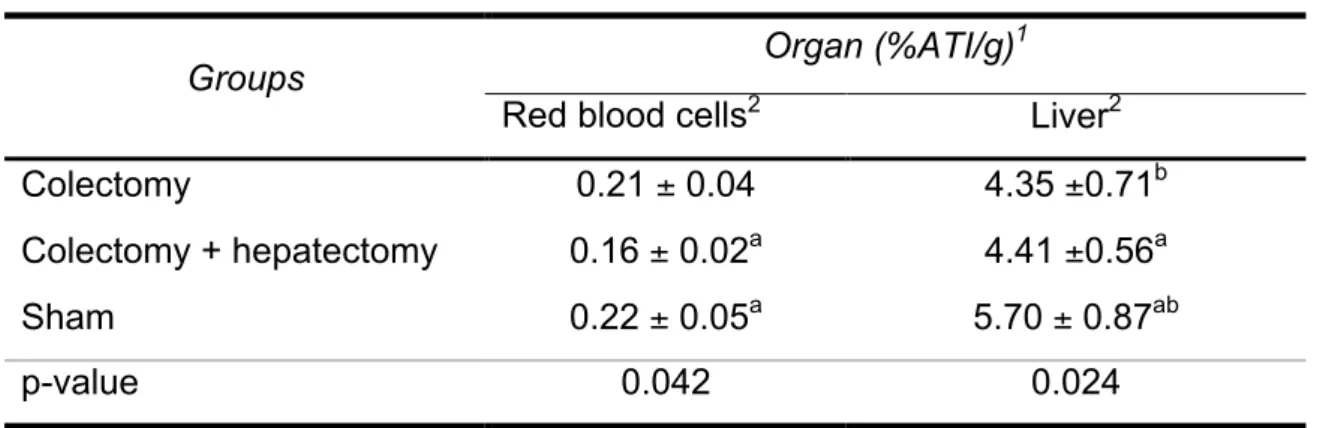
Table 1 - 99mTc-phytate biodistribution studies for each group.
Groups Organ (%ATI/g)
1
Red blood cells2 Liver2
Colectomy 0.21 ± 0.04 4.35 ±0.71b
Colectomy + hepatectomy 0.16 ± 0.02a 4.41 ±0.56a
Sham 0.22 ± 0.05a 5.70 ± 0.87ab
p-value 0.042 0.024
Mean±Standard deviation
1. Percent of radioactivity per gram of tissue
2. Dosages in each column, followed by the same letter differ significantly (Tukey test).
Rats from colectomy and colectomy+hepatectomy groups had significantly
lower 99mTc-phytate uptake in the liver than in the sham group rats (p=0.024). The
99m
Tc-phytate uptake in the liver of colectomy rats was higher than in the
colectomy+hepatectomy group rats, but the difference was not significant (p>0.05).
when the colectomy+hepatectomy group rats were compared with sham rats
(p=0.042). These data are summarized in table 1.
Table 2–Serum levels of liver enzymes and alkaline phosphatase in colectomy, colectomy+hepatectomy and sham rats.
Groups AST (u/L)1 ALT (u/L)1 Alkaline phosphatase (u/L)1
Colectomy 37,67 ± 1,37a 47,33 ± 2,50a 170,6± 22,91b
Colectomy +
hepatectomy 155,00 ± 13,67
ab
76,33 ± 6,89a 232,3 ± 28,93ab
Sham 44,33 ± 4,72b 51,17 ± 3,19 180,7 ± 20,35a
p-value <0,001 <0,001 <0,001
Mean ± Standard deviation
1. Dosages in each column, followed by the same letter, differ significantly (Tukey test). AST, aspartate animotransferase; ALT, alanine aminotraferase
Serum levels of AST, ALT and alkaline phosphatase were significantly higher
in colectomy+hepatectomy rats than in colectomy group rats (p<0.001), signaling that
hepactectomy contributed to these results. Comparing the serum levels of AST, ALT
and alkaline phosphatase from colectomy group with sham rats, the results were
similar (p>0.05) (Table 2).
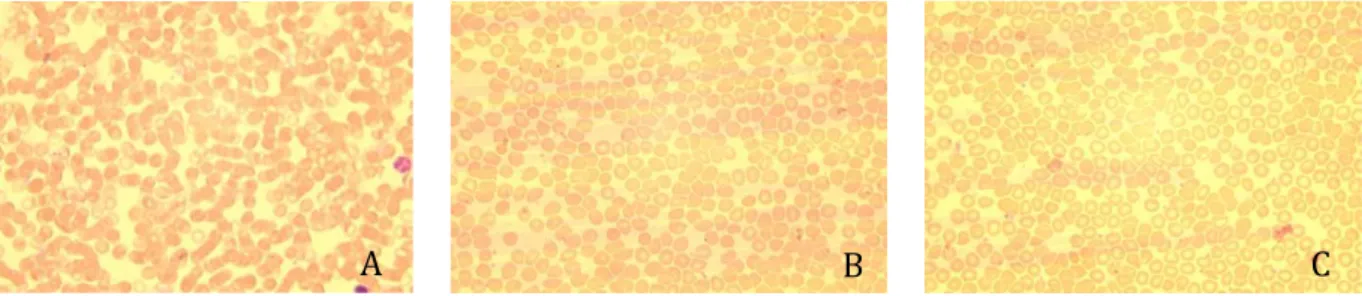
The qualitative and quantitative evaluation of the shape of red blood cells
under optical microscopy was performed and alterations on the shape and
morphometric measures were not found, when compared the three groups (Figure
1).
Figure 1 – Photomicrography of red blood cells from (A) colectomy, (B) colectomy +hepatectomy and (C)
sham rats. 1000x.
DISCUSSION
It is well established in the area of digestive surgery that surgical resection is
the most effective treatment for isolated liver metastasis in patients with colorectal
cancer13. Perioperative morbidity and mortality does not differ between simultaneous
resections and staged procedures for selected patients with liver metastases.
Meanwhile, patients undergoing simultaneous resections could expect a short
duration of surgery and postoperative hospitalization as well as less blood loss during
surgery13. Although the treatment for patients with synchronous colorectal cancer
liver metastases remains controversial, surgical resection of both the primary tumor
and liver metastases is the only option offering a potential cure13.
In the experimental model used in this work we did not include induction of
colon cancer, because our objective was to examine the repercussion of colectomy
associated partial hepatectomy without carcinogenesis. After the standardization of
the technique in the pilot study, the morbidity was low and there was not mortality
during the 30 days of observation of all rats. Despite the great surgical trauma, the
animals progressed well until the end of the experiments. Weight loss in the first
week was observed in the animals from colectomy+hepatectomy group, but they had
a satisfactory recovery in the three subsequent weeks. These findings corroborate
the statement that hepatectomy increased morbidity, but over time the animals had
satisfactory evolution.
However, at the end of the observation and collection of biological samples,
we detected significant changes in some parameters, when the groups were
compared. There was a significant reduction in 99mTc-phytate biodistribution in the
liver of colectomy+hepatectomy animals, compared with the sham group, but no
difference was observed comparing with colectomy group. This finding may be
interpreted based on the hypotesis that after 30 days liver regeneration was sufficient
to compensate any disfunction, normalizing the 99mTc-phytate uptake.
The distribution of radiocolloids in the liver has been shown to correlate well
with the severity of chronic liver diseases, the severity of histologic fibrosis,
prognosis, and hepatic function14. Thus, liver uptake of 99mTc-phytate colloid
provides a practical index of hepatic function and image, by using planar scintigraphy
techniques15. In a study from our laboratory it was demonstrated that in
controls, suggesting that the operation favored the hepatic uptake of the
radiopharmaceutical. This result coincided with the improvement in liver function,
confirmed by the better alanine aminotransferase, aspartate aminotransferase and
lactic dehydrogenase activities in splenectomized rats, compared with controls16.
Otherwise, in the present study the lower liver 99mTc-phytate uptake coincided with a
lower alanine aminotransferase, aspartate aminotransferase and alkaline
phosphatase activities in colectomy+hepatectomy rats, than in sham rats.
Nuclear medicine procedures have proven increasingly effective imaging
modalities in the study of several disorders17. Besides the disease, these procedures
could be altered by medications, surgery and natural products that could change the
biodistribution of radiopharmaceuticals in a specific target or the fixation of 99mTc to
blood constituents16,18. In general, the labeling of blood constituents could decrease
by the action of drugs and trauma:(a) changing of the cellular membrane structure or
modifying the transport systems of pertechnetate ions into cells, (b) by direct
oxidation or generation of free radicals, (c) by direct inhibition (chelating action) of
pertechnetate ions, or (d) binding at the same sites on the blood constituents3. In this
study we observed that pertechnetate labeling of red blood cells of the
colectomy+hepatectomy rats was lower than in sham rats. This data is relevant,
because red blood cells labeling is an important method for diagnosis of digestive
and renal bleeding19. Interactions of some factors resulting from hepatic resection
may be involved with the ion transport systems of pertechnetate ions, decreasing the
labeling of red blood cells with pertechnetate. This could in part, explain the data
obtained.
CONCLUSION
In conclusion, hepatectomy associated with colectomy lowered the liver and
erytrocytes uptake of pertechnetate in rats, coinciding with changes in hepatic
enzymatic activity.
REFERENCES
1. Lochan R, White SA, Manas DM. Liver resection for colorectal liver
metastasis. Surg Oncol. 2007;16:33–45.
2. Lee WS, Yun SH, Chun HK, Lee WY, Kim SJ, Choi SH, Heo JS, Joh JW, Choi
D, Kim SH, Rhim H, Lim HK. Clinical outcomes of hepatic resection and
radiofrequency ablation in patients with solitary colorectal liver metastasis. J
Clin Gastroenterol. 2008;42:945–9.
3. Arano, Y. Recent advances in 99mTc radiopharmaceuticals. Ann Nucl Med
2002, 16:79-93.
4. Chacon DA, Araujo Filho I, Villarim Neto A, Medeiros AC. Biodistribuição do
radiofármaco pertecnetato de sódio (Na99mTcO4) em ratos submetidos a
ressecção extensa de intestino delgado. Acta Cir Bras. 2007;22: 430-5.
5. Medeiros AC, Filho IA, Medeiros VB, Pinheiro LA, Freire FH, Azevedo IM,
Brandão-Neto J. Comparing reconstruction with ileocecal graft to jejunal
interposition pouch after total gastrectomy in rats. J Invest Surg. 2007;20:41-8.
6. Rêgo AC, Villarim Neto A, Azevedo IM, Araújo-Filho I, Egito ES, Medeiros AC.
Biodistribution of Technetium-99m pertechnetate after total gastrectomy and
Roux-en-Y jejunal pouch. J Invest Surg. 2010;23:94-100.
7. Rêgo AC, Ramalho RA, Egito ES, Araújo-Filho I, Azevedo IM, Palestro CJ,
Medeiros AC. Biodistribution of technetium-99m pertechnetate after total
colectomy in rats. Appl Radiat Isot. 2010;68:2169-73.
8. Rêgo AC, Araújo-Filho I, Azevedo IM, Jácome DT, Ramalho R A, Medeiros
AC. Biodistribution of technetium-99m pertechnetate after Roux-en-Y gastric
bypass (Capella technique) in rats. Acta Cir Bras. 2010;25:9-12.
9. Zink SI, Ohki SK, Stein B, Zambuto DA, Rosenberg RJ, Choi JJ, Tubbs DS.
Noninvasive evaluation of active lower gastrointestinal bleeding: comparison
between contrast-enhanced MDCT and 99mTc-labeled RBC scintigraphy. Am
J Roentgenol. 2008;191:1107-14.
10. Hunt A, Frier M, Johnson R, Berezenko S, Perkins A C. Preparation of
Tc-99m-macroaggregated albumin from recombinant human albumin for lung
perfusion imaging. Euro J Pharm Biopharm. 2006; 62: 26-31.
11. Schneider A, Attaran M, Gratz K F, Bleck J S, Winkler M, Manns M P, Ott M.
hepatocytes in rabbits: assessment of shunting and portal hemodyn changes.
Exp Transplant. 2003; 75: 296-302.
12. Berezina T L, Zaets S B, Machiedo G W. Alterations of red blood cell shape in
patients with severe trauma. J Trauma-Injury Infect Crit Care. 2004; 57: 82-7.
13. Jong M, van Vledder M, Ribero D, Hubert C, Gigot J, Choti MA, Schulick
RD, Capussotti L, Dejong CH, Pawlik TM. Therapeutic efficacy of combined
intraoperative ablation and resection for colorectal liver metastases: an
international, multi-institutional analysis. J Gastrointest Surg. 2011;15:336–44.
14. Hoefs JC, Wang F,Kanel G. Functional measurement of nonfibrotic hepatic
mass in cirrhotic patients. Am J Gastroenterol. 1997; 92:2054–8.
15. Kikuchi M, Tomita K, Nakahara T, Kitamura N, Teratani T, Irie R, Yokoyama
H, Suzuki T, Yokoyama T, Taguchi T, Tanaka S, Noguchi M, Ohkura T, Hibi T.
Utility of quantitative 99mTc-phytate scintigraphy to diagnose early-stage
non-alcoholic steatohepatitis. Scand J Gastroenterol. 2009;44:229-36.
16. Pereira KRSG, Açucena MKMT, Villarim-Neto A, Rêgo ACM, Bernardo-Filho
M, Azevedo IM, Medeiros AC. Biodistribution of the radiopharmaceutical
technetium-99m-sodium phytate in rats after splenectomy. Braz Arch Biol
Technol. 2008;51:203-7.
17. Lodge MA, Braess H, Mahmoud F, Suh J, Englar N, Geyser-Stoops S,
Jenkins J, Bacharach SL, Dilsizian V. Developments in nuclear cardiology:
transition from single photon emission computed tomography to positron
emission tomography-computed tomography. J Invasive Cardiol.
2005;17:491-6.
18. Fonseca AS, Frydman JN, Rocha VC, Bernardo-Filho M. Acetylsalicylic acid
decreases the labeling of blood constituents with technetium-99M. Acta Biol
Hung. 2007; 2:187-98.
19. Howarth DM. The role of nuclear medicine in the detection of acute
gastrointestinal bleeding. Semin Nucl Med. 2006;36:133-46.
Correspondence: Aldo Cunha Medeiros (aldo@ufrnet.br)
Av. Nilo Peçanha 620, Natal-RN, Brazil 59012-300 Conflict of interest: none.
5.2. Artigo publicado no periódico Journal of Investigative Surgery. 2011;24:109-14.
(Qualis B1). ISSN 0894-1939
Metabolism and gastric remnant changes after Roux-en-Y Gastric
Bypass in rats.
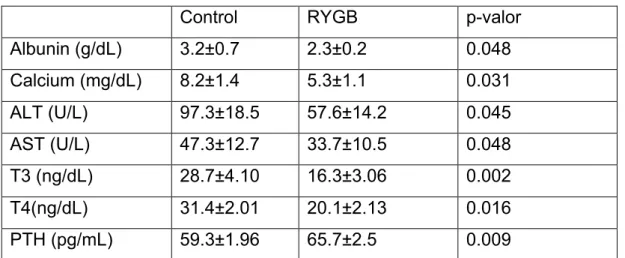
Aldo Cunha Medeiros, Amália Cínthia Meneses Rêgo, Ítalo Medeiros Azevedo, Marília D. Ferreira Carvalho, Vítor Brasil Medeiros, Irami Araújo-Filho.
Department of Surgery, Postgraduate Program in Health Sciences, Federal University of Rio Grande
do Norte, Natal, Brazil.
ABSTRACT
Background: The Roux-en-Y gastric bypass (RYGB) may affect gastric microbiology
as well as the histology of the excluded stomach. Therefore, this study aimed to
investigate these issues in rats. Methods: Twelve rats were randomly allocated to a
RYGB group (n=6) and nonoperated control group (n=6). After 30 postoperative
days, all rats were killed. Samples of the remnant stomach mucosa were harvested
for bacterial and fungal count such as colony-forming units/g and histology. Results:
The excluded stomach mucosa of RYGB rats showed higher bacterial and fungal
count, atrophy, intestinal metaplasia and neutrophilic polymorphonuclear
inflammation than in controls. Conclusions: This work showed that a model of murine
RYGB significantly modified the microbiota/histology of the excluded stomach.
Keywords: Bariatric surgery, Gastric microbiology, Histology, Roux-en-Y gastric bypass, Rats
INTRODUCTION
Morbidity and mortality are strongly correlated to the level of obesity [1], and
the list of diseases with a causal factor for obesity continues to expand. The failure of
most current approaches to control morbid obesity has led to the development of
(bariatric surgery). Patients have achieved effective weight loss after bariatric surgery
and most have had complete resolution or improvement of their diabetes,
hypertension, hyperlipidemia, and obstructive sleep apnea [2], in addition to reduced
long-term mortality [3]. The Roux-en-Y gastric bypass (RYGB) is the predominant
approach used in the United States [4] and Brazil [5]. After the adoption of RYGB,
occasional concern has arisen regarding bacterial overgrowth in the upper digestive
tract, especially in the excluded stomach. Gastric juice is an important barrier against
bacterial colonization and an essential component of the gut barrier, which protects
the organs from infection when vagal innervation is lost [6].
Although the procedure can be successful, it is associated with a number of
metabolic and structural complications. These complications are sometimes subtle
and difficult to diagnose early. Since these patients have limited physiologic reserve,
it is imperative that complications are identified early by image procedures and
appropriately managed [7]. One of the most widely used diagnostic methods in
identifying a great number of diseases and metabolic disorders is the use of
radiopharmaceuticals, radioactive compounds used in diagnostic procedures as
sources of radiation and tracers. Examination of gastric emptying, liver function,
thyroid function, bone disorders, etc, are often used in patients undergoing bariatric
surgery. Radiopharmaceutical biodistribution may provide important information
about their uptake to target organs and their function, but post-surgery data are
scarce [8]. It is important to investigate the biodistribution of technetium-99m
pertechnetate after RYGB, since it is highly secreted by gastric mucosa. After this
operation the stomach is mostly bypassed, the metabolism is affected, and changes
in biodistribution are expected. Drugs and surgery may interfere in the biological
behavior of radiopharmaceuticals used in scintigraphy and single photon emission computed tomography (SPECT). Technetium-99m pertechnetate is used in more
than 80% of scintigraphic examinations [9-11]. Thus, the biological effects of
technetium-99m pertechnetate and its uptake to various organs may be altered.
RYGB is a major surgery and may therefore result in important anatomical and
metabolic changes as well as unpredictable complications [7]. Accordingly,
scintigraphic studies may be needed in the postoperative period. Given that the
biodistribution of technetium-99m pertechnetate is expected to cause changes in
may produce false-positive or false negative images, leading to repetition of nuclear
medicine procedures with unnecessary radiation exposure for patients.
The aim of this study was to analyze the effects of RYGB on gastric microbiology,
metabolism, histology and technetium-99m pertechnetate biodistribution in rats.
METHODS
The use of laboratory animals followed the Council for International Organization
of Medical Sciences Ethical Code for animal experimentation and the Brazilian
guidelines for the scientific use of animals (Law no. 11.794). The protocol was
approved by the Institutional Research Ethics Committee. Rats were observed in
individual polypropylene cages at room temperature of 24ºC, relative humidity of
45%, 12-hour light/dark cycles, with food and water ad libitum. For preoperative
procedures, rats were deprived of food for 16 to 18 hours and anesthetized with a
mixture of ketamine and xylazine (200 mg: 5 mg, 0. 8 ml/kg, intraperitoneally). For
postoperative pain control, 1.5 mg/kg of tenoxicam (Roche, Brazil) was administered
subcutaneously, once a day for 3 days.
Operative and laboratory procedures
Twelve Wistar rats (349.3 ±10.7 g) were equally divided into RYGB and control
groups. The rat abdomens were shaved and prepared with 70% alcohol. All the
surgical procedures were carried out by the same well-trained investigator,
experienced in animal surgery. Three previous series of experiments were conducted
in sequence to develop the RYGB model. A midline incision was made, exposing the
stomach and distal esophagus. The stomach was divided 2 cm below the esophagus
and both gastric ends were oversewn using a running 6-0 polypropylene suture. The
suture lines were then embrocated. The jejunum was divided 16 cm below the
ligament of Treitz, creating a 16 cm biliary-pancreatic limb. A 4 to 5 mm end-to-side
gastrojejunostomy was sewn using interrupted 6-0 polypropylene sutures on the
anterior surface of the gastric fundus. The stump of the proximal jejunum was closed
with a running suture. A 7 to 8 mm side-to-side jejunojejunostomy was sewn 10 cm
which the abdomen was closed in layers, using a running 4-0 nylon suture. Rats
drank water and a 10% glucose plus 2% saline solution starting 24 hours after the
operation and for the first 3 days. This was followed by a solid diet (Labina-Purina®).
For the first three postoperative days, rats were hydrated with normal saline solution
(20ml) injected subcutaneously to prevent dehydration. A surgical microscope with
10x magnification (DF Vasconcelos, São Paulo, Brazil) was used for anastomosis.
The control group rats (n=6) were not operated.
The animals remained under observation for 30 days after surgery and under
anesthesia, injected with 0.1 ml of technetium-99m pertecnetate via the orbital
plexus, corresponding to radioactive activity of 0.66 MBq. Thirty minutes after
radiopharmaceutical administration, blood samples were obtained by cardiac
puncture to determine serum dosages. Furthermore, a midline laparotomy was
performed under sterile conditions. The defunctionalized stomach was opened and
intragastric material (including mucosa) was harvested for culture. Samples were
collected from the nonoperated stomach of control rats. Samples were then removed
from the liver, kidney, heart, lung, thyroid, stomach and femur. The tissue samples
were washed in 0.9% saline and weighed on a precision scale (Mark 160®, Bel
equipment, Italy). Radioactivity was determined in an automatic gamma counter
(Wizard 1470®, Perkin-Elmer, Finland). The results were shown in counts per minute
(CPM), corrected by disintegrations per minute (DPM). The efficiency of the gamma
counter was 86%, as specified by the manufacturer. The specific activity of each
sample was calculated by dividing absolute count in DPM by weight (DPM/g). The
percentage radioactivity of each sample (% ATI/g) was calculated by dividing its
specific activity (DPM/g) by the total radioactivity of each animal.
Laboratory tests
Blood samples were centrifuged immediately at 3000 rpm for 10 min. and serum
samples stored at -80°C until analysis. Serum albumin, calcium, alanine (ALT) and
aspartate aminotransferase (AST) levels were assayed using a Konelab 60i analyzer
(assay kit from Weiner, São Paulo, Brazil). The levels of free triiodothyronine (T3),
free thyroxin (T4) and parathyroid hormone (PTH) were determined by
radioimmunoassay using an [I125] and PTH assay kit (Diagnostic Products, Los
Microbiological analysis
The excluded stomach was opened and antral specimens (5 mm
punch-biopsy) for bacterial quantification were obtained on day 30. In control rats, samples
were harvested from the antrum of the non operated stomach. They were then
individually weighed and homogenized in 1 ml of sterile 0.9% saline solution using a
sterile technique. Serial dilution was performed, and samples were plated onto
trypticase soy agar containing 5% sheep blood agar for colony counts of viable
aerobic bacteria. Aliquots were spread on blood/agar plates for Gram positives and
agar McConkey for Gram negative bacteria. Incubation proceeded at 37˚C for 48 h.
The number of colony-forming units (CFU)/g was counted in 100-µl aliquots of fluid.
Fungi were inoculated in acidified agar/dextrose/potato plates, and incubation
proceeded at 25˚C for 7 days. The number of colonies was computed by colony
counter, and all colony counts were expressed as the number of colony-forming units
per gram of tissue (CFU/g).
Statistical analysis
The data were expressed as mean ± standard deviation. Statistical analysis for
group comparison was performed using the Student t test, at a significance level of
0.05.
RESULTS
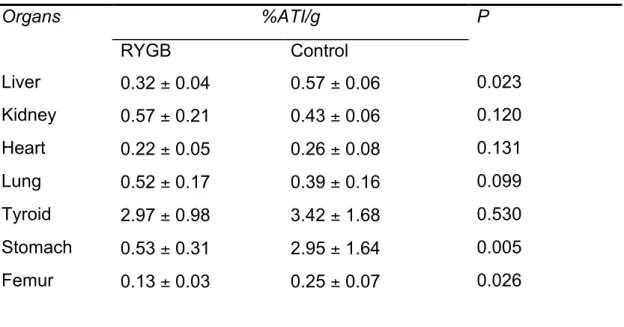
All animals survived the study. Table 1 summarizes the descriptive results of
percentage radioactivity (% ATI) in the organs of rats from groups RYGB and