P . b . b . 0 4 Z 0 3 5 8 5 0 M , V e r l a g s p o s t a m t : 3 0 0 2 P u r k e r s d o r f , E r s c h e i n u n g s o r t : 3 0 0 3 G a b l i t z
Homepage:
www.kup.at/
gefaessmedizin
Online-Datenbank mit
Autoren- und Stichwortsuche
www.kup.at/gefaessmedizin
Indexed in EMBASE/COMPENDEX/GEOBASE/SCOPUS
Offizielles Organ der Österreichischen Gesellschaft
für Internistische Angiologie (ÖGIA)
Offizielles Organ des Dachverbandes der
Gefäßmedizinischen Gesellschaften Österreichs
Member of the
Das Milzarterienaneurysma: Klinik
Diagnostik und Therapie – Eine
Kasuistik und Übersicht
Pfabe FP
Zeitschrift für Gefäßmedizin 2014;
Jetzt in 1 Minute
Früh-erkennung der PAVK: boso
ABI-system 100
PAVK – Die unterschätzte Krankheit
Die periphere arterielle Verschlusskrank-heit (PAVK) ist weitaus gefährlicher und verbreiteter als vielfach angenommen. Die getABI-Studie [1] zeigt, dass 20 % der > 60-Jährigen eine PAVK-Prävalenz aufweisen. Die PAVK wird oft zu spät diagnostiziert. Das liegt vor allem da-ran, dass die Betroffenen lange Zeit be-schwerdefrei sind und eine entsprechen-de Untersuchung daher meist erst in akuten Verdachtsfällen erfolgt. Mit dem Knöchel-Arm-Index („ankle- brachial in dex“ [ABI]) ist die Diagnose einer PAVK durchführbar. Der Knöchel-Arm-Index (ABI) ist ein wesentlicher Marker zur Vorhersage von Herzinfarkt, Schlag-anfall und Mortalität.
PAVK-Früherkennung mit dem boso ABI-system 100: Ein Gewinn für alle. Eine präzise und schnelle, vaskulär orientierte Erst untersuchung.
Der entscheidende Wert für die Dia-gnose der PAVK ist der Knöchel-Arm-Index („ankle-brachial index“ [ABI]). Das boso ABI-system 100 ermittelt die-sen Wert zeitgleich und oszillometrisch an allen 4 Extremitäten. Die eigentliche Messung dauert dabei nur ca. 1 Minu-te. Ein ABI-Wert < 0,9 weist im
Ver-gleich mit dem Angiogramm als Gold-standard mit einer Sensitivität von bis zu 95 % auf eine PAVK hin und schließt umgekehrt die Erkrankung mit nahezu 100 % Spezifität bei gesunden Perso-nen aus.
Das boso ABI-system 100 wurde wei-terentwickelt und ist jetzt optional mit der Messung der Pulswellenge-schwindigkeit ausgestattet.
Optional ist das boso ABI-system 100 ab sofort auch mit der Möglichkeit zur Messung der
Pulswellengeschwindig-keit (ba) verfügbar. Mit der Messung der Pulswellengeschwindigkeit („pulse wave velocity“ [PWV]) kann eine arteri-elle Gefäßsteifigkeit diagnostiziert wer-den. Die Steifigkeit der arteriellen Ge-fäße nimmt mit einer fortschreitenden Arteriosklerose zu, was sich durch eine Erhöhung der Pulswellengeschwindig-keit darstellt. PWV und ABI-Wert er-möglichen eine noch fundiertere Risi-kostratifizierung von kardiovaskulären Ereignissen.
Literatur:
1. http://www.getabi.de
Weitere Informationen:
Boso GmbH und Co. KG Dr. Rudolf Mad
A-1200 Wien
Handelskai 94–96/23. OG E-Mail: rmad@boso.at
Neues aus der Medizintechnik
18 Z GEFÄSSMED 2014; 11 (2)
Das Milzarterienaneurysma: Klinik, Diagnostik und
Therapie – Eine Kasuistik und Übersicht
F.-P. Pfabe
Aus dem Asklepios Klinikum Uckermark, Schwedt, Deutschland
Einleitung
Das Aneurysma der A. lienalis stellt die häufi gste Lokalisa-tion viszeraler Aneurysmen dar, deren Ursache die Arterio-sklerose, entzündliche-infektiöse Veränderungen und ange-borene Bindegewebspathologien sind. Der Verlauf ist über-wiegend asymptomatisch, die gefürchtetste Komplikation ist die Ruptur, die mit einer hohen Letalität, insbesondere in der Schwangerschaft, einhergeht. Aneurysmagröße und -morpho-logie, natürlicher Verlauf, Ätiologie und bestehende Komorbi-ditäten bestimmen Zeitpunkt und Therapieform. Diagnostisch ist eine Angio-CT mit 3D-Rekonstruktion der Goldstandard. Neben operativen Strategien haben sich endovaskuläre/inter-ventionelle Techniken etabliert.
Krankengeschichte
Anamnese
Nach röntgenologischer Beschreibung einer Kalkringfi gur links paravertebral LWK 1 im November 2012 (Abb. 1) wur-de im Oktober 2013 ambulant bei einem 72-jährigen Patienten mittels Duplexsonongraphie (Abb. 2) und kontrastmittelver-stärkter Computertomographie ein Aneurysma der A. lienalis (32 × 26 × 26 mm) diagnostiziert (Abb. 3).
Das Risiko-Profi l für eine Arteriosklerose war durch patho-logische Fettstoffwechsel-Parameter charakterisiert. Der all-gemeine Gefäßzustand wies einen elongierten und dilatativen Aspekt auf.
Stationäre Aufnahme und Befunde
Klinischer Status
Bei der Aufnahme sahen wir einen 72-jährigen Patienten in gutem AZ und leicht adipösem EZ. Die Körpergröße betrug 172 cm, das Gewicht 82 kg (BMI 27,1). Es wurde ein Blut-druck von 140/80 mmHg beidseits und eine regelmäßige Herzfrequenz von 80/min registriert. Cor, Pulmo und das Ab-domen waren physikalisch unauffällig, der neurologische Be-fund und der Pulsstatus regelrecht.
Labor bei Aufnahme bzw. Erstwerte (Normwerte in Klammern) Hb 7,9 mmol/l (8,7–10,9); Leuko 3,8 gpt/l (4,4–11,3); Ery 4,27 tpt/l (4,8–5,7); Baso 1,2 % (0,0–1,0), Mono 13,3 % (2– 12); TG 2,0 mmol/l (0,35–1,8); HDL 0,80 mmol/l (1,0–4,0); LDL-HDL-Quotient 3,89 (0,0–3,5); im Normbereich Lipase 0,57 µmol/s*l (0,00–1,07); Amylase 1,31 µmol/s*l (0–1,67) und übrige Parameter.
Therapie und Verlauf
Im November 2013 erfolgte die stationäre Aufnahme zu ei-nem geplanten interventionellen Therapieversuch. Aufgrund des äußerst geschlängelten Gefäßverlaufes war trotz Verwen-dung unterschiedlicher Materialien und Techniken eine siche-re Sondierung der A. lienalis und die Implantation eines ge-coverten Stents nicht möglich (Abb. 4). Ein Embolisations-verfahren wurde wegen des breitbasigen Aufsitzens und des schwer zu visualisierenden Halses des nach dorsal gelegenen Aneurysmas verworfen.
For personal use only. Not to be reproduced without permission of Krause & Pachernegg GmbH.
Abbildung 2: Duplexsonographische Darstellung des Aneurysmas der A. lienalis
Fallbericht
19
Z GEFÄSSMED 2014; 11 (2)
Die chirurgische Resektion des Aneurysmas (Kontinuitätsre-sektion) erfolgte im Intervall von 4 Wochen unter Anlage ei-ner spannungsfreien End-zu-End-Anastomose in fortlaufen-der Nahttechnik (5 × 0 Surgipronaht) im mittleren Drittel fortlaufen-der A. lienalis. Das Operationspräparat wies makroskopisch ein 3,2 × 3,0 × 2,8 cm großes Aneurysma mit kalzifi zierender und atheromatöser Wandveränderung auf. Ein Gefäßstück von 2,3 cm Länge und 9 mm Durchmesser war intimal durch gelb-liche, teils kalkharte Veränderungen charakterisiert. Eine ekta-tische Aufweitung von 1,3 × 1,3 × 1,3 cm Größe, die präope-rativ nicht beschrieben wurde, fand sich in unmittelbarer Nähe des Aneurysmas (Abb. 5 a–c).
Postoperativ entwickelte sich eine transfusionspfl ichtige An-ämie (Hb 5,7) aufgrund einer intraperitonealen Einblutung
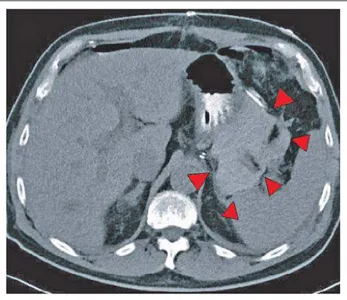
(Bursa omentalis), die am 4. postoperativen Tag eine Revisi-on des Cavum peritRevisi-oneum mit Hämatomausräumung (8 × 6 × 10 cm großes Hämatom) erforderlich machte (Abb. 6). Bei suffi zienter Anastomose fanden sich diffuse kleine Blu-tungsquellen im Bereich der früheren Aneurysmalokalisation, die sorgfältig gestillt wurden.
Eine passagere, asymptomatische Erhöhung der Pankreas-Enzyme (Amylase 4,55; Lipase 4,54) werteten wir im wei-teren Verlauf bei sonomorphologisch und computertomogra-phisch unauffälligem Pankreas als operationsbedingte Al-teration. Nach Relaparatomie unkomplizierter Verlauf mit Normalisierung der Pankreasenzyme und Entzündungspara-meter.
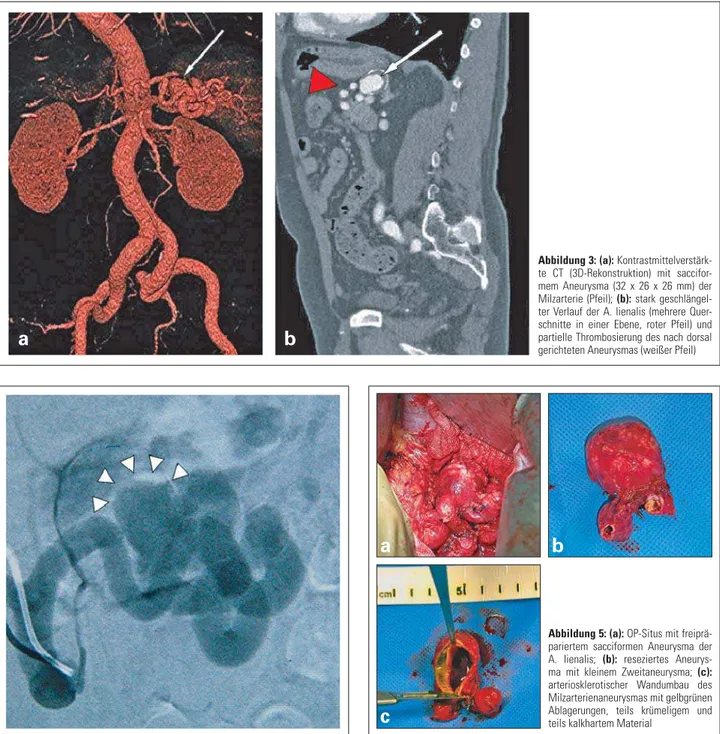
Abbildung 4: Angiographische Darstellung des sacciformen Aneurysmas (Pfeile) und des stark geschlängelten Verlaufs der A. lienalis
Abbildung 3: (a): Kontrastmittelverstärk-te CT (3D-Rekonstruktion) mit saccifor-mem Aneurysma (32 x 26 x 26 mm) der Milzarterie (Pfeil); (b): stark geschlängel-ter Verlauf der A. lienalis (mehrere Quer-schnitte in einer Ebene, roter Pfeil) und partielle Thrombosierung des nach dorsal gerichteten Aneurysmas (weißer Pfeil)
a b
Abbildung 5: (a): OP-Situs mit freiprä-pariertem sacciformen Aneurysma der A. lienalis; (b): reseziertes Aneurys-ma mit kleinem ZweitaneurysAneurys-ma; (c):
arteriosklerotischer Wandumbau des Milzarterienaneurysmas mit gelbgrünen Ablagerungen, teils krümeligem und teils kalkhartem Material
a b
Fallbericht
20 Z GEFÄSSMED 2014; 11 (2)
Diskussion
Aneurysmatische Veränderungen viszeraler Arterien sind sel-ten und betreffen lediglich 0,1–2,0 % der arteriellen Aneurys-men. Diese treten solitär auf oder imponieren bei systemischer Wandpathologie als Aneurysmose [1, 2].
Mit 80 % sind der Truncus coeliacus und seine Äste am häufi gs-ten betroffen, wobei die A. lienalis in 60 % und die A. hepatica und ihre Äste in 20–30 % betroffen sind.
Als einziges viszerales Aneurysma weist das Aneurysma der A. lienalis einen geschlechtsspezifi schen Unterschied zuguns-ten des weiblichen Geschlechts (4:1) auf [1, 2].
Das Aneurysma verum der A. lienalis ist überwiegend arte-riosklerotischer Natur (60 %), seltener sind eine fi bromusku-läre Dysplasie, kongenitale Bindegewebsdefekte, Traumen oder entzündliche und infektiöse Prozesse Ursachen der Ge-fäßwandpathologie. Schwangerschaftsassoziierte hormonel-le Veränderungen, ein alternierender Fluss in der Portal vene, eine portale Hypertonie sowie Flussveränderungen in der Milzarterie führen zu einer Schädigung der elastischen Fasern und begünstigen die Aneurysmaentstehung.
Pseudoaneurysmen beruhen dagegen auf Gefäßarrosionen, die im Rahmen einer akuten oder chronischen Pankreatitis oder als Komplikation endovaskulärer und kathetertechni-scher Prozeduren im hepatobiliären System entstehen [2, 3]. Neben Pseudo- und wahren Aneurysmen können morpholo-gisch das fusiforme und das sacciforme sowie topographisch organbezogen das intra- und extralienale Milzarterienaneurys-ma unterschieden werden [2].
Da sichere Angaben über die Wachstumstendenz des Visze-ralarterienaneurysmas nicht existieren, ist der natürliche Ver-lauf des Milzarterienaneurysmas, wie bei allen Viszeralarte-rienaneurysmen, nicht sicher vorhersehbar und bei 75 % der Patienten durch eine langjährige asymptomatische Phase
cha-rakterisiert. Dagegen werden jedoch 95 % der jungen Frauen, die ein Milzarterienaneurysma haben, im 3. Trimenon symp-tomatisch [4, 5].
Komplikationsbedingte Symptome nehmen ab einem Aneu-rysmadurchmesser von 2 cm zu, wobei die Spontanruptur die gefürchtetste Komplikation darstellt.
Das Rupturrisiko wird bei einer Aneurysmagröße von > 2 cm mit 30–40 % beschrieben und ist mit einer Letalität von 46– 75 % vergesellschaftet. Besonders prädisponieren Aneurys-men der A. lienalis bei Mul tipara in 25–45 % zu Rupturen. Bei Nicht-Schwangeren beträgt das Rupturrisiko 3–10 % bei einer Letalität von 10–25 %. Das mykotische Aneurysma ist eben-falls durch ein hohes Rupturrisiko aufgrund der schnellen Pro-gredienz charakterisiert [2, 4, 6, 7].
Die rupturassoziierte Einblutung kann retroperitoneal oder in die Bauchhöhle, in das Gallengangs- oder Pankreasgang-system sowie in die Begleitvene (AV-Fistel) erfolgen. Ein klinisches Prodromalstadium mit linksseitigen Oberbauchbe-schwerden geht der Ruptur eines Aneurysmas der A. lienalis oft voraus. Die fatalen Folgen einer Ruptur bedingen die hohe Letalität, die maternal mit 70–75 % und fetal bis zu 95 % be-schrieben wird.
Gastrointestinale Schmerzen, ein Schockzustand mit Blut-druck- und Hb-Abfall sind bei Schwangeren richtungswei-send [4, 5, 8].
Neben der Ruptur sind als weitere Komplikationen die peri-phere Embolisation, die thrombotische Okklusion (Ischämie, Milzinfarkt) und die Kompression benachbarter Strukturen (Passagebehinderung des Magen-Darm-Traktes, hepatobiliä-re Stauung, Milzvenenverschluss) zu nennen [1].
Wie in der Kasuistik beschrieben, erfolgt die Diagnosestel-lung eines asymptomatischen Viszeralarterienaneurysmas in der Regel zufällig (Kalkschatten, pulsierender/perfundierter Tumor, Strömungsgeräusch) oder durch Abklärung unspezi-fi scher gastrointestinaler Symptome bei Auftreten einer Kom-plikation. Methode der Wahl sind die Computertomographie und die Angio-CT mit 3D-Rekonstruktion, die eine sichere Beurteilung der Gefäßmorphologie sowie benachbarter Struk-turen erlauben [1, 2, 4].
Abgesehen von Schwangeren ist eine intraarterielle Mesente-rikographie unverzichtbar, die durch Darstellung der Kollate-ralzirkulation (Aa. gastricae breves) eine individuelle Behand-lungsplanung wie auch eine endovaskuläre Therapie in glei-cher Sitzung ermöglicht und abgelaufene periphere Thromb-embolien demaskieren kann.
Die Therapie des Milzarterienaneurysmas wird durch Größe, Morphologie, Lokalisation und Symptomatik sowie Komorbi-ditäten und Patientenwunsch bestimmt. Eine Aneurysmagrö-ße von > 2 cm ist das entscheidende Kriterium bei der Indi-kationsstellung, während kleinere Aneurysmen engmaschig kontrolliert werden sollten. Lediglich das mykotische und das Pseudoaneurysma stellen eine absolute Therapieindikation dar [1, 2, 6].
Fallbericht
21
Z GEFÄSSMED 2014; 11 (2)
Einige Autoren empfehlen dagegen eine Aneurysmaausschal-tung bei einer Größe, die das 3–4-Fache des originären Ge-fäßdurchmessers beträgt. Dies erscheint sinnvoll, da die A. lienalis einen variablen Diameter von 4–11 mm aufweisen kann [2, 4, 9].
Für Milzarterienaneurysmen gilt, wie für Viszeralarterien-aneurysmen allgemein, dass Patienten mit einem hohen ope-rativen Risiko, bei denen endovaskuläre Techniken nicht indi-ziert sind, engmaschig kontrolliert und ab einem Durchmesser von 5 cm operiert werden sollten [2].
Eine absolute Behandlungsindikation stellt das symptoma-tische Aneurysma der A. lienalis dar, wobei sowohl ruptur-bedingte Blutungen als auch Organischämien allgemein mit einer hohen Letalität vergesellschaftet sind.
Während die freie Ruptur mit hämodynamischer Instabilität eine Domäne des chirurgischen Vorgehens ist, kommen endo-vaskuläre Methoden bei gedeckter Ruptur oder zur passageren Blutstillung durch Katheterblockade des zuführenden Gefäßes zum Einsatz. Bei Schwangeren gilt das chirurgische Vorge-hen (fehlende Strahlenbelastung) als Therapie der Wahl, eben-so bei infl ammatorisch-mykotischen Aneurysmen, wobei hier das befallene Gefäßsegment und das umgebende Gewebe re-seziert werden [8].
Das chirurgische Vorgehen beim Aneurysma der A. lienalis besteht in Abhängigkeit von der Lokalisation, der Größe und der Qualität der Kollateralzirkulation (Aa. gastricae breves), in der Ligatur, der Kontinuitätsresektion, der Rekonstruk-tion durch ein Interponat/Bypass oder einer Splenektomie bei hilusnaher Lokalisation oder Aneurysmose. Ein Pseudoaneu-rysma infolge einer Pankreatitis kann eine Pankreasschwanz-resektion erfordern.
Mögliche Komplikationen sind Fisteln, Blutungen, Hämato-me, Hernien und Pankreatitiden, die auch in der vorliegenden Kasuis tik den postoperativen Verlauf maßgeblich geprägt ha-ben [5].
Aufgrund des operativen Zugangstraumas, der perioperati-ven Morbidität (7,1–12,0 %) und Letalität (0–5 %) werden bei Viszeralarterienaneurysmen zunehmend endovaskuläre Tech-niken favorisiert [2, 9, 10].
Mit den Embolisationsverfahren und den gecoverten Stents stehen 2 etablierte Verfahren zur Auswahl, deren Einsatz von der Morphologie der zu- und abführenden Gefäße (Diameter, Kinking, Kalzifi kation) wesentlich beeinfl usst wird. Ist für ge-coverte Stents das Vorhandensein einer Landungszone erfor-derlich, so ist eine optimale, sicher zu sondierende Konfi gura-tion des Aneurysmahalses Voraussetzung für die Anwendung eines Embolisationsverfahrens [2, 4, 6].
Bei Viszeralarterienaneurysmen liegt die primäre Erfolgsrate embolisierender Verfahren bei 72–98 %, während die Morbi-dität endovaskulärer Verfahren mit 14–25 % und die Mortali-tät mit 2,8–8,3 % beschrieben werden. Komplikationen und Risiken eines endovaskulären Vorgehens sind eine Infarzie-rung durch Gefäßverlegung (6–20 %), eine spätere Ruptur
des Aneurysmas bei ineffektivem Coilpacking (18–35 %) und eine Blutung (8 %) [2, 3, 4, 9–12].
Insbesondere die A. lienalis ist häufi g durch einen stark elon-gierten und gekinkten Gefäßverlauf charakterisiert, an dem eine interventionelle Therapie scheitern kann, wie die vorlie-gende Kasuistik zeigt. Eine Embolisation war in unserem Fall auch aufgrund der Aneurysmamorphologie (breitbasig auf-sitzend, unzureichende Visualisierung des nach dorsal abge-henden Aneurysmahalses) kontraindiziert. Letztendlich wur-de das chirurgische Vorgehen im geschilwur-derten Fall als The-rapie der Wahl postoperativ durch die histopathologische Be-fundung des Resektionspräparates mit Nachweis eines kleinen Zweitaneurysmas bestätigt.
Allgemein gilt die chirurgische Ausschaltung eines solitären Viszeralarterienaneurysmas als Sanierung, wobei im Lang-zeitverlauf Nahtaneurysmen auftreten können. Die laparos-kopische Ausschaltung eines Aneurysmas der Viszeralarterien ist nur in Ausnahmefällen, bei guter Zugänglichkeit des Gefä-ßes, möglich [2, 9, 10].
Im Gegensatz zum offen-chirurgischen Vorgehen sind nach in-terventioneller Behandlung bildgebende Kontrollen erforder-lich und Zweiteingriffe im Verlauf nicht auszuschließen.
Fazit für die Praxis
Viszeralarterienaneurysmen sind eine seltene Entität arte-rieller Aneurysmen, die in 60 % die A. lienalis betreffen. Der natürliche Verlauf ist lange asymptomatisch, klinische Symptome sind Ausdruck einer Komplikation und häu-fi g unspezihäu-fi sch. Angio-CT und DSA-Angiographie sind wichtige diagnostische Methoden. Die Ruptur ist die ge-fürchtetste Komplikation, die am häufi gsten bei Schwange-ren mit einer hohen Mortalität auftritt.
Die Rupturwahrscheinlichkeit nimmt ab einem Aneurys-madurchmesser > 2 cm deutlich zu. Mit chirurgischen und endovaskulären Techniken stehen alternative Techniken so-wohl bei der Ruptur als auch elektiven Versorgung zur Ver-fügung.
Danksagung
Mein Dank gilt Herrn D. Hinc und Herrn D. Sud für die Über-lassung der intraoperativen Bilddokumentation.
Interessenkonfl ikt
Der korrespondierende Autor gibt an, dass kein Interessen-konfl ikt vorliegt.
Literatur:
1. Diagnostik und Therapie der Aneurysmen des Truncus coeliacus, der A. lienalis, hepati-ca und mesenterihepati-ca. (DGG), www.gefässchir-urgie.de/.../LL_Viiszeralarterienaneurysmen_ 2011.pdf (Zuletzt gesehen: 23.3.2014). 2. Meyer A, Lang W.Viszeralarterienaneurys-men. Gefässchirurgie 2011; 16: 355–62.
3. Sessa C, Tinelli G, Porcu P, Aubert A, et al. Treatment of visceral artery aneurysms: de-scription of a retrospective series of 42 aneu-rysms in 34 patients. Ann Vasc Surg 2004; 18: 695–703.
Fallbericht
22 Z GEFÄSSMED 2014; 11 (2) 5. Hanschke D, Eberhardt E. Riesenaneurysma der A. lienalis – eine Kasuistik. Gefässchirurgie 2002; 7: 70–3.
6. Guillon R, Garcier JM, Abergel A, Mofi d R. Management of splenic artery aneurysms and false aneurysms with endovascular treat-ment. Cardiovasc Intervent Radiol 2003; 26: 256–60.
7. Grotemeyer D, Gabitz K, Balzer K, Reinecke P, Poll L, Sandmann W. Das mykotische Viszeral-arterienaneurysma. Chirurg 2004; 75: 533–40. 8. Lauschke H, Rudolph J, Textor J, Strunk H, Remig J. Das Viszeralarterienaneurysma. Zentralbl Chir 2002; 127: 538–42.
9. Carr SC, Mahvi DM, Hoch JR, Archer CW, et al. Visceral artery aneurysm rupture. J Vasc Surg 2001; 33: 806–11.
10. Chiesa R, Astore D, Guzzo G. Viszeral ar-tery aneurysms. Ann Vasc Surg 2005; 19: 42– 8.
11. Gabelmann A, Gorich J, Merkle EM. Endo-vascular treatment of visceral artery aneu-rysms. J Endovasc Ther 2002; 9: 38–47 12. Tulsyan N, Kashyap VS, Greenberg RK, et al. The endovascular management of visceral artery aneurysms and pseudoaneurysms. J Vasc Surg 2007; 45: 276–83.
Korrespondenzadresse Dr. med. Frank-Peter Pfabe
Asklepios Klinikum Uckermark GmbH Klinik für Gefäßmedizin
D-16303 Schwedt Auguststraße 23
Die neue Rubrik im Journal für Kardiologie:
Clinical Shortcuts
In dieser Rubrik werden Flow-Charts der Kardiologie kurz und bündig vorgestellt
Zuletzt erschienen:
Interventionelle kathetergestützte
Diagnostik der Synkope
Aortenklappenimplantation (TAVI)
J Kardiol 2015; 22 (5–6): 132–4.
J Kardiol 2014; 21 (11–12): 334–7.
Einsatz einer perioperativen Blockertherapie
Kardiologische Rehabilitation nach
zur Reduktion von Morbidität und Mortalität
akutem Koronarsyndrom (ACS)
J Kardiol 2015; 22 (1–2): 38–40.
J Kardiol 2015; 22 (9–10): 232–5.
Besuchen Sie unsere Rubrik
P
聺
Medizintechnik-Produkte
boso ABI-system 100 Boso GmbH & Co KG IntelliSpace Cardiovascular
Philips Austria GmbH, Healthcare
BioMonitor 2
BIOTRONIK Vertriebs-GmbH CT TAVI Planning mit
syngo.CT Cardiac Function-Valve Pilot Siemens AG Österreich
STA R Max
Stago Österreich GmbH