www.jped.com.br
ARTIGO
ORIGINAL
Whole-exome
sequencing
as
a
diagnostic
tool
for
distal
renal
tubular
acidosis
夽
Paula
Cristina
Barros
Pereira
a,
Flávia
Medeiros
Melo
a,
Luiz
Armando
Cunha
De
Marco
a,b,
Eduardo
Araújo
Oliveira
a,c,
Débora
Marques
Miranda
a,ce
Ana
Cristina
Simões
e
Silva
a,c,∗aInstitutoNacionaldeCiênciaeTecnologia---MedicinaMolecular(INCT-MM),UniversidadeFederaldeMinasGerais(UFMG), BeloHorizonte,MG,Brasil
bDepartamentodeCirurgia,FaculdadedeMedicina,UniversidadeFederaldeMinasGerais(UFMG),BeloHorizonte,MG,Brasil cDepartamentodePediatria,UnidadedeNefrologiaPediátrica,LaboratórioInterdisciplinardeInvestigac¸ãoMédica,
FaculdadedeMedicina,UniversidadeFederaldeMinasGerais(UFMG),BeloHorizonte,MG,Brasil
Recebidoem11denovembrode2014;aceitoem25defevereirode2015
KEYWORDS
ATP6V0A4; ATP6V1B1; Children;
Distalrenaltubular acidosis;
Genetics; Whole-exome sequencing
Abstract
Objective: Distalrenaltubularacidosis (dRTA)ischaracterized bymetabolicacidosis dueto impairedrenalacidexcretion.Theaimofthisstudywastodemonstratethegeneticdiagnosis offourchildrenwithdRTAthroughuseofwhole-exomesequencing.
Methods: Twounrelatedfamilieswereselected;atotaloffourchildrenwithdRTAandtheir parents,inordertoperformwhole-exomesequencing.Hearingwaspreservedinbothchildren fromthefirstfamily,butnotinthesecond,whereinatwinpairhadseveredeafness. Whole--exome sequencingwasperformedintwo pooledsamples andfindings wereconfirmedwith Sangersequencingmethod.
Results: Two mutations were identifiedin the ATP6V0A4 and ATP6V1B1 genes. In the first family,anovelmutationintheexon13oftheATP6V0A4genewithasinglenucleotidechange GAC→TAC (c.1232G>T)was found,which causedasubstitutionofaspartic acidtotyrosine inposition 411.In thesecond family,ahomozygousrecurrent mutationwithone base-pair insertion(c.11491155insC)inexon12oftheATP6V1B1genewasdetected.
Conclusion: Theseresultsconfirmthevalueofwhole-exomesequencingforthestudyofrare andcomplexgeneticnephropathies,allowingtheidentificationofnovelandrecurrent mutati-ons.Furthermore,forthefirsttimetheapplicationofthismolecularmethodinrenaltubular diseaseshasbeenclearlydemonstrated.
©2015SociedadeBrasileiradePediatria.PublishedbyElsevierEditoraLtda.Allrightsreserved.
DOIserefereaoartigo:
http://dx.doi.org/10.1016/j.jped.2015.02.002
夽 Comocitaresteartigo:PereiraPC,MeloFM,DeMarcoLA,OliveiraEA,MirandaDM,SimõeseSilvaAC.Whole-exomesequencingasa diagnostictoolfordistalrenaltubularacidosis.JPediatr(RioJ).2015;91:583---89.
∗Autorparacorrespondência.
E-mail:acssilva@hotmail.com(A.C.SimõeseSilva).
PALAVRAS-CHAVE
ATP6V0A4; ATP6V1B1; Crianc¸as;
Acidosetubularrenal distal;
Genética;
Sequenciamentototal doexoma
Sequenciamentototaldoexomacomoferramentadediagnósticodeacidosetubular renaldistal
Resumo
Objetivo: Aacidosetubularrenaldistal(ATRd)écaracterizadaporacidosemetabólicadevido àexcrec¸ãorenal de ácido prejudicada.O objetivo desteartigo é apresentar o diagnóstico genéticodequatrocrianc¸ascomATRdcomusodosequenciamentototaldoexoma.
Métodos: Selecionamosduasfamíliasnãorelacionadas,quatrocrianc¸ascomATRdeseuspais, parafazerosequenciamentototaldoexoma.Aaudic¸ãofoipreservadaemambasascrianc¸asda famíliaum,porémemnenhumacrianc¸adafamíliadois,naqualumpardegêmeasteveperda auditivasevera.Fizemososequenciamentototaldoexomaemdoisconjuntosdeamostrase confirmamososachadoscomométododesequenciamentodeSanger.
Resultados: Duasmutac¸õesforamidentificadasnosgenes ATP6V0A4eATP6V1B1.Nafamília um,detectamosumanovamutac¸ãonoéxon13dogeneATP6V0A4comumaalterac¸ãoemum nucleotídeo únicoGAC→ TAC (c.1232G>T)que causousubstituic¸ãode ácido aspártico por tirosinanaposic¸ão411.Nafamíliadois,detectamosumamutac¸ãorecorrentedohomozigoto cominserc¸ãodeumpardebases(c.11491155insC)noéxon12dogeneATP6V1B1.
Conclusão: Nossosresultados confirmamo valor dosequenciamento total doexoma para o estudodenefropatiasgenéticascomplexasepermitemaidentificac¸ãodemutac¸õesnovase recorrentes.Adicionalmente,demonstramosclaramentepela primeiravezaaplicac¸ãodesse métodomolecularemdoenc¸astubularesrenais.
©2015SociedadeBrasileiradePediatria.PublicadoporElsevierEditoraLtda.Todososdireitos reservados.
Introduc
¸ão
Aacidose tubularrenal distal (ATRd)é uma doenc¸arenal raraecomplexadevidoaumdefeitonaexcrec¸ãodacarga de ácidos(H+ e íons de amônia) em células alfa
interca-ladasdo ducto coletor. O acúmuloda cargade ácidos no néfrondistal resultanoconsumo e nareduc¸ãodotampão debicarbonato/CO2nosangue.1 Asprincipais característi-casclínicasdaATRdsãovômito,diarreiae/ouconstipac¸ão, perdadeapetite,polidipsiaepoliúria.Aacidosecrônicaeas alterac¸õessecundáriascomovômito,poliúriaedesidratac¸ão afetamocrescimentoelevamaumdéficitdecrescimento. Estudos de ultrassom podem mostrar nefrocalcinosee/ou nefrolitíase.2 Emgeral,aATRdapresentabomprognóstico casodiagnosticadaprecocementeeotratamentoalcalinoé contínuo.Casonãotratada,aATRdcausaretardodo cresci-mentoeraquitismoemcrianc¸aseosteomalaciaemadultos. Pode ocorrer deteriorac¸ão da func¸ão renal ao longo dos anos.3
A ATR distal pode ser transmitida como uma caracte-rística autossômica dominante ou recessiva.4 O fenótipo autossômico dominante normalmente aparece moderada-mente na adolescência ou na vida adulta;4 um dos pais padece e é o portador da doenc¸a ou a doenc¸a se dá por meio de uma mutac¸ão de novo. Foram identificadas mutac¸ões nogeneSLC4A1em famílias comATRd autossô-micadominante.2,5,6 Ossintomasnofenótipoautossômico recessivoaparecempredominantementenainfânciaouna primeirainfância,quandooretardodocrescimentoémuito comum.Essavariávelpodeocorrercomousemsurdezeos paisnãosãoafetados.2 AATRdautossômicarecessivaestá associada a mutac¸ões em quaisquer dos seguintes genes:
SLC4A1,7ATP6V0A4eATP6V1B1.2,8Indivíduossem deficiên-ciasauditivasnormalmentesãoportadoresdemutac¸õesno
geneATP6V0A4,aopassoqueaquelescomsurdez
apresen-tammutac¸õesnogeneATP6V1B1.Emaproximadamente20% dospacientescomATRd,nenhumamutac¸ãofoiencontrada em quaisquer desses genes relacionados.3 De fato, exis-tempacientescomATRdcomsurdezsemmutac¸õesnogene
ATP6V1B1eoutroscomaudic¸ãonormalquenãoapresentam
mutac¸õesnogeneATP6V0A4.3Essesachados sugeremque outros transportadores oucanais podemcausar ATRd.Em termosdecomplexidade,sabe-sequealgunspacientescom mutac¸õesnogeneATP6V0A4desenvolvemsurdezapenasna segundadécadadevida.Portanto,hámuitosfatoresaserem elucidadosemtermosdecorrelac¸õesfenótipo-genótipo.8---10 Atéagora,jásãoconhecidasmaisde20mutac¸õesnogene
ATP6V0A4.
O sequenciamento total do exoma fornece cober-tura de mais de 95% dos éxons, que contêm 85% das mutac¸ões causadoras de doenc¸as em doenc¸as mendelia-nas e muitos polimorfismosde nucleotídeo simples(SNPs) compredisposic¸ãoparadoenc¸asem todoogenoma.11,12 O sequenciamento total doexoma é interessante para ava-liar a patogênese da doenc¸a e reconhecer novos genes ou mutac¸ões patogênicos relacionados a doenc¸as, princi-palmenteàsdoenc¸asmendelianas.11,12 Nessesentido,este estudo pretendeu avaliar a utilidade do sequenciamento totaldoexomaparaodiagnósticogenéticodeATRd.
Pacientes
e
métodos
Avaliac¸ãoindividualeclínica
Nefrologia Pediátrica da Universidade Federal de Minas Gerais(UFMG),Brasil.Aprimeirafamília(famíliaum) con-sistiaemdoisirmãosafetados,umameninaeummenino, com ATRd, porém sem surdez, com pais não afetados. A segunda família (família dois) apresentava um par de gêmeasmonozigóticas(duasmeninas),diagnosticadascom ATRd e surdez nervosa, com mãe saudável; o pai é des-conhecido. Todos os pacientes foram submetidos a um protocolosistemático,incluindoavaliac¸ãoclínicae nutricio-nal,medic¸õeslaboratoriais,ultrassonografiarenaleanálise genética.Oconsentimentoinformado,aprovadopelo con-selhodeéticainstitucionaldaUFMG,foiobtidodetodosos participantes;nocasodascrianc¸as, tambémfoiobtidode seuspaise/ouresponsáveislegais.
Extrac¸ãodoDNA
ODNAgenômicofoiextraídode5mLdesangueperiférico depacientescomATRdedeseuspais,comousodominikit QiampBloodDNA (Qiagen®, Milão,Itália), deacordo com
as instruc¸ões do fabricante. Todas as amostras tiveramo controledequalidadeverificadocomrelac¸ãoàpurezacomo usodeumespectrofotômetroNanodrop(ThermoScientific®,
Waltham,EUA).AsamostrasdeDNAforamarmazenadasa −20◦Catéouso.
Sequenciamentototaldoexoma
Osequenciamentodoexomafoifeitoemdoisconjuntosde amostrasparaaprimorarosresultados.As amostrasforam divididasemconjuntosnoquedizrespeitoàscaracterísticas clínicasdospacientes.OprimeiroconjuntoapresentavaDNA dosdoisirmãoscomATRdsemsurdezeosegundo,dasirmãs gêmeascomATRdrelacionadaàsurdez.Acaptac¸ãodoarray foi usada para isolar os respectivos genes humanos (Seq-CapEZHumanExomeLibraryv2.0,Roche®,Basileia,Suíc¸a)
e esses genes foram sequenciadosna plataformaIllumina HiSeq2000(Sigma-AldrichCorporation®,Missouri,EUA).
Dadosdefiltragem
Asprincipaisetapasaseguirforamfeitasparapriorizaras variáveisdealta qualidade:(i)variáveisemregiões inter-genéticas, intrônicas e não traduzidas (UTR) e mutac¸ões sinônimasforamexcluídasdaanálise ajusante;(ii) variá-veis com índice de qualidade menor do que 20 foram excluídas; (iii) somente o índice de conservac¸ão (phy-loP) da comparac¸ão de humanos e 43 vertebrados acima de 3 foi considerado; (iv) após essa selec¸ão inicial, os genes restantes foram filtrados pela func¸ão. O software Polyphen2 (http://genetics.bwh.harvard.edu/pph2/) pre-viu possíveis impactos de variáveis. O conjunto final de variáveis selecionadas passou por inspec¸ão visual com o uso do Integrative Genomics Viewer.13 Variáveis polimór-ficas anteriormente descritas em dados públicos foram investigadas e comparadas com as variac¸ões encontra-das no exoma atual. As mutac¸ões selecionadas para investigac¸ão em cada grupo deste estudo não foram encontradas em sequenciamentos de exomas anteriores (http://evs.gs.washington.edu/EVS/).
Validac¸ãodedados
O sequenciamento de Sanger da reac¸ão em cadeia da polimerase (PCR) foi usado na análise para confirmar os dados.Todosospacientese seuspaisforamsubmetidosa PCR.Produtosdeamplificac¸ãodetamanhoadequadoforam identificadoscomousodeeletroforeseemgelde poliacri-lamida.Osprodutos forampurificadoscomo kitQIAquick PCR (Qiagen®, Milão, Itália) e então submetidos a uma
reac¸ão de sequenciamento com o uso tanto de
iniciado-resforward quanto reversecom o ABI BigDye Terminator
CycleSequencing Kit v3.1em umanalisadorgenético ABI PRISM3730XL(AppliedBiosystems®,FosterCity,EUA).Cada
leiturafoialinhadaao sequenciamentode referênciae as mutac¸ões foramidentificadascomo softwareSequencher
(http://www.genecodes.com). Todos os iniciadores foram
projetadoscomaferramentaon-linePrimer3.Osiniciadores
doéxon12dogeneATP6V1B1 foram:
5’TTGACCCCTCGGA-ATGTAGG3’ e 5’CCGGACCCTCTTCTCCTTAC3’ (tamanho do produto: 238 pares de bases). Os iniciadores do éxon 13 do gene ATP6V1B1 foram: 5’ATGCAAATCGTGGAGCTGTG3’ e 5’ATGAATCAGGGCAAGACGGT3’ (tamanho do produto: 264paresdebases).
Estudosestruturaisdasmutac¸ões
Osalinhamentos deproteínas e sequências deDNA foram feitos com os softwares ClustalW e MultAlin (http://
multalin.toulouse.inra.fr/multalin/), respectivamente. A
previsãodasubstituic¸ãodeaminoácidosnafunc¸ãobiológica da proteína foi avaliada com o uso tanto do soft-warePolyPhen-2quanto doProvean (http://provean.jcvi.
orgehttp://genetics.bwh.harvard.edu/pph2/,
respectiva-mente).
Resultados
ATRdsemsurdez
Essa família consistia em dois irmãos, uma menina de 13 anos e seu irmão de sete, com uma ATRd bem defi-nida.Ameninafoiaprobanda,diagnosticadacomATRdaos quatromeses.Osachadosiniciais foramdéficit de cresci-mento,acidosemetabólicahiperclorêmicacompHdaurina excepcionalmentealto(7,0),pH dosanguevenosonormal (7,36),taxadefiltrac¸ãoglomerularnormalenefrocalcinose. O menino foi diagnosticado no primeiro mês de vida, após uma desidratac¸ão grave com acidose metabólica, hipocalemia, elevac¸ão transitória da creatinina sérica e hipocalcemia.Sua primeiraultrassonografiarenalmostrou nefrocalcinosebilateral.Atabela1resumeasmanifestac¸ões clínicasebioquímicasbásicasquelevaramaodiagnósticode ATRdemcadapaciente.Ospaisnãoforamafetadose tive-ramumfilhomaisvelhoquefaleceuaosquatromesescom sintomassemelhantes.
Tabela1 AchadosclínicosebioquímicosiniciaisdepacientescomATRd
Achados/Pacientes II2---Família1 II3---Família1 II1---Família2 II2---Família2
Idade 4meses 1mês 2anos 2anos
Sexo Feminino Masculino Feminino Feminino
Surdez/SNHL Ausência Ausência Presenc¸a Presenc¸a
Pesoaonascer(g) Nãodisponível 3,450 2,340 2,300
Peso(g) 3,960 3,760 8,250 8,300
ZPI <−3 0 <−3 <−3
Altura(cm) 54,5 50,0 73,5 74,0
HAZ <−3 −2 <−3 <−3
Nefrocalcinose Presenc¸a Presenc¸a Ausência Ausência
Manifestac¸õesiniciais Déficitde crescimento, desidratac¸ão
Vômitoe desidratac¸ão
Raquitismo,déficitde crescimento,retardo docrescimento
Raquitismo,déficit decrescimento, retardodo crescimento
Creatininasérica(mg/dL) 0,4 1,7 0,5 0,5
pHdosanguevenoso 7,36 7,16 7,23 7,12
Bicarbonatosérico(mmol/L) 19,0 8,0 15,9 13,7
Potássiosérico(mEq/L) 3,8 2,0 4,0 4,1
Cloretosérico(mmol/L) 109 118 117 123
pHdaurina 7,5 7,1 7,0 7,0
Osnúmerosromanosindicamaposic¸ãodafamílianalinhagem:II2,família1significaasegundaprobanda(filha)dafamíliaum;II3,
família1significaoterceiroprobando(filho)dafamíliaum;II1,família2---aprimeirafilhagêmeadafamíliadois;II2,família2---a
segundafilhagêmea;SNHL,perdaauditivaneurossensorial;ZPI,escoreszdepesoporidade;HAZ,escoreszdealturaporidade.
Após filtrar os dados do exoma, selecionamos o gene
ATP6V0A4paraestudo.Observamosumaalterac¸ãoem um
nucleotídeoúnicoGAC→TAC(c.1232G>T)noéxon13que causousubstituic¸ãodeumaminoácido:ácidoaspárticopor tirosina na posic¸ão 411 (p.D411Y). Essa alterac¸ão no ami-noácido foi preditiva de ser danosa pelo Provean e pelo PolyPhen-2.Essamutac¸ãoocorreemumaminoácido evoluti-vamenteconservadoeafetaresíduosaltamentepreservados (dadosnãoapresentados).
Ospacientes e seuspais foramsubmetidos ao sequen-ciamento de Sanger ao usar o iniciador projetado para o
éxon13dogeneATP6V0A4.Osdoisirmãosapresentarama
mesmamutac¸ãoemhomozigose(c.1232G>T),aopassoque ambosospaisapresentaramumtrac¸oheterozigótico(fig.1A e B). Essa é umanova mutac¸ão autossômica recessivade ATRd.
ATRdcomsurdez
EssafamíliaconsistiaemumpardegêmeascomATRd asso-ciadaasurdeznervosa.Asmeninasforamdiagnosticadasaos doisanosapósumlongoperíododetratamentopara raqui-tismo e retardo do crescimento somente com assistência nutricional.Característicasclínicasebioquímicasnoinício sãoapresentadasnatabela1.
Osequenciamentototaldoexomaconduzidonafamília doisgerou4375SNVse2416INDELs.Apósfiltrarasvariáveis, obtivemossomenteumgenecandidatorestante(tabela2). Selecionamos, com base nos dados do exoma, o gene ATP6V1B1comocandidatonessegrupo.Umainserc¸ãodeum pardebaseshomozigótico(c.11491155insC)noexoma12 foidetectada(fig.2A).AsduasgêmeascomATRd apresenta-ramainserc¸ãodescrita.FizemosaPCRdamãenãoafetada
Tabela2 Priorizac¸ãodavariávelparaafamíliaumefamíliadois
Família1 Família2
Parâmetros Númerodevariáveis Númerodevariáveis
Totaldevariáveis 3.993 6.791
Regiõesintergênicas,intrônicaseUTRemutac¸õessinônimasforam excluídas
1.445 1.912
Variáveiscomíndicedequalidade<20foramexcluídas 879 1.012
PhyloP<3foramexcluídas 131 215
Selec¸ãoporfunc¸ão 15 14
PhyloP<0,7foramexcluídas 10 6
Selec¸ãocomousodabasededadosdegenescomreferênciacruzadaeo aplicativoIGV
1 1
Genecandidate 1 1
A
l:1
ll:1 ll:2 ll:3
l:2 WT
T
T
G
G T
T
∗
GA
A
C
I.1
I.2
II.2
II.3
B
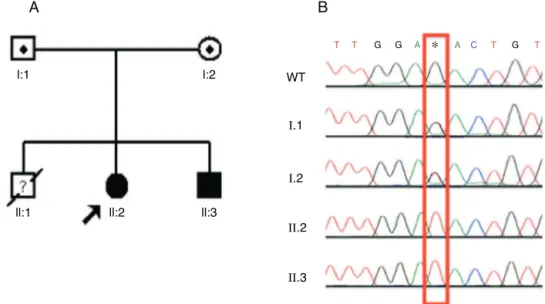
Figura1 Identificac¸ão,linhagemdafamíliaumeresultadosdesequenciamentoparamutac¸ãoc.1232G>T.A)Alinhagemmostra osestadosafetados,identificadoresindividuaisegenótiposnocódon411.Asetaindicaoprobando.B)Cromatogramasdo sequen-ciamentodoDNAemqueosdoisirmãosafetadostêmsubstituic¸ãodohomozigotoGporTemc.1232.Essasubstituic¸ãoocorreem heterozigoseemambosospais.WT,aleloselvagem.*Sequêncianucleotídicamutada.
A
l:1 Allele1wt Allele2Ins Consensus
1.14 1.15 1.164 1.174
lI:1
lI:2 l:2
WT
T A AT A
C C C C C C CC C
I.2
II.1
II.2
B
C
Figura2 Identificac¸ão,linhagemdafamíliadoiseresultadosdesequenciamentoparamutac¸ãoc.11491155insC.A)Identificac¸ão damutac¸ãoc.11491155insCcomosoftwareMultAlin. B)A linhagemmostra osestadosafetados,identificadores individuaise genótiposemc.1149-1155insC.Asetaindicaosprobandoseoindivíduocom‘‘?’’temsituac¸ãodogenótipoincerta.C)Cromatogramas desequenciamentodeDNAdiretodemembrosdafamíliaemqueosdoisirmãosafetadostêminserc¸ãohomozigóticadeumCea mãetemumtrac¸oheterozigótico,conformemarcadopelacaixavermelha.WT,aleloselvagem.
(paidesconhecido).Osdoisirmãosapresentaramamesma mutac¸ãohomozigótica,aopassoqueamãeapresentouessa inserc¸ãonaheterozigose(fig.2BeC).
Discussão
Vários erros de DNA estão localizados em éxons e levam a alterac¸ões estruturais nasproteínas e alterac¸ões funcionais.3Dessaforma,osequenciamentototaldoexoma analisa esses éxons de uma maneira rápida e com bom custo-benefício e permiteavaliac¸ão genéticadas doenc¸as
ainda é desafiadora, pois essas técnicas ainda são muito caraseainterpretac¸ãodedadosétrabalhosaedifícil.11,12 Estudos recentessugerem queo sequenciamento total do exoma seria útil para avaliar a patogênese da doenc¸a e reconhecernovosgenes oumutac¸õespatogênicos relacio-nadosadoenc¸as,principalmenteàsdoenc¸asmendelianas.16 Assim,nopresenteestudo,usamososequenciamentototal doexomaseguidopelosequenciamentodeSangercomouma estratégiaparao diagnósticogenéticodeATRdem quatro crianc¸as.
Nossos resultadosmostraram, pelaprimeira vez,a uti-lidade do sequenciamento total do exoma em doenc¸as tubulares renais e permitiram a identificac¸ão de uma mutac¸ão recorrente e uma nova mutac¸ão patogênica na ATRd.As formasherdadas deATRdapresentamtrês variá-veis:autossômicadominanteeautossômicarecessiva,com ousemsurdez.4Adoenc¸adominantenormalmentese apre-sentamaissuavementenaadolescênciaounavidaadultae temsidorelacionadaapenasamutac¸õesnotrocador bicar-bonato/cloreto(AE1).Por outro lado,avariávelrecessiva ocorrenainfânciaounaprimeirainfância,quandooretardo docrescimentoémuito comum,4 conformeobservado em nossoscasos.AATRdautossômicarecessivatemsido rela-cionadaa mutac¸õesnosgenes ATP6V1B1e ATP6V0A4,que codificamassubunidades a4e B1da ATPasede próton do tipovacuolar(V-ouH+-ATPase),respectivamente.17-22Além disso,mutac¸õesnogeneSLC4A1,responsávelpela expres-sãodeproteínasAE1,tambémforamdetectadasemcasos deATRdautossômicarecessivasemsurdez.23-28
Defato,mutac¸õesemdiferentessubunidadesdabomba deprótonexpressasemtecidosrenaisedeouvidospodem causardefeitostubularesrelacionadosàsurdez.17AATPase deprótondotipovacuolar(V-ouH+-ATPase)éumabomba de várias subunidades essencial para a acidificac¸ão nor-mal. Dois domínios estruturais formam essa bomba: V0 ligado à membrana e V1 citoplasmático ou periférico. Cada domínio incluía múltiplas subunidades (a---e e A---H, respectivamente), responsáveis pela hidrólise do ATP e transportedeprótons,respectivamente.4OgeneATP6V1B1 codifica a subunidade B1, ao mesmo tempo em que o
geneATP6V0A4codificaasubunidadea4.OprótonATPase
vacuolaréexpressoapicalmenteemcélulasrenais␣ inter-caladas,nacócleaenosacoendolinfático.Combasenotipo deperdaauditiva,otipodemutac¸õespodesersuspeito.A perdaauditivacondutivafoiobservadaemmutac¸õesda iso-formaintracelulardeanidrasecarbônica(AC),considerando queaperdaauditivaneurossensorial(SNHL)foiassociadaa mutac¸õesnosgenesATP6V1B1eATP6V0A4.18-20Dessaforma, encontramosumainserc¸ãodeumpardebaseshomozigótico (c.1149 1155insC)noéxon12dogeneATP6V1B1emgêmeas comSNHL.Mutac¸õesnogeneSLC4A1normalmentenão apre-sentamassociac¸ãocomsurdez.22-28 Portanto,apresenc¸ae otipodesurdezauxiliamnadistinc¸ãodediferentesformas deATRd.
Nasduas famílias desteestudo, ospaisnãoforam afe-tados,aATRdteveinícioprecoceelevou aoimpedimento docrescimentodurante ainfância.Portanto,asmutac¸ões
nogene SLC4A1(proteínasAE1) foramaltamente
diferen-tesemnossospacientes.Nafamíliaum,osequenciamento doexomaidentificou umanova mutac¸ão homozigótica no
geneATP6V0A4.Combaseem relatóriosanteriores10 eem
nossascaracterísticasclínicasebioquímicas,essegenefoi
selecionadocomopossívelcandidatoparabuscarmutac¸ões, pois nenhuma perda auditivafoi detectada nos pacientes afetados.Observamosumaúnicaalterac¸ãonucleotídicano éxon13quecausou substituic¸ãodeumaminoácido:ácido aspárticoportirosinanaposic¸ão411.Essaalterac¸ãono ami-noácido foi preditiva de ser danosa pelo Provean e pelo PolyPhen-2. Infelizmente, não fizemos estudos funcionais paradecifrarafunc¸ãoprecisadessamutac¸ão.Entretanto, deve-semencionarqueessamutac¸ãoocorreemum aminoá-cidoconservadoevolutivamenteeafetaresíduosaltamente preservados.Alémdisso, asubstituic¸ãodeácidoaspártico portirosinapodealteraraspropriedadesquímicasda pro-teínaemregiõescríticas.Porexemplo,essaalterac¸ãopode modificaropontoisoelétricodaproteína,considerandoque a tirosina é um aminoácidoneutro, ao passo queo ácido aspárticoéumácido.
Asgêmeasdafamíliadoisapresentaramperdaauditiva neurossensorial e sintomasde início precocede ATRd.Os fenótipos juntamente com os dados do exoma total nos levaramainvestigarogeneATP6V1B1.Dessaforma, cons-tatamosumamutac¸ãopreviamentedescrita,9quetambém foiconfirmadapelosequenciamentodeSanger.Entretanto, deve-se destacarque asmutac¸õesdosgenes ATP6V1B1ou
ATP6V0A4nãoforamencontradasemalgumasfamíliascom
formasrecessivasprimáriasdeATRd.Háváriosoutrosgenes candidatosparaaATRdrecessiva,29principalmenteos rela-cionados aostransportadores deprótons.Nesse sentido,o usodosequenciamentototaldoexoma,juntamentecomas característicasfenotípicas,poderesultarnadescobertade novasmutac¸õese alterac¸õesgenéticasnessadoenc¸a com-plexaerara.
Em resumo,o sequenciamentototal doexomaseguido pelo sequenciamento Sanger foi uma estratégia bem--sucedidanaidentificac¸ãodenovaserecorrentesmutac¸ões em nossoscasosdeATRd.Entretanto,asvariac¸ões genéti-caspossíveiscausadorasdealterac¸õesnotransportetubular renal,principalmentenasformasrecessivasdeATRd,ainda devemserelucidadas.
Conflitos
de
interesse
Osautoresdeclaramnãohaverconflitosdeinteresse.
Agradecimentos
Este estudo foi parcialmente patrocinado pelo Conse-lho Nacionalde Desenvolvimento Científico e Tecnológico (CNPq), Brasil, e pelaFundac¸ão deAmparo à Pesquisado Estadode MinasGerais (Fapemig),Brasil, atravésda Con-cessão do Instituto Nacional de Ciência e Tecnologia ---Medicina Molecular (INCT-MM): Fapemig: CBB-APQ-00075-09/CNPq573646/2008-2.Dr.LADeMarco,Dr.EAOliveira, Dr.DMMirandaeDr.ACSimõeseSilvareceberamumabolsa depesquisadoCNPq.
Referências
2.Fry AC, Karet FE. Inherited renal acidoses. Physiology (Bethesda).2007;22:202---11.
3.EscobarL,MejíaN,GilH,SantosF.Distalrenaltubularacidosis: ahereditarydiseasewithaninadequateurinaryH+excretion. Nefrologia.2013;33:289---96.
4.Pereira PC, Miranda DM, Oliveira EA, Silva AC. Molecular pathophysiology of renal tubular acidosis. Curr Genomics. 2009;10:51---9.
5.BruceLJ,CopeDL,JonesGK,SchofieldAE,BurleyM,PoveyS, etal.Familialdistalrenal tubularacidosisisassociatedwith mutationsintheredcellanionexchanger(Band3,AE1)gene. JClinInvest.1997;100:1693---707.
6.KaretFE, Gainza FJ, Györy AZ, Unwin RJ,Wrong O, Tanner MJ, et al. Mutations in the chloride-bicarbonate exchanger geneAE1causeautosomaldominantbutnotautosomal reces-sivedistal renal tubular acidosis. Proc Natl AcadSci U SA. 1998;95:6337---42.
7.TanphaichitrVS,SumboonnanondaA,IdeguchiH,ShayakulC, BrugnaraC,TakaoM,etal.NovelAE1mutationsinrecessive distalrenaltubularacidosis.Loss-of-functionisrescuedby gly-cophorinA.JClinInvest.1998;102:2173---9.
8.Vargas-PoussouR,HouillierP,LePottierN,StrompfL,LoiratC, BaudouinV,etal.Geneticinvestigationofautosomalrecessive distalrenaltubularacidosis:evidencefor earlysensorineural hearinglossassociatedwithmutationsintheATP6V0A4gene.J AmSocNephrol.2006;17:1437---43.
9.KaretFE,FinbergKE,NelsonRD,NayirA,MocanH,SanjadSA, etal.MutationsinthegeneencodingB1subunitofH+-ATPase causerenaltubularacidosiswithsensorineuraldeafness.Nat Genet.1999;21:84---90.
10.SmithAN,SkaugJ,ChoateKA,NayirA,BakkalogluA,OzenS, etal.MutationsinATP6N1B,encodinganewkidneyvacuolar protonpump116-kDsubunit,causerecessivedistalrenal tubu-laracidosiswithpreservedhearing.NatGenet.2000;26:71---5.
11.SmithA,BoycottKM,JarinovaO.LakeLouisemutation detec-tion meeting 2013: clinical translation of next-generation sequencingrequiresoptimizationofworkflowsand interpreta-tionofvariants.HumMutat.2014;35:265---9.
12.RabbaniB,TekinM,MahdiehN.Thepromiseofwhole-exome sequencinginmedicalgenetics.JHumGenet.2014;59:5---15.
13.RobinsonJT,ThorvaldsdóttirH,WincklerW,GuttmanM,Lander ES,GetzG,etal.Integrativegenomicsviewer.NatBiotechnol. 2011;29:24---6.
14.ChoiM,SchollUI,JiW,LiuT,TikhonovaIR,ZumboP,etal. Gene-ticdiagnosisbywholeexome capture andmassively parallel DNAsequencing.ProcNatlAcadSciUSA.2009;106:19096---101.
15.BonnefondA,DurandE,SandO,DeGraeveF,GallinaS,Busiah K,etal.Moleculardiagnosisofneonataldiabetesmellitususing
next-generation sequencing ofthe whole exome.PLoS ONE. 2010;5:e13630.
16.YangY,MuznyDM,ReidJG,BainbridgeMN,WillisA,WardPA, etal.Clinicalwhole-exomesequencingforthediagnosisof Men-deliandisorders.NEnglJMed.2013;369:1502---11.
17.LangF,VallonV,KnipperM,WangemannP.Functional signifi-canceofchannelsandtransportersexpressedintheinnerear andkidney.AmJPhysiolCellPhysiol.2007;293:C1187---208.
18.StoverEH,BorthwickKJ,BavaliaC,EadyN,FritzDM,Rungroj N,etal.NovelATP6V1B1andATP6V0A4mutationsinautosomal recessivedistal renal tubularacidosiswithnew evidencefor hearingloss.JMedGenet.2002;39:796---803.
19.BatlleD,HaqueSK.Geneticcausesandmechanismsofdistal renaltubularacidosis.NephrolDialTranspl.2012;27:3691---704.
20.GilH,SantosF,GarcíaE,AlvarezMV,Ordó˜nezFA,MálagaS,etal. DistalRTAwithnervedeafness:clinicalspectrumand mutatio-nalanalysisinfivechildren.PediatrNephrol.2007;22:825---8.
21.MiuraK,SekineT,TakahashiK,TakitaJ,HaritaY,OhkiK,etal. Mutationalanalysesofthe ATP6V1B1and ATP6V0A4genes in patientswithprimarydistalrenaltubularacidosis.NephrolDial Transpl.2013;28:2123---30.
22.ElhayekD,PerezdeNanclaresG,ChouchaneS,HamamiS,Mlika A,TroudiM,etal.Moleculardiagnosisofdistalrenaltubular acidosisinTunisianpatients:proposedalgorithmforNorthern Africa populations for the ATP6V1B1, ATP6V0A4 and SCL4A1 genes.BMCMedGenet.2013;14:119.
23.AlperSL,DarmanRB,ChernovaMN,DahlNK.TheAEgenefamily ofCl/HCO3-exchangers.JNephrol.2002;15:S41---53.
24.SchusterVL.Functionandregulationofcollectingduct interca-latedcells.AnnuRevPhysiol.1993;55:267---88.
25.Chang YH, Shaw CF, Jian SH, Hsieh KH, Chiou YH, Lu PJ. Compoundmutationsinhumananionexchanger1are associ-atedwithcompletedistalrenaltubularacidosisandhereditary spherocytosis.KidneyInt.2009;76:774---83.
26.AlperSL.MolecularphysiologyandgeneticsofNa+-independent SLC4anionexchangers.JExpBiol.2009;212:1672---83.
27.Cheidde L,Vieira TC,LimaPR,SaadST, HeilbergIP.Anovel mutation in the anion exchanger 1 gene is associated with familialdistalrenaltubularacidosisandnephrocalcinosis. Pedi-atrics.2003;112:1361---7.
28.Wrong O, Bruce LJ, Unwin RJ, Toye AM, Tanner MJ.Band 3 mutations,distal renal tubularacidosis, andSoutheast Asian ovalocytosis.KidneyInt.2002;62:10---9.