U
niversidade Federal de Minas Gerais
–
UFMG
Instituto de Ciências Agrárias - ICA
Mestrado em Produção Vegetal
DERIVA DE GLYPHOSATE E CARFENTRAZONE-ETHYL
SOBRE A SEVERIDADE DA FERRUGEM (Puccinia psidii) EM
CLONES DE Eucalyptus grandis
SAMUEL ALVES DOS SANTOS
SAMUEL ALVES DOS SANTOS
DERIVA DE GLYPHOSATE E CARFENTRAZONE-ETHYL
SOBRE A SEVERIDADE DA FERRUGEM (Puccinia psidii) EM
CLONES DE Eucalyptus grandis
Montes Claros – MG 2016
Dissertação apresentada ao Curso de Mestrado em Produção Vegetal, área de concentração em Produção Vegetal, do Instituto de Ciências Agrárias da Universidade Federal de Minas Gerais, como requisito parcial para a obtenção do grau de Mestre em Produção Vegetal.
Área de concentração: Produção Vegetal
Elaborada pela Biblioteca Comunitária em Ciências Agrárias do ICA/UFMG S237d
2016
Santos, Samuel Alves.
Deriva de glyphosate e carfentrazone-ethyl sobre a severidade da ferrugem (Puccinia psidii) em clones de Eucalyptus grandis / Samuel Alves dos Santos. Montes Claros, MG: Instituto de Ciências Agrárias/UFMG, 2016.
71 f.: il.
Dissertação (Mestrado em Produção Vegetal) Universidade Federal de Minas Gerais, 2016.
Orientador: Prof. Dr. Leonardo David Tuffi Santos.
Banca examinadora: Acelino Couto Alfenas, Fernando da Silva Rocha, Francisco André Ossamu Tanaka, Leonardo David Tuffi Santos.
Referências: f: 64-71.
1. Eucalipto. 2. Fisiologia. 3. Anatomia foliar. 4. Ultraestrutura foliar. 5. Patologia florestal. I. Santos, Leonardo David Tuffi. II. Instituto de Ciências Agrárias da Universidade Federal de Minas Gerais. III. Título.
SAMUEL ALVES DOS SANTOS
DERIVA DE GLYPHOSATE E CARFENTRAZONE-ETHYL SOBRE A
SEVERIDADE DA FERRUGEM (Puccinia psidii) EM CLONES DE Eucalyptus
grandis
Prof. Dr. Leonardo David Tuffi Santos
(Orientador - UFMG/ICA)
Aprovada em 22 de fevereiro de 2016.
Montes Claros - MG
DEDICO
Aos meus pais,
“por me ensinarem que o respeito, a honestidade e humildade são as maiores
virtudes de um homem. E que as maiores
riquezas quase sempre estão na simplicidade
AGRADECIMENTOS
A Deus, por sempre ouvir minhas orações e atender meus pedidos.
À minha família e minha namorada Najara que, com muito apoio e carinho,
não mediram esforços para a conclusão desta etapa.
Ao meu orientador, o Prof. Leonardo David Tuffi Santos, pelo compromisso,
confiança e dedicação.
Aos meus coorientadores Prof. Acelino Couto Alfenas (UFV), Prof. Francisco
André Ossamu Tanaka (ESALQ/USP) e Prof. Bruno Francisco Sant’Anna dos Santos (UFPR) pela parceria e pela valorosa contribuição.
Ao Instituto de Ciências Agrárias da Universidade Federal de Minas Gerais,
em especial ao Programa de Pós-Graduação Mestrado em Produção
Vegetal, berço da minha formação.
À Clonar Resistência a Doenças Florestais LTDA, pela disponibilização das
mudas clonais.
Ao Departamento de Fitopatologia da UFV por ceder infraestrutura
necessária à realização dos experimentos.
À toda equipe do Laboratório de Patologia Florestal Molecular da UFV, em
especial à Michele pelo auxílio na condução dos experimentos.
A Autieres Faria pela contribuição durante as aplicações dos herbicidas.
A Gilmar do Núcleo de Microscopia e Microanálise da UFV, pelo fornecimento
da solução de Karnovsky.
Ao Prof. Júlio César pelo empréstimo do Analisador portátil de fotossíntese
LI-COR 6400XT e ao Eduardo Medina pelo auxílio durante as avaliações
Ao Núcleo de Apoio a Pesquisa em Microscopia Eletrônica Aplicada na
Pesquisa Agropecuária (NAP/MEPA) da Escola Superior de Agricultura “Luiz de Queiróz” (ESALQ/USP), pelo suporte durante o processamento e análise
das amostras em anatomia e ultraestrutura.
Aos membros do GPPLAN (Grupo de Pesquisa em Plantas Daninhas), pelo
apoio e contribuição.
Aos meus amigos da república Monastério: Mathias, Demerson, Gabriel e
Ronie, pelo convívio e amizade.
À coordenação de aperfeiçoamento de Pessoal de Nível Superior (CAPES),
pela bolsa de mestrado e auxílio financeiro.
À Fundação de Amparo à Pesquisa do Estado de Minas Gerais (FAPEMIG),
pelo aporte financeiro.
Ao Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPq),
RESUMO
A ação de herbicidas pode alterar a severidade da ferrugem (Puccinia psidii)
do eucalipto. Este trabalho teve como objetivos: (i) avaliar a tolerância dos
clones de eucalipto aos herbicidas carfentrazone-ethyl e glyphosate; (ii)
avaliar a severidade da ferrugem; (iii) avaliar os efeitos dos herbicidas na
anatomia e ultraestrutura foliar e na fisiologia dos clones; e (iv) avaliar a
histopatologia da interação patógeno-hospedeiro. Para instalação dos
experimentos, foram utilizados dois clones de Eucalyptus grandis, sendo um
resistente (G-21), e outro suscetível (G-33) a P. psidii. As subdoses
herbicidas testadas foram testemunha, 86.4 g e.a. ha-1 de glyphosate, 3.0 g
e.a. ha-1 de carfentrazone-ethyl e a mistura de 86.4 g e.a. ha-1 de glyphosate
+ 3.0 g e.a. ha-1 de carfentrazone-ethyl. Dois dias após a aplicação (DAA) dos
herbicidas, foi realizada a inoculação do patógeno. Para análises anatômicas
e ultraestruturais, foram coletadas amostras foliares nos tempos zero, 6, 12 e
21 dias após a inoculação (DAI). A taxa fotossintética, a condutância
estomática e o rendimento efetivo do fotossistema II foram avaliados aos 4 e
23 DAA. A tolerância dos clones aos herbicidas e a severidade da ferrugem
foram avaliadas ao final dos experimentos com 23 DAA e 21 DAI,
respectivamente. Plantas dos dois clones apresentaram alterações na
anatomia foliar como erosão de ceras epicuticulares, degeneração de células
epidérmicas e parenquimáticas, sobretudo quando expostas à aplicação de
carfentrazone-ethyl e mistura. Plantas expostas à aplicação herbicida
apresentaram acúmulo de grãos de amido nos cloroplastos. O clone G-33 foi
o mais afetado e apresentou maior fitointoxicação, menor crescimento, menor
produção de massa seca e maior redução dos parâmetros fisiológicos
quando tratado com a mistura herbicida, seguida das subdoses isoladas de
carfentrazone-ethyl e glyphosate, respectivamente. O crescimento, o
desenvolvimento e os parâmetros fisiológicos do clone G-21 não foram
afetados pela subdose isolada de carfentrazone-ethyl. A manifestação da
doença ocorreu apenas no clone suscetível a P. psidii. Plantas do clone
G-33, expostas aos herbicidas, apresentaram menor severidade da ferrugem.
apresentaram abaixo do ponto de infecção camadas de células
parenquimáticas em intensa divisão celular, além de uma “pré-pústula” com desenvolvimento reduzido em relação às plantas testemunha. Aos 12 DAI, as
pústulas estavam totalmente formadas e com grande produção de
urediniósporos nas plantas testemunha. Entretanto, as plantas expostas à
aplicação apresentaram, abaixo do ponto infecção, tecido de
compartimentalização estratificado entre duas a quatro camadas, limitando a
área colonizada pelo fungo, além de pústulas sem produção de esporos ou
com produção reduzida. A fitointoxicação e a redução na taxa fotossintética,
decorrentes da ação dos herbicidas, estão correlacionadas com a redução da
severidade da doença no clone G-33. Conclui-se que o clone G-33 é mais
sensível aos herbicidas testados. E que a deriva dos herbicidas glyphosate e
carfentrazone-ethyl, aplicados de forma isolada ou em mistura, não altera o
nível de resistência do clone resistente a P. psidii (G-21), no entanto, reduz a
severidade da ferrugem do eucalipto nas plantas do clone suscetível (G-33),
sobretudo quando usados em mistura.
Palavras-chave: Eucalipto. Fisiologia. Anatomia foliar. Ultraestrutura foliar.
ABSTRACT
The action of herbicides could affect the severity level of rust (Puccinia psidii)
of eucalyptus. The present study aimed to: (i) assess the tolerance of the
eucalyptus clones to carfentrazone-ethyl and glyphosate; (ii) assess the
severity of rust; (iii) evaluate the effects of the herbicides in anatomy and leaf
ultrastructure and physiology of clones; and (iv) evaluate the histopathology of
host-pathogen interaction. For installation the experiments were used two
Eucalyptus grandis clones, one resistant (G-21), and other susceptible (G-33)
to fungus P. psidii. The herbicides doses tested were zero, 86.4 g a.e. ha-1 of
glyphosate, 3.0 g a.e. ha-1 of carfentrazone-ethyl and mixture (86.4 g a.e. ha-1
of glyphosate + 3.0 g a.e. ha-1 of carfentrazone-ethyl). Two days after
application (DAA) of herbicides, was performed the inoculation of the
pathogen. For anatomical and ultrastructural analysis, leaf samples were
collected at: zero; 6; 24: 21 days after inoculation (DAI). The photosynthetic
rate, stomatal conductance and the effective yield of photosystem II were
evaluated at 4 and 23 DAA. The tolerance of the eucalyptus clones to
herbicides and rust severity were assessed at the end of the experiments (23
DAA and DAI 21, respectively). Plants of the two clones showed changes in
leaf anatomy, as erosion of epicuticular waxes, degeneration of epidermal
cells and parenchyma, especially when exposed to application of
carfentrazone-ethyl and mixture. In addition, plants exposed to herbicide
application showed an accumulation of starch granules in the chloroplasts.
The G-33 clone was the most affected, with higher phytotoxicity, lower growth,
lower dry matter production and greater reduction of physiological
parameters, when treated with the herbicide mixture, followed by single doses
of carfentrazone-ethyl and glyphosate, respectively. The growth, development
and physiological parameters of the G-21 clone were not affected by the
single dose of carfentrazone-ethyl. The disease occurred only in clone
susceptible to P. psidii. The plants of G-33 clone, exposed to herbicides had
lower disease severity. At 6 DAI, plants of this clone, that were exposed to
herbicide application, showed below the point of infection, layers of
reduced development when it compared to the control plants. At 12 DAI, the
pustules were fully formed and with great production of urediniospores in
control plants. However, plants exposed to the herbicides application
presented, below the point of infection, compartmentalization fabric with two
until four layers, limiting the area colonized by the fungus, and pustules with
no or reduced production of spores. The phytointoxication and the reduction in
photosynthetic rate, due to herbicide action, are correlated with the decrease
on severity of rust in the G-33 clone. In summary, it is concluded that G-33
clone is more sensitive to herbicides. And that the drift of the herbicides
(glyphosate and carfentrazone-ethyl), applied alone or in mixture, does not
alter the level of resistant of the G-21 clone. However, reducing the rust
severity of de Eucalyptus in the plants of the susceptible clone (G-33),
especially when used in mixture.
Keywords: Eucalyptus. Physiology, Leaf anatomy, Leaf ultrastructure, Forest
LISTA DE ABREVIATURAS E SIGLAS
DAT - Dias após transplantio
NPK - Nitrogênio; fósforo; potássio
MSPA - Massa seca da parte aérea
DAA - Dias após aplicação
DAI - Dias após inoculação
IMc - Índice de McKinney
Iafi - Índice de área foliar infectada
NMUP - Número médio de urediniósporos produzidos
MIP - Manejo Integrado de Pragas
MEV - Microscopia eletrônica de varredura
MET - Microscopia eletrônica de transmissão
Ep - Epiderme
PP - Parênquima paliçádico
Es - Estômato Ct - Cutícula
Ti - Tilacóide
Cl - Cloroplasto
Pr - Peroxissomo
GA - Grão de amido
TF - Taxa fotossintética líquida
CE - Condutância estomática
Hi - Hifas fúngicas Ur - Urediniósporos
µm - Micrômetros
LISTA DE FIGURAS
Figura 1 - Ação herbicida indireta sobre os mecanismos de
defesa estruturais de plantas aos patógenos (B-E) e
direta sobre a germinação de esporos ou crescimento
de hifas (F-G). A. Hospedeiro sem mecanismos de
defesa; Esporos (Es) germinam e hifas (Hi) penetram
de forma direta através de apressórios (Ap) ou por
aberturas naturais. B. Na presença de tricomas (Tr) os
esporos germinam, mas não atingem a epiderme. C.
Cutícula espessa (Ct) e ceras epicuticulares (CE)
formam barreiras à penetração. D. Efeito dos
herbicidas sobre os tricomas favorece a penetração.
E. Degeneração das ceras epicuticulares e cutícula, facilitando a penetração. F e G. Moléculas herbicidas
(MH) inibem a germinação de esporos... 30
Figura 2 - Efeito da deriva dos herbicidas em folhas da parte
basal da copa, exposta à aplicação, de clones de
Eucalyptus grandis 24 horas após aplicação. A, B, E e
F. Folhas sem presença de sintomas de intoxicação. C,
D, G e H. Folhas com sintomas de intoxicação. Setas
indicam pontos necróticos causados pelo
carfentrazone-ethyl. Mistura = 86,4 g e.a. ha-1 de
glyphosate + 3 g e.a. ha-1 de carfentrazone-ethyl.
Barras = 1cm... 38
Figura 3 - Efeito da deriva dos herbicidas em folhas da parte
apical da copa, protegida da aplicação, de clones de
Eucalyptus grandis 10 dias após aplicação. A, E e G.
Folhas sem presença de sintomas de intoxicação. B,
C, D, F, G e H. Folhas com sintomas de intoxicação
com clorose na borda e ápice foliar. Mistura = 86,4 g
carfentrazone-ethyl. Barras = 1cm... 39
Figura 4 - Efeito da deriva dos herbicidas em folhas da parte
apical da copa, protegida da aplicação, de clones de
Eucalyptus grandis 23 dias após aplicação. A, E e G.
Folhas sem presença de sintomas de intoxicação. B,
C, D, G e H. Folhas com sintomas de intoxicação com
clorose distribuída por todo limbo foliar. Mistura = 86,4
g e.a. ha-1 de glyphosate + 3 g e.a. ha-1 de
carfentrazone-ethyl. Barras = 1cm... 40
Figura 5 - Microscopia eletrônica de varredura. Efeito da deriva
dos herbicidas na face abaxial de folhas da parte basal
da copa, exposta à aplicação, em clones de
Eucalyptus grandis 2 dias após aplicação. A-B. Células
do complexo estomático com turgor e ceras
epicuticulares com conformação característica a
espécie. C-H. Ceras epicuticulares erodidas (asteríscos). E e G. Degeneração de parede, seta
indica ruptura da cutícula (Ct) nas células guardas do
complexo estomático. Mistura = 86,4 g e.a. ha-1 de
glyphosate + 3 g e.a. ha-1 de carfentrazone-ethyl.
Barras = 25 µm... 42
Figura 6 - Microscopia eletrônica de varredura. Efeito da deriva
dos herbicidas na face adaxial de folhas da parte basal
da copa, exposta à aplicação, em clones de
Eucalyptus grandis 2 dias após aplicação. A-B.
Células epidérmicas com turgor e ceras epicuticulares
com conformação característica à espécie. C-H. Ceras
epicuticulares erodidas (asteríscos). Mistura = 86,4 g
e.a. ha-1 de glyphosate + 3 g e.a. ha-1 de
carfentrazone-ethyl. Barras = 25 µm... 43
Figura 7 - Microscopia de luz. Efeito da deriva dos herbicidas em
clones de Eucalyptus grandis 2 dias após aplicação.
A-D. Células com conformação e turgor característico
à espécie. E-H. Células epidérmicas degradadas
(asteriscos); células parenquimáticas com perda de
turgor (setas). Abreviações: Ep – epiderme; PP – parênquima paliçádico; PL – parênquima lacunoso; Es
– estômato. Mistura = 86,4 g e.a. ha-1 de glyphosate + 3 g e.a. ha-1 de carfentrazone-ethyl. Barras = 25
µm... 44
Figura 8 - Microscopia eletrônica de transmissão. Efeito da
deriva dos herbicidas em folhas da parte apical da
copa, protegida da aplicação, de clones de Eucalyptus
grandis 14 dias após aplicação. A. Cloroplasto de uma
folha sadia (planta testemunha) com os tilacóides (Ti)
perfeitamente organizados em granum. B. Cloroplasto
(Cl) de uma folha clorótica (planta exposta à deriva
dos herbicidas) com tilacóides totalmente
desorganizados. C. Célula de folha oriunda de uma
planta testemunha. Nas amostras analisadas não
foram observadas presença de peroxissomos. D.
Célula de planta exposta à deriva de
carfentrazone-ethyl com presença de peroxissomos (Pr); detalhe
evidenciando tal organela. Barras = 1 µm... 46
Figura 9 - Microscopia eletrônica de transmissão. Acúmulo de
grãos de amido nos cloroplastos de folhas da parte
apical da copa, protegida da aplicação, de Eucalyptus
grandis 14 dias após aplicação. A-B. Cloroplastos sem
grão de amido. C-H. Cloroplastos com presença de
grãos de amido (setas). Abreviações: Cl – cloroplasto; GA – grão de amido. Mistura = 86,4 g e.a. ha-1 de glyphosate + 3 g e.a. ha-1 de carfentrazone-ethyl.
Figura 10 - Rendimento efetivo do FS II (A), Taxa fotossintética
líquida (B) e Condutância estomática (C) 4 dias após
aplicação dos herbicidas. Letras minúsculas
comparam as médias dentro de um mesmo clone,
enquanto que as maiúsculas dentro do mesmo
tratamento herbicida. Médias seguidas das mesmas
letras não diferem entre si pelo teste de Tukey a 5%
de probabilidade de erro. Barras = erro padrão da
média. Mistura = 86,4 g e.a. ha-1 deglyphosate + 3 g
e.a. ha-1 de carfentrazone-ethyl... 48
Figura 11 - Rendimento efetivo do FS II (A), taxa fotossintética
líquida (B) e condutância estomática (C) 23 dias após
aplicação dos herbicidas. Letras minúsculas
comparam as médias dentro de um mesmo clone,
enquanto que as maiúsculas dentro do mesmo
tratamento herbicida. Médias seguidas das mesmas
letras não diferem entre si pelo teste de Tukey a 5%
de probabilidade de erro. Barras = erro padrão da
média. Mistura = 86,4 g e.a. ha-1 deglyphosate + 3 g
e.a. ha-1 de carfentrazone-ethyl... 49
Figura 12 - Fitointoxicação (A), altura total (B) e massa seca da
parte aérea (C) 23 dias após aplicação dos herbicidas.
Letras minúsculas comparam as médias dentro de um
mesmo clone, enquanto que as maiúsculas dentro do
mesmo tratamento herbicida. Médias seguidas das
mesmas letras não diferem entre si pelo teste de
Tukey a 5% de probabilidade. Barras = erro padrão da
média. Mistura = 86,4 g e.a. ha-1 deglyphosate + 3 g
e.a. ha-1 de carfentrazone-ethyl... 53
Figura 13 - Espectro de infecção de Puccinia psidii na face abaxial
das folhas de clones de Eucalyptus grandis 21 dias
grande produção de esporos. B-D. Folhas de plantas
expostas aos herbicidas: detalhe evidencia pústulas
com pontos secos, aparentemente com produção
reduzida de urediniósporos. E-H. Folhas do clone
resistente sem presença de infecção. Mistura = 86,4 g
e.a. ha-1 deglyphosate + 3 g e.a. ha-1 de
carfentrazone-ethyl... 55
Figura 14 - Severidade da ferrugem no Clone G-33, suscetível a Puccinia psidii. A. Índice de McKinney. B. Índice médio
de área foliar infectada. C. Número médio de
urediniósporos. Médias justapostas seguidas das
mesmas letras não diferem entre si pelo teste de
Tukey a 5% de probabilidade. Barras = erro padrão da
média. Mistura = 86,4 g e.a. ha-1 deglyphosate + 3 g
e.a. ha-1 de carfentrazone-ethyl.... 56
Figura 15 - Microscopias de luz e eletrônica de varredura. Efeito
da deriva dos herbicidas na formação das pústulas 6
dias após a inoculação de Puccinia psidii em plantas
do clone G-33. A-B. Pré-pústulas grandes. C, E e G.
*Ocorrência de divisão celular na região abaixo da
infecção (asteríscos). D e F. Pré-pústula com
desenvolvimento reduzido. H. Pré-pústula má-formada
(sem produção de esporos). Abreviações: Ep -
epiderme; PP - parênquima paliçádico; Hi - hifas.
Mistura = 86,4 g e.a. ha-1 de glyphosate + 3 g e.a. ha-1
de carfentrazone-ethyl. Barras = 50 µm... 58
Figura 16 - Microscopias de luz e eletrônica de varredura. Efeito
da deriva dos herbicidas nas pústulas 12 dias após a
inoculação de Puccinia psidii em plantas do clone
G-33. A-B. Pústulas com alta produção de
urediniósporos (Ur). C e E. Tecido de
células. D e F. Pústulas com produção reduzida de
esporos. G. Tecido de compartimentalização com três
camadas. H. Pústula seca (sem produção de
urediniósporos). Abreviações: Ep - epiderme; PP -
parênquima paliçádico; Hi - hifas. Mistura = 86,4 g e.a.
ha-1 de glyphosate + 3 g e.a. ha-1 de
LISTA DE TABELAS
Tabela 1 - Análise de correlação entre as variáveis estudadas
para determinar a tolerância dos clones aos
herbicidas... 52
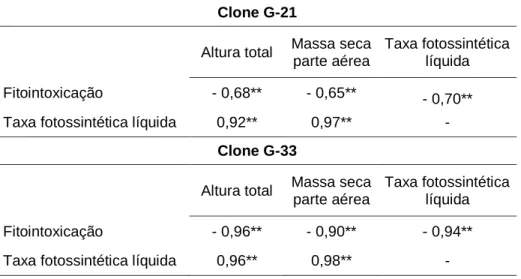
Tabela 2 - Análise de correlação entre as variáveis estudadas
para determinar a tolerância aos herbicidas e as
variáveis características da severidade da ferrugem
SUMÁRIO
1. INTRODUÇÃO...20
2. REFERENCIAL TEÓRICO...22
2.1. Importância dos herbicidas glyphosate e carfentrazone-ethyl em florestas de eucalipto...22
2.2. Efeitos da deriva de herbicidas em culturas...23
2.3. Ferrugem do eucalipto: importância e ciclo de relações patógeno-hospedeiro...24
2.4. Mecanismos de defesa das plantas aos patógenos...26
2.5. Herbicidas X doenças de plantas...27
3. MATERIAL E MÉTODOS...31
3.1. Obtenção das mudas...31
3.2. Instalação dos experimentos...31
3.3. Aplicação dos herbicidas...32
3.4. Inoculação do patógeno...32
3.5. Avaliação da tolerância dos clones aos herbicidas...33
3.6. Avaliação da severidade da ferrugem...33
3.7. Análises fisiológicas...34
3.8. Anatomia e ultraestrutura foliar...35
3.9. Análise estatística...36
4. RESULTADOS E DISCUSSÃO...37
4.1. Tolerância dos clones aos herbicidas...37
4.1.1. Efeitos dos herbicidas na morfologia, anatomia e ultraestrutura foliar e na fisiologia das plantas...37
4.1.2. Fitointoxicação, altura total e massa seca da parte aérea...51
4.2. Severidade da ferrugem e histopatologia da interação Puccinia psidii X Eucalyptus grandis...54
5. CONCLUSÃO...63
20
1. INTRODUÇÃO
O uso de herbicidas para controle de plantas daninhas em plantios de
eucalipto tem levantado questionamentos sobre impactos negativos ao
ambiente e à cultura. Dentre eles, está a alteração no nível de severidade da
ferrugem do eucalipto causada pelo fungo Puccinia psidii (TUFFI-SANTOS et
al., 2007; TUFFI-SANTOS et al., 2011).
Dentre os cinco herbicidas registrados para uso em eucalipto no Brasil
(AGROFIT, 2016), o glyphosate é o mais utilizado, principalmente pelo seu
amplo espectro de ação e baixo custo. Em razão principalmente da pressão
de seleção, em áreas com aplicação constantes de glyphosate existem
diversos relatos de plantas daninhas resistentes à molécula (NEVE et al.,
2003; VARGAS et al., 2007; DUKE; POWLES, 2008; POWLES, 2008;
BECKIE, 2011; NORSWORTHY et al., 2011; GREEN, 2012; SHANER et al.,
2012). Por apresentar eficiência desejável sobre plantas daninhas resistentes
ao glyphosate, como Commelina ssp. (WERLANG; SILVA, 2002), o herbicida
carfentrazone-ethyl tem sido bastante utilizado como alternativa ou em
mistura ao glyphosate. Outro fato importante é que dentre os herbicidas
registrados para a cultura, apenas o glyphosate e o carfentrazone-ethyl são
aceitos pelas certificadoras para ser utilizado em florestas de eucalipto (FSC,
2015).
Glyphosate e carfentrazone-ethyl são herbicidas não seletivos ao
eucalipto, por isso as aplicações devem ser realizadas de forma dirigida
sobre as plantas daninhas, evitando o contato indesejado com a cultura
(RODRIGUES; ALMEIDA, 2011). Mesmo tomando esse cuidado, durante as
aplicações parte do produto pode sofrer arraste pelo vento e atingir as
plantas de eucalipto por deriva (TUFFI-SANTOS et al., 2006). Quando isso
ocorre, as plantas de eucalipto podem apresentar murcha, clorose e necrose
nas folhas (TUFFI-SANTOS et al., 2006), o que pode afetar o crescimento e
21
O Manejo Integrado de Pragas (MIP) consiste na gestão de técnicas de
manejo de plantas daninhas, insetos, patógenos, nematoides, artrópodes e
vertebrados bem como de suas interações (SANYAL; SHRESTHA, 2008).
Nessa concepção, o estudo da influência da deriva de herbicidas sobre a
severidade de doenças é de extrema importância, pois, a época em que são
intensificadas as aplicações herbicidas para manejo de plantas daninhas
coincide com a fase em que o eucalipto apresenta condições favoráveis à
ocorrência da ferrugem em campo. A ferrugem do eucalipto afeta
preferencialmente tecidos jovens e brotações (ALFENAS et al., 2009).
Apesar de ser doença comum em viveiros, jardins e minijardins clonais, a
ferrugem pode ser problema em plantas no campo de até dois anos de idade
(ZAUZA et al., 2008), já que, logo após o plantio, as plantas encontram-se em
grande crescimento vegetativo com grande quantidade de tecidos tenros.
Embora existam trabalhos que constataram que a deriva do herbicida
glyphosate reduz a severidade da ferrugem em mudas de eucalipto
(TUFFI-SANTOS et al., 2007; TUFFI-(TUFFI-SANTOS et al., 2011), ainda não é bem
esclarecido como os efeitos da deriva de herbicidas sobre plantas de
eucalipto contribuem para a redução da severidade da ferrugem. Nesse
contexto, objetivou-se com o presente trabalho: (i) avaliar a tolerância de dois
clones de Eucalyptus grandis aos herbicidas carfentrazone-ethyl e
glyphosate; (ii) avaliar a severidade da ferrugem em plantas previamente
expostas à deriva desses herbicidas; (iii) avaliar as alterações causadas pela
deriva na anatomia e ultraestrutura foliar e na fisiologia das mudas de
eucalipto; e (iv) analisar em microscopia de luz e eletrônica de varredura e de
22
2. REFERENCIAL TEÓRICO
2.1. Importância dos herbicidas glyphosate e carfentrazone-ethyl em florestas de eucalipto
O manejo de plantas daninhas representa uma das práticas mais
importantes no cultivo do eucalipto. Sem controle, a interferência das plantas
daninhas pode acarretar perdas de até 40% na produtividade da floresta
(TAROUCO et al., 2009). No caso das empresas florestais, que geralmente
cultivam extensas áreas, a escassez de mão de obra, associada à
necessidade de atingir elevados índices de produtividade com menor custo
de produção, tem levado ao aumento no uso de herbicidas para controle de
plantas daninhas.
O glyphosate é o principal herbicida utilizado na eucaliptocultura, pelo
seu baixo custo e amplo espectro de ação. O ambiente aliado ao uso
frequente do mesmo herbicida pode favorecer a seleção de indivíduos
tolerantes e/ou resistentes a um ou mais mecanismos de ação herbicida
(HANSON et al., 2013). Em áreas com uso constante de glyphosate, existem
diversos relatos de plantas resistentes à molécula desse herbicida (NEVE et
al., 2003; VARGAS et al., 2007; DUKE; POWLES, 2008; POWLES, 2008;
BECKIE, 2011; NORSWORTHY et al., 2011; GREEN, 2012; SHANER et al.,
2012). Assim, a mistura de herbicidas com mecanismos de ação distintos,
mas com efeito sinérgico, aumenta o espectro de ação e melhora
consideravelmente a eficiência de controle (KUMAR; JHA, 2015;
McCULLOUGH et al., 2015; WALSH et al., 2015; WALSH et al., 2014).
O herbicida carfentrazone-ethyl possui boa eficiência sobre plantas
daninhas tolerantes ao glyphosate como trapoerabas (Commelina sp.)
(WERLANG; SILVA, 2002). Dentre os produtos registrados para uso em
eucalipto (AGROFIT, 2016), além do glyphosate, apenas o herbicida
carfentrazone-ethyl é permitido pelas certificadoras para ser utilizado (FSC,
2015). A certificação florestal é de grande importância, pois, produtos
23
forma, esse herbicida tem sido testado e bastante utilizado em plantios
comerciais de eucalipto, tanto em aplicações isoladas ou em mistura ao
herbicida glyphosate, já que os dois herbicidas apresentam efeito sinérgico
(WERLANG; SILVA, 2002).
Glyphosate e carfentrazone-ethyl são herbicidas não seletivos ao
eucalipto, por isso as aplicações devem ser realizadas de forma dirigida
sobre as plantas daninhas, evitando o contato indesejado com a cultura
(RODRIGUES; ALMEIDA, 2011). Mesmo tomando esse cuidado, parte do
produto pode sofrer arraste pelo vento durante as aplicações, fenômeno
conhecido por deriva, ou mesmo de forma direta atingir as plantas de
eucalipto (TUFFI-SANTOS et al., 2006).
2.2. Efeitos da deriva de herbicidas em culturas
Herbicidas não seletivos apresentam efeito tóxico quando em contato
com as culturas. Portanto, ao utilizar esses herbicidas, as aplicações devem
ser realizadas de forma dirigida sobre as plantas daninhas, evitando o
contato indesejado com plantas da cultura. Ainda que seja tomada essa
precaução, parte do produto pode sofrer arraste pelo vento e atingir as
culturas por deriva (SILVA; SILVA, 2012).
Os efeitos negativos da deriva de herbicidas em culturas são
comprovados por diversos estudos (YAMASHITA; GUIMARÃES, 2005;
TUFFI-SANTOS et al., 2009; MACHADO et al., 2010; COSTA et al., 2012).
No Eucalipto, por exemplo, a intoxicação é caracterizada pela presença de
folhas cloróticas, podendo, em alguns casos, evoluir para necrose, redução
no crescimento e morte da planta (TUFFI-SANTOS et al., 2006).
Herbicidas, em geral, afetam a fisiologia e o metabolismo das plantas.
Plantas expostas a aplicações de glyphosate apresentam redução na
produção de açúcares, aminoácidos e proteínas (MACHADO et al., 2010;
LANGARO et al., 2014; VARGAS et al., 2014), e na taxa respiratória
24
afeta o crescimento e desenvolvimento das plantas, o que limita o incremento
de matéria seca na parte aérea (GUSMÃO et al., 2011; FRANÇA et al., 2010;
TIBURCIO et al., 2012).
O efeito de adjuvantes presentes na formulação comercial dos
herbicidas pode provocar degeneração de tricomas, da cutícula e erosão das
ceras epicuticulares (TUFFI-SANTOS et al., 2009; SANTOS et al., 2015),
afetando as barreiras naturais das plantas à penetração de patógenos.
Adicionalmente, herbicidas podem alterar a síntese de produtos oriundos do
metabolismo secundário como as fitoalexinas, que são compostos com
propriedades antimicrobianas (RIZZARDI et al., 2003), bem como aumentar a
atividade de enzimas ligadas aos mecanismos de defesa das plantas
(PEREIRA et al., 2009). O que pode interferir de forma positiva ou negativa
na severidade de doenças.
2.3. Ferrugem do eucalipto: importância e ciclo de relações
patógeno-hospedeiro
O fungo Puccinia psidii Winter, agente causal da ferrugem do eucalipto,
está amplamente distribuído pela América do Sul e Central (GLEN et al.,
2007) e encontra-se em ampla dispersão mundial, com relatos no Japão
(KAWANISHI et al., 2009), China (ZHUANG; WEI, 2011), Austrália
(CARNEGIE; LIDBETTER, 2012) e nos EUA, mais precisamente nos estados
da Flórida, Califórnia e Havaí (MELLANO, 2006; UCHIDA et al., 2006).
Recentemente, foi relatada sua ocorrência na Indonésia (McTAGGART et al.,
2016). No Brasil, o primeiro relato do fungo em eucalipto foi em 1944, em
mudas de Corymbia citriodora no Rio de Janeiro (JOFFILY, 1944). Além do
eucalipto, P. psidii afeta diversas espécies de plantas da família Myrtaceae
(CARNEGIE; LIDBETTER, 2012).
Em condições de ambiente favorável, P. psidii infecta
preferencialmente tecidos tenros como folhas, botões florais, frutos e ramos
(ALFENAS et al., 2009). Por isso, a doença é mais observada em cepas,
25
em plantas com até dois anos de idade (ZAUZA et al., 2008). Em genótipos
altamente suscetíveis pode causar ainda deformações, necroses, hipertrofia,
minicancros e morte das porções terminais de crescimento (ALFENAS et al.,
2009).
Embora existam fungicidas registrados para uso na cultura do
eucalipto, a estratégia mais eficiente e econômica para o manejo da doença
consiste no uso de genótipos resistentes. Manter a doença abaixo do nível de
dano econômico é importante, já que, sem adoção de medidas de controle,
as perdas de produtividade são consideráveis.
P. psidii é um fungo biotrófico, assim necessita de tecidos hospedeiro
vivos para infectar e colonizar. Sua sobrevivência é baseada em estruturas
denominadas urediniósporos, que quando depositados sobre a superfície
foliar do hospedeiro, em condições de umidade favorável, germinam e
penetram de forma direta através da formação de apressório (XAVIER et al.,
2015).
A formação da hifa primária é observada entre 12 e 18 horas após a
inoculação. A partir dessa hifa primária formam-se, dentro das células do
hospedeiro, os haustórios, que são estruturas ramificadas que servem para o
patógeno nutrir-se de substâncias oriundas do metabolismo celular do
hospedeiro (XAVIER et al., 2001).
Em hospedeiros suscetíveis, a partir de três dias após a inoculação
(DAI), ocorre ramificação das hifas fúngicas, a fim de colonizar os tecidos
hospedeiros. Aos 6 DAI, é possível observar hipertrofia dos tecidos
colonizados (XAVIER et al., 2001). A formação das pústulas, sintoma mais
característico da doença, ocorre a partir exposição da massa de
urediniósporos aos 9 DAI (XAVIER et al., 2001). Visualmente, essa massa de
esporos apresenta coloração ferrugínea/amarelada (ALFENAS et al., 2009).
A relação entre patógeno-hospedeiro é muito íntima e equivalente a
uma batalha em que os envolvidos desenvolveram uma série de mecanismos
26
2.4. Mecanismos de defesa das plantas aos patógenos
Após contato com a superfície das plantas, o patógeno infecta e
coloniza os tecidos hospedeiros, enquanto que esses também utilizam de
mecanismos para se defender da infecção (AMORIM; PASCHOLATI, 2011).
Os mecanismos de defesa das plantas aos agentes patogênicos são
classificados como estruturais e bioquímicos. Dentre os diversos mecanismos
de defesa, existem aqueles que já estavam presentes nas plantas antes do
contato com o patógeno e outros que são estimulados em resposta à
infecção. Quando já presentes nos tecidos hospedeiros, antes da infecção,
dizemos que fazem parte dos mecanismos pré-formados. Já quando são
produzidos em reposta à infecção, são chamados de pós-formados
(STANGARLIN et al., 2011).
A superfície foliar é o primeiro obstáculo encontrado pelos patógenos.
Folhas com grande quantidade de tricomas podem envolver esporos fúngicos
e impedir que, mesmo após germinação, não consigam atingir as demais
células epidérmicas e penetrar no hospedeiro. Plantas de feijoeiro com maior
densidade de tricomas apresentaram maior tolerância à antracnose (JERBA
et al., 2005). Após os tricomas, a presença de cutícula mais espessa
associada à deposição de ceras epicuticulares, sobretudo na região da
cavidade estomática, são barreiras importantíssimas à penetração
(REINA-PINTO; YEPHREMOV, 2009). Os estômatos são a principal via de
penetração por aberturas naturais (AMORIM; PASCHOLATI, 2011). Nesse
sentido, a densidade estomática pode ser outro mecanismo importante de
defesa das plantas contra a penetração (PAZ-LIMA et al., 2010).
Como resposta à infecção, destacam-se a formação de halos, papilas,
zonas de lignificação ou de abscisão e tilose (AMORIM; PASCHOLATI,
2011). As papilas são projeções das células epidérmicas com intuito de
aumentar o espaço entre a parede celular e a membrana no exato local onde
27
resistência a Fusarium culmorum em trigo está associada à formação de
papilas (KANG; BUCHENAUER, 2000). Zonas de suberização ou camadas
de abscisão são fundamentais para evitar a progressão da doença. Após a
infecção, a zona de suberização isola o patógeno em determinada área já
contaminada do hospedeiro e dificulta o fluxo de água e nutrientes do
hospedeiro para o fungo e o trânsito de toxinas e enzimas do patógeno para
o hospedeiro (STANGARLIN et al., 2011).
Na relação patógeno-hospedeiro, os mecanismos bioquímicos
produzidos pelas plantas são mais versáteis. Dentre as substâncias
pré-formadas, têm-se: ácido clorogênico, ácido protocatecóico e catecol, α -tomatina, avenacinas, tuliposídeos, glicosídeos fenólicos, inibidores protéicos
e enzimas de defesa vegetal. Em meio aos compostos de defesa formados
após a infecção, podemos citar as espécies reativas de oxigênio, o óxido
nitroso e as fitoalexinas (STANGARLIN et al., 2011). Oriundas do
metabolismo secundário, as fitoalexinas possuem propriedades
antimicrobianas e são produzidos pelas plantas em resposta a estresses
físicos, químicos ou biológicos (AMORIM; PASCHOLATI, 2011;
STANGARLIN et al., 2011).
2.5. Herbicidas X doenças de plantas
Os herbicidas podem interferir direta ou indiretamente sobre os
mecanismos de defesa das plantas aos patógenos (FIGURA 1d-e), como
também diretamente sobre a germinação e o crescimento de fungos
fitopatogênicos (FIGURA 1f-g). Em ambos os casos, podem afetar de forma
positiva ou negativa a severidade de doenças em culturas.
Os efeitos de adjuvantes sobre os mecanismos de defesa estruturais
pré-formados podem favorecer a penetração dos patógenos ao hospedeiro.
Ao promover perda de turgor e degeneração dos tricomas, o espaço entre o
esporo fúngico e a superfície foliar é reduzido, o que possibilita que, após a
germinação, as hifas fúngicas penetrem no hospedeiro (FIGURA 1d). Além
28
adjuvante, facilita a penetração (FIGURA 1e). Pulverizações em folhas de
Brassica napus com os herbicidas dalapon, carbetamida e propizamida
reduziram a quantidade e alteraram a forma das ceras epicuticulares, o que,
favoreceu a infecção por Cylindrosporium concentricum (RAWLINSON et al.,
1978).
O efeito herbicida é mais complexo e depende do mecanismo de ação
do herbicida utilizado. O glyphosate é um herbicida não seletivo e seu
mecanismo de ação afeta a rota do ácido chiquímico, precursor envolvido na
defesa de plantas a patógenos, destacando-se: taninos, antocianinas, ácido
salicílico, lignina, flavonas, isoflavonas e cumarinas (BUCHANAN et al., 2000;
SRIVASTAVA, 2001). Dessa forma, plantas sensíveis previamente expostas
ao glyphosate podem tornar-se mais vulneráveis ao ataque de patógenos.
Por outro lado, o glyphosate pode apresentar efeitos prejudiciais
diretos sobre a germinação de esporos fúngicos (FIGURA 1f) ou no
crescimento de hifas fúngicas (FIGURA 1g). A rota do chiquimato é afetada
pelo herbicida glyphosate e também está presente em fungos e bactérias
(RICHARDS et al., 2006), por isso a importância desse herbicida no manejo
de agentes fitopatogênicos. O glyphosate inibiu o crescimento de Rhizoctonia
solani, Ceratocystis fimbriata, Cryphonectria cubensis, Phytophthora capsici,
Macrophomina phaseolinea, Sclerotium rolfsii, Fusarium oxysporum e
Mirothecium roridum, que são fungos causadores de doenças importantes em
feijoeiro, mangueira, eucalipto, pimentão e tomateiro (ROSA et al., 2010).
Efeito inibitório desse herbicida também foi relatado por Tuffi Santos et al.
(2011) sobre a germinação e crescimento in vitro de Puccinia psidii causador
da ferrugem do eucalipto.
Outro grupo importante é constituído pelos herbicidas inibidores da
PROTOX, como o herbicida carfentrazone-ethyl. Ao inibir a síntese dessa
enzima, ocorre acúmulo de protoporfirinogênio IX, que, na presença de luz e
de oxigênio, resulta na formação de espécies reativas de oxigênio (SILVA;
SILVA, 2012), que são compostos importantes na defesa de plantas aos
pós-29
formados (STANGARLIN et al., 2011). Por outro lado, plantas sensíveis
tratadas com esses herbicidas apresentam pontos necróticos nas folhas, já
que, na presença de luz, essas espécies reativas de oxigênio acionam a
peroxidação de lipídeos, resultando na morte celular por degeneração das
membranas plasmáticas. Tal fato reduz a infecção por patógenos biotróficos,
que obrigatoriamente necessitam de tecido hospedeiro vivo para se instalar e
reproduzir (BEDENDO, 2011).
Além do efeito direto sobre o patógeno ou indireto sobre os
mecanismos de defesa das plantas aos patógenos, as plantas daninhas
podem ser hospedeiras em potencial para uma gama variada de agentes
fitopatogênicos (NTIDI et al., 2012; ALTINOK, 2013; GONÇALVES et al.,
2015). Nesse sentido, o uso de herbicidas para manejo de plantas daninhas
representa grande importância no surgimento e severidade de algumas
doenças. O uso de herbicidas é a principal estratégia utilizada para o manejo
da podridão radicular causada por Rhizoctonia solani e Rhizoctonia oryzae
em cultivos de cevada (BABIKER et al., 2011). Em três anos de experimentos
em campo, os autores supracitados observaram que, quando o manejo
químico de plantas daninhas com glyphosate era empregado, houve redução
significativa da gravidade da doença na safra seguinte (BABIKER et al.,
2011). Entretanto, a ação herbicida leva à redução da biodiversidade vegetal
nas áreas cultivadas decorrente do controle de plantas daninhas. E a
presença de uma espécie cultivada isoladamente pode favorecer certas
doenças (ALTIERE, 1999).
Outro ponto importante é a influência do uso de herbicidas sobre
insetos, que muitas vezes podem atuar como vetores, sobretudo em doenças
causadas por vírus (GUTIÉRREZ et al., 2013; MAUCK et al., 2015). Egan et
al. (2014) observaram redução de três espécies de herbívoros e o aumento
30
Figura 1 - Ação herbicida indireta sobre os mecanismos de defesa estruturais de
plantas aos patógenos (B-E) e direta sobre a germinação de esporos ou
crescimento de hifas (F-G). A. Hospedeiro sem mecanismos de defesa;
Esporos (Es) germinam e hifas (Hi) penetram de forma direta através de
apressórios (Ap) ou por aberturas naturais. B. Na presença de tricomas
(Tr) os esporos germinam, mas não atingem a epiderme. C. Cutícula
espessa (Ct) e ceras epicuticulares (CE) formam barreiras à penetração.
D. Efeito dos herbicidas sobre os tricomas favorece a penetração. E.
Degeneração das ceras epicuticulares e cutícula, facilitando a
penetração. F e G. Moléculas herbicidas (MH) inibem a germinação de
esporos.
Fonte: Elaborada pelo autor, 2016, a partir de informações extraídas dos trabalhos
WYSS; MÜLLER-SCHÄRER, 2001; LARSON et al., 2006; TUFFI-SANTOS et al.,
2009; ROSA et al., 2010; AMORIM; PASCHOLATI, 2011; STANGARLIN et al., 2011;
31
3. MATERIAL E MÉTODOS
3.1. Obtenção das mudas
Para condução dos experimentos foram utilizadas mudas de dois
clones de Eucalyptus grandis, G-21 e G-33, previamente classificados como
resistente (JUNGHANS et al., 2003a) e suscetível, respectivamente. As
mudas foram cultivadas e cedidas pela Clonar Resistência a Doenças
Florestais LTDA. Aos 60 dias de idade, estas foram transplantadas para
vasos de 2l, contendo substrato MecPlant® enriquecido com 1,3kg de fosfato
super simples e 600g de Osmocote® (NPK, 19-6-10) para cada 100kg de
substrato. Durante o transplantio cada muda recebeu 100ml de solução de
MAP®. Em seguida, foram mantidas em casa de vegetação até o momento
da inoculação. Vinte dias após transplantio (DAT) as mudas se encontravam
com altura entre 30-40cm e bem galhadas (aproximadamente 10 galhos).
3.2. Instalação dos experimentos
O trabalho foi realizado em dois ensaios consecutivos, sendo o
primeiro em fevereiro de 2015 e o segundo em abril do mesmo ano,
mantendo-se as mudas e o método, à exceção da concentração de inóculo.
Após o término do primeiro, ensaio, as plantas foram podadas, para retirada
dos galhos que receberam aplicação herbicida e de folhas que estavam
infectadas. Posteriormente, as plantas foram adubadas com 100 ml/planta de
solução do adubo Biofert Universal® (NPK: 6-4-4), diluído em água (1:100).
As plantas permaneceram em repouso por 20 dias. Em seguida, quando não
apresentavam mais sintomas de intoxicação causada pelo herbicida, foi
realizado o segundo ensaio.
Em ambos os ensaios, utilizou-se delineamento experimental em
blocos casualizados com 10 repetições, em esquema fatorial 2 x 4 (dois
clones e quatro subdoses de herbicidas). Para cada parcela experimental, foi
considerado um vaso contendo uma planta de eucalipto. Os herbicidas
32
SPOTLIGHT® e o glyphosate na formulação ROUNDUP ORIGINAL®. As
subdoses testadas foram 0 (controle); 6% da dose máxima recomendada
pelo fabricante (50g e.a. ha-1) de carfentrazone-ethyl; 6% da dose
recomendada (1440g e.a. ha-1) de glyphosate; e a dose em mistura (6%
carfentrazone-ethyl + 6% de glyphosate).
3.3. Aplicação dos herbicidas
No primeiro ensaio, a aplicação foi realizada aos 20 DAT das mudas,
enquanto no segundo ensaio, ela foi realizada em abril (20 dias após o
término do primeiro ensaio). Ambas as aplicações foram realizadas
simulando deriva no terço inferior da copa das plantas de eucalipto.
Utilizou-se pulverizador costal pressurizado por CO2, equipado com barra contendo
dois bicos modelo TT 110.02, calibrado para aplicar 150 L ha-1 de calda. Para
evitar contato do produto com outras partes da planta, a parte superior da
copa foi protegida por saco plástico no momento da aplicação, de modo a
deixar apenas a porção inferior da copa (aproximadamente 3 galhos) exposta
ao produto.
3.4. Inoculação do patógeno
A inoculação foi realizada dois dias após a aplicação dos herbicidas.
Utilizou-se o isolado UFV-2 de Puccinia psidii (raça 1), obtidos de plantas de
Eucalyptus grandis em Itapetininga, São Paulo, Brasil (XAVIER et al., 2001),
cuja coleção encontra-se depositada na micoteca da UFV. O isolado foi
previamente multiplicado em mudas de Jambo (Sygyzium jambos) (RUIZ et
al., 1989). Os urediniósporos produzidos foram coletados aos 12 dias após
inoculação em Jambo, e, para inoculação nas plantas de eucalipto,
preparou-se suspensão com concentração de 2x104 mL-1 para o primeiro ensaio, e de
2x105 mL-1 para o ensaio realizado em abril.
A suspensão de urediniósporos foi atomizada homogeneamente em
ambas as faces do limbo foliar, por toda planta, com o auxílio de atomizador
33
aferir a eficiência da inoculação, foram distribuídas aleatoriamente, em meio
às plantas de eucalipto, três plantas de Jambo (espécie suscetível a
ferrugem). As mudas inoculadas foram mantidas em câmara de nevoeiro, no
escuro, por 24 horas e posteriormente levadas para câmara de crescimento
com temperatura ajustada para 22oC, com fotoperíodo de 12 horas (RUIZ et
al., 1989) e intensidade luminosa de 130 µmoles de fótons m2 s-1.
3.5. Avaliação da tolerância dos clones aos herbicidas
A tolerância dos clones aos herbicidas foi avaliada através do
percentual de fitointoxicação, do crescimento das plantas em altura e da
produção de massa seca da parte aérea (MSPA). As avaliações de
fitointoxicação foram realizadas aos 23 dias após a aplicação (DAA), através
de observações visuais, em que se adota escala de 0 a 100%, na qual zero é
a ausência de intoxicação e 100% a morte da planta. Observações diárias
durante todo o período de condução dos ensaios foram realizadas para
avaliação de possíveis sintomas de intoxicação causados pelos herbicidas.
Ao final do ensaio 2, para avaliar o crescimento, foi mensurada a altura
total entre a base do substrato até o ápice de todas as plantas. Em seguida,
as plantas foram coletadas rente ao substrato e armazenadas em sacos de
papel. Após secagem em estufa de ventilação forçada ajustada para 65°C, as
plantas foram pesadas diariamente durante cinco dias até atingirem peso
constante.
3.6. Avaliação da severidade da ferrugem
A avaliação da severidade foi realizada aos 21 DAI, através do índice
de McKinney (IMc), índice médio de área foliar infectada e do número médio
de urediniósporos produzidos. Para isso, em cada planta, foram marcados
três galhos representativos do estágio de infecção da planta e em cada galho
foram escolhidas duas folhas.
Para gerar o índice de incidência da doença, foi realizada avaliação
34
de severidade (S0, S1, S2 e S3) (JUNGHANS et al., 2003b), sendo S0=0,
S1=1, S2=2 e S3=3. O índice de McKinney (MCKINNEY, 1923; modificado
por COOKE, 2006) foi calculado de acordo com a seguinte fórmula:
Imc % =∑ f x vN x X x
na qual: f = classe de infecção; v = número de folha que apresentou cada
classe; N = total de folhas avaliadas; X = maior valor entre as classes (nota
3).
As duas folhas escolhidas de cada ramo para avaliar o IMc foram
coletadas e fotografadas. As imagens foram submetidas ao software de
análise de imagem, Image Pro-Plus Versão 4.5, para determinação do índice
de área foliar infectada (Iafi), obtido através da divisão da área infectada pela
área sadia. Após obtenção das imagens, foram retirados de cada folha, com
auxílio de furador de 6mm de diâmetro, dois discos, que foram colocados em
tubo do tipo Eppendorfs de 2 mL, no qual foi adicionado 10 µL de Tween 20®,
sendo o volume completado com água destilada. Após homogenização em
agitador magnético por um minuto, 170µL da suspensão foi transferida para
câmera de Neubauer, e a contagem do número médio de uredinióporos
produzidos (NMUP) foi realizada em duplicata, em microscópio de luz.
3.7. Análises fisiológicas
A fisiologia dos clones de eucalipto foi avaliada aos quatro e aos 23
DAA, em folhas expandidas da parte apical da copa (protegida da aplicação).
Os parâmetros avaliados foram a condutância estomática, a taxa
fotossintética líquida e o rendimento efetivo do fotossistema II, sendo esse
último, obtido através da fluorescência da clorofila a. Para determinar a troca
de gases da folha foi utilizado analisador portátil de fotossíntese LI-6400 XT.
Durante a avaliação, utilizou-se luz interna controlada, na intensidade de
1000 µmoles de fótons m2 s-1 e CO
35
leituras foram feitas em triplicatas e registradas quando o coeficiente de
variação (CV) do aparelho se encontrava abaixo de 5%.
3.8. Anatomia e ultraestrutura foliar
Para avaliar os efeitos dos herbicidas na anatomia e ultraestrutura
foliar nas plantas de eucalipto e a histopatologia da interação Puccinia psidii
X Eucalyptus grandis, amostras foliares foram coletadas para análise em
microscopia de luz e microscopia eletrônica de varredura e de transmissão.
As coletas foram realizadas aos 0, 2, 6 e 12 dias após inoculação
(DAI). A coleta no tempo zero, exclusivamente com intuito de avaliar os
efeitos provocados pelo herbicida foi realizada imediatamente antes da
inoculação e em folhas de galhos do terço inferior da copa sujeitas à
aplicação do herbicida. As demais coletas foram realizadas em folhas da
parte apical da copa. As amostras foram fixadas em solução de Karnovsky
(KARNOVSKY, 1965) e, para melhor penetração da solução fixadora, estas
foram colocadas em dessecador, sendo o ar retirado com bomba de vácuo
(0,1mmHg) por 20 minutos.
Para análise em microscopia de luz, as amostras foram desidratadas
em série crescente de etanol (30, 50, 70, 90 e 100%, sendo esta última
lavagem repetida 3 vezes) e polimerizadas em resina acrílica tipo metacrilato.
Cortes transversais com 7 µm de espessura foram obtidos em micrótomo
rotativo manual Reichert, corados em azul de toluidina pH=4,0 (O‘BRIEN; McCULLY, 1981) e montados em lâmina e lamínula, utilizando como meio de
montagem o Entellan®. Após observação, foi realizada documentação
fotográfica, utilizando microscópio de luz (modelo Zeiss Axioskop 2) com
câmera digital acoplada (modelo MRC3).
Para análise em microscopia eletrônica de varredura (MEV), as
amostras foram pós-fixadas em tetróxido de ósmio 1%, desidratadas em série
de acetona (30, 50, 70, 90 e 100%, repetindo-se a última lavagem 3 vezes) e
secas ao ponto crítico (modelo Balzers CPD 030). Após montagem em
“stubs” utilizando fita de carbono dupla face, as amostras receberam
36
o material foi analisado em microscópio eletrônico de varredura (modelo
Zeiss LEO 435-VP), sendo as imagens registradas em arquivos digitais.
Para análise em microscopia eletrônica de transmissão (MET), as
amostras foram retiradas do Karnovsky lavadas por três sessões (10 minutos
cada) em tampão cacodilato a 0,05M e pós-fixadas em tetróxido de ósmio 1%
por uma hora. Em seguida, contrastadas em acetato de uranila a 0,5%
(pernoite), desidratadas em acetona (30, 50, 70, 90 e 100%, sendo esta
última lavagem repetida 3 vezes) e polimerizadas em resina (SPURR),
permanecendo em estufa a 70°C por período de três dias. Após obtenção
dos bloquinhos (material polimerizado), foram realizados cortes ultrafinos
(70nm de espessura), que foram contrastados com acetato de uranila e
citrato de chumbo (REYNOLDS, 1963), sendo observados ao microscópio
eletrônico de transmissão.
3.9. Análise estatística
Os dados foram submetidos à análise de variância e, quando
pertinente, as médias foram comparadas pelo teste de Tukey a 5% de
significância. Dados avaliados nos dois ensaios como a fitointoxicação e os
dados de severidade da ferrugem tiveram os resultados processados e
analisados através da análise conjunta de dados (OLIVEIRA, 1993). As
variáveis quantitativas estudadas foram submetidas ao teste de correlação de
37
4. RESULTADOS E DISCUSSÃO
4.1. Tolerância dos clones aos herbicidas
4.1.1. Efeitos dos herbicidas na morfologia, anatomia e ultraestrutura foliar e na fisiologia das plantas
Folhas da parte basal da copa das plantas de eucalipto expostas à
aplicação de 3g e.a. ha-1 de carfentrazone-ethyl, apresentaram pontos
cloróticos e necróticos 24h após aplicação (FIGURA 2). Na parte apical da
copa, protegida da aplicação, os sintomas começaram a aparecer aos 10
dias após aplicação (DAA) (FIGURA 3).
Plantas dos clones G-33 e G-21 submetidas à aplicação dos herbicidas
apresentaram clorose no ápice e bordas foliares (FIGURAS 3b-d, f, h).
Porém, nas plantas do G-21 expostas a 3 g e.a. ha-1 de carfentrazone-ethyl,
nenhum sintoma visual de intoxicação foi observado (FIGURA 3g).
Os sintomas evoluíram e, aos 23 DAA, as plantas dos dois clones que
receberam as aplicações dos herbicidas apresentaram clorose distribuída por
todo o limbo foliar (FIGURA 4), à exceção das plantas do clone G-21
submetidas à subdose isolada de carfentrazone-ethyl. Estas não
apresentaram sintomas de intoxicação na parte apical da copa (FIGURA 4g).
O carfentrazone-ethyl é um herbicida de efeito rápido. Plantas
sensíveis tratadas com esse herbicida acumulam protoporfirinogênio IX, que
na presença da luz, catalisa a formação do oxigênio singleto, responsável
pela peroxidação de lipídeos e degeneração das membranas plasmáticas
(SILVA; SILVA, 2012). Assim, pontos necróticos de coloração marrom ou
palha (FIGURA 2) são os sintomas mais característicos da intoxicação por
carfentrazone-ethyl, os quais podem aparecer no mesmo dia da aplicação do
produto. Tais sintomas também foram observados por Tuffi-Santos et al.
(2006), em plantas de eucalipto aos dois dias após aplicação (DAA).
Entretanto, o herbicida glyphosate possui efeito mais lento. Embora existam
relatos do surgimento de clorose em eucalipto aos 4 e aos 6 dias após
38
presente trabalho, os primeiros sintomas foram observados aos 10 DAA.
Essa diferença na velocidade de aparecimento dos sintomas de intoxicação
pode estar ligada à dose do glyphosate utilizada e ao genótipo envolvido.
Figura 2 - Efeito da deriva dos herbicidas em folhas da parte basal da copa, exposta à aplicação, de clones de Eucalyptus grandis 24 horas após aplicação. A,
B, E e F. Folhas sem presença de sintomas de intoxicação. C, D, G e H.
Folhas com sintomas de intoxicação. Setas indicam pontos necróticos
causados pelo carfentrazone-ethyl. Mistura = 86,4 g e.a. ha-1 de
glyphosate + 3 g e.a. ha-1 de carfentrazone-ethyl. Barras = 1cm.
39
Figura 3 - Efeito da deriva dos herbicidas em folhas da parte apical da copa, protegida da aplicação, de clones de Eucalyptus grandis 10 dias após
aplicação. A, E e G. Folhas sem presença de sintomas de intoxicação. B,
C, D, F, G e H. Folhas com sintomas de intoxicação com clorose na borda
e ápice foliar. Mistura = 86,4 g e.a. ha-1 deglyphosate + 3 g e.a. ha-1 de
carfentrazone-ethyl. Barras = 1cm.
40
Figura 4 - Efeito da deriva dos herbicidas em folhas da parte apical da copa, protegida da aplicação, de clones de Eucalyptus grandis 23 dias após
aplicação. A, E e G. Folhas sem presença de sintomas de intoxicação. B,
C, D, G e H. Folhas com sintomas de intoxicação com clorose distribuída
por todo limbo foliar. Mistura = 86,4 g e.a. ha-1 deglyphosate + 3 g e.a. ha
-1 de carfentrazone-ethyl. Barras = 1cm.
41
Em relação aos efeitos na anatomia e ultraestrutura foliar, plantas
tratadas com subdoses de glyphosate e carfentrazone-ethyl, aplicados
isoladamente, apresentaram células com ceras epicuticulares erodidas nas
faces abaxial (FIGURA 5) e adaxial (FIGURA 6) da epiderme. Além da
erosão das ceras epicuticulares, plantas do clone G-33 expostas à deriva de
ethyl e da subdose em mistura (glyphosate +
carfentrazone-ethyl) apresentam perda de turgor e ruptura da cutícula das células-guardas
do estômato (FIGURAS 5e, g).
Em corte transversal, nota-se que o efeito mais prejudicial avaliado aos
dois dias após aplicação dos herbicidas foi provocado pela aplicação de
carfentrazone-ethyl (FIGURA 7). Folhas dos dois clones diretamente
expostas à aplicação do referido herbicida apresentaram células da epiderme
adaxial e dos parênquimas paliçádico e lacunoso degradadas (FIGURAS
7e-h).
A erosão de ceras epicuticulares e degeneração da cutícula,
decorrentes do efeito de adjuvantes presentes na formulação comercial dos
herbicidas, também já foram relatados anteriormente para o eucalipto
(TUFFI-SANTOS et al., 2009) e para outras plantas (RAWLINSON et al.,
1978; SANTOS et al., 2015; TUFFI-SANTOS et al., 2015).
O herbicida carfentrazone-ethyl inibe a síntese da enzima
protoporfirinogênio oxidase, que nas plantas, encontra-se nos cloroplastos
(SILVA; SILVA, 2012). Isso pode explicar a degeneração de células de
parênquima paliçádico, que é o tecido mais fotossintéticamente ativo, bem
como a desorganização dos tilacoides dos cloroplastos, observadas em
42
Figura 5 - Microscopia eletrônica de varredura. Efeito da deriva dos herbicidas na
face abaxial de folhas da parte basal da copa, exposta à aplicação, em
clones de Eucalyptus grandis 2 dias após aplicação. A-B. Células do
complexo estomático com turgor e ceras epicuticulares com conformação
característica a espécie. C-H. Ceras epicuticulares erodidas (asteríscos).
E e G. Degeneração de parede, seta indica ruptura da cutícula (Ct) nas
células guardas do complexo estomático. Mistura = 86,4 g e.a. ha-1 de
glyphosate + 3 g e.a. ha-1 de carfentrazone-ethyl. Barras = 25 µm.
43
Figura 6 - Microscopia eletrônica de varredura. Efeito da deriva dos herbicidas na
face adaxial de folhas da parte basal da copa, exposta à aplicação, em
clones de Eucalyptus grandis 2 dias após aplicação. A-B. Células
epidérmicas com turgor e ceras epicuticulares com conformação
característica à espécie. C-H. Ceras epicuticulares erodidas (asteríscos).
Mistura = 86,4 g e.a. ha-1 de glyphosate + 3 g e.a. ha-1 de
carfentrazone-ethyl. Barras = 25 µm.
44
Figura 7 - Microscopia de luz. Efeito da deriva dos herbicidas em folhas da parte basal da copa, exposta à aplicação, de clones de Eucalyptus grandis 2
dias após aplicação. A-D. Células com conformação e turgor
característico à espécie. E-H. Células epidérmicas degradadas
(asteriscos); células parenquimáticas com perda de turgor (setas).
Abreviações: Ep – epiderme; PP – parênquima paliçádico; PL –
parênquima lacunoso; Es – estômato. Mistura = 86,4 g e.a. ha-1 de
glyphosate + 3 g e.a. ha-1 de carfentrazone-ethyl. Barras = 25 µm.