Ar
tigo Técnico
por microrganismos
Biodegradation potential of microcystins by microorganisms
Francine Kuriama
Mestre pelo Programa de Pós-graduação em Engenharia de Edificações e Saneamento da Universidade Estadual de Londrina (UEL) – Londrina (PR), Brasil.
Emília Kiyomi Kuroda
Professora Adjunta C do Departamento de Construção Civil do Centro de Tecnologia e Urbanismo da UEL – Londrina (PR), Brasil.
Karla Bigetti Guergoletto
Mestre e Doutoranda do Programa de Pós-graduação em Ciência e Tecnologia de Alimentos da UEL – Londrina (PR), Brasil.
Sandra Garcia
Professora e Pesquisadora do Departamento de Ciência e Tecnologia de Alimentos da UEL – Londrina (PR), Brasil.
Gisele Maria de Andrade de Nobrega
Professora Adjunta B do Departamento de Biologia Geral do Centro de Ciências Biológicas da UEL – Londrina (PR), Brasil.
Kiyomi Tsuji
Kanagawa Prefectural Institute of Public Health – Chigasaki, Japão.
Ken-Ichi Harada
Meijo University – Nagoya, Japão.
Elisa Yoko Hirooka
Professora Associada C do Departamento de Ciência e Tecnologia de Alimentos da UEL – Londrina (PR), Brasil.
Resumo
Para minimizar os problemas relacionados à ocorrência de cianobactéria em águas destinadas ao consumo humano há necessidade de se realizar estudos de alternativas técnicas de tratamento com destaque aos biofilmes com potencial de degradação de microcistinas (MC). O presente trabalho teve como objetivo avaliar o potencial de degradação de MC pela bactéria Sphingosinicellamicrocystinivorans B9, diferentes cepas de leveduras e bactérias probióticas. O teste foi efetuado com extrato de MC e diferentes quantidades de biovolume e densidade celular dos microrganismos. Os tratamentos foram mantidos a 27°C com rotação de 100 rpm e as amostras para análise de MC e contagem dos microrganismos foram retiradas após 0 e 96 horas de contato. A bactéria B9 apresentou maior degradação de MC, chegando a 98% após 96 horas.
Palavras-chave: cianotoxinas; microcistinas; biodegradação; bactéria B9; leveduras; bactérias probióticas.
Abstract
To minimize problems related to the occurrence of cyanobacteria in water for human consumption there is need to investigate alternative treatment techniques with emphasis on biofilms with the potential degradation of microcystins (MC). This study aimed to evaluate the potential degradation of MC by bacteria Sphingosinicella microcystinivorans B9, different strains of yeast and probiotic bacteria. The test was carried out with the extract obtained from strain Microcystis sp. In the tests biomass and cultures of microorganisms were used and the treatments were maintained at 27°C with 100 rpm. Samples for analysis of MC and for counting the microorganisms were collected at 0 and 96 hours. The bacterium B9 presented the highest potential of degradation of MC reaching 98% after 96 hours.
Keywords: cyanotoxins; microcystin; biodegradation; bacterium B9; yeast; probiotic bacteria.
Na agricultura, o biocontrole de patógenos tem sido prioritaria-mente realizado com a introdução de organismos antagonistas ao alvo a ser protegido. Entre os utilizados, alguns pesquisadores têm preferido as leveduras, especialmente quando o objetivo dos traba-lhos é a proteção de frutos destinados ao consumo in natura. Essas têm se mostrado promissoras para o uso no controle das doenças que ocorrem em pós-colheita (KRAEMER et al., 2007).
A espécie Saccharomycescerevisae e espécies filogeneticamente próxi-mas são as mais empregadas pelo homem que as utilizam nas indústrias de fermentação alimentícia e de bebidas. As principais características que tornam as leveduras interessantes para usos industriais são sua facilida-de facilida-de obtenção e multiplicação, utilização facilida-de nutrientes na forma mais simples, possibilidade de cultivo independente do ambiente, pequena exigência de água e área, formação de produtos de valor nutritivo, além de serem consideradas seguras para uso de maneira geral (DEL RIO, 2004). Adicionalmente, estudos têm demonstrado a capacidade desta espécie em remover metais pesados da água, tornando uma alternativa promissora para descontaminação ambiental (WANG; CHEN, 2006).
Outro tipo de microrganismos que podem promover a degrada-ção de microcistinas são os microrganismos probióticos, que quando consumidos através de uma dieta, conferem benefícios à saúde de humanos e animais. Estudos feitos com Lactobacillus e Bifidobacteria
mostraram que esses microrganismos são relativamente eficientes para remoção de MC, porém é preciso adaptá-los para serem utili-zados em escala real (NYBOM; SALMINEM; MERILOUTO, 2007).
Assim, o objetivo desse trabalho foi avaliar o potencial de degra-dação de MC em águas pela bactéria Sphingosinicella microcystinivo-rans B9 e por diferentes cepas de leveduras e de bactérias probióticos.
Material e métodos
As condições empregadas no teste foram selecionadas através dos resultados obtidos do experimento efetuado anteriormente, no qual foram testadas diferentes condições com a finalidade de encontrar as condições ideais para o teste de varredura. Assim as condições ideais foram: 1 mL de cultura acrescidos de 1 mL de meio e 1 mL de biovo-lume acrescidos de 1 mL de meio.
Preparação do extrato de
Microcystis sp
A cepa de cianobactéria Microcystis sp foi cultivada em meio ASM-1 estéril por 20–30 dias em temperatura de 25±1ºC, intensida-de luminosa intensida-de 35 mE.m-2.s-1, fotoperíodo de 12 horas.d-1 e aeração
contínua. Em seguida, as culturas foram centrifugadas a 5.000 rpm por 20 minutos para obtenção de biovolume. Estas foram congeladas a -20ºC, liofilizadas (Liotop L101/Liobras) e ressuspensas em água ultrapura. Para liberação da toxina foram realizadas, repetições de três séries de congelamento/descongelamento do biovolume, segui-das de armazenamento a -20ºC até o momento de uso.
Introdução
O aumento da concentração de nutrientes, principalmente de ni-trogênio e fósforo em mananciais de água para abastecimento públi-co, favorece a proliferação de cianobactérias, que em alguns casos são produtoras de toxinas (cianotoxinas). Essas toxinas podem acarretar graves consequências para a saúde humana e de animais, devido ao seu potencial cancerígeno.
As cianobactérias são microrganismos procariotos, geralmente aquá-ticos, que realizam fotossíntese com liberação de oxigênio, possuem uma ampla diversidade de formas, devido às adaptações morfológicas, bioquímicas e fisiológicas adquiridas durante seu longo processo evolu-tivo. Algumas cianobactérias são potencialmente toxigênicas, tais como os gêneros Microcystis, Cylindrospermopsis, Anabaena, Aphanizomenon e
Planktothrix (OLIVEIRA-BITTENCOURT; MOLICA, 2003).
As cianotoxinas presentes na água podem afetar a saúde humana, tanto pela ingestão como por contato em atividades de recreação no ambiente, ou ainda pelo consumo de pescado contaminado, poden-do ter ação neurotóxica, hepatotóxica ou serem irritantes por contato (BRASIL, 2003).
No Brasil, a Portaria nº 2.914 do Ministério da Saúde (BRASIL, 2011) obriga o monitoramento de cianobactérias e cianotoxinas, es-tabelecendo o valor máximo permitido de 1,0 mg.L-1 de microcistinas
para água de consumo humano.
No Brasil, a presença de cianobactérias em mananciais é um grave problema enfrentado pelas Estações de Tratamento de Águas (ETA) que utilizam as tecnologias de tratamento por ciclo completo (DI BERNARDO; MINILLO; DANTAS, 2010) ou mesmo de filtração direta, pode resultar no aumento do custo de tratamento de águas, uma vez que a remoção de metabólitos dissolvidos como as ciano-toxinas, gostos e odores indesejáveis requer, em geral, a aplicação de processos específicos de tratamento. Além disso, dependendo da espécie e do número de indivíduos de cianobactérias, pode ocorrer a redução da duração das carreiras de filtração e/ou comprometimento da qualidade da água produzida.
Com o intuito de controlar os problemas causados pelas cia-nobactérias, em muitos sistemas de tratamento de água é aplicada a pré-cloração para inativação desses microrganismos. Entretanto, esse pré-tratamento pode promover a lise celular, com consequente liberação de metabólitos secundários como as microcistinas, que não são removidas pelas técnicas de tratamento usuais, e favorecer a for-mação de subprodutos organohalogenados.
Isolamento e cultivo dos microrganismos
A cepa de Sphingosinicella microcystinivorans B9 cedida pelo
Laboratory of Environmental Sciences, Faculty of Pharmacy, Meijo University Nagoya, Aichi, Japão, foi isolada do Lago Tsukui, Kanagawa. Para realização dos experimentos a cepa foi mantida em meio sólido (Sakurai) a 25ºC, incubando-se por 48–72 horas e culti-vada em meio líquido (peptona de caseína 0,2%, extrato de levedura 0,1% e glicose 0,05%) a 25ºC por 72 horas.
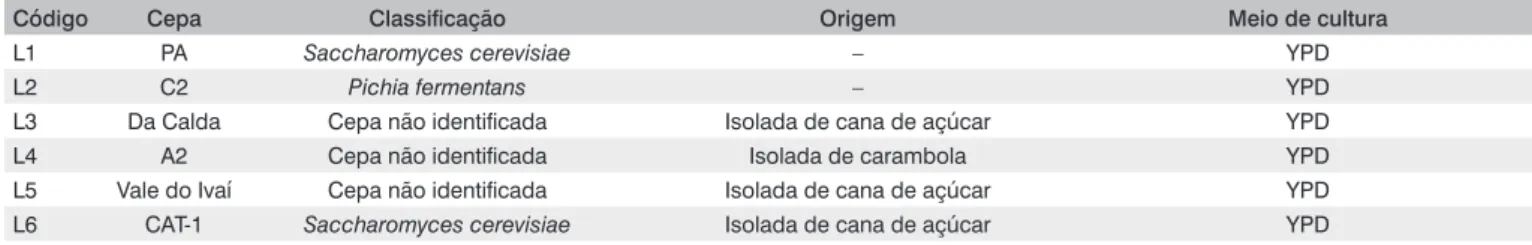
As leveduras utilizadas são mostradas na Tabela 1, para realização dos testes elas foram cultivadas em meio YPD (extrato de levedura 1%, glicose 2% e peptona 2%) a 25ºC por 24 horas.
As culturas de bactérias probióticas utilizadas (Tabela 2) foram ativadas 3 vezes em Caldo MRS a 37°C por 18 horas, previamente aos experimentos.
Os grãos de kefir de água (mistura de bactérias lática, acética e le-vedura) foram cultivados previamente 3 vezes em solução de açúcar mascavo à temperatura ambiente, por 24 horas.
Preparação do teste
Primeiramente adicionaram-se 8 mL do extrato de Microcystis sp
(com concentração de 1 mg.L-1 de microcistinas) em frascos de
vi-dro com capacidade máxima de 50 mL. Os diferentes tratamentos (Figura 1 e Tabela 3) foram realizados adicionando-se 1 mL de bio-volume (condição experimental A) ou do inóculo (cultura contendo microrganismos já adaptados) de bactéria B9 ou levedura ou bacté-rias probióticas + 1 mL de meio específico de cada microrganismo. No teste com grãos de kefir foi adicionado apenas 1 g do grão + 1 mL da solução de açúcar mascavo 5%.
Os tratamentos foram mantidos a 27°C com rotação de 100 rpm por 96 horas. Nos tempos 0 e 96 horas foram retirados 1 mL para
análise de MC, realizada através do método de imunoensaio enzy-me-linked immunosorbent assay (ELISA) (kits de Beacon Analytical Systems Inc.) e 1 mL para contagem dos microrganismos.
Contagem de microrganismos
Para a bactéria B9, a contagem foi realizada por meio de diluições decimais e seriada em solução salina 0,85% estéril, inoculação em ágar Sakurai com incubação a 25ºC por 72 horas.
Para as leveduras, as amostras foram fixadas com formol 4% e a contagem celular foi realizada em câmara de Neubauer/micros-cópio Motic BA 210.
O teste de viabilidade e a contagem de bactérias probióticas fo-ram efetuados por meio de diluições decimais e seriadas de 1 mL da amostra em solução salina 0,85% estéril, inoculação em ágar MRS e incubação a 37ºC por 48 h.
Resultados e discussão
Independentemente da condição testada, a bactéria B9 apresen-tou a maior degradação de MC com 95 e 98% de degradação quando adicionada na forma de cultura — condição experimental A e biovo-lume centrifugado, condição experimental B, respectivamente. Essas eficiências comprovam os resultados obtidos por Tsuji et al. (2006), em que a imobilização da cepa de Sphingosinicellamicrocystinivorans
B9 em biorreatores constituídos de resinas de poliéster mostrou eli-minação completa de MC-LR após 24 horas.
A Figura 2 mostra os resultados do teste de degradação de MC nos tempos 0 e 96 horas pela bactéria B9 e pelas leveduras testadas.
Dentre as cepas de leveduras testadas, a maior eficiência de de-gradação foi obtida com biovolume da cepa Vale do Ivaí (L5) a qual apresentou 37% de degradação após 96 horas de incubação, seguida
Tabela 1 – Cepas de leveduras utilizadas no teste de varredura para degradação de microcistinas.
Código Cepa Classificação Origem Meio de cultura
L1 PA Saccharomyces cerevisiae – YPD
L2 C2 Pichia fermentans – YPD
L3 Da Calda Cepa não identificada Isolada de cana de açúcar YPD
L4 A2 Cepa não identificada Isolada de carambola YPD
L5 Vale do Ivaí Cepa não identificada Isolada de cana de açúcar YPD
L6 CAT-1 Saccharomyces cerevisiae Isolada de cana de açúcar YPD
Tabela 2 – Cepas de bactérias probióticas e grãos de kefir utilizadas no teste de varredura para degradação de microcistinas.
Código Cepa Classificação Origem Meio de cultura
P1 LPR Lactobacillus plantarum e rhamnosus Sacco MRS
P2 Bb12 Bifidobacterium lactis Christian Hansen MRS
P3 LC-1 Lactobacillus casei Christian Hansen MRS
P4 Kefir água Laboratório de Ciência de Alimentos (UEL) Açúcar mascavo
P5 La-5 Lactobacillus acidófilos Christian Hansen MRS
Tabela 3 – Condições experimentais do teste de varredura para degradação de MC por bactéria B9 e diferentes cepas de leveduras, bactérias probióticas e grãos de kefir.
Código Condições experimentais
A Extrato de MC + 1 mL za cultura** + 1 mL de meio* B Extrato de MC + 1 mL de biovolume** + 1 mL de meio*
*meio específico dos microrganismos: B9 – Sakurai ou leveduras – YPD ou bactérias probióticas – MRS ou kefir – açúcar mascavo.
**microrganismo específico B9 ou leveduras ou bactérias probióticas. MC: microcistinas.
do biovolume de CAT-1 (L6), com 24%. As outras cepas apresenta-ram resultados abaixo de 13% de degradação, sendo assim considera-das insatisfatórias para uso na biodegradação e biocontrole.
Por outro lado, as condições de manutenção das leveduras são bastante simples quando comparadas às da bactéria Sphingosinicella microcystinivorans B9 e às das bactérias probióticas, podendo-se cons-tituir como alternativa promissora para estudos futuros, desde que sua capacidade de degradação seja potencializada.
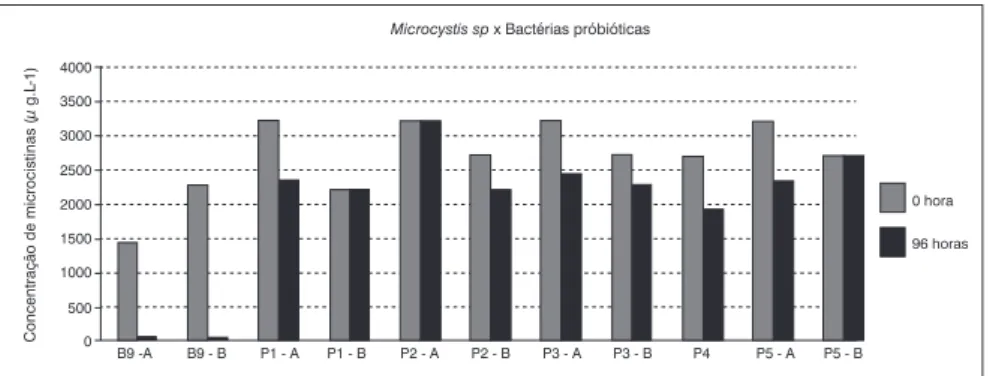
Entre as bactérias probióticas, o maior percentual de degradação foi de 27%, obtido pela cepa La-5 (P5) adicionada na forma de inócu-lo. O percentual de degradação de MC dos grãos de kefir (P4), foi de 29% após 96 horas de incubação. Estudos feitos com Lactobacillus e
Bifidobacteria mostraram que esses microrganismos são eficientes para remoção de MC, porém é preciso adaptá-los para serem utilizados em escala real (NYBOM; SALMINEM; MERILOUTO, 2007).
A Figura 3 mostra os resultados do teste de degradação de MC nos tempos 0 e 96 horas pela bactéria B9, pelas bactérias probióticas testadas e pelo kefir.
Conclusão
A bactéria Sphingosinicella microcystinivorans B9 foi eficiente, sen-do capaz de degradar entre 95 e 98% das MC presentes nos meios com concentração da ordem de 1 mg.L-1 em 96 horas de incubação.
De uma maneira geral, as capacidades de degradação de MC pelas leveduras e bactérias probióticas foram limitadas. Entre as Figura 1 – Esquema do teste de varredura para avaliação do potencial de degradação de microcistinas pela bactéria B9 e diferentes cepas de leveduras, bactérias probióticas, e grãos de kefir.
solução
de
açúcar
1 g grãos de
kefir
Sakurai
B9
YPD
Levedura
s
1 mL
biovolume
1 mL
MRS
Bactérias
probióticas
Sakurai
+
B9
Sakurai
YPD
+
Levedura
s
MRS
+
Bactérias
probióticas
MRS
1
mL
cultura
1 mL
Condição A
Condição B
YPD
Referências
BRASIL. MINISTÉRIO DA SAÚDE. (2011) Portaria n° 2.914 publicada em 14 de dezembro de 2011 no Diário Oficial da União nº 239 – Seção 1 p. 39-46
BRASIL. MINISTÉRIO DA SAÚDE. FUNDAÇÃO NACIONAL DE SAÚDE. (2003) Cianobactérias tóxicas na água para consumo humano na saúde pública e processos de remoção em água para consumo humano. Brasília: Ministério da Saúde, Fundação Nacional de Saúde. 56p.
DEL RIO, D.T. (2004) Biossorção de cádmio por leveduras
Saccharomyces cerevisiae. 66 f. Dissertação de mestrado – Escola
Superior de Agricultura “Luiz de Queiroz” da Universidade de São Paulo, Piracicaba.
DI BERNARDO, L.; MINILLO, A.; DANTAS, A.D. (2010) Florações de
algas e de cianobactérias: Suas influências na qualidade da água e nas
tecnologias de tratamento. São Carlos: Editora LDiBe.
leveduras testadas, a isolada do Vale do Ivaí (L5) apresentou o maior porcentual de degradação, 37%, após 96 horas de incu-bação. Em relação às bactérias probióticas as maiores eficiências
foram obtidas pela cepa La-5 (P5) com degradação de 27%, en-quanto os grãos de kefir (P4) apresentaram 29% de degradação de MC.
Figura 2 – Degradação de microcistinas pela bactéria B9 e seis cepas de leveduras utilizando extrato de Microcystis sp contendo microcistinas.
Microcystis sp x Leveduras
Concentração de microcistinas
(µg.L-1)
4000
3500
3000
2500
2000
1500
1000
500
0
B9 - A B9 - B L1 - A L1 - B L2 - A L2 - B L3 - A L3 - B L4 - A L4 - B L5 - A L5 - B L6 - A L6 - B
96 horas 0 hora
Figura 3 – Degradação de microcistinas pela bactéria B9, quatro cepas de bactérias probióticas e kefir utilizando extrato de Microcystis sp contendo microcistinas.
Microcystis sp x Bactérias próbióticas
Concentração de microcistinas (µ g.L
-1) 4000
3500
3000
2500
2000
1500
1000
500
0
B9 -A B9 - B P1 - A P1 - B P2 - A P2 - B P3 - A P3 - B P4 P5 - A P5 - B
KRAEMER, B.; PETRINI, L.J.; KREIN, T.; GREGOLIN, C.; NEUNFELT, T.H.; LOHMANN, T.R.; STANGARLIN, J.R. (2007) Utilização de leveduras para controle biológico de podridão em morango. In: Encontro Anual de Iniciação Científica, XVI.
MARUYAMA, T.; PARK, H.; OZAWA, K.; TANAKA, Y.; SUMINO, T.; HAMANA, K.; HIRAISHI, A.; KATO, K. (2006) Sphingosinicella microcystinivorans gen. nov., sp. nov., a microcystin-degrading bacterium. International
Journal of Systematic and Evolutionary Microbiology, v. 56, n. 1, p. 85-89.
NYBOM, S.M.K.; SALMINEM, S.J.; MERILOUTO, J.A.O. (2007) Removal of microcystin-LR by strains of metabolically active probiotic bacteria.
FEMS Microbiology Letters, v. 270, n. 1, p. 27-33.
OLIVEIRA-BITTENCOURT, M.C.; MOLICA, R. (2003) Cianobactéria invasora. Revista Biotecnologia Ciência e Desenvolvimento, n. 30, p. 82-90. Disponível em: < http: www.biotecnologia.com.br/revista/bio30/ cianobacteria.pdf>.
TSUJI, K.; ASAKAWA, M.; ANZAI, Y.; SUMINO, T.; HARADA, K. (2006) Degradation of microcystins using immobilized microorganism isolated in a eutrophic lake. Chemosphere, v. 65, n. 1, p. 117-124.
WANG, J.; CHEN, C. (2006) Biosorption of heavy metals by
Saccharomyces cerevisiae: a review. Biotechnology Advances, v. 24,
Errata
Potencial de biodegradação de microcistinas por microrganismos
Página 185, onde se lê:
Figura 2 – Degradação de microcistinas pela bactéria B9 e seis cepas de leveduras utilizando
extrato de Microcystis sp contendo microcistinas.
Microcystis sp x Leveduras
Concentração de microcistinas
(µg.L-1)
4000 3500 3000 2500 2000 1500 1000 500 0
B9 - I B9 - J L1 - I L1 - J L2 - I L2 - J L3 - I L3 - J L4 - I L4 - J L5 - I L5 - J L6 - I L6 - J
96 horas 0 hora
Figura 3 – Degradação de microcistinas pela bactéria B9, quatro cepas de bactérias probióticas e kefir
utilizando extrato de Microcystis sp contendo microcistinas.
Microcystis sp x Bactérias pró-bióticas
Concentração de microcistinas (µ g.L
-1) 4000
3500 3000 2500 2000 1500 1000 500 0
B9 - I B9 - J P1 - I P1 - J P2 - I P2 - J P3 - I P3 - J P4 P5 - I P5 - J
96 horas 0 hora
Leia-se:
Microcystis sp x Leveduras
Concentração de microcistinas
(µg.L-1)
4000 3500 3000 2500 2000 1500 1000 500 0
B9 - A B9 - B L1 - A L1 - B L2 - A L2 - B L3 - A L3 - B L4 - A L4 - B L5 - A L5 - B L6 - A L6 - B
96 horas 0 hora
Figura 2 – Degradação de microcistinas pela bactéria B9 e seis cepas de leveduras utilizando
extrato de Microcystis sp contendo microcistinas.
Microcystis sp x Bactérias próbióticas
Concentração de microcistinas (µ g.L
-1) 4000
3500 3000 2500 2000 1500 1000 500 0
B9 -A B9 - B P1 - A P1 - B P2 - A P2 - B P3 - A P3 - B P4 P5 - A P5 - B
96 horas 0 hora