UNIVERSIDADE ESTADUAL PAULISTA “JÚLIO DE MESQUITA FILHO”
FACULDADE DE CIÊNCIAS AGRONÔMICAS
CAMPUS DE BOTUCATU
AVALIAÇÃO DE DESEMPENHO DE FIBRAS LIGNOCELULÓSICAS
NA SORÇÃO DE ÓLEOS DIESEL E BIODIESEL
ADRIANA FERLA DE OLIVEIRA
BOTUCATU – SP Novembro – 2010
UNIVERSIDADE ESTADUAL PAULISTA “JÚLIO DE MESQUITA FILHO”
FACULDADE DE CIÊNCIAS AGRONÔMICAS
CAMPUS DE BOTUCATU
AVALIAÇÃO DE DESEMPENHO DE FIBRAS LIGNOCELULÓSICAS
NA SORÇÃO DE ÓLEOS DIESEL E BIODIESEL
ADRIANA FERLA DE OLIVEIRA
Orientador: Prof. Dr. Alcides Lopes Leão Co-Orientador: Prof. Dr. José Cláudio Caraschi
BOTUCATU – SP Novembro – 2010
DEDICO
AGRADECIMENTO
Aos meus pais, Bernardino e Nely, pelo amor e compreensão em todos os momentos da minha vida e por sempre acreditar em min.
Ao meu irmão Bernardo por sempre estar do meu lado.
A meu esposo Luciano Caetano de Oliveira pela colaboração neste trabalho.
Ao meu sogro e sogra Ailton e Vera pelo carinho e auxílio durante o doutorado.
Ao meu orientador Prof. Dr. Alcides Lopes Leão pela orientação e amizade.
Ao meu co-orientador Prof. Dr José Cláudio Caraschi pelas sugestões e contribuições neste trabalho.
Ao meu tio Adilson pelo auxilio e amizade.
As professoras Maria Márcia Sartori e Margarida Juri Saeki pelas sugestões e contribuições no exame de qualificação.
Ao meus amigos e colegas Evaristo, Joyce, Humberto, Sivoney, Vitor, Matheus pela amizade e grande ajuda no desenvolvimento do trabalho.
Ao técnico de laboratório Diego do Laboratório de Resíduos Sólidos e Compósitos pela amizade e auxílio neste trabalho.
A todos os Professores da Pós-graduação em Agronomia – Energia na Agricultura pela contribuição em minha formação.
Aos funcionários do Departamento de Ciências Ambientais.
Aos funcionários do Programa de pós-graduação.
Aos colegas professores da UFPR - Campus Palotina, Helton José Alves, Suzana Stefanello, Patrícia da Costa Zonetti e Carina Kozera pela colaboração no decorrer desta pesquisa.
Aos técnicos de laboratório Éderson e Sandonaid da UFPR - Campus Palotina pelo auxílio com as imagens de microscopia.
Ao técnico de laboratório Cleber Moretti da UFSCar pelas imagens de MEV.
Ao Sr. Martinho (CETESB - Botucatu-SP) pela atenção e informações prestadas.
SUMÁRIO
Página
LISTA DE ABREVIATURAS... X LISTA DE SIMBOLOS... XI LISTA DE FIGURAS... XII LISTA DE TABELAS... XIV RESUMO... XV SUMARY... XVII
1 INTRODUÇÃO... 1
2 REVISÃO DA LITERATURA... 4
2.1 Óleo Diesel... 4
2.1 BioDiesel... 5
2.3 Derramamento de óleo... 6
2.4 Sorventes... 7
2.5 Fibras Vegetais Comerciais... 9
2.5.1 Coco ... 11
2.5.2 Curauá ... 12
2.5.3 Turfa ... 14
2.6 Materiais Vegetais Não Comerciais... 15
2.6.1 Paina... 15
2.6.2 Macrófitas Aquáticas ... 17
2.6.2.1 Taboa... 15
2.6.2.2 Aguapé... 19
3 MATERIAIS E MÉTODOS... 21
3.1 Materiais... 21
3.1.1 Biosorventes... 21
3.1.2 Óleos Combustíveis... 22
3.2 Métodos... 22
3.2.1 Coleta e Preparação dos Biosorventes... 22
3.2.2.1 Determinação do Teor de Umidade... 24
3.2.2.2 Determinação do Teor de Cinzas... 24
3.2.2.3 Preparo das Amostras para Determinação do Teor de Lignina e Holocelulose... 25
3.2.2.4 Determinação de Lignina... 25
3.2.2.5 Teor de Holocelulose... 26
3.2.2.6 Teor de Celulose... 26
3.2.2.7 Teor de Hemecelulose... 27
3.2.2.8 Teor de Gordura... 27
3.2.2.9 Análise Elementar... 28
3.2.2.10 Densidade Aparente das Fibras... 28
3.2.2.11 Classificação Granulométrica... 28
3.2.2.12 Hidrofobicidade das Fibras... 29
3.2.2.13 Testes de Flutuabilidade ... 29
3.2.2.14 Análise Termogravimétrica – TGA... 30
3.2.2.15 Microscopia Eletrônica de Varredura - MEV... 30
3.2.2.16 Microscopia Óptica... 31
3.2.2.17 Método para Determinação do Poder Calorífico Superior (PCS), Inferior (PCI) e Útil (PCU) ... 31
3.3 Ensaios de Sorção... 32
3.3.1 Ensaios em Sistema Seco... 33
3.3.2 Ensaios em Sistema Estático... 35
3.3.3 Ensaios em Sistema Dinâmico... 35
3.3.4 Determinação da Água Sorvida pelos Biosorventes... 36
3.4 Análise Estatística... 36
4 RESULTADOS E DISCUSSÕES... 38
4.1 Caracterização Físico-Química dos Biosorventes... 38
4.2 Sorção de Óleo em Sistema Seco ... 46
4.3 Sorção de Óleo em Diferentes Sistemas (Seco, Estático e Dinâmico)... 65
4.4 Caracterização Microscópica dos Biosorventes... 73
4.6 Análise Energética dos Biosorventes... 84
5 CONCLUSÕES... 86
6 REFERÊNCIAS BIBLIOGRÁFICAS... 88
LISTA DE ABREVIATURAS
Aguapé ID - Aguapé inteiro Diesel Aguapé IB - Aguapé inteiro Biodiesel ANP - Agência Nacional do Petróleo
ASTM - American Society Testing Materials B - Biodiesel
BIOPAR - Bioenergia do Paraná D - Diesel
ECOSORB - Empresa que comercializa a turfa como biosorvente EPA - Environmental Protection Agency
Eq. - Equação
G1 - Granulometria ≤180μm G2 - Granulometria 180-424μm G3 - Granulometria 425-850μm G4 - Granulometria 850-3350μm
ITOPF - The International Tankers Owner Pollution Federal Limited MEV - Microscopia Eletrônica de Varredura
PETROBRAS - Petróleo Brasileiro S.A PCS – Poder Calorífico Superior PCI – Poder Calorífico Inferior PCU – Poder Calorífico Útil Taboa ID - Taboa inteira Diesel Taboa IB - Taboa inteira Biodiesel
LISTA DE SÍMBOLOS
μm - Micrometro °C - Graus Celsius mL - Mililitro g - Grama
rpm - Rotação por minuto min - Minutos
kJ/kg - Kilojoule por kilograma %C - Teor de Carbono
LISTA DE FIGURAS
Página
Figura 2.1 - Fibra de Coco... 12
Figura 2.2 – Curauá... 13
Figura 2.3 - Fibra de Curauá... 13
Figura 2.4 - Turfa ... 14
Figura 2.4 - Paineira (Ceiba speciosa St. Hil.) ... 15
Figura 2.5 - Fruto verde da paineira... 16
Figura 2.6 - Fruto maduro e a paina... 16
Figura 2.7 – Taboa (Typha dominguensis) ... 18
Figura 2.8 - Aguapé (Eichhornia crassipes) ... 19
Figura 3.1 – Biosorventes Utilizados ... 22
Figura 3.2 – Sistema Seco ... 34
Figura 3.3 – Sistema de Filtração ... 34
Figura 3.4 – Sistema Estático ... 35
Figura 3.5 – Sistema Dinâmico ... 36
Figura 4.1 – Distribuição granulométrica para os biosorventes (% massa)... 42
Figura 4.2 – Valores médios de sorção de diesel e erro padrão em relação à granulometria para os biosorventes; Coco, Curauá e Turfa... 50
Figura 4.3 - Valores médios de sorção de diesel em relação à granulometria e tempo de exposição para os biosorventes Coco, Curauá e Turfa... 51
Figura 4.4 - Valores médios de sorção de biodiesel e erro padrão em relação à granulometria para os biosorventes; Coco, Curauá e Turfa... 52
Figura 4.5 - Valores médios de sorção de biodiesel em relação à granulometria e tempo de exposição para os biosorventes Coco, Curauá e Turfa... 54
Figura 4.6 - Valores médios de sorção de diesel e erro padrão em relação à granulometria para os biosorventes; Taboa inteira, Taboa aérea e Turfa... 55
Figura 4.7 - Valores médios de sorção de diesel em relação à granulometria e tempo de exposição para os biosorventes Taboa inteira, Taboa aérea e Turfa.... 57
Figura 4.9 - Valores médios de sorção de biodiesel em relação à granulometria e tempo de exposição para os biosorventes Taboa inteira, Taboa aérea e
Turfa... 59
Figura 4.10 - Valores médios de sorção de diesel e erro padrão em relação à granulometria para os biosorventes; Aguapé inteiro, Aguapé aérea, Aguapé raiz e Turfa... 60
Figura 4.11 - Valores médios de sorção de diesel em relação à granulometria e tempo de exposição para os biosorventes; Aguapé inteiro, Aguapé aérea, Aguapé raiz Turfa... 61
Figura 4.12 - Valores Médios de sorção de biodiesel e erro padrão em relação à granulometria para os biosorventes Aguapé inteiro, Aguapé aérea, Aguapé raiz Turfa... 63
Figura 4.13 - Valores médios de sorção de biodiesel em relação à granulometria e tempo de exposição para os biosorventes Taboa, Curauá e Turfa... 64
Figura 4.14 – Valores médios de sorção de diesel em relação ao tempo de exposição e sistema para os biosorventes Paina, flor da Taboa e Turfa... 66
Figura 4.15 - Valores médios de sorção de biodiesel em relação ao tempo de exposição e sistema para os biosorventes Paina, flor da Taboa e Turfa. ... 69
Figura 4.16 - Valores médios de sorção de diesel em relação ao tempo de exposição e sistema para os biosorventes Aguapé inteiro, Taboa inteira e Turfa... 70
Figura 4.17 - Valores médios de sorção de biodiesel em relação ao tempo de exposição e sistema para os biosorventes Aguapé inteiro, Taboa inteira e Turfa. ... 71
Figura 4.18 – Imagens em Microscopia Eletrônica de Varredura - MEV... 76
Figura 4.19 – Imagens em Microscopia Óptica. ... 77
Figura 4.20 - Comportamento Termogravimétrico da fibra de Coco... 78
Figura 4.21 - Comportamento Termogravimétrico da fibra de Curauá... 79
Figura 4.22 - Comportamento Termogravimétrico para a Paina... 80
Figura 4.23 - Comportamento Termogravimétrico da flor da Taboa... 80
Figura 4.24 - Comportamento Termogravimétrico da Taboa inteira... 81
Figura 4.25 - Comportamento Termogravimétrico do Aguapé inteiro... 82
LISTA DE TABELAS
Página
RESUMO
distintas, que influenciam na sorção de óleo, seja por absorção ou adsorção. Os biosorventes investigados apresentaram capacidade de sorção de diesel e biodiesel semelhante ou superior ao sorvente comercial à base de turfa. As fibras de coco e curauá, devido à baixa flutuabilidade, mostram-se adequadas somente para sorção destes óleos em superfícies sólidas. As macrófitas aquáticas mostraram ser eficientes na sorção dos óleos nos três sistemas, assim como a paina que apresentou o melhor desempenho se comparada a todas as outras. A determinação do poder calorífico dos biosorventes mostra que estes podem ser utilizados na geração de energia antes e após serem utilizados como sorventes. Desta forma, esses materiais poderão ser empregados após estudos de viabilidade econômica neste setor e ainda incrementar a economia de regiões onde estes são abundantes.
_______________________
PERFORMANCE EVALUATION OF THE LIGNOCELLULOSIC FIBERS IN THE SORPTION OF DIESEL AND BIODIESEL OILS. Botucatu, 2010. 98p.
Tese (Doutorado em Agronomia/Energia na Agricultura) – Faculdade de Ciências Agronômicas, Universidade Estadual Paulista.
Author: ADRIANA FERLA DE OLIVEIRA Adviser: ALCIDES LOPES LEÃO
SUMMARY
similar or higher to the commercial sorbent made of peat. The coir and curauá fibers, due to the low buoyancy, were shown appropriated only for sorption of the oils in the three systems, as well as the silk floss, which presented the best performance when compared to the others. The determination of the calorific power of the biosorbents shows that they can be used for energy generation before and after they are used as sorbents. This way, those materials can be used after studies of economical viability in this sector and still to increase the economy of the areas where they are abundant.
_____________________
1 INTRODUÇÃO
A preocupação mundial com as questões ambientais tem aumentado consideravelmente nos últimos anos, não só no sentido a minimizar os efeitos causados pela poluição, mas na busca de meios alternativos e eficientes para recuperação de locais afetados. A iniciativa em buscar essas soluções, parte não somente de órgãos governamentais, mas também de organizações ambientais e institutos de pesquisa.
Derramamentos de óleo na terra e na água são uma preocupação para todos os países do mundo. Poluição por petróleo e seus derivados não representam somente uma perda física de material, produzem também efeitos negativos para a fauna, a flora e a vida humana, afetando a economia, turismo e laser devido às propriedades destes materiais (LIM; HUANG, 2007b, ANNUNCIADO et al., 2005).
Para combater estes derramamentos processos físicos, químicos e biológicos podem ser usados para remover ou recuperar o óleo em situ (SALANITRO et al., 1997; RIBEIRO et al., 2000). Um grande problema é que os estados e municípios raramente estão preparados e equipados para enfrentarem esta situação. Os órgãos que estão diretamente envolvidos nas ações de atendimento emergencial de acidentes com produtos perigosos são o Corpo de Bombeiros e os órgãos de meio ambiente.
empregadas, a magnitude dos danos evitados e a disponibilidade dos recursos necessários são alguns dos parâmetros importantes para a avaliação da eficácia de um atendimento emergencial (GOUVEIA; NARDOCI, 2007).
No caso específico de derramamento de óleo emprega-se geralmente material sorvente, podendo este ser de origem natural ou sintética (CHOI; CLOUD, 1992; LEE et al., 1999; TEAS et al., 2001). As fibras vegetais (fibras lignocelulósicas e resíduos agrícolas) são ecologicamente mais amigáveis que os sorventes sintéticos podendo apresentar maior capacidade de sorção a um baixo custo (ANNUNCIADO et al., 2005).
Algumas plantas aquáticas apresentam alternativa para o tratamento de águas poluídas através da técnica da fitorremediação e do aproveitamento da biomassa seca como sorventes naturais (HERY-SILVA; CAMARGO, 2002). Quando o meio aquático em que vivem é rico em nutrientes (nitrogênio e fósforo), apresentam uma fantástica capacidade de reprodução (GENTELINI, 2007). Nessas situações, são consideradas infestantes e nocivas, pois obstruem rios, lagos e represas, impedindo a navegação e alterando o ecossistema aquático. Esta biomassa abundante é aproveitada na produção de papel, alimentação animal, na produção de biogás e na fertilização de solos (HERY-SILVA; CAMARGO, 2002). Após seca e moída, a macrófita Salvinia herzoggi mostrou-se eficiente na sorção de óleo cru puro, em sistemas hídricos e como filtro (RIBEIRO et al., 2000; RIBEIRO et al., 2003).
Muitos são os trabalhos que relatam à capacidade de sorção de óleo cru, mas poucos descrevem a sorção de óleos menos viscosos como o diesel. Com o incentivo à produção de biocombustíveis, em especial o biodiesel, produto que vem para competir diretamente com o diesel de origem fóssil, é interessante que metodologias que visem remediar acidentes com o diesel também sejam testadas com o biodiesel. O estudo comparativo de metodologias de combate à poluição para os dois combustíveis poderá servir para aplicação em situação que venha a acontecer e como um incentivo à produção do biocombustível já que estes são menos nocivos ao ambiente.
Portanto, os objetivos desse trabalho são:
• Avaliar a capacidade sorvente das fibras vegetais coco (Cocos
nucifera) e curauá (Ananas erictifolius), paina (Ceiba speciosa) as macrófitas aquáticas taboa
(Typha sp.), o aguapé (Eichhornia crassipes) e a turfa frente aos óleos combustíveis diesel e biodiesel;
• Verificar a sorção de óleo diesel e biodiesel pelos biosorventes em sistema seco; em água doce, sendo que este com e sem agitação (sistema dinâmico e estático);
• Determinar para os biosorventes as características físico-químicas e energéticas.
2 REVISÃO BIBLIOGRÁFICA
2.1 Óleo Diesel
Segundo a Agência Nacional do Petróleo (ANP), óleo diesel é definido como: “Fração do petróleo composta principalmente por hidrocarbonetos alifáticos". O óleo diesel é ligeiramente mais denso do que o querosene e destila na faixa entre 250 e 400ºC. É usado como combustível em motores de combustão interna, nos quais a ignição ocorre pelo aumento de temperatura ao invés de faiscação. Os óleos diesel são classificados em: interior, metropolitano e marítimo (ANP, 2008).
Acidentes com óleo diesel no ambiente, constituem um evento comum e, muitas vezes, uma ocorrência de grandes proporções (GAO et al., 2000). O óleo diesel não é apenas fisicamente prejudicial para o ambiente, mas também quimicamente prejudicial, porque contém muitos compostos tóxicos em concentrações relativamente grandes (SALANITRO et al., 1997).
de 2004. Dentre essas emergências destaca-se que 19% dos acidentes ocorreram com o óleo diesel (CETESB, 2005).
2.2 Biodiesel
Segundo Shay (1993 apud FANGRUI; HANNAB, 1999) “Há cem anos atrás, Rudolf Diesel testou óleo vegetal como combustível em motores”. No entanto, com o advento do petróleo barato, frações de óleo cru foram refinadas para servir como combustível. Um dos combustíveis derivados do petróleo largamente utilizados em motores foi o óleo diesel o que ocasionou uma evolução considerável na tecnologia dos motores a diesel. Em 1930 e 1940 os óleos vegetais foram usados novamente como combustível, mas em geral em situações de emergência.
Devido aos altos preços do óleo cru, reservas limitadas de óleo fóssil e preocupação ambiental, novamente nos dias atuais os óleos vegetais e agora também gorduras animais tornam-se objeto de estudo como combustíveis (FANGRUI; HANNAB, 1999). A diferença é que desta vez, o foco são estudos para produção de biodiesel a partir de óleos vegetais e gorduras animais e não sua utilização in natura.
O biodiesel no Brasil surgiu de um estudo de viabilidade conduzido por um Grupo Interministerial, coordenado pela Casa Civil da Presidência da República. A definição brasileira do biodiesel, ditada pela Agência Nacional de Petróleo, Gás Natural e Biocombustíveis (ANP), em sua resolução No 42, define o biodiesel como: “Combustível composto de alquilésteres de ácidos graxos de cadeia longa, derivados de óleos vegetais ou de gorduras animais, conforme especificação da ANP. RESOLUÇÃO Nº 7, DE 19.3.2008”. (ANP, 2008).
Desde 1º de janeiro de 2010, o óleo diesel comercializado em todo o Brasil contém 5% de biodiesel. Esta regra foi estabelecida pela Resolução nº 6/2009 do Conselho Nacional de Política Energética (CNPE), publicada no Diário Oficial da União (DOU) em 26 de outubro de 2009, que aumentou de 4% para 5% o percentual obrigatório de mistura de biodiesel ao óleo diesel (RESOLUÇÃO, Nº 6, 2009). A contínua elevação do percentual de adição de biodiesel ao diesel demonstra o sucesso do Programa Nacional de Produção e Uso do Biodiesel e da experiência acumulada pelo Brasil na produção e no uso em larga escala de biocombustíveis.
O Brasil está entre os maiores produtores e consumidores de biodiesel do mundo, com uma produção anual, em 2009, de 1,6 bilhões de litros e uma capacidade instalada, em janeiro de 2010, para cerca de 4,7 bilhões de litros (ANP, 2010).
Desta forma, além dos benefícios ambientais como, livre de enxofre e de compostos aromáticos, alto número de cetano, teor médio de oxigênio, maior ponto de fulgor, menor emissão de partículas: HC, CO e CO2, caráter não tóxico e biodegradável, (FERRARI et al., 2005) a produção de biodiesel proporcionará benefícios sociais como novos postos de trabalho em todas as etapas da cadeia produtiva.
2.3 Derramamentos de Óleo
A "era da propulsão mecânica", iniciada em 1887, com a invenção dos motores à explosão, passou a utilizar a gasolina e o diesel como combustível. A indústria petroquímica surgiu em 1930, possibilitando a utilização de derivados do petróleo como componentes de explosivos (glicerina e tolueno), matéria sintética para roupas, solventes e medicamentos entre outros, que tiveram muita utilidade na Segunda Guerra Mundial (1939-1945) e que são utilizados até hoje. Da década de trinta até os dias atuais, a indústria do petróleo vem crescendo progressivamente (CETESB, 2008).
700 toneladas). A maioria dos acidentes ocorridos (84%) estão na categoria “menor que 7 t” (ITOPF, 2008).
O número de grandes vazamentos (>700 t) tem diminuído nos últimos trinta anos e a maioria dos acidentes é de médio ou pequeno porte (ITOPF, 2008), mas considerando que médio a pequeno porte são quantidades de 7 a 700 t os impactos ambientais criados são bastante expressivos.
Segundo Lim e Huang (2007a) estes acidentes podem ser ocasionados por falha humana ou displicência, atos deliberados como vandalismo, guerras e despejo ilegal, ou por catástrofes naturais como furacões e terremotos. As águas da costa e da linha costeira podem ser poluídas por petróleo em operações de perfuração, acidentes envolvendo petroleiros, escoamentos na exploração e produção, e derrames em operações de carregamento e de descarregamento (LIM; HUANG, 2007b).
Os óleos que são encontrados em águas contaminadas não são exclusividade do setor petroleiro e seus derivados como óleo cru, óleo diesel, e hidrocarbonetos leves como querosene, combustível de injeção e gasolina, podem ser também gorduras de origem vegetal e animal. As principais fontes industriais de resíduos oleosos incluem refinarias; indústria metal/mecânica e usinagem; e processadores de alimentos e as fontes de óleo em águas residuais municipais são de cozinha e resíduos humanos (SRINIVASAN; VIRARAGHAVAN, 2008).
Resíduos de óleo na água podem existir na forma livre, dispersa ou emulsificada. Métodos convencionais como separação por gravimetria, dissolução por flotação, coalescência, centrifugação, floculação e coagulação, muitas vezes não removem o óleo efetivamente ou a relação custo benefício não compensa a operação, pois alteram as características do óleo derramado (SRINIVASAN; VIRARAGHAVAN, 2010).
2.4 Sorventes
sorção é um termo geral utilizado para designar os processos de adsorção e absorção (TANOBE et al., 2007).
A adsorção envolve a acumulação entre fases ou a concentração de uma determinada substância ou classe de compostos em uma superfície ou interface e é um processo que está baseado na afinidade química entre o sorvente e sorvato através de uma grande área específica (WEBER et al., 1991). Portanto, adsorção é um processo de separação no qual certos componentes de uma fase fluída são seletivamente transferidos para a superfície de um sólido. Por outro lado, a absorção ocorre principalmente por ação da capilaridade e mecanismos de sucção nas operações envolvendo remoção de óleo por sorventes porosos (RIBEIRO et al., 2000).
A Agência de Proteção Ambiental (Environmental Protection Agency – EPA) dos Estados Unidos define absorventes como materiais que captam e retém o líquido de forma distribuída através da sua estrutura molecular causando um inchamento do sólido em 50% do seu volume inicial ou mais quando exposto a pelo menos 70% de excesso do fluido. Adsorventes são materiais insolúveis que são cobertos pelo líquido, por exemplo óleo na sua superfície, incluindo poros e capilares, sem o inchamento do sólido quando exposto em excesso de líquido acima de 50% (EPA, 2008).
A hidrofobicidade e a oleofilicidade são os fatores primários determinantes do sucesso dos sorventes. Outros fatores importantes incluem a retenção de óleo por longo período de tempo, quantidade de óleo sorvido por unidade de peso do sorvente e a reutilização e biodegradabilidade do sorvente (TEAS et al., 2001).
Segundo Rajakovic-Ognjanovic et al. (2008), a sorção, no estágio de tratamento de água poderia ser eficiente, não somente para a remoção de óleo, mas também, para remover todas as substâncias que possuem afinidade física (adsorção) ou química (quimisorção) por influência dos grupos ativos presentes nos sorventes. Devido às características multifuncionais dos sorventes, também são aplicados em vários estágios do tratamento de águas residuárias oleosas, com equipamentos adicionais no tratamento.
Segundo Melvold et al. (1988 apud, CHOI; CHOUD, 1992), os produtos minerais incluem perlita, vermiculitas, argila adsorvente e diatomita. Esses materiais não mostram suficiente flutuabilidade e retenção de óleo, sendo a capacidade de sorção geralmente baixa.
Fibras sintéticas como polipropileno, poliéster e poliamida (náilon) são largamente usadas como sorventes de óleo. No entanto, o uso de biodegradáveis ou resíduos agrícolas como sorventes de óleo ou filtros são uma alternativa preferível. Várias fibras biodegradáveis têm sido estudadas em pesquisas recentes para aplicação na limpeza em derramamentos de óleo e como filtros (LIM; HUANG, 2007a).
Segundo World Catalogue of Oil Spill Response Produts (1997/1998 apud SAITO et al., 2003) existe uma certa evolução na taxa sorção para os sorventes orgânicos. Para a sorção de óleo por fibras em geral, considera-se nos tempos de 5 minutos que a sorção é baixa, 5 - 10 minutos razoável e acima 10 minutos é boa.
Erva-de-leite (milkweed) e o algodão mostraram absorver significativamente mais óleo quando comparadas a materiais sorventes sintéticos comerciais (CHOI; CLOUD, 1992). Segundo Varghese e Cleveland (1998 apud LIM; HUANG, 2007b) filtros de quenafe (kenaf) podem remover do meio 70–95% de óleo estabilizado por surfactantes e emulsão de óleo na água. Deschamps et al. (2003) usaram algodão como um filtro para remover a camada de óleo na água deixando o efluente quase livre do óleo. Pasila (2004) estudou palheta alpista, fibra de linho e cânhamo e constatou que os materiais fibrosos foram capazes de separar óleo de água durante a filtração de água oleosa. A planta aquática salvinia, mostrou-se excelente na separação do óleo da água (RIBEIRO et al., 2003). Annunciado, et al. (2005) avaliaram a sorção de óleo cru pela paina mostrando absorver 85g de óleo cru/g de fibra.
2.5 Fibras Vegetais Comerciais
não surpreende, pois o mundo passa por um momento onde se busca utilizar ao máximo os recursos naturais e desenvolver novos processos e produtos (SATYANARAYANA et al., 2007).
Segundo Kozlowski (2004, apud SATYANARAYANA et al., 2007) entre tais recursos estão os materiais de lignocelulosicos, dos quais aproximadamente 2,5 bilhões de toneladas estão disponíveis e que foram usados desde 6000 a.c. Fibras estão disponíveis em muitos destes materiais, sendo também chamadas de plantas fibrosas, fibras naturais ou fibras vegetais.
As fibras lignocelulósicas são constituídas principalmente por três macromoléculas, um polifenol, a lignina, e dois polissacarídeos, a celulose e as hemiceluloses.
A celulose é o principal constituinte dos organismos vegetais, embora também seja encontrada em alguns organismos do reino animal, é considerado o mais abundante composto orgânico natural, sendo o principal componente da parede celular dos vegetais (NELSON; COX, 2006). Raramente ocorre na natureza no estado puro, mas é encontrada geralmente, misturada com ligninas, hemiceluloses, pectina, etc. A celulose é um homopolissacarídeo formado por unidades do monossacarídeo β-D-glicopiranose unidas por ligações glicosídicas do tipo β-(1→4), sendo a unidade repetitiva a celobiose (SOLOMONS; FRYHLE, 2002).
A medida que a densidade de empacotamento da celulose aumenta, re-giões cristalinas são formadas (MARTIM et al., 2009). Portanto, pode-se dizer que o aumento do índice de cristalinidade refere-se ao aumento da quantidade de celulose ao longo da fibra.
Em adição a estrutura cristalina, celulose contém áreas amorfas, não cristalinas, onde a estrutura ordenada inexiste. Esta composição, somada as irregularidades observadas nas cadeias cristalinas, tal como curvaturas que aumentam sua superfície, atribuem característica paracristalina a estrutura (Desvaux, 2005).
nas madeiras moles (gimnospermas) varia de 15 a 29% e nas gramíneas este conteúdo varia de 25 a 50% (FENGEL; WEGENER, 1984; D’ALMEIDA, 1988).
A grande quantidade de grupos hidroxila presente na celulose e nas hemiceluloses, confere propriedades hidrofílicas às fibras lignocelulósicas.
Os monossacarídeos que constituem as hemiceluloses podem ser divididos em quatro grupos principais: as pentoses, as hexoses, os ácidos hexurônicos e as desoxihexoses (FENGEL; WEGENER, 1984; D’ALMEIDA, 1988).
A lignina pode ser definida como uma macromolécula aromática altamente ramificada, amorfa, possuindo um grande número de grupamentos funcionais variados, de estrutura química muito complexa, baseada na unidade fenilpropânica (NELSON; COX, 2006).
2.5.1 Coco
O coqueiro (Cocos nucifera) é uma árvore da espécie Arecaceae, família Palmae, e seu fruto um produto industrial valioso em países tropicais (CHAKRABORTY et al., 2009).
Figura 2.1 - Fibra de Coco.
Grande quantidade de água de coco e produtos derivados do coco são produzidos e consumidos no Brasil e em muitos países. De acordo com dados oficiais são produzidos anualmente 6,7 milhões toneladas de resíduos de coco (casca). A casca é constituída principalmente de lignina e celulose (RODRIGUES et al., 2008).
O desenvolvimento de alternativas de aproveitamento de cascas de coco possibilita a redução da disposição de resíduos sólidos em aterros sanitários e proporciona uma nova opção de rendimento junto a sítios de produção (JÚNIOR, 2007).
2.5.2 Curauá
Figura 2.2 – Curauá (Ananas erictifolius).
O curauá não necessita de solos muito ricos, podendo ser plantado em solos de textura arenosa. Cada planta produz cerca de 24 folhas e o rendimento de fibra seca é de aproximadamente 6%. Um hectare produz 3.600 quilos de fibra seca (Figura 2.3) ao ano, embora esses valores variem bastante.
Figura 2.3 - Fibra de Curauá.
A composição química para o curauá é de 73.6% de celulose, 9.9% de hemiceluloses, 7,5 % de lignina e 0,9% de cinzas (CARASCHI; LEÃO, 2001).
2.5.3 Turfa
A turfa é uma substância fóssil, organo-mineral, originada da decomposição de restos vegetais, encontrada em áreas alagadiças como várzeas de rios, planícies costeiras e regiões lacustres (FRANCHI, 2004). Ela representa o estágio inicial da formação de carvão, originando-se da acumulação de matéria vegetal composta de musgos, plantas aquáticas diversas, material lenhoso, arbustos e líquens (Figura 2.4) (MORAES, 2001).
Figura 2.4 – Turfa.
O processo de decomposição da matéria orgânica ocorre em um ambiente ácido e de pouca oxigenação (PETRONI et al., 1999). A turfa contém, em geral, 90% ou mais de água e quando recolhida e seca ao ar, esse teor abaixa para valores médios próximos de 40% (MORAES, 2001). Do material seco possui acima de 70% de matéria orgânica em relação ao seu peso, podendo ser mais ou menos fibrosa, dependendo do grau de decomposição da matéria base (CANTHÉ, 2010).
Além do uso consagrado da turfa como fonte energética, observa-se, nos últimos anos, o incremento de sua utilização na agricultura, como insumo para produção de condicionadores de solos, biofertilizantes e substratos de mudas (SUFFERT, 1998). Nos últimos vinte anos, a turfa tem sido muito estudada, principalmente no Canadá, Estados Unidos e Europa, como alternativa tecnológica de utilização de um adsorvedor natural de baixo custo, aplicado ao tratamento de águas e efluentes contaminados por metais pesados e outras substâncias tóxicas (PETRONI et al., 1999).
2.6 Materiais Vegetais Não Comerciais
2.6.1 Paina
Paina é o nome dado aos tricomas (pêlos), comumente chamados de fibra e obtida dos frutos da paineira. Atualmente a paineira é chamada Ceiba speciosa A. St. -Hil. (Figura 2.4), sinônimo de Chorisia speciosa St. -Hil. (TROPICOS, 2010).
A paineira é uma grande árvore da família Malvaceae (Figura 2.5), (DUARTE, 2010) nativa da região tropical e subtropical da América do Sul (CARNEIRO-BELESKI et al., 2002). No hemisfério norte, até as Antilhas e o sul dos Estados Unidos (SOUZA et al., 2003). No Brasil ocorre em uma ampla área, que abrange, principalmente, as florestas mesófilas semidecíduas nos estados brasileiros de São Paulo, Minas Gerais, Goiás, Mato Grosso do Sul, Paraná, Santa Catarina e Rio Grande do Sul (FANTI; PEREZ, 2004).
Conhecida popularmente como paineira-rosa, paineira, árvore-de-paina, paina-de-seda, árvore-de-lã, barriguda, paineira-fêmea, paineira-de-espinho (CARNEIRO -BELESKI et al., 1999).
A espécie comumente apresenta 10 m a 15 m de altura e 30 cm a 60 cm de diâmetro à altura do peito (DAP - 1,3 m), podendo atingir 20 m a 30 m de altura e 120 cm de DAP (SOUZA et al., 2003).
As flores são hermafroditas e o fruto é uma cápsula oblonga deiscente (Figura 2.6). As sementes são envoltas por pêlos (paina) (Figura 2.7), que auxiliam a dispersão pelo vento. Cada árvore produz em média 300 a 700 frutos cada um com cerca de 120 a 200 sementes (ESPÉCIES ARBÓREAS BRASILEIRAS, 2010).
Figura 2.6 - Fruto verde da paineira.
Além da importância ecológica e ornamental, a madeira da paineira pode ser empregada na confecção de canoas, cochos, forros de móveis, na caixotaria e no fabrico de pasta celulósica (FANTI; PEREZ, 2004).
2.6.2 Macrófitas Aquáticas
Segundo Esteves, (1998) uma das primeiras menções às macrófitas aquáticas foi proposta por WEANER e CLEMENTS em 1938, que definiram, de maneira muito ampla, como plantas herbáceas que crescem na água, em solos cobertos por água ou em solos saturados com água. Macrófitas aquáticas é a denominação mais adequada para caracterizar vegetais que habitam desde brejos até ambientes totalmente submersos (isto é, debaixo d'água).
As macrófitas aquáticas são, em sua grande maioria, vegetais terrestres que, ao longo de seu processo evolutivo, adaptaram-se ao ambiente aquático; por isso apresentam algumas características de vegetais terrestres e uma grande capacidade de adaptação a diferentes tipos de ambientes, o que torna sua ocorrência muito ampla (TUNDISI; TUNDISI, 2008).
Segundo Esteves (1998), o fato das macrófitas aquáticas constituírem um grupo muito grande, elas são geralmente classificadas em cinco principais grupos, baseados em seu modo de vida (biótopo) no ambiente aquático. Esses grupos são:
a) Macrófitas aquáticas emersas: enraizadas no sedimento, porém as folhas crescem para fora da água. Ex: Typha, Pontederia, Echinodorus.
b) Macrófitas aquáticas com folhas flutuantes: enraizadas no sedimento e com folhas flutuando na superfície da água. Ex: Nymphaea, Vitoria e
Nymphoides.
d) Macrófitas aquáticas submersas livres: Permanecem flutuando submergidas na água. Podem se prender a pecíolos e caules de outras macrófitas. Ex:
Utricularia e Ceratophyllum.
e) Macrófitas aquáticas flutuantes: Flutuam livremente na superfície da água. Ex:.Eichhornia crassipes, Salvinia, Pistia.
2.6.2.1 Taboa
A taboa (Typha sp.) é uma espécie de água doce pertencente à família
Typhaceae, comumente conhecida como taboa, é uma planta perene, herbácea, rizomatosa,
aquática, com caule cilíndrico, podendo atingir até 3 m de altura, nativa da América do Sul (Figura 2.8). Sua inflorescência ocorre, mais ou menos, na altura das folhas, com longo pendúnculo provido de folhas caulinas e longa espiga terminal. As flores são masculinas no ápice e femininas na base (ALMEIDA et al., 2007).
Figura 2.8 – Taboa (Typha dominguensis).
Seus rizomas são comestíveis, possuindo valor protéico igual ao do milho e de carboidratos igual ao da batata (BIANCO et al., 2003). É uma espécie emergente cujas folhas são anfiestomáticas e apresentam grupos de fibras esclerenquimáticas por entre as células do parênquima paliçádico, logo abaixo da epiderme, e associados aos feixes.
É muito freqüente em margens de lagos, reservatórios, canais de drenagem e várzeas. Possui importância comercial, pois serve de matéria-prima para confecção de móveis e de celulose (KISSMANN; GROTH, 2000). Plantas de T. dominguensis absorvem metais pesados, inclusive o cobre, podendo contribuir para o saneamento ambiental. Indicada, também, como depuradora natural de ambientes aquáticos (GALLARDO-WILLIAMS et al., 2002).
2.6.2.2 Aguapé
O aguapé (Eichhornia crassipes) é uma planta aquática de flotação livre (Figura 2.9) originária da Amazônia na América do Sul. Hoje aparece em mais de 50 países nos cinco continentes em razão da sua utilização como planta ornamental pela beleza das suas flores (TAN et al., 2008).
Figura 2.9 - Aguapé (Eichhornia crassipes).
ambientes eutrofizados, o aguapé também tem a capacidade de remover metais pesados e outros contaminantes da água (GENTELINI et al., 2008). Contudo, durante sua senescência (período de envelhecimento da planta), os nutrientes absorvidos e metais pesados são liberados para o meio novamente, pelo seu processo de decomposição (ESTEVES, 1998).
3 MATERIAIS E MÉTODOS
3.1 Materiais
3.1.1 Biosorventes
As fibras vegetais selecionadas para os ensaios como biosorventes, coco (Cocos nucifera), (Figura 3.1) foram obtidas junto à empresa Sindifibras, Salvador-BA e a fibra de curauá (Ananas erictifolius) (Figura 3.1) foi obtida da empresa Poematec, Santarém-PA. A paina (Figura 3.1) foi coletada na Fazenda Experimental Edgardia – UNESP, Botucatu-SP.
As macrófitas aquáticas taboa (Typha sp.) e o aguapé (Eichhornia
crassipes) (Figura 3.1), também estudadas neste trabalho como biosorventes foram coletadas
no Setor de Aqüicultura da FMVZ - Faculdade de Medicina Veterinária e Zootecnia, localizada na Fazenda Experimental Lageado - UNESP, Botucatu-SP.
Figura 3.1 – Biosorventes Utilizados.
3.1.2 Óleos Combustíveis
O óleo diesel usado em todos os experimentos de sorção é comercial denominado como interior S1800, tendo sido adquirido em posto de combustível PETROBRAS, no município de Botucatu - SP. O biodiesel utilizado foi adquirido junto à empresa BIOPAR localizada no município de Rolândia - PR.
3.2 Métodos
As fibras de coco e curauá não necessitaram de coleta e preparação prévia uma vez que foram obtidas já desfibradas e secas.
A paina foi coletada de frutos secos das paineiras, posteriormente retiraram-se as sementes e acondicionou-se a fibra em sacos de polietileno.
As macrófitas aquáticas foram coletadas, lavadas com água corrente e em seguida foram drenadas naturalmente.
A macrófita taboa (Typha sp.) foi coletada cortando-se a planta próximo da raiz. No processo de preparação, uma parte da planta foi seca inteira e outra foi seca após separação da inflorescência do restante da planta (folhas e caule). A planta aguapé (E. crassipes) também foi seca inteira (parte aérea e raiz) e outra parte foi seca separadamente, parte aérea e raiz.
A secagem foi feita em estufa MARCONI, com circulação de ar à temperatura de 60 ºC até peso constante. Após seco o material foi armazenado em sacos de polietileno e guardado em local seco e arejado.
As amostras conforme preparadas foram submetidas à moagem em moinho de facas MARCONI, modelo MA-680.
Em seguida foram separadas em agitador de peneiras BERTEL, utilizando-se conjunto de peneiras com as respectivas aberturas: 3350 μm, 850 μm, 425 μm e 180 μm. O material classificado foi armazenado em sacos de polietileno, devidamente etiquetado em local seco e arejado.
3.2.2 Caracterização dos Biosorventes
3.2.2.1 Determinação do Teor de Umidade
O teor de umidade dos biosorventes foi determinado pelo método TAPPI 264 cm-97. Em uma balança com precisão de 0,0001 g e com o auxílio de um pesa filtro previamente tarado pesou-se aproximadamente 2 g de biomassa (m1). Após 4 h em estufa à temperatura de 103 ± 2 °C, levou-se o pesa filtro ao dessecador até atingir temperatura ambiente, pesando-o novamente (m2). O teste foi realizado em duplicata e o cálculo do teor de umidade foi realizado utilizando a equação:
Umidade (%) = [(m1 – m2)/m1]x100...(Eq. 1) Sendo:
m1 = massa da biomassa úmida (g) m2 = massa da biomassa seca (g)
3.2.2.2 Determinação do Teor de Cinzas
A determinação do teor de cinzas foi feita de acordo com a norma TAPPI T 211 om-93. Colocou-se o cadinho de porcelana na mufla sob tempertura de 525 ± 25 ºC por 30-60 minutos. Retirou-se o cadinho e, após esfriar em dessecador com sílica, pesou-se (m1) em balança analítica. Encheu-se o cadinho com 2 g de biomassa e deixou-se em estufa de um dia para o outro à temperatura de 103 ± 2° C. Após este tempo, retirou-se da estufa, deixou-o esfriar em dessecador com sílica e pesou-se (m2). Levaram-se os cadinhos para a mufla sob temperatura de 525 ± 25 ºC durante 3-5 h. Retirou-se da mufla e colocou-se em dessecador até temperatura ambiente e pesando-os (m3). Para as amostras de paina e flor da taboa, em razão do grande volume utilizaram-se para esta determinação as massas de 0,5 g e 1 g; respectivamente. O teste foi realizado em duplicata e o teor de cinzas foi determinado pela equação:
Sendo:
m1 = massa cadinho (g)
m2 = massa do cadinho + massa biomassa seca (g) m3 = massa do cadinho + massa de cinzas (g)
3.2.2.3 Preparo das Amostras para Determinação do Teor de Lignina e
Holocelulose
Para a determinação do teor de lignina pesou-se 1 g a.s. de amostra e para determinação do teor de holocelulose 2 g a.s. em cartuchos extratores de celulose. Extraiu-se em soxhlet com álcool-tolueno (1:2) durante 6 a 8 h. Substituiu-se a mistura de álcool-tolueno por álcool 96º e extraiu-se novamente durante 6 a 8 h. Removeu-se o saquinho do extrator e extraiu-se com água quente, por 1 h, 3 vezes. Deixou-se a amostra secar ao ar dentro do saquinho de papel de filtro durante 2 dias ou mais.
3.2.2.4 Determinação de Lignina
A determinação da lignina foi realizada empregando-se a norma TAPPI T222 om-98. Após a preparação prévia da amostra (3.2.2.3), transferiu-se toda a amostra do cartucho extrator de celulose para um béquer de 100 mL com 15 mL de H2SO4 72%, à temperatura de 18-20 ºC por 2 h homogeneizando periodicamente. Após 2 h, transferiu-se a amostra para erlenmeyer de 1 L usando 560 mL de água destilada mantendo em ebulição por 4 h, mantendo-se o volume de água constante. Após 4 h (sedimentação total da lignina), filtrou-se através de cadinho de vidro sinterizado (nº2) com auxilio de uma bomba à vácuo. Secou-se o cadinho em estufa a 103 ± 2 ºC, esfriou-se em dessecador e pesou-se. O teste foi realizado em duplicata e o teor de lignina foi determinado pela equação:
Sendo:
massa do resíduo = massa total - tara do cadinho
3.2.2.5 Teor de Holocelulose
A determinação da holocelulose foi realizada empregando-se a norma TAPPI T257 om-85. Transferiu-se toda a amostra preparada conforme 3.2.2.3, para um erlenmeyer de 125 mL e adicionaram-se 55 mL de água destilada, 3 mL de solução de clorito de sódio 20 % (NaClO2 20 %) e 2 mL de ácido acético (1:5). Colocou-se a amostra em banho termoestático a 70 ºC e a cada 45 minutos adicionaram-se mais 3 mL de NaClO2 e 2 mL de ácido acético, totalizando cinco adições. Após o último tratamento, filtrou-se através de cadinho de vidro sintetizado tarado de porosidade fina e lavou-se com 250 mL de água destilada. Secou-se em estufa, esfriou-se em dessecador e pesou-se. O teste foi realizado em duplicata e calculou-se a porcentagem de holocelulose através da expressão:
Holocelulose (%) = (massa do resíduo/2,0000)x100...(Eq. 4)
Sendo:
peso resíduo = peso total final – tara
3.2.2.6 Teor de Celulose
celulose em dessecador até massa constante. Determinou-se o teor de celulose a partir da seguinte expressão:
Celulose (%) = m1/m2x100...(Eq. 5)
Sendo:
m1 = massa de celulose seca (massa final do cadinho – tara) m2 = massa de holocelulose seca
3.2.2.7 Teor de Hemecelulose
Uma vez que, a holocelulose consiste na massa de celulose mais hemicelulose pode-se determinar a hemicelulose segundo a equação:
Hemicelulose (%) = Holocelulose (%) - Celulose (%)...(Eq. 6) Sendo:
Holocelulose (%) = Eq. 4 Celulose (%) = Eq. 5
3.2.2.8 Teor de Gordura
Para a determinação do teor de gordura, pesaram-se 2 g a.s. de amostra em cartuchos extratores de celulose (SILVA; QUEIROZ, 2002) Extraiu-se em soxhlet com éter de petróleo durante 6 a 8 h. Em seguida, destilou-se o éter presente no balão, secou-se o éter em estufa e pesou-se após esfriar em dessecador.
Gordura (%) = [(m3-m2)/m1]x100...(Eq. 7)
Sendo:
m2 = massa do balão
m3 = massa do balão + gordura
3.2.2.9 Análise Elementar
A caracterização das amostras quanto aos elementos carbono, hidrogênio e nitrogênio (C, H e N) foi realizada por análise elementar em equipamento Perkim Elmer CHN 2400, na Central Analítica do Instituto de Química da USP.
O teor de hidrogênio foi utilizado para determinação do Poder Calorífico Inferior (PCI)
3.2.2.10 Densidade Aparente das Fibras
Em uma balança com precisão de 0,0001 g e com o auxílio de uma proveta de 100 mL previamente tarada pesou-se a amostra do biosorvente. Calculou-se a densidade aparente dos biosorventes pela equação:
d = m/v... (Eq. 8)
d = densidade m = massa (g) v = volume (mL)
3.2.2.11 Classificação Granulométrica
h. Em seguida, pesou-se a massa correspondente a cada granulometria (m2) e calculou-se a porcentagem de cada fração presente na amostra.
Granulometria (%) = (m2x100)/m1...(Eq. 9)
Sendo:
m1 = massa inicial da amostra (g)
m2 = massa correspondente a granulometria (g) em cada peneira correspondente
3.2.2.12 Hidrofobicidade das Fibras
A hidrofobicidade dos biosorventes foi determinada empregando-se a metodologia descrita por Ribeiro et al. (2003). Pesou-se 1 ± 0,0001g de amostra (m1) em um béquer, em seguida adicionou-se 20 mL de água destilada sob agitação com bastão de vidro. Posteriormente adicionou-se 20 mL de hexano agitando-se por 3 minutos, seguido de repouso por 5 minutos. O material transferido para a fase orgânica foi retirado com um coletor, seco e pesado (m2). A hidrofobicidade foi calculada pela equação:
Hidrofobicidade (%) = (m2/m1)x100...(Eq. 10)
Sendo:
m1 = massa de amostra inicial (g)
m2 = material transferido para a fase orgânica (g)
3.2.2.13 Testes de Flutuabilidade
o sistema estático 2 ± 0,0001g de amostra foi imersa em uma coluna de água deionizada de 80 mm durante 15 minutos e a porção flutuante foi recolhida e calculada em relação à porção total. Para o sistema dinâmico 2 ± 0,0001g da amostra é colocada em uma coluna de 80 mm de água sob agitação (100 rpm) em agitador magnético durante 10 minutos e a porção flutuante é recolhida e calculada como no sistema estático. A flutuabilidade foi calculada seguindo a equação:
Flutuabilidade (%) = (m2/m1)x100...(Eq. 11) Sendo:
m1 = massa inicial m2 = massa flutuante
3.2.2.14 Análise Termogravimétrica – TGA
A análise termogravimétrica dos biosorventes foi realizada no Instituto de Química da USP, utilizando o analisador térmico NETZSCH TG 209 F1. A análise termogravimétrica foi conduzida em atmosfera de nitrogênio com uma taxa de aquecimento de 10 ºC/min. até 600 ºC com uma vazão de 100 mL/min.
3.2.2.15 Microscopia Eletrônica de Varredura - MEV
3.2.2.16 Microscopia Óptica
As amostras com melhor desempenho como sorventes foram analisadas em microscópio óptico Diag Tech, para se determinarem as características dos biosorventes após sorção do óleo. Este procedimento foi realizado no Laboratório de Microscopia da Universidade Federal do Paraná – Campus de Palotina.
3.2.2.17 Método para Determinação do Poder Calorífico Superior
(PCS), Inferior (PCI) e Útil (PCU)
As amostras utilizadas para análise do poder calorífico superior (PCS) foram moídas, secas e peneiradas em peneira ABNT 70, segundo norma ABNT – NBR 8633 e prensadas na forma de pastilhas com aproximadamente 1 ± 0,0001g cada uma e foram levadas em estufa a 103 ±2º C até a estabilização do peso, o que indica que a amostra está seca.
Após esse procedimento, as amostras foram novamente pesadas e queimadas em bomba calorimétrica ALEMMAR Modelo KL-5. A metodologia para obtenção do poder calorífico superior foi baseada no manual de instruções do calorímetro e adaptado segundo a norma ABNT-NBR 8633.
O calorímetro tem como unidade de calor kcal/kg, mas optou-se em transformar para kJ/kg (Sistema Internacional de Medidas), multiplicando-se os valores determinados nas equações para PCS, PCI e PCU por 4,18. A constante K da máquina utilizada foi determinada com ácido benzóico, sabendo-se previamente que o PCS do ácido benzóico é de 6318 kJ/kg. O valor obtido de K foi de 413,1228.
Para cada amostra de biosorvente testado determinou-se o poder calorífico superior médio, segundo a equação:
Sendo:
PCS = poder calorífico superior
K = constante do equipamento (413,1228) mH2O = massa de água (2700 g)
ΔT = variação de temperatura (ºC) m1 = massa seca (g)
O poder calorífico inferior (PCI) e o poder calorífico útil (PCU), foram determinados, segundo Brito (1993), segundo as equações descritas a seguir.
PCI = PCS-{600x[(9xH)/100]}...(Eq. 13)
PCU = PCIx{[(100- U)/100]- (6xU)...(Eq. 14)
Onde:
PCS = poder calorífico superior, determinado através de bomba calorimétrica PCI = poder calorífico inferior
PCU = poder calorífico útil H(%)= teor de hidrogênio U(%)= umidade do material
O PCI foi calculado com o material a 0% de umidade, e o PCU com as umidades determinadas (Eq. 1).
3.3 Ensaios de Sorção
Nos ensaios de sorção empregou-se metodologia semelhante à descrita por Lee et al. (1999).
3.3.1 Ensaios em Sistema Seco
Foi utilizado 0,5000 g da amostra, com a exceção da paina e da flor da taboa, onde empregou-se 0,1000 g devido ao grande volume ocupado. As amostras foram postas em contato com 20 g de óleo (aproximadamente 30 mL) de óleo (Figura 3.2) à temperatura de 20 a 25 0C durante tempos de 5, 10, 20, 40, 60 e 1440 minutos. Os materiais foram filtrados em filtro de náilon com abertura 60 mesh, com auxílio de um sistema de filtração QUIMIS por 1 minuto sob vácuo (Figura 3.3), em seguida pesados em uma balança digital analítica. Experimentos de sorção foram realizados para cada uma das fibras vegetais com três repetições. Para descontar qualquer óleo retido no filtro foram realizadas provas em banco em que o material sorvente foi substituído por pérolas de vidro, assim determinou-se a massa de óleo retida no filtro descontando-a da massa final. A sorção foi expressa em forma de quantidade de óleo sorvido por massa seca do material (m1) sorvente como mostra a equação:
S = (m2-m1-m3)/m1...(Eq. 15) Sendo:
S = sorção (g de óleo/g de sorvente seco)
Figura 3.2 – Sistema Seco.
Figura 3.3 – Sistema de Filtração.
3.3.2 Ensaios em Sistema Estático
Em um béquer contendo 80 mL de água destilada foram adicionados 20 g de óleo (Figura 3.4); em seguida as amostras foram adicionadas ao sistema e nos tempos de 5, 20, 60 e 1440 min. Após os tempos estabelecidos, as amostras foram filtradas e pesadas nas mesmas condições descritas no item 3.3.1.
Figura 3.4 – Sistema Estático.
3.3.3 Ensaios em Sistema Dinâmico
Figura 3.5 – Sistema Dinâmico.
3.3.4 Determinação da Água Sorvida pelos Biosorventes
3.4 Análise Estatística
O delineamento experimental utilizado para o sistema seco para cada grupo de biosorvente foi um fatorial 3X6X4, que consiste em três biosorventes, seis tempos de exposição, quatro granulometrias com três repetições cada. Exceto para o biosorvente aguapé, para o qual se utilizaram quatro biosorventes na análise.
Para análise dos sistemas para cada grupo de biosorvente, o delineamento experimental utilizado foi um fatorial 3X4X3 que consiste em três biosorventes, quatro tempos de exposição e três sistemas com três repetições cada. A variável resposta de ambas as análises foi sorção média de diesel e biodiesel.
4 RESULTADOS E DISCUSSÕES
4.1 Caracterização Físico-Química dos Biosorventes
Os biosorventes foram caracterizados quanto às suas propriedades químicas e físicas. Os resultados são apresentados nas Tabelas 4.1 a 4.4.
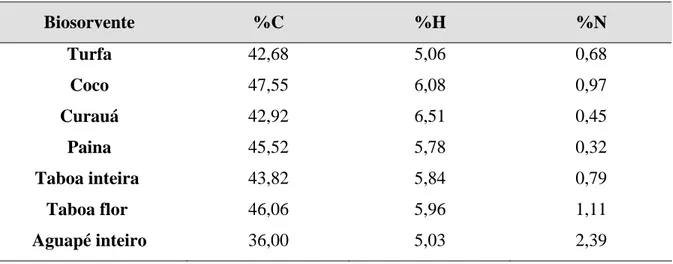
Os resultados da análise elementar do conteúdo de C, H e N para as amostras dos biosorventes (Tabela 4.1) mostram que, com exceção do aguapé inteiro, todos os biosorventes apresentam porcentagem de carbono em torno de 40%. Esses resultados são condizentes com a maior presença de cinzas (material mineral) no aguapé (Tabela 4.2).
não glicéricos, álcoois de cadeia longa, hidrocarbonetos e cetonas), esteróides e terpenos. Na decomposição dos lipídeos, triglicerídeos prontamente hidrolisam para ácidos graxos e glicerol, que é consumido pelos microorganismos como fonte de carbono e oxigênio. Os ácidos graxos residuais, ceras e esteróides persistem na turfa. A lignina constituída de compostos fenólicos de alta massa molar, é relativamente estável à decomposição, embora sejam decomponíveis em condições aeróbicas, em estruturas designadas quimicamente como ácidos húmicos.
Para os teores de nitrogênio, destaca-se que a paina apresentou o menor valor (0,32%), uma vez que os tricomas são formados de parede celular primária onde o teor de nitrogênio seria devido a estruturas celular. Destaca-se elevado teor de nitrogênio na inflorescência da taboa 1,11%. Para a inflorescência da taboa, como trata-se de aquênios de taboa (nome do fruto para esta espécie), existem reservas energéticas e protéicas, responsáveis diretas pelo teor de nitrogênio.
O aguapé inteiro apresentou o maior teor de nitrogênio 2,39%. Diversos estudos têm demonstrado que a composição química das diferentes partes das macrófitas aquáticas reflete a função da estrutura vegetal (ESTEVES; NOGUEIRA, 1991) e que ainda é provável existirem variações intraespecíficas, associadas às diferentes condições tróficas dos ambientes aquáticos, que podem influenciar nos conteúdos de nutrientes dos tecidos vegetais (ESTEVES, 1998).
Tabela 4.1 – Resultados da Análise Elementar (C, H, N) para os biosorventes (% massa).
Biosorvente %C %H %N
Turfa 42,68 5,06 0,68
Coco 47,55 6,08 0,97
Curauá 42,92 6,51 0,45
Paina 45,52 5,78 0,32
Taboa inteira 43,82 5,84 0,79
Taboa flor 46,06 5,96 1,11
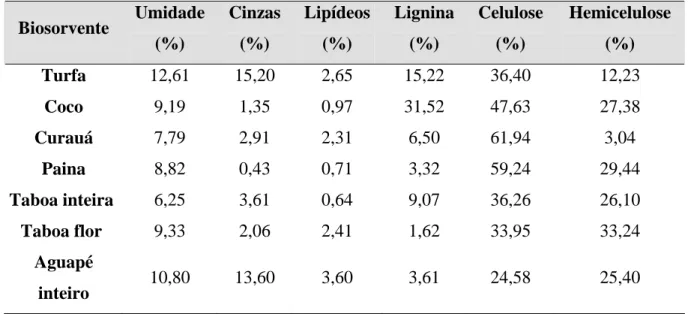
Na Tabela 4.2 são apresentados os valores da caracterização química dos biosorventes. Quanto ao teor de cinzas, Ribeiro et al. (2000) determinaram o teor de cinzas de 9,8% para o biosorvente à base de turfa, enquanto no presente estudo obteve-se o teor de cinzas de 15,20%. O teor de cinzas da turfa está relacionado com o conteúdo de argilo minerais presentes. A elevada quantidade de cinzas para a turfa deve-se à sílica presente nas turfeiras, como conseqüência das inundações periódicas do terreno. As turfas podem ser divididas em: turfa quase pura, com teores de cinza variando entre 10% e 15%; turfa impura ou argilosa, contendo teores de cinzas de 15% a 40%, e argilo-turfosa, quando o teor de argilo minerais se situa entre 40% e 70%, podendo coexistir em um mesmo local (MORAES, 2001).
Para o aguapé (E. crassipes), determinou-se um teor de cinzas de 13,6% para a planta inteira. Tan et al. (2008) quantificaram um teor de cinzas para a macrófita
E. crassipes de 21,16% (raízes) e 12, 72% (parte aérea), no entanto Scheneider e Rubio (1999)
determinaram para a planta inteira o teor de 20,3%, indicando que o teor de cinzas pode variar em razão de características do meio onde estas são coletadas e da preparação do material. Em especial para o teor de cinzas do aguapé (E. crassipes), pode-se atribuir a maior contribuição das raízes, uma vez que, como estas possuem a função de absorver nutrientes em contato com o meio líquido. As raízes são permeáveis a compostos solúveis e retêm em seus tecidos algas e microorganismos, que, por sua vez, contêm altas concentrações de materiais insolúveis como silicatos (RIBEIRO, 2000).
No que diz respeito à caracterização dos teores de lipídeos, lignina, celulose e hemicelulose (Tabela 4.2), o valor determinado de lipídeos para o aguapé inteiro (E.
crassipes) é semelhante ao determinado por Henry-Silva; Camargo (2002) (4,7%). Os lipídeos
e as proteínas são responsáveis pela estrutura da membrana celular e suas concentrações podem variar em virtude das condições tróficas dos ambientes em que vivem (ESTEVES, 1998). A composição lipídica não se deve somente às gorduras propriamente ditas, mas também, as ceras que, são biosintetizadas pelas plantas vasculares (RAVEN et al., 1976).
para a celulose de 47% (HILL et al., 1998) e 47,7% (RAVEENDRAN et al. 1995) e 25,9% determinado para a hemicelulose por Raveendran et al. (1995).
Para a fibra de curauá, determinaram-se teores de lignina, celulose e hemicelulose de 6,50%, 61,94% e 3,04% respectivamente. Esses teores são próximos àqueles encontrados na literatura; para a lignina (1,0 – 7,5%), celulose (69,0 – 74,1%) e hemicelulose (9,9 – 21,1%) (SANTOS et al., 2009; NEWSLETTERS, 2008; ARAÚJO, J. R. 2009).
Os teores dos principais constituintes da paina, se encontra dentro da faixa encontrada para as outras fibras, exceto para os teores de hemicelulose e celulose, os quais ficaram levemente superiores em relação às demais fibras. Para a caracterização da paina obtivemos teores de celulose e hemicelulose de 59,24% e 29,44%, respectivamente. Estes valores são semelhantes àqueles determinados por Annunciado et al., (2005); 54,1% e 27,5%. No entanto, para o teor de lignina, determinou-se 3,32%, inferior àquele determinado por estes autores de 15,1%.
Tabela 4.2 - Caracterização bioquímica dos biosorventes (% em massa).
Biosorvente Umidade
(%) Cinzas (%) Lipídeos (%) Lignina (%) Celulose (%) Hemicelulose (%)
Turfa 12,61 15,20 2,65 15,22 36,40 12,23
Coco 9,19 1,35 0,97 31,52 47,63 27,38
Curauá 7,79 2,91 2,31 6,50 61,94 3,04
Paina 8,82 0,43 0,71 3,32 59,24 29,44
Taboa inteira 6,25 3,61 0,64 9,07 36,26 26,10
Taboa flor 9,33 2,06 2,41 1,62 33,95 33,24
Aguapé
inteiro 10,80 13,60 3,60 3,61 24,58 25,40
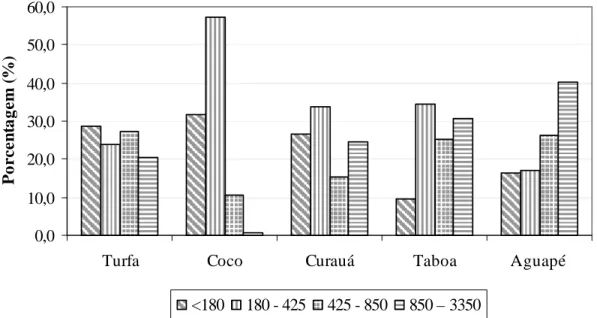
Quanto à caracterização granulométrica dos biosorventes inicialmente estudados (Figura 4.1), observa-se para a turfa uma distribuição homogênea de granulometria em torno de 20–28 %, o que não foi observado para os outros biosorventes. Pode-se destacar para a fibra de coco elevada quantidade de fibras (57,3%) com tamanho compreendido na faixa de 180-425 μm e pouquíssima quantidade na faixa de 850-3350 μm (0,6%).
0,0 10,0 20,0 30,0 40,0 50,0 60,0
Turfa Coco Curauá Taboa Aguapé
P o rce n ta g e m ( % )
<180 180 - 425 425 - 850 850 – 3350
Figura 4.1 – Distribuição granulométrica para os biosorventes (% em massa).
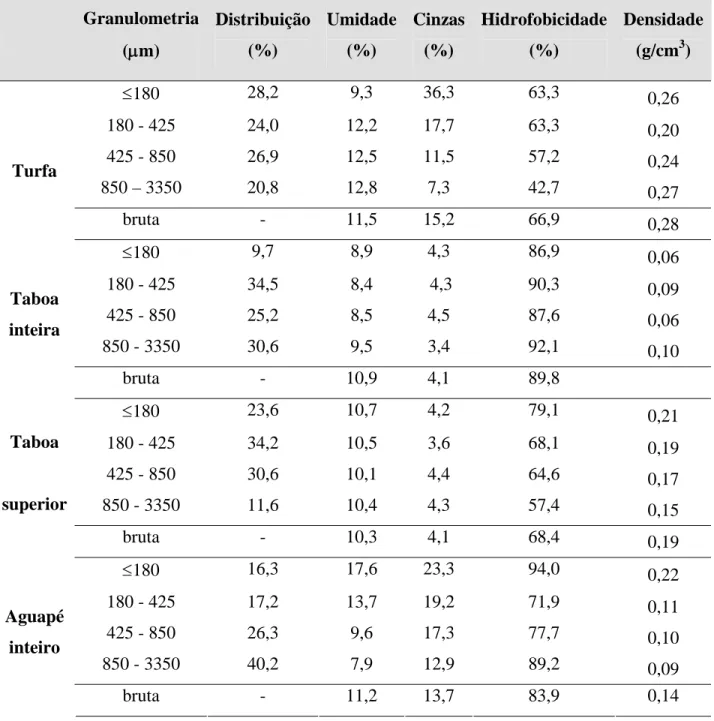
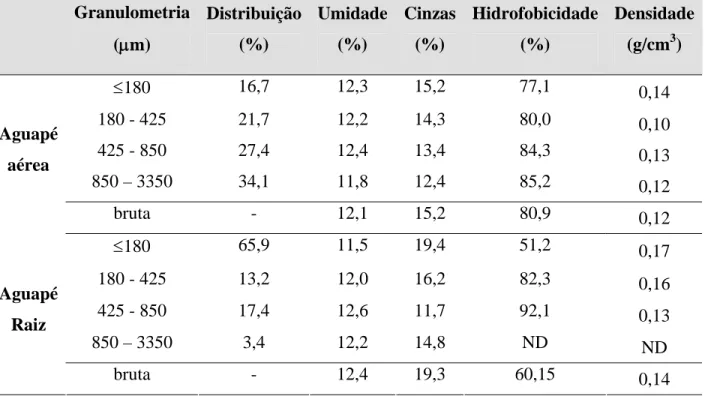
Na Tabela 4.3, pode-se observar as características físicas, físico-químicas e teor de cinzas para os biosorventes. Em uma caracterização mais detalhada dos biosorventes, estão expostos os teores de cinzas e o grau de hidrofobicidade para os intervalos granulométricos das frações.
Tabela 4.3 - Caracterização física, físico-química e teor de cinzas das frações granulométricas
dos biosorventes (% em massa).
Granulometria
(μm)
Distribuição (%) Umidade (%) Cinzas (%) Hidrofobicidade (%) Densidade
(g/cm3)
≤180 28,2 9,3 36,3 63,3 0,26
180 - 425 24,0 12,2 17,7 63,3 0,20
425 - 850 26,9 12,5 11,5 57,2 0,24
850 – 3350 20,8 12,8 7,3 42,7 0,27
Turfa
bruta - 11,5 15,2 66,9 0,28
≤180 9,7 8,9 4,3 86,9 0,06
180 - 425 34,5 8,4 4,3 90,3 0,09
425 - 850 25,2 8,5 4,5 87,6 0,06
850 - 3350 30,6 9,5 3,4 92,1 0,10
Taboa
inteira
bruta - 10,9 4,1 89,8
≤180 23,6 10,7 4,2 79,1 0,21
180 - 425 34,2 10,5 3,6 68,1 0,19
425 - 850 30,6 10,1 4,4 64,6 0,17
850 - 3350 11,6 10,4 4,3 57,4 0,15
Taboa
superior
bruta - 10,3 4,1 68,4 0,19
≤180 16,3 17,6 23,3 94,0 0,22
180 - 425 17,2 13,7 19,2 71,9 0,11
425 - 850 26,3 9,6 17,3 77,7 0,10
850 - 3350 40,2 7,9 12,9 89,2 0,09
Aguapé
inteiro
Tabela 4.3 - Caracterização física e físico-química das frações granulométricas dos
biosorventes (% em massa). Continuação.
Granulometria
(μm)
Distribuição (%) Umidade (%) Cinzas (%) Hidrofobicidade (%) Densidade
(g/cm3)
≤180 16,7 12,3 15,2 77,1 0,14
180 - 425 21,7 12,2 14,3 80,0 0,10
425 - 850 27,4 12,4 13,4 84,3 0,13
850 – 3350 34,1 11,8 12,4 85,2 0,12
Aguapé
aérea
bruta - 12,1 15,2 80,9 0,12
≤180 65,9 11,5 19,4 51,2 0,17
180 - 425 13,2 12,0 16,2 82,3 0,16
425 - 850 17,4 12,6 11,7 92,1 0,13
850 – 3350 3,4 12,2 14,8 ND ND
Aguapé
Raiz
bruta - 12,4 19,3 60,15 0,14
ND = não determinado
Para o aguapé inteiro e parte aérea, observa-se uma maior quantidade das maiores frações, que também apresentam hidrofobicidade superior em relação às frações menores.
Apesar de representarem uma porção menos hidrofóbica no que se refere à planta total, nos testes de hidrofobicidade constatou-se que a raiz migra da fase água para a fase de hexano, portanto são hidrofóbicas, como observado para a macrófita Salvinia
herzoggi (RIBEIRO, 2000).
Para a macrófita taboa, analisando-se o comportamento da planta inteira e da parte superior, verifica-se hidrofobicidade superior na taboa inteira. Este resultado pode ser relacionado ao fato de que, na taboa inteira, tem-se a inflorescência que possui uma hidrofobicidade 100%.
aparente determinada para a turfa e as macrófitas mostrou-se inferior a densidade da água (Tabela 4.3).
A paina e a flor da apresentaram as menores densidades aparentes 0,02 g/cm3 e 0,04 g/cm3, respectivamente. Segundo Annunciado et al. (2005), a paina apresenta densidade inferior a 0,64 g/cm3 determinada pela norma NBR 11931.
Os sorventes para compostos orgânicos, principalmente óleos, são empregados diretamente, no caso de derramamentos em superfícies sólidas ou corpos hídricos, portanto é importante avaliar as características de flutuabilidade (RUBIO, 2000).
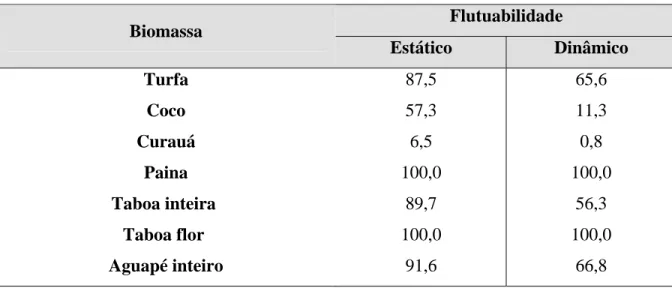
Com o intuito de investigar os biosorventes na sorção de diesel e biodiesel em sistemas hídricos, realizaram-se testes de flutuabilidade e os resultados nos sistemas estático e dinâmico são apresentados na Tabela 4.4. O fato da fibra do curauá ser menos densa que a água, não garante boa flutuabilidade, por causa da afinidade com água. As amostras de coco e curauá mostraram flutuabilidade baixa nos dois sistemas como descrito por Choi e Cloud (1992); materiais vegetais apresentam baixa flutuabilidade devido à baixa hidrofobicidade. Segundo Annunciado et al. (2005), em condições semelhantes às empregadas neste estudo, a flutuabilidade para o coco em sistema dinâmico foi de 49,9% e em estático de 20,6%, no entanto para a paina os resultados de flutuabilidade foram semelhantes.
Tabela 4.4 - Flutuabilidade em água deionizada dos biosorventes (% em massa).
Flutuabilidade Biomassa
Estático Dinâmico
Turfa 87,5 65,6
Coco 57,3 11,3
Curauá 6,5 0,8
Paina 100,0 100,0
Taboa inteira 89,7 56,3
Taboa flor 100,0 100,0
Aguapé inteiro 91,6 66,8
4.2 Sorção de Óleo em Sistema Seco
Inicialmente, o material comercial à base de turfa e os biosorventes (amostras brutas) foram submetidos a ensaios de sorção de óleo diesel nos tempos de 5, 10, 20, 40, 60 e 1440 min. Podem-se observar (Tabela 4.5) os valores médios de sorção deste óleo pelos biosorventes. Os biosorventes, com exceção das fibras de coco e curauá, apresentaram valores médios de sorção maiores ao da turfa, largamente empregada na biorremediação de acidentes envolvendo derramamentos de óleo.
A paina apresenta o maior valor médio de sorção de óleo diesel entre os biosorventes testados. Esta sorção assemelha-se ao observado para a fibra quenafe 7 a 8 g/g (massa de óleo diesel por massa de fibra) (LEE et al. 1999).
Tabela 4.5 - Sorção de óleo diesel pelos biosorventes (± desvio padrão)
Sorção (g/g) nos tempos (min)
Biosorvente 5 10 20 40 60 1440 Média
Turfa 1,26± 1,22± 1,17± 1,21± 1,26± 1,28± 1,23±
0,11 0,02 0,09 0,03 0,05 0,06 0,07
Coco 0,68± 0,78± 0,66± 0,70± 0,73± 0,98± 0,76±
0,22 0,10 0,08 0,09 0,08 0,16 0,16
Curauá 1,10± 1,18± 1,15± 1,27± 1,32± 0,74± 1,12±
0,18 0,18 0,08 0,21 0,30 0,05 0,25
Paina 7,89± 7,65± 6,97± 7,23± 7,02± 7,39± 7,36±
0,81 0,73 0,95 0,91 1,65 0,95 1,01
Taboa (inteira) 1,87± 1,96± 1,90± 2,08± 1,82± 2,13± 1,96±
0,28 0,15 0,17 0,27 0,13 0,17 0,22
Taboa (flor) 2,18± 2,40± 2,50± 2,60± 2,60± 2,59± 2,48±
0,17 0,20 0,17 0,08 0,28 0,17 0,23
Aguapé (inteiro) 2,15± 1,73± 1,65± 1,94± 1,48± 2,05± 1,83±
0,18 0,13 0,16 0,17 0,18 0,25 0,32
Esta diferença na sorção deve-se a diminuição da viscosidade do óleo reduzir a absorção dentro dos poros e vasos capilares, o óleo cru apresenta maior sorção pelos materiais devido a aderência na superfície do material e dentro dos poros durante a drenagem (TEAS et al., 2001). Portanto, o óleo diesel com baixa viscosidade é liberado pelo sorvente com mais facilidade diminuindo a eficiência do sorvente.