Diego Oliveira Cordeiro
Avaliação oxidativa do biodiesel de pinhão manso em diferentes
processos de purificação
_________________________________
Dissertação de Mestrado
Natal/RN, julho de 2013
INSTITUTO DE QUÍMICA
AVALIAÇÃO OXIDATIVA DO BIODIESEL DE PINHÃO MANSO EM DIFERENTES PROCESSOS DE PURIFICAÇÃO
Dissertação apresentada ao Programa de
Pós-Graduação
em
Química
da
Universidade Federal do Rio Grande do
Norte
(UFRN)
como
parte
dos
requisitos para obtenção do titulo de
Mestre em Química.
Orientador: Dr. Valter José Fernandes Júnior
2
aOrientadora: Drª. Marta Maria da Conceição
Natal
–
RN
UFRN / Biblioteca Central Zila Mamede. Catalogação da Publicação na Fonte.
Cordeiro, Diego Oliveira.
Avaliação oxidativa do biodiesel de pinhão manso em diferentes processos de purificação. / Diego OliveiraCordeiro. – Natal, RN, 2013. 101f. : il.
Orientador: Prof. Dr. Valter José Fernandes Júnior. Co-orientadora: Profa. Dra. Marta Maria da Conceição.
Dissertação (Mestrado) – Universidade Federal do Rio Grande do Norte. Centro de Ciências Exatas e da Terra. Instituto de Química. Programa de Pós-Graduação em Química.
1. Biodiesel - Dissertação. 2. Pinhão manso–Biodiesel - Dissertação. 3. Estabilidade oxidativa - Dissertação. 4. Processos de purificação - Dissertação. I. Fernandes Júnior, Valter José. II. Conceição, Marta Maria. III. Universidade Federal do Rio Grande do Norte. IV. Título.
ajudaram no meu crescimento pessoal, por nunca ter deixado meus problemas pessoais me derrubar e impedir de crescer.
A Professora Marta Maria da Conceição, que para mim é um exemplo vivo de pesquisadora dedicada e responsável. Cobrando, sugerindo e avaliando, ela foi sempre
presente em cada passo da minha pesquisa.
Ao Professor Valter José Fernandes Júnior pela orientação.
Ao Professor Raul Rosenhaim pelas análises realizadas no LACOM.
A Amanda Gondim e Camila Teixeira pelas análises de estabilidade oxidativa (P-DSC, Índice de acidez, Rancimat) que são as mais importantes do trabalho.
A Minha Mãe Maria das Graças Rocha Oliveira, que para mim é um exemplo de guerreira, talvez não seja a melhor mãe do mundo, mas sei que fez o seu possível para ser, nunca mediu esforços para me fazer uma pessoa feliz e realizada.
A meu Pai Harley Handenberg, pelo auxílio financeiro no início do meu mestrado, que sem isso era impossível poder me manter em Natal-RN.
As Minhas amigas do tempo de graduação, Rosiane e Suylan por sempre procurar está disponível a me acolher nos momentos que precisei.
A minha noiva Silvana que juntamente com minha mãe passou varias horas durante dias descascando dezenas de quilos de frutos secos de pinhão manso para retirar as sementes
que posteriormente foi descascada para retirar o albume. Um trabalho cansativo, repetitivo e duradouro.
A Janduir Egito, mais conhecido como “O Cumpadi”, meu grande amigo e companheiro de quarto em Natal. Sempre procurando ser prestativo, me ajudou em muitas coisas nesse período de mestrado, o qual merecia ter uma folha de agradecimento só com o nome dele.
Aos companheiros: da residência (Gilberlândio, Paulo, Alex, Marcio, Moises, Marcia, Karina e Aneliese), da casa, (Romerito, Sidney, Laudson, Marcinha e Rodrigo) e do Laboratório de Biocombustíveis (Clebson, Sandrinho, Cláudia, Vagner e Jakeline) pelos bons e importantes momentos vividos nesse mestrado. E a CAPES pela bolsa concedida.
“Os verdadeiros sábios não são aqueles que
têm muitos conhecimentos, mas sim aqueles
que sabem usar os conhecimentos que têm”.
O objetivo deste trabalho foi analisar a estabilidade oxidativa do biodiesel de pinhão manso obtido a partir de diferentes processos de purificação, sendo três via úmida com processos de secagens diferentes (em estufa a vácuo, em estufa convencional e com sulfato de sódio anidro) e um via seca (purificação com adsorvente silicato de magnésio). Matérias primas de diferentes qualidades (pinhão manso de safra antiga e safra recente) foram utilizadas. O óleo de pinhão manso foi extraído por extração mecânica e refinado. O biodiesel de pinhão manso foi obtido pela reação de transesterificação na rota etílica, utilizando catálise alcalina. As amostras de biodiesel foram caracterizadas por análises de Teor de água, Resíduo de carbono, Espectroscopia de Absorção na Região do Infravermelho e Termogravimetria. As curvas termogravimétricas das amostras purificadas PUsv* e PUsq* apresentaram as maiores temperaturas iniciais de decomposição, indicando serem mais estáveis, seguidas das amostras PU* e PUsc*. Além da amostra SP* apresentar a menor temperatura inicial, confirmando a
amostra sem purificação ser a menos estável termicamente. Os percentuais de perda de massa das amostras purificadas indicaram conversão em torno de 98,5%. Os resultados das análises
de resíduo de carbono e infravermelho sugeriram que a contaminação por impurezas é o principal fator para diminuição da estabilidade oxidativa do biodiesel. A estabilidade
oxidativa foi avaliada a partir de monitoramento periódico, utilizando as técnicas de Rancimat, Índice de Peróxido, Índice de acidez e Calorimetria Exploratória Diferencial Pressurizada. As amostras de biodiesel de pinhão manso que apresentaram melhor estabilidade oxidativa foram as da matéria prima de melhor qualidade e purificação por via úmida: PUsq* com secagem química, utilizando sulfato de sódio anidro e PUsv* com secagem a vácuo, as quais obtiveram estabilidade oxidativa de 6 horas no Rancimat no tempo 0 dias, no limite estabelecido pelo Regulamento Técnico Nº 4/2012 da ANP, sem a adição de antioxidante, sugerindo ser estes procedimentos os que menos influenciam na estabilidade oxidativa do biodiesel.
The objective of this study was to analyze the oxidative stability of biodiesel from jatropha obtained from different purification processes, three wet processes with different drying (in a vacuum oven, conventional oven and in anhydrous sodium sulfate) and dry (purification with magnesium silicate adsorbent). Raw materials of different qualities (jatropha crop ancient and recent crop) were used. The Jatropha oil was extracted by mechanical extraction and refined. The Jatropha biodiesel was obtained by the transesterification reaction in ethyl route using alkaline catalysis. The biodiesel samples were characterized by analysis of water content, carbon residue, Absorption Spectroscopy in the Infrared Region and Thermogravimetry.
Thermogravimetric curves of purified PUsv* PUsq* and had higher initial decomposition temperatures, indicating that the most stable, followed by samples PU* and PUSC*. Besides the sample SP* is a smaller initial temperature, confirming the sample without purification to be less thermally stable. The percentage mass loss of the purified samples showed conversion of about 98.5%. The results of analyzes carbon residue and infrared suggested that
contamination by impurities is the main factor for decreased oxidative stability of biodiesel. The oxidative stability was assessed from periodic monitoring, using the techniques of
Rancimat, peroxide index, acid value and Pressurized Differential Scanning Calorimetry. Samples of biodiesel from jatropha which showed better oxidative stability were of the best quality raw material and wet scrubbing: PUsq* with dry chemical, using anhydrous sodium sulfate and PUsv* with vacuum drying, which had oxidative stability 6 hours in Rancimat time 0 days, within the limits established by the Technical Regulation No. 4/2012 of the ANP, without the addition of antioxidant, suggesting that these procedures the least influence on the oxidative stability of biodiesel
1. INTRODUÇÃO... .... 12
2. OBJETIVOS... 14
2.1. OBJETIVO GERAL... 14
2.2. OBJETIVOS ESPECIFICOS... 14
3. FUNDAMENTAÇÃO TEÓRICA... 15
3.1. ENERGIA E MEIO AMBIENTE... 15
3.2. BIOCOMBUSTÍVEIS... 17
3.3. BIODIESEL... 18
3.3.1. Matéria-Prima... 21
3.3.2. Transesterificação... 25
3.3.3. Purificação do Biodiesel... 28
3.3.4. Parâmetros Físico-Químicos... 31
3.3.5. Estabilidade Térmica... 40
3.3.6. Estabilidade à Oxidação... 42
4. MATERIAIS E MÉTODOS... 51
4.1. OBTENÇÃO DA MATÉRIA PRIMA... 51
4.2. EXTRAÇÃO DO ÓLEO... 52
4.3. TRATAMENTO DO ÓLEO... 53
4.3.1. Degomagem... 53
4.3.2. Índice de acidez e Neutralização... 54
4.3.3. Lavagem... 56
4.3.4. Secagem... 57
4.4. SÍNTESE DO BIODIESEL DE PINHÃO MANSO... 57
4.5. PURIFICAÇÃO DO BIODIESEL... 59
4.6. CARACTERIZAÇÃO DO BIODIESEL... 62
4.6.1. Resíduo de Carbono... 62
4.6.2. Teor de Água... 62
4.6.3. Espectros de Absorção na Região do Infravermelho... 62
4.6.4. Termogravimetria... 63
4.7. ESTABILIDADE OXIDATIVA... 63
4.7.1. Rancimat... 63
4.7.2. Calorimetria Exploratória Diferencial Pressurizada (PDSC)... 63
4.7.3. Índice de Peróxido... 64
5.2. RENDIMENTO DO ÓLEO BRUTO DE PINHÃO MANSO... 65
5.3. INDICE DE ACIDEZ E RENDIMENTO DO ÓLEO PURIFICADO... 66
5.4. RENDIMENTO DO BIODIESEL... 67
5.4.1. Matéria Prima de Menor Qualidade... 68
5.4.2. Matéria Prima de Melhor Qualidade... 68
5.5. CARACTERIZAÇÃO DO BIODIESEL... 70
5.5.1. Espectros de Absorção na Região do Infravermelho... 70
5.5.2. Resíduo de Carbono... 72
5.5.3. Teor de Água... 73
5.5.4. Termogravimetria... 74
5.6. ESTABILIDADE OXIDATIVA... 77
5.6.1. Índice de Acidez (IA)... 78
5.6.2. Calorimetria Exploratória Diferencial Pressurizada (PDSC)... 79
5.6.3. Teste de Aceleração em Estufa... 83
5.6.4. Rancimat... 88
6. CONCLUSÃO... 92
ANP - Agência Nacional de Petróleo Gás Natural e Biocombustíveis. ASTM - Sociedade Americana de Testes e Materiais.
B100 - Biodiesel puro.
CEN - Comitê Europeu de Normalização. DTG - Termogravimetria derivada. EN - Norma Europeia.
G-20 - Grupo dos 20 países membros. GEE - Gases do Efeito Estufa.
IA - Índice de acidez.
ISO - International Organization for Standardization. IP - Índice de peróxido.
PDSC - Calorimetria exploratória diferenciada pressurizada. TG - Termogravimetria.
PSad - Biodiesel de pinhão Manso obtido pela matéria prima de menor qualidade, purificação via seca utilizando silicato de magnésio.
PSad* - Biodiesel de pinhão Manso obtido pela matéria prima de melhor qualidade, purificação via seca utilizando silicato de magnésio.
PU* - Biodiesel de pinhão Manso obtido pela matéria prima de melhor qualidade, purificação via úmida sem secagem.
PUsc - Biodiesel de pinhão Manso obtido pela matéria prima de menor qualidade, purificação via úmida com secagem térmica utilizando uma estufa convencional.
PUsc* - Biodiesel de pinhão Manso obtido pela matéria prima de melhor qualidade, purificação via úmida com secagem térmica utilizando uma estufa convencional.
PUsq - Biodiesel de pinhão Manso obtido pela matéria prima de menor qualidade, purificação via úmida com secagem química utilizando sulfato de sódio anidro.
PUsq* - Biodiesel de pinhão Manso obtido pela matéria prima de melhor qualidade, purificação via úmida com secagem química utilizando sulfato de sódio anidro.
PUsv - Biodiesel de pinhão Manso obtido pela matéria prima de menor qualidade, purificação via úmida com secagem térmica utilizando uma estufa a vácuo. PUsv* - Biodiesel de pinhão Manso obtido pela matéria prima de melhor qualidade,
purificação via úmida com secagem térmica utilizando uma estufa a vácuo. SP* - Biodiesel de pinhão Manso obtido pela matéria prima de melhor qualidade
sem processo de purificação.
Tabela 1. Especificação do Biodiesel B100 do Regulamento Técnico nº 4/2012 da
ANP... 20
Tabela 2. Ácidos graxos saturados que ocorrem nos óleos e gorduras... 22
Tabela 3. Ácidos graxos insaturados que ocorrem nos óleos e gordura... 22
Tabela 4. Viscosidade do Biodiesel de Várias Espécies Vegetais... 32
Tabela 5. Densidade do biodiesel obtido de diferentes origens... 33
Tabela 6. Número de Cetano do Biodiesel de Várias Espécies Vegetais... 34
Tabela 7. Ponto de Fulgor do Biodiesel de Várias Espécies Vegetais... 35
Tabela 8. Ponto de Fluidez (PF) e Ponto de Névoa (PN) do Biodiesel de Várias oleaginosas... 37
Tabela 9. Rendimento da extração do óleo bruto de pinhão manso das sementes de melhor e menor qualidade... 65
Tabela 10. Rendimento da purificação do óleo de pinhão manso obtido pela matéria prima de melhor e menor qualidade... 67
Tabela 11. Massa do biodiesel obtido pela matéria prima de menor qualidade... 68
Tabela 12. Massa do biodiesel obtido pela matéria prima de melhor qualidade... 69
Tabela 13. Resíduo de carbono (%) das amostras de biodiesel de pinhão manso obtido da matéria prima de menor qualidade... 72
Tabela 14. Resíduo de carbono (%) das amostras de biodiesel de pinhão manso obtido da matéria prima de melhor qualidade... 72
Tabela 15. Teor de água das amostras de biodiesel de pinhão manso em diferentes dias 73 Tabela 16. Dados termogravimétricos das amostras de pinhão manso obtido pela matéria prima de melhor qualidade... 77
Tabela 17. Índice de acidez (mg KOH/g) das amostras de biodiesel de pinhão manso obtidas pela matéria prima de menor qualidade em diferentes períodos... 78
Tabela 18. Índice de acidez (mg KOH/g) das amostras de biodiesel de pinhão manso obtidas pela matéria prima de melhor qualidade em diferentes períodos... 79
Tabela 19. Tempo do inicio da curva de PDSC das amostras de biodiesel obtidas pelas sementes de menor qualidade... 81
Tabela 20. Tempo do inicio da curva de PDSC das amostras de biodiesel obtidas pela matéria prima de melhor qualidade... 82
Tabela 21. Índice de peróxido do biodiesel de pinhão manso de 0 a 25 dias... 88
Tabela 22. Estabilidade oxidativa do biodiesel de pinhão manso obtida pela matéria prima de menor qualidade através do método Rancimat em diferentes períodos... 89
Figura 2. Representação da estrutura molecular do composto triacilglicerídeos... 25
Figura 3. Representação química da reação de transesterificação... 26
Figura 4. Representação do mecanismo da reação de transesterificação, rota etílica e catálise básica... 27
Figura 5. Representação do método Rancimat... 44
Figura 6. Esquema da etapa de iniciação da autoxidação... 47
Figura 7. Esquema da etapa da Propagação... 48
Figura 8. Esquema da reação de dimerização na etapa de terminação... 49
Figura 9. a) Fruto seco de pinhão manso; b) Semente de pinhão manso... 51
Figura 10. a) albume da semente de pinhão manso; b) Cilindro pronto para prensagem; c) Prensa hidráulica de 30 toneladas usada na extração... 52
Figura 11. Fluxograma dos processos de refino do óleo do pinhão manso... 53
Figura 12. Etapas do processo de degomagem: a) Agitação mecânica, b) Óleo de pinhão manso na centrifuga, c) separação de fases no funil de decantação.... 54
Figura 13. Processo de Neutralização do óleo de pinhão manso... 55
Figura 14. Lavagem do óleo de pinhão manso... 56
Figura 15. Fluxograma dos processos de síntese e purificação do biodiesel de pinhão manso... 57
Figura 16. Biodiesel de pinhão manso separado da glicerina... 59
Figura 17. Filtração do Biodiesel PSad e adsorvente... 60
Figura 18. Massa (g) das amostras de matéria prima de melhor e menor qualidade em diferentes etapas... 69
Figura 19. Espectros de infravermelhos das amostras: SP*, PU*, PSad*, PUsq*, PUsv*, PUsc*... 70
Figura 20. Curvas Termogravimétricas TG/DTG do óleo purificado de pinhão manso obtido das sementes de melhor qualidade... 75
Figura 21. Curvas termogravimétricas TG/DTG das amostras de biodiesel em diferentes procedimentos de purificação obtidas pela matéria prima de melhor qualidade: a) PU*, b) SP*, c) PSad*, d) PUsq*, e) PUsv*, f) PUsv*... 76
Figura 22. Curvas PDSC do biodiesel de pinhão manso obtidas da matéria prima de menor qualidade: a) PSad, b) PUsq, c) PUsv d) PUsc, analisados diferentes períodos... 80
Figura 23. Curvas PDSC do biodiesel de pinhão manso obtidas da matéria prima de melhor qualidade... 82
Figura 24. Amostras de Biodiesel sobre aceleração em estufa nos períodos: a) 0 dias, b) 3 dias, c) 11 dias d) 25 dias... 84
Figura 25. Gomas e sedimentos insolúveis presentes nas amostras: a) SP*, b) PSad*... 85
1. INTRODUÇÃO
O biodiesel é um combustível renovável derivado de óleos vegetais e gordura animal empregado para motores do ciclo diesel. Várias pesquisas abordam suas vantagens em comparação ao diesel derivado de petróleo, tais como: livre de enxofre e aromáticos, não é tóxico, facilmente biodegradável, seguro de manusear, produz menos poluentes atmosféricos, aumenta a lubricidade e as suas principais propriedades físico-químicas são comparáveis aos dos combustíveis convencionais. No entanto, o biodiesel apresenta algumas desvantagens, as principais são o alto custo de produção e a baixa estabilidade oxidativa, que acarreta em degradação e perda das propriedades físico-químicas durante armazenamento em longos
períodos (KARAVALAKIS, STOURNAS; KARONIS, 2010; GONÇALVES; NOLGUEIRA, 2007).
A estabilidade à oxidação é uma das propriedades mais importantes dos alquil ésteres de ácidos graxos que afetam principalmente a qualidade durante o armazenamento. O biodiesel tende a ser menos resistente à oxidação do que o diesel de petróleo, sua degradação gera produtos de oxidação que podem comprometer as propriedades do combustível, prejudicando sua qualidade e desempenho do motor (SAEED; PULLEN, 2012).
O biodiesel que apresenta uma das menores estabilidades oxidativas é proveniente do óleo da semente de pinhão manso (Jatropha curcas L.), por conter mais de 80% de ácidos graxos oleicos e linoleicos, que possuem na sua estrutura molecular insaturações, facilitando a formação de radicais livres. No entanto, o pinhão manso apresenta elevado rendimento de óleo bruto por hectare de plantação, não é utilizado como fonte alimentícia e seu biodiesel possui excelentes propriedades físico-químicas, em comparação aos biodieseis obtidos por outras matérias primas (BASILI; FONTINI, 2012).
O processo de purificação do biodiesel é uma das principais causas de seu elevado custo de produção, devido as indústrias ainda utilizarem grande quantidade de água para
retirar as impurezas do biodiesel durante o processo de transesterificação. Esse processo gera uma grande quantidade de efluentes, tais como compostos polares, resíduos de catalisadores e
A purificação é um processo que está diretamente ligado à estabilidade oxidativa do biodiesel. Uma purificação ineficiente pode deixar resíduos de impurezas na amostra, colaborando para acelerar a degradação. O teor de água, a contaminação por catalisador, resíduos de glicerina, e as condições de secagem contribuem significativamente para diminuição da estabilidade oxidativa.
2. OBJETIVOS
2.1.OBJETIVO GERAL
Analisar a estabilidade oxidativa do biodiesel de pinhão manso, obtido na rota etílica em diferentes processos de purificação.
2.2.OBJETIVOS ESPECIFICOS
Extrair e refinar o óleo de pinhão manso;
Analisar a qualidade do óleo pelo Índice de acidez;
Sintetizar o biodiesel de pinhão manso pela rota etílica em diferentes processos de
purificação;
Caracterizar o biodiesel obtido em diferentes processos de purificação, através da
determinação do Teor de água, Resíduo de carbono e Espectroscopia de Absorção na Região do Infravermelho;
Analisar a estabilidade oxidativa do biodiesel obtido em diferentes processos de
purificação, através dos métodos Rancimat, Calorimetria Exploratória Diferencial
Pressurizada (PDSC), Índice de Acidez e Índice de Peróxido;
Analisar a influência dos processos de purificação das amostras na estabilidade
térmica do biodiesel;
Verificar o quanto a qualidade da matéria prima pode influenciar no rendimento e na
estabilidade oxidativa do biodiesel;
Determinar qual método de purificação do biodiesel apresentou melhor estabilidade
3. FUNDAMENTAÇÃO TEÓRICA
3.1.ENERGIA E MEIO AMBIENTE
Nos últimos anos do século XX, se iniciou uma preocupação cada vez mais crescente envolvendo dois fatores primordiais para o desenvolvimento e qualidade de vida do homem. Estes fatores são o meio ambiente e energia, que em muitos casos caminham em lados opostos, visto que para produzir energia se faz necessário modificar o meio ambiente ou consumir reservas naturais como o petróleo, gás natural e carvão mineral (VICHI; MANSOR, 2009).
O consumo crescente de energia causa sérios desequilíbrios ambientais, que estão sendo perceptíveis até mesmo por cidadãos comuns, decorrentes dos constantes noticiários da mídia. O mais conhecido problema ambiental no momento é chamado desequilíbrio efeito
estufa. Esse fenômeno acontece através da absorção da radiação eletromagnética na faixa do
infravermelho emitido pelo sol, e absorvida pelos gases presentes na superfície terrestre, que
implica em um aumento nos movimentos rotacionais e vibracionais das moléculas, que consequentemente passam a emitir a radiação que foi absorvida. Dessa forma, as moléculas vizinhas irão absorver e emitir estas radiações, ocasionando uma reação em cadeia, espalhando a radiação por todas as direções da superfície, estabilizando o clima da terra em uma temperatura mais quente do que seria com a falta da atmosfera (TOLETINO; ROCHA-FILHO, 1998).
Nem todos os gases presentes na atmosfera são causadores do efeito estufa. Esse fenômeno é causado pelos gases: o monóxido de carbono (CO), o dióxido de carbono (CO2),
o metano (CH4), o óxido nitroso (N2O), os óxidos de nitrogênio (NOx), os
clorofluorcarbonetos (CFCs), os hidroclorofluorcarbonetos (HCFCs), os hexa fluoretos de enxofre (SF6) e água presente na atmosfera [H2O(l)] (MENDONÇA, 2000).
Dentre os gases citados, o dióxido de carbono é o que mais preocupa a comunidade
científica, no que se refere ao agravamento do efeito estufa, visto que é o gás mais produzido em decorrência das atividades humanas, na qual, tais atividades humanas são responsáveis
pela maior parte da concentração de CO2 na atmosfera (TOLETINO; ROCHA-FILHO, 1998).
Grande parte do CO2 emitidos pela ação do homem é proveniente de motores
Além deste problema ambiental, segundo o Conselho Mundial de Energia (World
Energy Council, 2011), as reservas de petróleo existentes no planeta são apenas suficientes
para o consumo em períodos de médio prazo (VICHI; MANSOR, 2009). Isso acarreta um grave problema, já que com o aumento da população mundial em conjunto com aumento de consumo de novas tecnologias, acelera ainda mais a necessidade por recursos energéticos.
Segundo o próprio Conselho, aproximadamente 90% da matriz energética mundial é derivada de fontes de energia não renováveis, nas quais, mais de um terço são provenientes do petróleo (Figura 1) e seus derivados (VICHI; MANSOR, 2009).
Figura 1. Oferta de energia no mundo em 2007, discriminada por setores.
Fonte: Vichi e Mansor, (2009).
Tendo em vista esta alta dependência mundial por energias não renováveis, principalmente derivados do petróleo, se fazem necessárias pesquisas para desenvolvimento
de novas fontes de energias renováveis alternativas, que além de suprir a demanda energética, possam contribuir para diminuição de alguns problemas ambientais que vem afetando
equilíbrio do nosso planeta, como é o caso do efeito estufa. Carvão Mineral;
26%
Petróleo e Derivados; 32% Urâno; 6%
Fontes Renováveis;
10%
Gás Natural; 21%
3.2.BIOCOMBUSTÍVEIS
Segundo a Agência Nacional do Petróleo, Gás Natural e Biocombustíveis – ANP os biocombustíveis são “combustíveis derivados de biomassa renovável para o uso de motores
de combustão interna ou, conforme o regulamento, para todo tipo de geração de energia, que
possa substituir parcialmente ou completamente combustíveis de origem fóssil” (SILVA, 2005). Existem outras definições mais simples de biocombustíveis, como as apresentadas por Vichi e Mansor (2009) que o definiu apenas como: “combustíveis renováveis derivados de
matéria-prima biológica”, podendo ser de origem vegetal e animal, como o bioetanol, o
etanol, o biodiesel, o biogás (metano). Sendo que destes biocombustíveis, o etanol é o mais consumido, cuja sua produção mais cresce no mundo. Um aumento superior a 10 vezes mais barris em apenas 25 anos (MURRAY, 2005).
No Brasil, a produção de biocombustíveis predominante também é a de etanol.
Segundo O Balanço Energético Nacional de 2008, foram produzidos 22,557x103 m3 de etanol, contra 373x103 m3 de biodiesel no país no ano de 2007 (VICHI; MANSOR, 2009). As
produções nacionais de bioetanol e biogás ainda são bastante pequenos.
Segundo o relatório publicado pela ONG americana Pew Charitable Thusts (Pew Charitable Thusts, 2010) o Brasil é o sexto entre os membros do G-20 (grupo formado pelas 20 maiores economias do mundo) que mais investe em energias renováveis. Cerca de US$ 7,6 bilhões de investimento em 2010, sendo que 40% desse valor são investidos em biocombustíveis, se tornando o país que mais investe nesse tipo de energia renovável no mundo. Estima-se que os investimentos em biocombustíveis no Brasil sejam de aproximadamente 61% dos recursos dos países destinados à energia renováveis no período de 2005 a 2010.
O biocombustível teve origem em Paris, durante uma exposição de motores em 1990, quando a companhia francesa Otto demonstrou que o funcionamento de um motor a diesel construído para ser alimentado com petróleo, teve um desempenho semelhante quando
consumia óleo de amendoim. O inventor destes motores foi o alemão Rudolf Diesel, que escreveu em seu livro (Combustíveis Líquidos) a utilização bem sucedida de óleo de
amendoim em máquinas de diesel (KNOTHE; GERPEN, 2006).
No entanto, a grande oferta de petróleo no mercado em conjunto com seus baixos
despertada uma preocupação sobre desenvolvimento de energias alternativas, que pudessem substituir os derivados de petróleo. Para minimizar essa crise o governo brasileiro criou o Pró-Álcool para fabricação de carros movidos a álcool, com intuito de reduzir o consumo de gasolina. (SILVA; FREITAS, 2008).
Nos anos 80, também se iniciou uma valorização mundial significativa sobre os impactos ao meio ambiente, na qual, foram elaborados vários estudos e relatórios. Os derivados de petróleo são colocados como um dos maiores causadores desse desequilíbrio ambiental, por emitirem gases causadores do efeito estufa (GEE), além de não serem combustíveis renováveis e biodegradáveis. Dessa forma, o uso dos biocombustíveis também tem como objetivo não somente reduzir significativamente as emissões de gases causadores do efeito estufa, mas também produzir um combustível que se adapte melhor aos pressupostos da sustentabilidade ambiental.
Alguns estudos mostram que o biocombustível pode chegar a apresentar um
potencial na redução de 90% em emissão de GEE (VICHI; MANSOR, 2009), além de ser renovável, biodegradável e não ser tóxico, o que justifica as pesquisas na área.
3.3.BIODIESEL
Segundo o Art. 2º da Resolução ANP Nº 14, DE 11.5.2012 - DOU 18.5.2012 o biodiesel é definido como:
combustível composto de alquil ésteres de ácidos carboxílicos de cadeia longa, produzido a partir da transesterificação e/ou esterificação de matérias graxas, de gorduras de origem vegetal ou animal, e que atenda a especificação contida no Regulamento Técnico nº 4/2012, parte integrante desta Resolução (ANP, 2012).
Ou seja, é um combustível alternativo ao óleo diesel, de fontes renováveis, que
consiste de moléculas de triacilglicerídeos. (MEIRA et al., 2011; GERIS et al., 2007). Esta
denominação de “biodiesel” foi utilizada primeiramente pelos pesquisadores chineses (GONÇALVES; NOGUEIRA, 2007).
carbono, visto que o gás carbono liberado na atmosfera na combustão, pode ser absorvido pelas plantas oleaginosas na fotossíntese, principalmente no desenvolvimento das sementes (RAMOS et al., 2000; GONÇALVES; NOGUEIRA, 2007).
Além de ser um combustível mais adequado ao meio ambiente, o biodiesel é um combustível que também apresenta propriedades físico-químicas semelhantes ao diesel convencional, como: conteúdo de energia, massa específica, viscosidade cinemática e número de cetano. Livre de enxofre e compostos aromáticos, com alto número de cetanos, combustão completa e um alto ponto de inflamação, na qual facilita o manuseio, a armazenagem e o transporte, sem comprometer a quantidade de energia ao motor, com desempenho praticamente o mesmo do diesel convencional, no que se refere à potência e ao torque. Por apresentar maior viscosidade em comparação ao diesel mineral, o biodiesel proporciona maior lubricidade promovendo uma redução no desgaste das partes móveis do motor. No entanto, viscosidade muito alta diminui a eficiência na queima do motor que gera a deposição de
resíduos, promovendo também o desgaste (RAMOS et al., 2000; CRUZ; LÔBO; FERREIRA, 2009; DUNN, 2006).
O Biodiesel puro pode ser denominado de B100, na qual B representa o biodiesel e o número (no caso 100) é o percentual do referido a quantidade do combustível numa mistura com o diesel convencional. Desde o dia 1º de janeiro de 2010, o óleo diesel comercializado em todo o Brasil passou a ser B5, ou seja, contém 5% de biodiesel. Esta regra foi estabelecida pelo Conselho Nacional de Política Energética (CNPE) a partir da Resolução nº 6/2009, que foi publicada no Diário Oficial da União (DOU) em 26 de outubro de 2009, aumentando de 4% para 5% o percentual obrigatório de mistura de biodiesel ao óleo diesel. (ANP, 2008).
Tabela 1. Especificação do Biodiesel B100 do Regulamento Técnico nº 4/2012 da ANP.
CARACTERÍSTICA UNIDADE LIMITE
MÉTODO ABNT
NBR ASTM D EN/ISSO
Estabilidade à oxidação a 110°C,
mín. (2) H 6 - - 14112
Massa específica a 20°C kg/m3 850 a
900 7148 14065 1298 4052 3675 12185
Viscosidade Cinemática a 40°C Mm2/s 3,0 a 6,0 10441 445 3104
Teor de Água, máx. (2) mg/kg 500 - 6304 12937
Contaminação Total, máx. mg/kg 24 - - 12662
Ponto de fulgor, mim. (3) °C 100,0 14598 93 3679
Teor de éster, min. % massa 96,5 15764 - 14103
Resíduo de carbono (4) % massa 0,050 15586 4530 -
Cinzas sulfatadas, máx. % massa 0,020 6294 874 3987
Enxofre total, máx. mg/kg 5 - 5453 20846
20884
Sódio + Potássio, máx. mg/kg 5
15554 15555 15553 15556 - 14108 14104 14538
Cálcio + Magnésio, máx. mg/kg 5 15553 - 14538
Fósforo, máx mg/kg 10 15556 4951 14107
Corrosividade ao cobre, 3h/50°C,
máx. - 1 15553 130 2160
Número de Cetano (5) - Anotar 14359 613
6890 (6) 5165
Ponto de entupimento de filtro a
frio, máx. °C 19 (7) 14747 6371 116
Índice de acidez, máx. mg KOH/g 0,50 14448 664 14104 (8)
Glicerol livre, máx. % massa 0,02 15341
15771 6584 (8)
14105 (8) 14106 (8)
Glicerol total, máx. % massa 0,25 15344 6584 (8) 14105
(10)
Monoacilglicerol, máx. % massa 0,8
15342 (8) 15344 15908
6584 (8) 14105(8)
Diacilglicerol, máx. % massa 0,2 15342(8) 15344
15908
6584(8) 14105(8)
Triacilglicerol, máx. % massa 0,2 15342(8) 15344
15908
6584(8) 14105(8)
Metanol ou Etanol, máx. % massa 0,20 15343 - 14111
Índice de Iodo (5) g/100g Anotar - - 14112 (8)
(2) A partir do dia 1º de Janeiro de 2013 até 31 de dezembro de 2013 será admitido o limite máximo de 350 mg/Kg e a partir do dia 1º de Janeiro de 2004 o limite máximo será de 200 mg/Kg.
No Brasil, principalmente no semiárido nordestino, há muitas terras pouco produtivas, algumas em estado de desertificação ou erosão. Com a ampliação do biodiesel no mercado nacional, milhares de agricultores podem cultivar uma enorme variedade de oleaginosas, com um baixo custo de produção em terras pouco produtivas, em consequência pode ocorrer um aumento de renda na comercialização da matéria prima para o biodiesel em conjunto com a melhoria do solo, evitando a erosão e a desertificação. O agricultor pode até utilizar culturas oleaginosas para incorporar nutrientes realizando uma rotação de culturas em suas terras (GONÇALVES; NOGUEIRA, 2007; ANP, 2012).
3.3.1. Matéria-Prima
As gorduras são as mais importantes reservas alimentares do organismo, seja ele de cunho vegetal ou mineral. As gorduras líquidas designam-se frequentemente por óleos. As
gorduras e óleos são substâncias insolúveis em água (hidrofóbicas), podem ser extraídas de várias substâncias como: soja, milho, linhaça, semente de algodão, semente de pinhão manso,
sebo, banha de porco, manteiga entre outros. (MORRISON; BOYD, 2005).
Segundo Gioielli, Chiu e Grimaldi, (2008), a aplicação da maioria dos óleos e gorduras naturais é bastante limitada pela constituição da sua estrutura molecular, impostas pela sua composição em ácidos graxos e em triacilgliceróis. Para ampliar seu uso, suas estruturas moleculares são modificadas através de métodos químicos, acarretando numa alteração nas características físico-químicas de um óleo ou gordura, que proporciona uma maior utilidade para produção e consumo de produtos alimentícios, cosméticos e energéticos.
Quimicamente as gorduras são constituídas por uma mistura de ésteres carboxílicos derivados de triglicerídeos, na qual estes compostos são denominados de ácidos graxos, e estes podem representar mais de 95% do peso molecular dos triglicerídeos, cujo tamanho de suas cadeias variam de acordo com a quantidade de átomos de carbono. Como também os ácidos graxos podem variar em diferentes graus de insaturação (RAMOS et al., 2000;
MORRISON; BOYD, 2005; MORETTO; FETT, 1998).
A composição química dos ácidos graxos varia de acordo com a espécie da
oleaginosa, a variação pode ser expressa pela relação molar entre os diferentes ácidos graxos presentes na estrutura (RAMOS et al., 2000). Dessa forma, a análise da composição de ácidos
Líquida de Alta Eficiência, Cromatografia em Fase Gasosa e Espectroscopia de Ressonância Magnética Nuclear de Hidrogênio (RAMOS et al., 2000).
Geralmente os ácidos graxos são classificados em duas categorias: saturados (Tabela 2) e insaturados (Tabela 3). Os principais ácidos saturados são: láurico, palmítico e esteárico; e insaturados: oléico, linolênico e linoléico (SOUZA-SOARES; SIEWERDT, 2005).
Tabela 2. Ácidos graxos saturados que ocorrem nos óleos e gorduras.
Símbolo e
número Fórmula Nome sistemático Nome trivial
C 4 CH3-(CH2)2-COOH butanóico Butírico
C 6 CH3-(CH2)4-COOH hexanóico Capróico
C 8 CH3-(CH2)6-COOH octanóico Caprílico
C 10 CH3-(CH2)8-COOH decanóico Cáprico
C 12 CH3-(CH2)10-COOH dodecanóico Láurico
C 14 CH3-(CH2)12-COOH tetradecanóico Mirístico
C 16 CH3-(CH2)14-COOH hexadecanóico Palmítico
C 18 CH3-(CH2)16-COOH octadecanóico Esteárico
C 20 CH3-(CH2)18-COOH eicoisanóico Araquídico
C 22 CH3-(CH2)20-COOH docosanóico Behênico
C 24 CH3-(CH2)22-COOH tetracosanóico Lignocérico
Fonte: Morrison e Boyd, (2005).
Ácidos insaturados encontrados em gorduras naturais predominam sobre os saturados, particularmente nas plantas superiores e nos animais que habitam em lugares de baixa temperatura. Esses ácidos são predominante na configuração espacial do tipo cis = Z
(SOUZA-SOARES; SIEWERDT 2005; MORETTO; FETT, 1998).
Tabela 3. Ácidos graxos insaturados que ocorrem nos óleos e gorduras.
Símbolo e
número Fórmula Nome sistemático
Nome trivial C 16:1 CH3-(CH2)5CH=CH(CH2)7-COOH 9-hexadecanóico Palmitoleico C 18:1 CH3-(CH2)7CH=CH(CH2)7-COOH 9-octadecanóico Oléico C 18:1 CH3-(CH2)5CH=CH(CH2)9-COOH 11-octadecanóico Pacênico C 18:2 CH3-(CH2)4(CH=CHCH2)2(CH2)6-COOH 9,12-octadecanóico Linolêico C 18:3 CH3CH2(CH=CHCH2)3(CH2)6-COOH 9,12,15-octadecanóico Linolênico C 20:4 CH3-(CH2)4(CH=CHCH2)4(CH2)2-COOH 5,8,11,14-eicoisanóico Araquidônico
3.3.1.1. Pinhão Manso
O Jatropha curcas L. popularmente conhecido como pinhão manso, pertence à família Euforbiáceas, a mesma da mamona e da mandioca, sendo provavelmente originário do Brasil (ARRUDA et al., 2004). Podendo ser encontrado em todo território Brasileiro, principalmente em regiões tropicais e temperadas. O seu cultivo pode ser ideal para a produção de biodiesel, visto que cresce rapidamente, é resistente à seca e não necessita preparação e cuidado da terra para o seu crescimento, conseguindo se desenvolver em terras degradadas, podendo ser empregado para recuperação de terras em fase de desertificação ou controle da erosão. (OPENSHAW, 2000).
Não serve para consumo alimentar humano. No entanto, o Jatropha curcas L. pode ser utilizado para reduzir as emissões de gases que provocam o efeito estufa, tanto diretamente (através da substituição de combustíveis fósseis com óleo extraído das sementes),
e indiretamente, através da fixação de estoques de carbono no solo e na biomassa vegetal. O arbusto vive em média 50 anos, sua altura varia entre dois a três metros, mas em
condições especiais pode chegar a cinco metros. O tronco tem a coloração cinza claro com diâmetro de aproximadamente 20 cm na base, na qual começa a se dividir (ARRUDA et al., 2004). Possui raízes pouco profundas e pouco ramificadas, o qual seu desenvolvimento irá depender de como foi plantada. Caso a planta seja proveniente de sementes, uma raiz principal e quatro raízes laterais se propagarão no solo (OPENSHAW, 2000). O caule é liso, de lenho mole, e casca contendo tanino (BASILI; FONTINE, 2012).
As folhas são tóxicas, de cor verde, largas e alternas, em forma de palma com três a cinco lóbulos e pecioladas, salientes na face inferior. Suas flores apresentam um grande potencial para apicultura, tem a coloração amarelo-esverdeadas, com a floração monóica, mas com sexo separado, apresentando na mesma planta, nas quais as maiores quantidades são de flores masculinas presentes nas extremidades das ramificações e femininas nas ramificações, que se diferencia pela ausência de pedúnculo articulado, que são largamente pedunculadas
(ARRUDA et al., 2004; OPENSHAW, 2000).
As sementes secas medem de 1,5 a 2 cm de comprimento e 1,0 a 1,3 cm de largura;
superfície de coloração gravite; tegumento rijo, quebradiço, de fratura resinosa. O albume tem cor branca, oleaginoso, contendo o embrião provido de dois largos cotilédones achatados. A
semente também apresenta uma quantidade significativa de óleo, entre 27,90 a 37,33% da sua massa total. Amido, albuminóides e materiais minerais, (como cinzas e nitrogênio) também fazem parte da composição (ARRUDA et al., 2004).
O óleo pode ser extraido de forma mecânica (atráves de uma pressão aplicada por uma prensa hidráulica) ou química (reagindo com hexano), sua composição consiste em uma variação de triglicerideos, na qual pode ser empregado para a fabricação de sabões, na indústria de cosméticos e como um combustível renovável (OPENSHAW, 2000). No entanto, não é recomendável a utilização direta de óleos vegetais no motor, visto que apresentam uma elevada viscosidade devido a uma maior quantidade de carbonos em comparação com combustíveis derivados do petróleo, que provoca na máquina o entupimento das linhas de combustível, filtros e injetores. Portanto, faz necessário que haja uma conversão de óleo vegetal em moleculas menores, o que predominantemente é feito através de um processo de transesterificação catalisada por base, para formação de biodiesel, substituto do diesel de
petróleo (BASILI; FONTINE., 2012).
Segundo Basili e Fontine (2012), o biodiesel derivado do óleo de pinhão manso tem
como sua composição de ácidos graxos, correspontente a: oleico (43,1%), linoleico (34,3%), esteárico (6,9%), palmítico (4,2%) e outros ácidos (1,4%). É importante enfatizar que a variação percentual da concentração de ácidos graxos pode apresentar mudanças, dependendo de vários fatores, como: clima, solo, localidade geografia e período de plantação e colheita.
O pinhão manso pode ser plantado a partir de sementes, plântulas e estacas. A melhor época para o plantio é na estação quente antes ou no início das chuvas. É recomendado que o espaçamento fosse alinhado perpendicularmente (como um xadrez entre os arbustos), com a distância de 2 ± 3 m por 1,5 ± 3 m. Assim, haverá entre 1100 ± 3300 plantas por hectare para uma horta simples e dupla. A produção pode passar de 10 toneladas por hectare ao ano, ou seja, aproximadamente 4 toneladas de óleo extraído por hectare. (OPENSHAW, 2000).
Apesar de ser uma planta que se adéqua bem a lugares com solo degradados e com
baixa ocorrência de chuva, seu crescimento irá depender da fertilidade do solo e principalmente da ocorrência de chuvas. O baixo nível de nutrientes dificulta o
desenvolvimento das sementes, como também a estiagem, onde é necessário que o local plantado tenha pelo menos uma precipitação anual de chuvas acima de 600 mm
Segundo Openshaw (2000), mesmo o cultivo de Jatropha curcas demonstra um potencial rentável com presuposto comportamental de um investimento ambientalmente sustentável, que é algo de grande evidência e importância na atualidade. Por fatores técnicos e econômicos, todo o potencial do pinhão manso está longe de ser empregado. Os produtores geralmente não conseguem a saída ideal de produtos, consequência da pouca experiência em comercializar seus produtos em conjunto com a falta de organização e planejamento.
Além disso, outras informações importantes, como o controle de pragas (plantas daninhas, fungos, insetos, entre outros) são bastante limitadas, existe pouca literatura sobre o assunto, visto que o plantio em grandes extensões se espera que tenha presença desses agentes biológicos (FRANCO; GABRIE, 2008).
3.3.2. Transesterificação
As moléculas de triacilglicerídeos são formadas por três ácidos graxos de cadeia longa, ligados na forma de ésteres a uma molécula de glicerol (Figura 2). Esses ácidos graxos
apresentam variação na cadeia carbônica (representado na Figura 2 por R) com diferentes: número de carbonos, orientação, quantidade de insaturação e posição das ligações duplas, dependendo da espécie vegetal e animal que foi extraída o óleo (GERIS et al., 2007).
Figura 2. Representação da estrutura molecular do composto triacilglicerídeos.
H2C
HC
H2C
OCOR" OCOR'
OCOR"'
Fonte: Knothe e Gerpen, (2006).
Existem vários procedimentos químicos para transformar os triacilglicerídeos em biodiesel, visto que as características e propriedades físico-químicas dos ésteres de ácidos graxos são mais semelhantes ao diesel fóssil, como as moléculas são menores a viscosidade diminui e a eficiência na combustão aumenta. O procedimento mais conhecido e utilizado é a transesterificação, já que é um método simples e rápido, não demanda muitos recursos de reagentes e materiais (GERIS et al., 2007).
(geralmente metanol ou etanol por apresentar baixo custo e polaridade alta) na presença de um catalisador, que acelera e aumenta o rendimento da reação (Figura 3) (GERIS et al., 2007).
Figura 3. Representação química da reação de transesterificação.
H2C
HC
H2C
OCR OCR
OCR O
O
O
C
O
O R
R'
H2C
HC
H2C
OH OH
OH
OH
R' Catalisador
+ 3 3 +
triglicerídeos
Biodiesel
Glicerina
Fonte: Knothe e Gerpen, (2006).
Na reação completa de transesterificação são formados dois intermediários de reações, denominados de monoacilglicerídeos e diacilglicerídeos, para depois formarem os produtos finais, que constitui 3 mols de biodiesel para cada mol de Glicerina. A glicerina é o produto secundário, mais denso que o biodiesel, por isso, pode ser separado utilizando um funil de separação (GERIS et al., 2007).
Os catalisadores empregados na transesterificação podem ser um ácido forte, uma base forte ou enzimas. Em geral, é mais comum encontrar nas literaturas referentes ao
biocombustível, reações de transesterificação empregando a catalise básica, utilizando hidróxidos de metais alcalinos, tais como: hidróxido de potássio (KOH) e hidróxido de sódio
(NaOH) nas quais são observados melhores rendimentos e seletividade. Também se utilizam catalisadores básicos não iônicos, por que apresentam a vantagem de não formar sabão e outros produtos indesejáveis (GERIS et al., 2007).
Figura 4. Representação do mecanismo da reação de transesterificação, rota etílica e catálise básica.
O B O OCOR"
OCOR'''
O C
R'
O H
O
OCOR" OCOR'
O
C
R' O
O "ROCO
R'''OCO O
C R' O
"ROCO
R'''OCO HO
BH Diacilglicerídeos
Rota Etílica
Biodiesel
Fonte: Adaptado de Geris et al., (2007).
Na primeira etapa do mecanismo proposto ocorre a reação entre o etanol e a base forte (geralmente KOH e NaOH), a partir da protonação da base, deixando o etanol oxidado para reagir através de um ataque nucleofílico ao triacilglicerídeos. O Etóxido formado na primeira etapa ataca uma das carbonilas localizadas nos extremos da molécula, (por estar mais
desprotegida) deslocando a carga eletrônica da ligação π para o oxigênio. Em seguida, ocorre
um rearranjo eletrônico que acarreta na quebra da ligação entre o carbono carbonilico e o oxigênio ligado ao triacilglicerídeo, formando o biodiesel e um intermediário tetraédrico. Este intermediário irá reagir com o catalisador hidrogenado na primeira etapa, formando um diaciglicerídeos. Este mecanismo vai se repedir ainda duas vezes até formar glicerina e três moléculas de biodiesel (SILVA, 2005).
Na indústria, a reação de transesterificação utiliza-se de uma razão molar equivalente
a 1 mol de óleo, para cada 6 mols de álcool na presença de 0,4% de hidróxido de sódio ou de potássio, porque o meio básico apresenta melhor rendimento e menor tempo de reação do que
3.3.3. Purificação do Biodiesel
A purificação do biodiesel consiste na última etapa do processo de síntese do biodiesel, que tem com objetivo retirar o excesso de impurezas adquiridas pelo processo. As principais impurezas são os intermediários de reações monoacilglicerídeos e diacilglicerídeos formados pela reação incompleta de transeterificação, o excedente de catalisador, a glicerina que não foi retirada em sua totalidade na decantação, a água emulsificada e os materiais insaponificáveis presentes na própria matéria-prima (tocoferois, esterois, hidrocarbonetos, alcoóis e produtos de degradação) (COSTA NETO et al., 2011). De acordo com os padrões das normas europeia 14103 e da ANP 15764 o biodiesel tem que apresentar pelo menos 96,5% de pureza (PREDOJEVIC, 2008).
Para que o biodiesel tenha um alto nível de qualidade estabelecido pelas especificações EN 14214, se faz necessário que o produto final tenha o máximo de isenção
destas impurezas citadas, que podem provocar danos em várias partes dos motores, principalmente na câmara de combustão através do seu acúmulo nos bicos injetores, que
acarretam falhas no funcionamento de motores, formação de incrustações, depósitos de sabão e corrosividade das peças (COSTA NETO et al., 2011).
A purificação do biodiesel pode ocorrer de duas formas denominadas de via úmida e via seca (FACCINI, 2008).
3.3.3.1. Purificação via úmida
A purificação do biodiesel via úmida consiste na adição de água destilada morna (em geral 50 °C) para retirar o excesso impurezas, uma vez que grande parte das impurezas é altamente solúvel em água, como também a água apresenta uma densidade maior do que o biodiesel, sendo facilmente separada pelo processo de decantação, tornando muito eficiente na remoção de contaminantes (MARTIN et al., 2011). A eficiência da água destilada nas
remoções das impurezas aumenta com o aumento da temperatura e dos volumes adicionados no biodiesel (AROUA; ATADASHI; AZIZ, 2011).
Segundo Martin et al., (2011), por apresentar essas características, a água destilada foi há poucos anos o principal método de purificação do biodiesel. E até hoje é o método mais
No entanto, a lavagem com água apresenta muitas desvantagens, a principal é a grande quantidade de água utilizada na lavagem do biodiesel, segundo Freire (2009), pode variar entre 400 a 850 mL de água destilada a cada 100 mL de biodiesel, dependendo do catalisador utilizado. Dessa forma, a água gera uma grande quantidade de efluentes até a produção final do biodiesel, que embora tenha uma baixa toxidade, o efluente não deve ser descartado sem tratamento adequado (MARTIN et al., 2011; COSTA NETO et al., 2011).
Outro problema que a água destilada pode ocasionar no processo de purificação, está na capacidade em promover hidrólise dos ésteres, formando radicais livres dos ácidos graxos, acelerando a etapa de iniciação no processo de autoxidação, diminuindo a estabilidade oxidativa do biodiesel. Como também, está associada à proliferação de micro-organismos e perca significativa do biodiesel (MARTIN et al., 2011; COSTA NETO et al., 2011).
Para minimizar a grande quantidade de efluentes gerados pela água destilada na lavagem do biodiesel é utilizada uma solução de ácidos fortes pouco concentrada na primeira
lavagem, geralmente 10% da solução em relação a massa do biodiesel, o ácido reage com excesso de base, neutralizado o catalisador e decompondo o sabão formado e diminuindo a
quantidade de água de lavagem (AROUA, 2011).
O biodiesel é altamente hidrofílico, logo na purificação via úmida, o biodiesel absorve muita água, portanto se faz necessário passar por um processo de secagem com o intuito de apresentar um teor de umidade máxima de 0,05%, estipulado pela norma America Societ for Testing and Materials (ASTM) D6751 (CRUZ; LÔBO; FERREIRA, 2009). O processo de secagem mais usual é feita através de uma estufa convencional a 105 °C. Também está sendo empregada a secagem em baixa pressão, utilizando uma estufa a vácu o a 60 ºC e pressões próximas de -1 bar. Na secagem química são utilizados reagentes que absorvem a água sem degradar ou reagir com o biodiesel. (VASCONCELOS et al., 2009).
Secagem feita em temperaturas elevadas por um longo período de tempo, afeta consideravelmente a estabilidade do biodiesel pelas etapas iniciais dos processos de autoxidação com a formação de oxigênio singleto, que facilita o processo reacional com
ácidos graxos insaturados, que são altamente susceptíveis à oxidação e os principais constituintes do biodiesel de pinhão manso (VASCONCELOS et al., 2009; OPENSHAW,
3.3.3.2. Purificação Via Seca (adsorção)
Segundo Varques (2010), a adsorção é o processo de transferência de substâncias (adsorvatos) de uma fase fluída (gás ou líquido) para a superfície de uma fase sólida (adsorvente).
Na purificação do biodiesel via seca, os adsorventes substituem a água destilada no processo de lavagem. Os Adsorventes apresentam em suas superfícies sítios ativos que têm o potencial de absorção seletiva de compostos polares (ácidos e básicos) e de materiais hidrofílicos, tais como o glicerol, monoacilglicerídeos e diacilglicerídeos (FACCIN, 2008; AROUA, 2011).
Este tipo de purificação apresenta algumas vantagens em relação à purificação via úmida, uma vez que não gera efluentes residuais que acarreta no aumento dos custos de produção do biodiesel e diminuição do tempo do processo de purificação (AROUA, 2011).
A adsorção pode apresentar natureza química ou física. Na adsorção química o processo é quase sempre irreversível, já que a energia de ligação envolvida é da mesma ordem
de grandeza das ligações químicas de formação de compostos. Já as forças envolvidas na adsorção física incluem forças intermoleculares de Van der Waals e interações eletrostáticas compreendendo as interações de polarização e dipolo (VASQUES, 2010).
Existem vários tipos de adsorventes empregados no biodiesel, os mais comuns são: silicato de magnésio, silicato de alumínio, silicato de sódio, silicato de cálcio, sílica gel, carvão ativado, óxidos metálicos, carbonatos, alumina ativada, e argilas (FACCIN, 2008; AROUA, 2011).
Faccin (2008) analisou o desempenho de alguns desses adsorventes citados na purificação do biodiesel de soja, e concluiu que os únicos adsorventes que apresentavam resultados dentro das normas nacionais e europeias eram silicato de magnésio e sílica gel.
Em seu procedimento experimental, Faccin (2008), utilizou 1% de silicato de magnésio em relação à massa do biodiesel, a uma temperatura de 75 ºC sobre agitação
3.3.4. Parâmetros Físico-Químicos
A variedade de triglicérides produz uma composição diversificada de ésteres monoalquílico de ácidos graxos com variações de quantidades de carbonos e insaturações, afetando os fatores que influência as propriedades e características do biodiesel e, consequentemente afeta na variação do desempenho do motor e na sua armazenagem. Portanto, se faz necessário o estudo dos aspectos físico-químico do biodiesel em consequência dessa variação de composição (FONSECA et al., 2010).
3.3.4.1. Viscosidade
A viscosidade é a medida da resistência da vazão em relação à fricção ou atrito interno ao escoamento de um líquido, é uma propriedade intrínseca dos óleos vegetais
(RAMOS et al., 2000; KNOTHE; GERPEN, 2006). Quanto maior a viscosidade do combustível, menor será a capacidade de atomização do combustível na câmara de
combustão, no momento de sua injeção. Acarretando a formação de depósitos no motor (KNOTHE; GERPEN, 2006).
A viscosidade surge através das forças intermoleculares de um líquido, mantendo-as unidas e restringindo seu movimento. A viscosidade aumenta em proporção ao número de átomos de carbono, ou seja, ao tamanho das cadeias, visto que quanto maior o tamanho da cadeia, maior a probabilidade das moléculas se entrelaçarem uns nos outros através das forças intermoleculares dificultando seu movimento. E diminui quando ocorre um aumento na insaturação, na qual, as configurações trans, apresentam viscosidade maior que a configuração cis (ATKINS 2005; KNOTHE; GERPEN, 2006).
A viscosidade diminui com o aumento da temperatura, visto que as moléculas com maior energia conseguem se deslocar mais facilmente. No entanto, o aumento da temperatura pode influenciar na degradação do óleo em função do tempo de degradação, que vai ocasionar
um aumento na viscosidade do mesmo (ZUNIGAR et al., 2011).
Em comparação ao diesel fóssil, os biodieseis apresentam maior grau de viscosidade,
que por sua vez tem uma menor viscosidade do que apresentada no seu óleo vegetal de origem. Principalmente se o óleo é derivado de mamona, que apresenta uma viscosidade
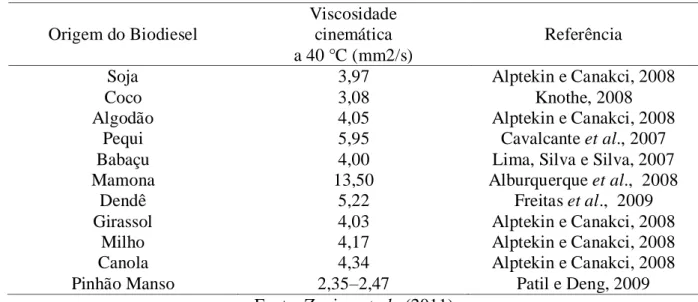
Portanto, como o biodiesel é composto por uma variedade de ésteres alquílico de ácidos graxos, proveniente de várias fontes de óleos vegetais e gordura animal. Subtende-se que cada matéria prima contenha sua viscosidade característica (Tabela 4).
Tabela 4. Viscosidade do Biodiesel de Várias Espécies Vegetais
Origem do Biodiesel
Viscosidade cinemática a 40 °C (mm2/s)
Referência
Soja 3,97 Alptekin e Canakci, 2008
Coco 3,08 Knothe, 2008
Algodão 4,05 Alptekin e Canakci, 2008
Pequi 5,95 Cavalcante et al., 2007
Babaçu 4,00 Lima, Silva e Silva, 2007
Mamona 13,50 Alburquerque et al., 2008
Dendê 5,22 Freitas et al., 2009
Girassol 4,03 Alptekin e Canakci, 2008
Milho 4,17 Alptekin e Canakci, 2008
Canola 4,34 Alptekin e Canakci, 2008
Pinhão Manso 2,35–2,47 Patil e Deng, 2009
Fonte: Zuniga et al., (2011).
3.3.4.2. Densidade
A densidade é uma propriedade da matéria que pode ser definida como a quantidade de massa de uma substância contida por unidade de volume. É empregada como indicativo de como a matéria está organizada num corpo, ou seja, matéria com alta densidade apresenta estrutura molecular compacta, podendo ser calculada utilizando uma expressão matemática simples, na qual a densidade é igual à massa sobre volume.
A densidade do óleo diesel fóssil é ligeiramente inferior ao apresentado por todos os biodieseis obtidos a partir de diferentes matérias primas, os quais possuem densidades variando entre 0,86 e 0,90 g/cm3 dependendo da composição dos monoestéres de ácidos graxos (ZUNIGAR, et al., 2011).
Tal parâmetro exerce um efeito direto sobre o desempenho do motor. Segundo Folquenin (2008), os valores de densidades acima da margem de regulagem podem elevar à mistura de ar/combustível, aumentando a emissão de poluentes como hidrocarbonetos,
monóxido de carbono e material particulado. Valores de densidade baixa favorecem a uma má formação de uma mistura de ar/combustível, que diminui potência do motor e aumenta o
Além de tudo, a densidade (Tabela 5) está relacionada diretamente com outros parâmetros físico-químicos de grande importância para o desempenho do motor alimentado pelo biodiesel, como é no caso do número de cetano e do poder calorífico (ALPTEKIN; CANAKC, 2008).
Tabela 5. Densidade do biodiesel obtido de diferentes origens.
Origem do Biodiesel Densidade a 15°C (g/cm3) Referência
Soja 0,88 Alptekin e Canakci, 2008
Algodão 0,88 Alptekin e Canakci, 2008
Babaçu 0,88 Lima et al., 2007
Mamona 0,917 a 20°C Mundstein, Gonçalves e Mota, 2007
Dendê 50 Almeida, 2001
Girassol 0,88 Alptekin e Canakci, 2008
Milho 0,88 Alptekin e Canakci, 2008
Canola 0,88 Alptekin e Canakci, 2008
Pinhão Manso 0,86 – 0,88 Patil e Deng, 2009
Fonte: Zuniga et al., (2011).
3.3.4.3. Número de Cetano
O número de cetano (NC), conceitualmente semelhante à escala de octanagem empregada para a gasolina, (termo britânico: petróleo) estabelecida para descrever a qualidade de ignição do diesel fóssil e seus componentes. Geralmente, um combustível que apresenta um alto número de octanas tende a ter um NC baixo e vice versa. O 2,2,4-trimetilpentano (iso-octano), é o padrão de alta qualidade e principal referência (ou principal combustível de referência PCR) para a escala de octanas da gasolina, apresentado número de octanas 100; enquanto que o n-heptano, representa o PCR de baixa qualidade, cujo número de octanas é 0. Para a escala de cetanos, o hexadecano (C16H34) designado por cetano, que dá origem ao
nome da escala (KNOTHE; GERPEN, 2006; ZUNIGA, et at., 2011).
As ramificações e o comprimento da cadeia são fatores preponderantes para influenciar o valor do número de cetano. Na qual, seu valor aumenta nas cadeias mais longas e diminui em relação ao grau de ramificação do composto (KNOTHE; GERPEN, 2006; BUENO, 2007).
O número de cetano de um combustível/biocombustível é determinado pela comparação de sua velocidade de ignição com as de um combustível de referência, que
(PIMENTEL; BELCHIOR, 2002; ZUNIGA et al., 2011). Assim, quanto menor for o tempo de retardamento da ignição, maior será o valor do número de cetano (KNOTHE; GERPEN, 2006). E quanto maior for o número de cetano do combustível, melhor será sua combustão em motor diesel (ZUNIGA et al., 2011).
Valores de NC baixos podem provocar: falhas no motor, trepidação, combustão incompleta; aumento excessivo da temperatura do ar e aquecimento lento do motor. No entanto, assim como os valores muito baixos do número de cetona, os valores muito altos deste parâmetro também podem ocasionar problemas no motor, já que a combustão pode ocorrer antes da mistura completa do ar com o combustível, acarretando numa combustão incompleta em conjunto com a liberação de fumaça (KNOTHE; GERPEN, 2006).
Por isso, foram estabelecidos padrões de qualidade do combustível/biocombustível em relação ao valor de NC em todo mundo. A norma ASTM D975 para combustível de diesel fóssil, utiliza como composto referência o hexadecano, na qual exigem um NC mínimo de 40,
enquanto o biodiesel devido aos seus muitos compostos graxos apresenta um valor mínimo de 47 (ASTM D6751) ou 51 (especificação europeia EN 14214) (KNOTHE; GERPEN, 2006).
Na Tabela 6, encontram-se os valores do número de cetano do biodiesel de várias oleaginosas.
Tabela 6. Número de Cetano do Biodiesel de Várias Espécies Vegetais.
Origem do Biodiesel Número de Cetano Referência
Soja 60,1 Alptekin e Canakci, 2008
Coco 67,4 Knothe, 2008
Algodão 60,3 Alptekin e Canakci, 2008
Pequi 60 Cavalcante et al., 2007
Babaçu 65 Turchiello, 2005
Mamona 46,5 Peres et al., 2007
Dendê 50 Almeida, 2001
Girassol 60,9 Alptekin e Canakci, 2008
Milho 60,9 Alptekin e Canakci, 2008
Canola 61,5 Alptekin e Canakci, 2008
Pinhão Manso 60,74 – 63,27 Patil e Deng, 2009
3.3.4.4. Ponto de Fulgor
O ponto de fulgor é definido como a temperatura mínima na qual é observada a liberação de vapores de um líquido combustível ou inflamável, em quantidades necessárias para formar uma mistura inflamável com o ar (CRUZ; LÔBO; FERREIRA, 2009; ZUNIGA,
et al., 2011). Em comparação com o diesel fóssil, o biodiesel apresenta valores de ponto de
fulgor, consideravelmente mais elevados, na qual varia entre 107°C a 205°C (Tabela 7), no entanto, pequenas quantidades de álcool adicionadas ao biodiesel ocasionam uma diminuição bastante relevante neste valor (CRUZ; LÔBO; FERREIRA, 2009).
O ponto de fulgor alto como o do biodiesel pode ser parâmetro muito importante em termos de segurança, pelo fato de poder ser manuseado, armazenado e transportado em condições ambientes sem oferecer riscos. Assim, o biodiesel constitui uma importante vantagem em relação a diesel fóssil, visto que seu alto ponto de fulgor reflete em um
combustível mais seguro, sem que afete a combustão direta no motor (CRUZ; LÔBO; FERREIRA, 2009; ZUNIGA et at., 2011).
Em relação aos valores de ponto de fulgor permitidos para o biodiesel, a Resolução ANP n. 04/2012 estabelece para o biodiesel nacional o valor mínimo de ponto de fulgor igual a 100°C (Tabela 7), (ZUNIGA et al., 2011).
Tabela 7. Ponto de Fulgor do Biodiesel de Várias Espécies Vegetais.
Origem do Biodiesel Ponto de Fulgor (°C) Referência
Soja 139 Alptekin e Canakci, 2008
Algodão 149 Alptekin e Canakci, 2008
Pequi 142 Cavalcante et al., 2007
Babaçu 112 Lima, Silval e Silva, 2007
Dendê 174 Almeida, 2001
Girassol 157 Alptekin e Canakci, 2008
Milho 192 Alptekin e Canakci, 2008
Canola 107 Alptekin e Canakci, 2008
Pinhão Manso 207 Evangelista, 2009
3.3.4.5. Ponto de Névoa e Ponto de Fluidez
De acordo com Ramos et al., (2000), Knothe e Gerpen (2006), o ponto de névoa corresponde à temperatura inicial em que a cristalização do óleo se torna visível [diâmetro (d)
≥ 0,5μm], formando uma suspensão túrbida ou enevoada, que influencia negativamente o sistema de alimentação do motor. Principalmente quando o motor é acionado em temperaturas a baixo do ponto de névoa, formando cristais (d~0,5-1 mm x 0,01 mm de espessura) que se fundem uns com os outros, formando grandes aglomerados que podem dificultar ou impedir o livre fluxo do biodiesel na tubulação e no filtro, ocasionando problema na partida do motor (KNOTHE; GERPEN, 2006).
Os ácidos que apresentam as cadeias mais curtas e insaturações são os menos suscetíveis aos efeitos negativos do motor proporcionados pelo ponto de névoa (Tabela 8). Na qual, quimicamente falando, ocorre através da capacidade de uma molécula se encaixar
facilmente numa rede cristalina através de suas forças intermoleculares. Cadeias pequenas de ésteres monoalquílico de ácidos graxos são mais polares que as cadeias maiores, dificultando
as interações intermoleculares. As ligações duplas impedem a livre rotação dos átomos de carbono envolvido no sistema, deixando a cadeia menos linear, se ajustando de forma menos eficiente, uma com as outras, em comparação com as cadeias saturadas (MORETTO; FETT 1998; MORRISON; BOYD, 2005).
Em relação ao ponto de fluidez, Zuniga et al., (2011) afirma “O ponto de fluidez
pode ser definido como a mais baixa temperatura em que o líquido escoa livremente”. Antes de o combustível entrar em ponto de névoa, primeiramente entra em ponto de fluidez, formando cristais invisíveis a olho nu, ou seja, com o diâmetro menor 0,5μm, que ficará disseminada na superfície do óleo.
Este parâmetro é utilizado para caracterizar a operacionalidade de escoamento do
combustível em baixas temperaturas, já que o ponto de fluidez afeta o emprego do
combustível no motor, principalmente em condições de clima frio. Por esta razão, o biodiesel