PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA
SIMULAÇÃO, POR DINÂMICA MOLECULAR, DAS INTERAÇÕES
ÁGUA-ETANOL-NaCl COM FOSFOLIPÍDEOS DE MEMBRANA
GUILHERME NOBRE LIMA DO NASCIMENTO
GUILHERME NOBRE LIMA DO NASCIMENTO
SIMULAÇÃO, POR DINÂMICA MOLECULAR, DAS INTERAÇÕES
ÁGUA-ETANOL-NaCl COM FOSFOLIPÍDEOS DE MEMBRANA
Tese apresentada ao Programa de Pós-Graduação em Química do Instituto de Química da Universidade Federal de Uberlândia, como requisito parcial para obtenção do título de Doutor em Química.
Área de concentração: Química.
Orientador:
Dr. Antonio Eduardo da Hora Machado.
Co-orientadores:
Dr. Eduardo de Faria Franca;
Dr. Tales Alexandre Aversi-Ferreira.
AGRADECIMENTOS
A Deus pela vida e por todas as oportunidades de crescimento; Aos meus familiares, pelo carinho, amor, amizade e suporte;
A minha esposa Lúcia Helena Almeida Gratão pela paciência, carinho e apoio;
Ao professor e orientador Antonio Eduardo da Hora Machado pela confiança, ensinamentos, paciência e apoio;
Ao professor e co-orientador Tales Alexandre Aversi-Ferreira, pelo incentivo, paciência, ensinamentos e amizade, e sua família, Roqueline e Emmanuel;
Ao professor e co-orientador Eduardo de Faria Franca pela ajuda, ensinamentos e paciência;
A todos os amigos e alunos do LABINECOP/LACIBS pelo carinho e apoio;
Aos colegas do LCQC e LAFOT-CM, UFU;
RESUMO
Eritrócitos, hemácias ou células vermelhas do sangue, são células únicas dentre as células de mamíferos. São isentas de organelas e núcleo, contendo em seu interior hemoglobina, circundada por uma membrana celular. Responsáveis pelo transporte de oxigênio dos pulmões aos tecidos, e dióxido de carbono dos tecidos aos pulmões, o que torna sua integridade importante para o bom funcionamento de todo o organismo. Uma das substâncias que podem gerar efeito sobre a membrana de eritrócitos é o etanol, encontrado em uma grande variedade de produtos. Neste trabalho, estudou-se o efeito das interações entre etanol, água e cloreto de sódio e fosfolipídeos de membrana, usando ensaios experimentais combinados a abordagem de dinâmica molecular. O sangue de dois ratos jovens foi utilizado nos ensaios de fragilidade osmótica de eritrócitos com concentrações crescentes de etanol, de 0 a 50% (v/v). Paralelamente, um estudo teórico envolvendo simulações por dinâmica molecular foi realizado, usando o pacote computacional GROMACS, onde se empregou dipalmitoilfosfatidilcolina – DPPC como modelo de membrana. Nas simulações, empregou-se o campo de força GROMOS 53a6, considerando um tempo de 60 ns para cada sistema com concentrações diferentes de etanol. Os resultados experimentais mostram que com o aumento da concentração de etanol há aumento da lise celular dos eritrócitos. No entanto, a partir de valores próximos a 35% (v/v), a lise é diminuída. Os dados teóricos ilustraram a afinidade do etanol pelos lipídeos de membrana, gerando alterações na orientação das cargas ao longo das bicamadas, formação de poros, alteração na permeabilidade pela mesma e deformações na maior concentração. Constata-se, com este estudo, que o efeito deletério do etanol sobre a membrana de eritrócitos não é dose-dependente e que o mesmo atua diretamente, por interações, com a estrutura da bicamada lipídica.
ABSTRACT
Erythrocytes or red blood cells are single cells among mammalian cells. They contain no organelles and nucleus, containing hemoglobin inside, surrounded by a membrane. They are responsible for transporting oxygen from the lungs to tissues and carbon dioxide from tissues to the lungs, which makes its integrity important for the proper functioning of the whole organism. One of the substances that may cause effects on erythrocyte membrane is ethanol, found in a wide variety of products. In this work, the interactions between ethanol, water and sodium chloride with membrane phospholipids was evaluated using experimental assays combined to molecular dynamics approach. The blood of two young rats was used to evaluate the effect of increasing concentrations of ethanol, 0-50% (v/v) on the osmotic fragility of the cells. In addition, a theoretical study involving molecular dynamics simulation was performed using the software package GROMACS, in which dipalmitoylphosphatidylcholine - DPPC was used as membrane model. GROMOS 53a6 force field was used in the computer simulations, considering a time of 60 ns for each system. The experimental results show that increasing ethanol concentration raises the lyse of the erythrocytes. However, for values higher or equal to 35% (v/v), the lysis is reduced. The theoretical data illustrated the affinity of ethanol by the membrane lipids, generating changes in the charge orientation along the bilayer, forming pores, changing the permeability and deforming the bilayer in high concentration of ethanol. It is noted, in this study, that the deleterious effect of ethanol on the erythrocyte membrane is non-dose dependent and that it acts, by interaction, with the structure of the lipid bilayer.
LISTA DE FIGURAS
LISTA DE TABELAS
LISTA DE ABREVIATURAS E SIGLAS
DL50 – dose letal media
DPPC – dipalmitoilfosfatidilcolina
GABA –ácido gama aminobutírico (neurotransmissor)
IUPAC - União Internacional de Química Pura e Aplicada (International Union of Pure and Applied Chemistry)
ME – meio extracelular MI – meio intracelular min. – minutos
SUMÁRIO
RESUMO... vi
ABSTRACT ... vii
LISTA DE FIGURAS ... viii
LISTA DE TABELAS ... xii
LISTA DE ABREVIATURAS E SIGLAS ... xiii
1 INTRODUÇÃO ... 1
2 FUNDAMENTAÇÃO BIOLÓGICA ... 2
2.1 Membrana celular ... 2
2.1.1 Constituição e funções ... 2
2.1.2 Estrutura e estabilidade de membranas – íons e água ... 4
2.2 Eritrócitos ... 5
2.2.1 Funções e estrutura ... 5
2.2.2 Morfologia e mudanças no formato da membrana de eritrócitos... 7
2.3 Etanol ... 8
2.3.1 Características ... 8
2.3.2 Efeitos biológicos ... 9
2.3.3 Efeitos do etanol sobre a membrana ... 12
3 FUNDAMENTAÇÃO TEÓRICA ... 13
3.1 Estudos teóricos ... 13
3.1.1 Estudos de dinâmica molecular ... 16
3.1.2 Modelos de membrana ... 17
3.1.3 Interações intermoleculares ... 19
4 OBJETIVOS ... 23
4.1 Objetivo geral ... 23
4.2 Objetivos específicos ... 23
5 MATERIAIS E MÉTODOS... 24
5.1 Teste in vitro do etanol sobre a membrana de eritrócitos ... 24
5.1.1 Obtenção do material biológico ... 24
5.1.2 Soluções-teste ... 24
5.1.3 Teste de fragilidade osmótica ... 24
5.1.4 Análise estatística ... 24
5.2 Estudo por dinâmica molecular ... 25
5.2.1 Estrutura básica ... 25
5.2.1.1 Célula básica ... 25
5.2.1.2 Célula básica de etanol ... 27
5.2.3 Detalhes computacionais ... 29
6 RESULTADOS E DISCUSSÃO ... 30
6.1 Teste in vitro do etanol sobre a membrana de eritrócitos ... 30
6.2 Simulações de dinâmica molecular ... 32
6.2.1 Energia total dos sistemas simulados ... 32
6.2.2 Visão geral dos sistemas estudados ... 35
6.2.3 Sistema na ausência de etanol ... 37
6.2.4 Sistema com etanol a 20%(v/v) ... 41
6.2.5 Sistema com etanol a 35%(v/v) ... 44
6.2.6 Sistema com etanol a 50%(v/v) ... 47
6.2.7 Análise geral dos resultados e discussões ... 51
7 CONCLUSÃO ... 54
8 PERSPECTIVAS ... 55
1 INTRODUÇÃO
O etanol (CH3CH2OH; PM: 46,07) é um álcool com características anfifílicas presente em bebidas alcoólicas, que são ingeridas em concentrações de 3 a 60%(v/v). É absorvido rapidamente pelo estomago e intestino delgado (Caballería, 2003; Umulis et al., 2005), locais onde verifica-se efeitos danosos dessa substância (Bujanda, 2000; Swanson et al., 2010).
O etanol está relacionado com mais de 60 condições médicas diferentes (Room et al., 2005) tais como a síndrome alcoólica fetal (Aversi-Ferreira e Nascimento, 2008; Ikonomidou et al., 2000; Armstrong e Abel; 2000; Burd et al., 2003), má formação do sistema neural em fetos (Lopes et al., 2009; Aversi-Ferreira et al., 2004; Ferreira et al., 2005; Ferreira e Penha-Silva, 2005; Aversi-Ferreira et al., 2006), doenças cardiovasculares (Brien et al., 2011) e distúrbios cognitivos (Brust, 2010; Gonthier et al., 2004; Kim et al., 2012).
Alguns trabalhos de simulação de dinâmica molecular verificaram a afinidade do etanol por fosfolipídeos de membrana, com alterações das propriedades da membrana e destruição da estrutura em bicamada (Feller et al., 2002; Patra et al., 2006; Gurtovenko e Anwar; 2009). Penha-Silva e colaboradores (2008), em estudo in vitro, observaram lise de eritrócitos humanos frente à exposição ao etanol em diferentes concentrações.
O etanol causa efeito depressor no sistema neural central, possivelmente por mecanismo de ação semelhante ao observado com os barbitúricos ao inibir o sistema Gabaérgico. Vale ressaltar que este é o segundo tecido do organismo humano com maior concentração de lipídeos (Salvati et al., 2000).
2 FUNDAMENTAÇÃO BIOLÓGICA
2.1 Membrana celular
2.1.1 Constituição e funções
Membrana celular ou membrana plasmática é um sistema dinâmico e complexo que constitui a parte mais externa do citoplasma celular. É composta de lipídeos, proteínas e glicídios, em proporções que variam de acordo com o tipo de membrana (ENGELMAN, 2005; JUNQUEIRA e CARNEIRO, 2008; RODRIGUES et al., 2009). A razão em massa de lipídeos e proteínas varia de 0,25 a 4,00. Porém, na maioria das membranas, a espécie predominante são os lipídeos, que se apresentam heterogêneos quanto ao tamanho da cadeia carbônica, saturação e estrutura da cabeça polar (BOCKMANN et al., 2003).
Dos lipídeos presentes nas membranas biológicas, há os fosfolipídeos, os esfingolipídeos e os esteróis (CASCIO, 2005). Na maioria das membranas, aproximadamente 10% dos lipídeos apresentam-se polarizados, o restante está na forma zwiterionica (BOCKMANN et al., 2003). Os lipídeos não se encontram em forma estática, fixados em um determinado ponto, eles apresentam movimentos nos sentidos horizontal e vertical da membrana, além de poder trocar de camada através em um movimento conhecido como flip-flop (translocação transmembrana) (Fig. 1) (GURTOVENKO e ILPO, 2007).
Figura 1. Modelo de membrana celular, ilustrando o movimento horizontal, vertical e flip-flop
O colesterol é um esterol constituinte da membrana responsável por diferentes funções como: permeabilidade da membrana, organização lateral de lipídeos, transdução de sinais e passagem de substâncias através da membrana (MAXFIELD e TABAS, 2005; WUSTNER, 2007).
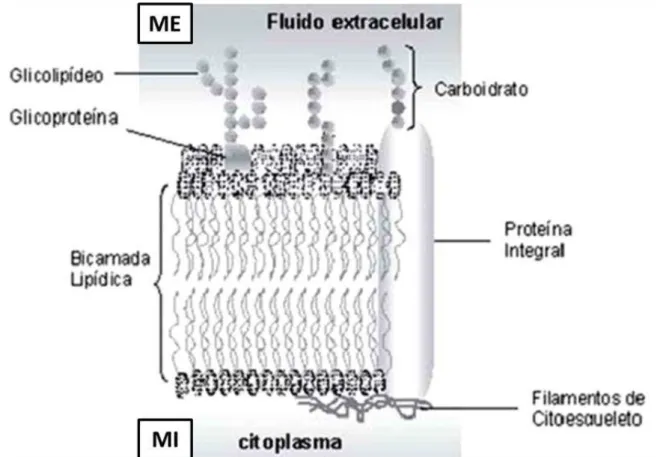
A organização das membranas desenvolve-se em uma arquitetura central em dupla camada de lipídeos (LEHNINGER et al., 2007). Singer e Nicholson (1972) propuseram um modelo conhecido como mosaico fluido (Fig. 2) para descrever a estrutura básica de uma membrana celular, onde se torna possível a movimentação de substâncias.
Figura 2. Modelo mosaico fluido da estrutura de uma membrana celular evidenciando a
bicamada lipídica e demais constituintes (MURADOR e DEFFUNE, 2007). ME = meio extracelular; MI = meio intracelular.
2.1.2 Estrutura e estabilidade de membranas – íons e água
As membranas biológicas têm cerca de 5 a 10 nm de espessura (PELTTARI e HELMINEN, 1979), o que a torna não visível à microscopia óptica, visualizada apenas em eletromicrografia, semelhante a duas linhas escuras separadas por uma linha central clara (Fig. 3).
Figura 3. Eletromicrografia de membrana celular de eritrócito humano (100.000X)
(ROBERTSON, 1981).
As células são circundadas por solução aquosa tamponada, em pH diferentes de acordo com o compartimento em que se encontram, e com presença de diferentes íons, Na+, K+, Ca2+, Mg2+ e Cl-, com variadas concentrações tanto no MI quanto no ME. A estrutura da bicamada lipídica é mantida pela presença desta solução aquosa, que gera repulsão entre esta e os lipídeos, os quais aprisionam suas cadeias carbônicas no interior da bicamada onde se interagem por interações não-covalentes, como as interações hidrofóbicas e forças de van der Walls (CAMPBELL, 2000). Mantendo, por outro lado, na porção externa da bicamada, as cabeças polares, que são capazes de interagir com a fase aquosa, por interações hidrofílicas (YEAGLE, 1989).
Esta solução aquosa, além de ditar função sobre a manutenção da estrutura, mencionada acima, exerce função sobre as transições de fase, ou de transporte através da membrana (YEAGLE, 1989).
A permeabilidade através da membrana se deve, entre outros fatores, a diferença na concentração de colesterol na mesma (TSUDA e NISHIO, 2003), à falta de ligações fortes entre as moléculas (ligações covalentes) e a presença de interações fracas que as mantêm. Fatores intrínsecos às moléculas, como o peso molecular e polaridade, também afetam a permeabilidade das mesmas pela bicamada, sendo esta impermeável aos íons, que dependem de canais iônicos para sua passagem ao meio intracelular. Apresenta ainda permeabilidade a água e aos gases oxigênio e carbônico (GOLDBERG et al., 2004; AGRE, 2006; WANG et al., 2007).
A integridade da estrutura das membranas pode ser afetada facilmente por uma série de eventos físicos, químicos e biológicos. Alterações de temperatura, concentrações iônicas, e substâncias como fármacos, drogas e nutrientes, por exemplo, o etanol, podem gerar danos às membranas, que por sua vez podem gerar alterações de função e, consequentemente, na função do órgão ou organismo afetado.
2.2 Eritrócitos
2.2.1 Funções e estrutura
Os eritrócitos, hemácias ou células vermelhas do sangue, são células únicas dentre as células de mamíferos. Viajam pelo sistema cardiovascular, por vasos de calibres diversos, como células individuais. Responsáveis pelo transporte de oxigênio dos pulmões aos tecidos, e dióxido de carbono dos tecidos aos pulmões, o que torna sua integridade importante para o bom funcionamento de todo o organismo, visto que a baixa oxigenação pode gerar necroses entre outros danos teciduais.
Figura 4. Estrutura da membrana de um eritrócito evidenciando os domínios da bicamada e
do citoesqueleto. (F – fosfatidilcolina; ES – esfingomielina; PI – proteína integral; CL – colesterol; FS – fosfatidilserina; FE – fosfatidiletanolamina).
O domínio da bicamada de eritrócitos é formado por partes ligeiramente iguais de lipídeos e proteínas. Os lipídeos encontrados são o colesterol, igualmente distribuídos em ambas às faces da bicamada, e fosfolipídeos que tem suas constituições diferenciadas em cada lado da bicamada. Exemplos de alguns fosfolipídeos encontrados nas membranas são as fosfatidilcolinas; responsáveis por maior fluidez; e as esfingomielinas responsáveis por maior rigidez. Permeando estes lipídeos encontram-se proteínas integrais que se estendem de dentro a fora do eritrócito (ELGSAETER et al., 1986; MURADOR e DEFFUNE, 2007).
2.2.2 Morfologia e mudanças no formato da membrana de eritrócitos
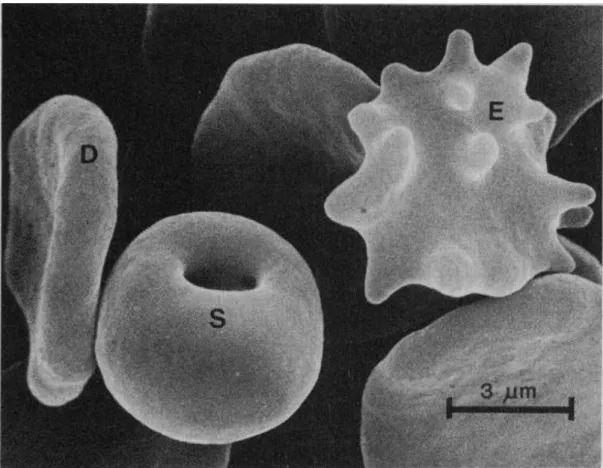
A morfologia normal dos eritrócitos é a forma de um disco bicôncavo conhecido como discoide (Fig. 5), mantida através de uma série de fatores, citados anteriormente, os quais em conjunto com os domínios da bicamada lipídica e do citoesqueleto assumem o menor nível de energia livre, obtendo a forma mais estável destas células (ELGSAETER et al., 1986).
Os eritrócitos podem assumir diferentes estruturas variando de formas com espículas ou contraídas conhecida como equinócitos e formas expandidas conhecidas como estomatócitos (ELGSAETER et al., 1986; SMITH, 1987; STOOKE et al., 1986) (Fig. 5).
Figura 5. Eletromicrografia de diferentes formas de eritrócitos; discoide (D), estomatócito (S)
e equinócito (E). (ELGSAETER et al., 1986).
As alterações na morfologia dos eritrócitos se devem a alterações diretas sobre a membrana celular (GEDDE e HUESTIS, 1997), e fatores como substâncias exógenas, fármacos e intoxicantes podem alterar esta estrutura (NELSON et al., 1983), podendo gerar a lise celular (RODRIGUES et al., 2009 ).
mesmas, pois aliado a todas as características mencionadas anteriormente adiciona-se a fácil disponibilidade e acessibilidade destas células (MURADOR e DEFFUNE, 2007; RODRIGUES et al., 2009).
Uma das substâncias que podem gerar efeito sobre a membrana de eritrócitos é o etanol.
2.3 Etanol
2.3.1 Características
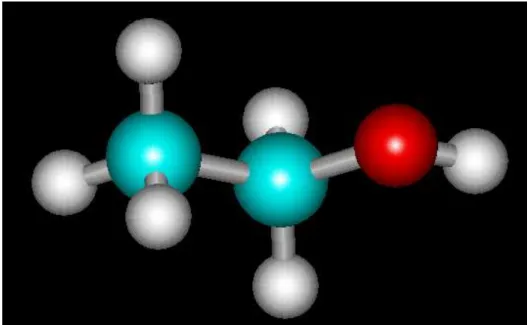
O etanol está presente em uma grande variedade de bebidas tais como cerveja, vinho, uísque, cachaça dentre outras; em combustíveis, produtos de limpeza, perfumes, produtos cosméticos e produtos de uso terapêutico. O etanol (Fig. 6) é um álcool, líquido incolor a temperatura ambiente, volátil, inflamável e de odor característico (FILHO et al., 2001; LARINI, 2003). Apresenta massa molecular de 46,07 g/mol, fórmula molecular CH3CH2OH, e constante dielétrica de 25,7 a 20°C. O grupo hidroxila confere polaridade à molécula e é responsável pelas interações intermoleculares com a água, sendo verificadas em testes de espectroscopia no infravermelho as ligações de hidrogênios (PEREIRA e ANDRADE, 1998). É uma molécula anfipática sendo miscível em água e gordura.
Figura 6. Estrutura molecular do etanol (bolas azuis: carbono; bolas brancas: hidrogênio e
2.3.2 Efeitos biológicos
O consumo de etanol através de bebidas alcoólicas gera dependência conhecida como alcoolismo, que é uma toxicomania considerada problema de saúde pública (ROOM et al., 2005) e que além de propiciar danos aos indivíduos, está relacionada a diversas fatalidades por acidentes de transito (LARINI, 2003).
O etanol é rapidamente absorvido pelo trato gastrointestinal se distribuindo por todos os tecidos. A concentração plasmática máxima de etanol é verificada em um tempo médio de 30 a 60 minutos, com variação de gênero, as mulheres apresentam concentrações plasmáticas maiores que os homens em um consumo de mesma dose (FILHO et al., 2001). A dose letal média (DL50) de etanol para o homem é de 7,5 – 9,5 g/Kg, por via oral. Em uma concentração plasmáticas de 4 g/L de sangue já é capaz de induzir o coma (LARINI, 2003).
Os efeitos observados em indivíduos expostos a esta substância são delírios, alucinações, sensação de despersonalização, ação anestésica e depressora do sistema neural central, problemas relacionados ao crescimento em adolescentes e efeitos sobre a embriogênese, como a síndrome alcóolica fetal (RILEY, 1990; HOLMUHAMEDOV e LEMASTERS; 2009; AVERSI-FERREIRA e NASCIMENTO, 2008). O mecanismo de ação não está muito bem definido, e algumas hipóteses propõe o efeito anestésico do etanol devido à ação deste sobre as proteínas e/ou lipídeos de membrana, potencializando o influxo de cloretos, logo o efeito do neurotransmissor GABA, similar à ação dos benzodiazepínicos e barbitúricos (BRUST, 2010).
Figura 7. Representação esquemática das ações do etanol sobre eritrócitos em solução
salina. Eritrócitos podem existir em estados morfológicos estomatócitos (S) ou um estado equinócitos (D). Cada estado morfológico pode representar um conjunto de formas diferentes. Baixas concentrações de etanol promovem a lise do estado S (rota 1). As concentrações de etanol intermediárias promovem a conversão dos eritrócitos do estado S para o estado D (rota 2) através do aumento da pressão osmótica. Altas concentrações de etanol promovem a lise do estado D (rota 3) (PENHA-SILVA et al., 2008).
Este efeito anômalo do etanol provavelmente não está condicionado ao fator força iônica, mas sim à sua interação direta com os fosfolipídeos de membrana, sendo este o questionamento deste trabalho.
É sabido que moléculas apolares em meio aquoso, diminuem a entropia do sistema em uma maior organização das moléculas de água para estabilização do mesmo, o que não é viável em termos termodinâmicos, logo não solubilizando as moléculas apolares em água (LEHNINGER et al. 2007). A associação do etanol com lipídeos de membrana é realizada por interações tipo van der Waals entre a parte apolar do etanol e do lipídeo (GURTOVENKO e ANWAR, 2009). Por outro lado, ligações de hidrogênio entre o etanol e a água devem favorecer um aumento da entropia do sistema.
Além dos efeitos já mencionados, o etanol é também responsável por uma síndrome conhecida como síndrome alcoólica fetal. Durante o período gestacional,
mães que fazem uso de bebidas alcoólicas, podem afetar o desenvolvimento embrionário do fetal, causando mal formações, pois esta substância afeta as células em diferenciação no tudo neural (AVERSI-FERREIRA et al., 2004). Este efeito é dependente não apenas da concentração do etanol, mas também do tempo de exposição ou mesmo o dia da exposição (AVERSI-FERREIRA e NASCIMENTO, 2008), onde o período inicial da gestação é o mais crítico. A criança exposta a esta substância, pode nascer com deficiências físicas e cognitivas (Fig.8).
Figura 8. Criança com síndrome alcoólica fetal (RIBEIRO et al., 1995).
2.3.3 Efeitos do etanol sobre a membrana
O estudo e entendimento das alterações nas propriedades e funções das membranas celulares em presença de solventes anfifílicos apresentam interesses em diferentes áreas biomédicas, como anestesiologia (CASCALES et al., 1998; KOUBI et al., 2001), criopreservação e solubilidade de membranas (GURTOVENKO e ANWAR, 2009).
Hipóteses sobre o mecanismo de ação dos anestésicos são discutidas e investigadas a mais de um século (TU et al., 1998) podendo ser divididas em duas vertentes, a primeira prediz que os efeitos destes fármacos são efetivadas pela interação destas moléculas com os lipídeos de membrana, e a segunda pela interação dos mesmos com proteínas inseridas na bicamada lipídica (BERTACCINI, 2010). Para a molécula de interesse neste estudo, o etanol, ainda não foi encontrado nenhum receptor de membrana, proteína, com o qual este se interaja para exercer sua ação, portanto acreditamos que esta interação aconteça seguindo a primeira hipótese.
3 FUNDAMENTAÇÃO TEÓRICA
3.1 Estudos teóricos
Com o conhecimento de determinadas propriedades físico-químicas da matéria, e de suas previsões através das leis da física, foi possível criar modelos capazes, em certa extensão, de agrupar, prever e desenvolver novos materiais (SANTOS, 2001). Estes modelos utilizam aproximações impostas para simplificar os eventos da natureza, havendo aí uma diferença entre modelo e teoria. Teoria é o conjunto de leis capazes de fornecer resultados e conclusões a partir de um número de variáveis conhecidas, já os modelos descrevem aspectos específicos de certas propriedades da natureza (SANTOS, 2001). Uma importante ferramenta utilizada para este fim é a modelagem molecular.
Segundo a União Internacional de Química Pura e Aplicada (IUPAC), a
modelagem molecular “é a investigação de estruturas moleculares e propriedades
usando química computacional e técnicas de visualização gráfica, a fim de fornecer uma representação tridimensional plausível sob um dado conjunto de circunstâncias”.
As aproximações utilizadas para os estudos de modelagem molecular são; a aproximação clássica, que inclui a mecânica molecular e a dinâmica molecular, e a aproximação quântica, que utiliza métodos ab initio, DFT e semi-empíricos (RODRIGUES, 2001).
O método quântico leva em consideração a estrutura eletrônica dos átomos, fixando os núcleos em uma posição fixa R, e resolvendo a equação de Schrodinger para se alcançar um mínimo de energia do sistema, estudando a posição da
“nuvem” eletrônica do átomo. A equação equivalente quanto-mecânica para
resolução da energia total do sistema dá-se através da soma dos operadores de energia cinética e potencial operando sobre a função de onda ψ, que é parametricamente dependente das posições dos núcleos (1) (SANT’ANNA, 2009):
(1)
sistemas com milhares de átomos, como é o caso dos sistemas estudados neste trabalho.
A mecânica molecular é um método que é utilizado para calcular a estrutura e a energia de moléculas, desconsiderando para isso a presença explícita do elétron, baseado na aproximação de Born-Oppenheimer. Desta forma admite-se que os
elétrons, que se “movem” de forma mais rápida que os núcleos, ajustam-se aos
movimentos destes últimos. Didaticamente podemos dizer que a mecânica molecular trata uma molécula como um conjunto de esferas, que são os átomos, conectadas por molas, que são as ligações químicas (Fig.9) (RODRIGUES, 2001).
Figura 9. Representação de uma molécula em modelagem molecular (esferas: átomos;
molas: ligações).
Figura 10. A) Deformação no comprimento (estiramento) de ligação; B) deformação no
ângulo de ligação; C) ângulo de torsão; D) Interações de van der Waals.
Ao final a energia total da molécula é dada pelo somatório destas equações / energias potencias (2):
A minimização de energia é um processo no qual a energia do sistema é levada ao mínimo em conjunto através de algoritmo matemático adequado (SANT’ANNA, 2009).
O modelo de dinâmica molecular foi o escolhido para este trabalho por possibilitar a resposta das hipóteses levantadas, com custo computacional reduzido, portanto é a este modelo que daremos maior enfoque a partir deste ponto.
3.1.1 Estudos de dinâmica molecular
O primeiro artigo sobre simulações de dinâmica molecular foi publicado em 1977 (McCAMMON et al., 1977). As simulações nesta época não passavam de 10 ps., porém o número de publicações tem aumentado desde então chegando aos dias de hoje, com simulações extrapolando 150 ns.
Para este trabalho, analisamos a interação do etanol com fosfolipídeos de membrana, o que por si só é um sistema bastante complexo, com milhares de átomos. Com o intuito de chegar mais próximo da realidade, necessitamos da energia cinética das moléculas, uma vez que o movimento das moléculas permite as colisões intermoleculares gerando assim novas conformações (SANT’ANNA, 2009). A resolução das equações de dinâmica molecular leva em consideração a evolução temporal das conformações alcançadas pelo sistema, conhecida como trajetória. Portanto, este modelo estuda propriedades dependentes do tempo, como o dobramento de uma cadeia peptídica ou de DNA, difusão ou movimento de solventes em torno do soluto (KARPLUS e McCAMMON, 2002).
Os cálculos na dinâmica molecular são clássicos, baseados na resolução da equação de movimento de Newton (3) para cada átomo:
(3)
onde, (F) é a força que gera aceleração (a) em um átomo de massa (m). Embora este tratamento clássico permita resoluções de sistemas com apenas duas partículas, faz-se necessário um tratamento numérico como segue (4):
Esta equação é conhecida como série de Taylor, e permite o cálculo para a posição de uma partícula após uma pequena variação de tempo. Para esta resolução é necessário o conhecimento prévio da posição r(t), da velocidade dr/dt e da aceleração d2r/dt2, além de aproximações para os termos de maior ordem. O cálculo é realizado para um determinado intervalo de tempo Δt, que tem grande
importância para a dinâmica molecular (SANT’ANNA, 2009). Este intervalo de
tempo da trajetória deve ser pequeno o suficiente para que a aceleração se mantenha constante, sendo na prática da ordem de 0,5 a 1,0 fs (KARPLUS e McCAMMON, 2002).
Diferentes pacotes computacionais são disponíveis na internet de forma livre (MORGON, 2001), como o pacote GROMACS, para estudos de simulação de dinâmica molecular. O GROMACS é um programa bem conhecido e utilizado e a escolha do mesmo levou em consideração a grande quantidade de informações disponíveis e de trabalhos que o utilizam.
3.1.2 Modelos de membrana
Dentre os estudos de dinâmica molecular de membranas biológicas, os modelos de bicamada são os mais comumente utilizados (SONNE et al., 2007). As simulações computacionais são uma ferramenta única para predizer eventos a nível atómica e gerar correlações com efeitos macroscópicos (SAIZ et al., 2002) como por exemplo o efeito de anestésicos de fármacos sobre membranas.
A limitação da utilização destas simulações está no tamanho do sistema, a escala de tempo e a precisão do campo de força que descreva as interações (ANÉZO et al., 2003) que irão ocorrer durante a trajetória da simulação. Porém com o avanço da capacidade de armazenamento e processamento dos computadores, sistemas mais complexos podem ser modelados. Alguns trabalhos têm utilizado modelos de bicamadas com presença de esfingolipídios, fosfolipídios, colesterol e/ou proteínas, porém em nosso estudo o interesse é a ação do etanol sobre fosfolipídeos de membrana, pois acreditamos ser o local de ação desta substância.
para o estudo de processos celulares (CHIU et al., 1995) visto que a bicamada lipídica é um fator determinante para o controle do metabolismo celular.
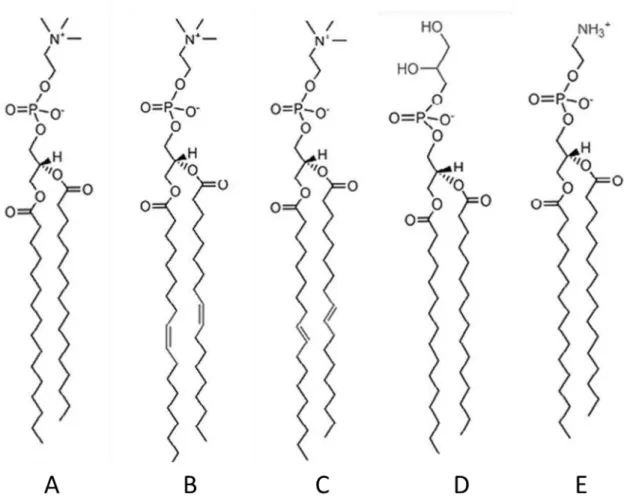
Alguns dos campos de força conhecidos e utilizados são o AMBER, CHARMM, OPLS e GROMOS. Estes apresentam vários fosfolipídeos parametrizados que podem ser utilizados em simulações computacionais. Alguns deles são representados na figura 11.
Figura 11. Estrutura de diferentes fosfolipídeos utilizados em simulações de dinâmica
molecular. (A: DPPC - dipalmitoilfosfatidilcolina; B: DOPC - dioleoilfosfatidilcolina; C: DEPC - dielaidoilfosfatidilcolina; D: DPPG-dipalmitoilfosfatidilglicerol; E: DPPE-dipalmitoilfosfatidiletanolamina).
Portanto, a escolha do fosfolipídeo deste trabalho levou em consideração os dados da literatura que suportavam a utilização deste modelo para uma boa correlação entre os dados teóricos e os efeitos macroscópicos investigados.
3.1.3 Interações intermoleculares
Quando átomos, moléculas e íons aproximam-se, dois fenômenos podem ocorrer: reações e/ou interações. As reações requerem a quebra e/ou formação de ligações com variações de energia da ordem de 50 a 100 kcal.mol-1, as interações envolvem a atração ou a repulsão entre as espécies químicas, sem envolver quebra e/ou formação de ligações, com variações de energia da ordem de 0,5 a 10 kcal.mol-1 (ROCHA, 2001). Portanto, as interações intermoleculares surgem do contato não reativo e são de natureza essencialmente elétrica dependentes da distância entre as espécies envolvidas.
As biomoléculas, como as proteínas, DNA e RNA tem sua estrutura tridimensional mantida pelas interações moleculares (LEHNINGER et al., 2007), assim como as membranas celulares (Fig. 12). As funções das biomoléculas e células estão intimamente ligadas a estas estruturas tridimensionais.
Figura 12. Fita de DNA, ilustrando as interações de hidrogênio entre nucleotídeos
(LEHNINGER et al., 2007).
As interações eletrostáticas são aquelas que resultam da interação entre dipolos e/ou íons de cargas opostas, cuja magnitude é diretamente dependente da constante dielétrica do meio e da distância entre as cargas (FRAGA, 2001).
Interações de dispersão, interações de London ou de van der Walls ocorrem quando átomos apolares apresentam flutuação local da densidade eletrônica transiente. Este é um tipo de interação fraca que varia no inverso a sexta potencia da distância (r-6), porém ocorre em grande número, e por isso contribui de maneira significativa para a estabilidade numa estrutura de macromolécula. As interações hidrofóbicas, assim como as de dispersão, são fracas e ocorrem em cadeias apolares em meio aquoso (BISSANTZ et al., 2010).
Outra força intermolecular importante é a interação de hidrogênio. Para esta interação é necessário a interação do hidrogênio com dois átomos eletronegativos. Um hidrogênio ligado a um primeiro átomo com alta eletronegatividade, passa a apresentar carga parcial positiva, o que facilita sua interação com o segundo átomo também eletronegativo (KOROLKOVAS e BURCKHALTER, 1998). Esta interação apresenta força maior que a dipolo-dipolo e está diretamente relacionada à estrutura tridimensional das biomoléculas e consequentemente as suas funções
As interações resultantes das colisões dos átomos nas simulações de dinâmica molecular são governadas através dos campos de forças que são parametrizados através de cálculos mecânico quânticos ou dados espectroscópicos, contendo a somatória de termos de energia relacionados a posições de equilíbrio do sistema (distância, ângulo, diedros, distância de van der Walls, interações de hidrogênio e eletrostáticas, entre outras).
Figura 13. Representação do raio de corte esférico em um sistema com condições
periódicas de contorno (EDUARDO, 2009).
Figura 14. Representação de um sistema com condições periódicas de contorno para o
4 OBJETIVOS
4.1 Objetivo geral
Estudar as interações entre as espécies químicas etanol com fosfolipídeos de membrana na presença de água e cloreto de sódio.
4.2 Objetivos específicos
Avaliar os efeitos in vitro de diferentes concentrações de etanol (0 a 50%(v/v)) em solução aquosa contendo cloreto de sódio (0,9% (p/v)) sobre eritrócitos de ratos;
5 MATERIAIS E MÉTODOS
5.1 Teste in vitro do etanol sobre a membrana de eritrócitos
5.1.1 Obtenção do material biológico
Para a obtenção do material biológico, o sangue, foram utilizados dois ratos Wistar, machos, com peso entre 180 e 200 g, devidamente aclimatizados no biotério da Universidade de Toyama.
Os animais (n=2) foram previamente anestesiados com pentobarbital, por via intraperitoneal. Posteriormente, realizou-se punção cardíaca para retirada do sangue com seringa contendo heparina.
O sangue heparinizado foi mantido em tubo de ensaio em banho-maria a 37°C, até o momento do teste.
5.1.2 Soluções-teste
As soluções teste foram feitas utilizando água Mili-Q, NaCl (Sigma) e etanol P.A. (Sigma), ambos dentro do prazo de validade. Foram então preparadas soluções de etanol de concentrações de 0 a 50%(v/v), variação de 5 em 5%, em solução de cloreto de sódio (NaCl) a 0,9%(p/v).
5.1.3 Teste de fragilidade osmótica
Em eppendorfs, foram acrescentados 1000 µL das soluções de etanol, em duplicata para cada material biológico, e um eppendorf de cada concentração (branco), para tara do equipamento. Todas as soluções foram previamente mantidas por 10 min. em banho-maria a 37°C, incluindo o material biológico, em seguida o sangue (40 µL) foi pipetado com uma micropipeta para cada um dos eppendorfs, exceto o tubo branco, deixando em incubação por mais 30 min. Logo após a incubação, o material foi centrifugado 2000rpm por 10 min. e então foram retirados os sobrenadantes e as leituras feitas em triplicata em espectrofotômetro a 540 nm.
5.1.4 Análise estatística
5.2 Estudo por dinâmica molecular
5.2.1 Estrutura básica
5.2.1.1 Célula básica
Uma caixa padrão de dimensões X=6,27256 nm, Y=6,29250 nm, e Z=14,80 nm, foi utilizada (Figura 15). O modelo para a bicamada lipídica foi gentilmente cedido por Andreas Kukol (KUKOL, 2009), já pré-equilibrada. O lipídeo utilizado foi o dipalmitoilfosfatidilcolina (DPPC) (Figura 16). A bicamada contém um total de 128 lipídeos, sendo 64 em cada lado da bicamada.
Figura 15. Caixa de simulação padrão visualizada pelo programa Molden, ilustrando suas
Figura 16. (A) Imagem gerada pelo software VMD, para a estrutura química de um
dipalmitoilfosfatidilcolina (DPPC) utilizado nas simulações; e (B) definição do número dos átomos para o lipídeo DPPC com suas respectivas cargas (PATRA et al., 2004).
Figura 17. Estrutura básica de simulação, com tamanhos aproximados de cada estrutura,
contendo dupla bicamada lipídica (linhas azuis), e um meio interno (M.I.) com 2413 moléculas de água (estruturas vermelhas), 7 íons Na+( esferas verdes) e 7 íons Cl- (esferas amarelas), e um meio externo (M.E.).
A água adicionada ao sistema foi previamente equilibrada em uma caixa de simulação contendo 2180 moléculas de água, em uma simulação de 2 ns, a 37°C.
5.2.1.2 Célula básica de etanol
Tabela 1. Número de espécies adicionadas em cada caixa de simulação de acordo
com as concentrações crescentes de etanol.
* %(v/v)
Com estas caixas prontas, duplicamos as mesmas e unimos com a célula básica de simulação, nas extremidades vazias, como exposto na figura 15, para então iniciarmos as simulações.
5.2.2 Simulações de dinâmica molecular
Após a finalização da modelagem dos sistemas de simulação, iniciamos uma minimização de energia com 10.000 passos, utilizando o algoritmo steepest descent, seguida de equilibração dos mesmos, com simulações de 0,1 ns com temperaturas crescentes de 0, 180 e 310 K, tendo fixadas as ligações.
As simulações então foram realizadas durante 60 ns em um ensemble isotérmico-isobárico (NPT), com tempo de integração de 2 fs.
As interações eletrostáticas e de van der Walls de curto alcance foram descritas utilizando raio de corte de 0,9 e 1,4 nm respectivamente. Já as interações eletrostáticas de longa distância foram consideradas empregando-se o método PME (Particle Mesh Ewald).
Foi utilizado o campo de força Gromos96 53a6 com as adaptações das cargas sugeridas por Kukol (2009) conforme descrito na figura 16.
5.2.3 Detalhes computacionais
As simulações dinâmicas foram realizadas utilizando pacote computacional Gromacs 4.5.4. Foram ainda utilizados os programas HyperChem 7, para modelagem do sistema; VMD 1.9 e Molden para visualização dos sistemas e vídeos das simulações.
6 RESULTADOS E DISCUSSÃO
6.1 Teste in vitro do etanol sobre a membrana de eritrócitos
Etanol é uma substância com conhecidos efeitos deletérios para os organismos vivos. Dentre outros, pode-se citar o efeito deletério sobre neurônios de ratos, cuja mãe ingeriu bebida alcoólica durante o período gestacional (LOPES et al., 2009; AVERSI-FERREIRA et al., 2006; AVERSI-FERREIRA et al., 2004).
De acordo com a farmacologia, um fármaco para exercer seu efeito, depende de sua concentração no sítio de ação, e para que isto ocorra, o mesmo depende de sua absorção e distribuição pelo organismo através do sangue (KATZUNG, 2010). Baseado nesta informação, um dos primeiros tecidos que o etanol entra em contato é o sanguíneo, visto sua rápida absorção no trato gastrointestinal. Uma interação sobre os eritrócitos com efeitos tóxicos pode gerar diminuição no transporte de oxigênio dos pulmões para os tecidos, e hipóxia tecidual.
A exposição dos eritrócitos de ratos em concentrações crescentes de etanol, de 0 a 50%(v/v), revelou um efeito anômalo com o maior rompimento dos eritrócitos em concentrações próximas a 20%(v/v), porém próximo a 35%(v/v) foi evidenciada uma diminuição desta lise, com aumento de lise somente a partir de 45%(v/v) de concentração de etanol (Fig. 18). A figura 18 ilustra este evento com aumento da concentração de etanol e a leitura do sobrenadante em espectrofotômetro. As cores vermelhas intensas mostram a exteriorização da hemoglobina devido ao rompimento das hemácias, e as cores mais claras indicam um menor rompimento/lise celular.
O efeito esperado para um fármaco é dose-resposta dependente, ou seja, com o aumento da dose há aumento da resposta, o que não foi observado neste estudo para o etanol, portanto sugerimos este ser um efeito anômalo.
Figura 18. A) Leitura da absorbância a 540 nm do sangue exposto a concentrações
crescente de etanol. B) Imagem do sobrenadante (Linha 1: A-etanol 5% (v/v); B-etanol 10%, C-etanol 15% (v/v), D-etanol 20% (v/v), E-etanol 25% (v/v), F-etanol 30%; Linha 2: A-etanol 35% (v/v); B-etanol 40% (v/v), C-etanol 45% (v/v), D-etanol 50% (v/v).
Figura 19. Absorbância, a 540 nm, do sangue exposto a baixas concentrações de etanol, de
forma crescente, em água e ausência de NaCl, demonstrando a lise celular desde as primeiras concentrações.
6.2 Simulações de dinâmica molecular
6.2.1 Energia total dos sistemas simulados
Figura 20. Comportamento temporal da energia total do sistema em concentrações
6.2.2 Visão geral dos sistemas estudados
Ao comparar a média de energia total dos últimos 10 ns de cada sistema simulado (Fig. 21B), podemos observar uma tendência ao aumento da energia pelos sistemas, mas com um pico a 10%, e uma diminuição a 20% de etanol. Este dado pode sugerir uma maior instabilidade e estabilidade respectivamente, mas no geral o aumento da concentração do etanol tende a desestabilizar o meio.
Para a área por lipídeo (Fig. 21C), também observamos um aumento da mesma até 35%, quando a partir deste ponto, há um decréscimo em 40 e 50%. Esta redução final não está relacionada à maior organização dos lipídeos, pelo contrário, nestas concentrações os lipídeos encontram-se visualmente desordenados com tendências à perda da estrutura em bicamada como observado nas imagens dos sistemas ilustrada a frente neste trabalho (Fig. 32A).
6.2.3 Sistema na ausência de etanol
No último frame da simulação do sistema na ausência de etanol, a bicamada lipídica mostrou-se integra e organizada (Fig.22A e Fig.23A) com densidades semelhantes na porção externa e interna de cada bicamada (Fig.22B), tendo ainda solvente nas porções polares dos DPPC’s.
Os íons sódios tenderam a uma maior densidade pela caixa na região de maior densidade dos íons fosfato da membrana (Fig.22C). Isso se justifica pela atração entre as cargas, positiva do sódio (+1) e negativa do grupo fosfato (-1). Esta interação do sódio pela membrana, pode justificar ainda a presença de mais solvente na porção polar da bicamada, uma vez que o sódio necessita de uma capa de solvatação.
Os íons cloreto estavam localizados juntamente com a água (Fig.22A), com densidade elevada na região entre as bicamadas (Fig.22C). Este resultado indica a preferência de interação destes íons pela água. Uma outra explicação desta preferencia dos íons sódio pela membrana e os íons cloreto pelo solvente, se dá pelo tamanho dos íons, pois o sódio sendo menor, tem maior capacidade de adentrar os lipídeos e interagir ao contrário do cloreto.
Figura 22. (A) Imagem da caixa de simulação com ausência de etanol no último frame da
Figura 23. (A) Imagem da bicamada, plano lateral, da simulação com ausência de etanol no
último frame da simulação; (B) Gráfico com perfil da densidade de cargas das bicamadas (DPPC), média dos últimos 5 ns. de simulações.
Os íons Na+ tendem a estabilizar a carga negativa da membrana (BOCKMANN et al. 2003) como observado ao interagir com os grupos fosfato (Fig.22C). O conjunto das interações iônicas gera um aumento do momento dipolo dos lipídeos (SHINODA et al., 2007) com regiões bem definidas como observado no gráfico da figura 23B.
Shinoda e colaboradores (2007) citam ainda que os íons Na+ penetram as membranas lipídicas, ligando-se aos grupos fosfatos de dois ou três lipídeos vizinhos o que provoca uma redução na área por lipídeo, assim como o observado em nosso estudo (Fig. 24). Esta redução de área indica uma redução da fluidez da membrana e maior adesão entre os lipídeos.
Figura 24. Comportamento temporal da área por lipídeo de uma monocamada de DPPC no
sistema com ausência de etanol.
Por outro lado, os lipídeos sem a presença de Na+, aumentariam as interações entre as cargas na porção polar entre lipídeos adjacentes, o que reduziria a interação óleo/água e demandaria uma menor entropia do sistema, pois as moléculas de água demandariam uma maior organização para interagirem com as cabeças polares.
Substâncias apolares como os lipídeos, geram um decréscimo na entropia no sistema, portanto, uma reação desfavorável, como acontece com a estrutura das bicamadas lipídicas, porém estas tende a dirimir estes efeitos sobre a entropia do sistema com as interações hidrofóbicas das cadeias apolares ordenadas no interior das bicamadas, expondo assim a cabeça polar para água adjacente.
6.2.4 Sistema com etanol a 20%(v/v)
No sistema simulado com presença de etanol a 20%(v/v), podemos observar que houve uma retração no tamanho da caixa em Z, que antes (Fig.22B) ultrapassava 13,5 nm e neste sistema está abaixo de 13 nm (Fig.25A). Esta retração pode ser explicada pela presença do etanol no sistema.
Verificamos também que o etanol interage com a porção polar da bicamada fosfolipídica, visualizado tanto no último frame da simulação (Fig.25A) quanto no gráfico de perfil das densidades de massas (Fig. 25B).
O oxigênio da hidroxila (EtOH-O) do etanol tem densidade aumentada na região próxima ao grupo fosfato dos lipídeos (Fig. 25C), o que gerou a diminuição na altura e o alargamento dos picos de densidade dos grupos fosfatos, bem evidente nas porções externas de cada bicamada.
Desta interação do etanol com a bicamada e o descolamento dos íons NA+, observamos uma desorganização dos lipídeos (Fig. 26A). Para a densidade de cargas nas porções externas de cada bicamada é evidente uma redução de tamanho e aumento da base neste sistema (Fig. 26B), porém isto foi pouco alterado para a porção interna. Este resultado nas cargas coincide com a variação observada nos picos de densidade dos grupos fosfato (Fig.25C).
Figura 26. (A) Imagem da bicamada, plano lateral, da simulação com 20%(v/v) de etanol no
A área por lipídeo também sofreu alteração (Fig. 27). Inicialmente observou-se um aumento, provavelmente pela interação do etanol e inicial deslocamento dos íons sódio, porém com a reorganização do sistema em presença de etanol, a área por lipídeo volta a diminuir, mas permanecendo em valores maiores ao observado no sistema anterior (Fig.24).
Este aumento da área entre os lipídeos pode ser resultado da deposição do etanol na bicamada, o que resultou em desorganização dos lipídeos e putativamente pode ser suficiente para diminuir as interações hidrofóbicas.
Figura 27. Comportamento temporal da área por lipídeo de uma monocamada de DPPC no
sistema com 20%(v/v) de etanol.
6.2.5 Sistema com etanol a 35%(v/v)
Os picos de densidade na porção interna das bicamadas (Fig.28C) tendem a seguir o padrão observado no sistema em ausência do etanol, porém na porção externa, é nítido a dispersão dos íons Na+, DPPC-P e DPPC-N (Fig.28C).
com perfil da densidade de massa do fosfolipídeo (DPPC), solvente (SOL) e etanol (EtOH); e (C) dos íons Cloreto (CL) e Sódio (NA), nitrogênio (DPPC-N) e fosfato (DPPC-P) do fosfolipídeo e oxigênio do etanol (ETOH -O) distribuídos pela caixa de simulação, média dos últimos cinco nanosegundos de simulação.
A maior densidade de etanol e água na porção externa das bicamadas reflete na área por lipídeo (Fig.29) que teve aumento quando comparado com os sistemas anteriores, com valores superiores a 0,66 nm2 em alguns momentos da simulação.
Figura 29. Comportamento temporal da área por lipídeo de uma monocamada de DPPC no
sistema com 35%(v/v) de etanol.
Figura 30. (A) Imagem da bicamada, plano lateral, da simulação com 35%(v/v) de etanol no último frame da simulação; (B) Gráfico com perfil da densidade de cargas das bicamadas (DPPC), média dos últimos 5 ns de simulações.
6.2.6 Sistema com etanol a 50%(v/v)
Os picos de densidade dos íons e grupos dos lipídeos e etanol seguem o mesmo padrão observado no sistema anterior.
Figura 31. (A) Imagem da caixa de simulação com 50%(v/v) de etanol no último frame da
fosfolipídeo e oxigênio do etanol (ETOH-O) distribuídos pela caixa de simulação, média dos últimos cinco nanosegundos de simulação.
Na figura 32A, observamos um desprendimento de lipídeos da membrana na porção externa e dispersão das cargas (Fig.32B), massa estrutura e as cargas tende a se manter na porção interna.
Figura 32. (A) Imagem da bicamada, plano lateral, da simulação com 50%(v/v) de etanol no
último frame da simulação; (B) Gráfico com perfil da densidade de cargas das bicamadas (DPPC), média dos últimos 5 ns de simulações.
etanol e água na bicamada lipídica, porém com a perda da estrutura em bicamada, isto reflete em diminuição de área por lipídeo.
Figura 33. Comportamento temporal da área por lipídeo de uma monocamada de DPPC no
sistema com 50%(v/v) de etanol.
Mesmo com todas as alterações observadas na área por lipídeo dos sistemas estudados, o número de moléculas de etanol que se encontravam presentes no meio interno das bicamadas foi pequeno (Tabela 2), o que demonstra a preferência de interação do etanol pelos lipídeos de membrana.
Tabela 2. Número de moléculas de etanol que se difundiram pelas membranas no
6.2.7 Análise geral dos resultados e discussões
De acordo com Campbell (2000) a estrutura em bicamada dos lipídeos é dependente unicamente da repulsão entre os lipídeos e a solução adjacente, e não a atração intrínseca entre porções não-polares, interações hidrofóbicas, que são dependentes da distância entre as moléculas. Os íons sódio ao neutralizarem as cargas negativas dos lipídeos e os íons cloretos ao polarizarem a solução aquosa (SHINODA et al., 2007; BOCKMANN et al., 2003), propicia um aumento de entropia e facilita esta interação óleo/água. O sistema busca por um estado termodinâmico mais estável, o que gera um número menor de moléculas de água ordenadas na periferia das bicamadas (LEHNINGER et al., 2007). Com as cabeças polares solvatadas e com presenças dos íons sódio, há um aumento na repulsão entre as cabeças polares e porção apolar dos lipídeos permitindo o aprisionamento destes últimos no interior da bicamada, onde interagem por interações hidrofóbicas.
Estes eventos foram evidenciados no sistema simulado em ausência de etanol, onde ficaram evidentes as interações e a densidade de cargas bem definidas pela caixa de simulação.
Com a presença do etanol no meio, o mesmo tende a se interagir com as porções polares das bicamadas lipídicas, mesmo com o aumento da área por lipídeo, e consequentemente a maior solubilidade da membrana, o etanol não teve uma maior entrada de etanol pela mesma, com maiores difusões a 35 e 50% nos sistemas simulados.
Para Frangopol e Mihailescu (2001) a partição álcool e membrana lipídica são governadas majoritariamente por três forças: i) repulsão entre álcool e água, que favorece a partição do primeiro nos lipídeos; ii) atração entre o grupo polar álcool e da cabeça polar dos lipídeos; e iii) atração entre a porção acil do álcool e a cadeia carbônica da membrana.
As alterações observadas pela ação do etanol, tanto no teste experimental como nos sistemas simulados não foram dose dependente, ou seja, para cada concentração de etanol tivemos respostas diferentes. Isto reforça o indício de que a ação do etanol está relacionada à organização do sistema, e não a força iônica.
No primeiro ponto de lise dos eritrócitos, ou seja, a 20% no teste experimental, os resultados da simulação de dinâmica molecular evidenciaram um deslocamento dos íons sódio e aumento de densidade do etanol e água na porção externa da bicamada, o que resultou em aumento da área por lipídeo, que gera aumento da solubilidade da membrana. Todos estes eventos aliados à diminuição da tensão superficial da água (FRANGOPOL e MIHAILESCU, 2001), podem explicar a lise celular evidenciada nesta concentração no teste experimental, pela entrada de água, que modifica a morfologia dos eritrócitos para estomatócitos e posterior rompimento das membranas.
Com o aumento da concentração de etanol até 35%, foi verificada a redução na lise dos eritrócitos no teste in vitro. Na simulação observamos novamente a deposição de mais moléculas de etanol na porção polar das bicamadas lipídicas, aumento da área por lipídeo, porém as porções externas das bicamadas apresentaram uma dispersão de cargas, não se mostrando bem definidas. Ainda é possível verificar que o sódio está novamente presente em maior concentração na bicamada independente do pico de concentração do etanol.
Com este resultado podemos inferir que o efeito anômalo observado no teste in vitro deve-se ao fato das moléculas de etanóis se aderirem à membrana, inicialmente, na porção externa, como nas concentrações abaixo deste valor, porém o sistema se estabiliza com a maior quantidade de moléculas de etanol, que passam a realizar ligações etanol-etanol, em detrimento da ligação etanol-lipídeo, formando clusters de etanol e água como citado no trabalho de Liu e colaboradores (2006).
Esta interação lipídeo-etanol-etanol anula a porção polar entre as moléculas de etanol, o que diminui a possibilidade de entrada de água para o interior da célula e sua lise por aumentarem novamente as interações hidrofóbicas na bicamada, e pelo etanol que interage em média a duas moléculas de água (LIU et al., 2006), ocasionando uma retração do sistema. Isto pode ser a transição do estado estomatócito para o estado equinócito verificado no estudo experimental.
porção externa tendem a sair da estrutura em bicamada. Este evento pode estar relacionado ao aumento das moléculas de etanol que, além de interagirem etanol-etanol como no sistema anterior, passam a interagir etanol-etanol-lipídeo.
O aumento destas moléculas não foi suficiente para exercer uma expressiva difusão de etanol pela membrana, mas o que se percebe é o aumento da densidade do etanol na membrana, reforçando a ideia de que o etanol apresenta preferencia de interação pelos lipídeos de membrana.
Neste sistema simulado a concentração de etanol e água e a profundidade destes na bicamada, podem ter induzido a uma maior repulsão entre o meio etanol/água e lipídeo, forçando assim os lipídeos a assumirem um novo grau de organização para que o sistema assuma novamente uma menor entropia. De acordo com Gurtovenko e Anwar (2009) esta nova organização é dada pela desestruturação da bicamada lipídica e formação de micelas. Logo o que temos na imagem do último frame da simulação é a tendência de perda de lipídeos da bicamada.
7 CONCLUSÃO
Concluímos com o estudo que o efeito in vitro do etanol sobre eritrócitos de ratos não segue um padrão dose-resposta dependente. Os eritrócitos necessitam da presença de cloreto de sódio para estabilizarem a estrutura da bicamada lipídica, pois sem esta solução, a mínima concentração de etanol já gera efeitos deletérios sobre os mesmos. Este efeito não está diretamente relacionado ao efeito osmótico e sim a interação do etanol com a membrana lipídica e com o sistema que a mantém.
Com o estudo teórico podemos observar a afinidade do etanol pelos fosfolipídeos de membrana gerando alterações na polaridade da bicamada e em sua permeabilidade. Ao aumentarmos a concentração do etanol não observamos alterações evidentes sobre a polaridade da membrana, porém a permeabilidade mostrou-se elevada até a concentração de 30%(v/v) do etanol o que sugere que o etanol se liga a membrana, diminui sua agregação e permite sua ruptura como observado no teste experimental.
Já com o aumento da concentração para entre 30 e 40% (v/v) observamos um efeito protetor, observado como diminuição da lise dos eritrócitos in vitro. Nestas concentrações os dados teóricos evidenciaram também uma elevada solubilidade com o cálculo da área por lipídeo, porém o mesmo não foi corroborado pela quantidade diminuída de etanol que permearam a membrana. Há um deslocamento das cargas na membrana, que podemos inferir nestas concentrações o etanol se adere a membrana, gera uma estabilização através da presença destas moléculas inseridas na bicamada, aumenta sua área, o que não significa aumento de solubilidade, e não gera lise como o observado no teste experimental.
8 PERSPECTIVAS
Este trabalho apresenta diferentes perspectivas para futuros estudos:
O mecanismo de ação do etanol ainda não está completamente elucidado, portanto mais estudos sobre este efeito deverão ser realizados;
Estudos dos efeitos dos fármacos anestésicos ainda permanecem não concluídos, sendo o etanol um destes representantes;
Refinamentos na metodologia poderão ser realizados futuramente nestes estudos como o aumento da escala de tempo, estudos com diferentes modelos de fosfolipídeos e outros íons como o potássio, magnésio e cálcio;
9 REFERÊNCIAS BIBLIOGRÁFICAS
AGRE, P. The aquaporin water channels. Proc. Am. Thorac. Soc. v. 3, n. 1, p. 5-13, 2006.
ANÉZO, C.; VRIES, A. H.; HOLTJE, H. D.; TIELEMAN, D. P.; MARRINK, S. J. Methodological Issues in Lipid Bilayer Simulations. J. Phys. Chem. B. v. 107, p. 9424-9433, 2003.
AVERSI-FERREIRA, T. A. Biologia Celular e Molecular. 1 ed. Campinas: Editora Átomo, 2008.
AVERSI-FERREIRA, T. A.; FERREIRA, N. R.; MORAIS, J. O. R.; PENHA-SILVA, N. Effects of acute prenatal exposure to ethanol on the postnatal morphology of the prefrontal cortex in wistar rats. Braz. J. Morphol. Sci. v. 21, n. 2, p. 99-103, 2004.
AVERSI-FERREIRA, T. A.; NASCIMENTO, G. N. L. The effect of acute and chronic exposure to ethanol on the developing encephalon: a review. Rev. Bras. Saúde Matern. Infant. v. 8, n. 3, p. 241-249, 2008.
AVERSI-FERREIRA, T. A.; RODRIGUES, H. G.; NERES, A. C.; FONSECA, L. C.; PENHA-SILVA, N. Estudo imunohistoquímico do bulbo olfatório de ratos Wistar submetidos à exposição pré-natal aguda com etanol. Biosc. J. v.22, n.1, p. 99-105, 2006.
BERTACCINI, E. J. The molecular mechanisms of anesthetic action: updates and cutting edge developments from the field of molecular modeling. Pharmaceuticals. v. 3, p. 2178-2196, 2010.
BISSANTZ, C.; KUHN, B.; STAHL, M. A Medicinal Chemist’s Guide to Molecular Interactions. J. Med. Chem. v.53, n.14, p.5061–5084, 2010.
BRUST, J. C. M. Ethanol and Cognition: Indirect Effects, Neurotoxicity and Neuroprotection: A Review. Int. J. Environ. Res. Public Health. v. 7, p. 1540-1557, 2010.
CAMPBELL, M. K. Bioquímica. 3 ed., Porto Alegre: Editora Artmed, p. 752, 2000.
CASCALES, J. J. L.; CIFRE, J. G. H.; TORRE, J. G. Anaesthetic mechanism on a model biological membrane: a molecular dynamics simulation study. J. Phys. Chem. B. v. 102, n. 3, p. 625-631, 1998.
CASCIO, M. Connexins and their environment: effects of lipids composition on ion channels. Biochim. Biophys. Acta, v. 1711, n. 2, p. 142-153, 2005.
CHIU, S. W.; CLARK, M.; BALAJI, V.; SUBRAMANIAM, S.; SCOTT, H. L.; JAKOBSSON, E. Incorporation of surface tension into molecular dynamics simulation of an interface: a fluid phase lipid bilayer membrane. Biophys. J., v.69, p. 1230-1245, 1995.
DIAKOWSKI, W.; GRZYBEK, M.; SIKORSKI, A. F. Protein 4.1, a component of the erythrocyte membrane skeleton and its related homologue proteins forming the protein 4.1/FERM superfamily. Folia Histochem. Cytobiol. v. 44, n. 4, p. 231-248, 2006.
EDUARDO, F. F. Caracterização molecular de biopolímeros em solução utilizando simulação computacional. 2009, p.181. Tese de doutorado – Universidade Federal de São Carlos. São Carlos, 17 de fevereiro de 2009.
ENGELMAN, D. M. Membranes are more mosaic than fluid. Nature. v. 438, 2005.
FELLER, S. E.; BROWN, C. A.; NIZZA, D. T.; GAWRISCH, K. Nuclear overhauser enhancement spectroscopy cross-relaxation rates and ethanol distribution across membranes. Biophys. J. v.82, p.1396–1404, 2002.
FILHO, A. A.; CAMPOLINA, D.; DIAS, M. B. Toxicologia na prática clínica. Belo Horizonte: Editora Folium, p. 368, 2001.
FRAGA, C. A. M. Razões da atividade biológica: interações micro e biomacromoléculas. Química Nova. v.3, p.33-42, 2001.
FRANGOPOL, P. T.; MIHAILESCU, D. Interactions of some local anesthetics and alcohols with membranes. Colloid Surf. B. v.22; p. 3–22, 2001.
GEDDE, M. M.; HUESTIS, W. H. Membrane potential and human erythrocyte shape. Biophys. J. v. 72, p. 1220-1233, 1997.
GOLDBERG, G. S.; VALIUNAS, V.; BRINK, P. R. Selective permeability of gap junction channels. Biochim. Biophys. Acta. v. 1662, n. 1-2, p. 96-101, 2004.
GURTOVENKO, A. A.; ILPO VATTULAINEN, I. Molecular Mechanism for Lipid Flip-Flops. J. Phys. Chem. B. v. 111, p. 13554-13559, 2007.
GURTOVENKO, A. A.; ANWAR, J. Interaction of ethanol with biological membranes: the formation of non-bilayer structures within the membrane interior and their significance. J. Phys. Chem. B. v.113, n.7, p.1983–1992, 2009.
HOLMUHAMEDOV, E.; LEMASTERS, J. J. Ethanol exposure decreases mitochondrial outer membrane permeability in cultured rat hepatocytes. Arch. Biochem. Biophys. v. 481, p. 226–233, 2009.
KATZUNG, B. G. Farmacologia básica e clínica. 10 ed. São Paulo: Editora Mcgraw-Hill, 2010.
KARPLUS, M.; McCAMMON, J. A. Molecular dynamics simulations of biomolecules. Nature Struct. Biol. v. 9, n. 9, p. 646-652, 2002.
KOROLKOVAS, A.; BURCKHALTER, J. H. Química Farmacêutica. São Paulo: Editora Guanabara Koogan, p.783, 1998.
KOUBI, L.; TAREK, M.; BANDYOPADHYAY,S.; KLEIN, M.L.; SCHARF, D. Membrane structural perturbations caused by anesthetics and nonimmobilizers: a molecular dynamics investigation. Biophys. J. v.81, p.3339–3345, 2001.
KUKOL, A. Lipid models for united-atom molecular dynamics simulations of proteins. J. Chem. Theory Comput. v.5, p. 615–626, 2009.
LARINI, L. Toxicologia. 3 ed. São Paulo: Editora Manole, p. 301, 2003.
LEHNINGER, A. L.; NELSON, D. L.; COX, M. M. Princípios de Bioquímica. 4 ed. São Paulo: Editora Sarvier, p. 1232, 2007.
LOPES, D. B.; NASCIMENTO, G. N. L.; CARVALHO, A. A. V.; NETO, A. C. S.; LIMA, N. E.; AVERSI-FERREIRA, T. A. Immunohistochemical study of acute effects of ethanol on midbrain of Wistar rats associated with the date of birth of neurons in encephalon. Int. J. Morphol. v. 27, n. 3, p. 677-682, 2009.
McCAMMON, J. A.; GELIN, B. R.; KARPLUS, M. Dynamics of folded proteins. Nature. v. 267, p. 285-290, 1977.
MAXFIELD, F. R; TABAS, I. Role of cholesterol and lipid organization in disease. Nature. v. 438, n. 1, 2005.