s
R
tÍI8v
uílvolâ EdlçÕo 2008-10 kâ. úruNrvERsirDADE
DE
Évonl,
&
INSTITUTO
SUPERIOR
DE
AGRONOMIA
rrMvERsrDADE
rÉcxrca
»r
r,rsBoA
Influência
dos
invertebrados
estuarinos
bentónicos
na especiação de metais
pesados
"Scrobicularta
plana"
Givaldo
Silvano
dos
Reis
Professor
Doutor
Pedro Raposo
deAlmeida
Professora
Doutora
Maria
Isabel Caçador
MESTRADo
Eu
GrsrÃo
r
CoxsnnvlçÃo
Dos REcuRsos
NaruRArs
Évou
s
tII
Àv
uárom EdlçÕo 2@&10 kà . út T]NTVERSIDADEDE ÉVORA&
INSTIIUTO
SI]PERIORDEIJNIVERSIDADE TÉCNICA DE LISBOA
Influência
dos
invertebrados
estuarinos bentónicos
na especiação de metais pesados:
es
"Scrobicularta
plana"
Givaldo
Silvano
dosReis
Lioonoiado em Ciências Biológicas
Tese apresentada à Universidade de Évora para obtengão do grau de Meshe em Gestão e Conservação dos RecuÍsos Naturais,
Orientação:
Professor Doutor Pedro Raposo de Almeida
@rofessor Auxiliar, Dopartamento de Biologia, Universidade de Évora)
Professora Doutora Maria Isabel Caçador
@rofessora Auxiliar corr Agregação, Departamento de Biologia Vegetal, Faculdade de Ciências da Universidade de Lisboa)
MESTRADo
EMGEsrÃo
ECoNSERvAÇÃo Dos REcuRsos
NATURATS)+À Çrg
.
OBJEcrvos
.1.
Oe,JecnvoGeRA1....2.
OBJEcrvosEsPEcÍFrcos...2
LOCAL
DE ESTUDO...2.1
EsruÁRroDoTEJo...2.2
DEFTNTÇÃoDESAPA1...2.3
SAPAL DAS HoRTAS (ALcocHErE)2.4
SAPALDo RosÁRro(MorrA)...3
ESPÉCIEESTUDADA...3.1.
ScaoarcuLAnnpr,cruÁ-Eco1oGrA...4
MATERIAL
E MÉTODOS4.1.
CoNSTRUÇÃoDoMESocosMos...4.2.
DELTNEAMENToESPERTMENTAL.4.3.
AvALtAÇÃo eRELTMTNAR Do pRoJEcro...4,4.
RECoLHA E PREPARAçÃo Do SEDIMENTo..4.5.
Recoun
E pREpARAçÁo Dos ANrMArs...4.6.
REcoLHADospELLErs...4,7.
QUANTIFICAÇÃo DE MATÉRIA oRGÂNICA (TGA)4.8.
ANÁLrsE DE DrsrRrBurÇÃo DE PARTICULAS.4.9.
ExrRAcÇÃosEouENcrALDos META|s...4.I
0.
ANÁLrsE ESrArísrcA...5
RESU1T4DOS...5.1
ANÁLrsE DA coMposrÇÃo DE MATÉRA oRGÂNrcA ...5.2
ANÁLrsE DE DrsrRrBurÇÃo DE PARTICULAS.5.3
AcUMULAÇÃoDEMETA|s...5.4
EspEcrAÇÃoDEMErArs...6
DTSCUSSÃO...7
REFERÊNCAS... 1.1 1.1 1.1 1.t TL1l
72t2
72\3
74 15 15t7
L7 18 18 18 20 202t
22 23 24 25 25 26 28 28 37 42GRADECIMENTOS
€.
Primeiramente quero agradecer a Deus pela protecção constantê, por tudo quetenho
alcançadona vida, por
ter
sempreposto no meu
caminho pessoasmaravilhosas, pela força
e
coragem que tenho adquirido sempre para vencer todos os percalços e desafios da vida..t
Aos
meus pais que, mesmo velhinhos,têm
sidoao
longoda
minha vida os meus grandes mêstres..t
As
lindas filhas Ana Catarina e Pauline, pelas pessoas que são parte da minha vida, também deste trabalho.*
Aos
mêus irmáos, Rosevaldo, lvando, Gilberto, Josevaldoe
Marilene, pelaspessoas
que são
e
acimade tudo são
realmente meus irmãose a
minha cunhada Ana..3.
Ao
Prof. Pedro Raposo de Almeida (orientador), pelas oportunidadesê
pelaconfiança
que
me concedeu, principalmente abrindoas
portasdo
CO, pelas palavras sábias e apoio técnico sempre..3.
À
Prof."
lsabel
Caçador
(co-orientadora)pelo
apoio
e
disponibilidade demonstrada.*
À
Proft. Teresa Ferreira, pelo apoio em todos os aspectos que obtive durante todo o tempo que estive no lSA, e a todos os outros professores do mestrado..&
Aos colegas de mestrado, pelo tempo de convivência juntos por êstes quasedois anos,
períodoque me
proporcionoumuitos
momentosde
rêflexão eaprendizado.
.!.
A
doutoranda Sílvia Pedro, colegade
projeclo, pela disposiçãoe
dedicâção, que apesar do seu volume de trabalho me ajudou bastante..:.
A todo pessoal do Centro de Oceanografia da FCUL, em especial à turma dolaboratório de Zoologia Marinha, pela convivência, carinho e apoio.
*
À
Xerox Comércio&
lndústria Ltda,nas
pessoasdo
Direc'tor Eng. AdilsonRamos,
e
do
Gerentede
QualidadeEng.
Luciano Coutinho,aos
analistas químicosdas
Plantasde
Tonere
OPC, ÁMaro, Emanuel Rocha, Sérgio daPaixão, Carlos Adailsom,
aos Eng. Joâo Tan
e
Marlon,a
F Cínara e Laís.Dias,
*
As pessoas do ISA com as quais tive uma óptima convivência, em especial as meninas da ADISA, pelo óptimo tratamento quê recebi durante todo o têmpo.*
À minha prima Silvana, o seu êsposo Clovis e às suas filhas Larissa e Lis Nare.lr
A todos os colegas de Mestradoe
Doutoramento do Brasil e de outros países que tive a grata oportunidade de conhecerJos na residência do ISA,,
A
Portugal e todos os Portugueses pelo acolhimento durante êste período quelá estive.
tt
As
minhas amigas
Patrícia,Zeza
e
Adriana
e
também
aos
colegas
doGreenpeace.
.:.
Ao
Coordenadordo
curso
de
Biologiada
Unüorge, Ednaldo,e
todos
os professores desta universidade..3. Aos meus amigos do Ténis em Portugal, Manuel, Chico, Antonio e Gaulter.
De tudo
ficaramtrês
coisas:a
cêrtêzade que
estavasempre
começando,a
certeza
de
que
era
preciso continuar e a cêrteza de que seria intenompido antes determinar. Fazer
da
intenupçáo um caminho novo, fazerda quêda, um passo de dança,
do
medo, uma escada, do sonho, uma ponte, da procura um encontro.ll Fernando Pessoa
LISTA DE FIGURAS
Figura
{
-
Distribuição geográfica de estuários a nível mundialFigura 2
-
Mapa do estuário do Tejo, sapais das Hortas e do RosárioFigura 3
-
Bancos de vasa intertidais do Sapal das HortasFigura 4
-
Bancos de vasa intertidais do Sapal do RosárioFigura 5
-
Scrobiculaia planaFigura 6 - Foto do mesocosmo
Figura 7
-
Desenho experimental dopoecto
Figura 8 - Gráfico de determinação da matéria orgânica
Figura 9 - Composição de matéria orgânica no Sedimento inicial
(§,
Pel/eÍs (B) e Sedimento-controlo (C)Figura
í0
- Gráfico de distribuição de partículas (%) das amostras desedimento e dos perleÍs
Figura
í{
- Gráfico comparativo de PSD entre as amostras desdimento
e pel/eÍs no mesmo intervaloFigura
í2
- Acumulação de Cd, Co, Gr, Cu, Ni, Pb and Zn no sedimento inicial (A), perreÍs (B) e sedimento controlo (C).Figura
í3
- Ordenação multidimensional não-métrica (nMDS) das amostras de sedimento onde as associações químicas de metais foram determinadas: O - sedimento inicial;o 'pellets;L
- sedimento controloFigura
í4
- Associações químicas de Cd, Co, Cr, Cu, Ni, Pb e Zn nosedimento inicial (A), pel/eÍs (B) e sedimento-controlo (C). Os
valores sobre as banas representam a soma das quatro fracçõês em ug.g-1 (peso seco).
7 13 14 15 17 18 20 22 26 2A 29 30 3'l
u
lll
LISTA DE TABELAS
Tabela
I
-
Valoresde
p
para
análisede
correlaçáode
Pearsonentre
aconcentração de metais pesados em cada fracção do sedimento e
teor de carbono orgânico das amostras; n.d.
-
abaixo do limite dedetecçáo
Tabela
ll
-
Valoresdo
potencial redox (Eh), pH, salinidadee
temperaturaregistados durante a exPeriência
Tabela
lll
-
Resultados das comparaçóesa
posteriori para a acumulação demetais nas diferentes fracções do sedimento entre os três grupos:
sedimento inicial
(A),
pellets
(B)
e
sedimento controlo
(C).Símbolos diferentes (o,o) representam diferenças estatisticamente
significativas entre grupos (p<0.05)
Tabêla lV
-
Concentraçáo total média dos metais nas amostras de sedimento inicial (A), pellets (B) e controlo (C) (pS.S-1, peso seco)32 27
37 36
ffiuêocta atos i,,]yr,,Fú,!fut esíart rros ôêrrrirrbos aa e§pêcirção ats n €áis pesaabs: Esgécie ?d.uúa,a Sctohlca'wia pfu'a
SIGLAS E
ACRóNIilOS
Eh
-
(Potencial
redox)
potencial
de
um
eléctrodo inerte
submerso
numasolução onde se verifica o fenómeno de oxi-redução, medida em
relaçãoao eléctrodo de referência.
ICNB
-
(lnstituto
de
Gonservação
da
Natureza
e
Biodivercidade) órgão
dogoverno de Portugal que têm como objectivo acompanhar e assegurar
aexecuçáo
das políticasde
conservaçãoda
naturezae da
biodiversidadee
a gestão das áreas
protegidas,visando
avalorização e o
reconhecimento público do património natural.ICP-MS
-
(lnductively Coupled Plasma Mass Spectrometry)
sigla
em
inglês para atécnica
utilizada na quantificação de metais pesados.MO
/
OM-
matéria orgânica.nMDS
(non-metric Multidimensional
scaling),
é
um
conjunto
de
técnicas
estatísticas relacionadas utilizado
na
visualização
de
informação
paraexplorar
semelhanças ou diferenças nos dados.MPs
-
Metais PesadospH
-
potencial
hidrogénioiónico,é
um
índiceque indica
a
acidez, neutralidade ou alcalinidadede
um meio qualquer.PSD
-
(Particle
Size
Distribution)
análise
de
distribuição
de
tamanho
de
partículas
usada para classiÍicar otamanho
de partículas do sedimento.,,/ruerrda ato, frrvatffioâ útr,rrrlp,a bantôntcoÉ rE §pactaçao arc
,,úk
p@atoa: ÉpáGra aafudrd, Sc,oô,tttffiút,.
SC
-Amostra
de controloSl
-
Sedimento
lnicialTGA
-
(termogravimetric Analysis) técnica utilizada na determinação do teor
de
matéria orgânica das amostras.tnfluência atos lnvêraêbídatos esluafinos bent'ntcos na êspectaçto de mêía,s p$rdosi ospécre estuttdala Scrobicutaíta plana
RESUTUO
Este trabalho consistiu em avaliar
a
influência dos moluscos bivalves na especiaçãode metais pesados (MPs) (Co, Ni, Cu, Zn, Cd, Pb, Cr) em sedimento estuarino. Neste
estudo
Íoi
utilizadoo
molusco bivalve Scrobrc ulariaplana (da Costa,
1778), umaespécie
bentónica predominantemente filtradora,que
se
distribuipor toda
costaatlántica
e
Sulda
Europa,e
constitui um recurso haliêutico com alguma importânciaem
Portugal. Estudos têm demonstrado que S- planaé
um bom bioindicador, razàopela qual tem sido muito utilizada nos programas de biomonitorização, principalmente
quando se pretende investigar a presença de metais pesados em substrato estuarino.
Os sapais escolhidos para a recolha dos animais e sedimentos situam-se no estuário
do Tejo: o sapal das Hortas (Alcochete), considerado de baixo nível de contaminação por metais pesados e onde foram recolhidos os animais; e o sapal do Rosário (Moita),
seleccionado
pelas
suas
característicase
considerávelpressão
antropogénica,contendo níveis elevados de metais pesados, e onde foram recolhidas as amostras de
sedimento. Esta experiência decorreu num mesocosmos
em
ambiente laboratorial,tendo sido
monitorizadosos
parâmetros abióticos considerados relevantespara
osucesso do ensaio. Ao todo foram utilizados 420 espécimes adultos da S. plana e 40 litros de sedimento, ambos previamente preparados. Os animais foram mantidos em
tanques com água salobra artificial e sedimento estuarino, aí permanecendo por 48h, tempo necessário para se alimentarem, sendo depois colocados em tanques apenas com água salobra artificial, para permitir a libertação e recolha dos pel/eÍs fecais Após a recolha, amostras dos pel/ets, do sedimento inicial (Sl) e sedimento controlo (SC) de
cada tanque foram centrifugadas, liofilizadas
e
armazenadas a4'C.
No processo deextracção sequencial, foi utilizado
o
procedimento descrito por Tessier etal'
(1979) emodificado posteriormente
por
Hullebushet
a/. (2005).A
determinaçãodos
metaispesados foi feita através de espectrometria
de
massa com indução de plasma (lCP-MS). Foi determinado o teor de matéria orgânica (MO) por análise termogravimétricaI
t rírtÚtcÍ' dÉ irry!yf,,tú, esÍrE rrort ôêatôrricos ,r, esp.rrtá{;to & t
túk
,4§,ados; êsÉci' êíl'da@ Sc'oô'Gt"ri' ph"tOGA)
e a
distribuiçãode
partículas (PSD) pela técnica
de
foto-sêdimentação(HORIBA). Neste trabalho foi avaliada a alteração na especiação química dos metais pesados induzida pela acção da s- plana através da comparação da concentração dos metais pesados nas diêrentes fracções definidas operacionalmente, no Sl, nos pel'ets
e
no SC. Nos resultados, o teorde
MO variou entre 7'5%e
9.3%, tendo os valoresmaiores oconidos
nos
perlêÍs,
mas
as
diferenças
não
foram
estatisticamente signiÍicativas (p>0.05.),tal
como nãofoi
significativaa
correlação entrea
MO
e
a concentraçãode
nas vármetais pesados nas francçóes.os
pel/eÍs apresentarammaior
concerúraçãode Cd, Cu, Pb
e
Zn, no
entanto,
esta
diferença não
foiestatisticamente significativa. A maioria dos metais pesados está ligada principalmente
à fracCão residual do sedimento. O teor de metais pesados nas amostras oooÍrêU na
seguinle ordem: fracção residual
>
fracção ligadaao
complexo MOe
sulfuretos >fracçáo ligada aos carbonatos > fracção de troca. Na fraccão de troca as diferenças
não foram significativas para a maioria dos metais, excepto para o Cu e Zn entre o SC
e os
outros dois gruposde
amostras; nesta fracção houve aumento detrês
(Cu) a dezassete vezes(Zn)
nos pel/eÚsem
relaçãoao
Sl e
SC. Na
ffaccãS-liSAdg--a9§carbonatos houve diferenças entre os pel/eÍs e SC e entre Sl e SC para o Cd, o Co, o
Cu
e o
Pb;
o
Gd
Íoi
cerca de dez vezes
superiornos
pel/eÍs;o
Ni
apresentou diferenças significativas entre os pel/eÍse o Sl e o
SC. Para o Zn houve diÍerenças significativas entreos
perletse
o
sl.
Na fraccão liqadaà
Mo
e
sulfuretos houvediferenças entre o Sl e os pel/ets para o Co, Ni e Zn, e para Cd e Cu entrc os pelleÍs e SC. Na fraccão residual. o Cd, Cu, Pb e Zn apresentaram diferenças entre os perleÍs e
SC.
Os
resultados
obtidos
evidenciaram
a
importância
da
S.
plana
nabiodisponibilizaÉo de determinados elementos, principalmente
o
Ni, não parecendoter a mesma relevância no caso do Co, Cr e Pb.
Palavras-chave:
Scrobicutaia p/ana,-
metais
pesados; sêdimentos
estuarinos;bioindicador, especiação química; estuário do Tejo, Portugal.
m,ràtch
tu
trrw,tu dú !!frf,,tl,o, bontôntco,,p c/prfiaeo.b moôrr pe.rdoa, aEpáara a6r4Éah Scroôbdrrr! Per.The
objecliveof
this work wasto
evaluatethe
iníluencêof
bivalve mollusca in thê speciationof
heavy metals, namely cobalt (Co), nickel (Ni), copper (Cu),zinc
(Zn),cadmium (Cd), lead (Pb) and chrome (Cr)
in
estuarine sediment. For this study we used thê bivalve Scroó,buraia
plana (da Costa, 1778),a
predominantly benthicÍiher-feeding
species.lt
is
geographically distributed throughoutthe Atlantic coast
andsouthern paÉ
of
Europeand
constitutesa
fishery resourceof
some importance inPortugal. Resêarch has shown that Scroôrbu/anb plana is a good bio-indicator, Íeason for which it has been widely used in biomonitoring programs, especially to investigate
the
presenceof
heavy metalsin
estuarine substrate.The salt
marshes chosen to collect the specimens and sediments used in the experiment are located in the Tagusestuary: HoÍtas saltmarsh (Alcochete), considêred
a
placewith
low-levelof
heavymêtals contamination and whêre
the
animals were collec'ted, and Rosário saltmarsh (Moita), presenting high levels ofhêaw
metals contamination and where thê sediment samples were collected. This experience took place in macrocosm environment in the laboratory and ênvironmêntal conditions monitored. Altogether 420 adult specimens of Scrobiculaia plana and 40 literÊ of sediment were used, both previously treated. The animals were placed into tanks with artificial brackish water and estuarine sediment and remained there for 48 hours, which was considercd to be enough time for feedingto occur; after that period the animals were placed in tanks with artificial brackish water for elimination and collec'tion of fecal pellets. Afier collection, the pêllets and sediment
samples
from
eachtank were
centrifuged, freezedried and stored at
4'C.
ln
the sequerúialeÍraction
procedure,we
usedthe
method describedby
TessiereÍ
a/.(í979) and later modified by Hullebusch eú aL (2005). Mass spec{rometry with induced coupled plasma (|CP-MS) was used to determine the heary metals.
The contênt of organic matter (OM) was determined by Thermo gravimetric Analysis (TGA), and particle size distribution (PSD) was also determined using
the of
Íírrránc&r dos n vcílbôrados e6&t irros ôorú6rrrcos rrt espec/áiçãp de múls peados: espáciê êít útdt ScroôrcÚÚt ra pralt
sedimentation technique
by
HORIBA.The
changein
chemical speciationof
heavy metals induced by the actionoÍ
Scrobiculaia plana was assessed by comparing the concentration of heavy metals in different frac{ions of the initial sediment, of pellets andcontrol sediment.
The
relationship betweenthe
concentrationof
heavy metals andorganic matter (OM)
was
also studied. TheOM
content ranged between 7 .5o and9.30%,
the
higher values occurred
in
the
pel/eÍs, but
the
differenceswere
not statistically significant (p>0.05)nor was
a
significant conelation betweenOM
andheavy metal fractions in all samples.
The pellets had higher concentrations of Cd, Cu, Pb and Zn, however, this difference between groups was not statistically signiÍicant,
thê
concentrationof
heavy metals inthe pellets differ from other samplês for Cd, Co, Cu, Ni, Pb and Zn. Most heavy metals
are primarily bonded to residual fraction. The content of heavy metals in the frac{ions
occuned in the following order: residual frac{ion> organic matter and sulfide complex > carbonates fraction > exchange fraction. ln the exchanqeable fraclion the differences
were generally not significant, except
for Cu
and Zn, where differences were Íound between initial sedimênt and the other two groups of samples; metals in this traction increased by three times (Cu)to
17 times (Zn) inthe
pellets when comparedto
theinitial and control sediment. ln the fraction bound to carbonates differences were found
betweên the pellets and control, and the control and the initial sediment for Cd, Co, Cu
and Pb; Cd was about ten times higher in pellets; Ni presented differences between the pellets and the initial and control sediments. For Zn there were significant differences between
the
pellets and initial sediment. ln the fraction boundto
orqanic matter andsulfides there were differences bêtween the initial sediment and the pellets for Co, Ni,
Zn and Cd and Cu between the pellets and control. ln the residual fraction, Cd, Cu, Pb
and Zn showed differences between
the
pellets and control. The results obtained inthis work have evidenced
the
importanceoÍ
S. plana inthê
bioavailabilityof
certainelements, particularly Ni; in the case of Co, Cr and Pb this species does not seem to
affect the availability to the biota.
ffiu$tc,€ dGs t vefiúraaros esÍrarriros ôêrríórrccs ra .!,p.rj,E,ção de
rn
ts P.sados-- ê3Pácrb êíüdtdt Sc,o,úctd'"a Pfu'a Keywords:Scrobiculaia ptana, heavy metals,
estuarine sediment,bio
indicators, chemical speciation, Tagus estuary, Portugal.tnftuência dos invertebrados esÍua rinos bentônicos na especraçâo de metais pesados-' Espécie estudada Scrobicularia plana
1
TNTRoDUÇÃoSegundo Pritchard (1967),
um
estuárioé
um corpo
de
água
costeiro,semi-fechado, que possui uma ligação Iivre como
o
mare que
no seu interiora
água sediluem de forma mensurável com a água doce proveniente da drenagem terrestre. No
estuário podem definir-se diferentes zonas
em
relaçãoao
nívelde
salinidade: zonalimnética
(*0,5),
oligohalina(0,5
5),
mesohalina(5
18),
polihalina(18 -30)
eeuhalina (30
-
40). Os ecossistemas estuarinos estão sujeitos a níveis muito elevadosde
contaminação, devidoà
sua localização, que, sendo privilegiada, está na origemdas elevadas pressões antropogénicas que sobre eles
se
abatem.E
neste contextoque se enquadra a contaminação dos respectivos sedimentos por metais pesados.
{F--
-*-eilrr *"'!\
Figura 1
-
Distribuição geográfica de estuários a nível mundial.Os sedimentos constituem um reservatorio natura! com concentrações vestigiais
de metais pesados, que ocorrem nos ambientes aquáticos por processos naturais (e.9.
intemperismo). Porém,
os
níveisde
contaminação são,às
vezes, potenciados peloefeito das actividades antropogénicas. Os metais depositados nos sedimentos podem
passar para a teia trófica estuarina ao serem incorporados pelos organismos de forma
It 1 ! \1
F
#
1tti
U nrf
]
tnfluância ctos Invertebractos eslÍ| ertnos bêntôntcos na esp*teçáo de mEaals posados. esPácie eíudada Scíoblcula,a P,ana
directa, como
é
o
casode
alguns organismos bentónicos,ou
indirecta, através de relações tróÍicas.A
incorporação dos metais pesados nos organismos pode produzirefeitos
adversos
se
a
concentração desses elementos atingirem
níveis
quereprêsentem toxicidade (Long
eÍ
al. 199O.Os
metais vestigiais estão presentes emdiferentes formas químicas,
e a
sua
biodisponibilidade para diferentes organismos aquáticosé
fortemente dependente destas formas (Ru2ió,í996).
Para além disso,dependendo
da
concentraçãoe
do grau de
complexidade,o
metal pode limitar o crescimento ou ser tóxico para organismos vivos (Meylan et al.' 2004).A
contaminaçãopor
metais pesadose
organometaisnos
estuáriose
águascosteiras tem origem principalmente nas actividades antropogénicas,
e
tem causadograndes
preocupaçõesaos
investigadores, administradorese
decisores
políticos (MikaceÍ
ar-, 1996).O
processode
acumulaçãode
contaminantes nos organismosaquáticos poderá
contribuir,em
parte, para
bioacumulaçãoe, de
certa
forma, produzirá efeitos negativos sobre o biota (Byrne & O'Halloran, 200,l). A relação entre aacumulação
de
metais
pesadosnos
sedimentose
o
comportamentotrofico
dosorganismos bentónicos
é
um
importantefactor que
afectaa
biodisponibilidade dediferentes metais no ambiente aquático (Monperrus et al,2OO7).
A
importância dos organismos bentónicos na dinâmica dos metais através dosrespectivos dejectos depositados na superfície do sedimento é vista pela comunidade científica com alguma preocupação, tendo sido feitos vários trabalhos focados na acção dos pel/eÍs fecais (daqui em diante designados pel/eÍs) e sobre o processo de transporte daqueles poluentes para
o
fundodo
mar (Fowler, 1982). Para alguns organismos osdejectos são o principal meio de eliminação de metais pesados (Small & Fowler 1973).
Existem poucas informações disponíveis sobre os metais vestigiais contidos no
material
fecal
dos
invertebrados bentónicos.As
partículas filtradas pelos filtradoresbentónicos
são
depositadasnos
sedimentos estuarinosatÍavés dos
perleÍse
daspseudo-fezes (pseudo-fezes são grupos de finas partículas que são processadas pelos
t frtúrcta aros tnvllúrafu Étt/É/drros
ffiticos
,a êspêcltçáo & ,'r6Úrit ,Gsados: esPóGie ê-§í.rdtdt ScroÔrcu t ,a p&rabivalves
e
não ingeridas, são envolvidas pelo muco, mantidas dentro da cavidade domanto, e depois expelidas pelo sifáo inalante ou pela margem ventral do manto (Berg
eÍ
a/.,
1996).Este
processo, conhecido como biodeposição, adiciona novo material aosedimento
e
pode
ser um
importantê caminhopara
a
deposiçãode
quantidades vestigiais de metais nêste ambiente.Estudos realizados nos pel/eÍs
de
invertebrados bentónicos revelarama
sua influência na concentraçãode
matéria orgânica,e a
geraçãode
núriêntes durantê adecomposição (Brown, 1986), demonstrando a possibilidade de os perlêÍs iníluenciarem
significativamente
o
ciclo
biogeoquímicodos
elementos vestigiais nos ecossistemas estuarinos. Muitos estudos têm demonstrado que a concentração de metais pesados nosedimento está relacionada com
o
tamanho das partículase
coma
concentração de matéria orgânica no sedimento (Fôrstner, 1979, Thorne&
Nickless, '1981), e que tanto os animais que se alimentam da matéria orgânica em suspensão, como os que rêtiramos seus alimentos de uma faixa restrita de tamanho de partículas do sedimento estáo expostos
a
este tipode
contaminação.É
importante compararas
concentrações dosmetais encontrados nos pelreÍs
com
o
tamanhodas
partículase a
composiÉo
de carbono orgânico, pois são dados essenciais para investigara
influência do tamanho das partículas na alimentação e a concentração de metais nos pel/ets excretados pelosanimais bentónicos. Um dos objectivos
dê
estudaro
ciclo biogeoquímico dos metaispesados
é
desenvolver
meios
de
compreender
o
impacto biológico
destescontaminantes com base nas suas concentrações no ambiente, e para isto é necessário compreender o comportamento biológico e geoquímico destes metais.
Quando um metal
é
introduzidono
ecossistema aquáticoé
imediatamentedistribuído
entre
materiais particuladose
soluções.A
concêntraçãodas
partículas(sedimento
ou
paÉículasem
suspensão) ligadasao
processode
sedimentaçâoe
adimensão
das
partículasdo
sedimento reflectema
combinaçãofísica
e
prooessosbiológicos (e.g- bioturbação) (Snelgrove
& Búman,
1994; Aller & Aller '1998; Munay eÍt rttuâDcia dos inyG,tebífu §firaúoos bo,ta6nlco.$ na espGcritoáo de ,rêrrtt pesrdos; êsÉcre esr.rdaaÍt SdoáIcat6,la ptzr,3
al.,2OO2; Meysman et al.,2006). Desta forma, os processos fisicos e biológicos afectam
as
comunidades macrozoobentónicas.De
modoque a
relação entre sedimentoe
osorganismos
é
consideradaum
caminho
bastante convenientepara
se
estudar
asustentabilidade do habitat (Sanders, 1958).
Os bivalves que se alimentam de material particulado em suspensão obtêm os
seus alimentos
a
partir da coluna de água, enquanto os que se alimentam demáéria
depositadatêm
comofonte de
alimentoa
matéria orgânica presenteno
sedimento.Estes alimentos são oriundos sobretudo da produção primária e do material particulado
depositado
da
colunade
água,que
pode ser fitoplânc{on, biodepósitos e/ou detritos(Navarro & Thompson, 1997).
Os moluscos bivalves são capazes de acumular altas concentra@es de metais
tóxicos
no
seu organismo sem evidenciar nenhum efeito adverso (MouneyraceÍ
ar.,1998). Nas
últimas décadas,os
êfeitos decorrentesda
absorçãode
metais pelos bivalves têm sido investigados intensivamente. Estes êstudos abrangem a dimensão e o sexo dos bivalves (Cossa eÍal.,
1979), as variaçóes de salinidade (Phillips, 't976), oscompostos orgânicos dissolvidos (Zamuda
et
a/.,
1985),a
concentraçãode
metaisdissolvidos
e
êspeciaçáo destes metais (Cobelo-García etal.,
2003), entreoúros.
Osmoluscos bivalves
sâo
compostos
por um
número
de
sistemas
sub-celularesimportantes
na
acumulação, regulaçãoe
imobilizaçãodos
metais essenciaise
não essenciais (Langston eÍ a/-, '1998).A
natureza geoquímicados
sedimentos,a
associação metal-sedimentoe
adistribuição relativa
dos
metais
na
água ligados
ao
sedimento, podemter
umainfluência
considerávelno
destino
final
da
biodisponibilidadedos
metais
nosorganismos aquáticos (Luoma
&
Bryan, 1982,Di Toro eÍ
ar., 1990, Lee&
Luoma,1998). A transferência dos metais do sedimento para os organismos bentónicos pode
afec{ar
o
comportamentodos
animais,
nomeadamenteo
comportamento trófico,,rfrtÉrrciô arí§ hrvqútãdos §üraíioos b.,/t|ónic.Àa na ?á,DêciacÁo ate múk násaós; espéGra ast áaÍ' ScroàJlíati, p,t ra
hábitos
de
vida, ciclo reprodutivo,taxa de
crescimentoe
tamanho (Cain&
Luoma '1990, Wanenef
ar.,í998).
Também outros animais que fazem parte da teia tróÍica podem sofrer impactos, dependo dos níveis de contaminação existente nestas fontesde alimentos.
A
presença de metais pesados nos moluscos, mesmo em quarÚidades vestigiais, representaum
risco paraa teia
trófica,tanto
paraos
indivíduosque
se alimentam directamente destes animais quanto indirectamente, pois estes têm muitafacilidade
em
reter substâncias tóxicas nos seus organismos. Pela forma como serelacionam com o habitat, principalmente a forma como retiram os alimentos do meio,
os moluscos bentónicos estão directamente expostos à contaminação por metais. Na
sua alimentação, o Homem pode Íicar exposto directamente à contaminação presentê
nestes animais através do seu consumo, que dependêndo dos níveis de contaminação e do tipo de metal podem trazer consequências irreversíveis para a sua saúde.
,i|f,uarck ar(E irM.,úôdos Éatüh,.,,, furranicc§ tE especraçro de rraÚlrb pesadosí €spécre o§rldrda sc,oóicÍ"t'ít pla"'
í.í.
Objectivos
1.í.í.
Obiectivo Geralo
objectivo principal deste trabalho foi avaliara
possívelalteraÉo
na especiação demetais pesados
em
sedimentosde
sapal, após passagem pelo tracto digestivo do molusco bivalve scroÓiculaia
plana, utilizando paraa
experiênciaos
pel/eÍs fecais desta espécie.í.í.2.
Objectivos
EsPecíficosi.Verificaradiferençaentreaconcentra@odemetaispesadosnosedimento
estuarino e nos pel/eÍs de Scrobicularia plana;ii.
Determinara
concentraÉo
de
metais pesadosnas
diÍerentes fracções dosedimento estuarino e nos pelreÍs de Scrobiculaia plana;
iii.
verificar a diferença no teor de matéria orgânica do sedimento e dos perreÍs;iv.
Determinara
relaçãoentre
o
têor
de
matéria orgânicae
concentração demetais pesados no sedimento e nos pelreÍs;
tnfluência dos rnverÍebrados estuarinos bentõnicos na especiação de metais pesados; Espécie estudada Scrobicularia plana
2
LoCAL
DE ESTUDO2.1
Estuário do TeioO
local escolhido como suporte do trabalhofoi
o estuário do Rio Tejo(Fig 2).O
estuário
do
Tejo
(38'44'N,9o08'W) está entre
os
maiores estuáriosda
Europaocidental, com aproximadamente
320
km2,e
apresenta uma grande diversidade dehabitats, como salinas, sapais e vasa. Encontram-se neste estuário importantes locais
de
reprodução, nidificação, alimento, repousoe
abrigo
para várias espécies. Esteestuário contém uma
das
mais
importanteszonas húmidas
da
Europa,
sendoconsiderado um santuário para aves, peixes, moluscos e crustáceos.
10ü krn UT lí) CD (.1 7 L N
J
rÍr ú 0 (rl 7o
UF
z. r{ J l-do
z. lrJ Uo
lI, r') Ê0 (.-) 7 -w 9"21', WE"ü9' w8"57',Figura 2
-
Mapa do estuário do Teio, sapais das Hortas e do Rosário.2.2
Definição de sapalOs sapais são ecossistemas intertidais que constituem uma interface entre o
meio terrestre
e o
meio marinho(um
estuárioou
o
mar), possuindo elementos eatributos de ambas
as
comunidades, terrestree
aquática (Wiegertet al.,
1981). Emgeral,
os
sapais encontram-se distribuídosnas
médiase
altas
latitudesde todo
oplaneta, sendo substituídos por mangais nas regiões tropicais (Boaden & Seed, 1985).
Ocorrem
em
zonas adjacentesa
estuários, baíasou
rias,em
áreas protegidas da Ju
F-oío
ÍL Lisboa o lt JI
'l i rr) ,p aancosdcvasa Rosárro Sapal §apal das Honas Canal prÍncípale esteiros 0ceano Atlânticom
lnftuência dos invertebrados estuarinos hentônicos na especíaçáo de metais pesados.' espécie estudada Scrobicularia plana
acção directa
das
vagas
e
das
correntes.
Formam-sena
zona
inteftidal
peladeposição sucessiva de sedimentos finos provenientes das marés que periodicamente
os
inundam (Wiegert&
Freeman, 1990).A
vegetaçãoé
um elemento caracterizantedos sapais, como também intervém activamente na sua formação. Actua como uma
armadilha
de
sedimentos, permitindoa
sua
deposição,e
protege-osda
erosão (Packham & Willis, 1997).2.3
Sapal das Hortas (Alcochete)Neste sapal,
localizado
no
concelho
de
Alcochete
(N3Bo45'24.79" eW8o57'59.59'), foi feita
a
recolha dos animais para o trabalho experimental.O
sapaldas Hortas (Fig. 3) está inserido na Reserva na Natural do estuário do Tejo, que faz
parte
das
áreas protegidaspelo
ICNB.A
razáoda
escolha deste ambiente para acolheita dos animais prendeu-se com o facto de deste sapal apresentar baixos níveis de perturbaçõa de origem antropogénica. De acordo com estudos feitos anteriormente
neste local, verifica-se
a
existênciade
valores baixosde
contaminaçãopor
metais pesados, justificando assim a nossa escolha.Figura 3
-
Bancos de vasa inteÉidais do Sapal das Hortas.tnfluência dos invertehrados esÍua rinos benlônicos na especÍaçáo de metais pesados-' espécie esÍudada Scrobicularia plana
2.4
Sapaldo
Rosário (Moita)O sedimento utilizado no trabalho experimental foi recolhido no sapal do Rosário
("N38'39'20.85"
e
W8'59'48.35").
A
escolha
do
sapal
do
Rosário (Fig.a)
comofornecedor do sedimento para a experiência relacionou-se com o facto de este ser um
sapal que
apresenta grandes perturbaçõesde
origem antropogenica. Neste sapalexiste
um
pequeno porto
onde
ocorrem vários
tipos
de
contaminações, comoconsequência
da
actividade pesqueirae
de
actividades correlacionadas; recebetambem efluentes domésticos, industriais
e
agrícolas. De acordo com estudos feitos anteriormente neste sapal, verificou-se um nível elevado de contaminação por metais pesados. Com base nestes estudose
nos aspectos observados pode-se concluir queé
um local que está sob grande impacto ambiental, justificando então escolha destecomo local
de
colheitados
sedimentos,de
forma
a
potenciara
observação de resultados.Figura 4
-
Bancos de vasa intertidais do Sapal do Rosário.tnftuência dos invertebrados esÍua rinos bentônicos na especiação de metais pesados; espécie estudada scrobicularia plana
3
Espécie Estudada3.1.
Scrobicularia plana-
EcologiaO
molusco bivalve Scrob icularia plana (da Costa 1778),a
lambujinha, vive emburacos permanentes que podem atingir os 20 cm
de
profundidade, nos sedimentos intertidais com características polihalinas, que podem ser, desde a lama a areia,e
àsvezes
cascalho (Verdelhoset
al.,2005).
Embora obtenhaparte
do
seu
alimentoatravés dos seus Iongos sifões, filtrando
as
partículasda
água quandoa
maré estácheia,
S.
plana(Fig.
5)
ingere
essencialmente partículasque
se
depositam no sedimento (Hughes, l969),
principalmentenos
períodosde
maré baixa. Os
seussifões são por vezes
predadospor
caranguejos, peixese
aves;
contudo,a
autoregeneração ocorre em poucas semanas. A reprodução ocorre normalmente no verão;
as larvas são livres, com uma fase planctonica que dura 2 a 3 semanas até sofrerem
metamorfose para a fase adulta. Esta espécie tem uma ampla distribuição geográfica,
podendo ser encontrada desde a costa Atlântica até ao sudoeste de lnglaterra e Africa
(Tebble,1976). E uma espécie mais tolerante às variações de salinidade e temperatura
do
que
a
maioriados
bivalves estuarinos (Bryan&
Hummerstone, 1977)-A
sualongevidade pode chegar a mais de dez anos, geralmente atingindo um comprimento
de 4-5 cm,
e
a
suataxa de
crescimento podeser
estimadaa
partirdos
anéis da concha (Hughes, 1970).lnfluência dos invertebrados esÍuarinos bentõnicos na especÍaçáo de metais pesados; espécre estudada Scrobicularia plana
Figura 5 - Scrobicularia plana.
A
Scrobicularia planatem
várias característicasque a
tornam muito apelativacomo objecto
de
estudo,
principalmentepela
sua
resistênciaàs
variações
dasalinidade
e
temperatura. Porser
muito resilientea
alteraçôes ambientaistem
sidomuito usada, tanto em programas de biomonitorização, como em testes de toxicidade (Byrne & O'Halloran, 2001; García-Luque et a\.,2004). Por todas estas características,
este
molusco bivalve
tem
sido
largamente utilizado
em
vários
trabalhos,principalmente quando se pretende investigar bioacumulação de substâncias tóxicas,
como os metais pesados. E ainda uma espécie de alguma importância económica em Portugal e em todo o litoral mediterrânico.
16
r;,ldo tr
l{À t
inr:
ffi
itlnfluência dos inverlebrados esÍuarinos hentônicos na especiação de metais pesados.'espécie estudada Scrobicularia plana
4
MATERTAL EMÉToDos
4.1.
Gonstrução do mesocosmosPara
a
realizaçãodeste
projectofoi
necessáriomontar
uma
estrutura emlaboratório que representasse uma réplica
o
mais proxima possíveldo
habitatde
S.plana, composto pelos seguintes elementos: um tanque em vidro com capacidade total
de 800L, 7 pequenos tanques rectangulares com capacidade de 30L cada
(Fig.6).
Notanque
de
maior capacidadefoi
colocada águaaté
uma alturade 12
cm, onde foiinstalado sistema
de
refrigeraçãoe
circulaçãode
água, com objectivode
manter atemperatura
constante
(17oC+l-
1.0'C).
Foi
instaladotambém
um
sistema
deiluminação artificial para simular
a
alternância dia/noitedo
habitat (12D.12N). Estas condições ambientais foram definidas a partir de informações encontradas na literatura e das simulações feitas durante a fase do teste experimental.Figura 6
-
Foto do mesocosmos.17
l)
flI.l:"
muarcia dG i,,vqú,at'os í*,Ú,,adnos benÍanicos .E e5p.Gi.l,áo d.,,6ú,,s pesado$ espáGie eslr,d.& sc,oà,clfui. pF,na
4.2.
Delineamento EspêÍimentalEste
trabalho consistiuem
avaliarem
ambientede
mesocosmoa
possívelalteração na especiação de metais pesados presentes no sedimento de sapal, após passagem pelo trac{o digestivo do molusco bivalve
s.
plana. Foi realizado tendo emconta
o
pressuposto queque os
espécimenes adultosde S'
plana, atravésdo
seuprocêsso de alimentação
e
excreçáo, poderão influenciar uma possível alteração na especiação de metais pesados nos sedimentos estuarinos. Para testar estahiÉtese
foi
avaliadoo
teorde
metais pesados contido nos pel/eÍs excretados pelos animais,comparando com o sedimento do início e do final da experiência (sedimênto controlo).
4.3.
Avaliação preliminar doproiecto
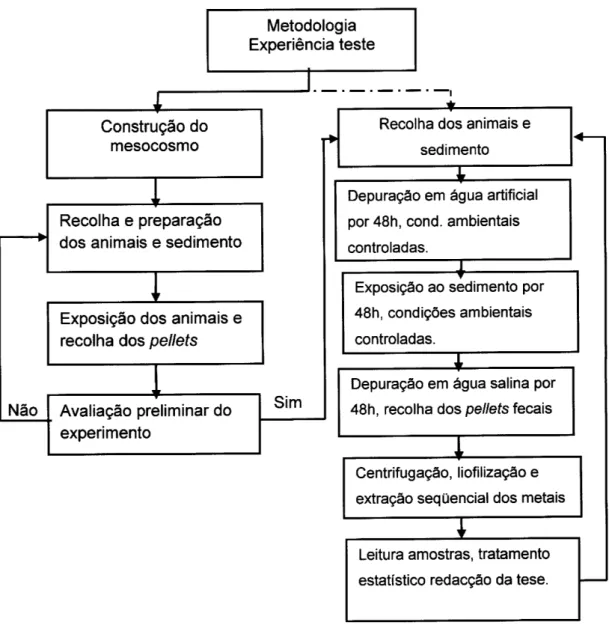
Foi montado um dispositivo experimental com o objectivo de avaliar e definir as condições
a
aplicar no projecto final (Fig. 7). Esta fase serviu tamkÉm para testar a eficiênciado
mesocosmosem
reproduzirem
laboratórioas
condições próximas àsexistentes no habitat de
s.
plana. Nesta experiência teste foram utilizados 60 animais num tanque com sedimentoe
água preparada artificialmênte com salinidadede
24PSU e condições ambientais equivalentes às encontradas no habitat de origem.
A partir do suoesso obtido no teste, e promovendo algumas conecções em função das
dimensôes da experiência,
foi
possível deÍinir as condiçõês paraa
configuração finaldo trabalho.
4.4.
Rêcolha e preparação dosêdimento
Para o trabalho foi necessário um total de c- 40 L de sedimento que foi recolhido
no
sapal do
Rosário-As
amostras foram recolhidasa
partir da camada superior dosedimento
(0.5
a
I
cm
de
profundidade).Apos
a
recolha,e
no
mesmodia,
as amostras de sedimentos foram passados por um cÍivo com malha de 250 pm, com offiuarrcia afu irM{,í(lÔrafu ôst arrrrcr ôêrrúrlicos ra êspecragáo dê Ílêút s pesados: êrÉ6re o§Í.rdrara Scro,ticul.r'/. p6,na
objectivo
de
removera
macrofauna, detritose
areia grosseira' Apóso
processo de crivagem, as amostras foram homogeneizadas e distribuídas em duas fases distintaspelos aquários de 30L, até uma altura de cerca de 7cm; em seguida foi adicionada a
água salobra preparada artificialmente até atingir 15 cm de altura. Os aquários foram
condicionados durante
24h em
condiçôes controladasde
temperatura, salinidade,luminosidade
e
oxigenação próximas das ambientais, paraa
posterior coloução dosanimais.
O
sedimerúo remanescente, utilizadona
segundafase da
experiência, foipreservado a 4"C.
Sim
Metodologia Experiência teste
Recolha dos animais e sedimento
Construção do
li-.I:FltfdaFfi'im
Depuraçáo em água artificial
por 48h, cond. ambientais controladas.
Recolha e preparação dos animais e sedimento
Exposição ao sedimento por 48h, condi@es ambientais controladas.
Exposição dos animais e
recolha dos pel/eÍs
Não
DepuraÉo em água salina por 48h, recolha dos pel/efs fecais
Avaliação preliminar do experimento
Centritugação, lioÍilizaÉo e extraÉo sequencial dos metais
Leitura amostras, tratamento estatístico redacção da tese.
Figura 7
-
Desenho expeÍimental do ptojecto.4.5.
Recolha ê pÍepaÍaçâo dosanimais
Para
a
experiênciaforam
utilizados420
exemplaresadultos
de S.
prana,recolhidos no Sapal das Hortas. Após a recolha, os animais foram colocados em água
salobra preparada artificialmente durante
7
dias em condiçõês controladas idênticasàs ambientais (temperatura, salinidade, luminosidade e oxigenação), com o objec{ivo
de
eliminaro
conteúdo residual existentenos
respectivostractos
digestivos dosexemplarês
e
aclimatá-lospara
a
experiência.Após
o
períodode
depuração osanimais
foram
distribuídos
nos
sete
tanques previamente preparados
com
o sedimento, perfazendo um total de 60 animais por tanque.4.6.
Recolha dospelíeÍs
Durante
a
experiência os animais ficaram nos tanques expostos ao sedimêntodurante
48h,
tempo definidona fase
de teste
como sendoo
necessáriopara
osexemplares
se
alimentaremdo
sedimento.Após esse
períodoos
animais foramretirados
e
colocados
em
água
preparada artificialmentepor
mais
48h,
paraeliminação do conteúdo do tubo digestivo. Após este período,
e
utilizando uma pipetadescartável
de 5
ml, foram feitasas
colheitas dos pel/eÍse
colocados em tubos decentrífuga
de
10 ml.
As
amostras foram cerúrifugadase
armazenadasa
4oC. No processo de recolha não foram consideradas as amostras de pseudofezes.O
processo descritono
passo4.6 deste
capítulofoi
repetidopor mais uma
vez utilizandoos
mesmos exemplaresde
S. plana, trocando apenas os sedimentos dos tanques. O objec{ivo de replicara
experiência foi aumentar a quantidade de amostra necessária aos testes. Para cada sériedo
trabalhoforam
recolhidas amostras do sedimento de todos dos tanques no inícioe
no finalde
cada experiência. Após as recolhas dos pel/eÍs nas duas fases,as
amostras foram lioÍilizadase
armazenadaspara a posterior extracção de metais.
mua,cb dos inv.,/(,,,ús Éa,.,rtno' be,lt6t,tco5 ,b êspec,s9ão de mgÚ',s pêsadosj espé.,ê osÍUdad' sc,oôícü,',,' Pâ,a
4.7.
QuantiÍicaçâo de matéria orgânica (TGA)Para determinar o teor de matéria orgânica das amostras
foi
utilizada a técnica Thermogravimetric AnalysisoGA).
Esta técnica consistena
dissociaçãode
massaorgânica com base em variações de temperatura. O sistema
(IGA)
é composto de umforno de alta precisão com aquecimento controlado até a temperatura de 100@C, uma
micro-balança
de alta
precisão,em
platina, resistenteas
altas temperaturase
queregista a perda de peso em relação à variação de temperatura.
$mFL:f,orbsmpb4l2+4)
TGA tu D_D$C..{2{}Ú
3 n
Figura 8
-
GráÍico de dêteminação da matéria otgânica'Este
sistemaé
alimentadopor um gás inerte
(Nz),gás
de
purga,e
um gás
decombustáo
(Oz). Uma grande vantagem deste sistema
é
poder trabalhar
com pequenas quantidadesde
amostrae
mesmoassim
permitium
elevadograu
deprecisão
nos
resultados.No
processode
decomposição/quantiÍicaçáoda
matériaorgânica, as amostras foram aquecidas da temperatura ambiente até uma tempêratura
de
550"C, (Fig.8)
(pontode
cálculoda
MO),em
atmosferade
Nze
uma taxa deaquecimento
de
3o"C/minutopara uma massa
de
aproximadamente 20mg.
Emseguida a mesma amostra continuou sendo aquecida até 800"C em atmosfera de 02,
mantendo
a
mesmataxa
de
aquecimento (3o'C/min.), temperaturafinal onde
écalculado o têor de matéria inorgânica na amostra. Todas as amostras foram testadas
lrútu&lcia alos Ínvorlobftclos estuartnos bê ,nlcos ia especiaçáo cte metars pêsraíos: espécie Qltudaata Scrobicutaria p,ana
em triplicado.
os
cálculosda
percentagemde
carbono orgânicoe
inorgânico foramrealizados utilizando um programa da TA lnstruments, que faz a interpolaçáo do pico
da
dissociaçãoda
amostrana
respectiva temperatura'tendo em
consideração a massa total de amostra utilizada.4.8.
Análise dedistribuição
dê paÉículesPara
a
análise
de
distribuiçãode
paÍtículas
nas
amostrasfoi
utilizado oequipamento Horiba CAPA-700 Particle
Size
Ditribution Analyzer
e
a
técnicacorrespondente. Esta técnica
é
baseada no princípio da foto-sedimentaçáo em fase líquida.A
mediçãoé
feita usandoo
princípio de transmissão óptica, que combina aequação de sedimentação com a relação de proporcionalidade entre a absorvância e
a concentração de partículas, ou seja, uma determinada partícula se tem um diâmetro (D)
e
uma densidade (p) dentro de uma solução de densidade (pn),e
um coeficiente de viscosidade(trtr)
e, como tal, irá precipitar a uma velocidade constante de acordocom
a
lei do efeito gravitacional. Na prática, as partículas têm vários diâmetros,e
avelocidade
de
sedimentação vai depender do tamanhoda
partícula. Partículas comdiâmetros maiores (D1) precipitarão primeiro.
o
método de transmissão óptico mede ograu de sedimentaçáo da partícula pela quantidade de luz transmitida pela soluçáo, a
intensidade da luz transmitida é absorvida pelo detector localizado do lado oposto da
célula
de
leitura.A
solução
utilizadaneste teste
foi
glicerinaem
água,
a
qualapresentou uma viscosidade
de 60.5
cP.As
amostrasforam
homogeneizadas nasolução de glicerina com ajuda
de
um banhode
ultra-sons, durante 15 segundos eutilizando a potência mínima para não quebrar as partículas; como branco foi utilizada
a mesma solução de glicerina em água.
Com
o
objectivo de abranger uma distribuição coma
maior amplitude possível'as
análises foram feitasem
duas etapas, envolvendo intervalos distintos(í20pm
a4pme4Uma0.4pm).
lÍnfrtÉrci., ús irv.,íEÚrado! osÍrraírit4r ôerrroricos ra ê§pêclrçáo d. rrrêÚaE pBadosr s§pécre ?5ía/dea,a Sctútctí',ria PÉ,íÉ
4.9.
Extracção sequencial dos metaisAntes
de
iniciar
a
extracção,todo
o
materialde
laboratório envolvido noprocesso
foi
devidamente descontaminado, primeiro numa soluçáode
HNOsa
10%durante 24h, e depois numa solução de HCI
a
10oÁ por 48h, e lavado em seguida portrês vezes com água desionizada para remover qualquer resíduo de ácido presente.
Para
a
êxtracção sequencialfoi
utilizadoo
procedimênto descrito por TessiereÍ
ar-(í979) e
modificado por Hullebusch et al. (2OO5). O método de extracção foi utilizadopara determinar a especiação química dos metais pesados (Cd, Co, Cr, Cu, Ni, Pb e
Zn),
tanto
nas amostrasde
sedimento, comonos
pellets,e
consistena
extracçáosequencial
de
fracções definidas operacionalmentea
partir
de
1
g
de
amostra, conforme se explica a seguit:ío passo:
extracção da fracção de troca com 10 ml de solução de acetato de amónia (ph7) 'lM;
agita-se duranteth
a
uma rotaçãode
150 rpme à
temperatura ambientee
centrifuga-se durante 10 minutosa
4000 rpm; apósa
cêntrifugação, osobrenadante é recolhido para análise;
?
passo: fracção ligada a carbonatos. Adicionam-se'10 ml de uma soluçáo 1Mde
ácidoaético,
agita-se durante th a
uma rotaçãode
150 rpme
à
temperatura ambientee
centrifuga-se durante 10 minutosa 4000
rpm; apósa
centrifugação' osobrenadante é recolhido para análise;
30 passo: fracção ligada à matéria orgânica e sulfuretos. Adicionam-se 5 ml de uma solução
a
30% de HzOz (PH 2, ajustado com NHO3); agita-se durante 3ha
150rpm
e
à temperatura de35'C,
cerúrifuga-se duÍante '10 minutos a 4000 rpm; após a centrifugação, o sobrenadante é recolhido para análise;40 passo, fracção residual ou litogénica
-
adicionam-se '10 ml de Aqua Regia(HNOa:HC| 1:3, v/v) e submete-se a uma digestÉio de elevada pressão (em reactores
de
TeÍlon@ fechados)durante
3h
a
110'C;
aguarda-seo
retomo
da
solução
àmtÉtch ar.§ lnvet/f;á,",das €síuarrros ócírúnicos ,â êsoêcrrcáo .tê n eÉlÍs pêtad(}sj espáciê êttt dtdt ScrolÍcrrÍ,aia p,r,,t
temperatura ambiente, filtra-se
e
períaz-seo
volume para 10ml com água ultra-pura (Miili-o);50
passo:
extracção total,em
bombas de Teflon; pesa-se 0.1g
da amostra,adicionam-se 2 ml de Agua Regra (HNO3/HC| 1:3 v/v), e submete'se a uma digestão
de elevada pressão (em reactores de Teflon@ fechados) durante 3h a '110"C; perfaz-se o volume conforme necessário até 10 ml com água Mili-Q.
Após a extracção, as amostras foram armazenadas a 4"C.
As
concentraçõesdos
metais
(Cd,
Co,
Cr,
Cu,
Ni, Pb
e
Zn)
foram
determinadasatravés
deEspec{rometria de Massa com induçáo de plasma acoplada (|CP-MS).
4.'10. Análise estatísüca
Todas as análises foram realizadas no programa STATISTICA 9.0 Analysis Pack
(StatSoft,
lnc., 2008).
Foramúilizados os testes
t-Studente
Mann-Vvhitney paracomparar os grupos de amostras envolvidas na análise para os dados paramétricos e não-paramélricos, respectivamente (Sokal & Rohlf, 1995: ZaÍ, 1999). Foi também feita
a análise de correlação entre os metais associados a cada fracção do sedimento e o
teor
de
matéria orgânicade
cada
amostra,tendo sido
utilizadoo
coeÍiciente de conelação de Pearson e análise de MDS por se ter verificado o carác{er paramétrico dos dados para esta análise.5
,rfru&rcia dos hw{,úraatolt e,rürarrirros óeíÍ{t bos ,ra e§peElaçáo d. men is peâdos: €péc,e .sfirdtdt Scmôícü,'"t Ph'a
5.í
Análise da composição de matéria orgânicaO teor de matéria orgânica variou entre 7.5oÂ
e
9.3o/o, para todas as amostrasavaliadas (sedimento inicial, perleÍs
e
sedimento controlo) (Fig. 9).As
amostras depelreÍs
(B)
e
controlo(C)
apresentaram concentraçõesmais
elevadasde
carbonoorgânico
em
relaçãoa
amostrade
sedimento inicial, porém, estas diferenças emrelação ao sedimento inicial (A) não foram estatisticamente significativas (p>0-05). O
valor médio mais elevado
foi
registado paraos
pel/eÚs, enquantoque o
sedimento inicial foi que apresentou menor valor médio de carbono orgânico.p8,00
L'
I
z,so7,OO
Figura
9:
Composiçãode
matéria orgânica no Sedimento inicial(A),
Pellets(B)
e
Sedimenb-controlo (C).A
análise de correlaçãode
Pearson entrea
acumulaçãode
metais nas váriasfracçôes
do
sedimentoe
dos
pel/etse
o
teor
de
carbono orgânico(Tab.
l)
nãoapresentou
valores
significativos
para
nenhuma
das
fracções
das
amostrascomparadas. 9,50 9,00 &50 6,50 6,00 A B c
a
25fr/ruârrcia atÉ l,,vqúrafu ea,,,,fi,nos futÍ/órricoa na q§,P€f,iação ah meàis pêsadosi .spécrê ê5t dad. Sc,oÔ,cr'&ti' p'4"
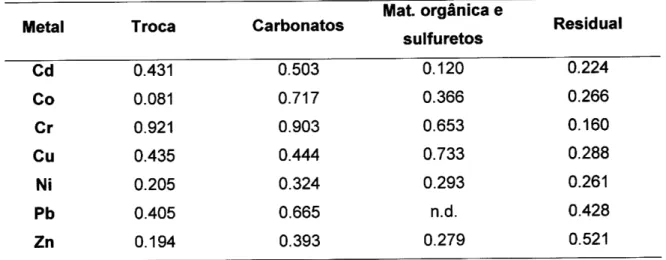
Tabela I -valores de p para análise de correlaçâo de Pearson entre a @ncentlEção de metais pesados em cada fracçáo do sedimento e teor de carbono orgânico das amostras; n.d. - abaixo do limite de detecçáo.
TÍoca Carbonatos
at
orgânica esulÍuretos
itEflíIl?tl
cd
GoCr
Cu Ni Pb Zn 0.43í 0.081 o.921 0.435 0.205 0.405 0.194 0.503 o.717 0.903 o.444 o,324 0.665 0.393 o.120 0.366 0.653 0.733 0.293 n.d. o.279 o.224 0.26ô 0.160 0.288 0.26'l o.428 o.5215.2
Análise dedistribuição
deA
análisede
distribuiçãode
partículas (Fig.10) demonstrou comportamentobastante semelhante
para
as
amostras
do
sedimento inicial
e
Íinal,
quando considerandoas
partículas inferioresa
4pm.As
amostrasde
perleÍs foramas
que apresentaram distribuição mais uniforme entre 0.4Um e 4.0Um. As partículas de maiorcalibre (entre 40pm
e
120pm) estão presentesem
todasas
amostrase
com umafrequência bastante similar. Comparando
a
distribuição entre 4pme
0.4pm para astrês amostras (Fig. 11), veriÍica-se que houve uma redução significativa no tamanho médio das partículas presentes nos pel/eús, quando comparado com as amostras de sedimento inicial e controlo. Em geral não se verificaram grandes dÚerenças entre as
amostras.
Observa-seque
a
distribuiçãode
partículas
de
todas
as
amostrasapresentou características multi-modais.
o $ L (I, -o (§ .2 (§ (l) L ,§ u = .o = g o LL -Tt õ -oc Ot = a. §) ÍD o C f o, o-qt
=
a f §)»iei+i+i*-"*i,ri{6i*--r"
"*t
nts,'"v ro§ .}e,ov oosps 21,0 100,00 0,00 18,0 t 40,00 15,0 2,0 9,0 6,4 3,0 0,0 80,00 60,00 20,00 (§ :g E o
c
o EE
0)a
tnftuência dos inver-tebrados estua rinos bentínicos na especração de ,netais pesados.' espécie estudada Scrobicularia plana
o o (§ -o (§ o 0) L (I, ,o c (O = o c) tL 21,0 18,0 15,0 12,O s,0 6,0 3,0 0,0 .r't o -o c Ot = o. íI' q) c} E 3 E § o 0)
=
=5 g) 0,0 20,0 100,0 80,0 60,0 40,0 \l L --, m .9 (ú () o LL a oõ
o--Tt d -oC (D, f 9. 0) q) o E = o, o-§)=
= = 0,"i"'i+i,;i"r]*i'ri+|+i+'-'.";4;q';r.1t4
*"
100,0 o (§ L o -o (§ .z (§ 0) L (§ 'õ E (0) = o (l) LL 40,0 20,0 0,0 80,0 60,0 21,O 18,0 15,0 12,0 9,0 6,0 3,0 0,0 C) o ot-c
o O o tr c) E E o U)Figura 10: Gráfico de distribuição de partículas (%) das amostras de sedimento e dos pel/efs.
27 ?
/
I
í
/
lnftuência dos inyerÍebrados esÍuarinos bentônicos na especlaçáo de metais pesados.'espécie estudada Scrobicularia plana 45,0 40,0 35,
0+
30,0r
Sed. Inicial Controlo n Sed. Digerido 0,0 120 -60
60-40 ?0-4 <4 pmFigura 11. Gráfico comparativo de PSD entre as amostras de sedimento e pellets no mesmo
intervalo.
5.3
Acumulação de metaisOs pel/efs
de
Scrobicularia plana apresentaram maior concentração de Cd, Cu,Pb
e
Zn, quando
comparadoscom
o
sedimentoinicial
e
de
controlo, tendo-severificado o inverso para os outros elementos (Co, Cr e Ni) (Fig. 12). No entanto, esta
diferença verificada entre os grupos não foi estatisticamente significativa.
5.4
Especiação de metaisA
acumulaçãode
metais encontrada nos pe//eÍsde
Scrobicularia plana diferedos resultados obtidos para
o
sedimento iniciale
sedimento controlo parao
Cd, Co,Cu, Ni,
Pbe Zn,
considerando todasas
associações químicas simultaneamente naanálise de ordenação muldimensional (nMDS)
(Fig
13).A
associação química de Cd,Co, Cu, Ni, Pb e Zn nas quatro fracções do sedimento usado nesta experiência estão
demonstradas na Figura 14.
s
o
o
o-28n
o
E
ô
+
t
tnfluência dos inveftebrados esÍuarinos bentànicos na especraçáo de metais pesados: espécie estudada Scrobicularia plana
';
(,, 1.60 ó =L 1,40 E C) 1,20 1,00 0,80 0,60 0,40 0,20 0,00 q oI f-= CJ 60,00 50,00 40,00 30,00 20,00 10,00 0,00:
600.00 CD g, a c 500,00 N 400,00 300,00 200,00 100,00 0,00r
12.00 o) ó f-c? (,l :L O q (I, 1 -o (L 35,00 30,00 25,00 20,00 15,00 10,00 5,00 0,00 140,00 120,00 100,00 80,00 60,00 40,00 20,00 0,00ABC
ABC
ABC
o
10,00 O 8,00 6,00 4,00 2,00 0,00:
25.00 o) ó=-z
20,00 15,00 10,00 5,00 0,00ABC
ABC
ABC
ABC
Figura 12
-
Acumulação de Cd, Co, Cr, Cu, Ni, Pb and Zn no sedimento inicial (A), pelefs (B)e sedimento controlo (C).
n
tr
T
o
@ @o
ffi ffi @o
t
o
ffi ffif, Mt
O&
@tr
o
29il
n
o
ô
o
o
ô
o
ü
tr
tr
mufurcIa aros irry.,lêbtús esÚt ritos óêrlÚôrrlcos ,ra úp€{,açro & me6,iç peados: GsÉa,e êsÍ/dad, Sc,oÔ'cubà p'a'a
cd
Co CrCu Ni Pb
Zn
Figura í3 - Ordenação multidimensional não-métrica (nMDS) das amostras de sedimento onde as associações químicas de metais foram determinadas: O - sedimento inicial; a - perleÍq
A
-sêdimento controlo.
A
maioria dos metais está ligada principalmente a fracção residual (Fig.í4). A
peroentagemde cada
metal ligadaàs
quatro fracções definidasseguiu a seguinte ordem: fracção residual > complexo matéria orgânica > carbonatos
> fracção de troca, com pequenas excepções.
Os valores do potencial redox e de pH foram praticamente constantes durante toda a experiência