UNIVERSIDADE DE LISBOA
FACULDADE DE CIÊNCIAS
DEPARTAMENTO DE BIOLOGIA ANIMAL
REMEDIAÇÃO DE AQUÍFEROS CONTAMINADOS
POR NITRATOS
(UM CASO DE ESTUDO POR BIORREMEDIAÇÃO)
Joana Madeira
MESTRADO EM ECOLOGIA E GESTÃO AMBIENTAL
2010
UNIVERSIDADE DE LISBOA
FACULDADE DE CIÊNCIAS
DEPARTAMENTO DE BIOLOGIA ANIMAL
REMEDIAÇÃO DE AQUÍFEROS CONTAMINADOS
POR NITRATOS
(UM CASO DE ESTUDO POR BIORREMEDIAÇÃO)
«Dissertação de mestrado orientada pela Prof. Doutora
Maria do Rosário Carvalho e pela Doutora Sandra Chaves»
Joana Madeira
MESTRADO EM ECOLOGIA E GESTÃO AMBIENTAL
2010
i
Agradecimentos
Em primeiro lugar, agradeço às minhas orientadoras, sem as quais teria sido impossível concretizar este trabalho. Obrigada por toda a ajuda, pelo interesse no decorrer do meu trabalho e pela simpatia com que sempre esclareceram as minhas dúvidas. No fundo, obrigada pela amizade.
Agradeço aos meus pais por me terem apoiado incondicionalmente em todos os passos da minha vida, pela força que me deram nos momentos mais complicados e também pela intensidade com que vivem as minhas alegrias e sucessos. À minha mãe por me ter acompanhado nas idas a Serpa para a amostragem de água subterrânea e ao meu pai por toda a ajuda na impressão e encadernamento da tese.
Ao Ricardo por estar sempre do meu lado…um verdadeiro companheiro, que não mede esforços para me fazer sentir feliz.
Agradeço à Professora Cataria Silva por toda a ajuda prestada nas determinações dos aniões por cromatografia iónica, uma verdadeira batalha!
À Professora Maria Manuela Simões, da Faculdade de Ciências e Tecnologia da Universidade Nova de Lisboa, por tornar possível a repetição de algumas análises de cromatografia iónica.
Ao ”Fred”, pela amizade e companhia durante as longas horas de trabalho laboratorial e por estar sempre disponível para ajudar.
A todas as pessoas que conheci no ICAT, em especial à Lara, ao Daniel, ao Sérgio e ao Ricardo, pela amizade e preocupação que sempre tiveram comigo. Não podia deixar de agradecer à Cátia por TODA a ajuda e também pelas brincadeiras que aliviaram os dias de laboratório mais cansativos.
A todos os meus colegas de mestrado que adorei conhecer e que me fizeram sentir em “casa” nesta faculdade, especialmente a Sara, a Mafalda, a Ana Rita, a “Vó”, a “Seta” e a Dora.
ii
Resumo
A eliminação de nitrato nas águas subterrâneas é prioritária em vários países, dada a sua toxicidade e presença generalizada.
A biorremediação, por bioestimulação, consiste numa estratégia de remoção de nitrato frequentemente adoptada dada a sua acção rápida, baixo investimento e aplicação in-situ. Para além das vantagens referidas, aparenta ser a solução mais adequada do ponto de vista ambiental e prático.
Neste estudo, a actividade microbiana é utilizada como principal factor de redução de nitrato a azoto molecular, através da estimulação do processo de desnitrificação biológica, após a adição de uma fonte de carbono à água subterrânea (etanol, serradura, carvão, ácido cítrico ou ácido acético).
O local de estudo corresponde ao aquífero Serpa-Brinches, caracterizado como livre e pouco profundo, o que aumenta o seu risco de poluição.
O principal objectivo deste trabalho consiste na elaboração de uma proposta de remediação do aquífero Serpa-Brinches, a partir da selecção da fonte de carbono mais eficiente na remoção de nitrato e com produção mínima de compostos tóxicos, bem como na identificação das bactérias desnitrificantes capazes de efectuar esta remoção de nitrato do aquífero. Pretendeu-se ainda simular o fluxo e movimento de partículas no aquífero, para identificar a técnica de aplicação in-situ mais adequada à estratégia de biorremediação desenvolvida neste estudo.
Palavras-chave: Nitrato, biorremediação, desnitrificação, aquífero Serpa-Brinches.
iii
Abstract
Nitrate is a pollutant with priority to be removed from groundwater, due to its toxicity and widespread presence.
Bioremediation, trough biostimulation, is a nitrate removal strategy frequently adopted because it has a quick action, low investment requirement and on-site application. It also appears to be the most suitable solution from an environmental and practical perspective.
In this study, the microbial activity is used as the main factor for reducing the nitrate to nitrogen gas, by stimulating the process of biological denitrification after the addition of a carbon source to a groundwater (ethanol, citric acid, acetic acid, sawdust or coal).
The study site is the Serpa-Brinches aquifer, characterized as unconfined and shallow, what leads to a higher risk of pollution.
The main goal of this work was the elaboration of a remediation proposal for the Serpa-Brinches aquifer, from the selection of the most efficient carbon source that provides a higher rate of nitrate reduction, with a minimal production of other toxic compounds and the identification of the autochthones denitrifying bacteria that can perform this nitrate removal. It was also pretended to simulate the aquifers flow and particle movement, to identify the on-site application most suited to the bioremediation strategy developed in this study.
1
Índice
Agradecimentos ... i Resumo ... ii Abstract ... iii I. Introdução geral ... 31. Características gerais dos sistemas aquíferos ... 3
2. Origens e consequências da poluição por nitrato ... 3
3. Prevenção e remoção de nitrato da água subterrânea ... 5
II. Aquífero Serpa-Brinches ... 7
III. Objectivos gerais ... 11
IV. Biorremediação de águas subterrâneas contaminadas por nitrato ... 12
1. Introdução ... 12
2. Objectivos ... 15
3. Materiais e Métodos ... 16
3.1) Amostragem da água subterrânea ... 16
3.2) Ensaios microbiológicos ... 18
3.2.1) Fontes de carbono ... 18
3.2.2) Preparação dos meios de cultura ... 19
3.2.3) Avaliação da capacidade de desnitrificação ... 19
3.2.4) Método do número mais provável ... 20
3.2.5) Conservação de células ... 21
3.3) Ensaios químicos ... 22
3.3.1) Caracterização físico-química da água ... 22
4. Resultados e discussão ... 25
4.1) Primeiro ensaio ... 25
4.1.1) Remoção de nitrato e nitrito e determinação do NMP ... 25
4.1.2) Composição da água ... 27
4.1.3) Avaliação da variação da determinação de aniões ... 28
4.1.4) Carbono total dissolvido ... 29
4.2) Segundo ensaio ... 29
4.3.1) Remoção de nitrato e nitrito e determinação do NMP ... 29
4.3) Terceiro ensaio ... 30
2
4.3.2) Composição da água ... 32
4.3.3) Avaliação da variação da determinação de aniões ... 32
4.3.4) Carbono total dissolvido ... 33
4.4) Quarto ensaio laboratorial ... 34
4.4.1) Remoção de nitrato ... 34
4.4.2) Composição da água ... 35
5. Conclusões ... 35
V. Isolamento e identificação do consórcio bacteriano mais eficiente na remoção de nitrato da água subterrânea ... 36
1. Introdução ... 36
2. Objectivos ... 37
3. Materiais e métodos ... 37
3.1) Preparação dos meios de cultura ... 37
3.2) Isolamento dos microrganismos do consórcio seleccionado ... 37
3.3) Extracção do DNA ... 38
3.4) PCR „fingerprinting‟ ... 38
3.5) Amplificação de genes ribossomais e identificação por sequenciação ... 40
4. Resultados e discussão ... 41
5. Conclusões ... 46
VI. Modelação do escoamento no aquífero Serpa-Brinches, com aplicação de biorremediação ... 46
VII. Considerações finais ... 52
VIII. Referências ... 52
IX. Anexos ... 56
3
I. Introdução geral
1. Características gerais dos sistemas aquíferos
As águas subterrâneas representam um papel importante no ciclo hidrológico terrestre, sobretudo ao nível das reservas estratégicas de água doce.
O ciclo da água subterrânea divide-se em três etapas: a recarga, a circulação de água no subsolo e a descarga.
A recarga (entrada de água no sistema hidrogeológico) dá-se, principalmente, a partir do excedente da precipitação, ou seja, a alimentação é feita pela água que não é evaporada, evapotranspirada ou sujeita a escorrência superficial. Por outro lado, a entrada de água também pode ser proveniente de rios ou de lagos que alimentam o aquífero, ou da injecção directa em furos (recarga artificial).
A qualidade natural das águas subterrâneas, sem a intervenção do Homem, depende da composição da água de precipitação, da composição do solo, da natureza geológica do aquífero, das propriedades físicas, químicas e biológicas do meio envolvente e da própria água, bem como da extensão e tempo de contacto da água com o meio envolvente (Todd, 1959 in Ferreira, 1997).
A poluição das águas subterrâneas pode ser pontual ou difusa. Na poluição pontual a origem da carga poluidora é bem definida, como por exemplo descargas provenientes de fábricas. Na poluição difusa não é possível determinar a exactidão dessa origem, correspondendo normalmente a áreas extensas, como é o caso de áreas de irrigação e zonas urbanas.
Um dos principais casos de poluição difusa em águas subterrâneas corresponde à sua contaminação por nitrato (NO3-), que resulta geralmente do excedente de azoto aplicado na agricultura e que não é absorvido durante o ciclo vegetativo das plantas, acabando por ser transportado para a zona saturada1 e disseminado por áreas extensas.
2. Origens e consequências da poluição por nitrato
A eliminação de nitrato nas águas subterrâneas é prioritária em vários países, dada a toxicidade e presença generalizada deste poluente nas mesmas (Della Rocca
et al, 2006).
1
4 As principais causas de poluição por nitrato em Portugal têm origem, sobretudo, na intensificação da agricultura de regadio e na actividade pecuária (Environmental Performance of Agriculture in OECD Countries since 1990: Main Report, 2008).
Na agricultura, a tendência para a intensificação da produtividade durante grande parte dos últimos cinquenta anos, foi acompanhada pelo crescimento significativo da utilização de fertilizantes, sobretudo de azoto inorgânico. Durante este período, a evolução da agricultura tem-se caracterizado por uma redução das pastagens permanentes e das zonas “tampão” (valas e sebes, zonas húmidas, entre outras), o que favorece o escoamento superficial, a erosão e a lixiviação dos nutrientes para os ecossistemas aquáticos e águas subterrâneas. A actividade pecuária também aumentou durante a maior parte deste período, contribuindo para uma maior carga global de azoto sobre os solos agrícolas da EU, resultante do estrume produzido pelos animais, principalmente bovinos, suínos, aves de capoeira e ovinos (Aplicação da Directiva 91/676/CEE do Conselho relativa à protecção das águas contra a poluição causada por nitrato de origem agrícola - Síntese dos relatórios dos Estados-Membros relativos a 2000, 2003).
As práticas de adubação não controladas (aplicação de fertilizantes em excesso e em época errada, entre outras) provocam a acumulação de compostos azotados no solo. O ião nitrato é muito solúvel na água e não é retido pelo “complexo adsorvente” do solo. É, portanto, facilmente lixiviado pelas águas de percolação até à zona saturada. O processo de lixiviação pode ser muito lento em função das características do solo e do subsolo em causa. No entanto, nas águas subterrâneas o ião nitrato apresenta elevada mobilidade, devido à sua grande solubilidade, à sua adsorção praticamente nula e a um retardamento baixo ou nulo, podendo migrar facilmente a longas distâncias a partir da sua entrada no sistema (Ribeiro et al).
A aplicação de estrumes e chorumes2, enquanto fertilizantes orgânicos, contribui igualmente para o aumento de nitrato, devido à nitrificação da amónia resultante da fermentação de compostos azotados presentes nos dejectos animais (Ribeiro et al).
Vários países da União Europeia detectaram, através de estações de monitorização, que entre 1996 e 1998 as suas águas subterrâneas apresentavam uma concentração superior a 50 mg NO3-/l (valor máximo permitido para água de consumo humano), (Schipper et al, 2004). Em Portugal, durante esse período de tempo, mais de 50% das estações de monitorização de águas subterrâneas em zonas vulneráveis ao
2
Constituído essencialmente por uma mistura de dejectos sólidos e líquidos animais com restos de rações e água de lavagem.
5 nitrato registaram concentrações deste anião superiores ao valor máximo permitido para água de consumo humano (OCDE, 2008).
3. Prevenção e remoção de nitrato da água subterrânea
A poluição por nitrato pode ser prevenida através da redução da libertação de nitrato para o ambiente, ou do controlo das suas fontes e ainda pelo tratamento da água contaminada.
A prevenção da libertação de nitrato para o meio ambiente é uma ferramenta que pode ser implementada através de legislação que actue directamente sobre essas práticas, tal como a Directiva 91/676/CEE do Conselho de 12 de Dezembro de 1991, vulgarmente referida como “Directiva Nitratos”. Esta é relativa à protecção das águas contra a poluição causada por nitrato de origem agrícola e determina que os Estados Membros designem as zonas que drenam para as águas poluídas ou susceptíveis de o serem, por nitrato de origem agrícola, como Zonas Vulneráveis com base em resultados de monitorização, prevendo também a elaboração dos respectivos Programas de Acção (Della Rocca et al, 2006; Aplicação da Directiva 91/676/CEE do Conselho relativa à protecção das águas contra a poluição causada por nitrato de origem agrícola - Síntese dos relatórios dos Estados-Membros relativos a 2000, 2003). Dando seguimento ao determinado na “Directiva Nitratos”, Portugal elaborou um Código de Boas Práticas Agrícolas a aplicar voluntariamente pelos agricultores, tendo em vista eliminar ou minimizar tanto quanto possível os riscos da poluição difusa de origem agrícola. Nele se estabelecem “orientações e directrizes de carácter geral, na tomada de medidas que visem racionalizar a prática das fertilizações e de todo um conjunto de operações e de técnicas culturais que directa ou indirectamente, interferem na dinâmica do azoto nos ecossistemas agrários, por forma a minimizar as suas perdas sob a forma de nitrato e, assim, proteger as águas superficiais e subterrâneas desta forma de poluição” (Ribeiro et al).
Outra ferramenta legal igualmente importante no que diz respeito à gestão sustentável e à protecção das águas subterrâneas é a Directiva 2000/60/CE, do Parlamento europeu e do Conselho, de 23 de Outubro (“Directiva Quadro da Água” - DQA), que estabelece um quadro de acção comunitária no domínio da política da água, transposta para a ordem jurídica nacional pela Lei n.º58/2005, de 29 de Dezembro (“Lei da Água”) e pelo Decreto-Lei n.º 77/2006, de 30 de Março. A DQA e a “Lei da Água” salientam que as medidas previstas nos Planos de Gestão de Bacia Hidrográfica têm por objectivo: “proteger, melhorar e restaurar as águas subterrâneas,
6 prevenir a sua poluição e deterioração e assegurar um equilíbrio entre a sua captação e renovação”. Estes objectivos deverão ser atingidos até 2015.
Uma das grandes preocupações acerca da presença de nitrato em água para consumo humano está relacionada com a toxicidade deste composto. O nitrato pode ser reduzido a nitrito pelo metabolismo humano. Quando esta redução ocorre no organismo humano a hemoglobina é oxidada a metemoglobina, impedindo o transporte normal do oxigénio pelo sangue, causando uma doença designada metemoglobinémia, ou síndrome do bebé-azul devido à cianose das células o que torna a pele azulada, afectando maioritariamente bebés com menos de 6 meses de idade (Agostinho e Pimentel, 2005).
Actualmente, há necessidade de mais estudos que relacionem a ingestão de nitrato com a ocorrência de carcinomas. Segundo alguns autores (van Loon et al, 1997; Yang et al, 2007) ainda não é possível afirmar a existência dessa ligação, embora existam alguns estudos efectuados que o descreverem para determinados casos (Soares, 2000; Gulis et al, 2002, Agostinho e Pimentel, 2005).
Devido às potenciais consequências derivadas da ingestão de nitrato, é fundamental recorrer atempadamente a técnicas adequadas à sua remoção, de modo a evitar o consumo de água contaminada, uma vez que os tratamentos convencionais não removem eficazmente este composto (Soares, 2000). Há, assim, necessidade de baixar a concentração de nitrato presente na água até a níveis permitidos pela Comunidade Europeia, para que a água consumida não cause problemas de saúde pública. Ao longo do tempo foram desenvolvidas várias técnicas de remediação de aquíferos, resumidas no Quadro 1. As mais promissoras consistem no tratamento
in-situ dos contaminantes.
Quadro 1 -Algumas das mais importantes técnicas de remediação de aquíferos (Della Rocca et al,
2006; Hígidus, 2009; Díaz et al, 2000; Prakasa Rao et al, 2006; Fenton et al, 2008; De Heredia et al,
2005;Shrimali et al, 2001; Iwamoto et al, 2001).
In-situ: Tratamento Físico/Químico: ■ Recarga artificial ■ Redução química ■ Adsorção física
■ Injecção de ar (air sparging) Tratamento Biológico: ■ Biorremediação – Bioatenuação – Bioestimulação – Bioaumento ■ Barreiras Reactivas – Biorremediação – Troca-iónica – Osmose inversa Ex-situ: Tratamento Físico/Químico: ■ Bombagem e tratamento – Troca – iónica – Osmose inversa – Electrodiálise
7
II. Aquífero Serpa-Brinches
O aquífero de Serpa-Brinches, objecto deste estudo, corresponde ao Sector Este do Sistema Aquífero dos Gabros de Beja (SAGB; Figura 2; Duque 1997, 2005, Duque e Almeida, 1998; Paralta, 2000). Localiza-se na província do Baixo Alentejo, entre Beja e Serpa e estende-se pelos concelhos: Ferreira do Alentejo (a Oeste), Beja (no centro) e Serpa (a Este) (Figura 1).
Figura 1 – Localização geográfica do SAGB (350 km2
) e da área de estudo (60 km2), (Duque, 2005). A principal utilização dos recursos subterrâneos deste aquífero é o abastecimento público e privado a partir de furos e uso agrícola e pecuário a partir essencialmente de poços. Estas captações, até há pouco tempo, garantiam na totalidade o abastecimento do concelho, que conta com uma população aproximada de 10000 habitantes. Desde que o abastecimento passou a ser realizado preferencialmente a partir da Albufeira do Enxoé, algumas das captações existentes (7 em Serpa e 2 nos arredores de Brinches) passaram a constituir uma reserva estratégica de água (Paralta) (Figura 2).
O SAGB é essencialmente constituído por gabros e dioritos, pertencentes ao Complexo Ígneo de Beja e ao Complexo Ofiolítico de Beja-Acebuches. Em termos hidrogeológicos, estas litologias apresentam um comportamento hidrodinâmico e hidroquímico relativamente homogéneo, o que permite considerá-las num único conjunto.
Figura 2 - Principais usos das captações inventariadas na área entre Serpa e Brinches.
8 O sistema exibe um comportamento misto de características porosas e fissuradas (Duque, 1997, 2005; Duque e Almeida, 1998; Paralta, 2000). Apresenta comportamento de aquífero livre, i.e., não está limitado superiormente por uma formação impermeável, estando a água em equilíbrio com a pressão atmosférica. Duque (2005) definiu três níveis produtivos para o SAGB, consoante as suas características hidráulicas (Figura 3): o primeiro corresponde à zona alterada, onde a circulação de água é efectuada por meio poroso; o segundo nível diz respeito à zona fracturada, sendo esta a principal responsável pela recarga do sistema aquífero; e o terceiro nível corresponde à zona compacta, onde a probabilidade de ocorrerem fracturas com interesse hidrogeológico diminui com a profundidade.
Duque (2005), através de interpretação de dados de 30 furos, estimou a transmissividade média de 37,9 m2/dia para este aquífero, mediana de 16,2 m2/dia, mínimo de 3,1 m2/dia e máximo de 371,4 m2/dia. Segundo este autor, a distribuição da transmissividade tem uma grande variabilidade espacial, como é característico de aquíferos fracturados, sendo que as áreas do aquífero com menor transmissividade se encontram representadas ao redor de Serpa.
Devido à heterogeneidade deste aquífero a condutividade varia localmente, observando-se variações entre 0,0002 m/dia a 25 m/dia (Duque, 2005). Os valores mais baixos estão associados às zonas constituídas por blocos mais compactos e os valores mais elevados a zonas mais alteradas e fracturadas.
Com base na monitorização de níveis piezométricos em furos e poços do SAGB, Duque (1997) e Duque e Almeida (1998) realizaram um trabalho de modelação numérica determinística, o qual permitiu estimar os potenciais hidráulicos em regime de equilíbrio neste sistema aquífero. Paralta (2000) realizou a modelação estocástica para o sector Serpa-Guadiana e definiu os sentidos de fluxo e gradientes hidráulicos (Figura 4). A superfície piezométrica acompanha aproximadamente o modelado topográfico, com gradientes suaves entre 2 e 4% para Oeste, encontrando-se a
Figura 3 - Estrutura vertical do SAGB proposta por Duque (2005).
9 poucos metros de profundidade (entre 0,75 e 5 m de profundidade, Duque e Almeida, 1998), embora na época estival o nível piezométrico desça alguns metros.
Figura 4 - Superfície piezométrica e sentidos de fluxo para o aquífero gabróico da margem esquerda do Guadiana, a partir de medições de Setembro de 1998 (Paralta, 2000).
Estas características geológicas e hidrogeológicas fazem com que este aquífero seja muito vulnerável à contaminação.
A principal fonte de recarga do sistema aquífero provém da precipitação que se infiltra em toda a área de afloramento do sistema, embora as zonas mais elevadas sejam mais propícias para esse efeito. O sistema descarrega através de nascentes e, fundamentalmente, nas linhas de água, até ser atingido o nível de equilíbrio.
Segundo Paralta (2000), os recursos hídricos totais disponíveis anualmente para recarga são de 69,7 mm, ou seja, 14% da precipitação média anual, o que representa para a área do sector Serpa-Guadiana do SAGB (aproximadamente 60 km2) cerca de 4,2 x 106 m3/ano. Este valor não representa, no entanto, a infiltração eficaz ou recarga, uma vez que alguns recursos (não quantificados) se perdem por escorrência ao longo das linhas de água acabando por afluir ao rio Guadiana.
A água subterrânea proveniente deste aquífero apresenta, geralmente, elevada mineralização, apresentado medianas de condutividade eléctrica e resíduo seco de 684 µS/cm e 484 mg/l, pH com tendência alcalina (> 7) e fácies bicarbonatadas calco-magnesianas dada a circulação da água em rochas ígneas básicas (gabros), (Paralta, 2000). Na Figura 5 pode ser observada a distribuição espacial da composição da água subterrânea captada na região entre Serpa e Brinches, através de diagramas de Stiff.
10 Figura 5 - Diagramas de Stiff para águas captadas na região entre Serpa e Brinches (Paralta, 2000)
O principal problema ao nível do consumo humano das águas deste aquífero prende-se com os teores em nitrato, que frequentemente ultrapassam o limite legalmente imposto, 50 mg/l (Duque e Almeida, 1998, Duque, 2005, Paralta, 2000, Paralta e Francés, 2000).
A degradação da qualidade da água subterrânea, resultante da contaminação difusa por nitrato, tem origem no excedente de azoto (N) aplicado na agricultura, sob a forma de azoto amoniacal (NH4+), ureia e outros compostos azotados usados nos fertilizantes, que não é absorvido durante o ciclo vegetativo, acabando por ser transportado para a zona saturada e disseminado por extensas áreas.
Duque (2005) cruzando informação sobre a quantidade de precipitação e as concentrações do ião nitrato nas águas subterrâneas encontrou uma forte correlação entre ambas, uma vez que as concentrações mais altas de nitrato correspondiam aos períodos de maior precipitação. A irregularidade climática, com frequentes regimes torrenciais, provoca a lixiviação precoce dos fertilizantes. O facto das épocas de fertilização coincidirem com o semestre húmido, ou seja, com o período de recarga útil dos aquíferos (em especial durante o trimestre Jan-Mar/Abr), provoca alterações sazonais e cumulativas na qualidade da água subterrânea do SAGB.
11 Duque (2005) propôs o modelo conceptual de transporte vertical da massa de nitrato para a água subterrânea do SAGB (Figura 6), com o objectivo de explicar a variabilidade e os picos de concentração desta espécie na água. Após a remoção das culturas estivais ficam retidas grandes quantidades de azoto no solo, sob diversas formas: mineralizado, NH4+, NO3-, entre outras. Nesta altura, as fendas de retracção apresentam grandes profundidades, podendo chegar a entrar em contacto com a superfície freática. Quando ocorrem as primeiras chuvas, as fendas de retracção constituem uma via preferencial para a infiltração de água no solo, lixiviando o nitrato e os pesticidas que aí se encontram, disponibilizando-os para a zona não saturada3. Posteriormente, dá-se a subida gradual dos níveis piezométricos, o que irá contribuir para a difusão do nitrato a partir da matriz do solo. Após o fecho das fendas de retracção, a sua contribuição para a difusão de nitrato desvanece-se e domina o fluxo pela matriz do solo.
Figura 6 - Modelo conceptual proposto por Duque (2005), relativo às três fases de transporte vertical de massa de nitrato para as águas.
III. Objectivos gerais
Este estudo teve como principal objectivo, a avaliação da eficiência da remoção de nitrato de uma água subterrânea contaminada por este. Foram usadas técnicas de
3
Zona que se situa imediatamente abaixo da superfície topográfica e acima do nível freático, onde os espaços vazios entre as partículas estão parcialmente preenchidos por gases (essencialmente ar e vapor de água) e por água. A água contida nesta zona encontra-se à pressão atmosférica, podendo ser utilizada pelas raízes das plantas ou contribuir para o aumento das reservas de água subterrânea.
12 biorremediação e simulados os seus efeitos num aquífero, utilizando modelação numérica de fluxo e transporte de massa, de modo a seleccionar a melhor estratégia de remediação.
Para a aplicação da técnica de biorremediação foi seleccionado o aquífero de Serpa-Brinches, localizado no sector Este do Sistema Aquífero dos Gabros de Beja, sistema classificado como “Zona Vulnerável” à contaminação por nitrato, pela Portaria nº 1100/2004 de 3 de Setembro.
A aplicação da biorremediação neste trabalho é inovadora, uma vez que não tinha sido empregue em Portugal, embora apresente um elevado potencial dadas as suas vantagens (baixo investimento, acção rápida, aplicação in-situ, entre outras), tal como sugerem trabalhos efectuados no estrangeiro (Pickup et al, 2001; Israel et al, 2009). Desta forma, contribui-se para o aumento do conhecimento técnico relativamente a este tipo de medidas de remediação, em Portugal.
IV. Biorremediação de águas subterrâneas contaminadas por
nitrato
1. Introdução
Neste trabalho, entre as várias técnicas de remediação de aquíferos, investiu-se na aplicação de um método de biorremediação, uma vez que estas metodologias têm recebido especial atenção pela comunidade científica como medida biotecnológica eficaz na descontaminação de ambientes poluídos. Em termos gerais, a biorremediação consiste na utilização de determinados microrganismos de forma a degradar substâncias nocivas para o ambiente e para os seres vivos, transformando-as em substâncitransformando-as com pouca ou nenhuma toxicidade (Abdeloutransformando-asa et al, 2000).
A biorremediação oferece várias vantagens comparativamente às técnicas químicas e físicas convencionais. A vantagem mais atractiva desta técnica consiste na sua aplicação in-situ, causando uma perturbação mínima do sistema. Outra grande vantagem corresponde à capacidade extensiva de degradação de compostos sintéticos por parte dos microrganismos, o que permite a aplicação desta técnica em locais contaminados por vários poluentes (Iwamoto et al, 2001). É capaz de tratar contaminantes diluídos e com grandes áreas de dispersão, requer investimentos baixos, tem uma acção rápida e pode ser aplicada em simultâneo com outros tratamentos químicos e físicos (Boopathy, 2000).
13 Como principais desvantagens desta metodologia consideram-se o facto de alguns contaminantes não serem passíveis de ser biodegradados (metais pesados, por exemplo), o metabolismo de certos microrganismos poder levar à produção de compostos tóxicos e por consistir numa estratégia com aplicação específica em cada local, requerendo sempre estudos prévios de pequena escala anteriores à sua aplicação no terreno (Boopathy, 2000).
Numa estratégia de biorremediação podem-se considerar três métodos hierarquizados por complexidade crescente (Iwamoto et al, 2001):
– Bioatenuação: consiste em monitorizar o progresso natural de degradação, em determinados pontos de recolha de amostras, ao longo do tempo (Iwamoto et al, 2001).
– Bioestimulação: adopta-se quando a degradação natural dos contaminantes não se dá ou é muito lenta, manipulando o ambiente de modo a que a biorremediação seja estimulada. Essa estimulação é feita através da adição de nutrientes com dadores de electrões e/ou fontes de carbono. Contudo esta adição tem de ser efectuada de forma bastante controlada, uma vez que em muitos dos casos os compostos químicos adicionados ao ambiente são tóxicos, havendo a necessidade de monitorizar cuidadosamente todo o processo. É expectável, pela acumulação de evidências científicas, que a aplicação in-situ da bioestimulação se torne numa tecnologia segura de descontaminação (Iwamoto et al, 2001).
– Bioaumento: corresponde à terceira escolha desta hierarquia, ou seja, quando nenhuma das anteriores pode ser aplicada. Consiste na maximização das capacidades de biodegradação dos locais contaminados, através da inoculação de bactérias que apresentem as capacidades catalíticas desejáveis de forma a degradar os contaminantes alvo. Considera-se que esta é uma abordagem bastante eficiente, apresentando, contudo, a desvantagem de poder causar efeitos desconhecidos no ecossistema, uma vez que são introduzidas grandes quantidades de bactérias. Após a remediação é necessário confirmar que as bactérias injectadas não se mantêm viáveis, de forma a não afectarem por um longo período a comunidade biológica autóctone do local (Iwamoto et al, 2001).
A biorremediação do nitrato tem por base um processo do ciclo do azoto, designado desnitrificação biológica, que permite a ocorrência da redução do nitrato a óxidos de azoto, originando por fim um produto não tóxico, o azoto gasoso.
14 NO3- → NO2- → NO - → N2O → N2
Existem mais de 45 géneros de bactérias e fungos capazes de reduzir o ião nitrato a nitrito. Contudo, esta redução não resulta sempre numa diminuição do azoto removido, pois neste caso só constituem interesse os microrganismos desnitrificantes capazes de reduzir o nitrato a azoto gasoso, facilmente removido do ecossistema a tratar, contribuindo deste modo para a redução do nitrato presente no meio (Fahrner, 2002).
As bactérias desnitrificantes apresentam algumas características em comum: ubiquidade; variabilidade; plasticidade metabólica e grande capacidade de transferência horizontal de genes, permitindo a aquisição de novas características e maior facilidade de adaptação ao ambiente onde se encontram (Rivett et al, 2008).
As bactérias presentes em aquíferos obtêm energia a partir da oxidação de compostos orgânicos ou inorgânicos, podendo ser, respectivamente, heterotróficas ou autotróficas. As bactérias autotróficas usam carbono inorgânico como fonte de carbono, enquanto que as heterotróficas utilizam carbono. As bactérias desnitrificantes podem ser encontradas a grandes profundidades nos aquíferos e são geralmente anaeróbias facultativas heterotróficas (Rivett et al, 2008).
O carbono orgânico tende a ser oxidado preferencialmente num processo de respiração aeróbia, na qual o aceitador final de electrões é o oxigénio. Isto porque este processo é o mais favorável em termos energéticos. Quando há um excesso de carbono orgânico as bactérias aeróbias utilizam o oxigénio dissolvido até este ser consumido, momento a partir do qual, outros aceitadores de electrões se tornam energeticamente favoráveis. À medida que os níveis de oxigénio vão diminuindo, as bactérias anaeróbias facultativas vão começar a utilizar os restantes dadores de electrões disponíveis. Algumas destas bactérias anaeróbias facultativas utilizam o nitrato como aceitador de electrões. (Rivett et al, 2008).
A ausência de oxigénio e a presença de carbono orgânico, enxofre e ferro reduzidos, facilitam a ocorrência de desnitrificação. Importa garantir que a redução de nitrato é feita até à obtenção de azoto gasoso, uma vez que os produtos intermédios da desnitrificação (óxidos de azoto: nitrito, óxido nítrico e óxido nitroso) são mais tóxicos do que o próprio nitrato, contribuindo para a chuva ácida, aquecimento global e para a destruição da camada de ozono, podendo ainda prejudicar a saúde (nitrito). Quando o nível de oxigénio é muito baixo forma-se azoto gasoso mas quando os níveis de oxigénio são intermédios ou variáveis, as reacções podem parar na formação de óxidos de azoto. Quando os valores de nitrato são muito elevados ou o
15 pH é muito baixo a desnitrificação pode parar na formação de óxido nitroso (Rivett et
al, 2008).
Dos factores que poderão contribuir para o insucesso da desnitrificação biológica podemos identificar o teor de oxigénio, a concentração de aceitadores de electrões, a presença de bactérias desnitrificantes e a quantidade de carbono orgânico presente no meio (factor mais condicionante
).
Outros factores limitantes, mas que apenas influenciam secundariamente as taxas de desnitrificação, correspondem à concentração de nitrato no meio, disponibilidade de nutrientes, pH, temperatura e presença de toxinas. Em seguida, alguns destes factores limitantes serão explicados de forma mais detalhada (Rivett et al, 2008):A desnitrificação biológica ocorre perante concentrações de oxigénio dissolvido abaixo de 1 ou 2 mg-O2/l. DeSimone e Howes (1998) observaram que quanto menor for a concentração em oxigénio maior serão as taxas de desnitrificação, uma vez que o nitrato, como aceitador final de electrões na cadeia respiratória, é menos favorável energeticamente do que o oxigénio.
A gama de pH óptima para as bactérias desnitrificantes heterotróficas encontra-se geralmente situada entre 5,5 e 8 (Rust et al, 2000). Valores de pH fortemente ácidos (pH <5) inibem a desnitrificação, parando a reacção química na formação de produtos intermédios, altamente prejudiciais ao ambiente e à saúde (Brady and Weil, 2002). Rust et al (2000) refere como limite superior de pH o valor de 8,3, acima do qual a desnitrificação não ocorre.
Na desnitrificação biológica a gama óptima de temperaturas está situada entre 25 e 30 ºC mas normalmente o processo pode ocorrer entre 2 e 50 ºC (Brady and Weil, 2002). Robertson et al (2000) demonstrou a relação entre a temperatura da água e os níveis de desnitrificação através de um sistema de barreira reactiva, onde verificou que o aumento de temperatura na gama anteriormente referida era acompanhado de um aumento da taxa de desnitrificação.
2. Objectivos
Pretendeu-se avaliar a aplicabilidade da biorremediação na redução da concentração de nitrato no aquífero Serpa-Brinches, uma vez que esta técnica requer estudos específicos em cada local. Assim, procurou desenvolver-se uma metodologia capaz de reduzir a concentração de nitrato no aquífero em estudo a valores inferiores ao permitido por Lei.
16 A técnica de biorremediação seleccionada teve como base a acção desnitrificante de microrganismos autóctones do aquífero, após a adição de um substrato orgânico (ácido acético, ácido cítrico, etanol, serradura ou carvão), contribuindo para a redução da concentração de nitrato na água subterrânea em estudo. Pretendeu-se, portanto, avaliar a capacidade da comunidade microbiana do aquífero reduzir o nitrato, tendo como fontes de carbono cada um dos substratos referidos de forma a seleccionar o mais eficiente e com menor produção de compostos tóxicos.
3. Materiais e Métodos
3.1) Amostragem da água subterrânea
Na realização deste trabalho foram feitas quatro amostragens de água subterrânea proveniente do aquífero Serpa-Brinches, sendo que a primeira foi efectuada a 25 de Janeiro, a segunda a 8 de Março, a terceira a 3 de Maio e a última a 26 de Julho. A água recolhida em cada amostragem foi utilizada na realização de um ensaio laboratorial, tendo sido efectuados quatro ensaios no total.
Sendo o aquífero de Serpa-Brinches relativamente uniforme do ponto de vista litológico, químico e ambiental, optou-se por recolher água num poço onde se juntam água extraídas por várias captações para se proceder aos ensaios laboratoriais. Para além do mais, tendo em conta os prazos definidos para uma dissertação de mestrado, seria demasiado moroso proceder a experiências com água recolhida em várias captações do aquífero. Deste modo, as quatro amostragens foram efectuadas no poço da “Horta dos Banhos” (Figura 7), captação da Câmara Municipal de Serpa (CMS) que reúne e distribui água para a rede de distribuição de água da cidade de Serpa.
17 Figura 8 - Localização da captação de água subterrânea objecto de estudo - “Horta dos Banhos”
(adaptado de Calçada, 2009)
A selecção da captação da “Horta dos Banhos” para a recolha da água teve também em consideração a sua localização no terreno (Figura 8), tendo em conta o objectivo de se proceder à remediação do aquífero. Considerou-se que a melhor estratégia a adoptar corresponderia à escolha de um ponto de captação que se encontrasse localizado a montante do fluxo do aquífero, de forma a que o escoamento para jusante da água subterrânea tratada diminuísse a concentração dos contaminantes presentes através do processo de diluição.
Em cada amostragem foram recolhidos aproximadamente vinte e cinco litros de água subterrânea, em garrafões de plástico com capacidade de cinco litros. Os garrafões foram previamente limpos com álcool. No local da amostragem procedeu-se novamente à lavagem dos recipientes, por três vezes, com água subterrânea a amostrar. Os garrafões foram cheios até à zona do gargalo.
Idealmente, durante o transporte os garrafões deveriam encontrar-se refrigerados de forma a manter as características biológicas iniciais mas tal não foi possível. Por este motivo, após o seu transporte foram imediatamente colocados no frigorífico.
O espaço que decorreu entre as amostragens e o início de cada ensaio laboratorial correspondeu sensivelmente a vinte e quatro horas, nunca podendo
18 exceder as quarenta e oito horas para minimizar possíveis alterações nas populações de microrganismos.
3.2) Ensaios microbiológicos 3.2.1) Fontes de carbono
Neste estudo de biorremediação por bioestimulação, foram testadas inicialmente cinco fontes de carbono, com o objectivo de avaliar qual delas apresentava maior eficácia na remoção de nitrato da água subterrânea. Pretendeu-se comparar a acção de uma fonte de carbono de referência com a acção de quatro fontes de carbono alternativas.
Para fonte de carbono de referência escolheu-se o etanol, uma vez que era a mais frequentemente usada em estudos similares (Soares, 2000; Gómez et al, 2000; Shrimali e Singh, 2001; Nuhoglu et al, 2002; Jordan et al, 2008). As fontes de carbono alternativas (ácido acético, ácido cítrico, serradura e carvão) foram seleccionadas com base na pesquisa bibliográfica efectuada (Shrimali e Singh, 2001; Shelobolina et al, 2003; Della Rocca et al, 2006; Garcia et al, 2007; Israel et al, 2009), excepto o carvão que consistiu uma inovação, uma vez que não se encontraram estudos realizados com ela. Procurou-se assim averiguar as potencialidades da sua utilização em biorremediação de aquíferos contaminados por nitrato.
As vantagens decorrentes da utilização de fontes de carbono como a serradura e o carvão consistem no seu baixo custo, podendo estas constituir desperdícios de certas indústrias e/ou manufacturas, bem como na facilidade da sua remoção da água subterrânea após o tratamento estar feito, sendo esta remoção muito mais complicada para fontes de carbono que se encontrem totalmente diluídas.
A pesquisa bibliográfica efectuada relativamente às concentrações de etanol habitualmente usadas para este fim mostrou valores díspares entre os diferentes trabalhos consultados. Deste modo, optou-se por usar uma concentração de 0,1 M de etanol (C2H6O) para o primeiro ensaio laboratorial, com a possibilidade de se alterar esta concentração nos ensaios que se seguissem. Para o ácido acético (CH3COOH) adoptou-se a mesma concentração que o etanol, uma vez que possuem a mesma quantidade de carbono.
Como o ácido cítrico (C6H8O7) apresenta três vezes mais carbono do que o etanol e o ácido acético, usou-se uma concentração três vezes inferior (0,030 M).
Uma vez que foi extremamente difícil encontrar referências bibliográficas que fornecessem informações acerca das concentrações a utilizar de serradura e carvão,
19 adoptou-se para ambas a concentração de 1% (10 g/l), pois uma concentração superior delimitaria demasiado a sua homogeneização na água.
3.2.2) Preparação dos meios de cultura
A serradura utilizada nos ensaios laboratoriais foi adquirida em forma de „brickets‟, que foram posteriormente desfeitos manualmente de forma a torná-la mais acessível aos microrganismos presentes na água subterrânea. O carvão também foi partido (com o auxílio de um martelo) de maneira a diminuir a sua granulometria.
Na preparação dos meios de serradura, carvão e etanol (concentrações definidas no ponto 3.2.1), utilizou-se a água subterrânea amostrada, filtrada sob vácuo com um filtro de 0,22 µm.
Para a preparação dos meios de ácido acético e ácido cítrico, estes foram adicionados à água subterrânea amostrada na concentração adoptada (ponto 3.2.1) e posteriormente autoclavados para esterilização.
O meio NB („Nutrient Broth‟ – para um litro: 10 g de triptona, 5 g de extracto de carne e 5 g NaCl) foi preparado de acordo com as instruções do fabricante (20g/l), com água milli-RO (osmose inversa) e esterilizado na autoclave. Este meio foi usado por ser bastante rico do ponto de vista nutricional, tendo a capacidade de suportar o crescimento da maioria dos microrganismos.
3.2.3) Avaliação da capacidade de desnitrificação
Para cada ensaio foram preparados três conjuntos de balões, contendo cada um destes conjuntos 300 ml de meio correspondente a cada fonte de carbono a testar. Os balões continham meio até perto do limite da sua capacidade, de modo a minimizar a difusão de oxigénio e criar condições favoráveis à desnitrificação. Foram depois incubados à temperatura ambiente (≈ 20ºC). Foi ainda preparado um conjunto de balões controlo, contendo apenas a água de captação, sem fonte de carbono (Figura 9).
Ao fim de 1, 2 e 4 semanas foi recolhida a água de um dos balões correspondentes a cada fonte de carbono para se proceder a determinações químicas e à estimativa do número de microrganismos viáveis pelo método do número mais provável (NMP).
20 Figura 9 - Esquema das recolhas dos balões incubados.
Foi realizado um quarto ensaio, apenas com o objectivo de determinar o tempo necessário para que a comunidade microbiana reduzisse o nitrato presente no meio para valores inferiores ao legislado para água de consumo humano (50mg/l), assim não se considerou necessário determinar o NMP, tendo sido apenas realizada a quantificação da concentração de aniões por cromatografia iónica.
O objectivo desta estratégia é simular da melhor maneira possível em laboratório o que poderá acontecer no aquífero e observar os resultados da bioestimulação ao longo do tempo, tendo como substrato diferentes fontes de carbono.
3.2.4) Método do número mais provável
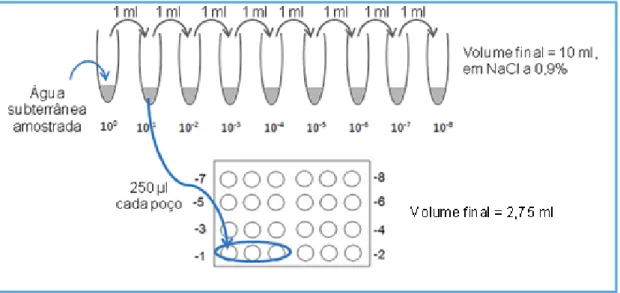
O método do número mais provável (NMP) pode ser utilizado na estimativa do número de microrganismos viáveis presentes em amostras de diversas origens (águas, solos, entre outras) (Mara e Horan, 2003).
Este método é baseado na diluição à extinção de uma população microbiana. Em última análise, a partir de uma dada diluição a amostra não irá conter nenhuma célula com capacidade de se dividir (célula viável). Geralmente, usam-se 3, 5 ou 10 réplicas de cada diluição preparada num factor 1/10 (Mara e Horan, 2003). Existem tabelas com os valores de NMP já calculados para estas condições (Tabelas de McGrady).
Para se poder aplicar este método, é necessário cumprir uma série de pressupostos (Marques-Pinto e Galhardo, 1983):
i. As amostras e as diluições foram adequadamente homogeneizadas; ii. Os microrganismos estão casualmente distribuídos;
iii. A presença de um ou mais organismos num tubo resulta sempre em crescimento;
21 iv. Não actua nenhum inibidor de crescimento dos microrganismos.
O método do NMP foi aplicado com o objectivo de estimar o número de microrganismos presentes na água subterrânea amostrada (estado inicial da população microbiana antes da bioestimulação), assim como monitorizar a sua evolução ao longo do tempo (Figura 10). A evolução temporal foi possível determinando o NMP nos balões inoculados e recolhidos ao fim de 1, 2 e 4 semanas.
As placas foram incubadas uma semana à temperatura ambiente e os resultados foram lidos considerando crescimento positivo os que apresentaram turvação do meio.
Figura 10 - Determinação do NMP de microrganismos presentes nas amostras analisadas
O NMP foi estimado com base no crescimento nas várias diluições, segundo as regras definidas (Marques-Pinto e Galhardo, 1983) e por leitura das tabelas de McGrady.
3.2.5) Conservação de células
Em cada recolha recuperaram-se as células de 100ml de cada um dos meios. Para isso procedeu-se à centrifugação em tubos graduados de 50ml (5 minutos, 3900 rpm, 10 ºC). Após descartar o sobrenadante em excesso, foi adicionado glicerol a 50% ao conteúdo dos tubos e após transferência para tubos „eppendorf‟ a conservação foi feita a -70ºC.
As células foram preservadas com o objectivo de serem posteriormente utilizadas no isolamento dos microrganismos do consórcio que contribuir para a maior redução de nitrato do meio.
22 3.3) Ensaios químicos
3.3.1) Caracterização físico-química da água
A caracterização físico-química da água amostrada na captação da “Horta dos Banhos” foi efectuada através da determinação, em laboratório, dos seguintes parâmetros e técnicas utilizadas:
i. pH – potenciómetria
O pH de uma água representa uma medida da sua acidez ou da sua alcalinidade, sendo traduzida pela concentração de hidrogeniões nela presentes e influenciada pelo carácter tampão que lhe confere. O valor de pH de uma água é influenciado pela sua origem e pela natureza dos terrenos que atravessa. Na maior parte dos casos, os valores de pH da água situam-se entre 6,5 e 8,5. A necessidade da monitorização destes valores na água para consumo humano advém do facto de águas ácidas (pH<7) poderem originar corrosão de tubagens metálicas, que podem levar à presença de teores elevados de certos metais pesados, como o chumbo e o cádmio. No caso oposto, quando as águas são alcalinas (pH>8) podem provocar certos inconvenientes, tais como a diminuição da eficiência da desinfecção devido à alteração das formas de cloro presentes e facilitar a formação de incrustrações, bem como ao desenvolvimento de cheiros e sabores intensos, desaconcelháveis do ponto de vista do consumo (Mendes e Oliveira, 2004).
O Decreto-Lei nº. 306/2007, de 27 de Agosto, define que a gama de valores de pH permitida para águas de consumo humano se situa entre 6,5 e 9.
ii. Condutividade – condutivimetria
A condutividade eléctrica de uma água permite avaliar o seu grau de mineralização, através da relação existente entre o teor de sais minerais dissolvidos na água e a resistência que ela oferece à passagem da corrente eléctrica. A origem desses sais pode ser devida a processos de lixiviação dos solos e rochas por onde a água circula, mas também contaminantes que entrem no aquífero.
Uma mineralização elevada da água pode ser traduzida sob a forma de sabores desagradáveis, de processos de corrosão ou de formação de depósitos.
O Decreto-Lei nº. 306/2007, de 27 de Agosto, estabelece o valor paramétrico de 2500 µS/cm a 20ºC, correspondente à condutividade máxima permitida.
23 Os valores de potencial redox, que é um parâmetro que mede a tendência para a oxi-redução de uma água, mostram se ocorreu maior ou menor dissolução de oxigénio. Em águas naturais, o oxigénio atmosférico é o oxidante preferencial e, por sua vez, a matéria orgânica corresponde ao maior redutor.
Quando é adicionada matéria orgânica a um sistema que tem sido isolado do oxigénio atmosférico, dá-se um decaimento das condições aeróbias, consumindo-se todo o oxigénio livre, após o que o potencial redox diminui e se estabelecem condições anaeróbias favoráveis à redução de nitrato, nitrito e por fim de sulfato (Langmuir, 1997).
iv. Carbono total dissolvido – titulação do CO2 livre e Alcalinidade
O Carbono dissolvido numa água subterrânea pode ter várias origens: dissolução do CO2 (g) da atmosfera, dissolução do CO2 (g) presente nos solos como resultado da actividade biológica, dissolução de carbonatos (por exemplo: CaCO3, MgCO3, CaMg(CO3)2) do solo da zona de infiltração ou das rochas do aquífero e outras origens tais como dissolução de carvões ou CO2(g) de origem profunda.
A dissolução do CO2 (g) na água pode ser descrita por quatro reacções químicas (i – iv) e é regida pela cinética dessas reacções, pelas constantes de equilíbrio termodinâmico e pelo pH da água.
i. CO2 (g) + H2O ↔ CO20 + H2O ii. CO20 + H2O ↔ H2CO3 iii. H2CO3 ↔ H+ + HCO3
-iv. HCO3- ↔ H+ + CO3
2-Figura 11 -Distribuição das maiores espécies de carbono inorgânico dissolvido, em função do pH da água, 25ºC (Freeze e Cherry, 1979).
A pH baixo, H2CO3 é a espécie de carbono dominante presente na água e para valores de pH elevados a forma dominante corresponde a CO3-. Para a habitual gama de pH da água subterrânea (6-9), a espécie predominante de carbono é HCO3- (Figura
24 11), motivo pelo qual esta forma é considerada um dos principais constituintes inorgânicos dissolvidos em água subterrânea (Freeze e Cherry, 1979).
v. Aniões: cloreto, Brometo, nitrato, nitrito, fosfato e sulfato – cromatografia iónica Estas determinações foram efectuadas através de cromatografia iónica, uma vez que esta técnica analítica é simples e rápida, possuindo também a vantagem de requerer um pequeno volume de amostra.
A concentração destes iões em água para consumo humano é controlada através de legislação, nomeadamente pelo Decreto-Lei nº. 306/2007, de 27 de Agosto, onde são descritos os valores limite para diversos parâmetros químicos que possam colocar em risco a sua qualidade.
Tabela 1 - Valores paramétricos estabelecidos para efeitos de controlo da qualidade da água destinada ao consumo humano (DL nº. 306/2007, de 27 de Agosto).
Parâmetro Valor paramétrico Unidade
Cloreto 250 mg/l Cl Nitrato 50 mg/l NO3
Nitrito 0,5 mg/l NO2
Sulfato 250 mg/l SO4
vi. Catiões: cálcio, magnésio, sódio e potássio – absorção atómica de chama vii. Sulfuração total: H2S, HS- e S- – titulação pelo método da ditizona (Arnórsson,
1991).
O sulfureto de hidrogénio é um gás tóxico, inflamável e que apresenta um cheiro característico a ovos podres (Mendes e Oliveira, 2004).
Nas águas subterrâneas podem ser encontradas espécies reduzidas de Enxofre (H2S, HS- e S2-) quando se verifica um défice do oxigénio dissolvido. Tal pode ocorrer por circulação da água em profundidade, por ausência de contacto com a atmosfera de algumas zonas do aquífero, por reacções químicas aquosas que consomem o oxigénio presente na água, ou por contaminação.
A presença de sulfuretos não é directamente perigosa, contudo se forem oxidados podem levar à formação de ácido sulfúrico, o que pode provocar corrosão das canalizações. O principal problema consiste no odor e no sabor da água com esta substância. Por este motivo, este parâmetro na água para consumo humano deve estar compreendido entre 50 e 100 µg/l, para que não seja detectado organolepticamente (Mendes e Oliveira, 2004).
25
4. Resultados e discussão
4.1) Primeiro ensaio
4.1.1) Remoção de nitrato e nitrito e determinação do NMP
A partir da análise da Figura 12, pode observar-se que a atenuação natural do aquífero, descrita pelo controlo, não tem capacidade para reduzir a concentração de nitrato presente no meio até valores permitidos por Lei para águas de consumo humano. Este facto oferece sustentação à técnica utilizada neste trabalho, uma vez que não sendo a atenuação natural do aquífero capaz de remover por si só o nitrato, torna-se necessário recorrer à bioestimulação.
Figura 12 - Concentrações de nitrato presente nas amostras do primeiro ensaio.
De todas as fontes de carbono utilizadas, observa-se que a mais eficiente é a serradura, dado que permite remover na totalidade o nitrato presente na água (Figura 12), situação que nenhuma das restantes fontes de carbono permitiu alcançar. No entanto, esta elevada remoção de nitrato teve como consequência a formação de nitritos (Figura 13) acima do limite estipulado por Lei (0,5 mg/l), tendo atingido na primeira semana de tratamento um valor vinte vezes superior a este (10 mg/l) e 10 vezes maior no final do tratamento (5 mg/l). Uma possível explicação para este facto é a presença nestas amostras de bactérias capazes de reduzir o nitrato a nitrito mas incapazes de reduzirem o último. Por outro lado, as bactérias desnitrificantes podem reduzir inicialmente o nitrato a nitrito, resultando na acumulação deste e só depois seguir a via da desnitrificação (Figura 13).
0 10 20 30 40 50 60 70 0 1 2 3 4 Controlo Carvão Serradura Etanol Valor limite Tempo (semanas) mg/l
26 Figura 13 - Concentrações de nitrito presente nas amostras do primeiro ensaio.
A segunda fonte de carbono mais eficiente foi o etanol (fonte de carbono de referência), tendo permitido uma redução de nitrato de 86% (Figura 12). Tal como na serradura, a elevada redução de nitrato levou à acumulação de nitrito muito acima do valor permitido, tendo ultrapassado este em 14 vezes (7 mg/l) (Figura 13).
O carvão, das três fontes de carbono testadas, foi a única que não foi capaz de suportar a remoção eficiente do nitrato presente no meio (12% de remoção), não tendo sido atingido o valor limite imposto na Lei (Figura 12). Uma vez que a utilização do carvão não permitiu remover a maior parte do nitrato existente no meio, não houve uma formação de nitrito tão elevada. Ainda assim, o valor de nitrito resultante da adição do carvão esteve também acima dos 0,5 mg/l durante a duração do tratamento (Figura 13).
Apesar de a partir da segunda semana de ensaio as diluições usadas na estimativa do NMP de microrganismos não possibilitarem a extinção dos microrganismos e não ser possível determinar com precisão o NMP ao fim de quatro semanas de incubação, é ainda assim possível retirar dos resultados várias informações importantes.
A relação observada entre as fontes de carbono em termos de eficiência de remoção de nitrato manteve-se também ao nível do NMP de microrganismos presentes nas amostras tratadas (Figura 14). A serradura, que demonstrou ser a fonte de carbono com maior eficiência em termos de remoção de nitrato, foi também a fonte de carbono que permitiu suportar o crescimento do maior número de microrganismos. Dada a ausência de oxigénio no meio, a presença de nitrato e a serradura como a única fonte de carbono, estes microrganismos deverão corresponder a desnitrificantes que permitem a remoção de nitrato com utilização de serradura como fonte de carbono. De forma concordante, o NMP para o meio com etanol é inferior ao da
0 2 4 6 8 10 12 0 1 2 3 4 Controlo Carvão Serradura Etanol Valor limite mg/l Tempo (semanas)
27 serradura, tal como a eficiência de remoção de nitrato, sendo o carvão o menos eficiente, quer na remoção, quer em suportar o crescimento de microrganismos (Figura 14).
Figura 14 - Determinação do NMP das amostras do primeiro ensaio.
A tentativa de determinar o número de microrganismos nos meios que continham as fontes de carbono a testar, pelo método do NMP, não forneceu informações, uma vez que o aspecto visual destes meios (muito heterogéneos) impede a leitura dos resultados. Devido a este facto, os resultados apresentados referem-se apenas ao uso do meio NB.
Finalmente, a análise química efectuada aos meios constituídos pelo ácido acético e cítrico permitiu concluir que o uso destas fontes de carbono nas concentrações adoptadas para este trabalho era inadequado. Isto porque o uso do ácido acético e do ácido cítrico baixou drasticamente o pH da água (3,4 e 2,7, respectivamente), inviabilizando a utilização destas fontes de carbono nas condições adoptadas. Os pHs referidos não suportam o crescimento da maior parte das bactérias desnitrificantes e para além disso, a água para consumo humano não pode apresentar pH inferior a 6,5 (Decreto-Lei n.º 306/2007 de 27 de Agosto).
4.1.2) Composição da água
A água amostrada para a realização do primeiro ensaio revelou a seguinte composição (Tabela 2): 0 1 2 3 4 Etanol Serradura Carvão Tempo (semanas) 10 9 6 3 0 log 10 NMP (cé lu la/ml)
28 Tabela 2 – Caracterização da água amostrada no primeiro ensaio.
Catiões (mg/l) Aniões (mg/l) Condutividade (µS/cm) pH Cálcio 73,6 Bicarbonato 318,4 754 7,3 Magnésio 23,2 Cloreto 47,1 Potássio 0,53 Nitrato 58,7 Sódio 31,3 Sulfato 43,5
Nesta amostra não foi detectada a presença de brometo, fosfato, nitrito, amónia e H2S. 4.1.3) Avaliação da variação da determinação de aniões
A avaliação da variação da determinação dos aniões e pH foi feita através do cálculo da média e desvio padrão (Tabela 3). Não foi possível efectuar, com sucesso, repetições para todas as amostras devido a problemas técnicos com o cromatógrafo utilizado nestas determinações. Por este motivo, o cálculo da variação associada às determinações de aniões correspondeu apenas a oito amostras (67%).
Tabela 3 – Valores da média e desvio padrão para as determinações químicas.
Amostra Parâmetro Cloreto Nitrato Nitrito Sulfato
Controlo 1ª Recolha Média 51 52,8 0 44,3 Desvio Padrão 0,8 0,2 0 3,3 2ª Recolha Média 43,3 61,5 0 40,1 Desvio Padrão 11 8,2 0 4,3 3ª Recolha Média 31,8 58,2 0 41,3 Desvio Padrão 0,5 0,2 0 0,1 Carvão 2ª Recolha Média 41,4 54,2 0 32,5 Desvio Padrão 10,5 14,3 0 0,6 3ª Recolha Média 40,7 51,8 2,3 38,6 Desvio Padrão 4,6 8,8 3,3 2,6 Serradura 2ª Recolha Média 36,3 0,8 9,5 36,2 Desvio Padrão 9,4 1,1 0,1 5 3ª Recolha Média 55,5 0,2 5 58,7 Desvio Padrão 23,7 0,2 2,8 23,2 Etanol 2ª Recolha Média 36,5 29,4 8,7 37,1 Desvio Padrão 1,7 0,6 0,4 0,7
Para algumas determinações houve grandes variações de desvio padrão, sobretudo para o cloreto e sulfato, sendo de realçar que estas variações não se encontram tão relacionadas com o nitrato e nitrito (aniões fundamentais para o estudo em causa). Mesmo considerando estas variações para os valores determinados, as conclusões não são inviabilizadas.
29 4.1.4) Carbono total dissolvido
De todas as fontes de carbono utilizadas, observa-se que a serradura é a que permite uma maior libertação de carbono total para o meio, ao longo do tempo (Figura 15). Esta situação deve-se, provavelmente, ao facto de contrariamente às fontes de carbono líquidas, a serradura ficar em contacto com a água e se dissolver gradualmente ao longo do tempo. Por outro lado, distingue-se do carvão (a outra fonte sólida) por ser mais solúvel. Embora isto ocorra em laboratório pelo modo estático do ensaio, in-situ poderá não acontecer uma vez que o contacto entre a serradura e a água se fará com a água em circulação.
O etanol, ao ser bastante solúvel na água, é imediatamente dissolvido no meio. Este facto explica o aumento inicial da concentração de carbono na água e o seu gradual decréscimo a partir da segunda semana de tratamento.
O Carvão correspondeu à fonte de carbono menos eficiente na libertação de carbono para o meio, tendo decrescido linearmente ao longo do tempo (Figura 15). Tal pode ter sucedido, devido à sua velocidade de dissolução ser inferior ao seu consumo.
Figura 15 - Determinação do carbono total para o primeiro ensaio. 4.2) Segundo ensaio
4.3.1) Remoção de nitrato e nitrito e determinação do NMP
O ensaio não forneceu confiança nos resultados, uma vez que a leitura do NMP de microrganismos presentes nas amostras analisadas indicou a ocorrência de contaminações nos ensaios microbiológicos, pelo que se optou por não o considerar para o estudo. 0 150 300 1 2 3 4 Controlo Etanol Carvão Tempo (semanas) mg/l
30 4.3) Terceiro ensaio
4.3.1) Remoção de nitrato e nitrito e determinação do NMP
Através da análise da Figura 16, constata-se que a tendência observada para o nitrato no primeiro ensaio laboratorial se continua a verificar. A atenuação natural do aquífero, demonstrada pelo controlo, continua a não permitir a redução eficaz do nitrato, apesar de se observar uma remoção de 52% no final da primeira semana de incubação. Uma possível explicação é que a fracção desnitrificante da população microbiana consiga, de facto, reduzir o nitrato à custa do carbono presente na água. Com o passar do tempo, este carbono é esgotado e a remoção de nitrato é interrompida. No carvão verifica-se uma tendência semelhante. Em ambos os casos observa-se um aumento posterior dos valores de nitrato (Figura 16), que poderá ser explicado por uma eventual lise das células e libertação de compostos que originem a formação de nitrato.
Figura 16 - Concentração de nitrato presente nas amostras de água subterrânea analisadas no terceiro ensaio laboratorial.
A serradura voltou a permitir a maior eficiência de redução de nitrato (Figura 16), tal como se verificou no primeiro ensaio, tendo sido observada a sua eliminação total. Tal como era expectável houve formação de nitrito em consequência dessa redução (Figura 17), mas no final do ensaio o nitrito foi todo removido. Assim, é possível inferir que uma fracção da população microbiana presente nestas amostras tem a capacidade de efectuar a desnitrificação completa do nitrato, promovendo a sua remoção sem acumulação de nitrato no final do processo.
O etanol, neste ensaio laboratorial, torna a permitir a remoção de uma grande percentagem do nitrato presente inicialmente no meio (74%) (Figura 16), tendo
0 10 20 30 40 50 60 70 0 1 2 3 4 Controlo Carvão Serradura Etanol Valor limite mg/l Tempo (semanas)
31 também como consequência a produção de nitrito, onze vezes (5,5 mg/l) acima do permitido por Lei (Figura 17).
O carvão é novamente a fonte de carbono menos eficiente na remoção de nitrato, tendo removido apenas 8% da sua concentração no final do tratamento (Figura 16). Apesar da baixa remoção de nitrato, deu-se formação de nitrito três vezes (1,5 mg/l) acima do limite (Figura 17).
Figura 17 - Concentração de nitrito presente nas amostras de água subterrânea analisadas no terceiro ensaio laboratorial.
A partir da segunda semana de ensaio, as diluições usadas na estimativa do NMP de microrganismos em NB foram aumentadas para 10-3 até 10-10, dado que as utilizadas no primeiro ensaio (10-1 a 10-8) não permitiram levar à extinção dos microrganismos.
Tal como no primeiro ensaio foi a serradura que permitiu suportar o crescimento do maior número de microrganismos (valor mais elevado de NMP - Figura 18). Considera-se uma vez mais que, dada a ausência de oxigénio no meio, a presença de nitrato e a serradura como única fonte de carbono, estes microrganismos poderão corresponder a desnitrificantes com capacidade de usar a serradura (Figura 18).
O NMP para o meio com etanol é inferior ao da serradura, bem como a eficiência de remoção de nitrato. O carvão é novamente a fonte de carbono menos eficiente na remoção de nitrato, suportando o crescimento do menor número de microrganismos (Figura 18). 0 2 4 6 8 10 0 1 2 3 4 Controlo Carvão Serradura Etanol Valor limite mg/l Tempo (semanas)
32 Figura 18 - Resultados microbiológicos (NMP) relativos às amostras do terceiro ensaio
laboratorial.
4.3.2) Composição da água
A água amostrada para a realização do terceiro ensaio revelou a seguinte composição (Tabela 4):
Tabela 4 - Caracterização da água amostrada no terceiro ensaio.
Catiões (mg/l) Aniões (mg/l) Condutividade (µS/cm) pH
Cálcio 93,8 Bicarbonato 314,8
546 6,7 Magnésio 25,7 Cloreto 30,8
Potássio 0,96 Nitrato 58,7 Sódio 34,8 Sulfato 47
Nesta amostra não foi detectada a presença de brometos, fosfatos, nitrito, amónia e H2S.
4.3.3) Avaliação da variação da determinação de aniões
Pelo mesmo motivo referido anteriormente apenas foram usadas oito amostras (67%) no cálculo das médias e desvio padrão (Tabela 5).
0 1 2 3 4 Controlo Etanol Serradura Carvão 9 6 3 0 log 10 NMP (cé lu la/ml) Tempo (semanas)