UNIVERSIDADE FEDERAL DE OURO PRETO ESCOLA DE NUTRIÇÃO
PROGRAMA DE PÓS-GRADUAÇÃO EM SAÚDE E NUTRIÇÃO
TEOR DE CONTAMINANTES INORGÂNICOS EM CACHAÇAS DO
QUADRILÁTERO FERRÍFERO (MG, BRASIL) ARMAZENADAS EM
COPOS DE PEDRA-SABÃO (ESTEATITO)
KARINE APARECIDA LOUVERA SILVA
KARINE APARECIDA LOUVERA SILVA
TEOR DE CONTAMINANTES INORGÂNICOS EM CACHAÇAS DO
QUADRILÁTERO FERRÍFERO (MG, BRASIL) ARMAZENADAS EM
COPOS DE PEDRA-SABÃO (ESTEATITO)
OURO PRETO, MINAS GERAIS, BRASIL 2015
Dissertação de mestrado apresentada ao Programa de Pós-graduação Stricto Sensu em Saúde e Nutrição da Escola de Nutrição da Universidade Federal de Ouro Preto, como requisito parcial para obtenção do título de Mestre em Saúde e Nutrição.
Área de Concentração: Bioquímica e Fisiopatologia da Nutrição
S586t Silva, Karine Aparecida Louvera.
Teor de contaminantes inorgânicos em cachaça do Quadrilátero Ferrífero (MG, Brasil) armazenadas em copos de pedra-sabão (Esteatito) [manuscrito] / Karine Aparecida Louvera Silva. - 2015.
62f.: il.: color; grafs; tabs; mapas.
Orientadora: Profa. Dra. Késia Diego Quintaes.
Dissertação (Mestrado) - Universidade Federal de Ouro Preto. Escola de Nutrição. Departamento de Nutrição Clínica e Social. Saúde e Nutrição.
1. Cobre. 2. Bebidas alcoólicas. 3. Cachaça. 4. Adsorção. I. Quintaes, Késia Diego. II. Universidade Federal de Ouro Preto. III. Titulo.
CDU: 663:612.393
5 AGRADECIMENTOS
Agradeço a Deus, minha fonte de vida, que, pelo Seu sublime amor, acolheu-me em todos os momentos nos Seus braços, acalentando-me e mostrando-me que, mesmo quando aos meus olhos a minha jornada e os obstáculos desta aparentavam-se difíceis, ajudou-me a buscar incessantemente força e determinação para não perder o meu foco e alcançar o meu objetivo.
À Professora Dra. Késia Diego Quintaes, pela magnífica orientação, amizade, carinho, confiança, dedicação e, sobretudo, pela oportunidade dada à realização deste trabalho.
À Fundação de Amparo à Pesquisa do Estado de Minas Gerais (FAPEMIG – Brasil), pelo apoio financeiro cedido a este projeto.
À Coordenação de Aperfeiçoamento de Pessoal de Nível Superior (CAPES – Brasil), pela concessão da bolsa de mestrado.
Ao Professor Dr. Eduardo Bearzoti, pela excelente contribuição e suporte dados a este trabalho.
A todos os professores da Universidade Federal de Ouro Preto, que me auxiliaram neste projeto, pelo conhecimento transmitido, pela disposição em ajudar-me com as dúvidas e pelo incentivo nesta caminhada.
À Universidade Federal de Ouro Preto e ao Programa de Pós-graduação em Saúde e Nutrição. Em especial à Jaqueline, secretária da Pós-graduação, e aos funcionários da Biblioteca da Escola de Nutrição, pelos inúmeros serviços prestados e pela amabilidade no atendimento.
6 À Isabela Fernandes, amiga da Pós-graduação, por toda amizade, apoio, força, atenção, dedicação e empenho em me ajudar nos pontos-chave deste trabalho. Aos meus pais, meus mestres e meu alicerce, pelo amor incondicional, apoio e proteção, que tanto fizeram para eu conquistar mais esta etapa. Os novos horizontes que conquistei até hoje foram por causa de vocês, que me instigaram a voar mais longe e acreditaram em mim.
Ao meu irmão Bruno e à sua esposa Flávia, pelo exemplo, amizade, paciência, apoio e incentivo, por cederem a casa deles aos finais de semana e torná-los mais alegres, por me fazerem acreditar em mim mesma e por me ensinarem que os grandes méritos da vida dependem basicamente de três características: humildade, ambição e determinação.
Ao meu noivo Samuel, meu porto seguro, pelo companheirismo, cumplicidade e paciência, que me confortou com seu amor em todos os momentos e me apoiou sem hesitar neste objetivo que tanto almejei.
Agradeço a todos os meus familiares e amigos, em especial às minhas avós e aos meus tios Ulisses e Luciana, que, independente da distância, mantiveram-se sempre ao meu lado, orando e torcendo por mim, para que eu conseguisse concluir mais esta etapa da minha jornada.
A todas as minhas amigas e amigos da Pós-graduação, em especial à Izabelle, Tereza, Ricardo, Cícero, Fernanda e Isabela, pela lealdade e cumplicidade, pelo apoio e incentivo e pelos momentos inesquecíveis em Ouro Preto, que jamais sonhei vivenciá-los.
7 “Talvez não tenha conseguido fazer o melhor, mas lutei para que o melhor fosse feito.
8 LISTA DE ILUSTRAÇÕES
Figura 1. Estrutura dos principais minerais geológicos do esteatito...20
Figura 2. Localização do Quadrilátero Ferrífero no Estado de Minas Gerais (QFMG)... 29
Figura 3. Esquema simplificado do delineamento experimental adotado ...31
Figura 4. Modelos de regressão ajustados com a concentração de Pb (mg∙L-1) em função dos ciclos de exposição a copos de pedra-sabão in natura, utilizando médias de oito marcas de cachaça e álcool etílico ...40
Figura 5. Modelos de regressão ajustados com a concentração de Ni (mg∙L-1) em função dos ciclos de exposição a copos de pedra-sabão in natura, em cinco marcas de cachaça comercializadas no Quadrilátero Ferrífero (MG, Brasil)...42
Figura 6. Teor médio inicial (mg∙L-1) e percentual (%) de Ni nas cinco marcas de cachaça estudadas ...44
Figura 7. Modelos de regressão ajustados com a concentração de Cu (mg∙L-1) em função dos ciclos de exposição a copos de pedra-sabão in natura em oito marcas de cachaça comercializadas no Quadrilátero Ferrífero (MG, Brasil)...46
9 LISTA DE TABELAS
Tabela 1. Procedência, teor alcoólico rotulado (%) e concentração média (mg∙L-1) de contaminantes inorgânicos em oito marcas de cachaça e no simulante* à base de álcool .. 35
Tabela 2. Comparação entre modelos de um ensaio em parcelas subdivididas, considerando três estruturas de covariâncias residuais: covariâncias nulas (C0), simetria composta (SC) e autorregressiva de ordem (AR1), utilizando o Critério de Informação de Akaike (AIC), o Critério de Informação Bayesiano (BIC), o logaritmo da verossimilhança (log L) e o Teste da Razão de Verossimilhanças (TRV) ... 38
Tabela 3. Estatísticas F das análises de variância ... 39
Tabela 4. Concentração de Cu e Ni (mg∙L-1) em oito marcas de cachaça comercializadas no Quadrilátero Ferrífero (MG, Brasil) e no simulante* à base de álcool, submetidas a diferentes ciclos de exposição a copos de pedra-sabão in natura (médias de três repetições) ... 41
Tabela 1A. Resultados obtidos para repetitibilidade e reprodutibilidade estudadas na determinação de metais em cachaça ... 60
Tabela 1B. Equações e valor do coeficiente de Pearson para as retas obtidas por regressão linear...61
Tabela 1C. Concentrações dos brancos utilizados para o cálculo do limite de detecção...62
10 LISTA DE SIGLAS
AI Ingestão Adequada
ANOVA Análise de Variância
ANVISA Agência Nacional de Vigilância Sanitária
AR Requerimento Médio
As Arsênio
ATSDR Agencyfor Toxic Substances and Disease Registry
Ca Cálcio
CCD Charge Coupled Device
Cd Cádmio
Co Cobalto
Cr Cromo
Cu Cobre
EFSA European Food Safety Authority
FAPEMIG Fundação de Amparo à Pesquisa do Estado de Minas Gerais
Fe Ferro
IBGE Instituto Brasileiro de Geografia e Estatística
IBRAC Instituto Brasileiro da Cachaça
ICP – OES Inductively Coupled Plasma – Optical Emission Spectrometry
IDA Ingestão Diária Aceitável
IDT Ingestão Diária Tolerável
INMETRO Instituto Nacional de Metrologia, Normalização e Qualidade Industrial
IOM Institute of Medicine
11 JECFA Join Expert Committee on Food Additives
LOAEL Menor Nível de Efeito Adverso Observado
LOD limite de detecção
MAPA Ministério da Agricultura, Pecuária e Abastecimento
Hg Mercúrio
Mg Magnésio
MG Minas Gerais
Mn Manganês
Ni Níquel
OMS Organização Mundial da Saúde
Pb Chumbo
PMTDI Limite Provisório Máximo Tolerável
PRI Referência de Ingestão Popoulacional
PTMI Ingestão Mensal Provisória Tolerável
PTWI Ingestão Semanal Provisória Tolerável
QFMG Quadrilátero Ferrífero de Minas Gerais
RDA Ingestão Dietética Recomendada
RF rádio frequência
Si Silício
UE União Euopeia
12 SUMÁRIO
1 INTRODUÇÃO ... 17
1.1 A cachaça ... 17
1.2 A pedra-sabão ... 19
1.4 Interferência da pedra-sabão no teor de contaminantes inorgânicos ... 26
2 OBJETIVOS ... 27
2.1 Objetivo geral ... 27
2.2 Objetivos específicos ... 27
3 MATERIAIS E MÉTODOS ... 28
3.1 Determinação dos contaminantes inorgânicos ... 30
3.2 Equipamento e condições de operação ... 32
3.3 Avaliação dos contaminantes inorgânicos ... 32
3.4 Qualidade analítica ... 33
3.5 Análise estatística ... 33
4 RESULTADOS E DISCUSSÃO ... 35
4.1 Teores dos elementos inorgânicos presentes nas cachaças e álcool etílico ... 35
4.2 Teores dos elementos no teste de exposição à pedra-sabão ... 37
5 CONCLUSÃO ...50
6 REFERÊNCIAS...51
7 APÊNDICE ... 59
13 RESUMO
14 50,4%) o teor de Cu, tornando adequado seu teor numa das cachaças e incrementar em até 622,2% (107,1 – 622,2%) o teor de Ni, especialmente nas primeiras 24 horas de contato. O modelo de regressão linear simples (R2: 71,19%) indicou um decaimento constante da concentração média de Pb em todas as bebidas, que variou de 18,3% a 54,5% no primeiro e último ciclos, respectivamente. Por outro lado, os teores de As e Cd se mantiveram inalterados durante todo o experimento. O contato da pedra-sabão in natura com soluções alcoólicas pode reduzir a concentração de Cu e Pb, em contrapartida pode elevar a concentração de Ni de forma não ser recomendável que bebidas contendo teores de Ni próximos ao máximo permitido pela legislação sejam expostas à pedra-sabão in natura.
15 ABSTRACT
16 that the contact of alcoholic beverages with raw soapstone was able to reduce up to 50.4% (from 14.3 to 50.4%) of the Cu content, regulating its level in one of these cachaças, and increase up to 622.2% (107.1 to 622.2%) of the Ni content, especially within the first 24 hours of contact. The simple linear regression model (R2: 71.19%) indicated a steady decrease of the average Pb concentration in all beverages, ranging from 18.3% to 54.5% in the first and last cycles, respectively. On the other hand, As and Cd concentrations remained unaltered throughout the experiment. The contact of raw soapstone with alcoholic solutions can reduce the concentration of Cu and Pb; on the other hand, it can increase the concentration of Ni so that it is not recommended to expose beverages containing Ni concentrations close to the maximum level allowed by the law to the raw soapstone.
17 1 INTRODUÇÃO
1.1 A cachaça
A cachaça, bebida legitimamente brasileira, é a terceira bebida alcoólica mais comercializada no mundo e a primeira bebida destilada mais consumida no Brasil (ABRABE, 2010). Estima-se que o Brasil possui capacidade instalada de produção de cachaça de aproximadamente 1,2 bilhão de litros anuais, porém se produz anualmente menos de 800 milhões de litros. Segundo o Instituto Brasileiro de Geografia e Estatística (IBGE, 2006) há aproximadamente 12 mil estabelecimentos produtores de cachaça no país,todaviaassociações regionais estimam existência de quase 15 mil estabelecimentos, sendo que são menos de 2 mil estabelecimentos, com 4.000 marcas devidamente registrados no Ministério de Agricultura (IBRAC, 2008).
É digno de nota que, entre os Estados brasileiros, os que mais se destacam na produção da cachaça são: São Paulo, Pernambuco, Ceará, Minas Gerais e Paraíba, e os que mais consomem cachaça são: São Paulo, Pernambuco, Rio de Janeiro, Ceará, Bahia e Minas Gerais. No que diz respeito ao âmbito internacional, no ano de 2014, a cachaça foi exportada para 66 países, com mais de 60 empresas exportadoras, gerando receita de US$ 18,33 milhões, um aumento superior a 10% em relação a 2013. Também, houve aumento acima de 10% no volume, sendo exportado um total de 10,18 milhões de litros. Os principais países de destino em valor foram: Alemanha, Estados Unidos, França, Portugal, Paraguai e Itália, e os principais países de destino em volume foram: Alemanha, Paraguai, Portugal, Estados Unidos, França e Bolívia (IBRAC, 2014).
18 A cachaça pode receber denominações diferenciadas, a saber: cachaça industrial e cachaça artesanal. A cachaça industrial é obtida em destiladores de coluna, também conhecidos como “destiladores contínuos". Já a cachaça artesanal é produzida em alambiques (MINAS GERAIS, 2007). Nessa perspectiva, as destilarias industriais produzem cerca de 300 mil litros por dia de cachaça, ao passo que nos alambiques geralmente são produzidos cerca de 100 a 1.000 litros por dia da bebida (JERÔNIMO; SILVA, 2005).
Estudos evidenciam que cachaças confeccionadas em alambiques de cobre (Cu) apresentam grande aceitação e são preferidas pelos consumidores. Adversamente a isso, as cachaças obtidas em alambiques fabricados com materiais como o aço inoxidável não têm a mesma predileção (NASCIMENTO et al., 1988; FARIA, 1989; NASCIMENTO et al., 1998). Cabe dizer que o Cu exerce um efeito importante na bebida, reduzindo a acidez e teores de aldeídos e compostos sulfurados, sendo esses fatores usualmente responsáveis pelo sabor e odor desagradáveis da bebida (CARDOSO et al., 2003).
Embora o Cu seja um micronutriente essencial ao homem, exposição prolongada a concentrações acima do requerimento orgânico pode ser nociva ao homem (MOSHA; WANGABO; MHINZI, 1996). Assim, há um limite de ingestão máxima tolerável (UL) de Cu para adultos estimado em 10 mg∙dia-1 (IOM, 2001). Em se tratando de cachaças, a legislação brasileira determina um limite máximo permitido (5 mg∙L-1) (BRASIL, 2005). Cabe ressaltar que o Cu está associado à formação de carbamato de etila em bebidas destiladas, composto potencialmente cancerígeno (ARESTA; BOSCOLO; FRANCO, 2001).
19 Outras bebidas alcoólicas também apresentam problema de contaminação por metais. Pesquisadores reportaram que a bebida grega Mouro pode apresentar deficiência no controle de qualidade em função da variação no teor de Pb (SOUFLEROS; MYGDALIA; NATSKOULIS, 2004). Um tipo de vinho comercializado na Hungria apresentou teores elevados de Cu (20 a 640 µg/L), Pb (6 a 90 µg/L) e cádmio (Cd) (0,05 a 16,5 µg/L), sendo a amplitude dos valores explicada pela diversidade da origem da bebida e também pelo efeito dos aditivos e equipamentos usados na produção (AJTONY et al., 2008).Além dos equipamentos, matéria-prima, substâncias adicionadas intencionalmente, tipo de processo e estocagem também são fatores que interferem no teor de metais das bebidas alcoólicas (IBANEZ et al., 2008).
Segundo a Resolução RDC nº 20, de 22 de março de 2007, da Agência Nacional de Vigilância Sanitária (ANVISA) (BRASIL, 2007), a qual aprovou o regulamento técnico sobre disposições para embalagens, revestimentos, tampas e equipamentos metálicos em contato com alimentos, os equipamentos de Cu sem revestimento não podem entrar em contato com produtos alimentícios devido à fácil transmissão do Cu do material para o produto final. Isso se aplica aos alambiques e utensílios de Cu, os quais necessitam ser revestidos internamente com material permitido pela legislação.
1.2 A pedra-sabão
O esteatito, popularmente conhecido como pedra-sabão, é uma rocha metamórfica de baixa dureza, formado por diversos minerais geológicos, entre os quais se destacam o talco – Mg3Si4O10(OH)2 –, a dolomita – CaMg(CO3)2 –, a actinolita – Ca2(Mg,Fe2+)5Si8O22(OH)2 –, e a clorita magnesiana – (Mg,Al,Fe)12[(Si,Al)8O20](OH)16. Também, são encontrados no esteatito alguns minerais acessórios como: pirita – FeS2 –, arsenopirita – FeAsS –, magnetita – Fe2+Fe
20
Figura 1. Estrutura dos principais minerais geológicos do esteatito
Talco Pirita Magnetita Anfibólios
Calcita Actinolita Titanita Epidoto
21 Durante o metamorfismo do esteatito, elementos podem ser incorporados aos minerais recristalizados, na maioria das vezes na forma de substituições. Pelos seus raios iônicos, valência e distribuição de carga, pequenas quantidades de Ni substituindo Mg na serpentina; Cr na posição do titânio na titanita; Cr substituindo o Fe, e Ni ou Co no lugar do Fe na magnetita; Ni ou Co substituindo o Fe na pirita; e cromo, Ni e titânio em cloritas, podem ser observados. Considerando elementos majoritários, Al pode ser encontrado substituindo tanto Si quanto Mg no talco. Trocas usuais incluem Fe e Mn em dolomitas, substituindo Mg (DEER; HOWIE; ZUSSMAN, 1966; LEINZ; CAMPOS, 1968).
Tem sido evidenciado que a migração majoritária de elementos da pedra-sabão pode seguir a composição da dolomita a qual tem sua solubilização favorecida por fatores como aquecimento e acidez. Este mineral foi considerado como sendo o principal candidato para fonte dos elementos detectados nos ensaios laboratoriais com ácido acético (QUINTAES, 2004; QUINTAES et al., 2004). Esta observação foi ainda reforçada quando associada à característica química da dolomita, a qual é referida como apresentando boa solubilidade em meio ácido, especialmente com elevação de temperatura (LEINZ; CAMPOS, 1968; QUINTAES et al., 2001). Microscopia realizada indicou também que o formato romboédrico exibido pela pedra-sabão após a exposição ao ácido acético é semelhante ao padrão descrito na literatura para a dolomita. Estatisticamente, por correlação de Person, também pode ser constada relação entre os elementos migrantes de forma relacionada à composição da dolomita (QUINTAES, 2006).
Localizado em Minas Gerais (Brasil), a região do Quadrilátero Ferrífero (QFMG) contém importantes e consideráveis jazidas de esteatito (ROESER et al., 1980; ROESER, 1987). As principais localidades com ocorrências de jazidas de esteatito na região do QFMG são: Santa Rita de Ouro Preto, Viriato, Acaiaca, Congonhas do Campo, Cachoeira do Brumado e Ouro Branco (ROESER et al., 1980).
22 pedra-sabão, tanto em laboratório (VILES, 1995; WARSCHEID; BRAAMS, 2000) como nas esculturas e edificações (QUINTAES et al., 2002), e podem ser potencializadas por microrganismos, acelerando o processo de deterioração da rocha (QUINTAES, 2006; NAMDAR; STACEY; SIMPSON, 2009).
As antigas civilizações curavam os recipientes de pedra-sabão com lipídios sob elevada temperatura. Esse procedimento impermeabiliza, reduz a porosidade, minimiza a deterioração e a perda de massa do material, resultando em aumento da resistência e da vida útil dos recipientes (QUINTAES et al., 2006, SANTI et al., 2009). Na atualidade, a cura continua sendo aplicada às panelas de pedra-sabão novas, sendo responsável pela redução no comprometimento da estrutura da panela, decorrente da acidez dos alimentos e do calor do cozimento (QUINTAES, 2006). No entanto, mesmo curada a panela de pedra-sabão ainda libera minerais de valor nutricional e metais de interesse toxicológico, como cálcio (Ca) e ferro (Fe), e o níquel (Ni), respectivamente (QUINTAES, 2000; QUINTAES et al., 2006).
O esteatito tem sido utilizado para esculpir recipientes, panelas e utensílios pequenos desde tempos remotos (QUINTAES, 2000; QUINTAES et al., 2002). Hoje, o uso do esteatito tem sido principalmente no artesanato, como: copos, panelas, jarros, canecas, souvenirs e jogos de tabuleiro, entre outros. Em determinadas cidades do Sudeste brasileiro, especialmente em Ouro Preto (MG), o uso culinário dos utensílios confeccionados em pedra-sabão é uma tradição (QUINTAES, 2000; QUINTAES, 2006).
1.3 Contaminantes inorgânicos
23 Os resultados de estudos referentes à ingestão dietética de metais traço têm sido comparados com a Ingestão Diária Aceitável (IDA) ou Ingestão Diária Tolerável (IDT) e pela Ingestão Semanal Tolerável (TWI), recomendadas pelo “Join Expert Committee on Food Additives” (JECFA), comitê que reúne de peritos da FAO/OMS e pela “European Food Safety Authority” (EFSA), que produz pareceres científicos e orientações sobre a segurança alimentar na União Europeia (UE), respectivamente. A IDA refere-se às substâncias que podem ser ingeridas diariamente sem riscos para a saúde, enquanto a IDT e TWI são usadas para enfatizar a importância de limitar a ingestão diária e semanal, respectivamente, de contaminação dos alimentos por um período sem que acarrete consideráveis riscos à saúde. Entretanto, para os elementos que são capazes de se acumular no organismo, a ingestão tolerável é expressa como Ingestão Semanal Provisória Tolerável (PTWI). O PTWI estabelecido pelo JECFA representa a exposição semanal de alguns contaminantes que podem causar efeitos adversos à saúde dos indivíduos (ZUKOWSKA; BIZIUK, 2008).
O PTWI pode variar conforme a natureza do contaminante. No caso do Cd, a mais recente avaliação do JECFA retirou o valor de PTWI e adotou um valor de Ingestão Mensal Provisória Tolerável (PTMI), sendo este situado em 25 μg∙kg-1 de peso corporal/por mês (WHO, 2013). Já a EFSA, em 2009, realizou uma avaliação sobre o Cd associado a riscos com alimentos e estabeleceu uma TWI de 2,5 µg∙kg-1 (EFSA 2009a). Em 2011, foi reavaliado este parâmetro e concluído que a TWI estabelecida anteriormente está apropriada (EFSA, 2012).
Para o Pb e As, a avaliação do JECFA feita em 2011 concluiu que o valor do PTWI existente não estava adequado e que não era possível estabelecer um valor de PTWI seguro, não havendo para ambos elementos proposição de valor seguro de ingestão diária (WHO, 2011a; WHO, 2011b). No caso do Pb, valores de exposição diária de 0,02 a 0,03 e 0,03 a 0,09 μg∙kg-1 de peso corporal por dia foram estimados para adultos e crianças menores de 4 anos de idade, respectivamente (WHO, 2011b).
24 de processos oncológicos, e também pelos efeitos adversos à saúde humana provocados pelo As (EFSA, 2009b; EFSA, 2010).
Para o Cu, que é micronutriente, em 1982 foi estabelecido pelo JECFA, o Limite Provisório Máximo Tolerável (PMTDI) situado na faixa de 0,05 a 0,5 mg∙kg-1 de peso corporal (WHO, 1982). Como se trata de um nutriente essencial, mais recentemente o Instituto de Medicina (IOM) estabeleceu a Ingestão Dietética Recomendada (RDA) e o Limite Máximo Tolerável (UL) como sendo de 900 µg∙d-1 e 10 mg∙dia-1 para adultos de ambos os sexos, repectivamente (IOM, 2001). Em se tratando da EFSA, foi concluido que o Requerimento Médio (AR) e a Referência de Ingestão Populacional (PRI) para o Cu não podem ser derivados para adultos, bebês e crianças, sendo propostos valores de Ingestão Adequada (AI), para as diferentes fases da vida, pautados no consumo e no balanço de Cu observado. No caso de adultos, os valores de AI para homens e mulheres é de 1,6 e 1,3 mg∙kg-1 de peso corporal por dia, respectivamente (HARVEY et al., 2003; TURNLUND et al., 2005).
Para o Ni, que não é nutriente, o valor de IDT situado em 12 µg∙kg-1 de peso corporal foi proposto pela OMS, sendo este valor estabelecido a partir do Menor Nível de Efeito Adverso Observado (LOAEL) (WHO, 2005). Diferentemente ao valor exposto de IDT pela OMS, a EFSA definiu um nível seguro de IDT de 2,8 µg∙kg-1, sendo este parecer científico baseado nos riscos para a saúde humana de Ni em alimentos, particularmente em vegetais, e também na água potável (EFSA, 2015).
Com relação às vias de exposição, segundo a OMS (WHO, 2001), a água contaminada representa a maior via de exposição do homem ao As. Estudos ambientais têm verificado que a contaminação de águas superficiais e subterrâneas pelo elemento emana principalmente das atividades de mineração, sendo as pilhas de rejeitos as principais fontes de liberação do elemento no meio ambiente (BOELL, 1994; WILLIAMS, 2001; SMEDLEY; ZHANG; LUO, 2003; KO et al., 2003).
25 Os compostos de Cu são usados na agricultura, no tratamento da água para controle de algas (sulfato de cobre penta-hidratado), na preservação de madeira, couro e tecido, e como aditivo em alimentos (AZEVEDO; CHASIN, 2003). Por outro lado, o Cu é um micronutriente essencial, sendo importante para o funcionamento adequado de vários sistemas enzimáticos (MOSHA et al., 1996). Todavia, a exposição humana a concentrações de Cu acima do UL resulta em prejuízos à saúde. Enfermidades oriundas do acúmulo de Cu são a doença de Wilson, doenças neurodegenerativas, como a esclerose, e as doenças de Menkes e de Alzheimer (WAGGONER; BARTNIKAS; GITLIN, 1999). Além do efeito adverso direto à saúde humana, estudo tem indicado que o Cu está associado à formação de carbamato de etila em aguardente, composto potencialmente cancerígeno. O principal precursor do carbamato de etila em bebidas destiladas é o íon cianeto, sendo o Cu um dos fatores que afetam essa formação (ARESTA et al., 2001).
A exposição do homem ao Ni pode ocorrer por inalação de ar, ingestão de água e alimentos ou via dermatológica. A Agency for Toxic Substances and Disease Registry (ATSDR) classifica o Ni e seus compostos como possíveis cancerígenos para o ser humano, quando expostos às concentrações superiores às que o organismo consegue suportar (ATSDR, 2005). Além disso, o Ni é um agente sensibilizante causador de dermatites de contato em pessoas mais sensíveis (SANTUCCI, 1993). No aspecto nutricional, o Ni não é considerado um nutriente (IOM, 2001).
O Pb é um elemento tóxico ao homem. Em crianças, podem ocorrer efeitos nocivos ao sistema nervoso, enquanto nos adultos a exposição excessiva pode ocasionar neuropatia periférica e nefropatia crônica. Ademais, a exposição do homem ao Pb resulta em disfunções nos sistemas gastrointestinal e reprodutivo (GOYER, 1991).
Em função da citada toxicidade destes elementos (As, Cd, Cu, Ni e Pb), existem legislações que estabelecem limites de tolerância em bebidas alcóolicas, como a alemã e a brasileira (BRASIL, 1965, 2005; BGBl, 2002).
26 efetuadas no cultivo de vegetais, na criação de animais, nos tratamentos zoos ou fitossanitários, ou como resultado de contaminação ambiental ou de equipamentos utilizados na elaboração e/ou conservação do alimento.
1.4 Interferência da pedra-sabão no teor de contaminantes inorgânicos
Mesmo sendo usados pelo homem por longa data, os utensílios culinários de pedra-sabão só foram estudados recentemente quanto às suas possíveis implicações nutricionais (QUINTAES, 2006). Os principais minerais que compõem o esteatito contêm elementos de relevância nutricional como Ca, Fe, Magnésio (Mg) e Manganês (Mn). Entretanto, contêm também elementos de importância toxicológica, como o Ni e o Al (QUINTAES, 2000; QUINTAES et al., 2002). Ensaios laboratoriais evidenciaram a possibilidade de transferência de contaminantes inorgânicos da pedra-sabão, como a migração de Pb e Cd a partir de amostras de esteatito em taxas inferiores a 100 μg/L e taxas de As, Cd, Pb e mercúrio (Hg), abaixo de 100 μg/L (CIVO, 1989; POLITÉCNICO DI TORINO, 1994).
A remoção de contaminantes inorgânicos de bebidas alcoólicas visando a atender aos parâmetros legais é de relevância tendo em vista que muitas bebidas podem apresentar contaminantes em níveis indesejáveis, colocando em risco a saúde do consumidor (MADUABUCHI et al., 2006; IBANEZ et al., 2008; PROVENZANO et al., 2010; ALKIS et al., 2014).
27 2 OBJETIVOS
2.1 Objetivo geral
Avaliar o comportamento de contaminantes inorgânicos (As, Cd, Cu, Ni e Pb) presentes em amostras de cachaças brasileiras comerciais quando submetidas ao contato com copos de pedra-sabão in natura e avaliar se os teores encontrados antes e depois de quatro ciclos de 24 horas de exposição ao esteatito atendem aos limites máximos estabelecidos pelas legislações brasileira e alemã (BRASIL, 1965, 2005; BGBl, 2002).
2.2 Objetivos específicos
Determinar os teores dos contaminantes inorgânicos As, Cd, Cu, Ni e Pb presentes em oito amostras de cachaças produzidas no Quadrilátero Ferrífero (MG, Brasil) e no simulante de bebida alcóolica e comparar com as legislações brasileira e alemã vigentes (BRASIL, 1965, 2005; BGBl, 2002).
28 3 MATERIAIS E MÉTODOS
Oito garrafas de distintas marcas de cachaça foram adquiridas no comércio de Belo Horizonte e Ouro Preto (MG, Brasil), carecendo da apresentação no rótulo de seu respectivo teor alcoólico e cidade de produção. Foi considerada como cachaça a aguardente de cana produzida no Brasil, com graduação alcoólica de 38 a 48% (v∙v-1) a 20 ºC, obtida pela destilação do mosto fermentado do caldo de cana-de-açúcar com características sensoriais peculiares, podendo ser adicionada com açúcares até 6 g∙L-1 (BRASIL, 2005).
O critério de seleção das bebidas integrantes do estudo considerou aquelas produzidas na região do QFMG (Figura 1) e registradas no Ministério da Agricultura, Pecuária e Abastecimento (MAPA). Esses critérios foram pautados no fato de que a região do QFMG1 pode apresentar água com maior teor de contaminantes inorgânicos, como o As, sendo essa também uma importante região produtora de cachaças. A seleção de cachaças com registro no MAPA considerou que estas devem possuir certo controle de qualidade na produção das bebidas. Além das cachaças, foi utilizado no experimento um simulante de bebida alcoólica produzido com solução de álcool etílico a 43% (v∙v-1) preparado com álcool etílico (Merck, Darmstadt, Germany) diluído em água deionizada (18,2 MΩ). Esse tratamento adicional foi realizado no intuito de avaliar o efeito da exposição do álcool etílico aos copos de esteatito in natura.
Paralelamente, foram avaliados 27 copos novos de pedra-sabão in natura com capacidade volumétrica aproximada de 20 mL, procedentes do distrito de Cachoeira do Brumado (Mariana, MG, Brasil). Todos os copos foram lavados com água usando esponja polimérica macia nova e solução diluída de detergente comercial, seguidas de enxágue em água corrente e por água destilada. A secagem foi feita em estufa, a 150 oC por dez minutos. Os copos foram então divididos em conjunto de três unidades, totalizando nove conjuntos de copos.
1 O QFMG engloba 35 cidades, a saber: Alvinópolis, Barão de Cocais, Belo Horizonte, Belo Vale,
29
Figura 2. Localização do Quadrilátero Ferrífero no Estado de Minas Gerais (QFMG)
Fonte: Georpark Quadrilatero Ferrífero.
Foram determinados os teores de As, Cd, Cu, Ni e Pb nas marcas de cachaça e na solução de álcool etílico antes e depois do contato com os copos de pedra-sabão. Cada marca de cachaça e da solução de álcool etílico teve parte do seu conteúdo vertido para um conjunto de três copos novos e limpos de pedra-sabão até preencher cerca de 2/3 da capacidade destes (aproximadamente 14 mL). Após o enchimento dos copos, estes foram tampados com vidro de relógio e mantidos em temperatura ambiente sob luz artificial constante.
30 homogeneizado individualmente dentro de béquer de vidro previamente descontaminado. Em seguida, cada amostra foi transferida para um frasco de vidro âmbar, com tampa de fechamento hermético, devidamente etiquetado e mantido sob refrigeração (4 oC) até o momento de manuseio (LÓPEZ-ARTÍGUEZ; CAMEÁN; REPETTO, 1996).
Em cada alíquota coletada nos tempos de contato, foi mensurada a concentração dos elementos As, Cd, Cu, Ni e Pb. Provas em branco foram conduzidas simultaneamente usando duplicata com béqueres de vidro descontaminados, utilizando o mesmo volume de líquido adotado para os copos de pedra-sabão. Os valores finais das concentrações foram obtidos pela dedução dos teores encontrados nas alíquotas subtraídos daqueles obtidos nas provas em branco para cada elemento.
Quatro ciclos de exposição (24 horas cada) foram realizados com coleta de amostras da forma descrita anteriormente. Entre cada ciclo de exposição, os copos foram lavados e secados da forma já mencionada.
3.1 Determinação dos contaminantes inorgânicos
Para a determinação de As, Cd, Cu, Ni e Pb, foram transferidos 5 mL das amostras de cachaça e do simulante para frascos de vidro descontaminados, isentos de contaminantes e microrganismos, e seu volume foi reduzido à metade em bloco digestor a 80 oC. Em seguida, foi adicionado 1,25 mL de ácido nítrico 65% e mantido em aquecimento a 95 oC por duas horas. Após resfriamento da solução, esta foi transferida quantitativamente para balão volumétrico de 25 mL com solução de ácido nítrico 5% (v∙v-1). A solução de ácido nítrico a 5% (v∙v-1) foi preparada a partir de ácido nítrico concentrado 65% (Merck, Darmstadt, Germany) e diluído em água deionizada (18,2 MΩ)(LÓPEZ-ARTÍGUEZ et al., 1996; FERNANDES et al., 2013). O esquema do estudo pode ser observado, a seguir, na Figura 2.
31
Figura 3. Esquema simplificado do delineamento experimental adotado
Belo Horizonte (MG)
Análise química (ICP-OES) Determinação de As, Cd, Cu, Ni e Pb. Amostras de cachaças
Ouro Preto (MG)
Cachoeira do Brumado (Mariana, MG) Cachaças (n=8) e álcool etílico
Copos de pedra-sabão in natura (n=27)
Quatro ciclos de exposição (24 horas cada) Higienização dos copos (simulação do uso natural)
Coleta de amostras
Refrigeração (4 0C)
Comparação com as legislações brasileira e alemã
32 3.2 Equipamento e condições de operação
As análises dos teores dos elementos investigados foram feitas em duplicata por aspiração direta das amostras de cachaças e simulantes mineralizadas com ácido nítrico por espectrometria de emissão. Para tanto, foi utilizado um espectrômetro de emissão com fonte de plasma com acoplamento indutivo (ICP OES) (Vista MPX Varian, Mulgrave, Austrália), com visão axial, equipado com uma fonte de radiofrequência (RF) de 40 MHz, um detector multielementar simultâneo de estado sólido do tipo CCD (Charge Coupled Device), uma bomba peristáltica, uma câmara de nebulização e um nebulizador sea spray. O sistema foi controlado pelo software ICP Expert e utilizou argônio líquido com pureza de 99,996% (Air Liquid, SP, Brasil) como gás de plasma.
As condições experimentais otimizadas de operação do equipamento foram: potência de RF (1000W); vazão do gás de nebulização (0,9 L∙min-1); vazão de argônio principal (15 L∙min-1); vazão de argônio auxiliar (1,5 L∙min-1); correção de fundo (2 pontos); tempo de integração e de leitura (10 s); número de replicatas (3); configuração da tocha (axial) e comprimentos de onda As (188,980 nm), Cd (214,439 nm), Cu (324,754 nm), Pb (220,353 nm) e Ni (221,648 nm).
3.3 Avaliação dos contaminantes inorgânicos
33 3.4 Qualidade analítica
A metodologia analítica foi validada seguindo as normas do Instituto Nacional de Metrologia, Normalização e Qualidade Industrial (INMETRO, 2011), sendo avaliados os parâmetros: linearidade, sensibilidade, seletividade, limite de detecção (LOD), exatidão e precisão. A precisão do método foi determinada pelo coeficiente de variação de sete repetições analíticas. A precisão intermediária foi realizada num intervalo de dois dias com o mesmo analista. A exatidão do método foi verificada por ensaios de recuperação, com adição de solução-padrão dos metais em solução de ácido nítrico 5% nos seguintes níveis de concentração: baixa (0,05 mg∙L-1), média (0,30 mg∙L-1) e alta (0,75 mg∙L-1). Para o Cu, foram usados os mesmos níveis de fortificação dos outros elementos e um nível mais alto (5 mg∙L-1). Todos os parâmetros avaliados estão apresentados na seção Apêndice desta dissertação.
3.5 Análise estatística
O experimento instalado correspondeu a um delineamento inteiramente casualizado (HINKELMANN; KEMPTHORNE, 2008), com nove tratamentos (oito cachaças e um simulante) e três repetições. As repetições, ou unidades experimentais, corresponderam aos copos de pedra sabão in natura, nos quais as cachaças estiveram acondicionadas.
34 tempo, e correspondem ao modelo clássico de parcelas subdivididas no espaço. Essas três estruturas de covariâncias foram comparadas utilizando o Critério de Informação de Akaike (AIC), o Critério de Informação Bayesiano (BIC) e o teste da razão de verossimilhança (este, quando aplicável).
Havendo diferenças significativas (p<0,05) entre as marcas das cachaças, estas eram comparadas utilizando o critério de agrupamento de Scott-Knott (SCOTT; KNOTT, 1974); e havendo diferenças significativas entre os ciclos de avaliação, modelos de regressão eram ajustados. Os dados foram analisados utilizando os softwares R (R CORE TEAM, 2013) e Sisvar (FERREIRA, 2011).
35 4 RESULTADOS E DISCUSSÃO
4.1 Teores dos elementos inorgânicos presentes nas cachaças e álcool etílico
As concentrações dos contaminantes inorgânicos nas oito cachaças e no álcool etílico estão apresentadas na Tabela 1, bem como as localidades de procedência e o respectivo teor alcoólico apresentado no rótulo de cada produto.
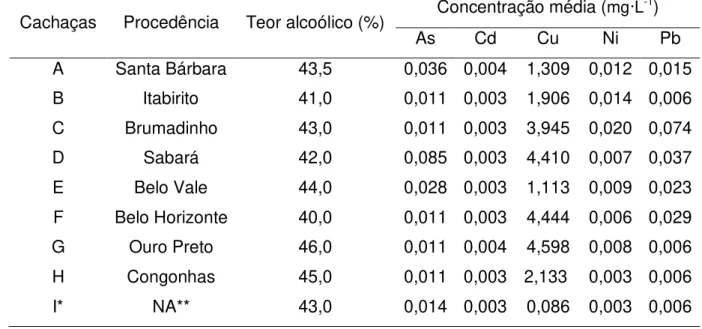
Tabela 1. Procedência, teor alcoólico rotulado (%) e concentração média (mg∙L-1) de contaminantes inorgânicos em oito marcas de cachaça e no simulante* à base de álcool
Cachaças Procedência Teor alcoólico (%) Concentração média (mg∙L
-1)
As Cd Cu Ni Pb
A Santa Bárbara 43,5 0,036 0,004 1,309 0,012 0,015
B Itabirito 41,0 0,011 0,003 1,906 0,014 0,006
C Brumadinho 43,0 0,011 0,003 3,945 0,020 0,074
D Sabará 42,0 0,085 0,003 4,410 0,007 0,037
E Belo Vale 44,0 0,028 0,003 1,113 0,009 0,023
F Belo Horizonte 40,0 0,011 0,003 4,444 0,006 0,029
G Ouro Preto 46,0 0,011 0,004 4,598 0,008 0,006
H Congonhas 45,0 0,011 0,003 2,133 0,003 0,006
I* NA** 43,0 0,014 0,003 0,086 0,003 0,006
** Não se aplica.
O álcool etílico usado como simulante de cachaça pode conter níveis traços de alguns elementos inorgânicos, podendo coincidir com os valores mínimos encontrados nas cachaças.
36 procedência e a composição das distintas bebidas utilizadas no presente estudo. Estudo realizado com cachaças comercializadas em Araraquara (SP, Brasil), verificou que essas bebidas apesentavam teor de As, análogo ao máximo permitido pela legislação brasileira vigente (CALDAS et al., 2009). No que diz respeito ao Cd, teores médios encontrados nas amostras de cachaças investigadas neste estudo (0,003 – 0,004 mg∙L-1) são semelhantes às concentrações médias (0,003 mg∙L-1) desse elemento em amostras de vinhos branco, rosé e vermelho, consumidos na Espanha (MENA et al., 1996). Todavia, os resultados encontrados neste presente estudo se contrapõem aos de outros estudos realizados com cachaças mineiras cujo teor de Cu excedeu o máximo tolerável (5 mg∙L-1) em percentuais que variaram entre 18,8 e 25,0% (FERNANDES et al., 2007; IBANEZ et al., 2008).
37 4.2 Teores dos elementos no teste de exposição à pedra-sabão
A análise estatística da concentração dos contaminantes comparando as marcas de cachaça em diferentes ciclos de exposição aos copos de pedra-sabão não foi efetuada para o Cd, pois as mensurações em todas as marcas de cachaça nos diferentes ciclos de exposição estiveram sempre na faixa de 0,003 mg∙L-1. Dentre as cento e oito mensurações do experimento, apenas 5 diferiram deste valor, correspondentes a uma única repetição de cada uma das seguintes combinações: a da cachaça B com 1 ciclo de exposição (0,004 mg∙L-1), a da cachaça C com 1 ciclo
de exposição (0,005mg∙L-1), a da cachaça G com 1 ciclo de exposição (0,005 mg∙L-1), a da cachaça F com 2 ciclos de exposição (0.004 mg∙L-1).
38
Tabela 2. Comparação entre modelos de um ensaio em parcelas subdivididas, considerando três estruturas de covariâncias residuais: covariâncias nulas (C0), simetria composta (SC) e autorregressiva de ordem 1 (AR1), utilizando o Critério de Informação de Akaike (AIC), o Critério de Informação Bayesiano (BIC), o logaritmo da verossimilhança (log L) e o Teste da Razão de Verossimilhanças (TRV)
Cu
Modelo Graus de Liberdade AIC BIC log L
C0 37 -30,82106 115,0577 21,58947
SC 38 -20,33413 66,17918 48,16706
AR1 38 -20,27903 66,23428 48,13951
Teste Graus de Liberdade TRV P-Valor
SC vs C0 1 = 53,1552 < 0,0001
AR1 vs C0 1 = 53,1001 < 0,0001
As
Modelo Graus de Liberdade AIC BIC log L
C0 37 -134,0257 -49,7891 104,0129
SC 38 -132,1672 -45,6539 104,0836
AR1 38 -132,0461 -45,5328 104,0231
Teste Graus de Liberdade TRV P-Valor
SC vs C0 1 = 0,1415 0,7068
AR1 vs C0 1 = 0,0204 0,8864
Pb
Modelo Graus de Liberdade AIC BIC log L
C0 37 -301,4403 -217,2037 187,7202
SC 38 -299,6041 -213,0908 187,8021
AR1 38 -300,1685 -213,6552 188,0843
Teste Graus de Liberdade TRV P-Valor
SC vs C0 1 = 0,1638 0,6857
AR1 vs C0 1 = 0,7282 0,3935
Ni
Modelo Graus de Liberdade AIC BIC log L
C0 37 -315,0456 -230,809 194,5228
SC 38 -331,2206 -244,7073 203,6103
AR1 38 -327,5024 -240,9890 201,7512
Teste Graus de Liberdade TRV P-Valor
SC vs C0 1 = 18,1749 < 0,0001
AR1 vs C0 1 = 14,4567 0,0001
39
Tabela 3. Estatísticas F das análises de variância
Cu As Pb Ni
Fonte de
Variação GLN
1 F GLD2 P-Valor F GLD P-Valor F GLD P-Valor F GLD P
-Valor
Cachaça
(C) 8
445,84 18 < 0,001 0,64 72 0,744 0,56 72 0,805 4,09 18 0,006
Ciclo (c) 3
486,52 54 < 0,001 0,53 72 0,661 4,05 72 0,010 12,79 54 <
0,001
C × c 24 33,58 54 < 0,001 0,88 72 0,631 0,7 72 0,837 1,48 54 0,118
1 Graus de liberdade do numerador.
2
Graus de liberdade do denominador.
Houve diferença significativa apenas entre os ciclos de exposição, em relação ao teor de Pb (Tabela 3). Tanto as marcas de cachaça como a interação entre marcas e ciclos de exposição apresentaram P-valores elevados (0,805 e 0,837). Isto sugere que um único modelo de regressão poderia descrever a variação da concentração de Pb em função do ciclo de exposição à pedra-sabão. O uso de modelo de regressão linear simples indicou um decaimento constante da concentração média de Pb que variou de 18,3% no primeiro ciclo a 54,5% no último ciclo (Figura 4), representando uma adsorção do contaminante em função do ciclo de exposição.
40
Figura 4. Modelos de regressão ajustados com a concentração de Pb (mg∙L-1) em função dos ciclos de exposição a copos de pedra-sabão in natura, utilizando médias de oito marcas de cachaça e álcool etílico
Quanto ao Ni, houve diferença significativa entre as marcas de cachaça, bem como entre os ciclos de exposição (Tabela 4). Embora a interação entre marcas de cachaça e ciclos de exposição não tenha sido significativa, utilizando um nível de significância de 5%, as marcas de cachaça foram estatisticamente diferentes com um e dois ciclos de exposição. Essas diferenças deixaram de ser significativas a partir do terceiro ciclo de exposição à pedra-sabão.
41
Tabela 4. Concentração de Cu e Ni (mg∙L-1) em oito marcas de cachaça comercializadas no Quadrilátero Ferrífero (MG, Brasil) e no simulante* à base de álcool, submetidas a diferentes ciclos de exposição a copos de pedra-sabão in natura (médias de três repetições)
C
ach
aça
s Concentração de Cu (mg∙L-1) Concentração de Ni (mg∙L-1)
Inicial 1º ciclo 2º ciclo 3º ciclo 4º ciclo Inicial 1º ciclo 2º ciclo 3º ciclo 4º ciclo
A 1,309 0,834 a1 1,074 b 1,093 a 1,126 a 0,012 0,012 a 0,005 a 0,005 a 0,014 a
B 1,906 1,212 b 1,420 c 1,389 b 1,430 b 0,014 0,029 b 0,019 b 0,014 a 0,013 a
C 3,945 2,275 c 3,031 d 3,339 d 3,365 d 0,020 0,009 a 0,011 a 0,006 a 0,007 a
D 4,410 2,826 d 3,571 e 3,985 e 4,062 e 0,007 0,036 b 0,026 b 0,019 a 0,007 a
E 1,113 0,695 a 0,827 a 0,923 a 0,939 a 0,009 0,065 c 0,036 b 0,029 a 0,035 a
F 4,444 2,745 d 3,642 e 3,985 e 4,065 e 0,006 0,025 b 0,031 b 0,011 a 0,011 a
G 4,598 3,942 e 4,218 f 4,503 f 4,597 f 0,008 0,030 b 0,022 b 0,015 a 0,018 a
H 2,133 1,058 b 1,511 c 1,732 c 1,764 c 0,003 0,016 a 0,007 a 0,006 a 0,003 a
I* 0,086 0,112 a 0,086 a 0,086 a 0,086 a 0,003 0,009 a 0,003 a 0,006 a 0,004 a
1. Para um mesmo elemento, médias seguidas de mesma letra são estatisticamente iguais segundo o
método de agrupamento de Scott-Knott a 5% de probabilidade.
O termo constante de tais modelos pode ser interpretado como o valor em torno do qual a concentração de Ni tende a se estabilizar. Como exemplo, para a marca B, esta concentração foi em torno de 0,0076 mg·L-1. Para a marca F houve a necessidade de inclusão de um parâmetro referente ao quadrado desta variável, a fim de evitar variação significativa devido à falta de ajuste para um modelo de regressão. A estimativa do termo constante para esta marca foi negativa, mas não significativamente diferente de zero.
42 contaminante, o que se pode observar pela posição dos pontos correspondentes aos valores inciais (Figura 5).
Figura 5. Modelos de regressão ajustados com a concentração de Ni (mg∙L-1) em função dos ciclos de exposição a copos de pedra-sabão in natura, em cinco marcas de cachaça comercializadas no Quadrilátero Ferrífero (MG, Brasil)
Cachaça B Cachaça D
Cachaça E Cachaça F
N
i m
g
·L
-1 (y
)
N
i m
g
·L
-1 (y
)
N
i m
g
·L
-1 (y
)
N
i m
g
·L
-1 (y
)
Ciclo(x) Ciclo(x)
Ciclo(x) Ciclo(x)
Cachaça G
Ciclo(x)
N
i m
g
·L
-1 (y
43 O Ni, em altas concentrações, é um elemento relativamente tóxico se comparado com os demais metais de transição (CEMPEL; NIKEL, 2006). A presença desse elemento em níveis elevados provoca uma doença de pele conhecida como „„níquel-eczema” (CRISTENSEN et al., 1999). O Ni é utilizado como um metal de liga para a produção de aço inoxidável dos tipos austenítico e martensítico, ambos amplamente empregados no contato com alimentos e bebidas, (DUGO et al., 2004), mas também pode ser o principal veículo de contaminação destes (CEMPEL; NIKEL, 2006).
Visando minimizar o efeito deletério do Ni à saúde humana, existem recomendações referentes à ingestão e ao teor deste elemento em bebidas. Sendo assim, no que tange ao consumo deste metal, a OMS propôs um valor de IDT situado em 12 µg∙kg-1, em contrapartida a UE estabeleceu um nível seguro de IDT de 2,8 µg∙kg-1 de peso corporal (WHO, 2005; EFSA, 2015). Em relação ao teor deste contaminante em bebidas, a legislação brasileira considera como aceitável quantidade inferior de Ni a 3,0 mg∙L-1 e a legislação alemã não estabelece limite espefícico para este elemento, possivelmente mantendo o valor do EFSA como apropriado (BRASIL, 1965; BGBl, 2002).
44
Inicial 1º ciclo 2º ciclo 3º ciclo 4º ciclo
T e o r d e Ni ( % ) Cachaça B 0,014 mg·L-1 0,029 mg·L-1 107,1% 0,019 mg·L-1 35,7% 0,014 mg·L-1
0,0% 0,013 mg·L-1- 7,1%
Inicial 1º ciclo 2º ciclo 3º ciclo 4º ciclo
T e o r d e Ni ( % ) Cachaça D
0,007 mg·L-1
0,036 mg·L-1 414,3% 0,019 mg·L-1 171,4% 0,007 mg·L-1 0,0% 0,026 mg·L-1 271,4%
Inicial 1º ciclo 2º ciclo 3º ciclo 4º ciclo
T e o r d e Ni ( % ) Cachaça E 0,009 mg·L-1 0,065 mg·L-1 622,2% 0,036 mg·L-1
300,0% 0,029 mg·L-1 222,2%
0,035 mg·L-1 288,9%
Inicial 1º ciclo 2º ciclo 3º ciclo 4º ciclo
T e o r d e Ni ( % ) Cachaça F 0,006 mg·L-1 0,025 mg·L-1 316,7% 0,031 mg·L-1 416,7% 0,011 mg·L-1 83,3% 0,011 mg·L-1 83,3%
Inicial 1º ciclo 2º ciclo 3º ciclo 4º ciclo
T e o r d e N i (% ) Cachaça G 0,030 mg·L-1 275,0% 0,022 mg·L-1 175,0% 0,015 mg·L-1 87,5% 0,018 mg·L-1 125,0% 0,008 mg·L-1
Figura 6. Teor médio (mg∙L-1) e percentual (%) de Ni nas cinco marcas de cachaça estudadas
45 marcas de cachaça em cada ciclo de exposição, bem como os ciclos de exposição para cada marca de cachaça. A marca de cachaça G apresentou a maior concentração média de Cu em todos os ciclos de exposição. Para as demais marcas, praticamente não houve alterações de classificação ao longo dos ciclos, à exceção das marcas H e B, que foram classificadas num mesmo grupo com um e dois ciclos de exposição aos copos de esteatito, mas em grupos diferentes com três e quatro ciclos, tendo, então, a marca B uma concentração de Cu estatisticamente inferior à da marca H (Tabela 4).
Conforme se observa pelas curvas de regressão ajustadas (Figura 7), em todas as marcas de cachaça, houve uma tendência aumento da concentração de Cu com o decorrer dos ciclos de exposição ao copo de pedra-sabão.
Para a marca G, houve a necessidade de inclusão de um parâmetro referente ao inverso do quadrado do número de ciclos de exposição. Após essa inclusão, os desvios de regressão não foram significativos, indicando a adequação do modelo. Para as demais marcas, modelos de regressão contendo apenas um parâmetro, correspondendo ao inverso do número de ciclos de exposição, foram satisfatórios. Também aqui em ambos os casos, o termo constante do modelo pode ser interpretado como o valor em torno do qual a concentração de cobre tende a se estabilizar à medida que o número de ciclos de exposição aumenta. Para a marca A, a concentração de Cu tende a se estabilizar em torno de 1,236 mg∙L-1.
46
Figura 7. Modelos de regressão ajustados com a concentração de Cu (mg∙L-1) em função dos ciclos de exposição a copos de pedra-sabão in natura em oito marcas 9de cachaça comercializadas no Quadrilátero Ferrífero (MG, Brasil).
Cachaça A Cachaça B
Cachaça C Cachaça D
C
u
m
g
·L
-1 (y
) C u m g ·L
-1 (y
) C u m g ·L
-1 (y
) C u m g ·L
-1 (y
) Ciclo(x) Ciclo(x) Ciclo(x) Ciclo(x) C u m g ·L
-1 (y
) C u m g ·L
-1 (y
) C u m g ·L
-1 (y
) C u m g ·L
-1 (y
)
Ciclo(x) Ciclo(x)
Ciclo(x) Ciclo(x)
Cachaça E Cachaça F
47 O Cu é um micronutriente essencial para o funcionamento adequado de vários sistemas enzimáticos desde que atenda a RDA e não ultrapasse o UL: 900 µg∙d-1 e 10 mg∙dia-1,repectivamente para adultos de ambos os sexos:, como definido pelo IOM ou PMTDI situado na faixa de 0,05 a 0,5 mg∙kg-1 de peso corporal proposto pela OMS ou AI para homens e mulheres adultas posto de 1,6 e 1,3 mg∙kg-1 de peso corporal por dia, respectivamente, segundo o estabelecido pela EFSA (WHO, 1982; IOM, 2001; HARVEY et al., 2003; TURNLUND et al., 2005).Concomitante a isso, o Cu é um componente da cachaça e advém nessa bebida devido ao seu amplo emprego na indústria de destiladores que são utilizados em sua confecção. Ao longo do processo de destilação e/ou do tempo em que o alambique está parado, há formação de carbonato básico de cobre (azinhavre), o qual pode ser dissolvido pelos vapores alcoólicos ácidos e transmitido à bebida de forma não intencional.
Adicionalmente, estudo evidenciou tendência à correlação entre o teor de carbamato de etila e o material do alambique, sendo o Cu coadjuvante na participação desse composto potencialmente cancerígeno (ARESTA et al., 2001). Desse modo, a limpeza apropriada do alambique e a utilização de destiladores confeccionados em aço inoxidável são recursos disponíveis para obtenção de cachaça com teor de Cu em concordância com o estabelecido pela legislação.
Cabe destacar que, além de copos e jarras de pedra-sabão, na atualidade, o mercado tem mostrado expansão nos artefatos de esteatito que podem entrar em contato com bebidas. Os cubos denominados “whisky stones®” representam uma nova categoria de produtos à base de pedra-sabão. Eles devem ser resfriados e utilizados em lugar do gelo em bebidas, mantendo-as frias e com a mesma concentração original de solutos graças a inércia térmica natural da pedra-sabão. A produção e a comercialização do whisky stones® estão sendo feitas pela empresa norte-americana Teroforma (Tero Design Holdings, LLC.).
48 adsorção dos metais Cu e Pb pelo material pode se justificar por meio da porosidade e/ou clivagem do cristal ou pela abrasão que o esteatito sofre ao ser torneado para confeccionar um utensílio. Em contrapartida, a origem dos elementos migrantes em bebidas alcoólicas pode estar relacionada à solubilização de porções terminais dos cristais minerais da rocha, rompidos mecanicamente durante a fabricação dos copos de pedra-sabão. As bordas fragmentadas de retículos apresentam redução na estabilidade química, especialmente nas partes periféricas, se comparadas às estruturas íntegras dos minerais (LEINZ; CAMPOS, 1968). Assim, a presença de Ni, principalmente nas amostras dos primeiros ciclos de exposição, pode estar relacionada às rupturas físicas dos cristais superficiais de talco com bordas danificadas.
49
Inicial 1º Ciclo 2º ciclo 3º ciclo 4º ciclo
1,212 mg·L-1
- 36,4%
1,420 mg·L-1
- 25,5% 1,389 mg·L
-1
- 27,1%
1,430 mg·L-1
- 25,0% T eo r d e C u (% ) Cachaça B
1,906 mg·L-1
Inicial 1º Ciclo 2º ciclo 3º ciclo 4º ciclo 2,275 mg·L-1
- 42,3%
3,031 mg·L-1
- 23,2%
3,339 mg·L-1
- 15,4%
3,365 mg·L-1
- 14,7% T eo r d e C u (% ) Cachaça C
3,945 mg·L-1
Inicial 1º Ciclo 2º ciclo 3º ciclo 4º ciclo 2,826 mg·L-1
- 35,9%
3,571 mg·L-1
- 19,0%
3,985 mg·L-1
- 9,6%
4,062 mg·L-1
- 7,9% T eo r d e C u (% ) Cachaça D
4,410 mg·L-1
Inicial 1º Ciclo 2º ciclo 3º ciclo 4º ciclo 0,695 mg·L-1
- 37,6%
0,827 mg·L-1
- 25,7%
0,923 mg·L-1
- 17,1%
0,939 mg·L-1
-15,6% T eo r d e C u (% ) Cachaça E
1,113 mg·L-1
Inicial 1º Ciclo 2º ciclo 3º ciclo 4º ciclo 2,745 mg·L-1
- 38,2%
3,642 mg·L-1
- 18,0%
3,985 mg·L-1
- 10,3%
4,065 mg·L-1
- 8,5% T e o r d e C u ( %) Cachaça F
4,444 mg·L-1
Inicial 1º Ciclo 2º ciclo 3º ciclo 4º ciclo 3,942 mg·L-1
- 14,3%
4,218 mg·L-1
- 8,3%
4,503 mg·L-1
- 2,1%
4,597 mg·L-1
- 0,0% T e o r d e C u ( %) Cachaça G
4,598 mg·L-1
Inicial 1º Ciclo 2º ciclo 3º ciclo 4º ciclo 1,058 mg·L-1
- 50,4%
1,511 mg·L-1
- 29,2%
1,732 mg·L-1
- 18,8% 1,764mg·L-1 - 17,3% T e o r d e C u ( %) Cachaça H
2,133 mg·L-1
Inicial 1º ciclo 2º ciclo 3º ciclo 4º ciclo 0,834 mg·L-1
- 36,3%
1,074 mg·L-1
- 18,0%
1,093 mg·L-1
- 16,5%
1,126 mg·L-1
- 14,0% T eo r d e C u (% ) Cachaça A
1,309mg·L-1
Figura 8. Teor médio (mg∙L-1) e percentual (%) de Cu nas oito marcas de cachaça estudadas
50 5 CONCLUSÃO
As cachaças produzidas no Quadrilátero Ferrífero (MG, Brasil) que foram avaliadas neste estudo apresentaram conformidade à legislação brasileira no que tange aos teores de contaminantes As 0,025 (0,011 – 0,085), Cd 0,003 (0,003 – 0,004), Cu 2,982 (1,113 – 4,598), Ni 0,01 (0,003 – 0,020) e Pb 0,024 (0,006 – 0,074) mg∙L-1. Entretanto, isso não ocorreu no que diz respeito à legislação alemã, pois 62,5% das marcas de cachaça avaliadas infringiram o máximo teor de Cu estabelecido (2 mg∙L-1) em 97,2; 120,5; 122,2; 129,9 e 6,6%, respectivamente.
Com relação ao comportamento dos contaminantes inorgânicos, foi evidenciado que o contato de bebidas alcoólicas com a pedra-sabão in natura pode reduzir em até 50,4% (14,3 – 50,4%) o teor de Cu e incrementar em até 622,2% (107,1 – 622,2%) o teor de Ni, especialmente nas primeiras 24 horas de contato. Durante a exposição das cachaças à pedra-sabão, também houve redução linear média no teor de Pb em todas as bebidas, variando de 18,3 a 54,5% no primeiro e último ciclos, respectivamente. Por outro lado, os teores de As e Cd se mantiveram inexpressivos e inalterados durante todo o experimento.
51 6 REFERÊNCIAS
AGENCY FOR TOXIC SUBSTANCES AND DISEASE REGISTRY – ATSDR. Toxicological Profile for Nickel. Public Health Service. Atlanta-US, 2005.
AJTONY, Z.; SZOBOSZLAI, N.; SUSKÓ, E. K.; MEZEI, P.; GYÖRGY, K.; BENCS, L. Direct sample introduction of wines in graphite furnace atomic absorption spectrometry for the simultaneous determination of arsenic, cadmium, copper and lead content. Talanta, v. 76, p. 627-634, 2008.
ALKIS, I. M.; SEVI, O¨z.; ATAKOL, A.; YILMAZ, N.; ANLI, R. E.; ATAKOL, O. Investigation of heavy metal concentrations in some Turkish wines. Journal of Food Composition and Analysis, v. 33, p. 105-110, 2014.
ARESTA, M.; BOSCOLO, M.; FRANCO, D. W. Copper (II) catalysis in cyanide conversion into ethyl carbamate in spirits and relevant reactions. Journal of Agriculture and Food Chemistry, v. 49, p. 2819, 2001.
ASSOCIAÇÃO BRASILEIRA DE BEBIDAS – ABRABE. São Paulo, 2010. Disponível em: <http://www.abrabe.org.br/cachaca.php>. Acesso em: 14 fev. 2014.
AZEVEDO, F. A.; CHASIN, A. A. M. Metais: Gerenciamento da toxicidade. São Paulo: Atheneu, 2003.
BOELL, R. J. Sorption of arsenic by iron oxides and oxyhydroxides in soils. Applied Geochemistry, v. 9, p. 279-286, 1994.
BGBl. Weinverordnung in Der Fassung Der Bekanntmachung. vom 14. Mai 2002 (BGBl. I, S. 1583), zuletzt geändert durch die Verordnung vom 28. März 2003 (BGBl. I, S. 453).
BRASIL. Ministério da Agricultura, Pecuária e Abastecimento. Instrução Normativa nº 13, de 29/06/2005. Padrões de identidade e qualidade para água ardente de cana e para cachaça. Diário Oficial [da] República Federativa do Brasil. Brasília, DF, 30 jun. 2005.
BRASIL. Ministério da Saúde. Agência Nacional de Vigilância Sanitária. Resolução RDC nº 20, de 22 de março de 2007. Aprova o regulamento técnico sobre disposições para embalagens, revestimentos, utensílios, tampas e equipamentos metálicos em contato com alimentos. Diário Oficial [da] República Federativa do Brasil. Brasília, DF, 26 mar. 2007.
BRASIL. Ministério da Saúde. Agência Nacional de Vigilância Sanitária. Decreto nº 55.871, de 26 de março de 1965. Diário Oficial [da] República Federativa do Brasil. Brasília, DF, 9 abr. 1965.
52 Alimentares – definições, classificação e emprego. Diário Oficial [da] República Federativa do Brasil. Brasília, DF, 28 out. 1997.
CALDAS, N. M.; RAPOSO JR, J. L.; GOMES NETO J. A.; BARBOSA JR, F. Effect of modifiers for As, Cu and Pb determinations in sugar-cane spirits by GFAAS. Food Chemistry, v. 113, p. 1266-1271, 2009.
CAMEÁN, A. M.; MORENO, I.; LÓPEZ-ARTÍGUEZ, M.; REPETTO, M. A.; GONZALEZ, A. G. Differentiation of Spanish brandies according to their metal content. Talanta, v. 54, p. 53-59, 2001.
CARDOSO, D. R.; LIMA-NETO, B. S.; FRANCO, D. W.; NASCIMENTO, R. F. Influence of the pot still on the chemical composition of sugar cane spirits: part II. Química Nova, v. 26, p. 165-169, 2003.
CEMPEL, M.; NIKEL, G. Nickel: A review of its sources and environmental toxicology. Polish Journal of Environmental Studies, v. 15, p. 375-382, 2006. CIVO. Internal Technical Report of Contaminants Metals in Soapstone Cookware. Ontvangen, 1989.
CRISTENSEN, J. M.; KRISTIANSEN, J.; NIELSEN, N. H.; MENNE, T.; BYRIALSEN, K. Nickel concentrations in serum and urine of patients with nickel eczema. Toxicology Letters, v. 108, p. 185-189, 1999.
DEER, W. A.; HOWIE, R. A.; ZUSSMAN, J. An Introduction to the rock forming minerals. Essex: Longman Press, 1966.
DUGO, G. L. A.; PERA, L. L. O.; TURCO, V.; DI BELLA, G.; SALVO, F. J. Determination of Ni (II) in beverages without any sample pre-treatment by adsorptive stripping chronopotentiometry (AdSCP). Journal of Agricultural and Food Chemistry, v. 52, p. 1829-1834, 2004.
EUROPEAN FOOD SAFETY AUTHORITY – EFSA. Scientific Opinion Cadmium in food. Scientific Opinion of the Panel on Contaminants in the Food Chain. The EFSA Journal, p. 1-139, 2009a.
EUROPEAN FOOD SAFETY AUTHORITY – EFSA. Scientific Opinion on Arsenic in Food. EFSA Panel on Contaminants in the Food Chain (CONTAM). EFSA Journal, v. 7, p.1351, 2009b.
EUROPEAN FOOD SAFETY AUTHORITY – EFSA. Scientific Opinion on Lead in Food. EFSA Panel on Contaminants in the Food Chain (CONTAM). EFSA Journal, v. 8, p. 1570, 2010.
53 EUROPEAN FOOD SAFETY AUTHORITY – EFSA. Scientific report of EFSA Cadmium dietary exposure in the European population. EFSA Journal, v.10, p. 2551, 2012.
EUROPEAN FOOD SAFETY AUTHORITY – EFSA. Statement on tolerable weekly intake for cadmium. The EFSA Journal, v. 9, p. 1975, 2011.
FARIA, J. B. A influência do cobre na qualidade das aguardentes de cana (Saccharum officinarum L.). 1989. 72p. Tese (Doutorado em Ciência dos Alimentos)- Faculdade de Ciências Farmacêuticas, Universidade de São Paulo, São Paulo, 1989.
FERNANDES, A. P.; SANTOS, M. C.; LEMOS, S. G.; FERREIRA, M. M. C.; NOGUEIRA, A. R. A.; NÓBREGA, J. A. Pattern recognition applied to mineral characterization of Brazilian coffees and sugar-cane spirits. Spectrohimica Acta Part B, v. 60, p. 717-724, 2005.
FERNANDES, I. C.; FAUSTO, M. A.; BEZERRA, O. M. P. A.; QUINTAES, K. D.; MORGANO, M. A.; CERQUEIRA, I. B. Levels of inorganic contaminants in Brazilian cachaças from the Quadrilátero Ferrífero region stored in steatite (soapstone) in natura cups. Química Nova, v. 36, p. 1360-1365, 2013.
FERNANDES, J. W.; CARDOSO, M. G.; VILELA, F. J.; MORAIS, A. R.; SILVA, V. F.; NELSON, D. L. Physicochemical quality of a blend of domestic cachaças from the south of Minas Gerais. Journal of Food Composition and Analysis, v. 20, p. 257-261, 2007.
FERREIRA, D. F. Sisvar: a computer statistic alanalysis system. Ciência e Agrotecnologia, v. 35, p. 1039-1042, 2011.
FLEISCHER, M.; MANDARINO, J. A. Mineral species, Mineralogical Record Inc. Tucson, 1995.
GALLAGHER, C. M.; CHEN, J. J.; KOVACH, J. S. The relationship between body iron store and blood and urine cadmium concentrations in US never-smoking, non-pregnant women aged 20-49 years. Environmental Research, v. 111, p. 702-707, 2011.
GEOPARK – Quadrilátero Ferrífero. Localização. Disponível em: <http://www.geoparkquadrilatero.org/?pg=geopark&id=162>. Acesso em: 21 mar. 2015.
GOYER, R. A. Toxic effects of metals – lead. In: AMDUR, M. O.; DULL, J.; KLAASSEN, C. D. (Ed.). Casareh and Doull’s toxicology – the basic science of poisons. New York: Pergamon Press, 1991.