UNIVERSIDADE
FEDERAL DE
UBERLÂNDIA
PRISCILLA ALVES
RIBEIRO
CARACTERIZAÇÃO
MOLECULAR
DE
ISOLADOS
DE
NEMATOIDES
ENTOMOPATOGÊNICOS
PRISCILLA ALVES
RIBEIRO
CARACTERIZAÇÃO
MOLECULAR
DE
ISOLADOS
DE
NEMATOIDES
ENTOMOPATOGÊNICOS
Trabalho
de
Conclusão
apresentado
ao
curso
de
Agronomia
da Universidade
Federal
de
Uberlândia,
Campus
Monte
Carmelo,
como
requisito
necessário
para
a
obtenção
do
grau
de
Engenheira
Agrônoma.
Orientadora: Prof
a
. Dra. Ana
Carolina
Silva
Siquieroli
PRISCILLA ALVES
RIBEIRO
CARACTERIZAÇÃO
MOLECULAR
DE
ISOLADOS
DE
NEMATOIDES
ENTOMOPATOGÊNICOS
Trabalho
de
Conclusão
apresentado
ao
curso
de
Agronomia
da Universidade
Federal
de
Uberlândia,
Campus
Monte
Carmelo,
como
requisito
necessário
para
a
obtenção
do
grau
de
Engenheira
Agrônoma.
Monte Carmelo,
13
de
dezembro
de
2018
Banca
Examinadora
Prof
a
. Dr
a
. Ana
Carolina
Silva
Siquieroli
Orientadora
Prof. Dr.
Bruno
Sérgio
Vieira
Membro
da
Banca
Prof
a
. Dr
a
.
Vanessa
Andaló
Mendes
de
Carvalho
Membro
da
Banca
RESUMO
1
INTRODUÇÃO...
5
2
OBJETIVO
...
7
3
REFERENCIAL
TEÓRICO
...
7
3.1
Nematoides
entomopatogênicos
no controle
biológico
de
pragas
...
7
3.2
Caracterização
molecular
de
nematoides
entomopatogênicos
... 9
4
MATERIAL
E MÉTODOS... 11
4.1
Multiplicação
dos
isolados
...
11
4.2
Caracterização
molecular
...
11
5
RESULTADOS
E
DISCUSSÃO
... 13
6
CONCLUSÃO...
18
RESUMO
Nematoides
entomopatogênicos (NEPs) estão sendo
cada
vez
mais
estudados
para
o
controle
de
pragas
por possuírem
boa
capacidade
de
adaptação
a
novos ambientes
e capacidade
de
se
disseminar,
em
busca
de
um
hospedeiro. Além
disso,
alguns
produtos
químicos
apresentam
sinergismo
com NEP,
possibilitando
reduções
na quantidade
de
produto
aplicado,
tempo
e
custo de
aplicação.
Estudos
visando caracterizar
a
variabilidade
genética
dos
isolados
de
NEPs
estão
aumentando
à
medida
que
o
controle
biológico
vem
se
firmando como
estratégia
importante
para
a
agricultura. As
variações
moleculares
encontradas nas
linhagens
naturais
dos
NEPs estão permitindo a
manutenção
de
isolados
com
características
cada
vez
mais
adequadas
às condições
específicas
de
cada
aplicação,
além
de
aproveitar a variabilidade
natural
para
a
seleção
de indivíduos
mais
virulentos
e
resistentes. O
objetivo
do
trabalho foi
caracterizar
molecularmente
dois isolados
de
nematoides entomopatogênicos
de potencial
uso
no
controle biológico
de
pragas,
obtidos do
banco de
entomopatógenos
do
Laboratório
de
Entomologia da
Universidade
Federal
de
Uberlândia,
Campus
Monte
Carmelo.
As sequências
de
nucleotídeos
obtidas
dos
isolados foram
comparadas
com
as
sequências de
oito
outras
espécies do gênero
Heterorhabditis
depositadas no
banco
de dados
Genbank,
através
do
programa
BLASTn.
As
identidades das
sequências
foram
calculadas
por
meio
do
GenBank
BLASTn,
e as
distâncias genéticas
e
a
árvore filogenética foram
calculadas
utilizando o
programa
MrBayes v.
3.1.2.
Para
o
alinhamento
múltiplo foi
utilizado
o
programa Clustal
X.
As
sequências
obtidas
foram
de
846
e
832 nucleotídeos
de
comprimento, referentes aos
isolados
MC01 e NEPET
11,
respectivamente.
A
espécie semelhante
mais
próxima
é
H.
amazonensis
(DQ665222.1),
com
95%
e 94% de
máxima
identidade
e
com as
maiores
pontuações máximas, 1373
e
1349
bits,
para
MC01
e
NEPET
11, respectivamente.
A
análise
filogenética
baseada
nas
sequências
da
região
18S
do rDNA
dos
isolados de Heterorhabditis
MC01
e
NEPET
11
mostra a formação de um
grupo
monofilético
com alto
valor
de
PP
(99,94%)
compreendendo
as
espécies H.
amazonensis
(DQ665222.1), e
os
isolados
MC01 e
NEPET
11.
Baseando-se
nas
técnicas
moleculares
empregadas
neste
trabalho, foi
possível
diagnosticar
a
espécie
dos isolados MC01
e
NEPET
11 como
H.
amazonensis.
1
INTRODUÇÃO
O
termo
entomopatogênico
refere-se à capacidade
de causar patogenia em
insetos
via
liberação
de
toxinas
ou outras
substâncias
de
caráter
inseticida
(ALMENARA
et al., 2012).
Associados de modo
específico
e
simbiótico
a
bactérias, em
especial
aos
gêneros
Xernorhabdus
e Photorhabdus
, as
quais são
patogênicas
aos
insetos, alguns
nematoides
tornaram-se
capazes
de
invadir
e
matar
um grande número
de
espécies
de
insetos,
caracterizando
o
hábito
entomopatogênico
(DELL'ACQUA,
2011),
sendo
utilizados
em
larga
escala
pelo
homem na agricultura (GARCIA,
2006).
Os
gêneros
representativos de nematoides entomopatogênicos
associados a
bactérias
são
dois:
Heterorhabditis
(Rhabditida: Heterorhabditidae)
e
Steinernema
(Rhabditida:
Steinernematidae)
(KAMITANI,
2010).
Nematoides entomopatogênicos
(NEPs)
das
famílias
Steinernematidae e
Heterorhabditidae
são
agentes de
controle
biológico
promissores
e particularmente
efetivos,
quando
aplicados
a
insetos que
habitam ou
passam
parte
do
seu
ciclo
de
vida
no
solo
(DELL'ACQUA,
2011).
Vários
aspectos favorecem
o
uso
de
NEPs
no controle
de
pragas,
como
a boa
capacidade de
se
locomoverem
no solo à procura
de hospedeiros para os
quais
são
atraídos
por
diferencial
no
teor
de
CO
2e,
possivelmente, por
componentes
fecais; ou
por
terem uma
extensa
lista de
hospedeiros, o que
ajuda a
sobrevivência
em condições
ambientais
nem
sempre
favoráveis;
ou
ainda,
pela
possibilidade de
multiplicação
e
armazenamento
em
laboratório
antes
de
serem aplicados
(GARCIA,
2006).
O
uso
indiscriminado
de
produtos
fitossanitários
na agricultura moderna
tem
ocasionado
sérios
problemas
ambientais os
quais
afetam diretamente
a
biota e
as
ações
dos
potenciais
inimigos
naturais nas
zonas
de
cultivo.
Com isso,
a
busca
por novos
e menos
impactantes
mecanismos
de
controle
de
pragas,
tornou-se
frequente
(MOLINA
et
al.,
2005).
Os
NEPs
associados
às
bactérias
simbióticas, representam um
sistema
único
de
controle biológico
de
insetos
(MOLINA et
al.,
2005), causando
septicemia e
morte do
hospedeiro
em 24
a
48
horas
(ANDALÓ
et
al.,
2006).
6
ao inseto,
promovendo
a
morte
deste em
até
48
horas. Essas
bactérias
produzem
antibióticos
os quais impedem
o
desenvolvimento
de outras
bactérias,
além
de
pigmentos que conferem ao
inseto
hospedeiro
já
morto,
coloração
característica
na cutícula (
Heterorhabditis:
coloração
marrom-avermelhada com
bioluminescência;
Steinernema
:
coloração
bronzeada
sem
bioluminescência)
(ANDALÓ
et
al.,
2006).
As
células
bacterianas
e
os
tecidos
do hospedeiro
funcionam
como
um
meio
rico
para crescimento
e
reprodução de
Heterorhabditis
. Os
nematóides
podem
desenvolver-se por
duas
ou
três
gerações
dentro do
hospedeiro
e
então
emergem
no solo
em
duas semanas.
No
gênero
Steinernema
,
na
primeira
geração formam-se
machos
e
fêmeas,
enquanto
no
gênero Heterorhabditis
,
formam-se
apenas
fêmeas
hermafroditas.
A
partir
da
segunda
geração,
formam-se machos
e
fêmeas
(GARCIA,
2006).
O potencial do uso dos NEPs no controle biológico é conhecido em diferentes ordens de insetos e em diferentes cultivos agrícolas, a exemplo no controle
das
ninfas
de
cigarrinha
e do bicudoda cana-de-açúcar
(LEITE et al., 2005; GIOMETTI et al., 2011);da
cochonilha
da
raiz
em
cafeeiro
(ALVES et al., 2009); da
lagarta da
espiga
do milho (ANDALÓ
et
al.,
2010);
da
lagarta-elasmo na cultura do milho (MAGNABOSCO,
2018);
dentre
outras
pragas
em
demais
culturas. No
Brasil uma
das
iniciativas
de
sucesso
foi
o
emprego
de
juvenis
infectantes
de
H.
indica
no controle
Spodoptera
frugiperda
(Smith)
(Lepidoptera:
Noctuidae),
uma
praga
da
cultura
do
milho
(GARCIA
et
al., 2008).
Este
processo
de
controle
biológico pode ser uma
ótima
alternativa
ao produtor
no
controle
de
pragas, uma vez que o uso
dos
nematoides
tende
a reduzir os
custos
e o consumo
de
agrotóxicos
no
campo.
Estudos
visando
caracterizar
a variabilidade genética dos isolados de
NEPs
estão
aumentando à
medida que
o
controle biológico
vem
se
firmando
como
estratégia importante
para
a
agricultura. As
variações
moleculares
encontradas nas linhagens naturais
dos
NEPs
estão
permitindo a manutenção
de
isolados
com
características
cada vez mais
adequadas
às
condições específicas
de
cada
aplicação, além
de
aproveitar
a
variabilidade
natural
para
a
seleção
de
indivíduos
mais
virulentos
e
resistentes
(ALMENARA et
al.,
2012).
Até 1980,
estudos
relacionados
à
taxonomia
de
NEPs
eram
confusos
e
as
descrições
de
novas
espécies
eram
duvidosas.
Com a
utilização
de
técnicas
moleculares, na
década
de
1990,
as
identificações
em
nível
de
espécie
começaram a
tornarem-se mais
confiáveis
(DELL'ACQUA
et
al.,
2013).
Ao
contrário
da taxonomia
descritiva,
em
que
são
necessários
diversos
indivíduos
e
estes
devem
estar
bem
preservados, considerando,
também,
o
estádio
de
desenvolvimento, as
técnicas moleculares
conferem
uma
identificação
rápida, precisa e altamente sensível,
não
estando
sujeita
às
variações
fenotípicas,
à
ação
do
ambiente, ao estádio
de
desenvolvimento
do
nematoide
e a
outros
fatores
que
possam
alterar a
morfologia
do
organismo
(DELL'ACQUA
et
al.,
2013).
Segundo
Dolinski
e
Moino
Jr
(2006)
o
gênero
Heterorhabditis
encontra-se
amplamente
distribuído
no
mundo.
No Brasil, amostragens
de
solo e
isolamento
de
NEPs
realizados
em
Rondônia,
Amazonas, Minas Gerais,
Rio
de
Janeiro
e
São
Paulo,
apontam
uma
maioria
de
isolados
do
gênero
Heterorhabditis
.
Andaló
et
al.
(2006) descreveram
H.
amazonensis
a
partir
de
indivíduos
coletados
em
uma
área florestal
da
cidade de
Benjamin
Constant,
no
norte
do
estado
do Amazonas, e
em
2009,
os
autores
identificaram
duas populações
de
nematoides
obtidas em
Lavras, Minas
Gerais, como
sendo
H.
amazonensis.
De
modo
semelhante,
isolados
de
Heterorhabditis
foram
coletados
em
áreas
de
cultivo e
de
fragmentos
de vegetação
nativa
na
região
de
Monte
Carmelo,
em Minas
Gerais,
e
em
regiões
do estado
do
Rio
Grande do
Sul, correspondendo
aos
isolados
MC01
e
NEPET 11,
respectivamente.
2
OBJETIVO
Teve-se
como
objetivo
caracterizar
molecularmente
dois
isolados de
nematoides
entomopatogênicos
de
uso
potencial
no controle biológico
de
pragas,
obtidos do banco de
entomopatógenos
do
Laboratório de
Entomologia
da
Universidade
Federal
de
Uberlândia,
Campus
Monte
Carmelo.
3
REFERENCIAL
TEÓRICO
3.1
Nematoides
entomopatogênicos
no
controle
biológico
de
pragas
8
um
hospedeiro. A
associação
mutualística
entre alguns
nematoides e bactérias
resulta
em
morte
rápida
dos
insetos
parasitados
(FERRAZ,
1998).
Além
disso, alguns
produtos
químicos
apresentam sinergismo
com
o
nematoide,
possibilitando
reduções
na
quantidade de
produto
aplicado,
tempo
e
custo
de aplicação
(KOPPENNHOFER;
KAYA,
1998).
O
uso dos
NEPs nos
sistemas
agrícolas
para
controle
de
insetos
tem
crescido
e
com
variações
no
grau
de
sucesso.
Os
nematoides
no
terceiro estádio
infectivo (JI)
podem viver
livremente, procurando
no
solo um
hospedeiro
suscetível.
Durante
esse
estádio
os
nematoides
não
se
alimentam
nem
se
multiplicam.
Uma vez
penetrando
em
um inseto
hospedeiro,
os
nematoides liberam a
bactéria
simbionte,
a
qual
em
combinação com toxinas produzidas
pelos
nematoides mata
o
hospedeiro dentro
de três
dias.
As
bactérias e tecidos
degradados do
hospedeiro
fornecem
fontes
de
nutrientes
para
o
desenvolvimento
dos
nematoides. Assim,
eles
passam duas gerações
dentro
do
hospedeiro
em
um
período
de
dez
dias, dependendo
da
temperatura
e do
inóculo
inicial
(ADAMS;
NGUYEN,
2002).
Desde
a
década
de
1930 os
NEPs
são
estudados e
explorados
para
o
controle
de
pragas
agrícolas.
No
entanto,
somente
a
partir dos
anos
2000
é
que
os
experimentos
com
NEPs
e
controle
biológico
de
pragas
e
vetores
ganharam
impulso
(ALMENARA et
al.,
2012).
A
primeira
espécie
de
NEPs
encontrada
no
Brasil foi
descrita
por
Pereira em
1937
e,
até os
anos
2000,
esta
era
a
única
espécie
descrita.
Andaló
et al.
(2006) descreveram
Heterorhabditis
amazonensis.
Dolinski
et al.
(2008), identificaram isolados
de
H. baujardi
e
H.
indica
. Todas as espécies isoladas
na
região Amazônica
(ALMENARA,
2011).
O potencial do uso dos NEPs no controle biológico é conhecido em diferentes ordens de insetos e em diferentes cultivos agrícolas, com
melhores resultados em
insetos
que
possuem ao
menos uma
fase
do
seu
desenvolvimento na
superfície do
solo
ou
em
galerias
(MAGNABOSCO,
2018).
No
Brasil,
um
exemplo de
sucesso
do
uso
de
NEPs como agente
de controle biológico,
foi descrito por
Garcia
et al.
(2008)
com
o
emprego
de
juvenis infectantes
de
H.
indica no
controle
de
lagarta
de
S. frugiperda
.
índices de mortalidade
(FEASTER; STEINKRAUS,
1996; ANDALÓ
et
al.,
2010; MERTZ,
2013).
O
uso
de
NEPs
está
intimamente
relacionado
ao
sucesso
de
programas
de
controle,
devido à
adaptação do
nematoide
ao
ambiente e
a
especificidade
ao
inseto
alvo (KAYA;
GAUGLER,
1993;
ANDALÓ
et
al.,
2009),
como
o
que ocorre
com
S.
scapterisci
Nguyen &
Smart que
é
eficaz
no
controle de
paquinhas
e
grilos,
mas
não é
eficaz
no controle
de
outros
insetos-praga
(NGUYEN
e
SMART,
1991).
Assim, o
uso
de
espécies
nativas de
nematoides
pode
ser
eficaz
quando utilizado
sobre
insetos específicos
e que vivem no
solo
ou em
ambientes
críticos
(KOPPENHOFER,
2000;
ARTHURS
et
al.,
2004).
Os
nematoides podem
ser
aplicados
através da pulverização ou
mesmo
por
sistemas
de
irrigação
por
gotejamento
ou
dispersão
(WENNEMANN
et al.,
2003; GARCIA et
al.,
2008), a fim
de
atingir as
pupas
no solo,
visando
à
aplicação
inundativa do
patógeno
na
área;
no
entanto,
após
a
aplicação,
é
possível
verificar
a
permanência
do
nematoide no solo
por
longo
período
de
tempo
(NAVON
et
al.,
2002),
o
que
possibilita
a
mortalidade
da
praga
por
diversos
anos
de
cultivo.
Assim, o
patógeno é
liberado de
forma
inoculativa, o
que
reduz os
custos
com o
controle
da
praga.
3.2
Caracterização
molecular
de
nematoides
entomopatogênicos
Nos últimos
anos
tem
se
intensificado
os
estudos
relacionados
à
identificação
e
caracterização de
NEPs,
porém
sua
a
taxonomia ainda
se
mostra complexa,
de
modo
que
se
torna
cada
vez mais difícil
a identificação
das espécies com
base
na
identificação
morfológica. Isto
se
deve
porque
a
irregularidade
observada
nos
dados
morfológicos das
fêmeas
de
primeira e
segunda
geração
resulta principalmente
de
variações
marcantes
na
qualidade
e
quantidade
de
nutrientes obtidos
dos
insetos
parasitados
(MINAS,
2012).
As
técnicas
de estudo
do
DNA
diferem
substancialmente
quanto
à
complexidade,
quantidade
de
amostra
necessária,
custo,
tipo
de
informação gerada
e
aplicabilidade.
Além
disso, possuem
a
vantagem
de
ser
um
processo
rápido
e altamente
sensível,
não estão sujeitas
a
variações fenotípicas,
à
ação
do
ambiente,
ao
estágio
de
desenvolvimento
do
nematoide
e
a
outros
fatores que
possam alterar
a
morfologia
do
organismo
(DELL'ACQUA,
2011).
10
dos
organismos. Os
genes
rDNA
estão organizados
em
unidades
que possuem
sequências
codificadoras
altamente
conservadas
(18S,
5.8S
e
28S)
e
sequências
intercalares,
que
em
geral
variam
dentro
e
entre
populações (ITS1 e
ITS2,
e ETS)
(ELDER;
TURNER, 1995).
A
técnica
de
amplificação do
DNA ribossômico
(rDNA)
por
reação
da
polimerase
em
cadeia
(PCR)
permite
a
amplificação
de
regiões específicas
do
DNA,
como o espaço
interno
transcrito
(ITS),
a qual tem
sequências
intercalares que
variam
dentro
e
entre
populações,
localizado
entre regiões
altamente
conservadas,
como as
regiões
correspondentes aos genes
18S
e
28S
que
também
são
alvos
de
estudos
e
servem
como
marcadores
para
comparação
entre
espécies
diferentes
(DELL'ACQUA,
2011).
A
utilização
de
marcadores
moleculares tem sido
importante
para
a
investigação
taxonômica de um
NEP,
sendo
a
sequência
do
18S
do
DNA
ribossômico, o
marcador mais
popular
para
identificação de
nematoides
desconhecidos.
Para
as
espécies
dos
gêneros de
Heterorhabditis
e
Steinernema
o marcador
molecular
de
melhor
representação
é a
sequência
de
DNA
da região
do espaço
interno
transcrito
do gene
ribossomal
(ITS rDNA). Esse
marcador
apresenta variações
substanciais
entre
as espécies de Heterorhabditis e
Steinernema.
Outro marcador
que prova
ser
útil para a discriminação
em
nível
da
espécie
são
as
regiões
da
subunidade
28S
ribossomal
(MINAS,
2012).
Perfis de fragmentos de rDNA restritos a região ITS ocorrem para várias espécies de
Heterorhabditis e Steinernema, e podem ser facilmente gerados a partir das sequências ITS
depositadas em bancos de dados públicos, como GenBank. Os padrões de bandas dos nematoides resultam da comparação com aqueles previstos a partir de espécies previamente analisadas. Quando idênticos, sugerem que pertençam à mesma espécie, até que uma análise mais aprofundada indique o contrário (MINAS,
2012).
4
MATERIAL
E
MÉTODOS
4.1
Multiplicação
dos
isolados
Os
dois isolados de
nematoides
entomopatogênicos analisados
(MC01
e
NEPET 11)
foram
obtidos
do
banco
de
entomopatógenos
do
Laboratório
de
Entomologia
da
Universidade
Federal
de Uberlândia,
Campus
Monte Carmelo.
O
isolado
MC01
foi
coletado
em áreas
de
cultivo
e
de
fragmentos
de vegetação
nativa
na
região
de
Monte Carmelo,
Minas
Gerais,
e o
isolado NEPET
11
em
regiões
do
estado
do
Rio
Grande
do
Sul.
Para
obtenção
de
fêmeas
de 1
a geração
foi
realizada
a
multiplicação
a
partir
dos
nematoides
contidos
nas
suspensões
armazenadas
em
câmara climatizada B.O.D.
a
16
±
2°C,
inoculando
1
mL
da suspensão em um
total
de
10
larvas de Tenebrio molitor
L.
(Coleoptera:
Tenebrionidae),
criadas
de
acordo
com
metodologia
de
Potrich et
al. (2007).
Após
inoculação,
as larvas
foram incubadas
em
B.O.D
a
temperatura constante de
26°C por tempo
necessário
para
ocorrer
a
infecção,
morte
das
larvas,
e
estas,
apresentarem
o
sintoma da
infecção. A
avaliação
da
mortalidade das
larvas
e
sintoma
da
infecção
pelo
nematoide
foi
realizada
ao 7°
e
14° dia
de incubação.
Fêmeas
hermafroditas
dos isolados
foram obtidas por
meio
do corte
e
abertura das
larvas
mortas
de
T. molitor
imersas em
solução
de cloreto de sódio
0,8% (NaCl 0,8%),
e
individualizadas.
4.2
Caracterização
molecular
Para
extração do
DNA
dos
isolados
MC01
e NEPET
11
foram maceradas
três
fêmeas
hermafroditas
em
25
pL de
suspensão
que
provoca
lise, composta
por
proteinase
K 800
pg
mL
-1
, P-
mercaptoetanol
1%
(v/v),
NaCl
0,2M
e Tris HCl
pH
8,0 0,2M; diluída
em
25
pL de
12
Em
seguida as
amostras
foram quantificadas
em
espectrofotômetro
NanoDrop®
(ND-1000) (Thermo Scientific,
Asheville,
NC, USA).
As
reações
de
amplificação
foram
realizadas
em um
volume
final
de
25 |iL
contendo
10
mM de
dNTP;
10 mM de
cada
primer
(18S
e
26S);
5
unidades
de
Taq
DNA
polimerase;
tampão
de
PCR
10X; e DNA
genômico
(84,6 ng
do
isolado
MC01
e
64,9 ng
do
isolado
NEPET
11).
O
fragmento
de DNA
correspondente
à
região
ITS foi
amplificado
com os
primers 18S: 5'-TTGATTACGTCCCTGCCCTTT-3' (
forward
)
e
26S: 5'-
TTTCACTCGCCGTTACTAAGG-3' (
reverse).
As
reações
de PCR
foram
realizadas
em
termociclador
Amplitherm Thermal
Cyclers
®nas seguintes
condições: 94
°C
por
7 minutos,
seguido
de
35
ciclos
de
60
segundos
a
94
°C,
60
segundos
a
55 °C
e 60
segundos
a
72
°C,
e
uma etapa
final para
extensão de
10
minutos
a
72 °C.
Os fragmentos
amplificados
foram
separados
em
gel
de
agarose
(1%) em
tampão
TBE
1X
(Tris
base
1M, Ácido Bórico
e EDTA
500 mM), utilizando corante
fluorescente
para
DNA Blue
Green
Loading
Dye
I
(LGC
Biotecnologia) na concentração
1:10.
Para estimar
o
tamanho dos fragmentos
foi
utilizado
marcador
Norgen
Biotek de
100
pares de
base.
Os géis
foram
submetidos à
luz ultravioleta
em um
sistema
de
fotodocumentação
de
géis
L-PIX
(Loccus
Biotecnologia)
para visualização
e análise.
Os
produtos
da
PCR
foram sequenciados
em
equipamento ABI-Prism
3500
Genetic
Analyzer (Applied
Biosystems)
utilizando-se
60
ng
de
DNA-molde
e
4,5
pmol
do
primer 18S
usado
na
amplificação.
O
sequenciamento
foi realizado
pela
empresa
ACTGene
Análises
Moleculares,
Alvorada,
RS.
As sequências
obtidas
foram comparadas
com
as
sequências
de
oito
outras
espécies do gênero
Heterorhabditis
depositadas
no
banco de
dados
Genbank,
National
Center
for
Biotechnology
Information
(NCBI)
disponível
online
no
website
http://www.ncbi.nlm.nih.gov através
do
programa
BLASTn.
Estas
incluem
sequências dos
genes
rRNA
18S,
5.8S
e 28S,
e
das
regiões
ITS1
e
ITS2
(com números
de acesso
correspondentes)
de:
H. amazonensis
(DQ665222.1);
H.
floridensis
(DQ372922.1);
H.
taysearae
(EF043443.1); H.
mexicana
(EF043444.1); H.
sonorensis
(KC633187.1);
H.
baujardi
(MF535519.1);
H.
indica
(MG914076.1);
e
H.
noenieputensis
(KY024497.1).
5
RESULTADOS
E
DISCUSSÃO
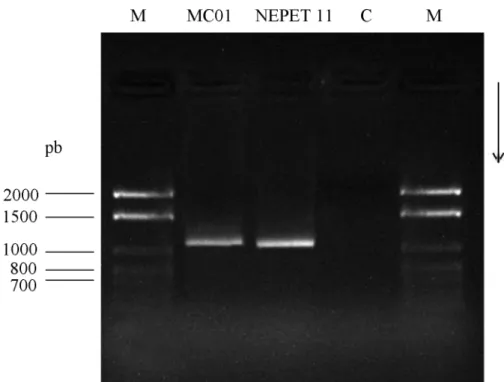
A
amplificação da
região
ITS
do
rDNA
dos
isolados
de
Heterorhabditis
produziu
fragmentos
com
tamanhos de
~1100
pares de
base
(pb)
(Figura 1).
Pelas análises
do
programa
BLASTn,
as
sequências
obtidas
foram
de
846
e
832
nucleotídeos
de comprimento, referentes
aos isolados MC01
e
NEPET
11,
respectivamente.
pb
2000
---1500
---1000
800
700
---M
MC01 NEPET
11
C
M
Figura
1 - Fragmentos
amplificados
por
PCR
da
região
ITS
do
rDNA
18S
de
isolados de
Heterorhabditis.
M
- marcador
molecular
de
100 pb;
MC01
e
NEPET
11
-
isolados
de
Heterorhabditis
;
C
-
controle.
A
seta
indica
a
direção
da
corrida.
14
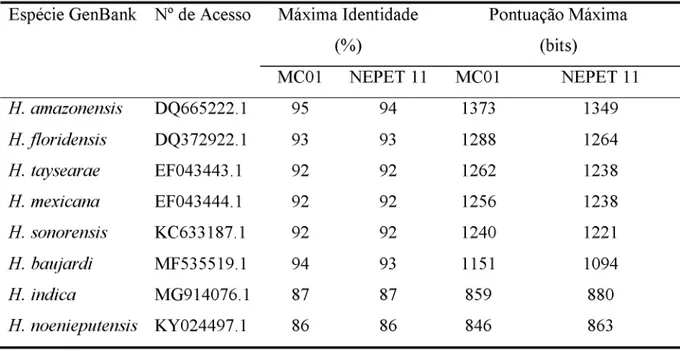
Tabela
1
-
Valores de máxima identidade (%) e pontuação máxima (bits) entre as sequências de nucleotídeos dos isolados de Heterorhabditis estudados e as depositadas no GenBank, pelo programa BLASTn.Espécie GenBank N°
de
Acesso
Máxima Identidade
(%)
Pontuação
Máxima
(bits)
MC01
NEPET
11
MC01
NEPET 11
H.
amazonensis
DQ665222.1
95
94
1373
1349
H.
floridensis
DQ372922.1
93
93
1288
1264
H.
laysearae
EF043443.1
92
92
1262
1238
H.
mexicana
EF043444.1
92
92
1256
1238
H.
sonorensis
KC633187.1
92
92
1240
1221
H.
haujardi
MF535519.1
94
93
1151
1094
H.
indica
MG914076.1
87
87
859
880
H.
noeniepulensis
KY024497.1
86
86
846
863
H. noenieputensis (KY024497.1)
H. indica (MG914076.1)
H. baujardi (MF3355I9.I)
H. taysearae (EF043443.I)
H. sonorensis (KC633I87.I)
H. mexicana (EF043444.1) H. amaxonensis (DQ665222.1)
H. floridcnsis (DQ372922.I)
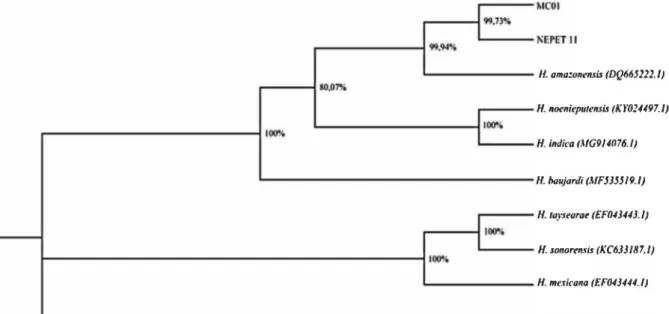
Figura
2 -
Árvore filogenética
bayesiana
de
espécies
de
nematoides
entomopatogênicos
do
gênero
Heterorhabditis
construída
a partir
das sequências
da
região
18S
do
rDNA.
Número
de
acesso
das
espécies
de Heterorhabditis
depositadas
no
Genbank
entre
parênteses. Os
números
fornecidos
nos
nós
de
ramificações são valores
de
probabilidade
posterior
(PP)
dados em
porcentagem
(%).
Na
árvore
filogenética (Figura 2),
observa-se a
formação de
um
grupo monofilético
com
alto
valor de
PP
(99,94%)
compreendendo
as espécies
H.
amazonensis
(DQ665222.1)
e
os
isolados
MC01
e
NEPET
11.
16
Meei DQ665222.1 NEPET
TC GAGAGGASTGGGGAATGCTATATC SGGRC TTTCGGGC TCTGGTATGAT TCGAGAAGAGTGGGGAC TGC TATATCGGGGC TTTCGGGC TC TGGTATGAT TCGAGAAGAGTGGGGAC TGC TAT ATC SGGRC TTTCGGGC TCTGGTATGAT
Meei DQ665222.1 NEPET
GGAAAC CATTTT AATC TTAATGGC TTGAACC GGGCGAAAGTC GTAAC AAG
ggaaaccattttaatcgcaatggcttgaaccgggcaaaagtcgtaacaag GGAAACCATTTTAATCGCAATGGCTTGAACCGGGCAAAAGTCGTAACAAG Meei DQ665222.1 NEPET GTATCTGTARGTGAACCTGCARATGGATCATCGTCGATACCTTATARGAA GTATCTGTAGGTGAACCTGCAGATGGATCATCGTCGATACCTTATAGGTA GTATCTGTAGGTGAACCTGCARATGGATCATCGTCGATACCTTATAKGTA MC 01 DQ665222.1 NEPET
TATGC TTTGATCACSAGATGC TGATAATCATGGAATC AAGC TTGTTCTTG TATGCTTTGATCACGAGATGCTGATAATCATGGAATCAAGCTTGTTCTTG TATGC TTTGATCMC SASATGC TGATAATCATGGAATC AAGC TTGTTC TTG
Meei DQ66S222.1 NEPET
ATTTCCGTCGGTGTCTCACCCCWTCTAACCTCTCGGASAGGTGTCTATTC ATTTCAGTCGGTGTCTCACCCCATCTAAGCTCTCGGAGAGGTGTCTATTC ATTTCMGTCGGTGTC TCACCCC WTC TAASC TC TCGGAGAGGTGTC TATTC
MC01 DQ66S222.1 NEPET TTGATTGGAGCCGATTTGAGTGACGGCAATGATAATTGGGTATGCTCCCC TTGATTGGAGCCGATTTGAGTGACGGCAATGATAATTGGGTATGCTCCCC TTGATTGGAGCCGATTTGAGTGACGGCAATGATAATTGGGTATGCTCCCC Meei DQ665222.1 NEPET
GTAAGGGTAGAGC AT AAGAC TTAATGAGC TGATC TASGTC TGTCGCC TCA GTAAGGGTAGAGC AT AAGAC TT AATGAGC TGATC TAGGTC TGTCGCCTCA GTAAGGGTAGAGCATAARAC TTAATGAGCTGATCTAGGTSTGTCGCC TCA
1 Meei 0Q665222.1 NEPET
C C AAAAACC CATC KATAGTTGGTGGC TAARTGATGAGAC TTTGTCAAAAT CC AAAAACCC ATCGATAGTTGGTGGC TAAGTGATGAGAC T T TGTC AAAAT CCAAAAACCCATCKATAGTTGGTGGCTAARTGATGAGACTTTGTCAAAAT
MC01 DQ665222.1 NEPET
C RC TAATC TGCTATGCGGGGAGCC TTAATGAGTTGTTCGTGTCACTTGAC CAC TAATC TGCTATGCGGGGAGCC TTAATGAGTTGTTCGTGTCACTTGAC C RC TAATC TGC TATGC GGGGAGC C TTAATGAGTTGTTCGTGTCAC TTGAC
MC01 DQ665222.1 NEPET CGACACAACCGCCAGTATCGGTAAATCTCTTCCCAATTAACTTGTTTCTA CGACACAACCGCCAGTATCGGTAAATCTCTTCCCAATTAACTT6TTTCTA CGACACAACCGCCMGTATCGGTAAATCTCTTCCCAATTAACTTGTTTCTA MC01 DQ665222.1 NEPET
GT AAAGGC T ATTGAGTAGTTGTGGAAC ATTAKCC TTAKCGATGGATCGGT GTAAAGGC T ATTGAGTAGTTGTGGAACATTAGCC TTAGCGATGGATCGGT RTAAAGGC TATTGAGTAGTTGTGGAAMATTAKCC TTAKC RATGGATC GGT
MC01 0Q665222.1 NEPET
TGATTCGC GT ATC 6ATGAAAAACGCAGC AAGC TGCGTTATTTGCC ACGAA TGATTCGCGTATC6ATGAAAAACGCAGCAAGCTGCGTTATTTGCCACGAA TGATTCGCGT ATCGATGAAAAACGC AGC AAGCTGCGTTATTTGCCACGAA
MC01 DQ665222.1 NEPET
TTGC AKAC GC TT AGAG TGGTGAAATTTTGAACGC RC AGCGCCGTTGGGTT TTGCAGACGCTTAGAGTGGTGAAATTTTGAACGCACAGCGCCGTTGGGTT TTGC AKAC GCTTAKAGTGGTGAAATTTTGAACGCRC AGC GCCGTTGGGTT
MC01 DQ665222.1 NEPET TTCCCTTCGGCACGTCTGGCTCASGGTTGTTTAATAGACTTCGGTATTGC TTCCCTTCGGCACGTCTGGCTCAGGGTTGTTTAATAGACTTCGGTATTGC TTCCCTTCGGCACGTCTGGCTCAKGGTTGTTTAATAGACTTCKGTATTGC MC01 DQ665222.1 NEPET
TTGGAAGGCGGC RWKAC CGTGAAC C ARAC RGTGATAGTGTCTAAATTGYG TTGGAAGGCGGCAATACCGTGAACCAAACGGTGATAGTGTCTAAATTGTG TTGKAAGGYGGC RAT AC C S TGAAC C AGAC RGTGAT AGTGTC T AAR T TG YG
MC 01 DQ665222.1 NEPET -TGCATGCCCCGTTACAGGGGAGAATGGTGGAYAAATGAASTTCTCTTAA GTGCATGCCCCGTTACAGGGGAGAATGGTGGTTAAATGAACTTCTCTTAA GTGCATGCCCCGTTACATGGGAGAATGGTWGATYAATGAASTTCTCTTAA MC01 DQ665222.1 NEPET AGMYCGA-SAGTAKTACGCTTCACTTATGGATRTGCCATGTATGAA----AGCCGGAGAAGTATTAGGTTTCACTTATGGATATGCCATGTATGAAATAC GACCGGA-SAGTAGTACGYTTCACTTAT...