AVALIAÇÃO SAZONAL DE CAROTENOS E TOCOFERÓIS NA MACROALGA MARINHA Amansia multifida (RHODOPHYTA)
FRANCISCO SANTIAGO LUCAS
Monografia apresentada ao bePartamento de Engenharia de Pesca, do dentro de Ciências Agrárias, da Universidade Federal do Ceará, como parte das exigências para obtenção do título de Engenheiro de Pesca.
L966a Lucas, Francisco Santiago.
Avaliação sazonal de carotenos e tocoferóis na Macroalga marinha Amansia multifida (Rhodophyta) / Francisco Santiago Lucas. – 2009.
24 f. : il. color.
Trabalho de Conclusão de Curso (graduação) – Universidade Federal do Ceará, Centro de Ciências Agrárias, Curso de Agronomia, Fortaleza, 2009.
Orientação: Profa. Dra. Silvana Saker Sampaio.
1. Alga marinha - Avaliação sazonal. 2. Engenharia de Pesca. I. Título.
COMISSÃO EXAMINADORA
c7,.
S a 1.
S
C- 144 pProf
cri à Silvana Saker Sampaio, Ph.D.
Orientadora
)/Y7YA,
,04)1ACit
Bióloga Márcia Barbosa de Sousa, M.Sc. Membro
( Uri
cIev-Eng. de Pesca Kelma Maria dos Santos Pires, M.Sc. Membro
VISTO
Prof. Moisés Almeida de Oliveira, D.Sc. Chefe do Departamento de Engenharia de Pesca
AGRADECIMENTOS
A Deus que, através do seu filho Jesus Cristo, usou e continua usando de misericórdia para com a minha vida. Devo tudo o que sou a Ti, ó Senhor.
À minha família pela disposição e inteiro apoio em todas as minhas decisões, frustrações e alegrias durante toda minha vida.
À professora Silvana Saker Sampaio pela representação de caráter e profissionalismo misturado à incrível amizade e afeto para com todos que com ela se relacionam.
A todos os meus amigos que galgaram o título de Engenheiro de Pesca juntamente comigo (Patrícia, Daniele, Vitor, Wictor, Ênio, Felipe Rocha, Felipe Ximenes, Rafahel, Frederico, Técio, Átila), amizades que levarei e lembrarei para toda a eternidade.
Às queridas monitoras e amigas Márcia Barbosa de Sousa e Kelma Maria dos Santos Pires, que, com muita paciência e dedicação, mostraram-me o caminho a ser percorrido para a realização desse trabalho.
SUMÁRIO
Página
LISTA DE FIGURAS v
LISTA DE TABELAS vi
RESUMO vii
1 INTRODUÇÃO 1
1.1 Carotenóides 1
1.2 Tocoferóis 2
2 MATERIAL E MÉTODOS 4
3 RESULTADOS E DISCUSSÃO 6
4 CONCLUSÃO 13
LISTA DE FIGURAS
Página
Figura 1 - Curva padrão do p-caroteno (Sigma) submetido à
saponificação e partição 6
Figura 2 - Curva padrão do a—tocoferol (Sigma) submetido à
saponificação e partição 7
Figura 3 - Curva padrão do 3—tocoferol (Sigma) submetido à
saponificação e partição 7
Figura 4 - Teores de a— e 3—caroteno nos extratos da alga marinha vermelha Amansia multifida, coletada na Praia do Pacheco,
Caucaia, Ceará em 2008 9
Figura 5 - Teores de a— e 3—tocoferol nos extratos da alga marinha vermelha Amansia multifida, coletada na Praia do Pacheco,
LISTA DE TABELAS
Página
Tabela 1 - Teores de c— e p—caroteno (média ± desvio padrão), nos extratos da alga marinha vermelha Amansia multifida
coletada na Praia do Pacheco, Caucaia, Ceará em 2008, e desidratada em estufa a 40°C por 15 horas 8
Tabela 2 - Teores de a— e 3—tocoferol (média ± desvio padrão), nos extratos da alga marinha vermelha Amansia multifida
coletada na Praia do Pacheco, Caucaia, Ceará em 2008, e desidratada em estufa a 40°C por 15 horas 10
Tabela 3 - Teores de retinol equivalente (RE) e tocoferol equivalente (TE) na alga marinha vermelha Amansia multifida coletada
na Praia do Pacheco, Caucaia, Ceará em 2008, e desidratada em estufa a 40°C por 15 horas 11
Tabela 4 - Porções (g) da alga marinha vermelha Amansia multifida
RESUMO
As algas são fontes importantes de nutrientes como polissacarídeos, fibras dietárias, minerais, proteínas, aminoácidos, ácidos graxos poliinsaturados e vitaminas hidrossolúveis e lipossolúveis. As algas da espécie
AVALIAÇÃO SAZONAL DE CAROTENOS E TOCOFERÓIS NA MACROALGA MARINHA Amansia multifida (RHODOPHYTA)
FRANCISCO SANTIAGO LUCAS
1 INTRODUÇÃO
O uso de macroalgas marinhas na alimentação humana data de épocas remotas no Japão e China, nos Séculos IV e VI, respectivamente, sendo eles dois e a República da Coréia, atualmente, os maiores consumidores (OLIVEIRA, 1997; McHUGH, 2003). Nos países do Ocidente elas são usadas principalmente como fonte de ficocolóides, como carragenanas e ágar. A França regulamentou o uso de algumas macroalgas para o consumo humano, dentre as quais se encontram Porphyra umbilicalis, Palmaria palmata, Gracilaria verrucosa e Chondrus crispus, todas pertencentes à divisão
Rhodophyta (MABEAU; FLEURENCE, 1993).
As macroalgas vermelhas, também chamadas de rodofíceas ou rodofitas, pertencem à divisão taxonômica Rhodophyta e constituem um grupo diversificado de organismos pertencentes ao Reino Plantae. Além de proporcionar a estabilidade dos ecossistemas naturais, elas apresentam uma variedade de compostos benéficos para o uso humano, sendo utilizados principalmente nas áreas de nutrição, indústrias de alimentos e biotecnologia (McHUGH, 2003; VIDOTTI-ROLLEMBERG, 2004). Dentre esses compostos podem ser encontrados os carotenóides com atividade de vitamina A e as vitaminas lipossolúveis, com destaque para a vitamina E.
1.1 Carotenóides
ao calor, luz e presença de oxigênio (BUNEA et al., 2008). Eles diferenciam-se em duas classes. Quando possuem somente átomos de carbono e hidrogênio em sua molécula são classificados como carotenos, como por exemplo, {3—caroteno e licopeno, e quando há presença de pelo menos um átomo de oxigênio na molécula são denominados xantofilas ou oxicarotenos, como por exemplo luteína e zeaxantina (STAHL; SIES, 2005). O f3-caroteno é a forma mais abundante na natureza e apresenta maior atividade de vitamina A (AMBRÓSIO et al., 2006).
Mais de setecentos e cinquenta carotenóides já foram identificados, mas dentre eles aproximadamente cinquenta ou sessenta são precursores de vitamina A (HORNERO-MÉNDEZ; BRITTON, 2002). Eles são produzidos por vegetais e micro-organismos para auxiliar na captação de energia luminosa. Os animais, por sua vez, são incapazes de sintetizá-los e, por essa razão, eles aportam nos organismos animais através de suas dietas (TAPIERO et al., 2004; CHEN; BERGMAN, 2005), sendo transformados em vitamina A, apresentando-se nas formas de retinol, ácido retinóico, retina) e retinil (RODRIGUEZ-AMAYA et al., 2008).
Os carotenóides demonstraram eficácia na prevenção e tratamento de doenças como o câncer, deficiências no sistema imunológico e catarata, agindo ainda como antioxidante (MELÉNDEZ-MARTÍNEZ et al., 2004).
Nas rodófitas os carotenóides mais comumente encontrados são a— e
p—caroteno, bem como seus derivados hidroxilados, luteina e zeaxantina, respectivamente (LIAAEN-JENSEN, 1977; ROWAN, 1989).
1.2 Tocoferóis
concentração de a—tocoferol em termos de atividade de vitamina E (BRIGELIUS-FLOHÉ; TRABER, 1999; BRAMLEY et al., 2000; DELLAPENNA; 2005). Os tocoferóis apresentam-se termoestáveis em ambientes livres de oxigênio, ocorrendo perda de estabilidade, ainda que lenta, na presença de luz, calor somado ao oxigênio e íons metálicos (BURNS et al., 2003; GÓMEZ-CORONADO et al., 2004).
A vitamina E desempenha ainda funções variadas no organismo animal como proteção contra doenças cardiovasculares, Alzheimer, Parkinson e vários tipos de câncer, agindo também na modulação da sinalização celular e na transcrição de genes (MEYDANI, 2000; BRIGÉLIUS-FLOHÉ et al., 2002; BIANCHINNI; PENTEADO, 2003; MUNTEANU et al., 2004). Essa vitamina pode ser encontrada em óleos vegetais, vegetais folhosos verdes (GÓMEZ-CORONADO et al., 2004; RIGOTTI, 2007), e também em algas marinhas (PIRES, 2007; SANTIAGO, 2008).
Existem alguns trabalhos desenvolvidos no Laboratório de Bioquímica Marinha da Universidade Federal do Ceará que quantificaram carotenóides provitamina A e tocoferóis em macroalgas marinhas (SOUSA, 2005; PIRES, 2007; NEPOMUCENO, 2008; SANTIAGO, 2008).
O objetivo do presente trabalho foi avaliar a variação dos teores de carotenóides provitamina A (a— e 0—caroteno) e de vitamina E (a— e
3—tocoferol) na macroalga marinha Amansia multifida pertencente a divisão
2 MATERIAL E MÉTODOS
As amostras da macroalga marinha vermelha Amansia multifida foram
coletadas bimensalmente em fevereiro, abril, junho, agosto, outubro e dezembro de 2008, durante as marés baixas na Praia do Pacheco, Caucaia-Ceará.
O material foi levado ao Laboratório de Bioquímica Marinha, do Departamento de Engenharia de Pesca da Universidade Federal do Ceará, lavado com água corrente para retirada de sal e remoção de epífitas, colocado em sacos plásticos identificados com o mês da coleta e armazenado a -18°C.
Para a secagem, as algas foram colocadas em estufa, à temperatura de 40°C durante 15 h.
As algas desidratadas foram trituradas em moedor doméstico (Candence, MDR 301). O material triturado foi usado na preparação dos extratos metanólicos, onde foram quantificados a— e í3—caroteno e a— e 3—tocoferol.
Três porções de 0,5 g de alga triturada foram colocadas em metanol-água (90:10, v/v), contendo 5% de hidróxido de potássio, na proporção 1:20 (p/v). Os extratos foram saponificados em banho-maria por 30 min a 70°C. Em seguida, foram resfriados à temperatura ambiente e centrifugados a 2.000 x g
por 5 min. Cinco mililitros dos extratos saponificados foram submetidos à partição em 2,5 mL de n-hexano e 1,5 mL de água mili-Q em plataforma misturadora por 10 min.
Porções de 1 mL das fases hexânicas foram transferidas para tubos de ensaio e evaporadas sob corrente de ar. Os resíduos foram suspensos em 1 mL de metanol no momento da análise cromatográfica e 100 1,LL foram injetados manualmente.
Diariamente uma solução padrão de f3—caroteno tipo 195% (C-9750, Sigma) em tetrahidrofurano (1 mg mL-1) foi preparada e diluída em metanol para 10 µg mL-1 (solução de trabalho), de modo que 0,5 µg de 3—caroteno fosse injetado na coluna. A concentração dessa solução de trabalho foi determinada a partir de sua absorbância em 450 nm, sendo a capacidade de absorção de luz igual a 0,2592 µg-1 mL-1 (SPECIFICATIONS AND CRITERIA FOR BIOCHEMICAL COMPOUNDS, 1972). A concentração de a—caroteno foi obtida a partir da concentração de f3—caroteno, pois segundo SAKER-SAMPAIO (1997), as áreas dos picos dos padrões correspondentes a 10 µg mL-1 de a—caroteno e J3—caroteno não apresentam diferença estatisticamente significativa.
Da mesma forma, soluções-padrão (1 mg ml..-1) de a—tocoferol (T-3251, Sigma) e 8—tocoferol (T-2028, Sigma) foram preparadas em tetrahidrofurano, e diluídas em metanol para 100 µg mL-1 (solução de trabalho), de modo que 5 µg de a— e de 6—tocoferol fossem injetados na coluna.
Os padrões foram processados, ou seja, submetidos à saponificação e à partição, separadamente e em combinação com 0,5 g de alga, para assegurar a detecção dos compostos de interesse onde eles foram adicionados intencionalmente.
A seguinte fórmula foi utilizada para quantificar tanto a— e 3—caroteno quanto a— e 8—tocoferol presentes nas amostras de alga desidratada e os resultados foram expressos em µg g-1 peso seco.
1 área amostra 1 g
;Ag g = x µg padrão na coluna x
área padrão g alga
70
60
y = 0,116 + 95,563 x (r = 0,9983 n = 6)
E 50
E 40
o
o
'a 30
o Q5 20
10
o
00 0.1 0.2 0.3 0.4 0.5 0.6 0.7 0.8
µg de p-caroteno na coluna
6
3 RESULTADOS E DISCUSSÃO
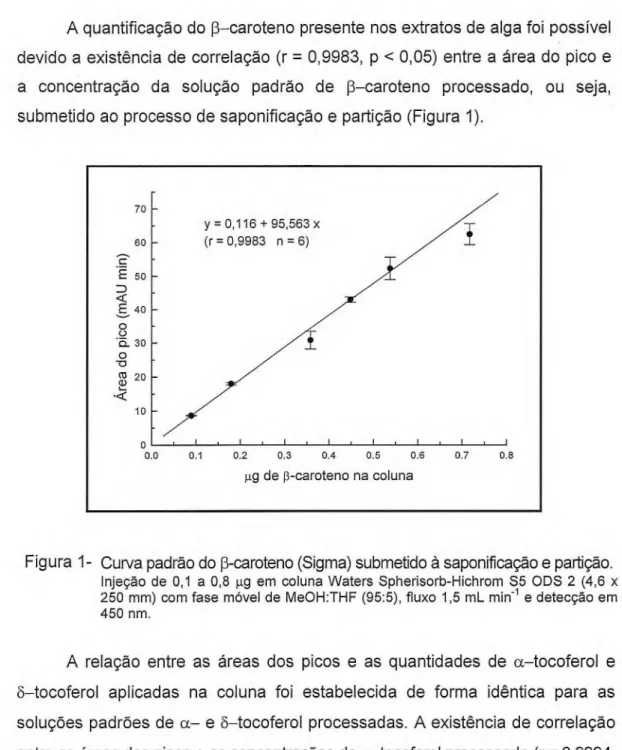
A quantificação do p—caroteno presente nos extratos de alga foi possível devido a existência de correlação (r = 0,9983, p < 0,05) entre a área do pico e a concentração da solução padrão de p—caroteno processado, ou seja, submetido ao processo de saponificação e partição (Figura 1).
Figura 1- Curva padrão do 3-caroteno (Sigma) submetido à saponificação e partição. Injeção de 0,1 a 0,8 µg em coluna Waters Spherisorb-Hichrom S5 ODS 2 (4,6 x 250 mm) com fase móvel de MeOH:THF (95:5), fluxo 1,5 mL min-1 e detecção em 450 nm.
y = -0,240 + 3,331 x (r = 0,9994 n = 7)
y = -0,566 + 3,036 x (r = 0,9971 n = 7)
-
E 25 —
E 20 —
o -o E. 15 — o
cu
• 10 -
s —
0
o 2 4 6 8 10 12
µg de 5-tocoferol na coluna
35 —
30
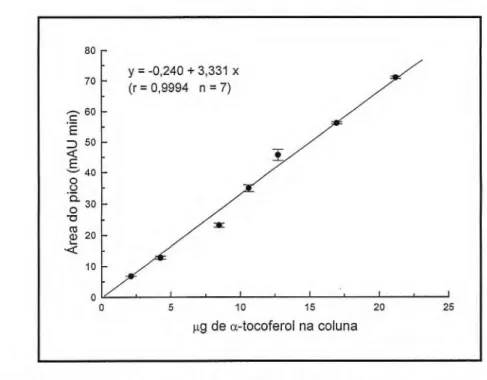
Figura 2 - Curva padrão do a—tocoferol (Sigma) submetido à saponificação e partição. Injeção de 2 a 25 µg em coluna Waters Spherisorb-Hichrom S5 ODS 2 (4,6 x 250 mm) com fase móvel constituída de MeOH:THF (95:5), fluxo 1,5 mL min-1 e detecção em 292 nm.
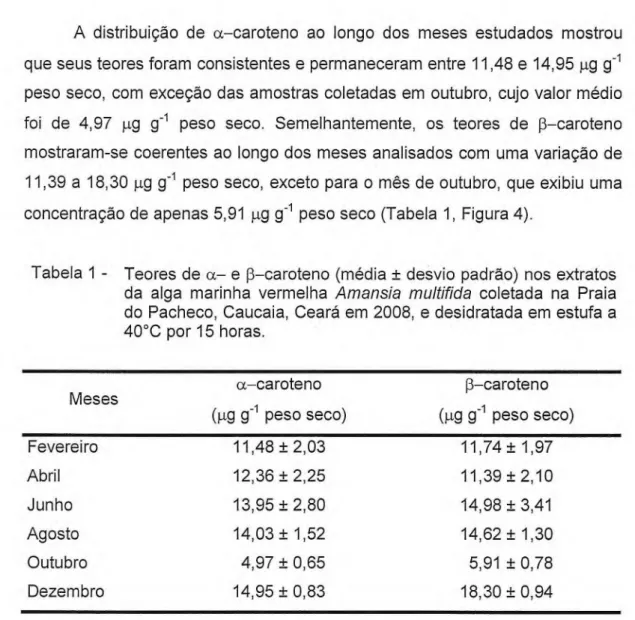
A distribuição de a-caroteno ao longo dos meses estudados mostrou que seus teores foram consistentes e permaneceram entre 11,48 e 14,95 µg g-1 peso seco, com exceção das amostras coletadas em outubro, cujo valor médio foi de 4,97 µg g-1 peso seco. Semelhantemente, os teores de p-caroteno mostraram-se coerentes ao longo dos meses analisados com uma variação de 11,39 a 18,30 µg g-1 peso seco, exceto para o mês de outubro, que exibiu uma concentração de apenas 5,91 µg g-1 peso seco (Tabela 1, Figura 4).
Tabela 1 - Teores de a- e p-ca rote n o (média ± desvio padrão) nos extratos da alga marinha vermelha Amansia multifida coletada na Praia
do Pacheco, Caucaia, Ceará em 2008, e desidratada em estufa a 40°C por 15 horas.
Meses a-caroteno
(µg g-1 peso seco)
i3-caroteno (µg g-1 peso seco)
Fevereiro 11,48 ± 2,03 11,74 ± 1,97
Abril 12,36 ± 2,25 11,39 ± 2,10
Junho 13,95 ± 2,80 14,98 ± 3,41
Agosto 14,03 ± 1,52 14,62 ± 1,30
Outubro 4,97 ± 0,65 5,91 ± 0,78
p-caroteno
eu
a-caroteno~11111111111~111111111F
0 2 4 6 8 10 12 14 16 18 20 22
µg g alga desidratada 1 a)
( é)
dez
out
ago
jun
abr
fev
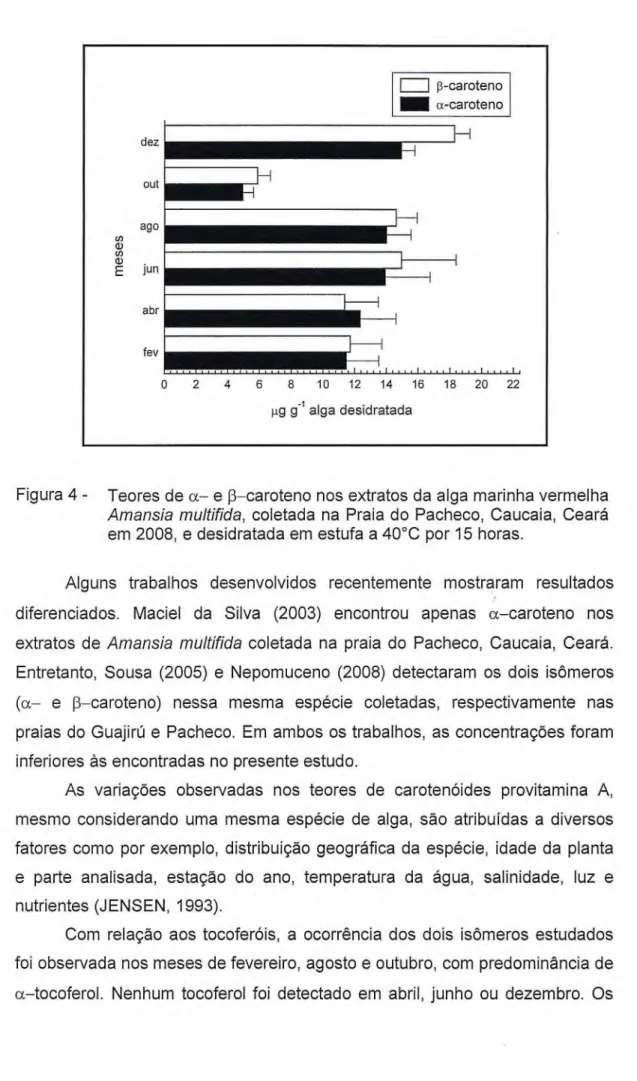
Figura 4 - Teores de a— e f3—caroteno nos extratos da alga marinha vermelha
Amansia multifida, coletada na Praia do Pacheco, Caucaia, Ceará em 2008, e desidratada em estufa a 40°C por 15 horas.
Alguns trabalhos desenvolvidos recentemente mostraram resultados diferenciados. Maciel da Silva (2003) encontrou apenas a—caroteno nos extratos de Amansia multifida coletada na praia do Pacheco, Caucaia, Ceará.
Entretanto, Sousa (2005) e Nepomuceno (2008) detectaram os dois isômeros
(a— e f3—caroteno) nessa mesma espécie coletadas, respectivamente nas
praias do Guajirú e Pacheco. Em ambos os trabalhos, as concentrações foram inferiores às encontradas no presente estudo.
As variações observadas nos teores de carotenóides provitamina A, mesmo considerando uma mesma espécie de alga, são atribuídas a diversos fatores como por exemplo, distribuição geográfica da espécie, idade da planta e parte analisada, estação do ano, temperatura da água, salinidade, luz e nutrientes (JENSEN, 1993).
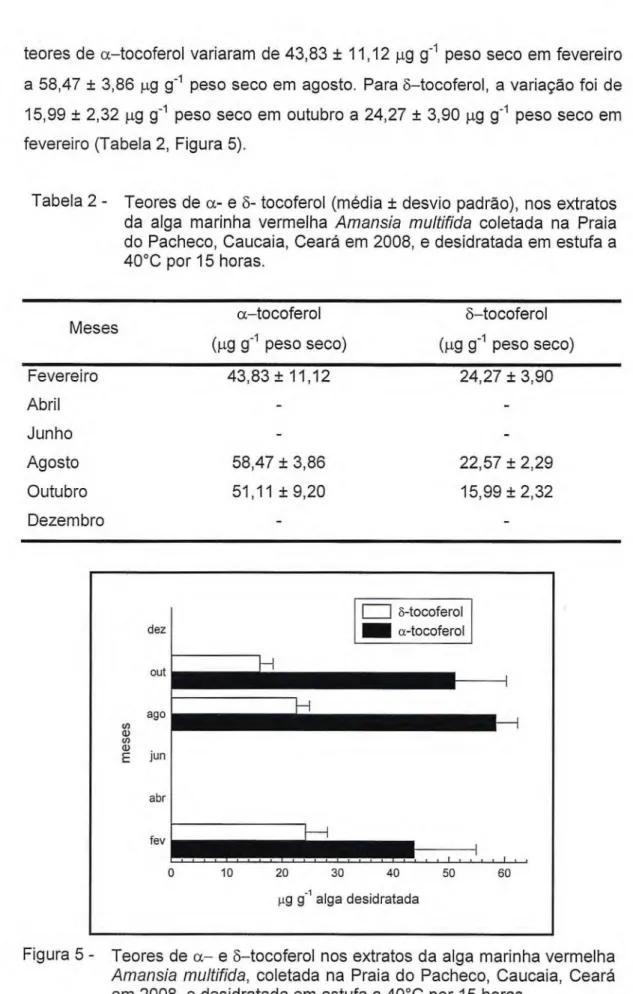
teores de a—tocoferol variaram de 43,83 ± 11,12 µg g-1 peso seco em fevereiro a 58,47 ± 3,86 µg g-1 peso seco em agosto. Para 8—tocoferol, a variação foi de 15,99 ± 2,32 µg g-1 peso seco em outubro a 24,27 ± 3,90 µg g-1 peso seco em fevereiro (Tabela 2, Figura 5).
Tabela 2 - Teores de a- e 3- tocoferol (média ± desvio padrão), nos extratos da alga marinha vermelha Amansia multifida coletada na Praia
do Pacheco, Caucaia, Ceará em 2008, e desidratada em estufa a 40°C por 15 horas.
Meses a—tocoferol
(µg g-1 peso seco)
8—tocoferol (µg g-1 peso seco) Fevereiro
Abril Junho
43,83 ± 11,12 24,27 ± 3,90
Agosto 58,47 ± 3,86 22,57 ± 2,29
Outubro Dezembro
51,11 ± 9,20 15,99 ± 2,32
Figura 5 - Teores de a— e 8—tocoferol nos extratos da alga marinha vermelha
Amansia multifida, coletada na Praia do Pacheco, Caucaia, Ceará
Foi detectado a-tocoferol nos extratos de A. multifida coletada na praia
do Guajirú, Trairi, Ceará, com concentração de 9,48 ± 3,83 µg gl peso seco (SOUSA, 2005). Já Santiago (2008) encontrou os dois isômeros analisados neste trabalho, com teores de 16,37 ± 3,26 µg gl peso seco para o cc-tocoferol e 10,64 ± 4,21 µg gl peso seco para o .3-tocoferol. Entre as quatro espécies de rodófitas analisadas pelo autor supracitado, A. multifida foi a que apresentou
maiores quantidades desses dois compostos com atividade de vitamina E. Segundo a Agência Nacional de Vigilância Sanitária (ANVISA), através da Resolução da Diretoria Colegiada (RDC) N2 269, de 22 de setembro de 2005 (BRASIL, 2005), a IDR de vitamina A consiste em 600 µg de RE para adultos. Cada 1 µg de p-caroteno corresponde a 0,167 µg de RE e cada 1 µg de outros carotenóides provitamina A, a 0,084 j..cg de RE. A partir dos valores estabelecidos para a IDR é possível classificar os alimentos como fontes excelentes ou úteis de um nutriente em particular.
A IDR de vitamina E consiste em 10 mg de a-tocoferol equivalente (a-TE) para adultos, considerando que 1 mg de d-a-tocoferol corresponde a
1,49 U.I. (BRASIL, 2005). Essa recomendação considera apenas o a-tocoferol entre os oito isômeros da vitamina E, por ser o único composto que mantém sua concentração no plasma humano (I0M, 2001).
As concentrações de retinol equivalente (RE) e tocoferol equivalente (TE) na alga marinha vermelha A multifida estão apresentadas na Tabela 3.
Tabela 3 - Concentrações de retinol equivalente (RE) e tocoferol equivalente (TE) na alga marinha vermelha Amansia multifida
coletada na Praia do Pacheco, Caucaia, Ceará em 2008, e desidratada em estufa a 40°C por 15 horas.
Meses RE (iLig g peso seco) TE (mg g 1 peso seco)
Fevereiro 2,925 0,0438
Abril 2,940
Junho 3,674
Agosto 3,620 0,0585
Outubro 1,404 0,0511
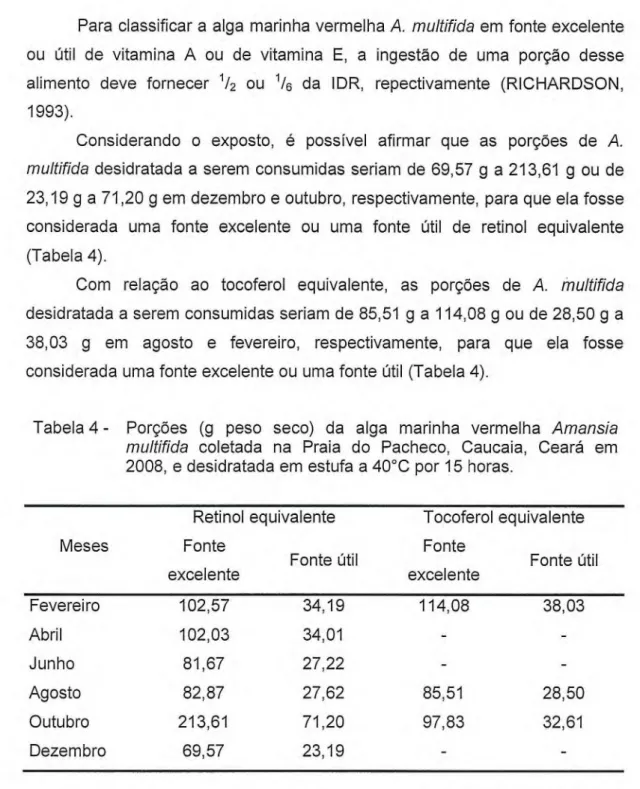
Para classificar a alga marinha vermelha A. multifida em fonte excelente
ou útil de vitamina A ou de vitamina E, a ingestão de uma porção desse alimento deve fornecer 1/2 ou 1/6 da IDR, repectivamente (RICHARDSON, 1993).
Considerando o exposto, é possível afirmar que as porções de A. multifida desidratada a serem consumidas seriam de 69,57 g a 213,61 g ou de 23,19 g a 71,20 g em dezembro e outubro, respectivamente, para que ela fosse considerada uma fonte excelente ou uma fonte útil de retino! equivalente (Tabela 4).
Com relação ao tocoferol equivalente, as porções de A. multifida
desidratada a serem consumidas seriam de 85,51 g a 114,08 g ou de 28,50 g a 38,03 g em agosto e fevereiro, respectivamente, para que ela fosse considerada uma fonte excelente ou uma fonte útil (Tabela 4).
Tabela 4 - Porções (g peso seco) da alga marinha vermelha Amansia multifida coletada na Praia do Pacheco, Caucaia, Ceará em
2008, e desidratada em estufa a 40°C por 15 horas.
Meses Retinol equivalente Fonte Fonte útil excelente Tocoferol equivalente Fonte Fonte útil excelente
Fevereiro 102,57 34,19 114,08 38,03
Abril 102,03 34,01 -
Junho 81,67 27,22 -
Agosto 82,87 27,62 85,51 28,50
Outubro 213,61 71,20 97,83 32,61
Dezembro 69,57 23,19
4 CONCLUSÃO
Na alga marinha vermelha Amansia multifida, desidratada a 40°C por 15 horas, os carotenóides provitamina A (a— e f3—caroteno) distribuiram-se quase que uniformemente ao longo do ano, com exceção do mês de outubro. Os teores de 13—caroteno foram sempre maiores que os de a—caroteno.
5 REFERÊNCIAS
AMBRÓSIO, C. L. B.; CAMPOS, F. A. C. S.; FARO, Z. P. Carotenóides como alternativa contra a hipovitaminose A. Revista de Nutrição, Campinas, v. 19, n. 2, p. 233-243, 2006.
BATISTA, E. S.; COSTA, A. G. V.; PINHEIRO-SANT'ANA, H. M. Adição da vitamina E aos alimentos: implicações para os alimentos e para a saúde humana. Revista de Nutrição, Campinas, v. 20, n. 5, p. 525-535, set./out. 2007.
BIANCHINI, R.; PENTEADO, M. V. C. Vitamina E. In: Vitaminas: aspectos nutricionais, bioquímicos, clínicos e analíticos. Barueri: Manole, p. 23-164. 2003.
BRAMLEY, P. M.; ELMADFA, I.; KAFATOS, A.; KELLY, F. J.; MANIOS, Y.; ROXBOROUGH, H. E.; SCHUCH, W.; SHEEHY, P. J. A.; WAGNER, K. H. Vitamin E. Journal of the Science of Food and Agriculture, West Sussex, v. 80, n. 7, p. 913-938, May 2000.
BRASIL. Resolução (2005). Resolução da Diretotia Colegiada (RDC) N2 269 de 22 de setembro de 2005 da Agência Nacional de Vigilância Sanitária. Regulamento técnico sobre a ingestão diária recomendada (IDR) de proteína, vitaminas e minerais. Diário Oficial [da] República Federativa do Brasil, Brasília, 23 de setembro de 2005.
BRIGELIUS-FLOHÉ, R.; KELLY, F. J.; SALONEN, J. T.; NEUZIL, J.; ZINGG, J. M.; AZZI, A. The European prospectiva on vitamin E: current knowledge and future research. American Journal of Clinicai Nutrition, Bethesda, v. 76, n. 4, p. 703-716, Oct. 2002.
BRIGELIUS-FLOHÉ, R.; TRABER, M. G. Vitamin E: function and metabolism. FASEB Journal, Bethesda, v. 13, n. 10, p. 1145-1155, July 1999.
BUNEA, A.; ANDJELKOVIC, M.; SOCACIU, C.; BOBIS, O.; NEACSU, M.; VERHÉ, R.; VAN CAMP, J. Total and individual carotenoids and phenolic acids content in fresh, refrigerated and processed spinach (Spinacia oleracea L.).
BURNS, J.; FRASER, P. D.; BRAMLEY, P. M. Identification and qualification of carotenoids, tocopherols and clorophylls in commonly consumed fruits and vegetables. Phytochemistry, Oxford, v. 62, n. 6, p. 939-947, Mar. 2003.
CHEN, M. H.; BERGMAN, C. J. A rapid procedure for analyzing rice bran tocopherol, tocotrienol and y-oryzanol contents. Journal of Food Composition and Analysis, San Diego, v. 18, n. 4, p. 319-331, June 2005.
DELLAPENNA, D. A decade of progress in understanding vitamin E synthesis in plants. Journal of Plant Physiology, Jena, v. 162, n. 7, p. 729-737, July 2005.
GÓMEZ-CORONADO, D. J. M.; IBANEZ, E.; RUPÉREZ, F. J.; BARBAS, C. Tocopherol measurement in edible products of vegetables origin. Journal of Chromatography A, Amsterdam, v. 1054, n. 1-2, p. 227-233, Oct. 2004.
HORNERO-MÉNDEZ, D.; BRITTON, G. Involvement of NADPH in the
cyclization reation of carotenoid biosynthesis. FEBS Letters, Oxford, v. 515, n. 1-3, p. 133-136, Mar. 2002.
10M - U.S. INSTITUTE OF MEDICINE. Food and Nutrition Board, Standing Committee on the Scientific Evaluation of Dietary Reference Intakes. Dietary Reference Intakes: for Vitamin A, Vitamin K, Arsenic, Boron, Cromium, Copper, lodine, Iron, Manganese, Molybdenium, Nickel, Silicon, Vanadium and Zinc. Washington, D. C.: National Academy Press, 2001. 797 p.
JENSEN, A. Present and future needs for alga and alga) products. Hydrobiology, Amsterdam, v. 260-261, n. 1, p. 15-23, June 1993.
LIAAEN-JENSEN, S. Algal carotenoids and chemosystematics. In: FAUKLER, D. J.; FENICAL, W. H. (eds.). Marine natural products chemistry. New York: Plenum Press, 1977. p. 239-259.
MABEAU, S.; FLEURENCE, J. Seaweed in food products: biochemical and nutritional aspects. Trends in Food and Technology, Oxford, v. 4, n. 4, p. 103-107, Apr. 1993.
McHUGH, D. J. A guide to the seaweed industry. FAO Fisheries Technical Paper n. 441. 105 p. Rome, 2003. Disponível em: <http://www.fao.org> Acesso em: 30 maio 2009.
MELÉNDEZ-MARTÍNEZ, A. J.; VICARIO, I. M.; HEREDIA, F. J. Importancia nutricional de los pigmentos carotenóides. Archivos Latinoamericanos de Nutrición, Caracas, v. 54, n. 2, p. 209-215, June 2004.
MEYDANI, M. Effect of functional food ingredients: vitamin E modulation of cardiovascular diseases and immune status in the elderly. American Journal of Clinicai Nutrition, v. 71, n. 6, p. 1665S-1668S, Suppl. S, June 2000.
MUNTEANU, A.; ZINGG, J. M.; AZZI, A. Anti-atherosclerotic effects of vitamin E — myth or reality? Journal of Cellular and Molecular Medicine, Bucharesst, v. 8, n. 1, p. 59-76, Jan./Mar. 2004.
NEPOMUCEMO, F. O. Extração e quantificação de a— e 3—caroteno em doze espécies de macroalgas marinhas "in natura" coletadas na praia do Pacheco, Caucaia, Ceará. 2008. 21 f. Monografia (Graduação) — Universidade Federal do Ceará, Fortaleza, 2007.
OLIVEIRA, E. C. Macroalgas marinhas de valor comercial: Técnicas de cultivo. Panorama da Aquicultura, Rio de Janeiro, v. 7, n. 42, p. 42-45, jul./ago. 1997.
PIRES, K. M. S. Avaliação sazonal de carotenóides provitamina A (a— e (3—caroteno) e vitamina E (a— e 3—tocoferol) em macroalgas marinhas pertencentes à família Caulerpaceae (Divisão Chlorophyta). 2007. 94 f. Dissertação (Mestrado em Engenharia de Pesca) — Universidade Federal do Ceará, Fortaleza, 2007.
RICHARDSON, D. P. Food fortification. In: OTTAWAY, P.B. (ed.). The Technology of Vitamins in Food. Glasgow: Blackie Academic & Professional, 1993, p. 233-245.
RIGOTTI, A. Absorption, transport, and tissue delivery of vitamin E. Molecular Aspects of Medicine, Amsterdam, v. 28, n. 5-6, p. 423-436, Oct./Dec. 2007.
ROWAN, K. S. The carotenoids. In:
Photosynthetic pigments of algae.
Cambridge: Cambridge University Press, 1989. chapter 4, p. 112-165.
SAKER-SAMPAIO, S.
Evaluation of
Palmaria palmateand
Laminaria digitata aspotential human food products.
1997. 165 f. Tese (PhD) —University of Portsmouth, Portsmouth, 1997.
SANTIAGO, J. G.
Extração e quantificação de
a-e 8-tocoferol em
macroalgas marinhas "in natura" utilizando cromatografia líquida de alta
eficiência.
2008. 23 f. Monografia (Graduação) — Universidade Federal doCeará, Fortaleza, 2008.
SOUSA, M. B.
Extração e quantificação de a—caroteno, p—caroteno e
a—tocoferol em macroalgas marinhas utilizando cromatografia líquida de
alta eficiência em fase reversa.
2005. 75 f. Dissertação (Mestrado) —Universidade Federal do Ceará, Fortaleza, 2005.
SPECIFICATIONS AND CRITERIA FOR BIOCHEMICAL COMPOUNDS. 3 ed. Washington: Ed. National Academy of Sciences, 1972.
STAHL, W.; SIES, H. Bioactivity and protective effects of natural carotenoids.
Biochimica et Biophysica Acta - Molecular Basis of Disease,
Amsterdam, v.1740, n. 2, p. 101-107, May 2005.
TAPIERO. H.; TOWSEND, D. M.; TEW, K. D. The role of carotenoides in prevention of human pathologies.
Biomedicine & Pharmacotherapy,
Paris, v.58, n. 2, p. 100-110, Mar. 2004.
VIDOTTI, E. C.; ROLLEMBERG, M. C. E. Algas: da economia nos ambientes aquáticos à biorremediação e à química analítica.