Eficácia do ácido indolbutírico de sementes de Phaseolus vulgaris L. e do
fungo Trichoderma sp. No enraizamento e desenvolvimento de estacas de
aceroleira
Efficacy of indolbutyric acid from seeds of Phaseolus vulgaris L. and
fungus Trichoderma sp. In rooting and development of acerola cuttings
DOI:10.34117/bjdv5n11-166
Recebimento dos originais: 07/10/2019 Aceitação para publicação: 15/11/2019
Rosa Betânia Rodrigues de Castro
Mestra em Microbiologia Agropecuária pela Faculdade de Ciências Agrárias e Veterinárias de Jaboticabal– FCAV/UNESP, SP, Brasil
Instituição: Universidade do Estado de Minas Gerais - UEMG
Endereço: Rua Vereador Geraldo Moisés da Silva, s/n – Universitário, Ituiutaba - MG, Brasil E-mail: rosa.castro@uemg.br
Rhaísa Candido Vilela
Graduada em ciências Biológicas pela Universidade do Estado de Minas Gerais Endereço:Rua C5, 527- Residencial Canaã 1, Ituiutaba - MG, Brasil
E-mail. rhaisacv@hotmail.com Osania Emerenciano Ferreira
Doutora em Microbiologia Agropecuária pela Faculdade de Ciências Agrárias e Veterinárias de Jaboticabal – FCAV/UNESP, SP, Brasil
Instituição: Universidade do Estado de Minas Gerais - UEMG
Endereço: Av. Professor Mario Palmério, 1001 - Universitário, Frutal – MG, Brasil E-mail: osania.ferreira@uemg.br
Eleusa Maria Ferreira Rocha
Doutora em Genética Molecular de Microrganismos pela Universidade de São Paulo (USP) Ribeirão Preto, SP, Brasil
Instituição: Universidade do Estado de Minas Gerais – UEMG
Endereço: Av. Vereador Geraldo Moisés da Silva s/n, Universitário, Ituiutaba, MG, Brasil E-mail: eleusa.rocha@uemg.br
RESUMO
Neste trabalho analisamos o desenvolvimento e enraizamento de estacas de Malpighia emarginata D.C (aceroleira) utilizando dois estimulantes naturais, um obtido de sementes de Phaesolus vulgaris L.(feijão) em germinação, rico em ácido indolbutírico e outro adquirido do fungo Trichoderma sp. Foram utilizados seis tratamentos com 10 estacas cada e 4 repetições, totalizando 240 estacas. Observou-se um resultado satisfatório no desenvolvimento das estacas, graças aos enraizantes naturais.
Palavras-chave: Enraizantes naturais, sustentabilidade ambiental, gestão ambiental ABCTRACT
In this work we analyzed the development and rooting of Malpighia emarginata D.C (aceroleira) cuttings using two natural stimulants, one obtained from germinating seeds of Phaesolus vulgaris L. (bean) and rich in the fungus Trichoderma sp. Six treatments with 10 cuttings each and 4 repetitions were used, totaling 240 cuttings. A satisfactory result was observed in the development of the cuttings, thanks to the natural roots.
Key words: Natural Roots, environmental sustainability, environmental management. 1 INTRODUÇÃO
A aceroleira (Malpighia emarginata D.C.) é uma planta frutífera de clima tropical, pertencente à família Malpighiacea, originária do Mar das Antilhas, Norte da América do Sul e América Central. Os frutos desta cultura se destacam, graças ao seu elevado teor de ácido ascórbico (vitamina C), que oscila entre 1000 e 1800 mg 100 g-1 (CUNHA NETO et al., 2012).
De acordo com Moura et al.(2007) a acerola pode ser pode ser propagada de forma sexuada, por meio de sementes e de forma assexuada ou vegetativa, através de enxertia ou estaquia. Entretanto, tendo em vista o aumento da cultura e procurando seu espaço junto ao mercado internacional a propagação por estaquia é o método mais eficiente, pois assegura maior precocidade na produção, bem como a transmissão das características genéticas da planta propagada.
Vários fatores podem intervir na formação de raízes na estaquia, a sanidade da planta matriz, o tipo de estaca, aplicação de reguladores vegetais, dentre outros (FACHINELLO et al., 2005).
Para acelerar e impulsionar o enraizamento das estacas aconselha-se a aplicação de reguladores vegetais, como o ácido indolbutírico (AIB) do grupo das auxinas antes do plantio, os quais levam à maior percentual de formação de raízes, melhor qualidade e homogeneidade no enraizamento (TAKATA et al., 2012).
Vale ressaltar, que atualmente a busca por métodos naturais de produção vegetal tem sido intensificada no setor de fruticultura. Os enraizantes naturais, ricos em AIB, também denominados bioestimulantes, são opções alternativas e de baixo custo com relação aos enraizantes convencionais químicos (ARBBIS, 2016).
Há estudos de que as sementes em germinação de feijão (Phaseolus vulgaris L.) possuem em sua composição níveis significativos de AIB que favorecem o enraizamento de estacas (SILVA et al., 2010).
Fungos do gênero Trichoderma estão entre os microrganismos mais comumente estudados como agentes de biocontrole de doenças e apresenta, também, atividade como promotores de crescimento de plantas (SANTOS, 2008). Muitas dessas espécies possuem a capacidade de se associar às raízes, formando uma interação interespecífica de simbiose, por mecanismos semelhantes àqueles de fungos micorrízicos.
Mediante ao exposto, o presente trabalho tem por objetivo estudar o efeito do ácido indolbutírico (AIB) obtido a partir do feijão, assim como a ação de um isolado de Trichoderma sp no enraizamento e desenvolvimento de estacas de aceroleira.
2 MATERIAIS E PROCEDIMENTOS
O presente trabalho teve os experimentos realizados nos Laboratórios de Biologia Geral, Microbiologia, Bioquímica e Biologia Vegetal da Universidade Estadual de Minas Gerais (UEMG), unidade Ituiutaba. O delineamento utilizado foi o Inteiramente Casualizado (DIC) com 6 tratamentos e 4 repetições contendo 10 estacas por repetição, totalizando 240 estacas de aceroleira com aproximadamente 15 cm de comprimento e dois pares de folhas cortadas ao meio, que foram submersas por 2 horas em seis tratamentos distintos: T1) estacas imersas em solução de 300 g. L-1 de sementes germinadas de feijão (Phaseolus vulgaris L.); T2) estacas imersas em solução de 500 g. L-1 de sementes germinadas de feijão (Phaseolus
vulgaris L.); T3) inóculo do isolado de Trichoderma sp. na concentração de 105UFC.mL -1; T4) 300 g. L-1 de sementes germinadas de feijão (Phaseolus vulgaris L.) e inóculo do
isolado de Trichoderma sp. na concentração de 105UFC.mL-1; T5) 500 g. L-1 de sementes
germinadas de feijão (Phaseolus vulgaris L) e inóculo do isolado de Trichoderma sp. na concentração de 105UFC.mL-1; T6) água destilada como controle. Após 120 dias do plantio das estacas, as características avaliadas foram: Massa da folha seca (MFS): obtida em estufa com circulação forçada de ar a 65ºC até atingir massa constante, seguida de pesagem em balança analítica e o valor expresso em gramas; Massa da folha fresca (MFF): determinada através da pesagem das folhas em balança analítica e expressa em gramas; de estacas enraizadas por cada unidade experimental, adotando 10 estacas como 100%; Porcentagem de sobrevivência (%SOBR): determinadas através do número de estacas vivas por cada unidade experimental, adotando 10 estacas como 100%.
Os resultados obtidos a partir dos atributos avaliados foram submetidos à análise de variância pelo teste F e as médias comparadas pelo teste de Duncan ao nível de 5% de probabilidade, utilizando o programa Agroestat versão 1. 0 (BARBOSA; MALDONADO, 2010).
2 RESULTADOS E DISCUSSÃO
Em todas as tabelas das características avaliadas dos tratamentos não aprece o T6(controle), porque para esse grupo não houve nenhuma evidência positiva, todas as estacas submetidas ao referido tratamento não sobreviveram.
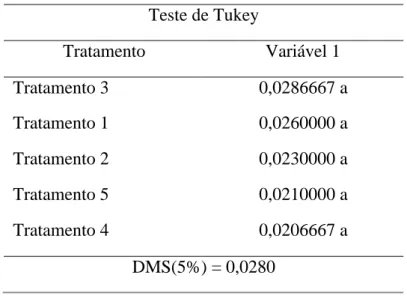
Foi feita a medição da massa seca das folhas para análise da eficiência dos tratamentos (Tabela 1).
Tabela 1. Avaliação da massa das folhas secas com 120 dias após o plantio das estacas de acerola no ano de 2018. Teste de Tukey Tratamento Variável 1 Tratamento 3 0,0286667 a Tratamento 1 0,0260000 a Tratamento 2 0,0230000 a Tratamento 5 0,0210000 a Tratamento 4 0,0206667 a DMS(5%) = 0,0280
Médias seguidas de letras iguais, minúsculas não diferem estatisticamente entre si, pelo teste de Tukey ao nível de 5% de probabilidade.
Esses resultados estão de acordo com Machado et al.( 2012), uma vez que afirmam que a influência de microrganismos sobre o desenvolvimento das plantas é ampla, incluindo os efeitos benéficos na germinação de sementes, emergência de plântulas, crescimento e produtividade de grãos. O emprego de promotores de crescimento de plantas para o incremento da produção agrícola será supostamente uma das táticas mais expressivas para a atualidade no mundo. Isso se deve à demanda emergente para a diminuição da necessidade de fertilizantes minerais e da necessidade para o desenvolvimento de uma agricultura sustentável. Com relação ao enraizante de feijão, observa-se algo bastante positivo, uma vez que na literatura clássica praticamente não há trabalhos científicos que testaram o seu estudo para esse fim.
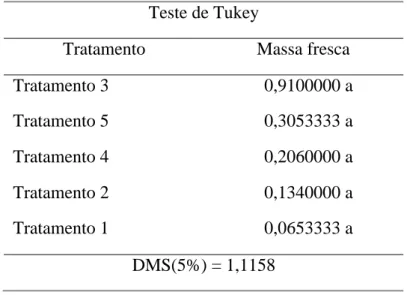
Outra característica analisada que corrobora para o efeito satisfatório dos enraizantes naturais foi a medição da massa da folha fresca (Tabela 2).
Tabela 2. Avaliação da massa das folhas frescas com 120 dias após o plantio das estacas de acerola no ano de 2018.
Teste de Tukey
Tratamento Massa fresca
Tratamento 3 0,9100000 a Tratamento 5 0,3053333 a Tratamento 4 0,2060000 a Tratamento 2 0,1340000 a Tratamento 1 0,0653333 a DMS(5%) = 1,1158
Médias seguidas de letras iguais, minúsculas não diferem estatisticamente entre si, pelo teste de Tukey ao nível de 5% de probabilidade.
Foi também analisado o comprimento da maior folha entre os tratamentos (Tabela 3).
Tabela 3. Avaliação do comprimento da maior folha com 120 dias após o plantio das estacas de acerola no ano de 2018. Teste de Tukey Tratamento Comprimento Tratamento 2 15,450000 a Tratamento 5 14,443333 a Tratamento 4 12,213333 a Tratamento 3 10,440000 a Tratamento 1 9,4066667 a DMS(5%) = 13,8871
Médias seguidas de letras iguais, minúsculas não diferem estatisticamente entre si, pelo teste de Tukey ao nível de 5% de probabilidade.
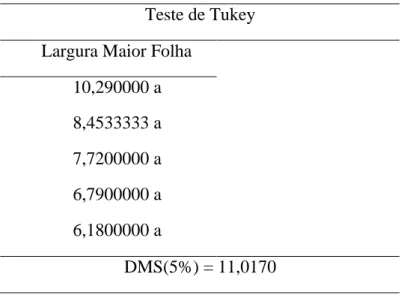
De forma semelhante ao estudo anterior, foi feita a avaliação da largura da maior folha (tabela 4).
Tabela 4. Análise da largura da maior folha com 120 dias após o plantio das estacas de acerola no ano de 2018.
Teste de Tukey Largura Maior Folha
10,290000 a 8,4533333 a 7,7200000 a 6,7900000 a 6,1800000 a DMS(5%) = 11,0170
Fungos do gênero Trichoderma são uns dos principais microrganismos de importância para a ampliação do crescimento vegetal. Este fungo pode induzir positivamente na germinação de sementes, no desenvolvimento e rendimento da cultura devido, também, à produção de substâncias promotoras de crescimento e melhoria na nutrição das plantas, principalmente pela solubilização de fósforo (OLIVEIRA et al., 2012).Tal afirmação vai de encontro com os resultados obtidos nesta pesquisa com relação à porcentagem de sobrevivência das estacas de acerola frente aos tratamentos ( Tabela 5).
Tabela 5. Porcentagem de Sobrevivência dos 6 tratamentos com 120 dias após o plantio das estacas de acerola no ano de 2018.
Tratamento Porcentagem Sobrevivência (%) Tratamento 3 20,0 Tratamento 4 17,5 Tratamento 5 17,5 Tratamento 1 12,5 Tratamento 2 Tratamento 6 5,0 0,0
A metodologia inicial teve que ser mudada, pois pelo proposto, as análises seriam após os 60 dias de plantio, porém, resolvemos esperar por mais 60 dias, totalizando assim 120 dias de plantio, pois os botões vegetativos precursores das folhas estavam em um estágio que necessitava maior desenvolvimento para as análises propostas. No entanto, mesmo transcorridos o tempo relatado não havia nenhum indício de formação de raízes, apenas folhas. Em decorrência desse fato tivemos também que mudar parte das análises que eram sobre as raízes, tivemos que fazer em função das folhas.
Tal fato descrito acima pode ser explicado Segundo Karami e Salehi, (2010), que relatam sobre que o potencial de enraizamento, bem como a qualidade e a quantidade de raízes nas estacas, podem variar com a espécie, cultivar, condições ambientais e condições internas da própria planta. Os fatores que interagem com o enraizamento das estacas não estão claramente esclarecidos, não permitindo a generalização do método de propagação partilhando do mesmo princípio, Hartmann et al. (2002), concluem que as estacas têm influência de alguns fatores de maior importância, como as condições fisiológicas da planta doadora (presença de carboidrato, substâncias nitrogenadas, aminoácidos, auxinas, compostos fenólicos e outras substâncias não identificadas), assim como o período de coleta e idade da planta matriz. Além dos fatores externos como disponibilidade de água e luminosidade. De acordo com Fachinello et al. (2005), a época do ano em que as estacas são coletadas está rigorosamente relacionada à sua consistência, sendo que aquelas coletadas em um período de crescimento vegetativo intenso (primavera/verão) tendem a enraizar mais, enquanto que aquelas coletadas no inverno são mais lignificadas e possuem menor capacidade
de enraizamento.
3 CONCLUSÃO
De forma geral os enraizantes naturais possuíram um efeito positivo no desenvolvimento de folhas e sobrevivência das estacas de aceroleira. Porém, a aplicação da estaquia acaba sendo uma tarefa complexa e que exige um conjunto de informações que não são encontradas de forma satisfatória na literatura. Assim, Pesquisas futuras sobre o esclarecimento acerca desse fato são sugeridas a fim de se estabelecer com precisão sobre o desenvolvimento das raízes nas estacas de acerola.
AGRADECIMENTO
REFERÊNCIAS
ARBBIS. Enraizantes-como fazer hormônios de crescimento para estacas, 2016. Disponível em:<http://www.arbbis.com/como-plantar/enraizantes-como-fazer- hormonios-de-crescimento-para-estacas-e-mudas/> Acesso em: 26 set.2017.
BARBOSA, J. C.; MALDONADO, J. W. AgroEstat: sistema para análises estatísticas de ensaios agronômicos. Jaboticabal/SP: Departamento de Ciências Exatas,2010.
BASTOS, D. C.; SCARPARE FILHO, J. A.; LIBARDI, M. N.; PIO, R. Estiolamento, incisão na base da estaca e uso do ácido indol-butírico na propagação da caramboleira por estacas lenhosas. Ciências Agrotécnicas, v. 33, n. 1, p. 313- 318, 2009.
CUNHA NETO, J., RABELO, M.C., BERTINI, C.H.C. M., MARQUES, G.V.,
MIRANDA, M.R.A. Caracterização agronômica e potencial antioxidantes de frutos de clones de aceroleira. Revista Ciência Agronômica, v.43, n.1, p. 713-721, 2012.
FACHINELO, J. C.; HOFFMANN, A.;NACHTIGAL, J. C. Propagação de plantas frutíferas. 1.ed.Brasília/DF: Embrapa Informação Tecnológica, 2005. 221p.
HARTMANN, H. T.; KESTER, D. E.; DAVIES JUNIOR, F. T.; GENEVE, R. L. Plant propagation: principles and pratices. 7. ed. New Jersey: Prentice–Hall, 2002. 880 p
KARAMI, A.; SALEHI, H. Adventitious Root Formation in Rohida(Tecomella undulata (SM.) Seem) Cuttings. Propagation of Ornamental Plants. 10/3: p.163- 165, 2010.
MACHADO; D. F. M.; PARZIANELLO, F. R.; SILVA, A. C. F.; ANTONIOLLI, Z. I. Trichoderma no Brasil: O fungo e o bioagente. Revista de Ciências Agrárias, Lisboa, v. 35, n. 1, p. 274-288, 2012.
MORANDI, M. A. B.; BETTIOL, W. Controle biológico de doenças de plantas no Brasil. In: .Biocontrole de doenças de plantas: uso e perspectivas. Jaguariúna/SP: Embrapa Meio Ambiente.2009. p.07-14.
e físico-químicas de frutos de clones de aceroleira (Malpighia emarginata D.C.). Revista Ciência Agronômica, v. 38, n. 1, p. 52-57, 2007.
OLIVEIRA, A. G.; CHAGAS JÚNIOR, A. F.; SANTOS, G. R.; MILLER, L. O.;
CHAGAS, L. F. B. Potencial de solubilização de fosfato e produção de AIA por Trichoderma spp. Revista Verde de Agroecologia e Desenvolvimento Sustentável, Pombal, v. 7, n. 3, p. 149-155, 2012.
ONO, E. O.; RODRIGUES, J. D. Aspectos da fisiologia do enraizamento de estacas caulinares. 1 ed. Jaboticabal/SP: FUNEP, 1996. 83p.
PRADO, A. Composição fenólica e atividade antioxidante de frutas tropicais. Piracicaba, 2009.94 f. Dissertação (Mestrado em Ciências e Tecnologia de Alimentos)- Escola Superior de Agricultura “Luiz de Queiroz”, Universidade de São Paulo(USP),Piracicaba/SP, 2009.
POMELLA, A.W.V.; RIBEIRO, R.T.S. Controle biológico com Trichoderma em grandes culturas – Uma visão empresarial. In: BETIOL, W.; MORANDI, M.A.B. (Orgs.). Biocontrole de doenças em plantas: uso e perspectivas. Jaguariúna/SP: Embrapa Meio Ambiente. 2009. p.239-244.
SANTOS, H. A. Trichoderma spp. como promotores de crescimento em plantas e como Antagonistas a Fusarium oxysporum.2008. 94 f. Dissertação (Mestrado em ciências agrárias) – Faculdade de agronomia e medicina veterinária, Universidade de Brasília(UNB), Brasília/DF, 2008.
SILVA, P. N. L.; COSTA, E.; FERREIRA, A. F. A.; SILVA, A. C. R.; GOMES, V. A. Enraizamento de estacas de aceroleira: efeitos de recipientes e substratos. Revista Agrarian, v.3, n.8, p.126-132, 2010.
TAKATA, W. H. S.; SILVA, E. G.; BARDIVIESSO, D. M. Enraizamento de estacas de Duranta repens Linn “Aurea” em função de doses de IBA. Revista Científica Eletrônica de Agronomia, v.21, n. 1, p. 1-9, 2012.