Braz. J. of Develop., Curitiba, v. 6, n.5, p.29262-29274 may. 2020. ISSN 2525-8761
Características del tratamiento farmacológico de pacientes
con anemia falciforme tratados en el centro de sangre de João Pessoa,
Paraíba, Brasil (2015-2016).
Características do tratamento farmacológico dos pacientes
com anemia falciforme tratada no hemocentro de João Pessoa, Paraíba,
Brasil (2015-2016).
DOI:10.34117/bjdv6n5-395
Recebimento dos originais: 20/04/2020 Aceitação para publicação: 20/05/2020
Maria José do Nascimento Brito
Programa de Doutorado em Saúde Pública da Universidad Americana – UA Instituição: Universidade Americana - UA
Endereço: Av. Brasília, 1100, Asunción, Paraguai. +595 21 288 8000 E-mail: mariajnbrito@hotmail.com
Elder Oliveira da Silva
Programa de Doutorado em Saúde Pública pela Universidad Columbia del Paraguay. Instituição: Universidad Columbia del Paraguay
Endereço: Calle 25 de Mayo Nº 658 y Antequera +595 21 490 811. E-mail: elder.enf@hotmail.com
Pasionaria Rosa Ramos Ruiz Diaz
Programa de Doutorado em Saúde Pública da Universidade Americana. Instituição: Universidade Americana - UA
Endereço: Av. Brasília, 1100, Asunción, Paraguai. +595 21 288 8000 E-mail: pasionariaramos@gmail.com
RESUMEN
Objetivo: Describir las características del tratamiento farmacológico de pacientes con anemia falciforme tratados en el centro de sangre de João Pessoa, Paraíba, Brasil, de 2015 a 2016. Método: Estudio cualitativo, descriptivo y transversal. La muestra comprendió 91 pacientes de un total de 119. El instrumento utilizado fue un cuestionario semiestructurado con preguntas abiertas y cerradas, con preguntas relacionadas a las características sociodemográficas y del tratamiento farmacológico recibido. Resultados: 58% (53) fueron hombres, edad media de 27,59 años. El 46% (42) contaba de 12 a 25 años, pardos 65% (59), solteros 58% (53), con educación incompleta 42% (38) y que vivían con sus padres 53% (48). El 73% (66) usa 4 a 7 medicamentos al día. El 100% (91) utilizaba analgésicos y vitaminas, 53% (48) la hidroxiurea como agente antineoplásico. EL 89% (81) presentó alergia. Los resultados negativos relacionados con las drogas, fueron problemas de salud no tratados 35% (32), falta de efectividad terapéutica 20% (18) y toxicidad 33% (30). Conclusión: se observan problemas de salud no tratados, falta de
Braz. J. of Develop., Curitiba, v. 6, n.5, p.29262-29274 may. 2020. ISSN 2525-8761 efectividad terapéutica y toxicidad, por lo que es necesario el monitoreo permanente del tratamiento farmacológico recibido por estos pacientes.
Palabras claves: Anemia de Células Falciformes; Quimioterapia; Cumplimiento y Adherencia
al Tratamento; Efecto colaterales.
RESUMO
Objetivo: Descrever as características do tratamento farmacológico de pacientes com anemia falciforme atendidos no hemocentro de João Pessoa, Paraíba, Brasil, de 2015 a 2016. Método: Estudo qualitativo, descritivo e transversal. A amostra foi composta por 91 pacientes, de um total de 119. O instrumento utilizado foi um questionário semiestruturado, com perguntas abertas e fechadas, com questões relacionadas às características sociodemográficas e ao tratamento farmacológico recebido. Resultados: 58% (53) eram homens, com idade média de 27,59 anos. 46% (42) tinham entre 12 e 25 anos, pardos 65% (59), solteiros 58% (53), com ensino incompleto 42% (38) e que moravam com os pais 53% (48). 73% (66) usam de 4 a 7 medicamentos por dia. 100% (91) usaram analgésicos e vitaminas, 53% (48) hidroxiureia como agente antineoplásico. 89% (81) apresentaram alergia. Os resultados negativos relacionados aos medicamentos foram problemas de saúde não tratados em 35% (32), falta de eficácia terapêutica em 20% (18) e toxicidade em 33% (30). Conclusão: são observados problemas de saúde não tratados, falta de efetividade terapêutica e toxicidade, razão pela qual é necessário o monitoramento permanente do tratamento farmacológico recebido por esses pacientes.
Palavras-Chave: Anemia Falciforme; Quimioterapia; Cumprimento e adesão ao Tratado;
Efeito colateral
.
1 INTRODUCCIÓN
La Organización Mundial de la Salud (OMS), estima que casi el 5% de la población mundial es portadora de alguna enfermedad relacionada a la hemoglobina (WEATHERALL DJ e CLEGG JB, 2001). Estudios nacionales sugieren una prevalencia aproximada de dos millones de personas con trazos falciformes, y ocho mil serían portadores de Anemia de Células Falciformes (AF) (CANÇADO RD e JESUS JA, 2007; BRASIL, 2018).
La AF constituye una disfunción hemolítica, definida por la presencia de la hemoglobina S (Hb S), la cual se encuentra como una hemoglobina modificada, proveniente de una cadena beta mutante de la globina(BRASIL, 2002). La Hb S lleva a la polimerización del eritrocito, haciendo que la misma adopte la forma de una “hoz”(GÓMEZ-CHIARI M, et al., 2003; ZAGO MA e PINTO ACS, 2007;).
Los medicamentos utilizados como rutina em el tratamiento de la AF en el Brasil, y recomendados por el Ministerio de Salud son; el ácido fólico (de uso continuo), penicilina oral
Braz. J. of Develop., Curitiba, v. 6, n.5, p.29262-29274 may. 2020. ISSN 2525-8761 o inyectable (hasta los 5 años de edad), antibióticos, analgésicos y anti-inflamatórios (en caso de complicaciones) (TOSTES MA, et al., 2009; BRASIL, 2016, 2018 )
La Hidroxicarbamida también conocida como Hidroxiuréia es comercializada con el nombre de Hydrea®, integra conjuntamente con los quelantes del hierro, la asistencia farmacéutica de complejidad media (JUNIOR AF, 2013; BRASIL, 2018)
Según el Tercer Consenso de Granada descrito por Hernández DS et al. (2014), los Resultados Negativos asociados a Medicamentos (RNMs) deben ser identificados y clasificados durante el estudio farmacoterapéutico, para lo cual son utilizados tres perfiles: el primero constituye la aparición de un problema de salud debido al fármaco; el segundo es una patología que no está siendo controlada y el tercero el surgimiento de una reacción indeseada ocasionada por el fármaco. Estos son clasificados en RNM de necesidad, RNM efectividad y RNM de seguridad (LEITE SN, 2008; PINTO LH. et al., 2015; SOLER O, et al., 2015).
De acuerdo con RNM de necesidad, existe el problema de salud no tratado, donde el paciente sufre un problema de salud asociado con no recibir la medicación que necesita, y el
efecto de la medicación innecesaria, donde el paciente sufre un problema de salud asociado con
la recepción de un medicamento que no se necesita (SANTOS JL e CHIN CM, 2012). Con respecto a la efectividad de la RNM, existe una inefectividad no cuantitativa, donde el paciente tiene un problema de salud debido a una ineficacia no cuantitativa en la medicación, y una
inefectividad cuantitativa, donde el paciente tiene un problema de salud debido a una ineficacia
cuantitativa de la medicación. De acuerdo con la RNM de seguridad o toxicidad, se incluye la
inseguridad no cuantitativa, cuyo paciente tiene un problema de salud debido a una inseguridad
no cuantitativa de un medicamento y una inseguridad cuantitativa donde el paciente tiene un problema de salud debido a una inseguridad cuantitativa de un medicamento (CORRER CJ et al, 2004; LEITE SN, 2008; SOLER O, et al., 2015).
A través del monitoreo farmacoterapéutico, es posible identificar y minimizar las IRM en pacientes con enfermedades crónicas. Sin embargo, desafortunadamente, esta estrategia todavía está infrautilizada. La observación de la aparición de IRM principalmente por el profesional farmacéutico es de gran relevancia para la identificación de reacciones adversas y sus soluciones, evitando el abandono o la adherencia incompleta a la terapia con medicamentos (CORRER CJ et al, 2004).
En vista de esto, el presente estudio presenta como objetivo describir las características del tratamiento farmacológico utilizado en pacientes con anemia falciforme tratados en el centro de sangre de João Pessoa, Paraíba, Brasil, durante el período de 2015 a 2016.
Braz. J. of Develop., Curitiba, v. 6, n.5, p.29262-29274 may. 2020. ISSN 2525-8761
2 MÉTODOS
Es un estudio cuantitativo, descriptivo, transversal y temporalmente prospectivo realizado en el Hemocentro de João Pessoa-PB en el período comprendido entre enero de 2015 a diciembre del 2016.
La población estuvo constituída de 119 pacientes portadores de AF que se encontraban registrados en la institución. La muestra comprendió 91 participantes, 25 de ellos no fueron encontrados por contar con su catastro desactualizado y, 3 (tres) rechazaron a participar de la investigación.
Para la recolección de datos fueron utilizados sus datos clínicos, y aplicado un cuestionario semiestructurado con preguntas abiertas y cerradas. El cuestionario consto de dos bloques; el primero de ellos referido a las variables sociodemográficas y el segundo referido a las características del tratamiento farmacológico.
En relación a los critérios éticos, esta investigación fue aprobada por el Comité de Ética en Investigación (CEP) con Seres Humanos del Hospital Universitário Lauro Wanderley de la Universidad Federal de Paraíba, según Resolución Nº 1.332.125 e CAAE: 49793015.5.0000.5183.
3 RESULTADOS
Analizando el perfil sociodemográfico de los pacientes, el 58% (53) fueron del sexo
masculino. El 46% (42) tenían edades comprendidas entre 12 y 25 años, con una media de edad
de 27,59 y un rango de 12 a 50 años. Según la raza, el 65% (59) fueron de raza parda. En lo que se refiere al estado civil, predominaron los solteros 58% (53). En relación a la escolaridad, fue prevalente la baja escolaridad con enseñanza incompleta 42% (38). La mayoría de los entrevistados vivían con los padres (53%, 48) y solamente 2% (2) vivían con los hijos. Según la
ocupación declarada, la mayoría eran estudiantes 38% (35), y funcionarios públicos 2% (2)
Braz. J. of Develop., Curitiba, v. 6, n.5, p.29262-29274 may. 2020. ISSN 2525-8761
Tabla 1 - Características sociodemográficas de los pacientes con anemia falciforme atendidos en el centro de sangre João Pessoa/PB (2015 – 2016).
Características sociodemográficas Frecuencia
n % Sexo Masculino 53 58 Femenino 38 42 Edad (años) 12 – 25 42 46 26 – 35 31 34 36 – 45 12 13 46 – 55 06 7 Edad media 27,59 Raza declarada Blanca 12 13 Parda 59 65 Negra 20 22 Estado civil
Casado (a) o unión estable 38 42
Soltero (a) 53 58
Escolaridad
No alfabetizado 02 2
Básica incompleta 38 42
Básica completa 16 18
Enseñanza media incompleta 07 8
Enseñanza media completa 19 21
Superior incompleta 02 2 Superior completa 07 8 Vive con Padres 48 53 Esposo (a) 18 20 Solo (a) 03 3
Esposo (a) e hijos (as) 12 13
Hijo (a) 02 2 Otra persona 08 9 Ocupación Desempleado 14 15 Jubilado/amparo social 13 14 Funcionário Público 02 2
Funcionário empresa privada 08 9
Estudiante 35 38
Otros 19 21
Fuente: Brito MJN, Silva EO, Ramos P. Características del tratamiento farmacológico de pacientes con anemia falciforme tratados en el centro de sangre de João Pessoa, Paraíba, Brasil (2015-2016).
Braz. J. of Develop., Curitiba, v. 6, n.5, p.29262-29274 may. 2020. ISSN 2525-8761 Al investigar sobre la cantidad de medicamentos que los pacientes utilizaban para el control de su enfermedad, 73% (66) usaban de 4 a 6 fármacos diariamente, y 27% (25) de 1 a 3 medicamentos.
Los grupos farmacológicos más utilizados por los pacientes fueron los analgésicos y vitaminas 100% (91), seguido de los agentes antineoplásicos 53%(48) y anti-inflamatórios 34,6% (31). El antidepresivo y anticonvulsivante Lamotrigina, fue utilizado solamente por dos pacientes. La mayor prevalencia se presentó con el uso de ácido fólico y dipirona 100% (91)
(Tabla 2).
Tabla 2 - Grupo farmacológico y medicamentos utilizados por los pacientes con anemia falciforme atendidos en el centro de sangre de João Pessoa/PB (2015 – 2016).
Grupo farmacológico Nombre del medicamento Frecuencia
n %
Analgésicos Celecoxibe, Codeína,
Dipirona, Morfina, Paracetamol, Tramadol 91 100 Antibióticos Amoxicilina, Benzetacil, Pen ve oral 09 10 Vitaminas Ácido Ascórbico Ácido fólico Complexo B 91 100
Anti-inflamatorios Diclofenaco,Ibuprofeno 31 34
Antiplaquetário Ácido Acetilsalicílico, Cilostazol 20 22
Agente quelante de hierro Deferasirox 14 15
Anti-hipertensivo Enalapril,Ramipril, Succinato de metoprolol 02 2
Anticoagulante Enoxaparina 03 3
Anticonvulsivo Fenobarbital 04 4
Agente Antineoplásico Hydrea® (Hidroxiureia) 48 53
Hipoglicemiante Insulina 03 3
Antidepresivo e
Anticonvulsionante Lamotrigina 01 1
Antiulceroso Omeprazol 04 4
Fuente: Brito MJN, Silva EO, Ramos P. Características del tratamiento farmacológico de pacientes con anemia falciforme tratados en el centro de sangre de João Pessoa, Paraíba, Brasil (2015-2016).
En lo que se refiere al perfil farmacológico, de los 91 pacientes, 53% (48) utilizaban el agente antineoplásico Hydrea® (Hidroxiureia) (Tabla 3).
Braz. J. of Develop., Curitiba, v. 6, n.5, p.29262-29274 may. 2020. ISSN 2525-8761
Tabla 3 – Perfil farmacológico del uso de Hydrea® (Hidroxiureia) utilizados por los pacientes con anemia falciforme atendidos en el centro de sangre de João Pessoa/PB (2015–2016).
Variables Frecuencia
n %
Utiliza Hydrea® (Hidroxiureia)
Si 48 53
No 43 47
Recibe orientación médica de como utilizar el medicamento
Si 48 53
No 00 0
Sabe porque está tomando el medicamento
Si 48 53
No 00 0
Fuente de información sobre el medicamento**
Orientación médica 48 53
Orientación farmacéutica 48 53
La prescripción del medicamento 30 63
Dejo de usar alguna vez el medicamento
Si 18 38
No 30 63
Dificultad en relación al uso del medicamento***
Adquirir el medicamento 09 19
Adaptarse a los horarios 07 15
Recordarse de tomarlo 15 31
Efectos adversos 20 42
No tienen dificultad 15 31
Fuente: Brito MJN, Silva EO, Ramos P. Características del tratamiento farmacológico de pacientes com anemia falciforme tratados en el centro de sangre de João Pessoa, Paraíba, Brasil (2015-2016).
* Las categorías estudiadas se expresaron como frecuencia (n) y porcentaje (%), caracterizando a la población en cuanto al perfil farmacoterapéutico; ** cantidad de pacientes que usan medicamentos; *** el paciente dio más de una respuesta.
En cuanto a las principales manifestaciones clínicas presentadas por los enfermos con AF, resalta las crisis alérgicas 89% (81) (Tabla 4).
Braz. J. of Develop., Curitiba, v. 6, n.5, p.29262-29274 may. 2020. ISSN 2525-8761
Tabla 4 – Antecedentes mórbidos personales presentados por los pacientes antes y durante el tratamiento con anemia falciforme tratados en el centro de sangre de João Pessoa/PB (2015 – 2016).
Principales problemas de salud y manifestaciones clínicas presentadas antes y durante el tratamiento
Frecuencia Antes Durante n % n % Crisis dolorosas 81 89 58 64 Insuficiencia respiratoria 20 22 18 20 Priapismo 11 12 06 7 Úlcera maleolar 14 15 09 10
Accidente Vascular Encefálico 06 7 02 2
Deformidad en el cuadril 01 1 00 0 Deformidad en el femúr 05 5 05 5 Pneumonia 06 7 03 3 Depresión 12 13 10 11 Colecistectomia 15 16 03 3 Esplenomegalia 09 10 01 1 Cansancio 15 16 12 13 Diabetes 02 2 02 2 Infección urinaria 06 7 02 2 Cardiomegalia 04 4 04 4 Fiebre reumática 05 5 05 5 Soplo cardíaco 04 4 04 4 Tuberculosis 01 1 01 1 Dactilitis 02 2 02 2
Fuente: Brito MJN, Silva EO, Ramos P. Características del tratamiento farmacológico de pacientes con anemia falciforme tratados en el centro de sangre de João Pessoa, Paraíba, Brasil (2015-2016).
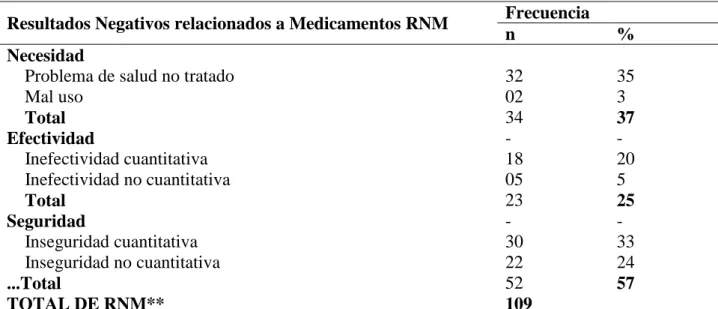
En lo que refiere a los RNMs utilizados durante la fase de evaluación, mencionaremos
los problemas de salud no tratados 35% (32), la falta de efectividad terapéutica (inefectividad
Braz. J. of Develop., Curitiba, v. 6, n.5, p.29262-29274 may. 2020. ISSN 2525-8761
Tabla 5 – Clasificación de los resultados negativos relacionados a medicamentos en los pacientes con anemia falciforme atendidos en el centro de sangre de João Pessoa/PB (2015–2016).
Resultados Negativos relacionados a Medicamentos RNM Frecuencia
n %
Necesidad
Problema de salud no tratado 32 35
Mal uso 02 3 Total 34 37 Efectividad - - Inefectividad cuantitativa 18 20 Inefectividad no cuantitativa 05 5 Total 23 25 Seguridad - - Inseguridad cuantitativa 30 33 Inseguridad no cuantitativa 22 24 ...Total 52 57 TOTAL DE RNM** 109
*As categorias estudadas foram expressas na forma de frequência (n) e porcentagem (%), caracterizando a população quanto ao perfil farmacoterapêutico; **paciente deu mais de uma resposta.
4 DISCUSIÓN
En el presente estudio, la enfermedad fue más prevalente en el sexo masculino, difiriendo con los resultados de Marques (2011) y Felix et al. (2010), donde la enfermedad fue más prevalente en el sexo femenino. Esta diferencia podría estar relacionada al tamaño de muestra utilizada (MARQUES M, 2011; FELIX AA, et al, 2010). Sin embargo, en los estudios realizados por Platt OS et al. (1994) la prevalencia fue mayor en pacientes con el sexo masculino, coincidiendo con estos resultados. Existen pocos estudios que indiquen que la variable sexo contribuya para la aparición de esta enfermedad al ser la AF una enfermedad genética y no relacionada al sexo.
En relación a la edad, los datos aquí presentados son coincidentes con la literatura, en lo que se refiere al predominio de esta enfermedad en la población joven económicamente activa (18 a 30 años) (PLATT OS, 1994; MARQUES M, 2011; FELIX AA, et al, 2010). En este estudio, el rango de edad fue mayor que el descrito en la literatura, ya que se incluyeron pacientes menores de 18 años y mayores de 30, o sea e 12 a 35 años.
Analizando por etnia, el 65% de los pacientes se declararon pardos. Este resultado diverge de otras investigaciones, donde esta enfermedad fue más prevalente en pacientes de raza negra (FELIX AA, et al, 2010; CAVALCANTI JM e MAIO MC, 2011). Aunque la AF sea más prevalente en individuos con fenotipo más africanizado, la misma también se encuentra presente
Braz. J. of Develop., Curitiba, v. 6, n.5, p.29262-29274 may. 2020. ISSN 2525-8761 en pacientes sin ninguna de estas características, esto es debido a la gran heterogeneidad de la población brasilera (FRY PH, 2005; CAVALCANTI JM e MAIO MC, 2011)
En lo que se refiere a la terapia medicamentosa, los medicamentos más utilizados son el ácido fólico y la dipirona, ambas drogas utilizadas por todos los pacientes. Estos datos confirman los resultados obtenidos en otras investigaciones (LOGGETTO SR, et al., 1999; MOUSINHO-RIBEIRO RC, et al., 2008; NAOUM PC, 2014). Según la Agencia Nacional de Vigilancia Sanitaria (ANVISA) Brasil (2018), el ácido fólico es un medicamento que debe ser de uso continuo en todo paciente con AF con el fin de mejorar la eritropoyesis. La dipirona es el analgésico de primera elección utilizado en caso de dolor debido a su potencial analgésico y efectos colaterales menores (WEATHERALL DJ e CLEGG JB, 2001; CANÇADO RD e JESUS JA, 2007; BRASIL, 2018). La tercera droga más utilizada es la Hydrea® (Hidroxiureia) con 53% de adhesión por parte de los pacientes. Este medicamento constituye una droga antineoplásica, única opción terapéutica de la AF, por su capacidad de reducir las crisis mejorando así la calidad de vida de los pacientes (WEATHERALL DJ e CLEGG JB, 2001; BRASIL, 2018).
El 47% de los entrevistados, no adhieren la Hidroxiureia, siendo la única opción terapéutica de la AF, según la Portaria nº 55 del 29 de enero de 2010 (BRASIL, 2018). Estos resultados son compatibles con el estudio realizado por Dantas et al (2012), en la cual 57% relataron también no utilizar el medicamento propuesto. La baja adhesión a la farmacoterapia, aumenta el riesgo de complicaciones.
El 26% de los entrevistados no presentan adhesión a la medicación por encontrarse dentro de los criterios de inclusión, pues sienten poco dolor (tienen crisis dolorosas con menor intensidad), lo cual constituye uno de los dos criterios de acuerdo con el Protocolo Clínico y Directrices Terapéuticas de la AF.
El 23% de los pacientes decidieron, por cuenta propia no usarlo, por ser un medicamento imunosupresor temiendo las reacciones adversas. Dos pacientes relataron ganas de usar la Hidroxiureia, pero no podían. El primero; por problemas hepáticos y el segundo por poseer aplasia medular. El 47% comenzaron a utilizar, pero se sintieron mal y abandonaron el tratamiento. En cuanto al 53% que se adhieren al tratamiento, solamente tres individuos decidieron continuar aún con las crisis, relatando posteriormente mejoras importantes.
El 19% de los pacientes relataron tener dificultades para adquirir el medicamento. Estas cifras son mucho menores al 36,6% de lo relatado por Dantas et al., (2012). Además de eso,
Braz. J. of Develop., Curitiba, v. 6, n.5, p.29262-29274 may. 2020. ISSN 2525-8761 aproximadamente, 31% presentaron problemas para recordar tomar la medicación. Estas cifras son semejantes a los 13% mencionados por el mismo autor.
Fue observado que el problema de salud más frecuente en los pacientes con AF fueron las crisis dolorosas, con una intensidad de leve a muy fuerte y una prevalencia del 89% antes del acompañamiento y del 64% después del acompañamiento, similar a la investigación realizada por Marques (2011), con crisis alérgicas en 83% de los pacientes antes del acompañamiento.
De entre todos los factores relacionados a las RNMs, los más frecuentes fueron aquellos que tenían que ver con la seguridad y la necesidad. En este grupo, la principal fue el problema
de salud no tratado 35% (32). Estos valores son mayores a los resultados encontrados por
Machado VP et al. (2013) y Marques (2011) que encontraron valores del 8,41% e 25%.
La inefectividad cuantitativa encontrada en el presente estúdio fue inferior al trabajo realizado por Machado VP et al. (2013), quienes obtuvieron resultados del 67,32%. La
inseguridad no cuantitativa 33% es semejante a los resultados encontrados por Machado VP et
al. (2013) de 42,9%. Sin embargo, Victório CJM et al. (2008) encontró apenas 6% de este tipo de inseguridad.
Las 109 repeticiones de RNM, se deben a que un mismo paciente pudo haber dado más de una respuesta. Estos resultados, son similares a los resultados encontrados por Hernanz BC (2007) de 90 RNM, mientras que en el trabajo de Marques (2011), este solo encontró 12 RNM. Estas diferencias podrían deberse a que en el estudio de Marques (2011), este trabajo con una muestra más pequeña.
5 CONCLUSIÓN
En los pacientes com AF tratados se observa problemas de salud no tratados, falta de efectividad terapeutica y toxicidad, por lo que es necesario el monitoreo permanente del tratamiento farmacológico recibido por estos pacientes.
CONFLICTOS DE INTERESES
Los autores declaran no tener conflictos de intereses.
CONTRIBUCIÓN DE LOS AUTORES
Todos los autores contribuyeron a la idealización del estudio, el análisis e interpretación de los datos y a la redacción del manuscrito, aprobando la versión final publicada. Se declaran responsables del artículo en su totalidad, garantizando su precisión e integridad.
Braz. J. of Develop., Curitiba, v. 6, n.5, p.29262-29274 may. 2020. ISSN 2525-8761
REFERÊNCIAS
BRASIL. Ministério da Saúde (BR). Agência Nacional de Vigilância Sanitária ANVISA. Manual de diagnóstico e tratamento de doenças falciformes. Brasília (DF): Ministério da Saúde, 2002. 142p.
BRASIL. Ministério da Saúde (BR). Portaria nº55/ GM/MS de 29 de janeiro de 2010, que aprova o Protocolo Clínico e Diretrizes Terapêuticas – Doença falciforme Brasília, DF. Ministério da Saúde, 2016.
BRASIL. Ministério da Saúde (BR). Secretaria de atenção à saúde secretaria de ciência, tecnologia e insumos estratégicos. Portaria conjunta nº 05, de 19 de fev. de 2018. Aprova o protocolo Clínico e Diretrizes Terapêuticas da Doença Falciforme.
CANÇADO RD, JESUS JA. A doença falciforme no Brasil. Rev. Bras. Hematol. Hemoter. v. 29, n.3, p.204-206, 2007.
CAVALCANTI JM, MAIO MC. Entre negros e miscigenados: a anemia e o traço falciforme no Brasil nas décadas de 1930 e 1940. História, Ciências, Saúde – Manguinhos, Rio de Janeiro v.18, n.2, p.377-406, 2011.
CORRER CJ, ROSSIGNOLI P, SOUZA RAP et al. Perfil dos farmacêuticos e indicadores de estrutura e processo em farmácias de Curitiba – Brasil. Segmento Farmacoterapêutico. v. 2, n. 1, p. 37-45, 2004.
FELIX AA, SOUZA HM, RIBEIRO SBF. Aspectos epidemiológicos e sociais da doença falciforme. Rev. Bras. Hematol. Hemoter. v. 32, n.3, p.203-208, 2010.
FRY PH. O significado da anemia falciforme no contexto da “política racial” do Governo Brasileiro 1995-2004. História, Ciências, Saúde – Manguinhos, v. 12, n. 2, p. 374-70, maio-ago. 2005.
GÓMEZ-CHIARI M, PUIGBERT JT, ARAMBURU JO. Drepanocitosis: Experiência de un centro. Annales de Pediatria, v. 58, nº 2, p. 95-99, 2003.
HERNÁNDEZ DS, CASTRO MMS, DÁDER MJF. Método Dáder Manual de Seguimento Farmacoterapêutico. Terceira edição; versão em português, 2014.
HERNANZ BC. Detección Resultados Negativos Asociados a la Medicación de Pacientes de la Unidad de Observación del Área de Urgencias. 2007. 191 f. Tese (Doutorado) - Curso de Farmácia, Universidade de Granada, Espanha, 2007.
JUNIOR AF. Indicação de Transfusão e Sobrecarga de Ferro na Doença Falciforme. In: Ivo ML. Hematologia: um olhar sobre a doença falciforme. Campo Grande: Ed. UFMS, p. 14-20, 2013.
LEITE SN. Adesão à Terapêutica Medicamentosa: o que o Farmacêutico tem a ver com isso? In: Cordeiro BC, Leite SN. O Farmacêutico na atenção à Saúde. 2ª Ed., Itajaí, Univali, 2008.
Braz. J. of Develop., Curitiba, v. 6, n.5, p.29262-29274 may. 2020. ISSN 2525-8761 LOGGETTO SR, PELLEGRINI-BRAGA J, COSTA-CARVALHO BT et al. Alterações imunológicas em pacientes com Anemia Falciforme. Revista Brasileira de Alergia e Imunopatologia, v.22, n.3, p.77-82, 1999.
MACHADO VP, COELHO FC, GARBINATO LR Identificação de Resultados Negativos aos Medicamentos em pacientes hipertensos. Interbio v.7 n.2 ISSN 1981-3775, 2013.
MARQUES M. Desenvolvimento de um modelo de atenção farmacêutica para pacientes portadores de anemia falciforme. 2011. 89 f. Trabalho de conclusão de curso (Farmácia-Bioquímica) - Universidade Estadual Paulista, Faculdade de Ciências Farmacêuticas, 2011.
MOUSINHO-RIBEIRO RC, CARDOSO GL, SOUSA IEL et al. Importância da avaliação da hemoglobina fetal na clínica da anemia falciforme. Rev. Bras. Hematol. Hemoter. 2008, vol.30, n.2, pp.136-141.
NAOUM PC, Naoum FA. Doença das células falciformes. 1ª ed. São Paulo: Savier; 2014. PINTO LH, SCHULTER LS. SIERTH R et al. O uso racional de medicamentos no Brasil dentro da Assistência Farmacêutica e suas implicações no presente. Revista Eletrônica de Farmácia, v. XII n. 1, p. 27–43, 2015.
PLATT OS, BRAMBILLA DJ, ROSSE WF, et al. Mortality in sickle cell disease – Life expectancy and risk factors for early death. New England Journal of Medicine, v. 330, n. 23, p. 639-1640, 1994.
SANTOS JL, CHIN CM. Anemia Falciforme: desafios e avanços na busca de novos fármacos. Química Nova, v. 35, n. 4, p.783-790, 2012.
SOLER O, ROSA MB, FONSECA AL et al. Assistência farmacêutica clínica na atenção primária à saúde por meio do programa saúde da família. Rev. Bras. Farm. v. 9, n. 1, p.37-45. 2010.
TOSTES MA, BRAGA JAP, LEN CA. Abordagem da crise dolorosa em crianças portadoras de doença falciforme, Revista de Ciências Médicas, Campinas, v.18, n.1, p.47-55, jan./fev., 2009.
VICTÓRIO CJM, CASTILHO SR, NUNES PHC. Identificação de potenciais problemas relacionados com medicamentos a partir da análise de prescrições de pacientes hipertensos.
Revista Brasileira de Farmácia, v. 89, n. 3, p. 233-235, 2008.
WEATHERALL DJ, CLEGG JB. Inherited haemoglobin disorders: an increasing global health problem. Bulletin of the World Health Organization, 2001;79(8):704-12
ZAGO MA, PINTO ACS. Fisiopatologia das doenças falciformes: da mutação genética à insuficiência de múltiplos órgãos. Rev. Bras. Hematol. Hemoter, v.29 n.3, p.207-214, 2007.