PROGRAMA DE PÓS-GRADUAÇÃO EM ENGENHARIA QUÍMICA
KELLY CRISTINA DOS SANTOS TEIXEIRA
ESTUDO DE COMPOSIÇÃO E ESTABILIDADE EM
EMULSÕES FORMULADAS A PARTIR DE ÓLEOS
LUBRIFICANTES VEGETAIS
T264e Teixeira, Kelly Cristina dos Santos
Estudo de estabilidade e composição em emulsões formuladas a partir de óleos lubrificantes vegetais / Kelly Cristina dos Santos Teixeira, 2008. 103 f. ; il. color. enc.
Orientador: Prof. Dr. Célio Loureiro Cavalcante Júnior Co-orientador: Prof. Dr. Horiberto Batista de Sant’Ana Área de concentração: Processos Químicos e Bioquímicos
Dissertação (mestrado) - Universidade Federal do Ceará, Centro de Tecnologia. Depto. de Engenharia Química, Fortaleza, 2008.
ESTUDO DE COMPOSIÇÃO E ESTABILIDADE EM
EMULSÕES FORMULADAS A PARTIR DE ÓLEOS
LUBRIFICANTES VEGETAIS
Dissertação de Mestrado submetida à Coordenação do Curso de Pós-Graduação em Engenharia Química, da Universidade Federal do Ceará, como requisito parcial para a obtenção do título de Mestre em Engenharia Química.
.
Orientadores:
Kelly Cristina dos Santos Teixeira
ESTUDO DE COMPOSIÇÃO E ESTABILIDADE EM
EMULSÕES FORMULADAS A PARTIR DE ÓLEOS
LUBRIFICANTES VEGETAIS
Dissertação submetida à Coordenação do Curso de Pós-Graduação em Engenharia Química da Universidade Federal do Ceará, como requisito parcial para a obtenção do título de Mestre em Engenharia Química. Área de concentração Processos Químicos e Bioquímicos.
À Jeová Deus.
À minha família, meus pais, meu irmão Mendes, minha cunhada Iana, minha irmã de coração Rose e minha querida avó Tereza, pelo amor e por confiarem no meu sucesso. Em especial, quero agradecer a minha mãe Loelia por seu amor incondicional me encorajando a conquistar até o que parecia impossível. Esse amor é o alicerce da minha vida.
Aos meus padrinhos, Lídio e Eliane, por serem, também, responsáveis por esta conquista. Meu respeito, admiração e eterno agradecimento.
Aos meus queridos primos e amigos, Roberto, Daniele, Eliziana, Fabíola, Rebeca e seu noivo Sebastião, pelos momentos descontraídos e pela amizade que temos. É muito importante saber que tenho vocês em minha vida.
Ao meu amigo e companheiro Cristiano, pelos importantíssimos conselhos, pela paciência em me escutar todas as vezes que precisei, por me dizer tantas vezes que eu conseguiria e que tudo daria certo e por seu amor. Tudo isso foi fundamental pra que eu chegasse até aqui. Á você, meu querido, meu muito obrigada!
À minha amiga querida Izabelly, por tudo que significou pra mim em todos esses anos de amizade. Por seus conselhos, sua força, sua lealdade e por seu exemplo de vida. Obrigada por tudo, minha grande, inesquecível, eterna, admirável e amada amiga.
Ao meu precioso amigo Edilson, pelos momentos maravilhosas que passamos juntos, por seu carinho, sua consideração, sua amizade, seu humor inteligente, sua paciência e seu carisma. Sempre terei você em meus pensamentos onde quer que estejamos.
agradecimentos.
Ao meu orientador Prof. Dr. Hosiberto Batista de Sant’Ana, pela orientação, por ter me acompanhado esses dois anos e pela amizade que temos. Meu muito obrigada!
Ao Prof. Dr. Marciano de Lucena Neto, por ter sido como um orientador pra mim, por sua ajuda que surgiu no momento que mais precisei, pelo conhecimento transmitido e por ter me ajudado com humildade e competência. Meu enorme agradecimento.
As professoras do Programa, Andréa Lopes e Luciana Rocha, pela atenção, pelas dúvidas esclarecidas e claro pelo conhecimento transmitido.
Ao prof. Dr. Rinaldo dos Santos, pelo empréstimo do viscosímetro e pelas análises realizadas no CEFET-CE
À minha “eterna” bolsista Kerolaine, pela ajuda com os experimentos e pelas gargalhadas nos descontraindo quando a “coisa” ficava difícil.
À colega de mestrado Juliana Rabelo, pelo trabalho realizado com os biossurfactantes e por sua disponibilidade em tirar minhas dúvidas.
Ao grupo GPSA, em especial ao Estelio, por ter estado sempre disposto a me ajudar.
As secretárias da ANP, Michelle e Jôse, por sempre me ajudarem quando precisei.
À secretária da Pós-Graduação Maria, pelo apoio e ajuda em toda parte burocrática do mestrado.
À ANP, pelo bolsa concedida.
O objetivo deste trabalho foi a obtenção de novas formulações de emulsões a partir de óleos vegetais lubrificantes (biolubrificante) do tipo éster de poliol com o intuito de fornecer base científica para o desenvolvimento de futuras formulações de fluidos de corte “emulsionáveis”. Através da construção de diagramas de fases e utilizando o conceito de BHL, fez-se a escolha do melhor sistema emulsionado, levando-se em consideração os aspectos principais relacionados à concentração de surfactante, de fase aquosa e fase oleosa. Inicialmente, foi realizado um estudo preliminar para seleção do melhor blend surfactante e melhores valores
de BHLs que produzissem emulsões com boa qualidade em termos de altura da fase inferior em % , AFD(%), e aspecto visual. O blend surfactante S40/T80 e os valores de BHL 9,10, 11 e
12 produziram os melhores resultados. Foram construídos diagramas representativos para o sistema blend S40/T80-água-biolubrificante empregando estes valores de BHL (9, 10, 11 e
12). O sistema emulsionado que apresentou a maior região de emulsão estável foi o que empregou o BHL 10. Após esta determinação foi realizado um planejamento experimental do tipo rede “Scheffé” com o interesse de estabelecer a melhor localização dentro da região de estabilidade que apresentassem as melhores condições para futuras formulações de fluidos “emulsionáveis”. As variáveis estudadas foram fração mássica da fase aquosa, fração mássica da fase oleosa e fração mássica de blend surfactante. A resposta analisada foi a viscosidade.
Verificou-se que a fração mássica do blend surfactante apresentou maior efeito sobre a
resposta viscosidade em relação às outras variáveis. Através da análise das curvas de isorespostas, verificou-se que para obter-se emulsões a base de biolubrificante com menores valores de viscosidade, as formulações devem ser realizadas com percentuais desurfactantes abaixo de 10%, sendo que os percentuais de fase aquosa devem estar no intervalo aproximado de 60% a 75% e os percentuais de fase oleosa devem estar no intervalo aproximado de 20% e 35%.
This dissertation aimed to get new formulation of emulsions from vegetable lubricants (biolubricants) as poliol ester to give scientific base to development of future formulation of cutting fluids. Through the construction of phases diagrams and using the HLB concept, it chose the better emulsion system, had thought the main points like percentage of surfactant blend, percentage of aqueous phase and percentage of oil phase. In the begging was realized a preliminary study to selection the better surfactant blend and better HLB that produced high stability emulsion. The stability was evaluated by the inferior phase size in % and visual aspect. The surfactant blend S40/T80 and the HLBs 9, 10, 11 e 12 produced the better results. It was made diagrams to represent the system surfactant blend S40/T80-biolubricant-water using this HLBs (9, 10, 11 e 12). The system that presented the bigger region of stable emulsion was the system that was made using HLB 10. After this determination, a experimental planning “Scheffé” net was realized to establish the better localization inside stable region that presented the better conditions to future formulation of cutting fluids. The variables percentage of surfactant blend, percentage of aqueous phase and percentage of oil phase was investigated. Viscosity was a response studied. The percentage of surfactant blend was the most statistically significant response on viscosity. The analysis of iso-responses curves showed that to obtain the emulsion from biolubricants with lower viscosity the formulation should be made with percentage of surfactant below 10%, percentage of aqueous phase between 60% and 75% and percentage of oil phase between 20% and 35%.
LISTA DE FIGURAS
FIGURA 2.1 Estrutura típica de um óleo vegetal e seus pontos críticos de instabilidade
indicando a presença de duplas ligações e hidrogênio ... .6
FIGURA 2.2 Reação de Transesterificação para síntese de ésteres lubrificantes lubrificantes...7
FIGURA 2.3 Éster de Trimetilopropano...7
FIGURA 2.4 Representação de uma molécula surfactante surfactante...9
FIGURA 2.5 Fenômenos de formação das micelas...13
FIGURA 2.6 Diagrama de fase de um surfactante iônico próximo ao ponto de Kraft..14
FIGURA 2.7 Diagrama de fase de um surfactante não iônico em água... 15
FIGURA 2.8 Fotografias de Emulsões...19
FIGURA 2.9 Estrutura representativa dos dois tipos de microemulsões...22
FIGURA 2.10 Diagrama ternário, mostrando a zona de microemulsão em um sistema de três constituintes...24
FIGURA 2.11 (a) Titulação com fase aquosa; (b) representação dos pontos de titulação e regiões do diagrama de fases...25
FIGURA 2.12 Diagrama de fases quaternário, mostrando a zona de microemulsão... ...26
FIGURA 2.13 Diagramas pseudoternário com relação tensoativo/cotensoativo constante...26
FIGURA 2.14 Diagramas pseudoternário com relação água/tensoativo constante...27
FIGURA 2.15 Representação gráfica da matriz de experiência...29
FIGURA 3.1 Representação esquemática das etapas de realização do trabalho...33
FIGURA 3.2 Preparo da emulsão em um desemulsibilizador...35
FIGURA 3.3 Ilustração da fase inferior...35
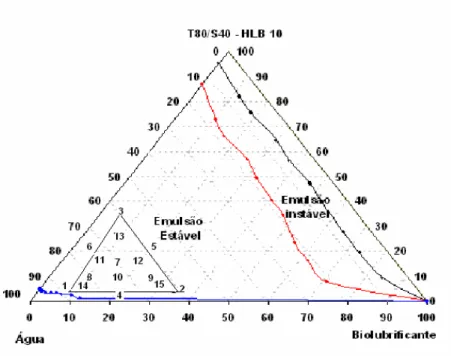
FIGURA 3.4 Representação da “Rede Scheffe” para o sistema água-biolubrificante-Blend T80/S40 BHL 10... ...42
água destilada, blend S40/T80...53
FIGURA 4.4 Diagrama ternário representativo do sistema Biolubrificante - Sabão de Mamona - Água...56
FIGURA 4.5 Diagrama peudoternário representativo do sistema óleo mineral naftênico (NH-20), água destilada, blend S20/T20 BHL 12...58
FIGURA 4.6 Rede Scheffé representativa dos pontos experimentais...61
FIGURA 4.7 Diagrama de Pareto indicando o efeito na viscosidade da emulsão formulada a partir de biolubrificante para o Planejamento experimental rede Scheffé...63
FIGURA 4.8 Gráfico de resíduos versus valores preditos pelo modelo polinomial de 1o ordem para viscosidade da emulsão...65
FIGURA 4.9 Curvas de Isorespostas representativas do comportamento da viscosidade na região de emulsão estável...66
FIGURA 4.10 Atividades emulsificantes de emulsões a base de óleo lubrificante e n-hexadecano para os experimentos realizados...69
FIGURA 4.11 Gráfico de estabilidade de emulsão referente ao experimento 1...70
FIGURA 4.12 Gráfico de estabilidade de emulsão referente ao experimento 2...71
LISTA DE TABELAS
TABELA 2.1 Métodos para identificar o tipo de emulsão...17
TABELA 2.2 Características de Emulsões e Microemulsões...23
TABELA 3.1 Caracterização físico-química do biolubrificante e do óleo mineral NH-20 segundo as normas da ASTM...31
TABELA 3.2 Nome comercial e nomenclatura química dos surfactantes testadas...32
TABELA 3.3 Nomenclatura Química e BHL dos tipos de Tween e Span usados na composição dos blend....37
TABELA 3.4 Percentual dos surfactantes requeridos na preparação de vários pares Tween/Span na faixa de BHL de 9 a 14...38
TABELA 3.5 Matriz Experimental...42
TABELA 4.1 Aspecto Visual e altura da fase inferior em % de emulsões obtidas a partir de 14 surfactantes comerciais...46
TABELA 4.2 Resultados do planejamento experimental rede Scheffé...61
TABELA 4.3 Estimativa dos efeitos principais na viscosidade da emulsão formulada a partir de biolubrificante...62
TABELA 4.4 ANOVA para analise de viscosidade da emulsão...65
TABELA 4.5 Constantes de Decaimento...72
LISTA DE QUADROS
SÍMBOLOS GREGOS
Tensão interfacial Excesso de superfície
RESUMO... vii
ABSTRACT... viii
LISTA DE FIGURAS... ix
LISTA DE TABELAS... xii
LISTA DE QUADROS... xiv
SÍMBOLOS GREGOS... xv
1. Introdução.... 1
2. Revisão Bibliográfica... 4
2.1. Biolubrificantes... 4
2.2. Aspectos gerais sobre os surfactantes... 8
2.2.1. Classificação... 9
2.2.2. Propriedades... 9
2.2.3. Balanço Hidrofílico-Lipofílico (BHL)... 10
2.2.4. Micelização... 12
2.2.5. Biossurfactantes... 15
2.3. Emulsão... 16
2.3.1. Teoria da formação de uma emulsão... 17
2.3.2. Parâmetros de estabilidade... 19
2.3.3. Fenômenos associados a instabilidade... 20
2.3.4. Microemulsões... 22
2.4. Diagramas de Fases... 24
2.5. Planejamento Experimental... 27
3. Materiais e Métodos... 29
3.1. Materiais... 29
3.1.1. Constituintes dos Sistemas... 29
3.2. Métodos... 31
3.2.1. Preparação do Sabão de Mamona... 33
3.2.2. Testes Preliminares para Seleção do Tipo de Surfactante... 33
3.2.6. Construção dos Diagramas de Fases... 37
3.2.7. Planejamento Experimental... 39
3.2.8. Estudo de estabilidade em meio de cultura contendo biossurfactante... 42
4. Resultados e Discussões... 44
4.1. Seleção Prévia do Surfactante Comercial... 44
4.2. Determinação dos melhores blends surfactantes e da faixa de BHL adequada... 47 4.3. Determinação das zonas de estabilidade a partir dos diagramas ternários... 49 4.3.1. Influência do BHL... 50
4.3.2. Efeito surfactante do sabão de mamona... 54
4.3.3. Influência da fase oleosa e do blend surfactante... 56
4.4. Definição do melhor sistema emulsionado... 58
4.5. Análise dos principais parâmetros que influenciam na viscosidade do sistema selecionado... 59 4.5.1. Curvas de Isorespostas para a viscosidade da emulsão... 65
4.6. Estudo de estabilidade em meio de cultura produtor de biossurfactante... 67
4.6.1. Atividade Emulsificante e Estabilidade de Emulsões... 67
4.6.2. Índice de Emulsificação....... 71
5. Conclusões ... 73
6. Referências Bibliográficas... 76
ANEXO... 81
ANEXO A... 81
Estudo e Composição e Estabilidade em Emulsões formuladas a partir de óleos Lubrificantes vegetais
1. INTRODUÇÃO
Este trabalho insere-se em uma linha de pesquisa que vem sendo desenvolvida
no Laboratório de Combustíveis e Lubrificantes do Departamento de Engenharia
Química, que, em parceria com o Projeto Rede de Combustíveis e Lubrificantes Fase 2,
visa o desenvolvimento de formulações de fluidos industriais especiais a partir de óleos
vegetais. Especificamente neste trabalho, concentrou-se no desenvolvimento de fluidos
de corte do tipo emulsionáveis
Uma das definições para fluidos de corte “emulsionáveis” diz que estes são
dispersões de óleo em água acompanhado pelo uso de surfactantes e aditivos (Skold e
Misra, 2000 citado por Guimarães, 2006). Estes fluidos são largamente utilizados em
operações de corte em metais, especialmente nas indústrias metal-mecânica, com a
finalidade de resfriar e lubrificar a região de contato entre a peça e a ferramenta de
corte.
A fase oleosa que entra na composição das emulsões pode ser do tipo mineral ou
vegetal. Devido à crescente preocupação com os impactos ambientais causados pelos
lubrificantes derivados do petróleo, a utilização de óleos biodegradáveis como os
lubrificantes vegetais (biolubrificantes) no processo de obtenção de fluidos de corte
emulsionáveis torna-se uma importante alternativa, reduzindo significativamente os
impactos ambientais e custos relacionados à destinação adequada da base oleosa usada.
Biolubrificantes são, em sua maioria, ésteres obtidos a partir de triglicerídeos
vegetais, ou até mesmo biodiesel, por rota química ou enzimática. Apresentam a
principal vantagem de serem biodegradáveis, partem de fontes renováveis, não são
tóxicos e apresentam um alto valor agregado. São obtidos por diferentes processos que
visam diminuir sua instabilidade térmica, hidrolítica e oxidativa, provenientes das
duplas ligações e dos hidrogênios β existentes nas estruturas dos óleos vegetais dos
quais se originam. Os diésteres e os ésteres de poliol são exemplos de biolubrificantes
produzidos a partir da reação de transesterificação entre ésteres vegetais e álcoois e
Estudo e Composição e Estabilidade em Emulsões formuladas a partir de óleos Lubrificantes vegetais
Para estabilização da emulsão faz-se necessário o uso de um agente
emulsificante que é responsável pela formação de um filme adsorvido, diminuindo a
tensão interfacial entre as fases imiscíveis, conferindo assim estabilidade ao sistema. A
escolha do surfactante pode ser feita a partir de um balanço semi-empírico que
determina o seu caráter hidrofílico ou lipofílico, denominado Balanço
Hidrofílico-Lipofílico (BHL) e é importante para a orientação do tipo de sistema a ser preparado. A
representação gráfica dos sistemas emulsionados a três constituintes
(água+óleo+surfactante) pode ser feita num diagrama triangular, mostrando as zonas de
emulsões estáveis, chamados diagramas de fases.
A construção de diagramas de fases, juntamente com o conceito de BHL,
auxiliaram neste trabalho a estudar as regiões de estabilidade para diferentes sistemas
emulsionados. Além disso, pode-se, a partir de um planejamento experimental,
determinar, dentro da região de estabilidade, pontos ótimos para formulações de fluidos
de corte.
Diante do que foi exposto acima, decidiu-se realizar neste trabalho um estudo de
composição e estabilidade de emulsões formuladas a partir de lubrificante
biodegradável do tipo éster de poliol, por intermédio da construção de diagramas de
fases e utilizando o conceito de BHL para escolha do sistema de melhor estabilidade,
com o interesse de fornecer base científica para desenvolvimento de futuras
formulações de fluidos de corte “emulsionáveis”. Para isso, foi proposto:
Formular emulsões a partir de óleos lubrificantes vegetais.
Estudar e otimizar os métodos de preparação destas emulsões.
Selecionar a classe de surfactantes mais adequada para preparação destas
emulsões.
Caracterizar as emulsões obtidas através de medidas físicas, tais como
volume de separações de fases e viscosidade.
Estudar a estabilidade destas emulsões através do levantamento do seu
perfil de viscosidade com o tempo.
Determinarmos os melhores sistemas emulsionados a partir da
Estudo e Composição e Estabilidade em Emulsões formuladas a partir de óleos Lubrificantes vegetais
Aplicar procedimentos de modelagem e otimização estatística para
processo de formulações das emulsões que servirão como base para
Estudo da Composição e Estabilidade em Emulsões formuladas a partir de óleos Lubrificantes vegetais
2. REVISÃO BIBLIOGRÁFICA
No presente capítulo faremos uma abordagem teórica sobre os aspectos relevantes no
desenvolvimento deste trabalho, mostrando alguns conceitos básicos e definições
fundamentais ao entendimento do processo de formulações de emulsões, visando facilitar a
compreensão dos resultados.
2.1. Biolubrificantes
Os biolubrificantes em geral são ésteres similares aos triglicerídeos naturais e
biodegradáveis (Bondioli et al., 2008). A definição de biodegradabilidade é a capacidade de
um produto se decompor por ação microbiológica no período máximo de um ano em água,
dióxido de carbono ou terra carbonácea. A biodegradabilidade de óleos minerais é de 20%
enquanto que para óleos vegetais é de 99% (Da Silva, 2008).
Devido à tendência mundial de crescente preocupação sobre o impacto ambiental
causado por derivados de petróleo, esses lubrificantes de origem vegetal se tornam uma
alternativa para os mercados externos que exigem produtos industrializados de forma
compatível com o meio ambiente. Para exemplificar, segundo Da Silva (2008), 1 litro de óleo
mineral polui 1 milhão de litros de água.
Atualmente, de acordo com dados do CENPES/Petrobrás, o mercado mundial de
lubrificantes produz cerca de 38 milhões de toneladas por ano de lubrificantes, dos quais
apenas 350 mil toneladas são biolubrificantes. Nos E.U.A, 32% dos 4,7 milhões de toneladas
de lubrificantes são descartados no meio ambiente, sendo que somente 5% são considerados
biodegradáveis. No mercado europeu o percentual de biolubrificantes é três vezes maior que o
mercado norte-americano.
As matérias primas utilizadas para produção dos biolubrificantes são basicamente
Estudo da Composição e Estabilidade em Emulsões formuladas a partir de óleos Lubrificantes vegetais
usadas, como por exemplo: soja, mamona, pinhão-manso, canola, girassol, etc. São exemplos
de biolubrificantes, os diésteres (ftalatos, adipatos e sebacatos) e os ésteres de poliol (Wagner
et al.,2001).
Além de conferirem biodegradabilidade aos biolubrificantes, os óleos vegetais
apresentam a vantagem de agregarem maior valor ao produto, apresentam baixa ou nenhuma
toxicidade, possuem boa lubricidade, possuem propriedades anti-corrosivas, alto índice de
viscosidade, baixa volatilidade, alto poder de solvência para aditivos e são obtidos a partir de
fontes renováveis (Bondioli et al., 2003).
Entretanto, devido à presença de duplas ligações e hidrogênios β (Figura 2.1) nas
moléculas de triglicerídeos, os óleos vegetais possuem limitadas estabilidades oxidativa,
térmica e hidrolítica (Wagner et al., 2001). Por estes serem pontos reativos e possuírem
facilidade de reagir com oxigênio presente no ar. Estas propriedades podem ser melhoradas
com a utilização de aditivos, porém o preço, a biodegradabilidade e a toxicidade do produto
lubrificante podem ser afetados. A utilização de processos químicos que reduzam ou
melhorem estes pontos críticos é uma alternativa para o processamento destes óleos, sem que
haja o comprometimento das suas boas propriedades.
Vale salientar que a maioria dos processos são desenvolvidos para os óleos de soja,
girassol e canola. Nestes processos o hidrogênio β é eliminado, levando à formação de ácidos
e olefinas. O grau de ramificação das moléculas de triglicerídeos determinam a fluidez, a
estabilidade hidrolítica e o índice de viscosidade. Quanto maior o grau de ramificação,
melhores são a fluidez e a estabilidade hidrolítica, e menor é o índice de viscosidade. Já o
grau de saturação determina a estabilidade oxidativa e a fluidez, quanto maior é o grau de
saturação, melhor é a estabilidade oxidativa, e pior é a fluidez (Da Silva, 2008). A
biodegradabilidade é impedida pela presença de substituintes alifáticos, estruturas cíclicas,
anéis aromáticos, carbonos quarternários, hétero-atomos e sistemas insaturados nas
moléculas, e diminui com aumento do peso molecular. Durante o processamento do óleo
vegetal, deve ser feita uma ponderação destas propriedades para que seja possível a síntese de
um lubrificante de boa qualidade.
Estudo da Composição e Estabilidade em Emulsões formuladas a partir de óleos Lubrificantes vegetais Figura 2.1 Estrutura típica de um óleo vegetal e seus pontos críticos de instabilidade, indicando a presença de
duplas ligações e hidrogênios β(Wagner et al., 2001).
Existem diversos processos que estão sendo estudados para síntese de biolubrificantes:
hidrogenção, oligomerização, alquilação de Friedel-Crafts, adição de radical (aciloxilação),
epoxidação, síntese de estolides, transesterificação de ésteres. Estas são alternativas para
síntese de biolubricantes com propriedades que garantam a sua utilidade industrial.
A hidrogenação, que consiste na eliminação das ligações duplas através da adição de
hidrogênio utilizando catalisadores de níquel, melhora a estabilidade oxidativa, porém
inviabiliza a fluidez (Baumann et al., 1988). A alquilação, que consiste na adição de radicais
alquil à molécula de triglicerídeo, melhora a estabilidade oxidativa e hidrolítica e a fluidez,
porém é bastante oneroso pelo alto consumo de catalisador. Os estolides oléicos, que são
obtidos a partir do agrupamento dos ésteres do ácido ricinoleico, são mais resistentes à
oxidação do que os básicos minerais e vegetais, porém sua obtenção ainda apresenta custo
elevado (Cermak and Isbell, 2003).
A transesterificação de ésteres para produção de biolubrificante consiste na reação
entre um éster (triglicerídeo vegetal ou biodiesel) e um álcool de cadeia ramificada,
resultando em um novo éster (Figura 2.2). Os principais ésteres produzidos são os di-ésteres e
Estudo da Composição e Estabilidade em Emulsões formuladas a partir de óleos Lubrificantes vegetais
R
O R' R'' OH
C O
+ R
O R'' C
O
R' OH +
Como exemplo de di-ésteres temos os sebacatos, adipatos e ftalatos. Os adipatos são
mais biodegradáveis do que os sebacatos, porém os sebacatos apresentam melhores
propriedades sob carga do que os adipatos.
Os ésteres de poliol, representados na Figura 2.3, apresentam melhor estabilidade
térmica por não possuírem hidrogênio β e por apresentarem um carbono quaternário no centro
de sua estrutura. Um exemplo de éster de poliol é o éster de trimetilopropano obtido a partir
da transesterificação do ricinoleato de etila (éster componente principal do biodiesel de
mamona) e o álcool trimetilopropano em meio catalisado por estanho (Wagner et al., 2001).
Figura 2.2 Reação de Transesterificação para síntese de ésteres lubrificantes.
O
C17H33OO
CH2 O C17H33O
O
O C17H33O
Estudo da Composição e Estabilidade em Emulsões formuladas a partir de óleos Lubrificantes vegetais Figura 2.3 Éster de Trimetilopropano.
A síntese de ésteres lubrificantes por transesterificação tem seu rendimento afetado
pelo equilíbrio e pode ser realizada por via química ou via enzimática. A primeira utiliza
catalisadores ácidos, como H2SO4, básicos como NaOH, resina de troca iônica, catalisadores
complexos à base de chumbo, oxalatos, ácido p-tolueno sulfônico, ácido fosfórico, etóxido e
metóxido de sódio, etc (Onken e Behr, 1996).
A rota química apresenta a vantagem de ter um custo acessível do processo em escala
industrial. No entanto, é um processo de baixa seletividade e necessita de um alto consumo
energético. No caso de catalisadores ácidos ou básicos, é possível a ocorrência de corrosão no
reator. Estes catalisadores também não funcionam adequadamente com álcoois superiores (de
cadeias ramificadas ou longas) (Da Silva, 2008).
A utilização de álcoois ramificados, como trimetilopropano, é importante para
obtenção de ésteres lubrificantes com propriedades aceitáveis. Os ésteres de poliol com
melhores características são obtidos a partir de álcoois de cadeias ramificadas. Neste caso,
uma alternativa é a utilização de catalisadores metálicos ao invés de catalisadores
homogêneos (ácidos ou básicos) (Wagner et al., 2001).
A rota enzimática consiste na utilização de catalisadores enzimáticos como as lípases,
e apresenta a vantagem de serem mais seletivas, além de permitirem condições mais brandas
de reação, rendimento elevado, biodegradabilidade, recuperação da enzima e menor curto
energético (Da Silva, 2008). Porém o custo do processo em escala industrial ainda é muito
oneroso (Westfechtel e Giede, 1999).
2.2. Aspectos gerais sobre os surfactantes
Os surfactantes são moléculas constituídas de duas regiões com características
diferentes; uma região polar ou hidrofílica, formada de grupos eletricamente carregados ou
Estudo da Composição e Estabilidade em Emulsões formuladas a partir de óleos Lubrificantes vegetais
cadeias hidrocarbônicas (De Lucena Neto, 2005). A presença, na mesma molécula, de duas
partes de afinidades diferentes caracteriza o termo anfifílico (Mittal, 1979), exibindo
propriedades de modificação das interações interfaciais por via da adsorção nas interfaces
(Myers, 1992).
A representação genérica de uma molécula anfifílica pode ser vista na Figura 2.4.
Figura 2.4 Representação de uma molécula surfactante.
2.2.1. Classificação
Uma das formas mais simples de classificação dos surfactantes é de acordo com sua
forma de dissociação, ou seja, sua porção hidrofílica. Desta forma, podem ser classificados
em iônicos, não iônicos e anfóteros (Shaw, 1975).
2.2.2. Propriedades
Devido a sua natureza anfifílica, os surfactantes possuem características de redução da
tensão interfacial através da formação de um filme adsorvido na interface das fases imiscíveis.
Como conseqüência, apresentam ação emulsionante, molificante, detergente, dispersante e
Estudo da Composição e Estabilidade em Emulsões formuladas a partir de óleos Lubrificantes vegetais
Em sistemas constituídos de dois líquidos, o resultado da ação surfactante é a redução
da tensão interfacial entre as duas fases. Quando adicionadas a estes sistemas, as moléculas
surfactantes se concentram diferentemente na interface e no interior de uma certa fase (De
Lima, 2004). Através da equação de Gibbs, podemos calcular a quantidade surfactante
adsorvido por unidade de área interfacial, e, com isso, expressar o equilíbrio entre as
moléculas situadas na interface e no interior da solução (Atwood & Florence, 1983).
Em sua forma mais geral a equação de Gibbs (Equação 2.1) pode ser escrita como:
dγ = - ΣΓidi i (2.1)
onde Γ é denominado de excesso de superfície, e representa a diferença de concentração de
uma determinada espécie molecular na interface e no interior de uma fase; dγ significa a
mudança na tensão superficial ou interfacial do solvente; Γi é a concentração do excesso de
superfície do i-ésimo componente e di i é a mudança no potencial químico do i-ésimo
componente do sistema ( De Lima, 2004).
2.2.3. Balanço Hidrofílico-Lipofílico(BHL)
A predominância de um dos caráteres hidrofílico ou lipofílico dota a molécula
surfactante de propriedades específicas e determina os seus tipos de aplicação. Para
quantificar os efeitos destas características, Griffin (1954) introduziu a noção semi-empírica
de Balanço hidrofílico-lipofílico (BHL).
A escala de Griffin, demonstrada no Quadro 2.1, apresenta a faixa de BHL e as
aplicações específicas para cada faixa. A cada substância surfactante é atribuído um número
que o inclui em um determinado grupo com propriedades específicas. Valores de BHL baixo
Estudo da Composição e Estabilidade em Emulsões formuladas a partir de óleos Lubrificantes vegetais
solubilidade na fase oleosa, quando comparado aquela na fase aquosa. Para valores de BHL
alto, ocorre o inverso.
Quadro 2.1 Escala de Griffin (1954).
FAIXA DE BHL SURFACTANTES
1 a 3 Agentes Anti-espumante
3 a 6 Agentes emulsificantes (A/O) BAIXA
7 a 9 Agentes Molhantes
8 a 13 Agentes Emulsificantes (O/A)
13 a 16 Detergentes ALTA
16 a 18 Agentes Solubilizantes
A escolha do melhor surfactante para um dado sistema pode ser feita a partir da noção
do BHL. Para sistemas em que a fase aquosa se apresenta em maior quantidade que a fase
óleo (emulsões O/A), devem ser utilizados surfactantes com alto valor de BHL (16 a 18). Para
sistemas em que a fase óleo é mais abundante do que a fase aquosa deve-se utilizar
surfactantes com baixo valor de BHL (3 a 6).
Segundo Davies e Rideal (1963) os valores de BHL podem ser calculados pela
contribuição de cada grupo, polar ou apolar da molécula anfifílica de acordo com a Equação
2.2.
BHL = Σ[(contribuição dos grupos hidrofílicos) – (contribuição dos grupos hidrofóbicos)] +
7 (2.2)
O valor atribuído pela contribuição dos principais grupos constituintes está
Estudo da Composição e Estabilidade em Emulsões formuladas a partir de óleos Lubrificantes vegetais Quadro 2.2 Valor numérico dos diversos grupos funcionais para o cálculo do BHL segundo o método de Davies
e Rideal (1963).
GRUPOS VALOR
HIDROFÍLICOS
GRUPOS VALOR
HIDROFÓBICOS
-SO4-Na+ 38,7 -C- -0,475
-COO-K+ 21,1 -CH- -0,475
-COO-Na+ 19,1 -CH2- -0,475
-SO3-Na+ 11,0 -CH3- -0,475
-N 9,4 -CH= -0,475
-COO- 2,4 -CF2- -0,870
-COOH 2,1 -CF3 -0,870
-OH 1,9
-O- 1,3
-O-CH2-CH2 0,33
O-CH2-CH2-CH2 -0,15
2.2.4. Micelização
A miscelização é o processo de formação de micelas quando a concentração de
surfactante atinge um limite alto e estes não podem mais se adsorver, não atuando na
diminuição da tensão interfacial.
2.2.4.1. Concentração Micelar Crítica (CMC)
Para que haja a diminuição da tensão interfacial, os surfactantes atuam como
Estudo da Composição e Estabilidade em Emulsões formuladas a partir de óleos Lubrificantes vegetais
fase aquosa, enquanto a região apolar é repelida pela mesma. Entretanto, com o aumento da
concentração do surfactante que deve ser adsorvido, esse valor tende a um limite em que a
partir desse ponto as moléculas não poderão mais se adsorver. Este é um ponto de saturação
na interface. Neste ponto inicia-se a formação espontânea de agregados moleculares, ou seja,
“micelas” (Nome et al., 1982 citado por De Lucena Neto, 2005).
Nos casos de agregados formados por surfactantes iônicos, o fenômeno chamado de
micela direta ocorre quando a região apolar da molécula surfactante se agrupa de forma a se
ter uma menor superfície em contato com a água, apontando para o interior do agregado,
enquanto as extremidades polares ficam dirigidas para o meio aquoso. A micela inversa é o
fenômeno oposto de orientação das moléculas em que as partes hidrofílicas se agrupam no
centro e as cadeias hidrófobas ficam voltadas para o meio externo. Estes fenômenos são
mostrados na Figura 2.5.
Figura 2.5 Fenômenos de formação das micelas (De Lucena Neto, 2005).
A concentração, a partir da qual ocorre o processo de micelização, a uma determinada
temperatura, é chamada de concentração micelar crítica – CMC, que é uma característica de
cada surfactante.
A concentração micelar crítica pode ser determinada pela mudança brusca de algumas
propriedades físico-químicas das soluções quando se varia a concentração do surfactante (De
Estudo da Composição e Estabilidade em Emulsões formuladas a partir de óleos Lubrificantes vegetais
2.2.4.2 Pontos de Krafft e de turbidez
Para os surfactantes iônicos, a partir de um determinado valor de temperatura, a curva
de solubilidade cresce exponencialmente e somente a partir deste valor, conhecido como
temperatura de Krafft é que se inicia o processo de micelização (Krafft e Winglow, 1985;
Rouviere e Faucompre, 1983). Segundo Shinoda et al (1963) esta temperatura seria o ponto de
fusão do surfactante hidratado.
Uma análise detalhada da Figura 2.6 mostra que abaixo da temperatura de Krafft (K) e
à baixas concentrações de surfactante, tem-se uma solução de monômeros, e em
concentrações mais elevadas, o surfactante hidratado precipita (zona I). Acima da temperatura
de Krafft e a baixas concentrações em tensoativo, tem-se uma solução de monômeros (zona
II) e, em concentrações mais elevadas, as micelas (zona III).
Figura 2.6 Diagrama de fase de um surfactante iônico próximo ao ponto de Krafft (De Lucena Neto, 2005).
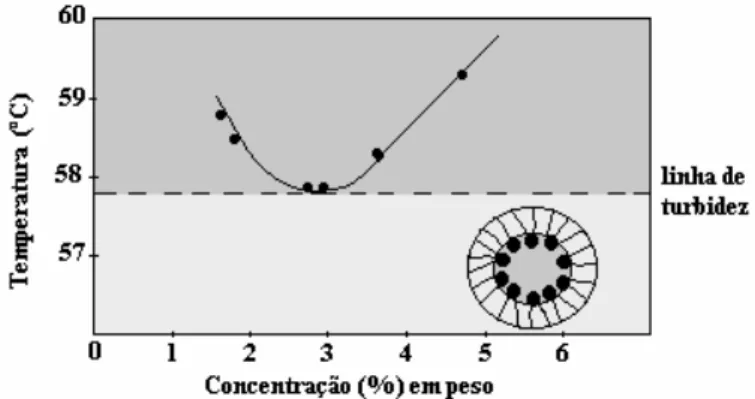
Vale salientar que os surfactantes não iônicos, por sua vez, não apresentam o
fenômeno Krafft. Entretanto, estes podem ser caracterizados pelos pontos de pertubação ou
turbidez. As soluções destes surfactantes, quando aquecidas, turvam-se, formando duas fases
a uma determinada temperatura e em uma determinada concentração (Figura 2.7). O mínimo
Estudo da Composição e Estabilidade em Emulsões formuladas a partir de óleos Lubrificantes vegetais
(Tietann, 1965). Desta forma, a micelização para este tipo de surfactante acontece abaixo do
ponto de turbidez (Corti et al.,1984).
Figura 2.7 Diagrama de fase de um surfactante não iônico em água (De Lucena Neto, 2005).
2.2.5. Biossurfactantes
A grande maioria dos surfactantes disponíveis comercialmente é sintetizada a partir de
derivados de petróleo. Porém, o crescimento da preocupação ambiental juntamente com as
novas legislações de controle do meio ambiente levou à procura por surfactantes naturais
como alternativas aos produtores existentes.
Compostos de origem microbiana que exibem atividade superficial são denominados
biossurfactantes, consistindo em subprodutos de seus respectivos sistemas metabólicos,
podendo ser encontrados em superfícies de células microbianas ou excretados
extracelularmente. São moléculas anfipáticas constituídas de uma porção hidrofílica e outra
hidrofóbica. Apresentam diversas vantagens em relação aos surfactantes sintéticos, tais como:
baixa toxicidade, alta biodegrabilidade, elevada compatibilidade ambiental, biodigestibilidade
e efetividade em condições extremas de temperatura, pH e força iônica (Cameotra e Makkar,
2004).
As bactérias, juntamente com as arqueobactérias, são as maiores responsáveis pela
Estudo da Composição e Estabilidade em Emulsões formuladas a partir de óleos Lubrificantes vegetais
produzidos, em alguns casos, em grandes quantidades em ambientes marinhos, solos e áreas
contaminadas por óleos. Uma dessas evidências é a presença de espuma e emulsão em regiões
de derramamento de petróleo em oceanos, bem como seu efeito positivo no aumento da
recuperação terciária de óleo (Maier, 2003).
Os biossurfactantes, de um modo geral, podem ser classificados em: glicolipídeos,
lipossacarídeos, lipopeptídeos, fosfolipídeos e ácidos graxos/lipídeos neutros (Zajic e Seffens,
1984), além dos poliméricos e particulados, sendo os lipopeptídeos os biossurfactantes mais
efetivos. Bactérias do gênero Pseudomonas aeruginosa produzem biossurfactantes que são
normalmente denominados ramnolipídeos, um glicolipídeo formado por uma ou duas
moléculas de ramnose e por uma cadeia de ácido graxo. Estes são os biossurfactantes mais
estudados e apresentam aplicações em diversos setores industriais e em biorremediação
(Desai et al., 1997).
2.3. Emulsão
Emulsão é um sistema composto por dois líquidos imiscíveis, em que um destes
líquidos está disperso em outro na forma de gotas macroscópicas (Edwards et al., 1991). A
adição de um agente emulsificante e a agitação suficiente são necessárias para transformar o
sistema numa fase contínua. Pelo estudo feito por Salager (1986), quando o óleo é a fase
dispersa, a emulsão é chamada de “Emulsão Óleo em Água” (O/A), e, quando o meio
disperso é aquoso, a emulsão é chamada de “Emulsão de Água em Óleo” (A/O).
O tipo de emulsão é de fácil identificação, através de métodos físicos e
Estudo da Composição e Estabilidade em Emulsões formuladas a partir de óleos Lubrificantes vegetais Tabela 2.1 Métodos para identificar o tipo de emulsão. Fonte: Machado (2002).
Método Emulsão O/A Emulsão A/O
Visual Textura Cremosa Textura Gordurosa
Corantes Corantes inorgânicos tingem
a emulsão
Corantes orgânicos tingem a
emulsão
Condutiviade Condutividade elétrica bem
mais elevada
Condutividade elétrica a
depender do potencial
elétrico aplicado
Miscibilidade A emulsão se mistura facilmente com um líquido miscível no
meio de dispersão (dispersante)
2.3.1. Teoria da formação de uma emulsão
Quando dois líquidos imiscíveis são misturados, mantendo-se agitação constante, as
duas fases tendem, inicialmente, a formar gotículas dispersas de um dos líquidos no interior
do outro. Quando a agitação cessa, as gotículas tendem a coalescer e os líquidos separam-se
novamente. Podemos, então, definir o tempo de vida de uma emulsão como o tempo
decorrido desde o momento em que os líquidos estão completamente homogeneizados, até a
separação total do sistema. Assim, o "tempo de vida" é maior quanto melhor for a estabilidade
do sistema. Neste ponto interessa-nos analisar mais detalhadamente os motivos que levam à
desestabilização da emulsão (De Oliveira et al., 2004).
Quando um dos líquidos divide-se no interior do outro forma-se uma fase interna,
dispersa ou descontínua, rodeada por uma fase externa, dispersante ou contínua. Assim, para o
processo de emulsificação é necessário um grande aumento de área interfacial (S1→S2),
ocasionando um aumento brusco da energia livre de superfície (G1→G2). Este fenômeno, em
Estudo da Composição e Estabilidade em Emulsões formuladas a partir de óleos Lubrificantes vegetais
∆G= G2-G1=γi x ∆S (2.3)
Onde γi representa a tensão interfacial entre as fases aquosa e oleosa, ∆G é a variação da
energia livre e ∆S é a variação da área interfacial.
Se considerarmos que o aumento da área interfacial (S1→S2) é imprescindível sob o
ponto de vista tecnológico, uma das alternativas para a estabilização de uma emulsão seria
fornecer energia mecânica, continuamente, de modo a manter a área interfacial aumentada.
Este fator, embora necessário para a dispersão, por si só não é suficiente, pois vence a barreira
da tensão superficial apenas temporariamente, enquanto durar a agitação.
Através da Equação 2.3, podemos verificar que o caminho mais viável para a
estabilização do sistema é a diminuição da tensão interfacial da dispersão, como forma de
reduzir a energia livre derivada da expansão da área interfacial. É possível verificar, também,
que a estabilidade da emulsão deverá ser maior quanto menor for a energia livre remanescente
da expansão da área interfacial, tendendo a um sistema termodinamicamente estável, caso em
que o aumento da energia livre seja totalmente compensado pela diminuição da tensão
interfacial.
Neste aspecto, os surfactantes, por possuírem a propriedade de diminuir a tensão
interfacial entre o óleo e a água, encontram seu papel fundamental na estabilização de
emulsões e microemulsões. Entretanto, esses compostos, com certas exceções, não
conseguem diminuir a tensão interfacial a ponto de contrariar totalmente a energia livre de
superfície provocada pelo aumento da área interfacial. Dessa forma, as emulsões comuns são
consideradas sistemas termodinamicamente instáveis e, no seu desenvolvimento tecnológico,
procura-se utilizar meios que possam retardar pelo maior tempo possível a separação das
fases.
Segundo Arnold et al. (1986), o comportamento de uma emulsão realiza-se como é
Estudo da Composição e Estabilidade em Emulsões formuladas a partir de óleos Lubrificantes vegetais Figura 2.8 Fotografias de Emulsões (Arnold et al., 1986).
2.3.2. Parâmetros de estabilidade
A propriedade física mais importante de uma emulsão é a sua estabilidade. Entende-se
por estabilidade de uma emulsão a capacidade da mesma em manter sua homogeneidade
durante um certo período de tempo. Conforme Rosa (2003), as emulsões estabilizadas
fisicamente são formadas sem adição de substâncias surfactantes, ou seja, aquelas em que a
estabilidade é mantida por cargas elétricas inerentes ao sistema ou a outras forças. Algumas
emulsões estáveis podem levar semanas ou meses para se separarem sem tratamento químico
ou até mesmo nunca se separarem. Outras emulsões instáveis podem se separar em suas fases
originais dentro de poucos minutos. A instabilidade da emulsão ou a razão pela qual as
partículas dispersas coalescem e quebram a emulsão, segundo estudos realizados por Manning
et al (1995), depende de alguns parâmetros, dentre estes, os principais são:
• Tensão Interfacial – quando as partículas colidem, rompem a película formada pelo filme
interfacial e há a coalescência. Porém quando um agente emulsificante está adsorvido em
torno da partícula, impede a coalescência e diminui a tensão interfacial causando a formação
Estudo da Composição e Estabilidade em Emulsões formuladas a partir de óleos Lubrificantes vegetais
• Envelhecimento da emulsão – à medida que o filme interfacial que reveste a partícula
emulsionada envelhece a adsorção de agentes emulsionantes se completa e a resistência da
película interfacial aumenta, até conseguir seu valor estável. Disto resulta que quanto mais
velha uma emulsão, mais estável fica. Por isso, o tratamento para romper uma emulsão deve
ser efetuado o mais cedo possível, inclusive de forma preventiva.
• Viscosidade da Fase Contínua – se esta viscosidade for muito alta, o coeficiente de difusão
e a freqüência de colisão baixa, deixando a emulsão muito mais estável.
• Temperatura – a adição de calor reduz a viscosidade do óleo que permite tanto a
coalescência mais rápida como a miscibilidade do óleo com a água.
Alguns tipo de emulsões podem “inverter” para produzir a emulsão oposta e essa
inversão pode conferir maior estabilidade ao sistema. As emulsões podem ser revertidas de
óleo/água para água/óleo e vice-versa pela variação de algumas condições, tais como:
temperatura do sistema, natureza do emulsificante ou sua adição, porcentagem de volume de
fase dispersa, a fase em que o emulsificante está dissolvido e outros. A relação entre o volume
das fases e a inversão das fases também podem representar um papel importante na
estabilidade das emulsões (Sajadi et al., 2003 citado por De Lima, 2004).
2.3.3. Fenômenos associados à instabilidade
Existem vários fenômenos associados a instabilidade das emulsões, dentre os
processos de quebra, podemos citar: cremagem, floculação e coalescência. Estes mecanismos
embora explicados separadamente podem ocorrer simultaneamente:
2.3.3.1. Cremagem
As gotículas presentes na fase interna da emulsão podem possuir valores de
densidades diferentes e estão, portanto, propensas a passar por um processo denominado de
Estudo da Composição e Estabilidade em Emulsões formuladas a partir de óleos Lubrificantes vegetais
formulação. A formação da cremeação representa um fenômeno reversível pelo fornecimento
mínimo de energia caso as partículas não se combinem. Podendo ser acelerado por
centrifugação e retardado pelo aumento da viscosidade da dispersão ou pela redução da
diferença de densidade efetiva entre as gotas e o fluido que as cercam (Ribins et al, 1992).
2.3.3.2. Floculação
Neste processo as gotículas da fase interna aglomeram-se fraca e reversivelmente. O
fenômeno é tipicamente causado por uma carga inadequada sobre as micelas, o que reduz a
força de repulsão entre as mesmas. As fases aquosa e oleosa permanecem distintas e não há
alteração nas dimensões das gotículas da fase interna. A floculação, assim como a cremeação,
pode ser revertida por meio da agitação do sistema. Este fenômeno ocorre freqüentemente em
emulsões inversas onde as forças de repulsão são de baixa intensidade, devido às pequenas
cargas das gotas.
2.3.3.3. Coalescência
Quando duas gotículas da fase interna se aproximam o suficiente, estas podem se unir
para formar uma gotícula maior. Esse processo é irreversível. Quando um número elevado de
partículas coalesce, o resultado é a separação completa das fases. Tal processo é
energeticamente favorável em quase todos os casos. Embora a coalescência resulte em
mudanças microscópicas significativas nas condições da fase dispersa, o processo pode não
resultar de imediato em uma alteração macroscópica aparente do sistema (De Lima, 2004).
Outros fatores que podem desestabilizar uma emulsão são: temperaturas elevadas de
armazenamento, a evaporação da fase aquosa, a contaminação microbiana e demais reações
Estudo da Composição e Estabilidade em Emulsões formuladas a partir de óleos Lubrificantes vegetais
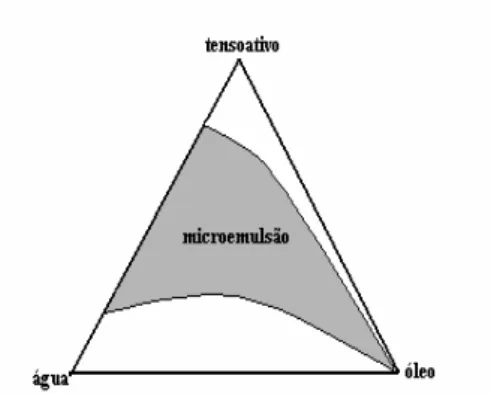
2.3.4. Microemulsões
Em alguns casos, as características químicas das moléculas surfactantes podem ser
favoráveis a formação de microemulsão (Figura 2.9), promovendo a íntima dispersão entra
fase oleosa e fase aquosa. Estes sistemas assim como as emulsões são sistemas monofásicos
dispersos e macroscopicamente homogênos, porém apresentam-se opticamente transparentes
e são mais estáveis termodinamicamente (De Oliveira et al, 2004)
Algumas vezes, dependendo do sistema, cotensoativos podem ser adicionados para
facilitar a estabilização de uma microemulsão. Álcoois e aminas de cadeia curta são exemplos
comuns. Estes exercem as seguintes funções:
• Reduzir as tensões interfaciais a níveis muito baixos
• Promover interações variadas na camada interfacial
• Melhorar a fluidez do filme interfacial.
Figura 2.9 Estrutura representativa dos dois tipos de microemulsões.
A característica mais importante do sistema microemulsionado é formar
espontaneamente a fase interna por homogeneização suave dos componentes da fórmula. Sua
Estudo da Composição e Estabilidade em Emulsões formuladas a partir de óleos Lubrificantes vegetais
suspensões e as emulsões, podendo ser utilizada por tempo muito mais amplo. As principais
diferenças entre emulsões e microemulsões estão apresentadas na Tabela 2.2
Schuluman et al (1982) propôs um modelo estrutural para microemulsões ricas em
óleo ou água. Segundo este modelo, as microemulsões são constituídas de microgotículas
dinâmicas dispersas, com um diâmetro variando entre 10 e 200 nm. Estas apresentam uma
camada mononuclear de surfactantes envolvendo-as como uma membrana. Assim como as
emulsões, as microemulsões podem ser do tipo óleo em água(O/A), onde as microgotículas
são ditas diretas e do tipo água em óleo (A/O), onde as microgotículas são ditas inversas. Em
cada caso as moléculas surfactantes se comportam de forma que cabeças polares estejam
voltadas para a fase aquosa, e suas caudas apolares para a fase óleo (De Lucena Neto, 2005).
As propriedades das microemulsões, como alta estabilidade, baixíssima tensões
interfaciais a baixas concentrações de surfactantes, capacidade de tornar miscível grande
quantidade de líquidos imiscíveis, garantem a estas uma potencial aplicação na industria. São
várias suas aplicações, como por exemplo: recuperação terciária do petróleo, obtenção de
membranas, processo de separação e purificação, processo de polimerização etc (De Lucena
Neto, 2005).
Tabela 2.2 Características de Emulsões e Microemulsões.
Emulsões Microemulsões
Instáveis, com separações de fases
Gotículas de tamanho relativamente grande
(1a 10 m)
Sistemas relativamente estáticos
Área interfacial moderadamente grande
Pouco surfactante é requerido para
estabilização
Pequena curvatura da interface água-óleo
Termodinamicamente estáveis
Agregados pequenos (da ordem de poucas
dezenas de nanômetros)
Sistemas altamente dinâmicos
Área interfacial bastante grande
Grande quantidade de surfactante é
necessária
O filme interfacial pode estar altamente
Estudo da Composição e Estabilidade em Emulsões formuladas a partir de óleos Lubrificantes vegetais
2.4. Diagramas de Fases
Quando se modifica progressivamente a composição de uma mistura de solventes
miscíveis, as mudanças que se produzirão na solução podem ser traduzidas por importantes
variações nas propriedades termodinâmicas dos compostos que a compõe. Por outro lado, as
observações dessas propriedades e sua evolução com a composição da solução podem
fornecer informações específicas sobre a estrutura do meio (De Lucena Neto, 2005).
O diagrama de fases descreve em que condição experimental é possível se obter
microemulsões, emulsões e as regiões limites de transição entre emulsões, fases separadas e
microemulsões O/A e A/O.
A representação gráfica dos sistemas emulsionados em que estejam presentes três
constituintes (água+óleo+surfactante) pode ser feita num diagrama triangular. A Figura 2.10
mostra um exemplo de diagrama em que se deseja determinar a região de microemulsão.
Figura 2.10 Diagrama ternário, mostrando a zona de microemulsão em um sistema de três constituintes.
Para construção do diagrama, prepara-se misturas binárias dos componentes,
correspondentes a cada lado do triângulo, como segue:
Mistura emulsiva (T) / fase oleosa (O) em várias proporções, titulando-se com a fase
Estudo da Composição e Estabilidade em Emulsões formuladas a partir de óleos Lubrificantes vegetais
direcionadas ao infinito de fase aquosa, isto é, convergentes ao vértice do triângulo que
representa 100% de fase aquosa (Figura 2.11.a). O mesmo procedimento pode ser utilizado
para a mistura emulsiva (T) / fase aquosa (A), a qual é titulada com a fase oleosa (O) (De
Oliveira et al, 2004).
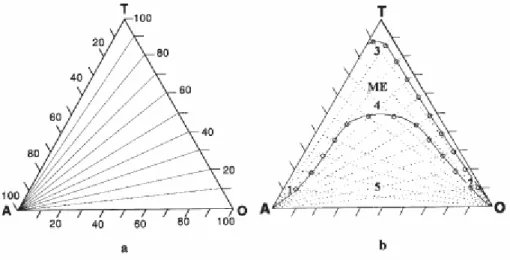
Figura 2.11 (a) Titulação com fase aquosa; (b) representação dos pontos de titulação e regiões do diagrama de
fases.
Geralmente esses dois procedimentos são suficientes para se definir o diagrama de
fases. Um exemplo deste diagrama está apresentado na Figura 2.11.(b) em que se deseja
encontrar a região de microemulsão representada pela zona ME . Os pontos da titulação
referem-se às modificações verificadas no sistema, tais como, separação de fases, sistema
transparente líquido, sistema transparente gel, sistema opaco, etc.
Se a água e o óleo forem misturados com um surfactante capaz de produzir uma
emulsão leitosa, e essa emulsão for titulada com um co-tensoativo apropriado até formar um
sistema opticamente transparente, pode-se determinar a relação tensoativo/co-tensoativo ideal
para a obtenção da microemulsão. Para descrição desse tipo de sistema, existem também os
diagramas quaternários e pseudoternários.
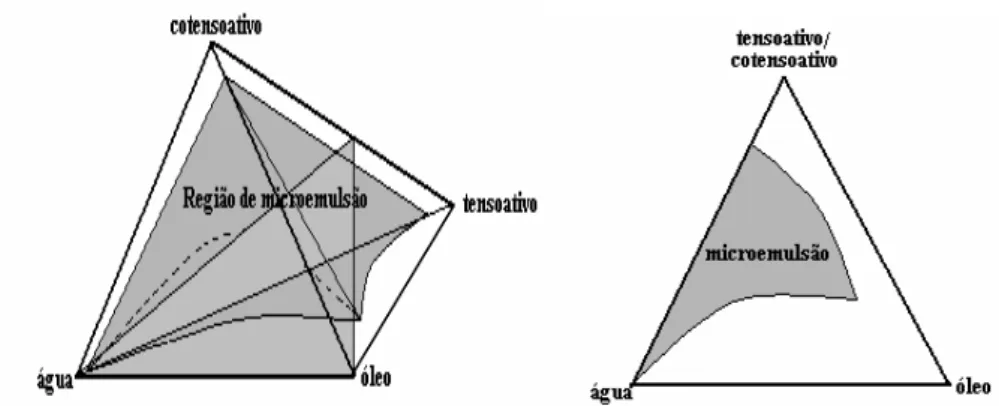
As emulsões estabilizadas por blends surfactantes ou as microemulsões a quatro
constituintes (água + óleo + surfactante + cosurfactante), são extensões dos diagramas
Estudo da Composição e Estabilidade em Emulsões formuladas a partir de óleos Lubrificantes vegetais
um tetraedro regular, como o da Figura 2.12. Onde cada vértice do tetraedro representa um
dos componentes puros.
Figura 2.12 Diagrama de fases quaternário, mostrando a zona de microemulsão.
O modo mais usual de descrever sistemas de quatro componentes é através do
diagrama de fases pseudoternário, onde fase aquosa, fase oleosa e mistura de
tensoativo/co-tensoativo para o caso de sistemas microemulsionados são representadas nos vértices do
triângulo. Esse tipo de diagrama também suporta outras misturas, como por exemplo óleo,
co-surfactante e água/co-surfactante. Estão representados nas Figuras 2.13 e 2.14.
Estudo da Composição e Estabilidade em Emulsões formuladas a partir de óleos Lubrificantes vegetais Figura 2.14 Diagramas pseudoternário com relação água/tensoativo constante.
2.5. Planejamento Experimental
Devido a necessidade crescente de otimização de produtos e processos, minimizando
custos e tempos, maximizando rendimento, produtividade e qualidade de produtos, dentre
outros objetivos, pesquisadores de diferentes formações vem buscando técnicas sistemáticas
de planejamento experimental (Rodrigues e Iemma, 2005). Com o desejo de agilizar o
desenvolvimento do processo e obter resultados que abranjam uma vasta região de estudo
Os planejamentos experimentais para estudos de misturas ou sistemas com dois ou
mais componentes têm uma importante diferença em relação aos planejamentos experimentais
fatoriais. Uma vez que as propriedades de uma mistura são determinadas pelas proporções de
seus “ingredientes”, e não pela sua quantidade total (Barros Neto et al., 2002). Se quisermos
otimizar as propriedades de uma mistura mudando a sua formulação, a soma das proporções
tem de dar sempre 100%. A existência dessa restrição impõe algumas modificações nas
metodologias aplicadas a planejamento fatorial e a modelagem de superfícies respostas, para
adaptá-las aos problemas específicos das misturas.
A rede Sheffé é uma metodologia de planejamento experimental utilizada em sistemas
formados por dois ou mais constituintes (Ramos, 1997). Para sistemas com três constituintes,
Estudo da Composição e Estabilidade em Emulsões formuladas a partir de óleos Lubrificantes vegetais
que são relacionadas em função da concentração relativa de cada ponto de um triângulo
eqüilátero (Sado e Sado, 1989 citado por De Lucena Neto, 2005).
Para uma mistura de K constituintes em proporções x1,x2,...,xj e Y uma propriedade a
ser analisada, o modelo consiste em determinar os valores dos parâmetros do polinômio que
melhor se ajuste ao comportamento da propriedade estudada, em função das frações dos
constituintes. Para verificar o ajuste do modelo comparamos os valores experimentais com
valores preditos pelo mesmo (Goupy, 1988).
A aplicação do plano de experiência consiste em dividir o sistema estudado em uma
rede de distribuição de pontos, de composição previamente definida no diagrama
pseudoternário, e, com os valores experimentais das respostas, aplica-se a Equação 2.4.
Y=∑ai + ∑aij +xij +∑ahijXhXiXj + .... + a12...X1X2...Xk (2.4)
Onde:
Y = respostas a ser analisadas;
ai, aij, ahij,... – parâmetros a ser determinados;
Xi, Xj, Xh,... Xk – composição do ponto especificado;
K – número de constituintes.
O objetivo do planejamento experimental é traduzir fielmente as variações de Y em
função dos Xi da maneira mais simples possível, gerando modelos determinados por uma
série de parâmetros (ai, aij, ahij,...) de acordo com o grau do polinômio.
O modelo mais simples para sistemas de dois ou mais componentes é o modelo aditivo
ou linear (Barros Neto et al., 1995). A expressão deste modelo está representado na Equação
2.5. Caso o modelo linear não se mostre satisfatório, o próximo passo é o ajuste de um
modelo quadrático. A expressão geral deste modelo para três componentes está representada
na Equação 2.6. Após análise e comparação dos modelos, aumenta-se o grau do polinômio até
Estudo da Composição e Estabilidade em Emulsões formuladas a partir de óleos Lubrificantes vegetais
Y= a1x1+a2x2+...+a3x3 (2.5)
Y= a1x1+a2x2+...+a3x3 + a12x1x2+a13x1x3+a23x2x3 (2.6)
Para uma melhor explanação dos pontos utilizados no modelo é montada uma matriz
de experiências, que define cada ponto no triângulo empregado, mostrado na Figura 2.15.
Figura 2.15 Representação gráfica da matriz de experiência.
A curvas de nível (curvas de iso-respostas) correspondentes ao modelo ajustado são
construídas, delas podemos concluir as melhores proporções dos componentes das quais serão
Estudo de Composição e Estabilidade em Emulsões formuladas a partir de Óleos Lubrificantes Vegetais
3. MATERIAIS E MÉTODOS
Este capítulo apresenta os materiais e métodos utilizados para realização dos
estudos de estabilidade e composição em emulsões formuladas a base de lubrificante
biodegradável do tipo éster de poliol, a partir da construção de diagramas de fases e
empregando o conceito de BHL para escolha do melhor sistema emulsionado.
3.1. Materiais
3.1.1. Constituintes dos Sistemas
Os sistemas objeto deste estudo foram formados por três constituintes:
surfactante, fase oleosa e fase aquosa. A seguir apresenta-se as suas principais
características.
• Fase Oleosa
O biolubrificante comercial Hatcol 2939, gentilmente cedido pela Innovatti
Performance Lubricants, foi utilizado como fase oleosa. Este biolubrificante é um ester
de poliol produzido a partir de uma reação de transesterificação entre um estér
(triglicerídeo vegetal) é um álcool de cadeia ramificada.
Para efeitos de comparação com os resultados do trabalho de mestrado de De
Lima (2004), em que foram produzidas emulsões a partir de óleo mineral naftênico
NH-20, reproduzimos este sistema utilizando óleo NH-20 fornecido pela Lubrificantes e
Derivados de Petróleo do Nordeste ( LUBNOR/PETROBÁS), como fase oleosa. A
Tabela 3.1 apresenta algumas propriedades referentes a caracterização físico-química do
biolubrificante e do NH-20. As análises foram feitas no Laboratório de Combustíveis e
Lubrificantes da UFC segundo metodologia padrão da American Society for Testing
Estudo de Composição e Estabilidade em Emulsões formuladas a partir de Óleos Lubrificantes Vegetais
Tabela 3.1 Caracterização físico-química do biolubrificante e do óleo mineral NH-20 segundo as normas
da ASTM.
Características HATCOL
2938
NH-20 Método
Viscosidade 400C
Viscosidade 1000C
Índice Viscosidade
Ponto de Fluidez
18,97 cSt
4,42 cSt
150
-610C
21,1 cSt
3,60 cSt
221
-450C
ASTM D-445
ASTM D-445
ASTM D-445
ASTM D-97
• Fase Aquosa
Água destilada foi utilizada como fase aquosa.
• Surfactantes
Foram testados catorze surfactantes comerciais fornecidos pela Sigma Aldrich e
Acros Organics. A Tabela 3.2 apresenta a nomenclatura química e nome comercial
destes surfactantes.
Utilizamos também como surfactante amostras de sabão de mamona (sabão de
ácidos graxos que, em sua maioria, são ácidos ricinoleícos) para analisarmos a ação
emulsificante do mesmo com o biolubrificante e água. Estes sabões foram obtido a
partir de uma reação de saponificação do óleo de mamona. A metodologia de obtenção
será descrita na próxima seção. Calculamos o BHL do sabão de mamona, segundo a
equação 2.2 descrita por Davies e Rideal (1963), e chegamos a um valor aproximado de
BHL=18. A utilização destes sabões é importante porque contribui com a
biodegradabilidade destes sistemas emulsionados. Além disso, estes emulsificantes são
Estudo de Composição e Estabilidade em Emulsões formuladas a partir de Óleos Lubrificantes Vegetais
Tabela 3.2 Nome comercial e nomenclatura química dos surfactantes testados.
NOME COMERCIAL NOMENCLATURA QUÍMICA
SDS
DBSS
Span 20
Span 40
Span 80
Tween 20
Tween 40
Tween 80
Brij 30
Brij 52
Brij 58
Igepal CO-210
Igepal CO-520
Igepal CO-720
Dodecil Sulfato de Sódio
Dodecil Benzeno Sulfonato de Sódio
Monolaurato de Sorbitan
Monopalmitato de Sorbitan
Monooleato de Sorbitan
Monolaurato de Sorbitan Etoxilado
Monopalmitato de Sorbitan Etoxilado
Monooleato de Sorbitan Etoxilado
Éter Laurilíco Etoxilado (4)
Éter Cetílico Etoxilado (2)
Éter Cetílico Etoxilado (20)
Nonil Fenol Etoxilado (1)
Nonil Fenol Etoxilado (4)
Nonil Fenol Etoxilado (11)
3.2. Métodos
A representação esquemática do que foi realizado nesse trabalho está mostrada