Braz. J. of Develop.,Curitiba, v. 6, n.5, p.26982-26993 may. 2020. ISSN 2525-8761
Avaliação do potencial citogenotóxico de extrato aquoso da folha de
Valeriana officinalis L
Evaluation of the cytogenotoxic potential of aqueous leaf extract of
Valeriana officinalis L
DOI:10.34117/bjdv6n5-229Recebimento dos originais: 25/04/2020 Aceitação para publicação: 13/05/2020
Jonis Franklin Leite dos Santos
Mestre em Genética e Melhoramento de Plantas pela Universidade do Estado de Mato Grosso Carlos Alberto Reyes Maldonado. Laboratório de Genética Vegetal e Biologia Molecular, Centro de Pesquisa e Tecnologia da Amazônia Meridional, Alta Floresta, MT,
Brasil.
E-mail: jonisfranklin@hotmail.com
Rosieli Barboza Bispo
Doutoranda em Genética e Melhoramento de Plantas pela Universidade Estadual do Norte Fluminense Darcy Ribeiro – UENF. Campos dos Goytacazes, Rio de Janeiro, Brasil.
E-mail: rosielibarboza.af@hotmail.com
Lorena Cristina Batista dos Santos
Mestre em Genética e Melhoramento de Plantas pela Universidade do Estado de Mato Grosso Carlos Alberto Reyes Maldonado. Laboratório de Citogenética e Cultura de Tecidos
Vegetais, Centro de Pesquisa e Tecnologia da Amazônia Meridional, Alta Floresta, MT, Brasil.
E-mail: lorenacrystyna@outlook.com
Isane Vera Karsburg
Doutora em Genética e Melhoramento pela Universidade Federal de Viçosa
Professora Adjunta da Faculdade de Ciências Biológicas e Agrárias, Universidade do Estado de Mato Grosso Carlos Alberto Reyes Maldonado. Laboratório de Citogenética e Cultura de
Tecidos Vegetais, Alta Floresta, MT, Brasil. E-mail: isane.karsburg@unemat.br
RESUMO
O objetivo desse estudo foi avaliar a citotoxicidade e genotoxicidade do extrato aquoso tipo infuso (EAI) de folhas de V. officinalis por meio do teste de Allium sativum. O extrato foi preparado a partir das folhas secas de V. officinalis, utilizando as seguintes dosagens: 2,5 g/L, 5 g/L, 7,5 g/L e 10 g/L. Para obtenção do extrato, a água foi aquecida e mantida em fervura por cinco minutos e vertida sobre o material vegetal (folhas), mantendo infuso por 10 minutos. O extrato foi filtrado, e juntamente com o bioindicador A. sativum, foram colocados em copos descartáveis com capacidade de 50 ml por 24, 48 e 72 horas. Posteriormente foram coletados os meristemas radiculares de A. sativum com aproximadamente 5 a 10 mm de comprimento em cada horário referenciado e fixado em etanol-ácido acético (3:1), conservados em
Braz. J. of Develop.,Curitiba, v. 6, n.5, p.26982-26993 may. 2020. ISSN 2525-8761 refrigerador até o uso. O extrato de V. officinalis respondeu de forma distinta nos horários testados de 24, 48 e 72 horas; conforme o aumento nas concentrações, apresentou diminuição significativa nas fases do ciclo celular, índice mitótico e células com irregularidades. Conclui-se que o extrato aquoso infuso apreConclui-sentou potencial citotóxico e genotóxico no ciclo celular em função do aumento nas concentrações testadas nas células meristemáticas de Allium sativum.
Palavras-Chave: Índice mitótico. Allium sativum. Bioindicador. Divisão celular. ABSTRACT
The aim of this study was to evaluate the cytotoxicity and genotoxicity of the aqueous infused type extract (EAI) of leaves of V. officinalis by means of the Allium sativum test. The extract was prepared from the dry leaves of V. officinalis, using the following dosages: 2.5 g / L, 5 g / L, 7.5 g / L and 10 g / L. To obtain the extract, the water was heated and boiled for five minutes and poured over the plant material (leaves), keeping infused for 10 minutes. The extract was filtered, and together with the bioindicator A. sativum, they were placed in disposable cups with a capacity of 50 ml for 24, 48 and 72 hours. Subsequently, the root meristems of A. sativum, approximately 5 to 10 mm long, were collected at each referenced time and fixed in ethanol-acetic acid (3: 1), kept in a refrigerator until use. The V. officinalis extract responded differently at the tested times of 24, 48 and 72 hours; according to the increase in concentrations, it showed a significant decrease in the phases of the cell cycle, mitotic index and cells with irregularities. It was concluded that the infused aqueous extract showed cytotoxic and genotoxic potential in the cell cycle due to the increase in the tested concentrations in the meristematic cells of Allium sativum.
Keywords: Mitotic index. Allium sativum. Bioindicator. Cell division. 1 INTRODUÇÃO
Desde a Antiguidade, as plantas têm sido consideradas fonte de alternativas terapêuticas, sendo utilizadas de forma empírica no tratamento de diferentes patologias (Moraes et al., 2010). Entretanto, o consumo de derivados de plantas necessita de atenção, pois várias espécies brasileiras não foram suficientemente estudadas no que se refere ao seu potencial toxicológico e/ou mutagênico (Simões et al., 2003).
Muitas plantas assim como medicamentos fitoterápicos já são utilizados e conhecidos na medicina para o tratamento da insônia como é o caso da Matricaria chamomilla L. (camomila), Melissa officinalis L. (melissa ou erva-cidreira), Passiflora 13 incarnata L. (maracujá), Piper methysticum G. Forst. (kava-kava) e a Valeriana officinalis L. (valeriana) (Veloso et al., 2008).
Para a compreensão da ação tóxica de alguns compostos, utiliza-se de experimentos laboratoriais. Estes utilizados para obtenção de dados e padronização de métodos, permitindo
Braz. J. of Develop.,Curitiba, v. 6, n.5, p.26982-26993 may. 2020. ISSN 2525-8761 assim prever e avaliar efeitos de toxicidade, variando sua concentração ou dosagem, em determinada espécie (Ferreira Filho, 2013).
Em relação à análise, ensaios e detecção, os bioindicadores vegetais são considerados mais sensíveis, simples e eficientes para o estudo da genotoxicidade na detecção de alterações no comportamento do ciclo celular, como: alface (Lactuta sativa L.), cebola (Allium cepa L.), tomate (Solanum lycopersicum L.) e alho (Allium sativum L.) (Grant, 1999 e Ma, 1995).
O método de avaliação de alterações cromossômicas em raízes de Allium é validado pelo Programa Internacional de Segurança Química (IPCS, OMS) e o Programa Ambiental das Nações Unidas (UNEP) como um eficiente teste para análise e monitoramento in situ da genotoxicidade de substâncias ambientais (Cabrera e Rodriguez, 1999).
Assim, diante da crescente utilização da espécie V. officinalis como alternativa terapêutica (calmantes, insônias e outros fins) pela população. O presente estudo teve como objetivo avaliar a citotoxicidade e genotoxicidade do extrato aquoso tipo infuso de folhas de Valeriana por meio do teste de Allium sativum.
2 MATERIAIS E MÉTODOS
O experimento foi realizado no Laboratório de Citogenética e Cultura de Tecidos Vegetais, Centro de Pesquisa e Tecnologia da Amazônia Meridional (CEPTAM), na Universidade do Estado de Mato Grosso Carlos Alberto Reyes Maldonado (UNEMAT), Campus Universitário de Alta Floresta, Mato Grosso, Brasil.
Foi preparado extrato aquoso do tipo infuso (EAI) a partir das folhas secas de V. officinalis, sendo utilizadas as seguintes dosagens: 2,5 g/L, 5 g/L, 7,5 g/L e 10 g/L. Para obtenção do EAI, a água foi aquecida e mantida em fervura por cinco minutos, contudo, o preparo consistiu em verter água em ponto de fervura (100 ºC) sobre o material vegetal (folhas), mantendo infuso por 10 minutos. Posteriormente, o extrato foi filtrado.
O bioindicador Allium sativum, em cada tratamento e repetições foram colocados em contato com o extrato aquoso de V. officinalis em copos plásticos descartáveis de 50 ml por 24, 48 e 72 horas, sendo coletadas as raízes do meristema apical de A. sativum com aproximadamente 5 a 10 mm de comprimento em cada horário referenciado e fixadas em etanol-ácido acético (3:1), posteriormente foram conservadas em refrigerador até o uso.
O experimento foi conduzido em delineamento inteiramente casualizado (DIC), sendo um tipo de extrato (EAI), quatro concentrações e dois tratamentos controle (água destilada e acetona), com 5 repetições cada.
Braz. J. of Develop.,Curitiba, v. 6, n.5, p.26982-26993 may. 2020. ISSN 2525-8761 No preparo das lâminas para avaliação do potencial citogenotóxico de V. officinalis, as raízes de A. sativum foram hidrolisadas em HCl 1N por 15 minutos e lavadas em água destilada por três vezes, durante cinco minutos cada lavada. A análise citogenética foi realizada segundo a técnica de esmagamento (Guerra & Souza, 2002), onde na confecção das lâminas utilizou-se o meristema apical das raízes, utilizou-sendo o material corado com, aproximadamente, 100 µl de orceína acética 2%. Com auxílio de um bastão de vidro o meristema foi fragmentado e, posteriormente, coberto com lamínula.
Foram preparadas dez lâminas por concentração, controle negativo e positivo. Foram analisadas 300 células por lâmina, totalizando 3.000 células por tratamento. As lâminas foram observadas, pelo método de varredura, em microscópio óptico, em magnitude de 400X, sendo que para cada lâmina foi registrado o número de células em cada fase do ciclo celular (intérfase, prófase, metáfase, anáfase e telófase), bem como, quando presentes, as alterações em cada uma delas.
O índice mitótico (IM) foi obtido por meio da equação IM = (nº de células em mitose/nº de células observadas) x 100.
A normalidade dos dados foi avaliada pelo teste de Lilliefors e os resultados referentes à variável IM foram transformados em Arco Seno √(x/100) onde x, representa o percentual de células em mitose (Vasconcelos et al., 2012). Os dados foram submetidos à análise de variância (ANOVA) e as médias comparadas pelo teste de Tukey (p ≤ 0,05). As análises estatísticas foram realizadas com auxílio do programa Genes (Cruz, 2016).
3 RESULTADOS E DISCUSSÕES
De acordo com a Tabela 1, os bulbos de Allium sativum responderam de forma distinta tanto ao extrato de V. officinalis quanto às concentrações testadas durante 24 horas e o aumento nas concentrações apresentou diminuição significativa na divisão celular, índice mitótico e células com irregularidades. O tratamento (T5) mostrou o maior número de divisões mitóticas e índice mitótico na dosagem de 10g/L, equiparando-se ao controle positivo (T6). Já os tratamentos (T2, T3 e T4) nas concentrações (2,5g/L, 5g/L e 7,5g/L) os números apontam semelhanças entre os respectivos valores. Dentre as fases da mitose, a Prófase e a Metáfase apresentaram valores superiores à Anáfase e Telófase. Bezerra et al. (2016), analisando efeitos tóxicos, citotóxicos, genotóxicos e mutagênicos em extratos da folha de Plectranthus barbatus em diferentes concentrações sobre o ciclo celular de Allium cepa, constatou em seus tratamentos diminuição significativa na divisão celular e índice mitótico. Para as células com
Braz. J. of Develop.,Curitiba, v. 6, n.5, p.26982-26993 may. 2020. ISSN 2525-8761 irregularidades, o controle positivo e o tratamento (T3) manifestou o maior número de células com anormalidades quando comparado aos demais tratamentos e controle negativo (Tabela 1). Estudos de citotoxicidade e genotoxicidade realizados em Allium cepa com dipirona e paracetamol apresentaram resultados semelhantes a este (Pinho et al., 2010).
Tabela 1 – Número de células de Allium sativum analisadas nos diferentes tratamentos e seus respectivos índices mitóticos, incluindo células em interfase, divisão celular e irregularidades durante 24 horas.
Tratamentos T1 T2 T3 T4 T5 T6 Céluas analisadas 3000 3000 3000 3000 3000 3000 Intérfase 2735 2845 2840 2860 2461 2600 Prófase 180 78 88 90 183 150 Metáfase 21 26 18 13 186 100 Anáfase 22 11 06 17 150 67 Telófase 42 26 17 17 02 40 Células c/ irregularidades 0 14 31 03 18 43 Índice Mitótico (%) 8,83% 5,1% 5,3% 4,6% 17,9% 13,3%
T1= Controle negativo (água destilada); T2= Chá de Valeriana 2,5g/L; T3= Chá Valeriana 5g/L; T4= Chá Valeriana 7,5g/L; T5= Chá Valeriana 10g/L e T6= Controle positivo (acetona). IM calculado pela regra de três simples.
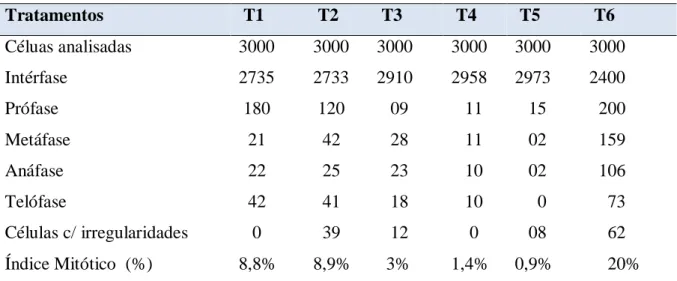
A Tabela 2 apresenta o total de células analisadas, bem como o número de células que foram observadas em cada uma das fases da divisão celular (mitose) de Allium sativum expostos ao extrato da folha do tipo infuso de V.officinalis. Observa-se que em todas as concentrações do extrato aquoso de V. officinalis, causou redução nas fases do ciclo celular, índice mitótico e células irregulares (Tabela 2). Esses resultados corroboram com estudos realizados em extratos aquosos de marcela, que inibiram significativamente a divisão celular em todas as concentrações da planta no sistema de Allium cepa (Fachinetto et al., 2007).
Braz. J. of Develop.,Curitiba, v. 6, n.5, p.26982-26993 may. 2020. ISSN 2525-8761
Tabela 2 – Número de células de Allium sativum analisadas nos diferentes tratamentos e seus respectivos índices mitóticos, incluindo células em interfase, divisão celular e irregularidades, durante 48 horas.
Tratamentos T1 T2 T3 T4 T5 T6 Céluas analisadas 3000 3000 3000 3000 3000 3000 Intérfase 2735 2733 2910 2958 2973 2400 Prófase 180 120 09 11 15 200 Metáfase 21 42 28 11 02 159 Anáfase 22 25 23 10 02 106 Telófase 42 41 18 10 0 73 Células c/ irregularidades 0 39 12 0 08 62 Índice Mitótico (%) 8,8% 8,9% 3% 1,4% 0,9% 20%
T1= Controle negativo (água destilada); T2= Chá de Valeriana 2,5g/L; T3= Chá Valeriana 5g/L; T4= Chá Valeriana 7,5g/L; T5= Chá Valeriana 10g/L e T6= Controle positivo (acetona). IM calculado pela regra de três simples.
A Tabela 3 com as mesmas concentrações anteriores aos tratamentos, expressa o número de células analisadas nas diferentes fases da divisão celular do meristema de Allium sativum. Os resultados apontam um maior número de células encontradas nos tratamentos (T3 e T6) em todas as fases da mitose. O índice mitótico demonstra diminuição significativa em relação ao aumento nas concentrações, exceto para os controles (NP) e tratamento (T3). Para as células com irregularidades o tratamento (T2) apresentou o maior número de células anormais e o tratamento (T3) mostrou zero anormalidade. Resultados semelhantes a esses foram encontrados em estudos realizados com o pó do mesocarpo da planta babaçu, na qual indicou inibição do índice mitótico e de todas as fases do ciclo celular, conforme aumento nas concentrações no sistema teste de Allium cepa (Silva et al., 2011).
Tabela 3 – Número de células de Allium sativum analisadas nos diferentes tratamentos e seus respectivos índices mitóticos, incluindo células em interfase, divisão celular e irregularidades, durante 72 horas.
Tratamentos T1 T2 T3 T4 T5 T6 Céluas analisadas 3000 3000 3000 3000 3000 3000 Intérfase 2735 2847 2299 2935 2954 2200 Prófase 180 55 62 19 18 230 Metáfase 21 29 213 24 09 210 Anáfase 22 11 182 0 04 167
Braz. J. of Develop.,Curitiba, v. 6, n.5, p.26982-26993 may. 2020. ISSN 2525-8761
Telófase 42 28 244 13 09 100
Células c/ irregularidades 0 30 0 09 06 93 Índice Mitótico (%) 8,8% 5,1% 23,3% 2,1% 1,5% 27%
T1= Controle negativo (água destilada); T2= Chá de Valeriana 2,5g/L; T3= Chá Valeriana 5g/L; T4= Chá Valeriana 7,5g/L; T5= Chá Valeriana 10g/L e T6= Controle positivo (acetona). IM calculado pela regra de três simples.
No teste de Allium sativum com o extrato seco de Valeriana nas concentrações (2,5g/L, 5g/L, 7,5g/L e 10g/L) em períodos de tempo (24, 48 e 72 horas), foi possível observar a toxicidade destes compostos em todos os tratamentos e fases da divisão mitótica, causando vários tipos de anormalidades. Em relação ao controle negativo (água destilada), não se observou nenhuma frequência anormal nas fases (Tabelas 1, 2 e 3). Bagatini et al. (2007), em estudos realizados com o gênero Achyrocline satureioides, popularmente conhecida como marcela, constatou em suas análises com os extratos da mesma a capacidade citotóxica, mas não genotóxica no sistema de Allium cepa.
Durante a análise das fotomicrografias das lâminas do experimento de Allium sativum, foi possível a visualização de aberrações cromossômicas (cromossomos soltos, fragmentos, pontes e cromossomos em atraso na anáfase) e células micronucleadas (Figura 1).
Figura 1 – Celulas mitóticas de Allium sativum obtida da exposição em diferentes concentrações da infusão de
V.officinalis . 1-Profase com formação de blocos cromossomos; 2-Profase com micronúcleo e Telófase com
Braz. J. of Develop.,Curitiba, v. 6, n.5, p.26982-26993 may. 2020. ISSN 2525-8761
com ponte e cromossomo isolado; 4- Metáfase com formação de cromossomos isolados; 5-Anáfase com cromossomo isolado; 6-Prófase com micronúcleo e cromossomo isolado.
As aberrações cromossômicas, segundo Costa e Teixeira (2012), são caracterizadas por modificações na estrutura ou no número de cromossomos, as quais podem ocorrer de forma espontânea ou serem resultantes de tratamentos com alguma substância.
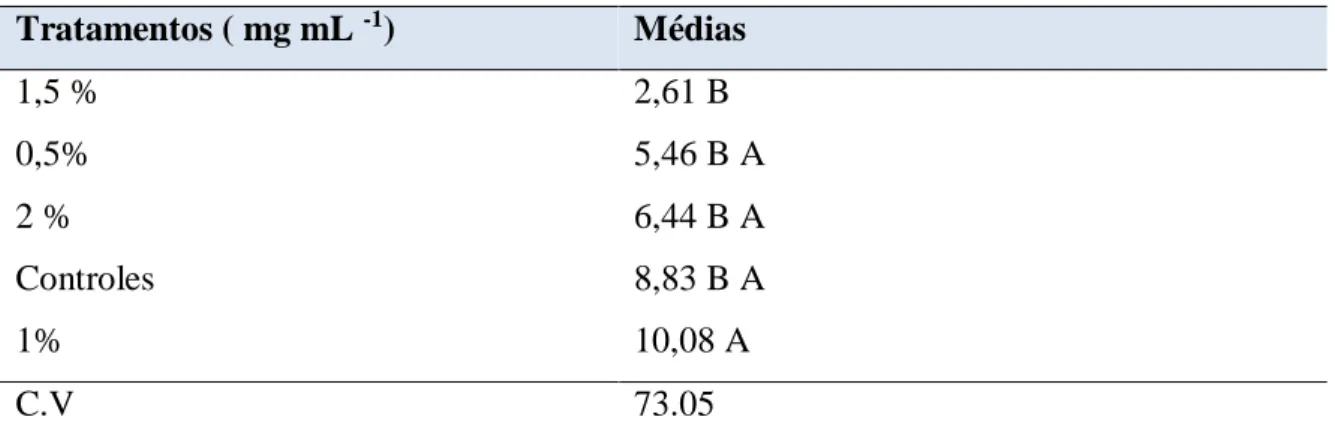
Tabela 4: Médias do efeito citotóxico das diferentes concentrações do extrato aquoso de valeriana sobre células da raiz de A. sativum. Tratamentos ( mg mL -1) Médias 1,5 % 2,61 B 0,5% 5,46 B A 2 % 6,44 B A Controles 8,83 B A 1% 10,08 A C.V 73.05
Médias seguidas pelas mesmas letras maiúsculas não diferem entre si pelo teste de Tukey a 1% de probabilidade. Controle negativo (água destilada), controle positivo (acetona).
Houve efeito significativo entre as diferentes concentrações com o chá de valeriana, conforme se observa na Tabela 4, pelo teste de Tukey. A concentração de 1% diferiu estatisticamente da concentração de 1,5%. Já as demais concentrações e controle negativo com água destilada não se diferiram estatisticamente.
Tabela 5: médias do efeito citotóxico de diferentes tempos de exposição de células radiculares de A. sativum sobre extrato aquoso de valeriana.
Tempo Médias
48 h 3,05 B
72 h 7,66 A
24 h 7,95 A
C.V 49.41
Médias seguidas pelas mesmas letras maiúsculas não diferem entre si pelo teste de Tukey a 1% de probabilidade.
Braz. J. of Develop.,Curitiba, v. 6, n.5, p.26982-26993 may. 2020. ISSN 2525-8761 Em se tratando dos horários em que as concentrações ficaram expostas, o tempo de (48h) diferiu estatisticamente das demais. Já para os horários de (24h e 72h), não diferiram entre si. Os dados originais foram transformados em arc sen x /100 e analisados estatisticamente. Diante do exposto, os resultados apresentados pelo teste, entre os horários e as concentrações com o chá de valeriana, indicam, assim, no composto a toxicidade. Isso se assemelha a estudos realizados na avaliação do potencial de genotoxidade por (Brambilla e Martelli, 2009).
A divergência entre concentrações de extratos aquosos da folha pode ser explicada tanto pela composição como pela quantidade de metabólicos extraídos. Considerando-se que a elevada temperatura na obtenção de EAI, podem provocar mudanças estruturais irreversíveis em substâncias termolábeis (Tiwari et al., 2011; Oliveira et al., 2016; Sá Jr. et al., 2016).
4 CONCLUSÃO
Os extratos aquosos do tipo infuso com as folhas Valeriana officinalis mostrou redução no processo de divisão do ciclo celular e índice mitótico em função do aumento nas concentrações testadas nas células meristemáticas de Allium sativum.
Valeriana officinalis apresentou em seu extrato com a folha no tipo infuso um potencial citotóxico sobre o teste de Allium sativum. Apontando um potencial genotóxico de alterações cromossômicas.
AGRADECIMENTOS
Os autores agradecem à Secretaria Municipal de Educação de Alta Floresta, ao Programa de Pós-Graduação em Genética e Melhoramento de Plantas. Laboratório de Genética Vegetal, Citogenética e Biologia Molecular da Universidade do Estado de Mato Grosso (UNEMAT) e a CAPES pelo apoio.
REFERÊNCIAS
BAGATINI, M. D.; SILVA, A. C. F.; TEDESCO, S. B. Uso do sistema teste de Allium cepa como bioindicador de genotoxicidade de infusões de plantas medicinais. Revista Brasileira de Farmacognosia, v. 17, n. 3, p. 444-447, 2007.
Braz. J. of Develop.,Curitiba, v. 6, n.5, p.26982-26993 may. 2020. ISSN 2525-8761 BEZERRA, C. M.; OLIVEIRA, M. A. S. Avaliação da toxicidade, citotoxicidade e genotoxicidade do infuso de malva-santa (Plectranthus barbatus Lamiaceae) sobre o ciclo celular de Allium cepa. Revista Eletrônica de Farmácia, v. 13, n. 4, p. 220-228, 2016.
BRAMBILLA, G.; MARTELLI, A. Genotoxicity and carcinogenicity studies of analgesics, anti-inflammatory drugs and antipyretics. Pharmacological Research, v. 60, n. 1, p. 1-17, 2009.
CABRERA, G. L.; RODRIGUES, D. M. G. Genotoxicity of soil from farmland irrigated with wastewater using three plant bioassays. A Mutation Research (MR), v. 426, n. 2, p. 211-214, 1999.
COSTA, C.; TEIXEIRA, J. P. Efeitos Genotóxicos dos Perticidas. Revista de Ciências Agrárias, v. 35, n. 2, p. 19-31, 2012.
CRUZ, C. D. Genes Software – extended and integrated with the R, Matlab and Selegen. Acta Sc. Agron, v. 38, n. 4, p. 547-552, 2016.
FACHINETTO, J. M.; BAGATINI, M. D.; DURIGON, J.; SILVA, A. C. F.; TEDESCO, S. B. Efeito anti-proliferativo das infusões de Achyrocline satureioides DC (Asteraceae) sobre o ciclo celular de Allium cepa. Revista Brasileira de Farmacognosia, v. 17, n. 1, p. 49-54, 2007.
FERREIRA FILHO, L. I. P. Estudo das alterações citogenômicas da medula óssea de trabalhadores rurais expostos a agrotóxicos. UFC – Departamento de Medicina Cliníca, 2013.
GRANT, W. F. Higher Plant Assays for the Detection of Chromosomal Aberations and Gene Mutations a Brief Historical Background on Their Use for Screening and Monitoring Environmental Chemicals. Mutation Research, Orlando, v, 426, n. 6, p. 107-112, 1999.
GUERRA, M.; SOUZA, M. L. Como observar cromossomos: um guia de técnicas em citogenética vegetal animal e humana. Ribeirão Preto: FUNPEC, p. 201, 2002.
Braz. J. of Develop.,Curitiba, v. 6, n.5, p.26982-26993 may. 2020. ISSN 2525-8761 MA, T. H.; XU, Z.; XU, C.; MCCONNELL, H.; RABAGO, E. V.; ARREOLA, G. A.; ZHANG, H. The Improved Allium/Vicia Root Tip Micronucleus Assay for Clastogeniciticy of Environmental Polluants. Mutation Research, Orlando, v. 334, n. 5, p. 185-195, 1995.
MORAES, J. Q.; NUNES, J. R. S.; PINHEIRO, A. P.; PESSOA, S. P. M. Etnobotânica de plantas medicinais com alunos do ensino médio de um colégio estadual de Tangará da Serra-MT. 3ª jornada científica da Unemat, Cáceres/MT Brasil, 20-24 setembro, 2010.
OLIVEIRA, V. B.; ZUCHETTO, M.; OLIVEIRA, C. F.; PAULA, A. F. S.; MIGUEL, M. D.; MIGUEL, O. G. Efeito de diferentes técnicas extrativas no rendimento, atividade antioxidante, doseamentos totais e no perfil por clae-dad de Dicksonia sellowiana (presl.). Hook, Dicksoniaceae. Revista Brasileira de Plantas Medicinais, v.18, n.1, p. 230-239, 2016.
PINHO, D. S.; STURBELLE, R. T.; MARTINHO-ROTH, M. G.; GARCIAS, G. L. Avaliação da atividade mutagênica da infusão de Braccharis trimera (Less.) DC. Em teste de Allium cepa e teste de aberrações cromossômicas em linfócitos humanos. Revista Brasileira de Farmacologia, v. 20, n. 2, p. 165-170, 2010.
SÁ JR. P. F.; MUNIZ, E. B.; PEREIRA, N. A.; OLIVEIRA, M. A. S. Atividade antimicrobiana in vitro dos extratos aquosos, hidroalcoólicos e alcoólicos de espécies da Anacardiaceae. Revista de Ciências Médicas e Biológicas, v. 15, n. 1, p. 56-61, 2016.
SILVA, A. P. S1.; MESQUITA, A. K. F2.; CAVALCANTE, A. A. 1.; NUNES, L. C. C. Avaliação Tóxica, Citotóxica e Genotóxica do Mesocarpo do Babaçu (Orbignya phalerata) Revista Environmental Toxicology and Pharmacology, Teresina –Pi, 2011.
SIMÕES, C. M. O.; SCHENKEL, E. P.; GOSMANN, G.; MELLO, J. C. P.; MENTZ, L. A.; PETROVICK, P. R. Farmacognosia: da planta ao medicamento, Porto Alegre: UFRGS, 5ª ed., 2003, 1102p.
VASCONCELOS, E. S.; REIS, M. S.; SEDIYAMA, T.; CRUZ, C. D. Estimativas de parâmetros genéticos da qualidade fisiológica de sementes de genótipos de soja produzidas em diferentes regiões de Minas Gerais. Semin. Ciênc. Agrár, v. 33, n. 1, p. 65-76, 2012.
Braz. J. of Develop.,Curitiba, v. 6, n.5, p.26982-26993 may. 2020. ISSN 2525-8761 VELOSO, D.; GUIDINI, P.; COMERIO, R. M. Plantas utilizadas em fitomedicamentos para os distúrbios do sono. Natureza on line, v. 6, n. 1, p. 29-35, 2008.
TIWARI, P.; KUMAR, B.; KAUR, M.; KAUR, G.; KAUR, H. Phytochemical screening and extraction: a review. Internationale Pharmaceutica Sciencia, v. 1, n. 1, p. 98-106, 2011.