UNIVERSIDADE DE SÃO PAULO
FACULDADE DE CIÊNCIAS FARMACÊUTICAS Programa de Pós-Graduação em Farmácia
Área de Análises Clínicas
POLIMORFISMOS DOS GENES LIGHT, MMP9, LT
α
, LGALS2,
VCAM1, ICAM1, E-SELECTINA E NF
κκκκ
B PODEM ESTAR
ASSOCIADOS COM DOENÇA ARTERIAL CORONARIANA
DÉBORA CAVICHIOLI
SÃO PAULO
- 2012 –
Dissertação para obtenção do grau de
MESTRE
Orientador:
UNIVERSIDADE DE SÃO PAULO
FACULDADE DE CIÊNCIAS FARMACÊUTICAS Programa de Pós-Graduação em Farmácia
Área de Análises Clínicas
POLIMORFISMOS DOS GENES LIGHT, MMP9, LT
α
, LGALS2,
VCAM1, ICAM1, E-SELECTINA E NF
κκκκ
B PODEM ESTAR
ASSOCIADOS COM DOENÇA ARTERIAL CORONARIANA
DÉBORA CAVICHIOLI
SÃO PAULO
- 2012 –
Dissertação para obtenção do grau de
MESTRE
Orientador:
Débora Cavichioli
Polimorfismos dos genes LIGHT, MMP9, LT
α
, LGALS2, VCAM1,
ICAM1, E-SELECTINA e NF
κ
B podem estar associados com doença
arterial coronariana
Comissão Julgadora da
dissertação para obtenção do grau de Mestre
Prof. Tit. Mario Hiroyuki Hirata Orientador/Presidente
____________________________ 1o. examinador
____________________________ 2o. examinador
Bom mesmo é ir a luta com determinação, abraçar a vida e viver com
paixão, perder com classe e viver com ousadia. Pois o triunfo pertence a
quem se atreve e a vida é muito bela para ser insignificante.
AGRADECIMENTOS
Aos meus pais, Antonio e Marlene, pela dedicação, confiança, por guiarem meu caminho e me apoiarem sempre.
Prof. Tit. Mario Hiroyuki Hirata, orientador e amigo, por todos os
ensinamentos, paciência, puxões de orelha, conselhos, preocupação, apoio e
confiança.
Profª. Tit. Rosário Dominguez Crespo Hirata, pelo incentivo, apoio e
sugestões no desenvolvimento deste projeto e demais atividades acadêmicas.
Cristina Moreno Fajardo, técnica do Laboratório de Biologia Molecular
Aplicada ao Diagnóstico da FCF/USP, sempre prestativa e paciente com todos os
alunos do laboratório.
Aécio Assunção Braga pelas longas horas no Pronto Socorro em busca de
pacientes e pelas infinitas extrações de RNA, quantificações e PCRs.
Aos alunos de aprimoramento e iniciação científica Lúcia Marie Simão,
Matheus Costa Almeida, Beatriz C. Lucas e Jessica Cassilla pela ajuda com
coletas, extrações, quantificações e experimentos.
Dra Vivian N. Silbiger e Dr. André D. Luchessi pelo apoio, confiança, ajuda
e conselhos.
Ao Instituto Dante Pazzanese de Cardiologia, em nome de sua diretora,
Dra. Amanda G.M.R. Souza, pelo acesso ao hospital e confiança.
Aos médicos e colaboradores do Instituto Dante Pazzanese de
Cardiologia, Dr. Fausto Feres, Dr. Ari Timerman, Dr. Marcelo Chiara Bertolami, Dr.
Marcelo Ferraz Sampaio, Dra. Elizabete Silva Santos, Dr. Luiz Minuzzo, Dr. Marcos
Paulo Pereira, Dr. Rui Fernando Ramos, Dra. Lara Reinel de Castro e Dr. Bruno
Sampaio Saba pela dedicação na seleção de pacientes e cuidados a eles
As amigas Paula Helena Lima, Adriana Regina Garófalo e Hui Tzu Lin Wang
pelo apoio, dedicação, conselhos e ajuda no desenvolvimento do meu trabalho.
Aos indivíduos que concordaram em participar deste estudo o meu muito
obrigado! Sem vocês este trabalho não poderia ser realizado.
Aos meus pais, Antonio José Cavichioli e Marlene Carvalho Cavichioli por
todo apoio e confiança depositados. Agradeço sempre por vocês terem me
guiado e por acreditarem nos meus sonhos. Agradeço a dedicação, amor,
carinho e paciência nesses anos de crescimento pessoal e profissional.
A Deus por me proteger e dar saúde para batalhar por mais essa
conquista e por colocar no meu caminho pessoas que me ajudaram a crescer
pessoalmente e profissionalmente.
Ao Conselho Nacional de Desenvolvimento Científico e Tecnológico –
CNPq, pela bolsa concedida.
A Fundação de Amparo a Pesquisa do Estado de São Paulo – FAPESP pelo
RESUMO
Cavichioli, D. Polimorfismos dos genes LIGHT, MMP9, LTα, LGALS2, VCAM1, ICAM1,
E-SELECTINA, NFκB podem estar associados com doença arterial coronariana.
INTRODUÇÃO: A síndrome coronariana aguda (SCA) constitui uma síndrome clínica geralmente causada por doença arterial coronariana (DAC) aterosclerótica e está associada ao infarto agudo do miocárdio (IAM) que pode muitas vezes levar a óbito. Aterosclerose é uma doença progressiva, sistêmica e de inicio precoce caracterizada pelo acúmulo de lipides e elementos fibrosos nas grandes artérias e recentemente foi considerada como uma afecção de origem inflamatória.
OBJETIVO: Avaliar a frequência genotípica de E-SELECTINA, MMP9, LIGHT, LTα, VCAM1, ICAM1, LGALS2 e NFκB em pacientes com infarto agudo
do miocárdio (IAM), angina instável (AI) e indivíduos que foram submetidos á angiocoronariografia e que apresentaram ausência de processo ateromatoso significativo. Assim como analisar a associação dos polimorfismos com a concentração sérica das formas solúveis das proteínas com a expressão gênica em leucócitos do sangue periférico, procurando estabelecer modelo de analise menos invasiva da aterosclerose.
CASUÍSTICA E MÉTODOS: O estudo foi realizado em um grupo de pacientes recrutados no Instituto Dante Pazzanese de Cardiologia (IDPC) com infarto agudo do miocárdio, angina instável e indivíduos que foram submetidos á angiocoronariografia e que apresentaram ausência de processo ateromatoso significativo. Foram incluídos no estudo 93 indivíduos sendo 47 com IAM com e sem supra ST compondo o grupo IAM e 46 com AI ou que foram submetidos á angiocoronariografia e que apresentaram ausência de processo ateromatoso significativo compondo o grupo SIAM, de ambos os sexos com idades entre 45 e 90 anos. Foi realizado o estudo dos polimorfismos dos genes LIGHT (rs344560 e
rs2291668), MMP9 (rs17576), LTα(rs909253 e rs1041981), LGALS2 (rs7291467),
VCAM1 (rs3176878), ICAM1 (rs281432), E-SELECTINA (rs5368) e NFκB
formas solúveis de VCAM1, ICAM1, E-SELECTINA e MMP9 utilizando o sistema
LUMINEX.
RESULTADOS: A frequência alélica e genotípica dos polimorfismos estudados (LIGHT [rs344560 e rs2291668], MMP9 [rs17576)] LTα [rs909253 e
rs1041981], LGALS2 [rs7291467], VCAM1 [rs3176878], ICAM1 [rs281432], E-SELECTINA [rs5368] e NFκB [rs17032705]) não apresentou relação com doença
arterial coronariana. Foi encontrada associação da expressão de LTα com
síndrome coronariana aguda (p<0,05) e relação de alguns dos polimorfismos estudados (6+3279C>T de LGALS2, 8+10029G>A de NFκB, 332-3499C>G de ICAM1, Lys178Glu de LIGHT e Asp693Asp de VCAM1) com alterações na expressão gênica, formas solúveis e parâmetros bioquímicos.
CONCLUSÕES: Não houve associação dos polimorfismos estudados com síndrome coronariana aguda assim como não houve associação das formas solúveis. Em relação á expressão gênica, foi encontrada associação da expressão de LTα com síndrome coronariana aguda (p<0,05) e alguns dos
polimorfismos estudados (6+3279C>T de LGALS2, 8+10029G>A de NFκB, 332-3499C>G de ICAM1, Lys178Glu de LIGHT e Asp693Asp de VCAM1) ocasionaram alterações da expressão gênica, formas solúveis e parâmetros bioquímicos.
ABSTRACT
Cavichioli, D. LIGHT, MMP9, LTα, LGALS2, VCAM1, ICAM1, E-SELECTINA, NFκB
polymorphisms may be associated with coronary artery disease.
BACKGROUND: Acute coronary syndrome (ACS) is a clinical syndrome usually caused by atherosclerotic coronary artery disease (CAD) and is associates with acute myocardial infarction (AMI) and sometimes can take to death. Atherosclerosis is a progressive disease characterized by the accumulation of lipides and fibrous elements in arteries and recently was considered a disease of inflammatory origin.
OBJECTIVE: Evaluated the genotypic frequency of E-SELECTIN, MMP9, LIGHT, LTα, VCAM1, ICAM1, LGALS2 e NFκB in patients with acute myocardial
infarction, unstable angina and individuals who were submitted to coronary angiography and had absence of significant atheromathous process. As well as analyze the polymorphism association with serum concentration of protein soluble forms with gene expression in peripheral blood leukocytes trying to establish a model less invasive to analyze atherosclerosis
MATERIALS AND METHODS: Study in a group of patients recruited in Dante Pazzanese of Cardiology Institute with acute myocardial infarction, unstable angina and in individuals who showed no significant atheromatous process. The study included 93 patients (47 with acute myocardial infarction and 46 with unstable angina or individuals who showed no significant atheromatous process) of both sexes with ages between 45 and 90 years. The genes polymorphisms study was by pyrosequencing, the gene expression was by PCR real time and soluble forms was dosage by LUMINEX.
RESULTS: The allelic and genotypic polymorphisms frequency studied (LIGHT [rs344560 e rs2291668], MMP9 [rs17576)] LTα [rs909253 e rs1041981],
LGALS2 [rs7291467], VCAM1 [rs3176878], ICAM1 [rs281432], E-SELECTINA
[rs5368] e NFκB [rs17032705]) don’t presented relation with coronary arterial
disease. Was found association with LTα gene expression and coronary acute
e Asp693Asp de VCAM1) with changes in gene expression, serum soluble forms and biochemical parameters.
CONCLUSION: Do not have association between polymorphisms studied and serum soluble forms with acute coronary syndrome. Was found association with LTα gene expression and coronary acute syndrome (p<0,05) and relation of
some polymorphism studied (6+3279C>T de LGALS2, 8+10029G>A de NFκB, 332-3499C>G de ICAM1, Lys178Glu de LIGHT e Asp693Asp de VCAM1) with changes in gene expression, serum soluble forms and biochemical parameters.
INDICE DE TABELAS
PÁGINAPÁGINAPÁGINAPÁGINA
TABELA 1 TABELA 1 TABELA 1
TABELA 1 ---- Biomarcadores para o diagnóstico de lesão miocárdica... 20202020
TABELA 2 TABELA 2 TABELA 2
TABELA 2 ---- Iniciadores utilizados nos ensaio de pirosequenciamento... 30303030
TABELA 3 TABELA 3 TABELA 3
TABELA 3 ---- Condições de amplificação pela PCR para pirosequenciamento... 33332222
TABELA 4 TABELA 4 TABELA 4
TABELA 4 ---- Número de catálogo dos ensaios utilizados na PCR em tempo real... 33334444
TABELA 5 TABELA 5 TABELA 5
TABELA 5 ---- Valores de inclinação da curva e eficiência dos ensaios de PCR em tempo real.... 33335555
TABELA 6 TABELA 6 TABELA 6
TABELA 6 ---- Características biodemográficas dos indivíduos do grupo IAM e SIAM... 33339999
TABELA 7 TABELA 7 TABELA 7
TABELA 7 ---- Perfil lipídico, bioquímico e hematológico dos indivíduos do grupo IAM e SIAM... 44441111
TABELA 8 TABELA 8 TABELA 8
TABELA 8 ---- Equilíbrio de Hardy-Weinberg... 44442222
TABELA 9 TABELA 9 TABELA 9
TABELA 9 ---- Distribuição da frequência alélica e genotípica dos SNPs... 44443333
TABELA 10 TABELA 10 TABELA 10
TABELA 10 ---- Blocos haplotípicos e frequência de associação dos genes LIGHT e LTα entre
os grupos IAM e SIAM... 44446666
TABELA 11 TABELA 11 TABELA 11
TABELA 11 ---- Expressão de mRNA em células do sangue periférico dos grupos IAM e SIAM... 44446666
TABELA 12 TABELA 12 TABELA 12
INDICE DE FIGURAS PÁGINA PÁGINAPÁGINA PÁGINA FIGURA FIGURA FIGURA
FIGURA 1111 ---- Esquema da implicação clínica da classificação das SCA... 18181818
FIGURA FIGURA FIGURA
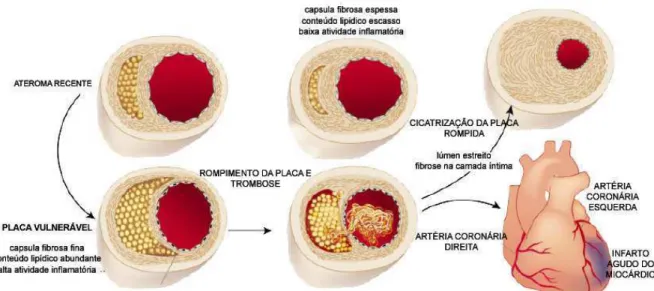
FIGURA 2222 ---- Modelo esquemático da formação da placa de ateroma... 19191919
FIGURA FIGURA FIGURA
FIGURA 3333 ---- Fotografia do gel de agarose a 1% do produto da PCR com gradiente de
temperatura de hibridização (TH) do gene LGALS2... 33332222
FIGURA FIGURA FIGURA
FIGURA 4444 ---- Blocos haplotípicos dos genes LIGHT (A) e LTα (B)... 45454545
FIGURA FIGURA FIGURA
FIGURA 5555 ---- Representação gráfica da expressão do mRNA dos genes LIGHT, LTα,
ICAM1, VCAM1, LGALS2 e NFκB em células do sangue periférico dos grupos IAM e SIAM 48484848
FIGURA FIGURA FIGURA
FIGURA 6666 ---- Representação gráfica da expressão do mRNA do gene MMP9 em células do
sangue periférico dos grupos IAM e SIAM... 49494949
FIGURA 7 FIGURA 7 FIGURA 7
FIGURA 7 ---- Representação gráfica das dosagens das formas solúveis no soro de MMP9,
ICAM1, VCAM1 e E-SELECTINA dos grupos IAM e SIAM... 50505050
FIGURA 8 FIGURA 8 FIGURA 8
FIGURA 8 ---- Representação gráfica da variação dos valores séricos de colesterol total em relação ao genótipo para o polimorfismo Thr60Asn (A) e -9-198A>G (B) de LTα e de ureia para o polimorfismo Hys468Tyr de E-SELECTINA (C) do grupo IAM...
53 53 53 53 FIGURA 9 FIGURA 9 FIGURA 9
FIGURA 9 ---- Representação gráfica da variação dos valores séricos de AST em relação ao genótipo para o polimorfismo 332-3499C>G de ICAM1 (A), de ureia para o polimorfismo Hys468Tyr de E-SELECTINA (B), de colesterol total (C), LDL-c (D) e Apo B (E) para o polimorfismo 332-3499C>G de ICAM1 e de LDL-c para o polimorfismo 111+36C>T de LIGHT (F) do grupo SIAM...
54 54 54 54
FIGURA 10 FIGURA 10 FIGURA 10
FIGURA 10 ---- Representação gráfica da variação da expressão gênica de ICAM em relação ao genótipo para o polimorfismo 6+3279C>T de LGALS2 (A), de NFκB para o polimorfismo 8+10029G>A de NFκB (B), de LGALS2 (C) e LTα (D) para o polimorfismo 332-3499C>G de ICAM1 e da variação das formas solúveis no soro de ICAM1 em relação ao genótipo para o polimorfismo 332-3499C>G de ICAM1 (E) e de E-SELECTINA para o polimorfismo Lys178Glu de LIGHT (F) para o grupo IAM...
FIGURA 11 FIGURA 11 FIGURA 11
FIGURA 11 ---- Representação gráfica da variação da forma solúvel no soro de VCAM1 em
relação ao genótipo para o polimorfismo Asp693Asp de VCAM1 do grupo IAM... 55558888
FIGURA 12 FIGURA 12 FIGURA 12
FIGURA 12 ---- Representação gráfica da variação da forma solúvel no soro de MMP9 em
LISTA DE ABREVIATURAS
aa aa aa
aa ---- aminoácidos
AI AI AI
AI –––– Angina Instável
ALT ALT ALT
ALT ---- Alanina Aminotransferase
Apo A Apo A Apo A
Apo A ---- Apolipoproteína A
Apo B Apo B Apo B
Apo B ---- Apolipoproteína B
AST AST AST
AST ---- Aspartato Aminotransferase
B2M B2M B2M
B2M –––– Beta 2-microglobulina
BCRE BCRE BCRE
BCRE ---- Bloqueio Completo de Ramo Esquerdo
CCS CCS CCS
CCS ---- Canadian Cardiovascular Society
cDNA cDNA cDNA
cDNA –––– Ácido Desoxirribonucleico complementar
CKMB CKMB CKMB
CKMB ---- Fração MB da creatinofosfoquinase
CML CML CML
CML ---- Células Musculares Lisas
C C C
CTTTT –––– Ciclo da linha de corte
DAC DAC DAC
DAC ---- Doença Arterial Coronariana
DATASUS DATASUS DATASUS
DATASUS ---- Banco de dados do Sistema Único de Saúde
DNA DNA DNA
DNA ---- Ácido Desoxirribonucleico
dNTP dNTP dNTP
dNTP –––– Desoxirribonucleotídeo Fosfato
EDTA EDTA EDTA
EDTA ---- Ácido Etilenodiaminotetracético
FCF FCF FCF
FCF ---- Faculdade de Ciências Farmacêuticas
FAM FAM FAM
FAM – Frequência do Alelo Menor
GAPDH GAPDH GAPDH
GAPDH –––– Gliceraldeído 3 fosfato desidrogenase
gl gl gl
HDL HDL HDL
HDL ---- Lipoproteína de alta densidade
HMBS HMBS HMBS
HMBS –––– Hidroximetilbilane sintase
HPRT1 HPRT1 HPRT1
HPRT1 –––– Hipoxantina Fosforibosiltransferase 1
IAM IAM IAM
IAM ---- Infarto Agudo do Miocárdio
ICAM ICAM ICAM
ICAM ---- Molécula de Adesão Intercelular
IDPC IDPC IDPC
IDPC ---- Instituto Dante Pazzanese de Cardiologia
IMC IMC IMC
IMC –––– Índice de Massa Corporal
LDL LDL LDL
LDL ---- Lipoproteína de baixa densidade
LGALS2 LGALS2 LGALS2
LGALS2 ---- Galectina 2
LIGHT LIGHT LIGHT
LIGHT – Ver TNFSF14
LTα LTα LTα
LTα ---- Linfotoxina alfa
MMP9 MMP9 MMP9
MMP9 ---- Metaloproteinase 9
MMPs MMPs MMPs
MMPs ---- Metaloproteinases
mRNA mRNA mRNA
mRNA –––– Ácido Ribonucléico mensageiro
NF NF NF
NFκκκκB B B B ---- Fator Nuclear Kappa B
OMS OMS OMS
OMS –––– Organização Mundial da Saúde
PCR PCR PCR
PCR ---- Reação em Cadeia da Polimerase
PCRus PCRus PCRus
PCRus ---- Proteína C Reativa ultra-sensível
RNA RNA RNA
RNA ---- Ácido Ribonucléico
SCA SCA SCA
SCA ---- Síndrome Coronariana Aguda
SDHA SDHA SDHA
SDHA –––– Complexo da succinato desidrogenase, subunidade A, flavoproteína (Fp)
SNPs SNPs SNPs
SNPs ---- Polimorfismos de um único nucleotídeo
SUS SUS SUS
TNFSF14 TNFSF14 TNFSF14
TNFSF14 ---- Fator de Necrose Tumoral 14
TSH TSH TSH
TSH ---- Hormônio tiroestimulante
TTTT4 4 4 4 livre livre livre livre –––– Fração livre da tiroxina
TTTTmmmm –––– Temperatura de Melting
UBC UBC UBC
UBC –––– Ubiquitina C
USP USP USP
USP ---- Universidade de São Paulo
UTR UTR UTR
UTR –––– Região não traduzida
VC VC VC
VCAM1 AM1 AM1 AM1 ---- Molécula de Adesão do sistema vascular
VLDL VLDL VLDL
VLDL ---- Lipoproteína de muito baixa densidade
X XX
SUMÁRIO
PÁGINAPÁGINAPÁGINAPÁGINA
1 INTRODUÇÃO ... 1 INTRODUÇÃO ... 1 INTRODUÇÃO ...
1 INTRODUÇÃO ... 11118888
2 OBJET 2 OBJET 2 OBJET 2 OBJETIVOS ...IVOS ...IVOS ...IVOS ... 22225555
2.1 OBJETIVOS GERAIS... 22225555
2.2 OBJETIVOS ESPECÍFICOS... 22225555
3 MATERIAIS E MÉTODOS ... 3 MATERIAIS E MÉTODOS ... 3 MATERIAIS E MÉTODOS ... 3 MATERIAIS E MÉTODOS ... 22226666
3.1 CASUÍSTICA... 22226666
3.2 AMOSTRAS BIOLÓGICAS... 22229999
3.3 DETERMINAÇÕES BIOQUÍMICAS... 22229999
3.4 ANÁLISE DOS POLIMORFISMOS... 3030 3030 3.5 ANÁLISE DA EXPRESSÃO GÊNICA... 33333333
3.6 ANÁLISE DAS CITOCINAS... 3636 3636
3.7 CONTROLE DE QUALIDADE DAS REAÇÕES... 3636 3636
3.8 ANÁLISE ESTATÍSTICA DOS DADOS... 3636 3636
4 RESULTADOS... 4 RESULTADOS... 4 RESULTADOS...
4 RESULTADOS... 3838 3838
4.1 CASUÍSTICA... 3838 3838
4.2 GENOTIPAGEM... 4141 4141
4.3 ANÁLISE DA EXPRESSÃO GÊNICA... 4646 4646
4.4 ANÁLISE DAS CITOCINAS SOLÚVEIS NO SORO... 4949 4949
4.5 ASSOCIAÇÃO DOS EFEITOS DOS POLIMORFISMOS NO PARAMETROS
BIOQUIMICOS E SÓCIO DEMOGRÁFICOS... 5050 5050
4.6 EFEITO DOS POLIMORFISMOS NA EXPRESSÃO GÊNICA E DOSAGEM DAS
5 DISCUSSÃO... 5 DISCUSSÃO... 5 DISCUSSÃO...
5 DISCUSSÃO... ... 5959 5959
6 LIMITAÇÕES DO ESTUDO... 6 LIMITAÇÕES DO ESTUDO... 6 LIMITAÇÕES DO ESTUDO...
6 LIMITAÇÕES DO ESTUDO... 7070 7070
7 CONCLUSÃO... 7 CONCLUSÃO... 7 CONCLUSÃO...
7 CONCLUSÃO... 7171 7171
REFERÊNCIAS BIBLIOGRÁFICAS... REFERÊNCIAS BIBLIOGRÁFICAS... REFERÊNCIAS BIBLIOGRÁFICAS...
REFERÊNCIAS BIBLIOGRÁFICAS... 7272 7272
APÊNDICES... APÊNDICES... APÊNDICES...
APÊNDICES... 8181 8181
ANEXOS... ANEXOS... ANEXOS...
18
1. INTRODUÇÃO
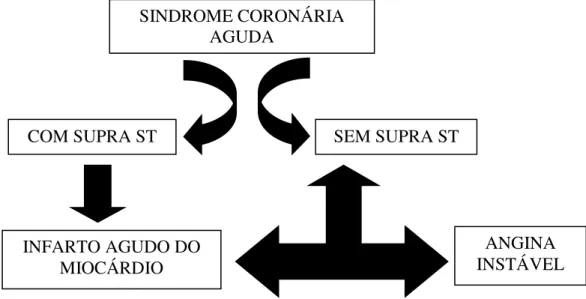
A síndrome coronariana aguda (SCA) constitui uma síndrome clínica geralmente causada por doença arterial coronariana (DAC) aterosclerótica e está associada ao infarto agudo do miocárdio (IAM) com alta morbidade e mortalidade (Erlichmann e Carvalho, 2007). A SCA é atualmente dividida entre aquelas que, além da apresentação clínica ao eletrocardiograma inicial há supradesnível persistente do segmento ST (SCA com supra ST) ou ausência de supradesnível persistente do segmento ST (SCA sem supra ST). No caso da SCA sem supra ST, o eletrocardiograma inicial pode revelar infradesnível do segmento ST, só alterações de repolarização (onda T) ou ser normal. Estas alterações refletem a gravidade da isquemia miocárdica subjacente que está associada ou não á necrose miocárdica, sendo chamada de IAM sem supra de ST ou Angina Instável (AI). Já a SCA com supra de ST é sempre um IAM, pois quase sempre está associada á necrose miocárdica (Erlichmann e Carvalho, 2007)
Aterosclerose é uma doença progressiva, sistêmica e de inicio precoce caracterizada pelo acúmulo de lipides e elementos fibrosos nas grandes artérias (Libby, 2002; Sampaio, 2005). Atualmente, entende-se o processo aterosclerótico não apenas como decorrência do acúmulo de lipides nas paredes dos vasos, mas também como consequência da disfunção endotelial e da ativação do sistema inflamatório (Libby, Okamoto et al., 2010).
Células do sistema imunológico dominam as lesões ateroscleróticas recentes e suas moléculas efetoras aceleram a progressão da lesão (Hansson,
Figura 1 – Esquema da implicação clínica da classificação das SCA Adaptado de (Erlichmann e Carvalho, 2007)
SINDROME CORONÁRIA AGUDA
COM SUPRA ST SEM SUPRA ST
INFARTO AGUDO DO MIOCÁRDIO
19
2005) devido à entrada de lipides e células inflamatórias na parede arterial levando a formação de um núcleo rico em gordura. Posteriormente, a secreção de citocinas e fatores de crescimento induzem á migração intimal e proliferação das células musculares lisas (CML) que participam decisivamente na formação da placa. Se as condições inflamatórias persistirem, o núcleo lipídico pode aumentar e a placa fica susceptível a ruptura (Libby, 2002; Sampaio, 2005).
Dois tipos de placas são importantes na determinação do risco de desencadeamento de isquemia aguda. As placas estáveis que apresentam escasso conteúdo lipídico, baixa atividade inflamatória e cápsula fibrosa espessa; e as placas vulneráveis, susceptíveis a trombose ou com alta probabilidade de progressão para oclusão da luz arterial (Sousa, Knobel et al., 2007).
Alguns fatores de risco para aterosclerose como, por exemplo, hipertensão, diabetes mellitus, tabagismo, obesidade, idade e sexo já estão bem definidos (Jan, Meng et al., 2010).
A taxa de mortalidade cardiovascular vem aumentando nos últimos anos e, de acordo com os dados do Sistema Único de Saúde (SUS) as mortes por IAM aumentaram 34% nos últimos 25 anos sendo que no ano de 2007 ocorreram cerca de 70 mil mortes por IAM no Brasil (Datasus). O estudo realizado no Instituto Dante Pazzanese de Cardiologia (IDPC) mostrou que a mortalidade hospitalar de pacientes com IAM é de 4,8% e, no ano de 2003, foram atendidos 832 pacientes sendo, 78 com diagnóstico de SCA com supra ST e 754 com diagnóstico de AI e/ou SCA sem supra ST (Dos Santos, Minuzzo et al., 2006).
20
Atualmente, para diagnóstico, estratificação de risco e tratamento de pacientes com síndromes isquêmicas são utilizados os seguintes biomarcadores (Singh, Martinezclark et al., 2010): CKMB (fração MB da creatinofosfoquinase)
massa, troponinas cardíacas e mioglobina.
Tabela 1 – Biomarcadores para o diagnóstico de lesão miocárdica
Biomarcador Inicio dos sintomas Pico Normalização
CKMB massa•••• 3-6 horas 16-24 horas 48-72 horas
Troponinas cardíacasº 4-8 horas 36-72 horas 5-14 dias
Mioglobina♦
1-2 horas 6-9 horas 12-24 horas
•Sensibilidade diagnóstica de 80% após 6 horas de evolução; ºMesma sensibilidade diagnóstica de
CKMM, ♦
Excelente para afastar o diagnóstico de IAM devido ao valor preditivo negativo que varia entre 83%-98% (Piegas, 2009).
Apesar da alta sensibilidade diagnóstica dos biomarcadores atuais, existe a necessidade de buscar marcadores complementares aos já existentes com o objetivo de aumentar a sensibilidade e especificidade no diagnostico da SCA.
Citocinas e moléculas de adesão têm sido analisadas como possíveis marcadores do processo aterosclerótico e correlacionadas com o aumento do risco para doença cardiovascular por apresentarem concentrações elevadas na corrente sanguínea de pacientes com síndromes isquêmicas (Filho, Filho et al.,
2005). A interação entre as citocinas inflamatórias e as células endotelais é um passo crítico na aterogênese levando á disfunção endotelial e inflamação promovendo o recrutamento adicional de células inflamatórias na parede do vaso (Sandberg, Halvorsen et al., 2009).
Estudos preliminares realizados pelo nosso grupo sugeriram uma forte participação de genes relacionados com resposta inflamatória indicando alguns como possíveis biomarcadores para o diagnóstico de SCA (Silbiger, 2010).
TNFSF14 (fator de necrose tumoral 14) também conhecido como LIGHT, é uma proteína transmembrana tipo II de 240 aminoácidos (aa), (Del Rio, Lucas et al., 2010) expresso por células T ativas e células dendríticas imaturas, induz
21
matriz, o acúmulo de lipídeos, formação de trombo e inflamação. Além disso, existem relatos de que LIGHT promove o aumento da expressão de quimiocinas e moléculas de adesão como VCAM1 (molécula de adesão do sistema vascular) e E-SELECTINA (Sandberg, Halvorsen et al., 2009).
A forma solúvel de LIGHT ativa as células endotelais e causa mudanças pró-trombóticas e inflamatórias e leva a um aumento da adesão de plaquetas ao endotélio. Pacientes com SCA com supra ST e AI possuem concentrações plasmáticas de LIGHT elevadas em comparação com pacientes normais (Liu, Fang et al., 2008).
Até o momento, não existem estudos correlacionando polimorfismos de LIGHT com DAC.
A família das metaloproteinases (MMPs) é composta por 20 enzimas divididas em 4 subgrupos: colagenases, estromelisinas, gelatinases e as metaloproteinases de membrana (Rowsell, Hawtin et al., 2002). As MMPs estão
presentes em diversos processos patológicos como inflamação, metástase tumoral, doenças respiratórias, lesão miocárdica, aneurisma vascular e remodelamento (Blankenberg, Rupprecht et al., 2003).
A MMP9 (metaloproteinase 9), também conhecida como gelatinase B ou 92kD colagenase tipo IV, é uma das MMPs altamente expressas em regiões vulneráveis a formação de placas ateroscleróticas e, por esta razão, sugere-se que esteja envolvida com processos de remodelamento associados com aterogênese e ruptura da placa (Rowsell, Hawtin et al., 2002; Blankenberg,
Rupprecht et al., 2003).
Diversos estudos genéticos observaram que alterações funcionais no gene da MMP9 estão relacionadas com a presença e severidade da doença cardiovascular. Uma troca de aminoácidos pode afetar a capacidade da proteína de se ligar ao seu substrato e levar a consequências na remodelação vascular e desestabilização da placa (Blankenberg, Rupprecht et al., 2003).
22
Sendo assim, a MMP9 poderia ser utilizada como um biomarcador circulante refletindo um estado pró-inflamatório ou como agente causador da desestabilização da placa (Blankenberg, Rupprecht et al., 2003).
A linfotoxina alfa (LTα), também conhecida como fator de necrose tumoral
beta (TNFB), é uma citocina pró-inflamatória, produzida nos estágios recentes da inflamação, que induz a adesão de moléculas e citocinas ao endotélio vascular (Tanaka e Ozaki, 2006; Li, Xu et al., 2010; Liu, Sheng et al., 2011).
A galectina 2 (LGALS2) está envolvida no trafico intracelular, modula a secreção de citocinas e adesão celular, codifica uma proteína envolvida na cascata da LTα e é expressa juntamente com a LTα na placa aterosclerótica
(Mangino, Braund et al., 2007; Li, Xu et al., 2010).
Polimorfismos no gene da LTα aumentam a expressão e os níveis
plasmáticos de várias citocinas em pacientes com DAC, como VCAM1 e E-SELECTINA, que também estão envolvidas no processo aterosclerótico, mostrando que têm um papel direto na progressão da doença (Liu, Sheng et al.,
2011).
Polimorfismos no gene da LGALS2 afetam a transcrição e causam alterações nas concentrações plasmáticas de LTα afetando o grau de inflamação
(Tanaka e Ozaki, 2006; Mangino, Braund et al., 2007).
Estudos mostram resultados inconclusivos ao verificar a associação dos
polimorfismos de LTα e LGALS2 com DAC. Na população americana LGALS2 foi
associada com DAC em mulheres e na população britânica não teve associação
já na população chinesa foi visto que polimorfismos no gene da LTα aumentam o
risco de IAM (Asselbergs, Pai et al., 2007; Mangino, Braund et al., 2007; Gao,
Zhang et al., 2010). Esses resultados ainda são controversos já que houve
influência de diversos fatores como, por exemplo, o número amostral, seleção dos grupos para o estudo e sabe-se que diferentes etnias têm respostas genéticas diferentes sendo assim, mais estudos são necessários para confirmar, ou não, essa associação.
Até o momento, não foi realizado nenhum estudo de associação destes genes na população brasileira.
A molécula de adesão intercelular 1 (ICAM1) é uma glipoproteína de superfície de 95kD (Jiang, Klein et al., 2002) que, juntamente com VCAM1 é
23
de leucócitos ao endotélio e, raramente, são expressas em artérias coronárias normais (Lu, Sheng et al., 2010).
E-SELECTINA é uma glicoproteína de superfície de 11kD (Wang, Liu et al.,
2010), é responsável pela adesão de neutrófilos, monócitos, eosinófilos e basófilos ao endotélio (Macias, Villaescusa et al., 2003). Geralmente não é
possível detecta-la quando não há ativação de células endoteliais mas, quando há estímulos pro inflamatórios, é rapidamente sintetizada em resposta a diversas citocinas (Wang, Liu et al., 2010).
As concentrações da forma solúvel de VCAM1 em pacientes com SCA é maior que a de pacientes com AI ou controles (Derhaschnig e Jilma, 2009) e, foi observado que a concentração da forma solúvel de ICAM1 aumenta anos antes de ocorrer o primeiro IAM (Jiang, Klein et al., 2002).
As concentrações de ICAM1 e E-SELECTINA na circulação periférica encontram-se elevadas em pacientes com IAM. Os picos de E-SELECTINA ocorrem de 4 a 6 horas após o inicio do evento e voltam aos valores basais em até 24 horas o que a torna um possível biomarcador se utilizada juntamente com os já existentes (Macias, Villaescusa et al., 2003).
Um estudo realizado por Filho e colaboradores observou que as dosagens de ICAM1, VCAM1 e E-SELECTINA no sangue periférico refletem diretamente os níveis dessas moléculas na circulação coronariana legitimando o uso de amostras periféricas para monitoramento e estratificação do risco em DAC (Filho, Filho et al., 2005).
O fator nuclear kappa B (NFκB) regula genes envolvidos na resposta imune e inflamatória (Collins, Read et al., 1995), desencadeia a transcrição de genes
resultando na liberação e ativação de citocinas, quimiocinas e moléculas de adesão (ex. ICAM1, VCAM1 e E-SELECTINA) (Collins e Cybulsky, 2001; Pare, Ridker et al., 2011), está envolvido em diversos processos como apoptose,
diferenciação e proliferação celular, apresenta expressão e atividade aumentadas em regiões propensas a desenvolver placas ateroscleróticas (Orr, Sanders et al.,
24
Pouco se sabe sobre o efeito de polimorfismos no gene NFκB em DAC. Na tentativa de contribuir para o conhecimento de alguns mecanismos moleculares envolvidos na fisiopatologia da doença cardiovascular, este trabalho teve como objetivo avaliar a frequência genotípica de E-SELECTINA (rs5368), MMP9 (rs17576), LIGHT (rs344560 e rs2291668), LTα (rs909253 e rs1041981),
VCAM1 (rs3176878), ICAM1 (rs281432), LGALS2 (rs7291467) e NFκB
25 2. OBJETIVOS
2.1. OBJETIVOS GERAIS
Avaliar a frequência genotípica de E-SELECTINA (rs5368), MMP9
(rs17576), LIGHT (rs344560 e rs2291668), LTα (rs909253 e rs1041981), VCAM1
(rs3176878), ICAM1 (rs281432), LGALS2 (rs7291467) e NFκB (rs17032705) em
pacientes com IAM, AI e indivíduos que foram submetidos á angiocoronariografia e que apresentaram ausência de processo ateromatoso significativo. Assim como analisar a associação dos polimorfismos com a concentração sérica das formas solúveis das proteínas com a expressão gênica em leucócitos do sangue periférico, procurando estabelecer um modelo menos invasivo de analise da aterosclerose.
2.2. OBJETIVOS ESPECÍFICOS
2.2.1. Determinar a frequência alélica e genotípica dos polimorfismos dos genes LIGHT (rs344560 e rs2291668), MMP9 (rs17576), LTα (rs909253 e
rs1041981), LGALS2 (rs7291467), VCAM1 (rs3176878), ICAM1 (rs281432), E-SELECTINA (rs5368) e NFκB (rs17032705) em pacientes com IAM, AI e
indivíduos que foram submetidos á angiocoronariografia e que apresentaram ausência de processo ateromatoso significativo.
2.2.2. Avaliar o efeito dos polimorfismos dos genes LIGHT, MMP9, LTα, LGALS2, VCAM1, ICAM1 e NFκB sobre a expressão do mRNA (ácido
ribonucleico mensageiro) em células mononucleares periféricas de pacientes com IAM, AI e indivíduos que foram submetidos á angiocoronariografia e que apresentaram ausência de processo ateromatoso significativo.
2.2.3. Associar as variações das concentrações séricas solúveis de
MMP9, VCAM1, ICAM1 e E-SELECTINA com os polimorfismos dos mesmos em
26
3. MATERIAIS E MÉTODOS
3.1. CASUÍSTICA
O estudo foi desenvolvido no Pronto Socorro, Hemodinâmica e Laboratório de Biologia Molecular do Instituto Dante Pazzanese de Cardiologia do Estado de São Paulo (IDPC) e Laboratório de Biologia Molecular Aplicada ao Diagnostico da Faculdade de Ciências Farmacêuticas da Universidade de São Paulo (FCF-USP).
O projeto foi aprovado pelo Comitê de Ética em Pesquisa do IDPC e da FCF-USP, conforme expresso pela Comissão Nacional de Ética em Pesquisa (Anexo A). Os indivíduos foram informados, pelo investigador principal ou membro da equipe colaboradora designada por ele, sobre os objetivos da pesquisa desenvolvida neste trabalho. Somente participaram do estudo aqueles que assinaram o Termo de Consentimento Livre e Esclarecido (Apêndice A).
3.1.1. CARACTERÍSTICAS DO GRUPO COM INFARTO
AGUDO DO MIOCÁRDIO (IAM)
Foram incluídos no estudo, 47 indivíduos de ambos os sexos com idades entre 45 e 90 anos com infarto agudo do miocárdio com e sem supra ST que faziam parte da rotina do Pronto Socorro do IDPC.
Todos os indivíduos incluídos neste grupo foram abordados um dia após a internação devido ao grande fluxo de pacientes no Pronto Socorro do IDPC. Para minimizar as diferenças dos resultados, todas as coletas foram realizadas no período da manhã seguinte a internação. Consequentemente, todos estavam sob uso de medicação tais como: ácido acetil salicílico, clopidogrel, atenolol ou carvedilol ou metoprolol, clexane ou heparina não fracionada, captopril ou enalapril ou losartan, sinvastatina, nitroglicerina ou propatilnitrato ou mononitrato de isossorbida.
27
viabilidade miocárdica ou contratilidade segmentar anormal (Thygesen, Alpert et al., 2007; Anderson, Adams et al., 2008).
3.1.2. CARACTERÍSTICAS DO GRUPO SEM INFARTO
AGUDO DO MIOCÁRDIO (SIAM)
Foram incluídos no estudo, 44 indivíduos com idades entre 45 e 90 anos, de ambos os sexos que foram submetidos a cineangiocoronariografia, por apresentarem sintomas clínicos indicativos de doença coronariana, na Hemodinâmica do IDPC e indivíduos com AI. Como angina instável admite-se uma variedade de apresentações clínicas que tradicionalmente podem ser distinguidas da seguinte forma: a) angina prolongada em repouso (> 20 minutos), b) novo episódio anginoso severo (classe III pela classificação da Canadian Cardiovascular Society – CCS), c) recente instabilização de angina prévia com
características de classe III pela CCS (angina em crescendo) e d) angina pós-infarto do miocárdio. As alterações eletrocardiográficas que tiveram relevância no diagnóstico de Angina Instável foram: a) infra-desnível de segmento ST < 0,5mm (< 0,05 mV) e b) inversão de onda T < 2 mm (< 0,2mV) (Anderson, Adams et al.,
2008). O critério de seleção para os indivíduos que foram submetidos a cineangiocoronariografia foi a ausência de lesão ateromatosa significativa.
Os indivíduos com AI foram abordados um dia após a internação devido ao grande fluxo de pacientes no Pronto Socorro do IDPC. Para minimizar as diferenças dos resultados, todas as coletas foram realizadas no período da manhã seguinte a internação. Consequentemente, todos estavam sob uso de medicação tais como: ácido acetil salicílico, clopidogrel, atenolol ou carvedilol ou metoprolol, clexane ou heparina não fracionada, captopril ou enalapril ou losartan, sinvastatina, nitroglicerina ou propatilnitrato ou mononitrato de isossorbida.
Já os indivíduos que foram submetidos a angiocoronariografia foram orientados a permanecer 12 horas de jejum.
3.1.3. CRITÉRIOS DE EXCLUSÃO
28
Para avaliação destas condições, aplicou-se um questionário aos indivíduos (Apêndice B) e, foram realizados os seguintes testes de triagem: glicemia, colesterol total e frações (HDL – lipoproteína de alta densidade, LDL – lipoproteína de baixa densidade e VLDL – lipoproteína de muito baixa densidade), triacilglicerol, apolipoproteína A e B (Apo A e Apo B), ureia, creatinina, AST (aspartato aminotransaminase), ALT (alanina aminotransaminase), PCRus (proteína C reativa ultra-sensível), T4 livre (fração livre da tiroxina), TSH (
thyroid-stimulating hormone – hormônio estimulante da tireoide) e hemograma completo.
3.1.4. VARIÁVEIS ANALISADAS
Os seguintes fatores de risco para doença arterial coronariana foram avaliados em todos os grupos:
1. Hipertensão Arterial: Conforme a V Diretriz Brasileira de Hipertensão Arterial, foram considerados hipertensos pacientes em uso de
medicação anti-hipertensiva ou que apresentaram pressão arterial
≥140x90mmHg (Júnior, 2006);
2. Diabetes Mellitus: Foram considerados diabéticos pacientes em uso de hipoglicemiantes orais, recebendo terapia com insulina ou que apresentaram glicose plasmática em jejum ≥126mg/dL ou glicemia de 2
horas ≥200mg/dL ((Who), 2006);
3. Tabagismo: Foram considerados tabagistas fumantes ativos, ou seja, com consumo mínimo de 1 (um) cigarro por dia, pelo menos por um ano ou que fumou no ano anterior á inclusão na pesquisa. Não fumante aquele que nunca fumou ou que parou de fumar a mais de um ano (Silva, Sousa et al., 1998);
4. Obesidade: O critério de obesidade foi baseado na Classificação Internacional da Organização Mundial da Saúde (OMS) de acordo com
o cálculo do índice de massa corporal (IMC). O índice foi calculado dividindo o peso, em quilogramas, pelo quadrado da altura, em metros. Foram considerados obesos os indivíduos que apresentaram IMC
≥30Kg/m2 ((Who)),
5. Sedentarismo: Foram considerados sedentários indivíduos que não praticavam atividade física regularmente.
29
3.2. AMOSTRAS BIOLÓGICAS
Os indivíduos dos dois grupos foram submetidos a uma única coleta de sangue na qual foram realizados os seguintes exames laboratoriais: glicemia, colesterol total e frações (HDL, LDL e VLDL), triacilglicerol, apolipoproteína A e B, ureia, creatinina, AST, ALT, PCRus, T4 livre, TSH e hemograma completo. Nessa
coleta foram obtidos aproximadamente 40mL de sangue utilizando o sistema de coleta a vácuo Vacutainer® (BD, Nova Jersey, EUA) sendo:
a. Quatro tubos (4mL) com anticoagulante EDTA (ácido etilenodiaminotetracético) para: extração de DNA (ácido desoxirribonucleico) genômico para detecção dos polimorfismos; extração de mRNA (ácido ribonucleico mensageiro) para análise da expressão gênica e hemograma completo;
b. Quatro tubos (5mL) com ativador de coágulo e gel separador e um tubo (4mL) com anticoagulante Heparina para: dosagens bioquímicas, atividades enzimáticas no soro e armazenamento do soro e plasma, para dosagens de proteínas e marcadores inflamatórios (mantidos a -20ºC)
3.3. DETERMINAÇÕES BIOQUIMICAS
Os exames laboratoriais foram realizados em colaboração com o Laboratório de Análises Clínicas do IDPC. Para realização da analise da série vermelha, branca e de plaquetas foi utilizado método citoquimico/isovolumétrico ou de impedância automatizados ABX Pentra 120 (ABX, Kyoto, Japão) e ABX Pentra 80 (ABX, Kyoto, Japão).
Para análise de AST, ALT, CK e CKMB (atividade), glicemia, ureia, creatinina, sódio, potássio, colesterol total, HDL e triacilglicerol foram utilizados os métodos colorimétricos e enzimáticos automatizados Dimension® RXL (Siemens
Healthcare Diagnostics, Deerfield, USA) e XPAND (Siemens Healthcare
Diagnostics, Deerfield, USA). O VLDL e LDL foram calculados, segundo a fórmula de Friedewald e colaboradores (Friedewa.Wt, Fredrick.Ds et al., 1972).
Para análise do TSH e T4 livrefoi utilizado o método de quimiluminescência
30
Para dosagens da PCRus, apo A e apo B foi utilizado o método de imunoensaio-turbidimétrico automatizado, com leitura no aparelho Hitachi-modelo 912 (Myco instrumentation, Renton, WA).
3.4. ANÁLISE DOS POLIMORFISMOS
3.4.1. EXTRAÇÃO DO DNA GENÔMICO
O DNA genômico dos 91 indivíduos incluídos no estudo foi obtido a partir do sangue total periférico, colhido com EDTA. O material foi extraído no equipamento QIAcube® (QIAGEN, GmbH, Alemanha) utilizando o QIAamp® DNA Blood Mini Kit (QIAGEN, GmbH, Alemanha), seguindo as orientações do
fabricante. A quantificação e análise do grau de pureza (relação A260/A280) do DNA
extraído foi realizada no NanoDrop® ND-1000 Spectrophotometer (Thermo Fisher
Scientific Inc. Wilmington, EUA). Foram utilizadas somente preparações de DNA que obtiveram relação A260/A280 entre 1,8 e 2,0 (Sambrook e Russel, 2001).
3.4.2. DETERMINAÇÃO DOS SNPS
(PIROSEQUENCIAMENTO)
A escolha dos SNPs (polimorfismos de um único nucleotídeo) a serem determinados pelo sistema PyroMarq Q24 (QIAGEN, GmbH, Alemanha) foi
realizada utilizando o banco de dados públicos dbSNP
(http//:www.ncbi.nlm.nih.gov). Os critérios como frequência do alelo menor (FAM) superior a 0,05% para SNPs presentes em regiões codificantes e superior 0,1% para SNPs presentes em regiões regulatórias como promotoras, 3’UTR (untranslated region – região não traduzida), 5’UTR e splicing foram utilizados
como argumento de busca. Os iniciadores para a PCR (reação em cadeia da polimerase) e reação de pirosequenciamento foram construídos utilizando o programa PyroMark Assay Desing 2.0 (QIAGEN, GmbH, Alemanha). Para cada
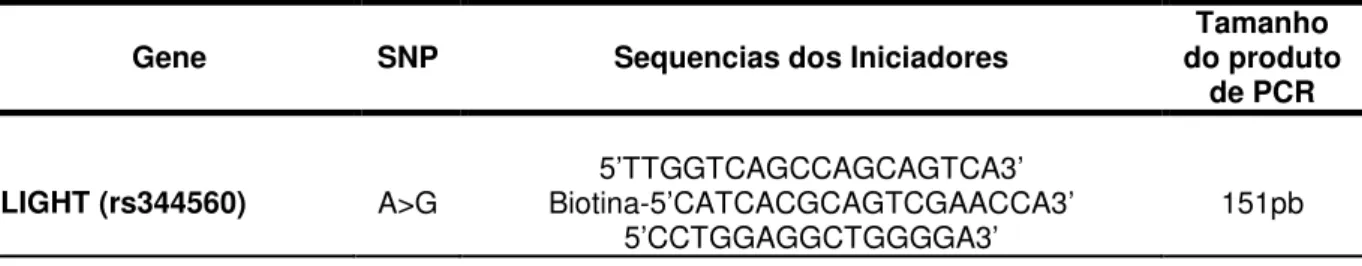
SNP, foram construídos três iniciadores, sendo que um deles é obrigatoriamente marcado com biotina totalizando 30 oligonucleotídeos. As sequencias dos iniciadores e os polimorfismos estudados encontram-se na tabela 2.
Tabela 2 - Iniciadores utilizados nos ensaio de pirosequenciamento.
Gene SNP Sequencias dos Iniciadores do produto Tamanho de PCR
5’TTGGTCAGCCAGCAGTCA3’
31
5’GGGTGGGTCTGGGTCTCTT3’
LIGHT (rs2291668) C>T Biotina-5’GGGTGACCATCTCTCCTAGACG3’ 102pb 5’CTGTTGCTGATGGGG3’
Biotina-5’ AAGGGGACAAGATGCAGTCA3’
LTα (rs909253) C>T 5’ GCTTCGTGCTTTGGACTACC3’ 276pb
5’CTCTGTTTCTGCCATG3’ Biotina-5’ATGCATCTTGCCCACAGC3’
LTα (rs1041981) A>C 5’AGGTGGATGTTTACCAATGAGG3’ 60pb
5’GAGCAGCAGGTTTGAG3’ Biotina-5’TCTCCCCCTTTCCCACATC3’
MMP9 (rs17576) A>G 5’GCAGGGTTTCCCATCAGC3’ 73pb
5’TCAGCATTGCCGTCC3’ 5’GCTGTGAGGAGGGATTTGAATT3’
E-SELECTINA (rs5368) C>T Biotina-5’CTTTGGGGCAATCTAGGTTCAG3’ 166pb 5’GAGGAGGGATTTGAATTA3’
5’GGCAACAAAGCAAGACTGTCTC3’
NFκκκκB (rs17032705) A>G Biotina-5’CAGTGCTGCCAGTGTTCTATTTC3’ 200pb 5’GGTGAACACGTTTAACCTA3’
Biotina-5’GCCACACAGACACTCACAGACGT3’
LGALS2 (rs7291467) A>G 5’AGGGAGCCATCTCCTGATGC3’ 74pb
5’CCTGATGCTTGGTGTTA3’ 5’CCATTTTGTTATTTTCCAGGAAGA3’
VCAM1 (rs3176878) C>T Biotina-5’TGGCAGGTATTATTAAGGAGGATG3’ 97pb 5’GGAAGAGAAAACAACAAA3’
5’GTGGAGGAGCTGGGACTTTC3’
ICAM1 (rs281432) C>G Biotina-5’TTCCAGTAAATCCAGCCTTCAGC3’ 99pb 5’GGAGTCATGGAGGGT3’
O protocolo inicial de otimização da PCR foi correspondente a Pyromark PCR Master Mix, CoralLoad Concentrate, 200ηM de cada iniciador, 10ηg de DNA
em uma reação com volume final de 25µl.
Para determinar a temperatura de hibridização dos iniciadores foi realizado um gradiente de temperatura onde, varia-se a temperatura de desnaturação (Tm).
E, para escolha da melhor temperatura de hibridização, foi realizada uma corrida eletroforética dos produtos da PCR em gel de agarose 1%.
32
bandas inespecíficas acima ou abaixo e de intensidade forte e homogênea que foi a coluna 5. Neste caso, a melhor temperatura de hibridização foi de 66ºC.
A tabela 3 resume as condições otimizadas e amplificação pela PCR para os polimorfismos estudados.
Tabela 3 – Condições de amplificação pela PCR para os polimorfismos dos genes LIGHT, LTA, MMP9, E-SELECTINA, NFKB, LGALS2, VCAM1 e ICAM1.
Polimorfismo Desnaturação Hibridação Extensão Ciclos
LIGHT A>G 94ºC/30seg 60ºC/30seg 72ºC/30seg 45
LIGHT C>T 94ºC/30seg 61ºC/30seg 72ºC/30seg 45
LTα C>T 94ºC/30seg 61ºC/30seg 72ºC/30seg 45
LTα A>C 94ºC/30seg 61ºC/30seg 72ºC/30seg 45
MMP9 A>G 94ºC/30seg 61ºC/30seg 72ºC/30seg 45
E-SELECTINA C>T 94ºC/30seg 61ºC/30seg 72ºC/30seg 45
NFκκκκB A>G 94ºC/30seg 61ºC/30seg 72ºC/30seg 45
LGALS2 A>G 94ºC/30seg 66ºC/30seg 72ºC/30seg 45
VCAM1 C>T 94ºC/30seg 60ºC/30seg 72ºC/30seg 45
ICAM1 C>G 94ºC/30seg 62ºC/30seg 72ºC/30seg 45
O protocolo para reação de pirosequenciamento consiste em purificação dos produtos da PCR, isolamento da fita (do produto da PCR) sintetizada com o iniciador marcado com a biotina, mistura através do sistema á vácuo dos produtos
M
2 3 4 5 6
33
purificados com os reagentes de pirosequenciamento (álcool 70%, solução de desnaturação e tampão de lavagem), adição dos nucleotídeos de acordo com a ordem de dispensação criada pelo programa PyroMark Assay Desing 2.0 e,
captura do sinal fluorescente pelo sistema a cada adição de nucleotídeos.
3.5. ANÁLISE DA EXPRESSÃO GÊNICA
3.5.1. EXTRAÇÃO DO RNA TOTAL
O RNA (ácido ribonucleico) de leucócitos totais dos 91 indivíduos incluídos no estudo foi extraído no equipamento QIAcube® (QIAGEN, GmbH, Alemanha)
utilizando o QIAamp® RNA Blood Mini Kit (QIAGEN, GmbH, Alemanha),
imediatamente após a colheita de sangue periférico, seguindo as orientações do fabricante. A quantificação e análise do grau de pureza (relação A260/A280) do RNA
obtido foi realizada no NanoDrop® ND-1000 Spectrophotometer (Thermo Fisher
Scientific Inc. Wilmington, EUA). Foram utilizadas somente preparações de RNA que apresentaram valores da relação A260/A280 entre 1,8 e 2,0 (Sambrook e
Russel, 2001).
3.5.2. ANÁLISE DA EXPRESSÃO DO mRNA PELA RT
SEGUIDA DA PCR EM TEMPO REAL
A quantificação da expressão do mRNA dos genes LIGHT, LTα, MMP9,
NFκB, LGALS2, ICAM1 e VCAM1 foi realizada por transcrição reversa do mRNA seguida de PCR (RT-qPCR) em tempo real, utilizando o sistema de amplificação
TaqMan Two Step RT-PCR (Life Technologies, Forest City, USA).
A primeira etapa consiste da síntese de cDNA (ácido desoxirribonucleico complementar) a partir de 200ηg de RNA, na presença de 200ηg de iniciadores aleatórios (random primers), DTT 20mM (Life Technologies, Forest City, USA),
200µM dNTP (Amersham-Pharmacia Biotech do Brasil, Brasil), 10.000U de transcriptase reversa (SuperScriptTM II RT RNase H-) e tampão RT (Tris-HCl 250mM pH 8,3, KCl 375mM, MgCl2 15mM) (Life Technologies, Forest City, USA).
A mistura foi incubada por 10 min a 25ºC, seguida de 50 min a 42ºC e 15 min a 70ºC. O cDNA obtido foi armazenado a -20ºC até a realização da qPCR.
Na segunda etapa, o cDNA de cada gene foi amplificado pela PCR em tempo real, utilizando-se iniciadores e sondas de detecção marcadas com FAM adquiridos no formato “TaqMan® Gene Expression Assay” (Life Technologies,
34
serem utilizados e identificados pelos números de catálogo de acordo com a
tabela 4.
Tabela 4 - Número de catálogo dos ensaios utilizados (iniciadores + sondas).
Gene Número de Catalogo
LIGHT Hs00542477_m1
MMP9 Hs00957562_m1
LTα Hs00608020_g1
NFκB Hs00231653_m1
ICAM1 Hs00164932_m1
VCAM1 Hs00174239_m1
LGALS2 Hs00197810_m1
GAPDH Hs00266705_g1
Os demais reagentes da PCR foram: solução denominada Master Mix
(MgCl2 25mM, dNTPs 10mM, AmpEraseR UNG 30U, enzima AmpliTaq Gold 150U
e tampão da reação) (Life Technologies, Forest City, USA). Para uso, essa solução foi diluída 2 vezes. O volume final foi de 10µl por reação e os ensaios foram realizados em duplicata.
O programa da PCR em tempo real foi constituído de: (1) um ciclo de 2 min a 50ºC (ativação da UNG); (2) um ciclo de 10 min a 95ºC (inativação da UNG); (3) 40 ciclos de 15s a 95ºC (desnaturação) e 1 min a 60ºC (hibridização e extensão).
Os sinais de fluorescência emitidos pelos fluoróforos das sondas TaqMan
foram detectados pelo equipamento ABI Prism 7500 FAST (Life Technologies,
Forest City, USA). Os dados foram analisados utilizando o programa System SDS Software (Life Technologies, Forest City, USA) que geram curvas
semi-logaritímicas dos sinais de amplificação. Esse programa fornece o parâmetro ciclo em que o sinal de florescência é significativo, denominado ciclo treshold (Ct)
(Bustin e Mueller, 2005). Para cada amostra de cDNA, o Ct de cada gene foi
registrado e comparado com o gene da gliceraldeído 3-fosfato desidrogenase (GAPDH) que foi utilizado como controle endógeno.
A escolha do controle endógeno foi feita avaliando 6 genes diferentes
(GAPDH, B2M (beta 2-microglobulina), HPRT1 (hipoxantina
35
subunidade A, flavoproteína (Fp)]; UBC (ubiquina C) e HMBS (hidroximetilbilane sintase)) em uma amostragem de cDNAs que incluíram pacientes randomizados entre caso e controle. Após a PCR em tempo real, os dados foram analisados no programa geNorm (Primer Design Ltd.). O gene com menor variação entre as
amostras foi o GAPDH.
A quantidade de cDNA utilizada nos ensaios foi otimizada a partir de curva-padrão que permite avaliar a linearidade da amplificação bem como a eficiência da mesma. Para essa finalidade, foram utilizadas diluições seriadas (1:4, 1:16; 1:64 e 1:256) de cDNA e os respectivos Ct foram plotados em gráficos que
permitem verificar a relação entre essas duas variáveis (Ct x log da diluição de
cDNA).
A eficiência da reação foi calculada de acordo com a inclinação da curva gerada pela seguinte fórmula: E= 10-1/α
-1 x 100, onde α é a inclinação da curva.
Segundo Livak e Schmittgen (2001), para a PCR em tempo real, ter alta eficiência (90% a 110%), a inclinação (do inglês slope) da curva-padrão deve ser próximo
de -3,3. Quando esses critérios não são atendidos, é preciso verificar as concentrações de iniciadores e sondas de outras curvas-padrão (Livak e Schmittgen, 2001).
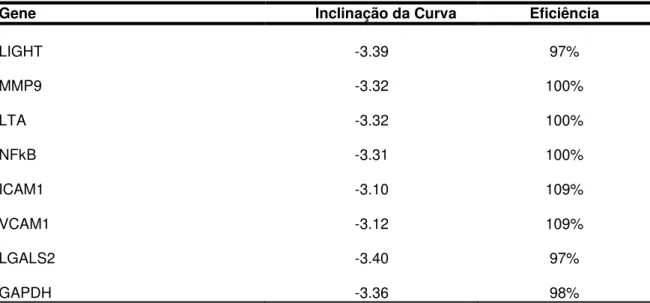
Na tabela 5, estão apresentados os resultados de inclinações (slopes) das
curvas e as respectivas eficiências dos ensaios.
Tabela 5 - Valores de inclinação da curva e eficiência dos ensaios de RT-PCR em tempo real.
Gene Inclinação da Curva Eficiência
LIGHT -3.39 97%
MMP9 -3.32 100%
LTA -3.32 100%
NFkB -3.31 100%
ICAM1 -3.10 109%
VCAM1 -3.12 109%
LGALS2 -3.40 97%
GAPDH -3.36 98%
Os valores de Ct obtidos nos ensaios foram utilizados para o cálculo da
36
(controle endógeno). Essa relação é denominada Delta Ct (∆Ct) e será calculada
pela fórmula:
∆Ct = (Ct gene alvo - Ct controle endógeno)
Os dados de ∆Ct foram transformados em escala logarítima (2 –∆Ct) para a
análise dos dados.
3.6. ANÁLISE DAS CITOCINAS
3.6.1. DOSAGEM DAS CITOCINAS PELO SISTEMA
LUMINEX
As amostras de soro dos 91 indivíduos incluídos no estudo foram obtidas a partir do sangue total periférico colhido em tubo com ativador de coágulo e gel separador. As amostras foram estocadas á temperatura ambiente por 30 minutos para coagular e, em seguida, foram centrifugadas a 1000xg por 10 minutos a 25ºC e o soro foi estocado a -20ºC.
A dosagem de MMP9, sICAM1, sVCAM1 e sE-SELECTINA foram dosadas utilizando o MILLIPLEX TM Human Cardiovascular Disease (CVD) Panel 1 kit
(Millipore, Missouri, USA) no equipamento LUMINEX® 200TM System (Luminex
Corporation, Austin, USA).
3.7. CONTROLE DE QUALIDADE DAS REAÇÕES
As amplificações realizadas pela PCR foram monitorizadas utilizando-se controle de reagentes (tubo no qual foram adicionados todos os reagentes para a reação de amplificação, exceto, a amostra de DNA ou cDNA) em cada conjunto de reações. Os ensaios de PCR em tempo real e LUMINEX foram feitos em duplicata.
3.8. ANÁLISE ESTATÍSTICA DOS DADOS
Os resultados foram analisados através do software SPSS 15 (SPSS Inc., Chicago, IL, EUA) e o nível de significância adotado foi de p<0,05.
Os dados referentes ao estudo do equilíbrio de ligação, D’, os valores da frequência alélica bem como o teste de qui-quadrado (χ2) e p valor, para essas
variáveis, foram obtidos através do programa Haploview 4.2 (Broad Institute, Cambridge, USA).
37
Antes de efetuar os testes de comparações das variáveis quantitativas, avaliou-se se os dados seguiam uma distribuição normal pelo teste de
Kolmogorov-Smirnov. Para dados paramétricos foi utilizado o teste t de Student
ou ANOVA. Para dados não paramétricos foi utilizado o teste de Mann-Whitney
ou Kruskal-Wallis
38
4. RESULTADOS
4.1. CASUÍSTICA
4.1.1. GRUPO COM INFARTO AGUDO DO MIOCÁRDIO
(IAM)
Inicialmente foram selecionados 52 pacientes com infarto agudo do miocárdio, 2 destes não preencheram os critérios de inclusão. Não foi possível obtenção da amostra biológica em 2 pacientes devido a uso de contraste e 1 apresentou alterações hormonais (T4 livre e/ou TSH aumentados). Sendo assim, o
grupo IAM foi composto por 47 indivíduos.
4.1.2. GRUPO SEM INFARTO AGUDO DO MIOCARDIO
(SIAM)
Inicialmente foram selecionados 48 pacientes sem infarto agudo do miocárdio, 2 destes apresentaram alterações hormonais (T4 livre e/ou TSH
aumentados). Sendo assim, o grupo SIAM foi composto por 46 indivíduos.
4.1.3. DADOS BIODEMOGRÁFICOS
Na tabela 6 estão representadas as características biodemográficas dos indivíduos do grupo IAM e SIAM. Foram incluídos no estudo 93 indivíduos, sendo 47IAM e 46 SIAM, de ambos os sexos com idades entre 45 e 90 anos.
Houve uma maior frequência de homens caucasianos nos dois grupos o que indica que diferentes etnias e o sexo podem influenciar no desenvolvimento e progressão da doença aterosclerótica (p>0,05).
A média de idade foi maior no grupo IAM do que no SIAM não apresentando dados estatísticamente significativos.
Os indivíduos de ambos os grupos apresentaram fatores de risco clássicos (hipertensão, obesidade, diabetes mellitus, tabagismo, sedentarismo e consumo de álcool) para o desenvolvimento de doença aterosclerótica.
O número de obesos em ambos os grupos foi relativamente pequeno não apresentando dados estatisticamente significativos. Apesar do pequeno número de obesos, vale ressaltar que muitos dos indivíduos estavam com sobrepeso (IMC 25 a 29kg/m2) e o aumento do IMC é um fator de risco independente para IAM.
39
dados estatisticamente significativos (p>0,05), a hipertensão é um fator de risco independente para doença cardiovascular.
A maioria dos indivíduos não eram diabéticos porém o grupo IAM foi composto por mais diabéticos que o SIAM confirmando o papel da diabetes na progressão e desenvolvimento da doença aterosclerótica.
Apesar do pequeno número de fumantes, vale ressaltar que muitos dos indivíduos eram ex-fumantes o que pode justificar o desenvolvimento da doença.
A prática de atividade física no grupo IAM foi maior que no grupo SIAM porém não apresentou valores estatisticamente significativos (p>0,05). Apesar da maioria dos indivíduos serem sedentários, o número de obesos é pequeno.
O consumo de álcool foi mínimo nos dois grupos e, a maioria consumidora encontra-se no grupo IAM.
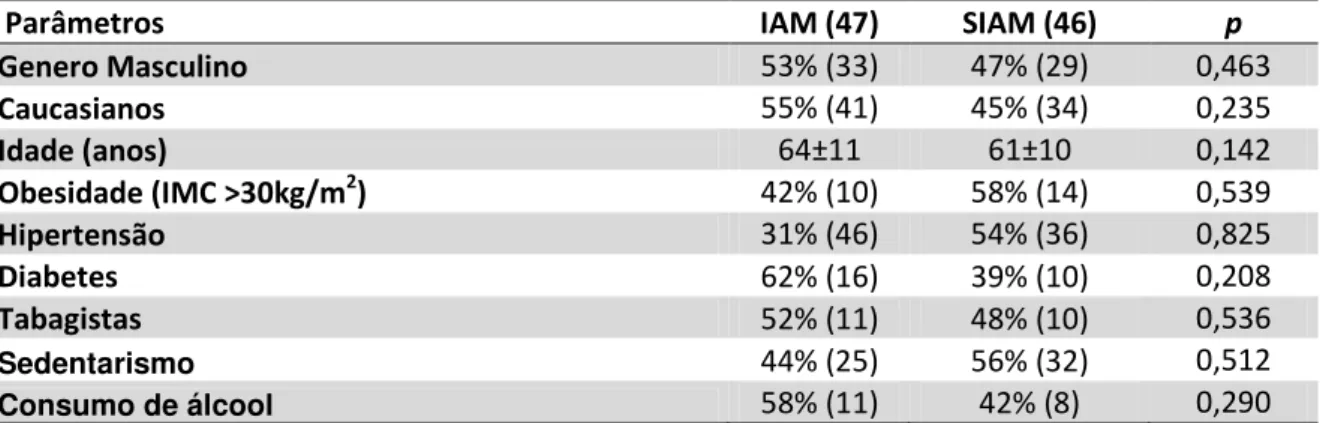
Tabela 6 - Características biodemográficas dos indivíduos do grupo IAM (infarto agudo do miocárdio) e SIAM (sem infarto do agudo do miocárdio).
Parâmetros IAM (47) SIAM (46) p
Genero Masculino 53% (33) 47% (29) 0,463
Caucasianos 55% (41) 45% (34) 0,235
Idade (anos) 64±11 61±10 0,142
Obesidade (IMC >30kg/m2) 42% (10) 58% (14) 0,539
Hipertensão 31% (46) 54% (36) 0,825
Diabetes 62% (16) 39% (10) 0,208
Tabagistas 52% (11) 48% (10) 0,536
Sedentarismo 44% (25) 56% (32) 0,512
Consumo de álcool 58% (11) 42% (8) 0,290
Nota: número de indivíduos entre parênteses. As variáveis contínuas são apresentadas como média ± desvio padrão, comparadas por teste t. Variáveis categóricas foram comparadas por qui-quadrado (χ2). IAM: infarto agudo do miocárdio; SIAM: sem infarto agudo do miocárdio; IMC:
índice de massa corpórea. * valores estatisticamente significativos. Os indivíduos com pressão arterial igual ou superior a 140x90mmHg e/ou que fazem uso de medicação anti-hipertensiva, foram considerados hipertensos (Júnior, 2006). Indivíduos que fazem uso de hipoglicemiantes orais ou que recebem terapia com insulina ou que apresentaram valores de glicose plasmática de jejum igual ou superior a 126mg/dL foram considerados diabéticos ((Who), 2006). Os indivíduos tabagistas ativos ou que fumaram no ano anterior a inclusão na pesquisa foram considerados tabagistas (Silva, Sousa et al., 1998).
Na tabela 7 está representado o perfil lipídico, bioquímico e hematológico dos indivíduos do grupo IAM e SIAM. Foram incluídos no estudo 93 indivíduos, sendo 47 IAM e 46 SIAM, de ambos os sexos com idades entre 45 e 90 anos.
Os valores glicêmicos foram maiores no grupo IAM quando comparados com o SIAM não apresentando valores estatisticamente significativos.
40
entre os grupos (p>0,05), são considerados fatores de risco para DAC. Tem-se que levar em consideração que os indivíduos faziam uso de hipolipemiantes.
As concentrações séricas de Apo A do grupo IAM foi de 126mg/dL e do grupo SIAM foi de 142mg/dL e após a transformação dos valores apresentaram valores aproximados porém foram estatisticamente significativos. Acredita-se que os grupos apresentaram esse perfil devido ao uso de hipolipemiantes.
Os demais exames de triagem como: ALT, AST, ureia, creatinina, PCRus, leucócitos e plaquetas não apresentaram diferença estatística entre os grupos (p>0,05). Esperava-se que as concentrações séricas das enzimas hepáticas ALT e AST fossem mais altas no grupo IAM já que estas se encontram elevadas no infarto. Acredita-se que esse perfil deve-se a administração de medicamentos no PS do IDPC. Para excluir a presença de doença hepática, foi realizada a razão AST/ALT e, todos apresentaram valores dentro dos padrões de referência normal (<2,0).
41 Tabela 7 - Perfil lipídico, bioquímico e hematológico dos indivíduos do grupo IAM (infarto agudo do miocárdio) e SIAM (sem infarto do agudo do miocárdio).
Parâmetros IAM (47) SIAM (46) p
Perfil Lipídico e Bioquímico
Glicemia (mmol/L) 6,3±2,0 6,1±2,4 0,432
Colesterol Total (mmol/L) 5,0±2,0 5,0±1,4 0,721
HDL – C (mmol/L) 1,1±0,3 1,2±0,3 0,142
LDL – C (mmol/L) 2,8±1,4 3,0±1,2 0,448
VLDL – C (mmol/L) 1,0±1,0 1,0±0,7 0,777
Triacilglicerol (mmol/L) 2,3±2,3 2,0±1,5 0,806
Apo A (g/L) 1,3±0,2 1,4±0,3 0,002
Apo B (g/L) 1,0±0,4 1,0±0,3 0,538
AST (µKat/L) 0,5±0,3 0,5±0,3 0,139
ALT (µKat/L) 0,7±0,5 0,7±0,4 0,560
Ureia (mmol/L) 7,1±3,0 6,5±2,0 0,551
Creatinina (µmol/L) 104±30 95±33 0,083
PCRus (mg/L) 9,6±19,8 3,8±4,0 0,948
Perfil Hematológico
Leucócitos (103/mL) 7,7±2,0 7,3±2,1 0,323
Plaquetas (103/µL) 242±68 225±63 0,223
Nota: número de indivíduos entre parênteses. As variáveis contínuas são apresentadas como média ± desvio padrão, comparadas por teste t ou por testes não paramétricos de Mann-Whitney. IAM:
infarto agudo do miocárdio; SIAM: sem infarto agudo do miocárdio; HDL-C: colesterol da lipoproteína de alta densidade; LDL-C: colesterol da lipoproteína de baixa densidade; VLDL-C: colesterol da lipoproteína de muito baixa densidade; APO A: apolipoproteína A; APO B: apolipoproteína B. T4 livre: fração livre da tiroxina; TSH: hormônio estimulante da tireoide; AST: aspartato aminotransaminase; ALT: alanina aminotransaminase.
4.2. GENOTIPAGEM
Foi realizada a genotipagem de 83 indivíduos. Algumas das amostras de DNA obtidas apresentaram valores da relação A260/A280 <1,8 ou >2,0 e por isso
não foram utilizadas na técnica de genotipagem.
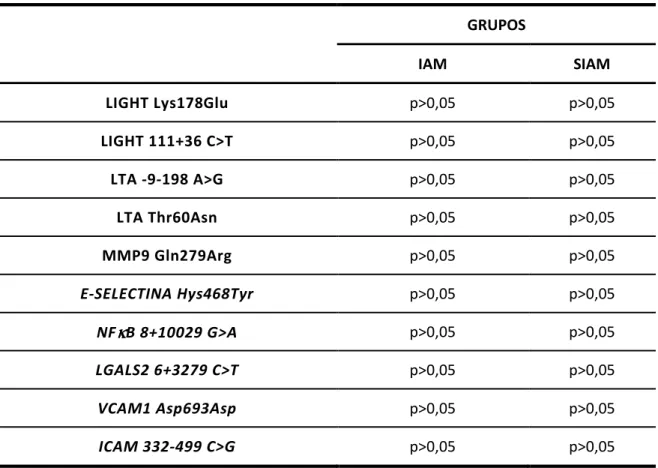
O equilíbrio de Hardy-Weinberg está representado na tabela 8.
As frequências alélicas e genotípicas dos polimorfismos Lys178Glu e 111+36C>T de LIGHT, Gln279Arg de MMP9, -9-198A>G e Thr60Asn de LTα,
6+3279C>T de LGALS2, Asp693Asp de VCAM1, 332-3499C>G de ICAM1, Hys468Tyr de E-SELECTINA e 8+10029G>A de NFκB encontram – se na tabela 9.
O equilíbrio de Hardy-Weinberg caracteriza que os resultados mostraram validade amostral.
42
6+3279C>T de LGALS2, Asp693Asp de VCAM1, 332-3499C>G de ICAM1, Hys468Tyr de E-SELECTINA e 8+10029G>A de NFκB (p>0,05) portanto os polimorfismos selecionados apresentaram ausência de associação com SCA na população deste estudo.
Os dados referentes ao estudo do equilíbrio de ligação estão representados na tabela 10 e figura 3. Através do programa Haploview 4.2 (Broad Institute, Cambridge, USA) foi feita a análise dos polimorfismos Lys178Glu e 111+36C>T de LIGHT e -9-198A>G e Thr60Asn de LTα e, foi possível observar
que os polimorfismos de LIGHT estão em equilíbrio de ligação, ou seja, o genótipo do cromossomo em um loco é independente de seu genótipo em outro sendo assim, não houve relação do haplótipo avaliado. Enquanto que os polimorfismos de LTα estão em desequilíbrio de ligação, ou seja, existe uma
associação não aleatória entre o genótipo do cromossomo em um loco e seu genótipo em outro.
Tabela 8 - Equilíbrio de Hardy-Weinberg para os polimorfismos estudados.
GRUPOS
IAM SIAM
LIGHT Lys178Glu p>0,05 p>0,05
LIGHT 111+36 C>T p>0,05 p>0,05
LTA -9-198 A>G p>0,05 p>0,05
LTA Thr60Asn p>0,05 p>0,05
MMP9 Gln279Arg p>0,05 p>0,05
E-SELECTINA Hys468Tyr p>0,05 p>0,05
NFκκκκB 8+10029 G>A p>0,05 p>0,05
LGALS2 6+3279 C>T p>0,05 p>0,05
VCAM1 Asp693Asp p>0,05 p>0,05
ICAM 332-499 C>G p>0,05 p>0,05