1 UNIVERSIDADE FEDERAL DO CEARÁ
CENTRO DE TECNOLOGIA
DEPARTAMENTO DE ENGENHARIA HIDRÁULICA E AMBIENTAL PROGRAMA DE PÓS-GRADUAÇÃO EM ENGENHARIA CIVIL
WELITON FREIRE BEZERRA FILHO
NITRIFICAÇÃO E DESNITRIFICAÇÃO SIMULTÂNEAS EM BIOFILTROS AERADOS COM ALTA DENSIDADE DE LODO
2 WELITON FREIRE BEZERRA FILHO
NITRIFICAÇÃO E DESNITRIFICAÇÃO SIMULTÂNEAS EM BIOFILTROS AERADOS COM ALTA DENSIDADE DE LODO
Tese apresentada junto ao Programa de Pós-graduação em Engenharia Civil, área de concentração: Saneamento Ambiental, como requisito para obtenção do título de Doutor em Engenharia Civil.
Orientadora: Prof.ª. Dra. Ana Bárbara de Araújo Nunes
Co-orientador: Prof. Dr. Cícero Onofre de Andrade Neto.
3 Dados Internacionais de Catalogação na Publicação
Universidade Federal do Ceará
Biblioteca de Pós-Graduação em Engenharia - BPGE
B469n Bezerra Filho, Weliton Freire.
Nitrificação e desnitrificação simultâneas em biofiltros aerados com alta densidade de lodo / Weliton Freire Bezerra Filho. – 2015.
123 p. : il. color., enc. ; 30 cm.
Tese (doutorado) – Universidade Federal do Ceará, Centro de Tecnologia,
Departamento de Engenharia Hidráulica e Ambiental, Programa de Pós-Graduação em Engenharia Civil, 2015.
Área de Concentração: Saneamento Ambiental. Orientação: Profa. Dra. Ana Bárbara de Araújo Nunes. Coorientação: Prof. Dr. Cícero Onofre de Andrade Neto. 1. Saneamento. 2. Nitrogênio. 3. Lodo - Tratamento. Título.
5 AGRADECIMENTOS
A minha família pelo apoio. A minha esposa Alessandra.
Ao professor André Calado, que durante as aulas no antigo CEFET, apresentou-me a engenharia sanitária. Além disso, agradeço por ter sido o meu terceiro orientador em diversas oportunidades.
Ao professor Cícero Onofre, por ter me aberto as portas para que eu pudesse participar de um projeto interessante e inovador na UFRN. E também pelas orientações sempre detalhistas e pertinentes.
À professora Ana Bárbara, por ter acreditado que uma orientação à distância daria frutos. Mesmo distante as orientações foram fundamentais para o sucesso deste projeto. Além disso, foi muito importante para resolver problemas que não tinham ligação direta com a orientação (como entrega de documentos na FUNCAP, por exemplo).
Ao funcionário da ETE do campus da UFRN, Erivan Martins, conhecido, e muito conhecido, por Bam. Sempre disposto e prestativo.
Aos meus colegas do LARHISA e aos bolsistas de iniciação científica que me ajudaram bastante durante o trabalho de campo.
Ao Programa de Pós Graduação em Engenharia Civil da Universidade Federal do Ceará, o programa de pós-graduação mais bem conceituado do norte e nordeste do país, e que muito me orgulha ter feito parte desta instituição.
Aos funcionários do Pós DEHA, especialmente Shirley, que me ajudou a resolver muitos problemas pelo telefone.
Aos professores André Bezerra e Fernando da Silva, que fizeram parte das bancas de qualificação e de defesa do doutorado, e aos professores Marcos Erick e Francisco Mauricio, que contribuíram bastante na banca de defesa deste trabalho.
6 RESUMO
O crescimento da população e aspectos relacionados ao gerenciamento de recursos hídricos, fazem com que seja extremamente importante a busca por sistemas de tratamento de esgoto simples, de baixo custo e simplicidade operacional, capazes de produzir efluentes com potencial de utilização para diversos fins compatíveis. Neste cenário, a utilização de reatores aerados como pós-tratamento de efluente anaeróbio mostra-se bastante promissor para a realidade brasileira. Este trabalho contribui para o desenvolvimento de novo sistema de biofiltros aeróbios para tratamento de esgotos sanitários, que está sendo desenvolvido na Universidade Federal do Rio Grande do Norte. O reator utiliza eletroduto corrugado cortado como material de enchimento, proporcionando elevado índice de vazios, e é capaz de produzir efluente com turbidez da ordem de 1 UT, 2 mg/L de SST e DQO abaixo de 40 mg/L. É objetivo deste trabalho investigar a capacidade de remoção de nitrogênio pelo processo de nitrificação e desnitrificação simultânea. O trabalho foi dividido em quatro fases, nas quais foi alterada a vazão de ar nos filtros, e, durante a fase 4, introduzida uma fonte suplementar de carbono. O sistema mostrou-se eficiente em relação à remoção de nitrogênio. Na configuração mais eficiente foi capaz de remover 56% do nitrogênio afluente, e na fase menos eficiente a remoção foi de 40%. A análise de componentes principais mostrou que a nitrificação foi o fator mais relevante para o processo. Concluiu-se que o sistema é capaz de remover nitrogênio pelo processo de nitrificação e desnitrificação simultânea. Além disso, é importante mencionar também que durante os mais de três anos de duração do experimento não foi necessária a remoção do lodo retido.
7 ABSTRACT
Population growth and aspects related to the management of water resources make it extremely important to search for simple wastewater treatment systems, low cost and operational simplicity, capable of producing effluent with potential use for various purposes compatible. In this scenario, the use of aerated reactors as post-treatment of anaerobic effluent appears to be quite promising for the Brazilian reality. This work contributes to the development of new aerobic biofilter system to treat sewage, which is being developed at the Federal University of Rio Grande do Norte. The reactor uses corrugated conduit cut as filler material, providing high void ratio, and is capable of producing effluent with turbidity of about 1 TU, 2 mg/L TSS and COD below 40 mg/L. It is objective of this work to investigate the nitrogen removal capacity of the simultaneously nitrification and denitrification process. The work was divided in four phases, in which changed the flow of air in the filter, and during phase 4, introduced a supplementary source of carbon. The system proved to be efficient in relation to the removal of nitrogen. In the most efficient configuration was able to remove 56% of the influent nitrogen, and less efficient removal stage was 40%. The principal component analysis showed that the nitrification was the most relevant factor for the process. It was concluded that the system is capable of removing nitrogen by simultaneous nitrification and denitrification process. Furthermore, it is also important to mention that during more than three years duration of the experiment the sludge removal is not required.
8 Lista de Figuras:
Figura 4.1: Detalhamento do sistema anaeróbio pré-existente ... 44
Figura 4.2: Tijolo cerâmico e peças plásticas, utilizados como material de enchimento para os filtros anaeróbios. ... 45
Figura 4.3: Planta baixa e corte esquemático dos filtros utilizados na pesquisa. ... 47
Figura 4.4: Calhas em PVC de 75 mm de diâmetro disposto sobre o material de enchimento (Esquerda). Canos de distribuição do esgoto com o mesmo diâmetro, dispostos sobre o fundo dos biofiltros (Direita). ... 47
Figura 4.5: Tela de retenção utilizada para segurar o material de enchimento no biofiltro. ... 48
Figura 4.6: Material de enchimento utilizado na pesquisa. ... 48
Figura 4.7: Detalhe do cano e do orifício controlador da vazão afluente. ... 49
Figura 4.8: Registro controlador da vazão da fonte externa de carbono. ... 49
Figura 4. 9: Local de coleta de lodo nos biofiltros aerados. ... 51
Figura 4. 10: Detalhe do amostrador utilizado na coleta de lodo ... 52
Figura 4. 11: Detalhe do material coletado ... 52
Figura 4.12: Compressores utilizados no suprimento de ar ... 57
Figura 4.13: À esquerda o regulador de pressão e vazão e à direita os rotâmetros utilizados para aferir as vazões de ar dos filtros. ... 57
Figura 4.14: (A) Cruzeta que recebe a vazão de ar do compressor e divide em três mangueiras perfuradas. (B) Mangueira perfurada com agulha que distribui o ar no interior do filtro. (C) Distribuição das mangueiras no interior do filtro (D) Distribuição dos canos. ... 57
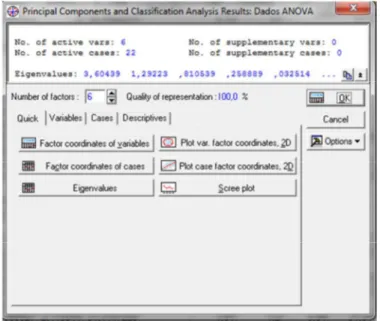
Figura 4. 15: Análise de componentes principais ... 65
Figura 4. 16: Exemplo de matriz de componentes principais ... 66
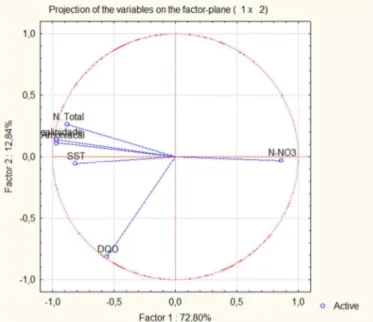
Figura 4. 17: Exemplo da representação gráfica dos componentes principais ... 66
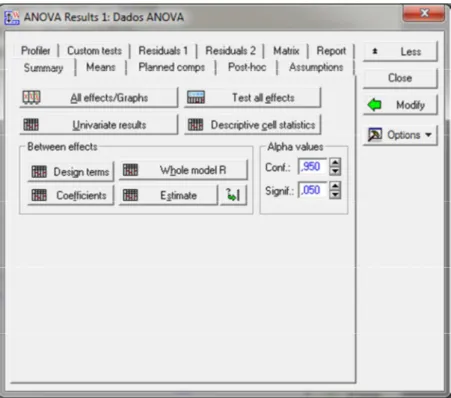
Figura 4. 18: Exemplo da análise da variância ... 67
Figura 4. 19: Exemplo de gráfico de análise da variância ... 68
Figura 4. 20: Exemplo da janela para realização do teste de Tukey ... 68
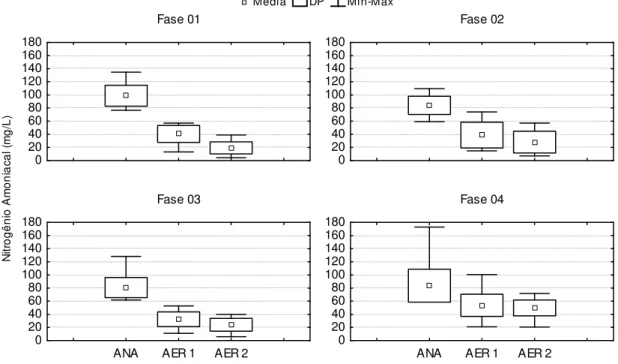
Figura 5.1: Box Plot do Nitrogênio Amoniacal ... 79
Figura 5.2: Box Plot do Nitrato ... 81
Figura 5.3: Box Plot do Nitrogênio Total ... 82
Figura 5.4: Box Plot da Alcalinidade ... 84
Figura 5.5: Box Plot da DQO ... 87
Figura 5.6: Box Plot da Turbidez ... 88
Figura 5.7: Box Plot do Sólidos Suspensos Totais ... 89
9
Figura 5.9: Análise gráfica dos fatores que mais influenciaram o experimento durante a fase 02. ... 96 Figura 5.10: Análise gráfica dos fatores que mais influenciaram o experimento durante a fase 03. ... 97 Figura 5.11: Análise gráfica dos fatores que mais influenciaram o experimento durante a fase 04. ... 98 Figura 5.12: Comparação entre as médias de nitrogênio amoniacal ao longo do
processo de tratamento. ... 100 Figura 5.13: Comparação entre as médias de nitrogênio amoniacal nas diferentes fases da pesquisa ... 101 Figura 5.14: Comparação entre as médias de nitrato ao longo do processo de
10 Lista de Quadros:
11 Lista de Tabelas:
Tabela 5.1: Detalhamento dos sólidos totais no interior do AER1 e AER2, ao final da
fase 4 da pesquisa ... 71
Tabela 5.2: Estatística descritiva da Fase 01 ... 72
Tabela 5.3: Estatística descritiva da Fase 02 ... 73
Tabela 5.4: Estatística descritiva da Fase 03 ... 75
Tabela 5.5: Estatística descritiva da Fase 04 ... 76
Tabela 5.6: Estatística descritiva da fonte suplementar de carbono ... 77
Tabela 5.7: Matriz de correlação da fase 01 ... 90
Tabela 5.8: Matriz de correlação da fase 04 ... 90
Tabela 5.9: Peso dos fatores no resultado final do experimento. ... 93
Tabela 5.10: Interferência dos fatores em cada parâmetro relacionado durante a fase 01. ... 93
Tabela 5.11: Interferência dos fatores em cada parâmetro relacionado durante a fase 02. ... 95
Tabela 5.12: Interferência dos fatores em cada parâmetro relacionado durante a fase 03. ... 96
Tabela 5.13: Interferência dos fatores em cada parâmetro relacionado durante a fase 04. ... 98
Tabela 5.14: Teste de Tukey para amostras desiguais comparando as médias de nitrogênio amoniacal ao longo do processo de tratamento. ... 100
Tabela 5.15: Teste de Tukey para amostras desiguais comparando as médias de nitrogênio amoniacal nas diferentes fases da pesquisa ... 101
Tabela 5.16: Teste de Tukey para amostras desiguais comparando as médias de nitrato ao longo do processo de tratamento. ... 103
Tabela 5.17: Teste de Tukey para amostras desiguais comparando as médias de nitrato nas diferentes fases da pesquisa ... 104
Tabela 5.18: Teste de Tukey para amostras desiguais comparando as médias de nitrogênio total ao longo do processo de tratamento. ... 105
Tabela 5.19: Teste de Tukey para amostras desiguais comparando as médias de nitrogênio total nas diferentes fases da pesquisa ... 106
Tabela 5.20: Teste de Tukey para amostras desiguais comparando as médias de alcalinidade ao longo do processo de tratamento. ... 107
Tabela 5.21: Teste de Tukey para amostras desiguais comparando as médias de alcalinidade nas diferentes fases da pesquisa ... 108
Tabela 5.22: Teste de Tukey para amostras desiguais comparando as médias de DQO ao longo do processo de tratamento. ... 109
12 SUMÁRIO
1 INTRODUÇÃO ... 14
2 Objetivos ... 15
2.1 Geral _________________________________________________________________ 15 2.2 Específicos ____________________________________________________________ 15 3 REVISÃO BIBLIOGRÁFICA ... 16
3.1 Remoção biológica de nitrogênio __________________________________________ 16 3.1.1 Nitrificação ... 17
3.1.2 Desnitrificação ... 24
3.1.3 Nitrificação e desnitrificação simultâneas ... 28
3.1.4 Oxidação Parcial da Amônia (SHARON) ... 31
3.1.5 Oxidação Anaeróbia da Amônia (ANAMMOX) ... 32
3.1.6 Remoção de Nitrogênio a partir do Nitrito (CANON) ... 34
3.2 Lodos Ativados _________________________________________________________ 35 3.3 Moving Bed Biofilm Reactor (MBBR) _______________________________________ 37 3.4 Biofiltro Aerado Submerso (BAS) __________________________________________ 38 3.5 Acúmulo de lodo _______________________________________________________ 40 4 MATERIAL E MÉTODOS ... 43
4.1 Descrição do reator anaeróbio pré-existente_________________________________ 44 4.2 Descrição do sistema aerado utilizado na pesquisa ____________________________ 45 4.3 Controle de Vazão ______________________________________________________ 49 4.3.1 Controle de vazão afluente ... 49
4.3.2 Controle de vazão da fonte de carbono ... 49
4.4 Índice de vazios ________________________________________________________ 50 4.5 Coleta de lodo _________________________________________________________ 50 4.5.1 Análise laboratorial do lodo ... 53
4.6 Fases da pesquisa ______________________________________________________ 53 4.7 Sistema de Aeração _____________________________________________________ 54 4.7.1 Furometria das mangueiras ... 58
4.8 Fonte externa de carbono ________________________________________________ 59
13
4.10 Procedimento de Partida no Sistema ______________________________________ 60
4.11 Operação ____________________________________________________________ 61
4.11.1 Perda de carga ... 61
4.12 Coleta e análises ______________________________________________________ 62 4.13 Tratamento dos Dados Obtidos __________________________________________ 63 4.13.1 Análise de componentes principais ... 64
4.13.2 ANOVA e teste de Tukey para amostras desiguais. ... 67
5 RESULTADOS E DISCUSSÃO: ... 70
5.1 Densidade de lodo ______________________________________________________ 70 5.2 Estatística Descritiva ____________________________________________________ 71 5.3 Box Plot ______________________________________________________________ 78 5.3.1 Box Plot Nitrogênio Amoniacal ... 78
5.3.2 Box Plot do Nitrato ... 80
5.3.3 Box Plot do Nitrogênio Total ... 82
5.3.4 Box Plot da Alcalinidade ... 84
5.3.5 Box Plot da DQO ... 86
5.3.6 Box Plot da Turbidez ... 88
5.3.7 Box Plot de Sólidos Suspensos Totais ... 89
5.4 Matriz de Correlação ____________________________________________________ 90 5.5 Análise de Componentes Principais. ________________________________________ 92 5.6 Análise de Variância (ANOVA) e Teste de Tukey ______________________________ 99 5.6.1 Nitrogênio Amoniacal ... 99
5.6.2 Nitrato ... 101
5.6.3 Nitrogênio Total ... 104
5.6.4 Alcalinidade ... 106
5.6.5 DQO ... 108
5.6.6 Turbidez e SST ... 110
6 Conclusões ... 112
7 Recomendações ... 113
14 1 INTRODUÇÃO
Os problemas causados pelo despejo de compostos nitrogenados nos ambientes aquáticos naturais são bastante conhecidos na academia e na indústria de tratamento de esgotos, assim como as tecnologias envolvidas na remoção do nitrogênio das águas residuárias.
Os lodos ativados apresentam-se como uma importante e eficiente alternativa tecnológica na remoção de nutrientes, entretanto, trata-se de tecnologia cara, especialmente no caso de pequenas plantas, complexa, e, principalmente, com produção excessiva de lodo.
Já os biofiltros aerados convencionais, produzem menos lodo, entretanto não se mostram tão eficientes no tocante à remoção de material nitrogenado (JORDÃO e PESSOA, 2009).
Em vista disso, este trabalho busca aprimorar uma tecnologia, inicialmente concebida na Universidade Federal do Rio Grande do Norte, pela equipe do professor Dr. Cícero Onofre de Andrade Neto.
A peculiaridade desta tecnologia se dá na capacidade de reter lodo em seu interior, produzindo efluente com concentrações médias de sólidos suspensos totais (SST) inferiores a 2 mg/L, sem a necessidade de etapa de separação de fases, e sem haver a necessidade de remoções constantes de lodo.
O reator distingue-se do sistema de lodos ativados, uma vez que conta com eletroduto corrugado cortado como material de enchimento, que serve para fixar biomassa. Por outro lado, se distingue também dos biofiltros aerados convencionais, pois possui índice de vazios da ordem de 90%, permitindo que a biomassa esteja em suspensão nos interstícios.
15 O tempo de retenção celular elevado é condição fundamental para a estabilização da comunidade bacteriana que promove a nitrificação e desnitrificação (VON SPERLING, 2012.; GONG et al., 2012.; BEZERRA FILHO et al., 2013). Desta forma, a idade de lodo elevada do reator em estudo deve tornar o projeto mais eficiente na remoção biológica de nitrogênio.
Por esta razão, o objetivo central deste trabalho é verificar a capacidade de remover compostos nitrogenados de efluentes tipicamente domésticos através do processo de nitrificação e desnitrificação simultâneas em biofiltros aerados com elevado índice de vazios, que permite alta densidade de lodo.
2 Objetivos
2.1 Geral
Aperfeiçoar tecnologia de tratamento de esgotos domésticos utilizando uma variação de biofiltros aerados, preenchidos com material plástico com alto índice de vazios, capaz de remover nitrogênio pelo processo de nitrificação e desnitrificação simultânea.
2.2 Específicos
• Avaliar a capacidade de nitrificação e desnitrificação simultâneas dos
biofiltros utilizando somente o carbono remanescente e comparar o desempenho adotando esgoto bruto como fonte externa de carbono.
• Avaliar a interferência da vazão de ar na remoção dos compostos
nitrogenados através da nitrificação e desnitrificação simultâneas.
• Avaliar a interferência da vazão de ar na remoção de sólidos suspensos
totais e turbidez.
• Determinar a influência do segundo biofiltro aerado na estabilização dos
16 3 REVISÃO BIBLIOGRÁFICA
O processo de nitrificação e desnitrificação simultânea já é bastante difundido no meio acadêmico e industrial. Entretanto, os reatores envolvidos neste processo geralmente são de biomassa suspensa ou misto de biomassa suspensa e aderida. Como este trabalho busca aplicar um biofiltro aerado de biomassa aderida e suspensa nos interstícios, algo ainda pouco explorado na literatura, a revisão a seguir traça um paralelo entre os reatores mais estudados e o reator alvo deste trabalho. Desta forma, procura-se deixar claras as diferenças entre eles.
Além disso, será apresentada a dificuldade que as plantas de tratamento aeróbio de esgoto apresentam no tocante ao tratamento e disposição final do lodo gerado. Contrapondo-se ao sistema apresentado neste estudo, que não gera lodo excedente que necessita ser removido de forma contínua.
Serão apresentados também os processos de transformação e remoção biológica de nitrogênio em esgotos sanitários, como: nitrificação, desnitrificação, nitrificação e desnitrificação simultâneas, SHARON, ANAMMOX e CANON.
3.1 Remoção biológica de nitrogênio
O material nitrogenado presente em águas residuárias compõe-se principalmente de nitrogênio amoniacal (NH3; NH4+) e nitrogênio orgânico.
Ocasionalmente ocorrem traços de formas oxidadas de nitrogênio, como nitrito (NO2-) e nitrato (NO3-) (VAN HAANDEL, KATO, VON SPERLING, 2009).
17 Basicamente, existem quatro maneiras de se converter nitrogênio em meio liquido: amonificação, assimilação, nitrificação e desnitrificação. Dentre estes processos, os que de fato são significativos, quanto à remoção biológica de nitrogênio são os processos sequenciais de nitrificação e desnitrificação.
Estes processos sequenciais promovem a conversão da amônia em nitrogênio molecular, e sua consequente liberação, em forma de gás, da massa líquida. Para que a nitrificação ocorra é fundamental a presença de oxigênio no meio. Além disso, é necessária a presença de bactérias autotróficas que oxidarão a amônia a nitrito e, posteriormente, a nitrato. Já a desnitrificação ocorre em ambiente anóxico (onde o aceptor de elétrons será o nitrato ou nitrito), neste processo, o nitrato, e em alguns casos o nitrito, será reduzido a nitrogênio molecular, através da ação de bactérias heterotróficas.
Entretanto, há algum tempo já é possível converter nitrogênio amoniacal em nitrogênio molecular dentro de um mesmo ambiente, o que se apresenta como nitrificação e desnitrificação simultânea (SND, sigla em inglês para Simultaneous Nitrification and Denitrification). É exatamente este processo que será explorado no presente trabalho.
3.1.1 Nitrificação
Tradicionalmente, a nitrificação é a oxidação de nitrogênio amoniacal realizada por microrganismos quimiolitoautotróficos e sob condições aeróbias estritas. A conversão do nitrogênio amoniacal em nitrato ocorre por meio de reações heterogêneas, em duas etapas: a primeira é chamada nitritação – oxidação de N-amoniacal a nitrito – e a segunda é denominada nitratação – oxidação do nitrito a nitrato (FLORÊNCIO et al., 2009).
18 Equação de Nitritação
2NH4+ + 3O2 2NO2- + 2H2O + 4H+ + Energia (3.1)
Equação de Nitratação
2NO2- + O2 2NO3- + Energia (3.2)
Reação de oxidação total
NH4+ + 2O2 NO3- + H2O + 2H+ + Energia (3.3)
Na nitritação a amônia é oxidada a nitrito através de reações bioquímicas principalmente por bactérias do gênero Nitrossomonas, contudo é possível observar nitritação por bactérias dos gêneros: Nitrossococus, Nitrosospira, Nitrosovibrio e Nitrosolobulus. Na nitratação o nitrito formado na fase anterior é oxidado a nitrato pelas bactérias do gênero Nitrobacter (METCALF e EDDY, 2004). Estudos recentes indicaram que algumas Arqueas que oxidam amônia também são capazes de promover a nitrificação, entretanto, o seu papel no tratamento de águas residuárias ainda não foi totalmente demostrado (MERTOGLU, et al. 2011; WANG, et al. 2012).
Apesar do processo de nitrificação ocorrer em dois passos sequenciais, o primeiro passo (oxidação de amônia a nitrito) é mais importante no tocante à cinética do crescimento bacteriano, uma vez que quando a população de bactérias nitrificantes está estabelecida, o processo de nitritação ocorre tão rapidamente que pode ser considerado instantâneo (MARTINKO e PARKER, 2000; WAKI. et al., 2009).
19 PAI et al. (2009) estudaram as taxas de crescimento das AOB e NOB em esgotos sanitários. Utilizaram uma unidade anaeróbia seguida por unidades aerada e anóxica. Os autores testaram a relação entre µ e três tempos de retenção hidráulicos diferentes. Concluíram que a taxa de crescimento estavam entre 0,88 e 0,95 d-1 para as AOB, e entre 1,40 e 2,58 d-1 para NOB.
A nitrificação é um processo que ocorre naturalmente, contudo, fatores como temperatura, pH, alcalinidade, relação ente carbono e nitrogênio, e oxigênio dissolvido, podem interferir e até mesmo inibi-la.
A taxa de crescimento máxima dos organismos nitrificantes (µmáx.) é
significativamente afetada pela temperatura. Desta maneira, Von Sperling (1996) citando Downing (1978), descreve o efeito da temperatura da seguinte forma:
Efeito da temperatura sobre o crescimento máximo dos organismos nitrificantes:
µmáx(T) = µmáx (20ºC). (T-20) (3.4)
Em que:
µmáx= taxa de crescimento máxima a uma temperatura T (d-1)
= Coeficiente de temperatura T = Temperatura (ºC)
Ainda segundo o autor, o intervalo considerado para o coeficiente está entre 1,08 e 1,13, sendo 1,10 o mais comumente utilizado. Desta forma, a taxa de crescimento dobra para cada acréscimo de aproximadamente 7ºC, e, inversamente, decresce a metade com a redução da mesma temperatura.
20 A temperatura pode influenciar decisivamente no desenvolvimento de determinados tipos de bactérias. Siripong e Rittmann (2007), estudaram sete diferentes plantas de lodos ativados no inverno e no verão, na cidade de Chicago nos EUA e compararam a comunidade de bactérias presentes. Chegaram à conclusão que diferentes comunidades de bactérias AOB e NOB coexistem nas duas situações. Entretanto, no inverno, as bactérias do gênero Nitrosospira são mais atuantes. No caso das NOB, os autores concluíram que temperaturas mais baixas podem representar um aumento na diversidade de bactérias NOB.
A influência do pH sobre a taxa de nitrificação é bastante ampla, variando entre 7,4 e 8,6 (SANTIAGO, 1999). De acordo com Villaverde (1997), dentro da faixa de pH delimitada por 5,0 e 9,0 o aumento de uma unidade de pH implica no aumento de 13% na eficiência de nitrificação. Metcalf e Eddy (2004) defendem que o pH ótimo para que a nitrificação ocorra está entre 7,5 e 8,0. Contudo, observam-se taxas de nitrificação consideráveis em ambientes com pH entre 7,0 e 7,5. Abaixo destes valores a velocidade de nitrificação pode cair entre 10 e 20%.
De acordo com a cinética de crescimento dos microrganismos nitrificantes apresentada por Von Sperling (2012), a faixa ótima de pH está entre 7,2 e 8,0.
O Crescimento da comunidade nitrificante em relação ao pH do meio pode ser expresso por:
µmáx(pH) = µmáx[1 - 0,83(7,2 – pH)] (3.5)
Em que:
µmáx(pH) = Taxa de crescimento máxima das bactérias nitrificantes para
um dado pH (d-1).
µmáx= Taxa de crescimento máxima das bactérias nitrificantes no pH de
7,2 (d-1).
21 com um sistema de lodo ativado que tratava esgoto sintético com concentração de amônia de 1g NH4+-N/L; 40 g NaHCO3/L, que funcionava como fonte de
carbono e controlava o pH; KH2PO4 500 mg/L; MgSO4 120 mg/L; NaCl 2000
mg/L.
Além disso, a temperatura e, principalmente o pH, determinam a forma da amônia presente (se na forma de íon ou na forma não ionizada, ou livre). Temperaturas acima de 25ºC aliada a pH elevado, superior a 8, podem levar a amônia à forma NH3, que é mais tóxica (Von Sperling, 1997).
Com relação à alcalinidade, quando observada a equação estequiométrica que rege o processo de nitrificação, verifica-se que há produção de dois moles de H+ por mol de nitrato formado. A produção de H+ faz com que o pH do meio tenda a diminuir. Para que isso não ocorra e venha a inibir a nitrificação é necessário que seja fornecida alcalinidade suficiente para impedir a diminuição do pH. Como a produção de 1,0 mol de H+ corresponde ao consumo de 1,0 mol de alcalinidade ou 50g CaCO3, calcula-se
que seja necessária na ordem de 7,14 mg CaCO3/ mg N (LOPES, 2009, VON
SPERLING, 1997.; METCALF e EDDY, 2004).
Normalmente o efluente de um sistema anaeróbio tratando esgotos domésticos possui alcalinidade suficiente para que a nitrificação ocorra, como apresenta: Araújo (2009), que alcançou a nitrificação com alcalinidade afluente de 303 mg CaCO3/L.
Almeida (2007), utilizando efluente doméstico em filtro biológico percolador preenchido com eletroduto cortado como pós-tratamento de um UASB, observou consumo de alcalinidade de 60,5 mg CaCO3/L para produzir
3,3 mg/L de N-NO3, e concluiu que a alcalinidade não foi fator limitante para a
nitrificação.
22 atingiram a nitrificação com uma concentração de oxigênio dissolvido variando entre 2 e 5 mg/L, trabalhando em um reator de batelada sequencial e tratando efluente avícola. Yuan e Gao (2010), estudando a influência de várias concentrações de OD na remoção biológica de amônia, concluíram que a concentração ótima de oxigênio no meio é de 2,5 mg/L.
A concentração de OD também influencia no grupo de bactérias que se desenvolve no interior do reator. Conforme apresentam Dytczak et al. (2008), que compararam um reator de lodos ativados com aeração continua com outro com aeração alternada. O TDH era 36h, o tempo de retenção celular de 12 dias e a temperatura em torno do 24ºC. Os autores concluíram que ambientes com baixa concentração de OD favorecem o desenvolvimento das bactérias do gênero Nitrosospira e Nitrospira. Enquanto ambientes com oxigênio abundante favorece o desenvolvimento das Nitrosomonas e Nitrobacter.
É importante mencionar que baixas concentrações de oxigênio dissolvido podem até aumentar a eficiência na transferência de oxigênio, diminuindo o consumo energético. Entretanto, a operação prolongada de um reator com baixas concentrações de OD podem resultar em acúmulo de nitrito (LIU e WANG, 2013), principalmente quando a temperatura do meio líquido estiver em torno de 30ºC (GUO, et al. 2008).
Van Haandel, Kato e Von Sperling (2009) explicam que na nitrificação o número de oxidação da amônia (-3) aumenta para (+5) no nitrato. Esta variação ocorre devido à transferência de 8 elétrons por átomo de nitrogênio, que são aceitos pelo oxigênio. Para que o processo ocorra em equilíbrio, são necessários quatro átomos (duas moléculas) de oxigênio para isso. Portanto, na nitrificação de 1 mol de N amoniacal, o consumo de oxigênio é de 64/14 = 4,57 mg O2/ mg N.
23 cresce. Quando a nitrificação se dá em reatores com biofilme este fator tem sido o mais limitante.
Os autores corroboram com Metcalf e Eddy (2004), que afirmam que para o bom desempenho de processos de nitrificação esta relação deve estar em torno de 5.
A inibição da nitrificação em ambientes com relação C/N muito elevada é explicada uma vez que as bactérias predominantes neste processo são autotróficas e tais microrganismos não se desenvolvem bem em ambientes com alta concentração de matéria orgânica carbonácea.
Essa afirmação é confirmada pelo estudo de Zhao et al. (2010). Os autores trabalharam por 9 meses com dois wetland, que tratava esgoto urbano. Eles testaram a influencia de três diferentes relações C/N na eficiência de remoção de nitrogênio. Concluíram que a remoção de nitrogênio foi mais eficiente com relação C/N ente 2,5 e 5. Acima deste valor o sistema começava a perder eficiência.
A concentração de amônia também determina o gênero de bactérias AOB e NOB que se destaca no meio. Bactérias do tipo Nitrosomonas europaea são comuns em ambientes com alta concentração de amônia, enquanto as bactérias do tipo Nitrosomoas marina, estão mais presentes em ambientes com concentração de amônia mais baixa. Para as NOB, tanto a Nitrobacter quanto a Nitrospira coexistem em ambientes ricos em amônia, para ambientes com concentrações mais baixas, a Nitrospira é mais dominante (WHANG et al., 2009).
Além disso, os organismos nitrificantes são sensíveis a substâncias tóxicas, especialmente as Nitrossomonas. Concentrações elevadas podem inibir a ação destas bactérias ou, até mesmo, matá-las.
24 Park e Bae (2009) estudaram a interferência na amônia livre e do ácido nitroso no processo de nitrificação. Concluíram que a constante de inibição (K1)
para as NOB foi de 46 µM para amônia livre e variou entre 1,7 e 6,8 µM para o ácido nitroso. Já para as AOB, K1 variou de 290 a 1600 µM para amônia livre, e
foi de 12 µM para o ácido nitroso. Estes resultados indicam que as NOB foram mais susceptíveis a sofrerem inibição do que as AOB. Este cenário pode favorecer o acúmulo de nitrito.
3.1.2 Desnitrificação
Muitas bactérias anaeróbias facultativas são capazes de utilizar nitrato como aceptor de elétrons. Neste caso, estes organismos utilizam nitrato como “transportador” de oxigênio, reduzindo-o a nitrogênio molecular ou amônia. Este fenômeno permite que as bactérias oxidem substrato mesmo na ausência de oxigênio molecular. (ESTEVES, 1998).
A Equação 3.7 mostra o processo de redução do nitrato a nitrogênio molecular, denominado desnitrificação.
Equação de Desnitrificação
NO3- NO2- NO N2O N2 (3.7)
A desnitrificação utilizando compostos carbônicos como doadores de elétrons é a forma mais conhecida de remoção de nitrogênio. É a etapa biológica em que ocorre a efetiva remoção do nitrogênio inorgânico nas formas de nitrito e nitrato com sua conversão para formas mais reduzidas, como N2O,
NO e N2.
25 Vibrio, Halobacterium e Methanomonas (PAYNE, 1981; GAYLE, 1989, apud METCALF E EDDY, 2004).
A desnitrificação pode ocorrer também pela ação de bactérias autotróficas que utilizam sulfetos como doadores de elétrons, alguns grupos de microrganismos que atuam neste cenário: Thiobacillusdenitrificanse Thiomicrospiradenitrificans (KUENEN et al., 1992), Pseudomonasstutzeri (MAHMOOD et al., 2009).
A desnitrificação, assim como ocorre com a nitrificação, também sofre a influência das condições ambientais. Porém, as bactérias envolvidas no processo de nitrificação são mais sensíveis que as envolvidas na desnitrificação, logo, quando a primeira se desenvolve a segunda também é possível (METCALF e EDDY, 2004).
Entre as condições ambientais mais importantes no processo de desnitrificação estão a temperatura, o pH, o oxigênio dissolvido, a fonte de carbono (relação C/N) e a concentração de substâncias tóxicas.
Com relação à temperatura, Van Haandel, Kato e Von Sperling (2009), afirmam que a desnitrificação aumenta com temperatura até um valor ótimo de 40ºC. Ainda segundo os autores, a dependência do pH é menor na desnitrificação do que na nitrificação, de modo que quando as condições de nitrificação são atendidas a desnitrificação também ocorrerá de maneira satisfatória.
Vacková et al. (2011) compararam a atividade desnitrificante em quatro temperaturas diferentes: 5, 8, 10 e 15ºC. Para o experimento eles utilizaram biomassa cultivada em lodo ativado a 5ºC. A esta biomassa foi adicionado esgoto sintético com concentração média de nitrato de 50 mg/L. os autores isolaram culturas de Paracoccus denitrificans e Pseudomonas fluorescens. Concluíram que, para ambas as culturas, a atividade desnitrificante foi diretamente proporcional à temperatura.
Warneke et al. (2011) estudaram a desnitrificação utilizando barris com 0,2 m3, testando 6 diferentes fontes de carbono (espigas de milho, palha de
26 madeira de eucalipto) e comparando duas temperaturas (16,8ºC e 27,1ºC). O
efluente utilizado apresentava as seguintes características: 14 – 17 mg/L de NO3—N; 6 – 7 mg/L de OD; 13,5 – 14 mg/L de carbono total. Dentre as 6 fontes
de carbono utilizadas, apenas em uma observou-se maior atividade desnitrificante na menor temperatura. Nas outras cinco, a atividade desnitrificante aumentou com a temperatura.
Altas concentrações de oxigênio dissolvido podem atrapalhar o processo de desnitrificação, uma vez que este elemento é prioritário na cadeia respiratória, e é necessário que ele não esteja presente, ou esteja em pequena concentração, para que as bactérias responsáveis pela desnitrificação utilizem o nitrato e o nitrito para respiração.
Hu et al. (2010), obtiveram desnitrificação em ambiente anóxico de efluente sintético com ausência de oxigênio dissolvido. Contudo, segundo Van Haandel e Marais (1999) a desnitrificação pode ocorrer na presença de oxigênio, desde que não ultrapasse 0,3 mg/L. Ferreira (2000) aponta como nível máximo 1,0 mg/L, a partir do qual ocorre inibição mais intensa da desnitrificação.
Substâncias tóxicas em altas concentrações podem inibir o processo. Contudo, como já foi dito, as bactérias desnitrificantes são menos sensíveis que as nitrificantes, com isso, havendo nitrificação provavelmente a desnitrificação também ocorrerá.
Para que a desnitrificação ocorra é necessário que haja um doador de elétrons, que no caso, é a matéria orgânica biodegradável. Esta fonte de carbono pode ser inserida após a etapa de nitrificação, e, segundo Van Handel, Kato e Von Sperling (2009), as fontes externas de carbono mais usuais são: o metanol, o etanol, a acetona e o ácido acético. Além dessas, pode-se utilizar o próprio esgoto bruto como fonte carbono.
27 conseguiram remover 88% do nitrogênio total, utilizando um reator sequencial em batelada, utilizando fonte interna de carbono.
A relação C/N varia de acordo com a fonte de carbono utilizada. Callado e Foresti (2002) testaram a desnitrificação com diferentes fontes de carbono, e atingiram a desnitrificação completa com as seguintes relações C/N: 0,93 para o metanol; 0,83 para etanol e 0,59 para o gás metano. Além disso, os autores apresentam a seguinte relação DQO/N: 2,86 para efluente anaeróbio e 5,52 para um substrato sintético que possuía características semelhantes ao esgoto doméstico.
Henze et al. (1997) apresentam uma relação ótima de DQO/N de 4 a 5, quando a fonte de carbono é a matéria orgânica, e de 3,1 a 3,7, para o caso da fonte de carbono ser o ácido acético. Kujawa e Klapwilk (1999) analisaram a literatura acerca da desnitrificação e apresenta uma relação DQO/N que varia desde 4 até 15. Além disso, verificaram que uma relação DQO/N abaixo de 3,5 a desnitrificação não é possível.
Yang et al. (2012) trataram esgotos domésticos em um sistema de lodos ativados. Os autores testaram três diferentes fontes de carbono – citrato, acetato e glicose. Concluíram que a desnitrificação ocorreu mais intensamente quando da adição do citrato e do acetato, 80% e 75% de eficiência na remoção de N respectivamente. No caso da glicose, a eficiência foi de 57%.
Essa grande variedade de relações C/N decorre do fato que sistemas biológicos similares podem ter diferentes relações ótimas de carbono e nitrogênio quando usados para tratar diferentes águas residuárias sob condições ambientais distintas. Por esta razão, a relação C/N ótima para sistemas desnitrificantes biológicos para tratar águas residuárias específicas deve ser determinada experimentalmente (IAMAMOTO, 2006).
O tipo de carbono disponível também influencia a taxa de crescimento bacteriano dos organismos desnitrificantes. Zhao et al. (2010) estudaram três diferentes fontes de carbono no tratamento de esgotos domésticos por wetland. Os autores apresentaram taxas de crescimento de 0,11, 0,12 e 0,08 d-1 para
28 A desnitrificação não é o único processo que pode ocorrer para remoção do nitrato, em meio anóxico. Este processo pode ocorrer através da Redução Assimilativa do Nitrato a Amônio. Neste processo o nitrato é convertido a nitrito e depois a amônia e sendo incorporado na forma de proteína ou acido nucléico à biomassa (BITTON, 2005).
Redução Assimilativa do Nitrato
NO3- NO2- NOH NO2OH NH4+ (3.8)
3.1.3 Nitrificação e desnitrificação simultâneas
Como o nome já deixa claro, o processo de nitrificação e desnitrificação simultânea (conhecido por sua sigla em inglês – SND) é o processo de remoção biológica do material nitrogenado que ocorre simultaneamente em um mesmo ambiente e em condições operacionais idênticas.
Chiu et al. (2007) afirmam que a nitrificação e desnitrificação simultânea ocorre devido a distribuição desigual do oxigênio dissolvido dentro do reator. Em ambientes com grande concentração de OD as bactérias nitrificantes são mais ativas, e em áreas com menor concentração de OD prevalecem as bactérias desnitrificante.
Contudo, algumas bactérias são capazes de promover a desnitrificação independentemente da concentração de OD, são exemplos desses organismos: Microvirgula aerofenitrificans (PATUREAU et al., 2000), T. pantotropha (GUPTA, 1997).
29 O tempo de retenção celular é fator preponderante no processo de SND. Como visto nos itens 3.1.1 e 3.1.2, os tempos de crescimento das bactérias envolvidas nos processos de nitrificação e desnitrificação são diferentes, desta forma, é necessário que o tempo de retenção celular seja suficiente para que todas as populações se estabeleçam.
Sistemas com tempo de retenção celular baixo podem, inclusive, impossibilitar a nitratação. É o caso do estudo realizado por Naseer et al. (2013). Os autores pesquisaram sobre nitrificação e desnitrificação simultâneas em sistema de lodos ativados alimentado com esgotos tipicamente domésticos. Concluíram que tempo de retenção celular entre 5 e 10 dias apresenta as condições mais propicias para que a nitratação seja inibida.
Nos lodos ativados é possível atingir a SND em sistemas de aeração prolongada (METCALF e EDDY, 2004).
Gong et al. (2012) trabalharam com uma associação entre reatores de leito fixo e móvel, conseguiram eficiência de até 42,2% na remoção de nitrogênio com tempo de retenção celular de 149 dias, tratando esgoto doméstico rural, com DQO média de 212 mg/L, Nitrogênio total de 72 mg/L e relação C/N de 2,94.
Hocaoglu et al. (2011) estudaram a nitrificação e desnitrificação simultâneas em um reator MBR, utilizando esgoto doméstico forte (DQO média de 930 mg/L, NH4+ média de 140 mg/L). Os autores auferiram a eficiência na
remoção de N comparando dois tempos de retenção celular, 20 e 60 dias. Concluíram que os resultados para o TRC de 60 dias foi significativamente mais eficiente do que os resultados para 20 dias (73% e 49% de eficiência, respectivamente).
30 Hocaoglu et al. (2011), nas condições citadas anteriormente, concluíram que no processo de SND a desnitrificação teve eficiência de 97% com concentração de OD entre 0,15 e 0,20 mg/L. Já quando a concentração foi elevada para a faixa de 0,5 a 0,55 mg/L, a eficiência na desnitrificação caiu para 37%
Diversos estudos indicam concentrações típicas de OD para a SND. A maioria trabalha com concentrações de OD em torno de 1 mg/L ou menores. É o caso Third et al. (2005), que trabalharam com biofiltro em batelada. Já He et al. (2009), testaram os efeitos de fatores biológicos no processo de SND, utilizando um reator MBR. Dentre as faixas de concentração de OD testadas, concluiu que acima de 1,5 mg/L a desnitrificação ficava menos eficiente.
Entretanto, há trabalhos que mostram resultados expressivos com concentrações de OD acima destes valores. Um exemplo é o estudo apresentado por Seifi e Fazaelipoor (2012). Os autores trabalharam com um reator de leito fluidizado que tratou esgotos com concentrações médias de DQO e NH4+ de 300 mg/L e 25 mg/L, respectivamente. A concentração de
oxigênio dissolvido foi de 2 mg/L e a eficiência na remoção de nitrogênio por SND foi de 60%.
Outro exemplo é o trabalho de Virdis et al. (2011), que atingiram 87% de eficiência na remoção de nitrogênio com concentração média de OD em torno de 5,7 mg/L.
Outro ponto importante no processo de nitrificação e desnitrificação simultâneas é a relação carbono nitrogênio (C/N). Xia et al. (2008), estudando um biofiltro compacto projetado para promover a nitrificação e desnitrificação simultâneas, concluíram que a concentração de bactérias AOB e NOB são inversamente proporcionais a concentração de material carbonáceo.
31 domésticos com as seguintes características médias: DQO = 380 mg/L; N = 38,4 mg/L; pH = 7,6 e SS = 190 mg/L.
Zielinska et al. (2012), trabalhando com um reator de lodos ativados, estudaram o impacto da relação DQO/N e OD na remoção de nitrogênio pelo processo de nitrificação e desnitrificação simultâneas. Utilizaram esgoto sintético com as seguintes características básicas: NTK de 63,1mg/L; Amônia 26,6 mg/L; DQO máxima de 434,8 mg/L. Concluíram que a maior eficiência de remoção de N por SND foi de 50% com relação de DQO/N de 6,8 e OD de 0,5 mg/L.
A relação DQO/NO3- aliada ao tipo de substrato utilizado pode interferir
no processo de desnitrificação. Ge et al. (2012) trataram esgotos domésticos em lodos ativados com diferentes fontes de carbono. Perceberam que quando a relação entre DQO/NO3- esteve acima de 6 a desnitrificação não foi completa,
ocorrendo acúmulo de nitrito.
Resultados similares foram observados por Xie et al. (2012). Os autores utilizaram reatores preenchidos com lodo granular em escala de laboratório. Concluíram que a relação DQO/NO3- acima de 7 favorecia a formação de nitrito
ao invés da formação de N2 na desnitrificação.
Este acúmulo é provocado pela competição por elétrons as redutase de nitrato e nitrito. Entretanto, o acúmulo ou não de nitrito dependerá do tipo de substrato utilizado. Substratos diferentes representam diferenças no metabolismo e na velocidade na transferência de elétrons, o que é decisivo nas taxas de redução de nitrito e nitrato (GE et al., 2012).
3.1.4 Oxidação Parcial da Amônia (SHARON)
No processo SHARON a nitratação é inibida, desta forma, a amônia é oxidada até nitrito. A nitrificação parcial permite a economia de aproximadamente 25% de energia, 30% na produção de lodo e, em torno de 20% menos emissão de CO2 (SRI SHALINI; JOSEPH, 2012). A equação 3.9
32 NH4 + 0,75O2 + HCO3- 0,5NO2- + 0,5NH4+ + CO2 + 1,5H2O (3.9)
Para que a nitrificação parcial ocorra é fundamental o controle de parâmetros como oxigênio dissolvido, pH, temperatura e tempo de detenção .
Lan et al. (2011) estudando o lodo proveniente de um tanque aerado que tratava lixiviado de aterro sanitário, concluíram que com tempo de detenção hidráulica de 9 dias, OD em torno de 0,5 mg/L e pH próximo a 8, é possível remover cerca de 86% do nitrogênio afluente com a combinação de nitrificação parcial e ANAMMOX.
Ainda segundo os autores, quando o tempo de detenção hidráulica é reduzido para 3 dias, a eficiência na remoção de N nas mesmas condições cai para 42%.
Xu et al. (2012) trabalharam com um reator granular aeróbio e efluente com baixa relação C/N, OD abaixo de 5 mg/L, pH entre 7,8 e 8 e temperatura de 25ºC. Observaram eficiência de 57% na remoção de nitrogênio via nitrito.
Estes valores de pH são corroborados por Sri-Shalini e Joseph (2012), que afirmam que as bactérias que oxidam amônia apresentam faixa ótima de pH entre 7,9 e 8,2. Enquanto as bactérias que oxidam nitrito têm pH ótimo entre 7,2 e 7,6.
3.1.5 Oxidação Anaeróbia da Amônia (ANAMMOX)
Para que a oxidação anaeróbia da amônia ocorra é fundamental que tenha havido previamente uma etapa de oxidação parcial da amônia. Neste caso, parte do nitrogênio deverá está na forma de nitrito.
33 NH4+ + 1,32NO2− + 0,066HCO3− + 0,13H+ 1,02N2 + 0,256NO3− +
0,066CH2O0,5N0,15 + 2,03H2O
(3.8)
Apesar de o nitrito ser elemento fundamental para que o processo ocorra, em concentrações elevadas ele torna-se inibidor.
Kimura et al. (2010) trabalharam com reator inoculado com lodo de reator de leito fixo, com temperatura de 36ºC e concentração de oxigênio dissolvido de 0,5 mg/L. Chegaram a conclusão que as bactérias ANAMMOX começam a apresentar inibição quando a concentração de nitrito atinge 300 mg/L. Quando a concentração de NO2- atinge 330 e 430 mg/L, a inibição é de
25% e 37%, respectivamente.
Entretanto, Yang et al. (2011), estudando um reator alimentado com esgoto sintético contendo basicamente NH4+ e NO2-, por 92 dias e com
temperatura que variou entre 23 e 33ºC. Afirmam que não houve inibição aparente quando a concentração de nitrito chegou a 465 mg/L com temperatura de 33ºC, e nem com concentração de 436 mg/L com temperatura de 23ºC.
A amônia também pode ser um agente inibidor. Fernández et al., (2012) estudaram um reator sequencial em batelada em escala de laboratório, inoculado com biomassa proveniente de biofiltro. Concluíram que 38 mg NH3N/L foram suficientes para inibir em 50% a atividade das bactérias
ANAMMOX, e que 100 mg NH3-N/L, foram suficientes para inibição de 80% da
atividade destas bactérias. Concluíram também que 11 µg HNO2-N/L foi
34 Outro elemento importante a ser considerado no processo ANAMMOX é o carbono. Geralmente este processo é indicado para águas residuárias com baixa concentração de carbono orgânico biodegradável (relação DQO/C menor que 0,5g de DQO/ g de N). Entretanto, relações maiores (entre 0,5 e 1,7 g de DQO/ g de N) também podem apresentar atividade ANAMMOX. (JENNI et al., 2014).
3.1.6 Remoção de Nitrogênio a partir do Nitrito (CANON)
A remoção de nitrogênio a partir do nitrito realizada por bactérias autotróficas (CANON, sigla em inglês para Completely Autotrophic Nitrogen Removal Over Nitrite) é a combinação dos processos de nitrificação parcial e oxidação anaeróbia da amônia em um mesmo reator.
Neste processo o oxigênio é fator limitante, por está razão deve ser mantido em baixas concentrações. Além disso, a atuação de bactérias autotróficas torna desnecessário o aporte externo de carbono. Estas características tornam o processo CANON mais econômico e ambientalmente correto (LI et al., 2012; LIU et al., 2012).
Liu et al. (2012) estudaram cinco reatores em escala de laboratório, alimentados com efluente com concentração de N ente 300 e 400 mg/L. Utilizando o processo CANON, atingiram eficiência de até 85% mantendo a concentração de OD abaixo de 0,7 mg/L.
Zhang et al. (2013) utilizaram reator MBR para comparar a remoção de N utilizando o processo CANON em esgotos sintéticos e domésticos. Para esgotos sintéticos a maior eficiência ocorreu para efluente com concentração média de amônia de 79,95 mg/L e concentração de média de OD de 0,15 mg/L. Já para os esgotos domésticos, a maior eficiência se deu para efluente com 88,04 mg/L de amônia e OD de 0,15 mg/L.
35 A remoção de nitrogênio a partir do nitrito, apesar de eficiente no tratamento de esgotos com baixa concentração de amônia, é mais indicado para efluentes ricos em amônia.
Zhang et al. (2014), que estudaram a interferência da concentração de amônia no CANON utilizando um MBR, concluíram que as bactérias que oxidam nitrito (NOB) desenvolveram-se apenas no reator com baixa concentração de amônia. Nos reatores com elevado nível de amônia, quem predominou foram as bactérias aeróbias que oxidam amônia (AerAOB) e as bactérias anaeróbias que oxidam amônia (AnAOB). Desta forma, a amônia também se mostrou limitante para que o processo CANON ocorresse.
Assim, o processo CANON apresenta-se como uma alternativa na remoção de nitrogênio em águas residuárias com baixa concentração de carbono e com economia de oxigênio.
3.2 Lodos Ativados
O sistema de lodo ativado é conhecido como unidades eficientes de remoção de material orgânico, sólidos em suspensão e, eventualmente, também macronutrientes, produzindo um efluente de alta qualidade (MEDEIROS, CAVALCANTI, VAN HAANDEL, 2005). No entanto, o sistema de Lodos Ativados não se configura tecnologia universal, haja vista apresentar elevados custos de implantação e operação, e demandar mão-de-obra sofisticada.
O lodo ativado é formado, principalmente de bactérias, algas, fungos e protozoários, sendo as bactérias os microrganismos de maior importância, uma vez que são responsáveis pela degradação da matéria orgânica e pela formação dos flocos.
36 A maior idade de lodo usual para sistemas de lodo ativado convencional é de 10 dias, sistemas de lodos ativados com idade de lodo entre 18 e 30 dias são considerados de aeração prolongada (SANTOS, 2009). Além disso, deve-se levar em consideração o tempo de detenção hidráulico (TDH), que para Von Sperling (2012) deve estar em torno de 16 a 24h para caracterizar um sistema de lodos ativados com aeração prolongada.
Von Sperling e Fróes (1998), em seu estudo de caracterização da estação de tratamento de esgotos de Morro Altos, na região metropolitana de Belo Horizonte, determinaram uma idade de lodo média de 26,2 dias, caracterizando assim um sistema de lodos ativados de aeração prolongada.
Esta elevada idade do lodo é um dos principais pontos favoráveis do reator. Quanto maior o tempo de permanência do lodo em seu interior menor será a quantidade de matéria orgânica por unidade de volume. Isto obrigará as bactérias a intensificar o catabolismo celular, passando a consumir a matéria orgânica de suas células. O lodo final produzido encontra-se bastante mineralizado e com um menor risco sanitário, além de produzir um efluente final com baixa concentração de sólidos suspensos totais e DBO.
A DBO solúvel do efluente final de um sistema de lodo ativado de aeração prolongada é praticamente desprezível. A DBO total deste tipo de sistema é em sua maioria devida aos sólidos em suspensão efluentes do decantador secundário (VON SPERLING e FRÓES, 1998).
Os lodos ativados são bastante eficientes na remoção de nitrogênio dos esgotos sanitários. É comum observar sistemas com eficiências próximas ou superiores a 90% (KIM et al., 2011; ZIELINSKA et al., 2012; FUKUSHIMA et al., 2013). Incluindo, neste cenário, estações projetadas para realizar a nitrificação e desnitrificação simultâneas (SATOH et al., 2003).
Com relação à carga de oxigênio aplicada ao sistema de lodos ativados, Jordão e Pessoa (2009) indicam que é recomendável aplicar 2,5 vezes a carga média de DBO5, para sistemas projetados para promover a nitrificação. Indicam
37 provenientes de reatores anaeróbios do tipo UASB, a carga de oxigênio recomendada é de 4 vezes a carga média de DBO5.
3.3 Moving Bed Biofilm Reactor (MBBR)
O MBBR, conhecido no Brasil por Reator de Leito Móvel com Biofilme, foi desenvolvido com o objetivo de compilar em um único sistema as características de duas tecnologias: a de lodos ativados e a de biofiltros. Desta forma, a biomassa se desenvolve aderida ao material suporte que, por sua vez, se move livremente no interior do reator.
Esta associação permite que o reator tenha uma série de vantagens em relação aos lodos ativados e aos biofiltros: Não necessita de recirculação de lodo; todo volume do reator é utilizado para o crescimento da biomassa; perda de carga insignificante; resistência a cargas de choque; requer menos espaço para implantação; a concentração de biomassa a ser separada é pelo menos 10 vezes menor (AYGUN et al., 2008; ØDEGAARD et al., 1999; JAHREN et al., 2002).
Contudo, algumas desvantagens são percebidas neste tipo de sistema. Schneider (2010) destaca o alto consumo energético e Reis (2007) aponta o alto custo efetivo de instalação e operação.
O MBBR pode ser operado em condições aeróbia, anóxica ou anaeróbia. No sistema aeróbio a própria agitação causada pela aeração provoca a circulação do material suporte no interior do reator. No caso dos sistemas anóxico e anaeróbio é necessário a utilização de um agitador mecânico.
38 Aspectos fundamentais para operação de um MBBR devem ser observados: Schneider (2010) apresenta a razão de recheio, a hidrodinâmica do reator, a vazão de ar (para sistemas operados aerobiamente), e a formação do biofilme como os mais relevantes.
A razão de recheio consiste na razão entre volume ocupado pelo material suporte e o volume total do reator. Aygun et al. (2008) recomendam que esta razão fique entre 30 e 70%. Para Rusten et al. (2006), razões superiores a 70% dificultam a boa movimentação do material suporte no interior do reator, este aspecto pode provocar um formação de um biofilme mais espesso, o que leva a uma perda de rendimento do reator.
A turbulência no interior do reator é fundamental para a boa eficiência do tratamento. Em sistemas aeróbios esta agitação é garantida pela própria aeração. Rusten et al. (2006) afirmam que esta agitação garante a transferência de oxigênio dissolvido e dos nutrientes até os microrganismos, evita a formação de zonas estagnadas e a formação de biofilme espesso.
Apesar de importante para o funcionamento do MBBR, uma agitação excessiva pode causar desprendimento muito acentuado do biofilme, podendo resultar em efluente com grande concentração de sólidos.
O material suporte representa uma proteção para o desenvolvimento do biofilme. De acordo com o que afirmam Lazarova e Manem (1995), os microrganismos que se desenvolvem aderidos a uma superfície de contato são menos afetados pelos fatores ambientais externos do que os microrganismos com crescimento em suspensão.
Nos sistemas MBBR o biofilme se desenvolve essencialmente na parte interna dos suportes, uma vez que, a parte externa dos suportes está constantemente colidindo umas com as outras, limitando o desenvolvimento do biofilme (RUSTEN et al., 2006; AYGUN et al., 2001).
3.4 Biofiltro Aerado Submerso (BAS)
39 matéria orgânica em esgotos domésticos. Suas principais vantagens são: a pequena ocupação de área, operação simples, o aspecto modular, simplificando extensões futuras, baixo impacto ambiental, efetivo no tratamento de odores, e a eliminação da decantação secundária, suprimindo problemas de separação de lodo em unidades de clarificação (GONÇALVES et al., 2001).
Os reatores com biomassa aderida são unidades que possuem suporte físico que permite a imobilização dos microrganismos responsáveis pela degradação de compostos orgânicos e inorgânicos presentes nos efluentes sanitários ou industriais (FLORÊNCIO et al. 2009). Estes reatores podem ser projetados de forma a permitir que ocorram os processos de nitrificação e desnitrificação, reduzindo, e em casos mais extremos até eliminando o nitrogênio presente no meio.
Em sua pesquisa, GÁLVEZ et al. (2003), observaram eficiência na oxidação do nitrogênio amoniacal de 100% e eficiência de 95% na desnitrificação. Para isto, os autores trabalharam com esgotos domésticos em escala de laboratório, utilizando um biofiltro aerado submerso (BAS) constituído por dois tubos de 6 cm de diâmetro e 2 metros de altura, preenchidos com argila expandida, com um TDH de 1,6h, vazão de ar de 7,8 m3/m2h e utilizando metanol na razão de DQO/N de 2,37 como fonte de carbono.
Cheng et al. (2009) trabalharam com uma associação entre reator anaeróbio e biofiltro aerado submerso, em escala de laboratório, tratando esgotos domésticos. Como material de enchimento, os autores utilizaram espuma de poliuretano, que permite 80% de vazios. Desta forma, aplicando o processo de nitrificação e desnitrificação simultâneas, alcançaram 94% de eficiência na remoção da amônia.
40 Esta configuração permite que o BAS seja mais compacto do que o sistema de lodos ativados e não necessitem de etapa de clarificação complementar dos seus efluentes.
Além disso, é importante configurar reatores capazes de concentrar a maior quantidade de biomassa por volume. O tempo de retenção celular elevado contribui favoravelmente a qualidade final do efluente (LOPES, 2009).
O efluente deste tipo de reator apresenta geralmente baixa concentração de sólidos e matéria orgânica e, normalmente, ocorre a nitrificação do efluente. Segundo Lopes (2009), este tipo de configuração tem elevada capacidade de responder a mudanças de temperatura, vazão, redução do pH e outras condições desfavoráveis, tais como a falta de oxigênio, conseguindo retomar a operação normal em curto espaço de tempo após sanadas as condições desfavoráveis.
Hirakawa, Piveli e Além Sobrinho (2001) aplicaram um BAS em escala piloto e com fluxo descendente, com leito fixo com 32,7L de volume aparente, no pós-tratamento de reator UASB (604L) com esgoto sanitário e verificaram o conjunto com eficiência de 91% na remoção de DBO. Ainda neste experimento observou-se que o BAS foi capaz de promover a remoção de nitrogênio amoniacal durante um determinado tempo. A taxa de aplicação deste experimento foi de 4 kgDQO/ m³.dia.
3.5 Acúmulo de lodo
Em um processo de transformação da matéria orgânica através da ação de agentes biológicos, é obvio afirmar que quanto maior o acúmulo desses agentes, mais eficiente e rápido será o processo de transformação.
Desta maneira, uma forma indicada para estimar a quantidade de microrganismos no interior dos filtros é determinar a quantidade de lodo retido em seu interior.
41 suporte) e nos espaços vazios entre eles. No caso dos biofiltros alvo desta tese, além desses ambientes a biomassa também se desenvolve nos interstícios do material de enchimento, permitindo que ela se acumule e se desenvolva em maior quantidade, e, consequentemente, apresente maior eficiência na remoção da matéria orgânica.
Von Sperling (1996) e Jordão e Pessoa (2009), dizem que o crescimento bacteriano, chamado também de produção de biomassa, pode ser expresso em função do substrato utilizado, de maneira que quanto mais substrato é assimilado maior é a taxa de crescimento bacteriano. Esta relação é apresentada na equação 3.9.
Produção bruta de sólidos
= . (3.9)
Na qual:
X = Concentração de microrganismos, SS ou SSV (g/m3)
Y = Coeficiente de produção celular (biomassa produzida por unidade de massa de substrato removido). Neste caso a biomassa pode ser apresentada na forma de SS ou SST, e a o substrato na forma de DBO5 ou DQO. (g/g)
S = Concentração de DBO5 ou substrato no reator (g/m3)
T = Tempo (d)
42 Produção líquida de sólidos
= . − . (3.10)
O coeficiente de produção celular (Y) é estimado através de testes laboratoriais utilizando o esgoto a ser tratado. Von sperling (1996) traz os seguintes valores para tratamento aeróbio:
43 4 MATERIAL E MÉTODOS
A pesquisa se desenvolve utilizando dois biofiltros aerados localizados no espaço físico da Estação de Tratamento de Esgotos do Campus Central da Universidade Federal do Rio Grande do Norte – UFRN – em Natal, e durou de setembro de 2012 até dezembro de 2014.
Estes biofiltros que apresentam elevado índice de vazios, são aplicados no pós-tratamento de efluentes anaeróbios e buscam remover biologicamente compostos nitrogenados de esgotos sanitários através do processo de nitrificação e desnitrificação simultâneas, sem, no entanto, serem necessárias remoções constantes de lodo.
Com o objetivo de aprimorar a tecnologia, utilizou-se eletroduto corrugado cortado para enchimento de biofiltros aerados de leito submerso, com alto índice de vazio (cerca de 90%), e consequente alta capacidade de retenção da biomassa no interior do reator, produzindo efluente com baixa turbidez, que dispensa a necessidade de decantadores secundários, reduzindo os custos de implantação e operação.
O filtro aerado com leito fixo de material plástico com alto índice de vazios, que de fato constitui uma nova tecnologia de tratamento de esgotos, porque tanto contém lodo em suspensão nos interstícios como retém biomassa aderida ao material de enchimento, que é o princípio de funcionamento dos biofiltros aerados submersos. Contudo, distinguem-se bastante destes, porque a grande quantidade de lodo retido nos interstícios tem papel de destaque na biodegradação, assim como distinguem-se também dos reatores de leito móvel com biofilme, porque o leito é fixo e retém maior quantidade de sólidos nos interstícios do material de enchimento.
44 4.1 Descrição do reator anaeróbio pré-existente
Os reatores utilizados nesta pesquisa foram inicialmente desenvolvidos para tratarem esgotos domésticos em condições anaeróbias e eram compostos por: um decanto-digestor prismático retangular com duas câmaras em série, seguido por um pequeno filtro de brita nº4 com fluxo ascendente (denominado Sistema RN), ladeados por quatro filtros anaeróbios, conforme Figura 4.1.
Figura 4.1: Detalhamento do sistema anaeróbio pré-existente
Fonte: Autor (2015)
O decanto-digestor prismático retangular possui duas câmaras em série, sendo a primeira com 2,25 m de comprimento, 1,40 m de largura e 1,20 m de profundidade, e a segunda com 1,65 m de comprimento, 1,40 m de largura e 1,20 m de comprimento, perfazendo um volume total de 8,82 m³. É construído em alvenaria de tijolo cerâmico revestido e impermeabilizado com argamassa de cimento e areia. As câmaras são separadas por uma fenda horizontal de 0,15 m de altura situada a 0,80 m da laje de fundo do tanque.
45 Cada filtro possui 4,00 m de comprimento, 0,70 m de largura e profundidade média útil de 1,20 m, totalizando 3,36 m³ de volume médio útil. Ao final de cada filtro existe um compartimento de 0,72 m³, que tem várias finalidades: limpeza do filtro para remoção do lodo em excesso através do esgotamento sem remoção do meio suporte; tratamento químico complementar eventual.
Dois filtros anaeróbios foram preenchidos com tijolo cerâmico e peças plásticas, conforme apresentado na Figura 4.2. Os outros dois foram preenchidos com eletroduto cortado, e serão detalhados à frente.
Figura 4.2: Tijolo cerâmico e peças plásticas, utilizados como material de enchimento para os filtros anaeróbios.
Fonte: Autor (2015)
Para esta pesquisa, o filtro anaeróbio preenchido com tijolo cerâmico foi desativado, permanecendo em funcionamento o tanque séptico, o filtro anaeróbio preenchido com peças plásticas e os dois filtros preenchidos com eletroduto cortado.
4.2 Descrição do sistema aerado utilizado na pesquisa
46 Além disso, baseado em pesquisas anteriores de Bezerra Filho et al. (2013) e Araújo (2009), percebeu-se que a quantidade de carbono que chegava aos biofiltros aerados era de difícil assimilação e em quantidade insuficiente para garantir o processo de desnitrificação. Para tentar minimizar este efeito negativo, o filtro preenchido com tijolo cerâmico foi desativado. Entretanto, essa medida não foi suficiente para garantir o carbono necessário para o metabolismo celular das bactérias desnitrificantes, sendo fundamental a introdução de uma fonte externa de carbono, que será apresentada posteriormente.
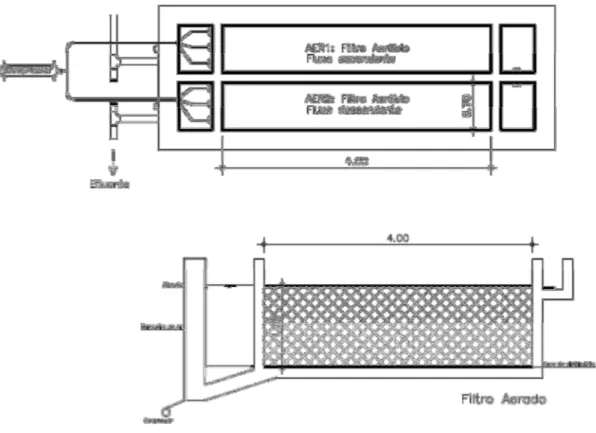
A Figura 4.3 apresenta a planta baixa e o corte esquemático dos biofiltros aerados submersos utilizados na pesquisa. Conforme se observa, cada filtro possui 4,00 m de comprimento, 0,70 m de largura e para o experimento foi adotada profundidade média da lâmina d’água de 1,22 m, totalizando 3,42 m³ de volume médio total. Desconsiderando o volume ocupado pelo material suporte, tem-se 3,08 m3 de volume útil.
O fluxo do esgoto no interior do sistema é o seguinte: o afluente (efluente anaeróbio) entra no primeiro filtro aerado (chamado AER1) pela parte inferior, através de três canos de PVC com diâmetro de 75 mm dispostos sobre o piso do filtro, e é recolhido na superfície por duas calhas feitas em cano de PVC, também com 75 mm de diâmetro, acomodadas sobre o material de enchimento; em seguida passa ao segundo filtro aerado (chamado AER2), onde o processo se inverte, o esgoto é distribuído por duas calhas na superfície e recolhido por três canos de PVC no piso do filtro, conforme observado na Figura 4.4. O efluente do AER2 é o efluente final do sistema.
47 Figura 4.3: Planta baixa e corte esquemático dos filtros utilizados na pesquisa.
Fonte: Autor (2015)
Figura 4.4: Calhas em PVC de 75 mm de diâmetro disposto sobre o material de enchimento (Esquerda). Canos de distribuição do esgoto com o mesmo diâmetro, dispostos sobre o fundo dos biofiltros (Direita).