ENE-204: Energia nuclear
Prof. Dr. Jose Rubens Maiorino Prof.Dr. João Manoel Losada Moreira
Engenharia da Energia CESC
Joserubens.maiorino@ufabc.edu.br
PLANEJAMENTO
•AULA 1(25/09): NOÇÕES DE FÍSICA ATÔMICA E NUCLEAR (MAIORINO)
•AULA 2(02/10): INTERAÇÃO DA RADIAÇÃO COM A MATÉRIA (MAIORINO)
•AULA 3(09/10): APLICAÇÕES NÃO ENERGÉTICAS PACIFICAS (MAIORINO)
•AULA 4(16/10): REATORES NUCLEARES E CICLO DO COMBUSTÍVEL (MOREIRA)
•AULA 5(23/10): TEORIA DO REATOR NUCLEAR (MOREIRA) -ESTATICA
•AULA 6(06/11): TEORIA DO REATOR NUCLEAR (MOREIRA) - DINÂMICA
•AULA 7(13/11): TERMO-HIDRÁULICA DE REATORES (MAIORINO)
•AULA 8(27/11): SEGURANÇA NUCLEAR E ACIDENTES (MAIORINO)
•AULA 10(04/12) ECONOMIA, IMPACTOS AMBIENTAIS E PERSPECTIVAS FUTURAS (MOREIRA)
A gênese da energia nuclear
•
1805: átomo indivisível
•
1896: descoberta da radioatividade (Bequerel).
Questiona-se a indivisibilidade do átomo
•
1897: descoberta dos elétrons (Thomson)
•
1898: Ra, Th, Po (Pierre e Marie Curie)
•
1911: modelo atômico de Rutherford
•
1913: modelo atômico de Bohr
A gênese da energia nuclear: a fissão
•
1931: Chadwick confirma a existência do nêutron
•
1934: Joliot Curie e a radioatividade artificial
•
1935: Fermi produz os primeiros núcleos radioativos
•
1937: Hahn, Meitner, Strassman e a fissão nuclear
•
1938: demonstração da emissão de nêutrons na fissão,
reações em cadeia (Joliot Curie)
2 dezembro 1942: o Chicago Pile I demonstra a
primeira reação de fissão nuclear em cadeia auto
As principais partículas
•
Elétron: m
e=9,10954x10
-31kg; e=1,60219x10
-19C
•
Pósitron: anti partícula do elétron
•
Próton: m
p=1,67265x10
-27kg; mesma carga do
elétron
•
Nêutron: m
n=1,67495x10
-27kg; n→p+β
(T
1/2
=12
minutos)
•
Fóton: ondas eletromagnéticas (m=0;
q=0,c=2,9979x10
8m/s)
Estrutura Atômica e Nuclear
zXA: nuclideo ou isótopo
A= numero de massa=
prótons(Z)+ nêutrons(N) Z= numero atômico ( numero
de prótons/elétrons)
• Isótopos: mesmo Z(
quimicamente idênticos):
1H1; 1H2(deutério);
1H3(trítio)/ 92U235(0,3%); 92U238 (99,7%). Estáveis ou
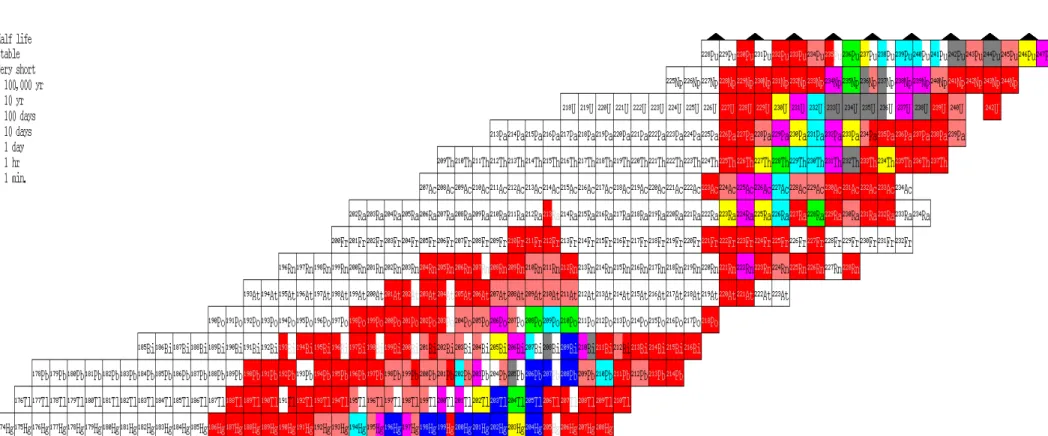
Tabela de Nuclideos
•
http://atom.kaeri.re.kr
Exemplo
•
Um copo de água contem 6,6x10
24átomos de
hidrogênio, sabendo-se que a abundancia
isotópica do deutério e 0,015 % em atomos,
quantos átomos de deutério existe no copo de
água:
Solução :
100%---6,6x1024 átomos de Hidrogênio
0,015--- átomos de D
Massa Atômica e Molecular
A massa atômica de um isótopo é definida como a
massa do átomo neutro relativo a massa atômica do
átomo neutro do
12C numa escala em que esta é
arbitrariamente tomada com o valor 12 , ou seja, a
massa atômica do isótopo
AZ, é dada por:
)
(
)
(
12
)
(
12C
m
Z
m
x
Z
M
A
Unidade de Massa Atômica
• O numero de Avogrado( Na=0,6022045x10-24),
é igual ao numero de átomos/moléculas contidos em uma massa atômica/massa molecular de qualquer elemento, então:
Massa do átomo do 12C: m(12C)=12/0,6022045=1,99268x10-23gr.
• Define-se 1 unidade de massa atômica(uma), como:
Massa Atômica e Molecular
Um elemento é constituído de vários isótopos , então se fi é a abundância isotópica em percentagem atômica do isótopo i com massa atômica Mi, então a massa atômica do elemento é dada por:
A massa molecular relativa ao 12C é a soma das massas
atômicas dos átomos que constituem a molécula. Por exemplo a massa molecular da molécula de O2 é
2x15,99938=31, 99876.
100
/
i i
i
M
f
Unidade de Massa Atômica
• O numero de Avogrado( Na=0,6022045x10-24),
é igual ao numero de átomos/moléculas contidos em uma massa atômica/massa molecular de qualquer elemento, então:
Massa do átomo do 12C: m(12C)=12/0,6022045=1,99268x10-23gr.
• Define-se 1 unidade de massa atômica(uma), como:
EXEMPLO
Usando os dados de massas atômicas da tabela,
calcule a massa atômica do oxigênio natural:
isótopo Abundância % atômica
Massa atômica
16O 99,759 15,99492
17O 0,037 16.99913 18O 0,204 17,99916
Solução:
Densidade Atômica
•
Calcular o numero de átomos/moléculas em 1 cm
3?
N=N
avρ/M(moléculas)
N
av=6,6022x10
23átomos/moléculas em 1 mol
N
i=n
iN
avρ/M(átomos)
•
Mistura
de
Elementos,
w
i=porcentagem
em
peso(w/o)
Raio Nuclear e Atômico
• Raio do átomo~2x10-10cm=2x10-2 A(1A~10-8 cm)
Exercícios Propostos
1. A massa atômica do59Co é 58,93319. Quantas vezes o 59Co é mais pesado que o 12C?
2. Quantos átomos existem em 10 gr de 12C?
3. O urânio Natural é composto de 3 isótopos 234U; 235U; 238U. A
abundância natural e as massas atômicas são dadas na tabela abaixo. Calcule a massa atômica do urânio natural?
Isótopo abundância% massa atômica
4. Estime o raio do núcleo do 238U e estime a densidade nuclear em g/cm3
levando em conta que cada nucleon tem massa de 1,5x10-24 gr.
234U 0,0057 234,0409
Exercícios Propostos
5.
6.
Estado da Matéria
LÍQUIDO SÓLIDO
GASOSO
Forças Intermoleculares!
Plasma
• Plasma e o quarto estado da matéria. Neste estado todas ligações químicas(moleculares) e atômicas são quebradas, e este estado e basicamente constituída de núcleo atômico(+)e elétrons(-)(matéria Ionizada em
movimento - Chama ou fogo,T=milhares- milhões K
).
Nota: Existem outros estados da matéria, por exemplo a matéria nuclear
Sólidos(Corpos Rígidos/deformáveis)
Estados da Matéria
Diamante
Grafite
Líquido(Fluidos incompressíveis)
um estadoda matériano qual a distânciaentre suas moléculasé suficiente para se adequar a qualquer meio (tomando sua forma),porém sem alterar o volume
Estados da Matéria
Gases( Flamengo Caos)- Fluidos Compreensíveis(
ρ
,V variam com P,T)
Distribuição de Maxweell
dE kT E
kT E kT
N dE
E
N( ) 2 exp[ / ]
k= constante de Boltzman=1,3806503x10-23 J/K
OU k=8.617X10-5 eV/K
Ponto de Vista Macroscópico e
Microscópico
Gelo Sólido H20 liquida Vapor
H e O (Gás) Plasma kT dE E EN N E 0 2 3 ) (
1 Temperatura e a medida da
Energia Media das Mol. ou átomos nRT PV T Nk PV T V Nk P kT E V E N P c
c
( ) 2 3 , 3 2
Teoria da Relatividade
Massa e Energia
Postulados da Teoria da Relatividade Especial(
Einstein, A. ,
Ann. Physik,4, 1905)
•
A velocidade da Luz( c ~ 300000 km/s)
independe do sistema de coordenadas e é
uma constante universal
•
As leis da Física( ex: Eqs de Maxwell) são
validas em qualquer sistemas inerciais de
Transformações de Lorentz
P
x x’
Σ Σ ’
v
)
(
;
)
(
' ' ' 'x
c
t
t
z
z
y
y
ct
x
x
c
v
1
)
1
(
2 1/2
Contração do Espaço e Dilatação do
Tempo
Considere 2 eventos ocorrendo simultaneamente em Σ( Δt=0) separados por Δx, então em Σ’, , ou seja γΔx, e desde que γ≥1, Δx≤Δx’, ou seja para um observador em repouso um objeto em
movimento tem seu comprimento diminuído quando comparado
com o mesmo objeto em repouso( contração de Lorentz). Da mesma maneira ,
eventos que ocorrem no mesmo local em Σ’( Δx’=0), e não simultâneos, no
sistema Σ, Δt=γΔt’≥Δt’, ou seja para um observador em repouso, a progressão do
tempo é diminuída para um observador em movimento. Este fato dá origem ao famoso paradoxo dos gêmeos, ou do filme de ficção científica o planeta dos macacos. Dois gêmeos no planeta terra, sendo que um parte para uma viagem espacial com velocidade próxima da luz, após alguns anos terrestres é com supressa que o gêmeo viajante verifica que seu irmão está muito mais velho do que ele. Cientificamente estes fenômenos podem ser constatados pelo fato que
os mésons μ que possuem um tempo de vida média de 2.26x10-6segundos pode
ser detectado na superfície da terra. Assim pela mecânica clássica o livre caminho médio seria de ~ 700 m, enquanto estes penetram ~30 km na
atmosfera( que seria equivalente a um encurtamento em sua vida para ~10-4
segundos.
ENERGIA NUCLEAR
•
A+B→ C+D: Q=[(M
A+M
B)- (M
C+ M
D)]c
2=
VARIAÇÃO DA ENERGIA CINÉTICA( 1 uma=
931.478 MeV)
•
235U +
1n→ (
236U)*→
140Cs +
93Rb + 3
1n + γ(
exemplo típico de fissão)+ neutrino
•
Calcule Q=931,478
∆M≈200 MeV
Elementos da Mecânica Quântica
Comprimento de Onda de Partículas
De Broglie( Tese de Doutorado, 1924): partícula de
momento p pode ser interpretada como uma onda de λ= h/p( h é a constante de Plank; E=hν). Em 1927 Davison&
Germer DEMONSTRARAM EXPERIMENTALMENTE O COMPORTAMENTO ONDULATÓRIO DE PARTÍCULAS( ELETRONS)
Mecânica Ondulatória( Schrondinger) Mecânica Matricial( Heisenberg)
Equação de Schondinger
• Max Plank: E=hυ( Emissão de corpo negro), h= 6.6256x10-27 erg.seg( quantum de Energia)
• Einsten- Efeito fotoelétrico(1905)- Premio
Nobel-Comportamento de partícula da radiação eletromagnética: Momento= hν/c=h/λ
• Niels Bohr( 1913): teoria semi clássica e quântica. Postulados: 1) Um sistema atômico existe em certos estados estacionários de energia Ej, 2) A transição entre estados estacionários é
acompanhada pela absorção ou emissão de energia, , 3) os estados estacionários
são dados por: n=1,2,...h
E E2 1
0
)
(
8
2 22
E
V
h
m
Para cada sistema existe umafunção(de onda),Ψ que descreve
totalmente o sistema
nh mv
r( ) 2
Estados Atômicos e Excitação
• A solução da Equação de Schondinger aplicada, por exemplo ao atomo de hidrogênio (V=e2/r), fornece que os elétrons somente podem ocupar
determinados níveis de energia( números quanticos).
Níveis de Energia do H
h E E2 1
Átomo de 6C12-Orbitas K,L,....( Valencia)
A energia suficiente para arrancar um elétron de uma orbita, e chamada de Energia de ionização
Estado fundamental nh mv
Núcleo Atômico
• Modelos das Camadas equivalente aos níveis de Energia do
átomo-Mecânica quântica
•
Modelo da Gota Liquida
(Bohr)
Energia de Ligação
Δ
=ZM
p+NM
n-M
AΔ
=Z(M
p+m
e)+NM
n-(M
A+Zm
e)
Δ
=ZM(
1H)+NM
n
-M
BE/NUCLEON=
Δ
/A(Energia de Ligação
por Nucleon)
Radioatividade
Cálculos de Radioatividade
λ=constante de desintegração radioativa (probabilidade de decaimento/unidade
A=atividade= λN(desintegracoes/segundo 1 Becquerel=1 des./seg
1 Curie(Ci)=3,7x1010des./seg