M
ONITORIZAÇÃO DAS CONCENTRAÇÕES PLASMÁTICAS DE
EFAVIRENZ
:
C
RITÉRIOS DE APLICABILIDADE À PRÁTICA
M
ONITORIZAÇÃO DAS CONCENTRAÇÕES PLASMÁTICAS DE
EFAVIRENZ
:
C
RITÉRIOS DE APLICABILIDADE À PRÁTICA
CLÍNICA E EFEITOS DO FÁRMACO A LONGO TERMO
Prova para obtenção de grau de Doutor em Ciências da Vida, especialidade de Farmacologia
orientada pela Sra. Professora Doutora Emília Monteiro na Faculdade de Ciências Médicas da
Agradecimentos
! " #
$ % " &
! & #
&
' & ( ) * + & , - . & "
& % )
/ & " / "
" / " "
0 * $ " &
1 " 0 / $ &
( # & "
& 2 " "
" & 2 $ % $ 3
0 * " $ " &4
5 3 6 5 7 68
) . " $ %
1 & " &
. 3 + 1
-& 2 3 1
$ . " &
-' & & & "
1 % & "
! " # &/ & ( 1
/ '9. 7
! $ & 3 " : " $ " &
$ & ;+<= + $
7 3 "
& " " 1 5
/ 86 "
" " " $ " 7
) 1 "
= & " 1 " - # # " $ "
$ < & - 3 %
" 8
$ + & $ 2 8 $ %
" : > 5 6
& ? % @ - %> % 7
Instituições onde o trabalho foi realizado
! "
# $ $ "
% & ' ( ) "
* + , ( (- ! !
. / # 0
Financiamento do trabalho
E , 2 3 4
5 ( # / 67* 8 89:;;98:<<=>
5 ? " 6 ?" 8 :<<:>
5 # 0
Artigos científicos com origem na tese de dissertação
* + / / 2 / 4
7 BC . / 5 ' B "
E E ' + /+5 D $ E5
B 7+ 6 >
7 " 7 " E E '
$ E5 F + F + ' + B 7+
:<<GH ;;4 II=5I 6 4 J =:G>
7 K 5C C " E 5
' ' D ' + / /
, D / + D + D + . / / :<<GH
J<4 ;<5;; 6 4 : 9=>
7 K 5C C " E " /5
5 ' $."5 + $ E5
B 7+ :<<;H ;=4 ;<=5;<9 6 4 J =:G>
* / 6 5 (- > ' 4 )" .
+ 6:<<L> 0 $ + A A 6:<<L> (
! <+; B $+ 6:<<G> $+ $)+ 9) ($: ) 6:<<M> $ )" A 6:<<M>
'
Contextualização histórica
$! 0 & A A C D A : 6
=MG=> A 3 '
, + +
, # 7 ! 2 A E .
$ ( N 2
( $ & 4 2 #
, ( ( '2 #
+ 6E $> :I ( 0 + 3 +
? ( /
(-( 0 ' '2 ( # 5
' ' ! =MM; # 5
' ( & (
0 , ' '2 67 =MMG>
( # 5 ' N O
/ ( ' , ' ' &
:< '2 ' 0 2'
! ! ' 6 / ' > (
' / ( E $ P & .9Q !
, ' / ' ( 0 6$ =MM;> E
' (- / '2 4 /
& .9Q 6 &/ > / ' 6 ' &/ >
(-- ' 2 (
' + =MM; =MML
( # 5 ' 0 & ' ,
'
& 6$ + =MMG> E
# ' / H
! / H '2
5 (- '2 + 8 H P
(-2' * , & '
! ' (- 3! # '
' , # # ' 0
'
& ( E $ /
' 2 &/ & (- # 0
# 5 ' , , & '!
! 3 ! ' ' #
. , # # 5& ' '
# '
+ # 4 0 ' !5 R
+ , !
'2 , ( ( 5 ' ! '
' 5 ! ' / ( ?
' 0 P ' 0 2'
2 ' # ! 4
( ( # 6 . % )" > 5
' 6 @ :<<=H S+ :<<=H :<<:>
E :<<L ' 5 # JJ +- '2
E $ 2' 6'9$+ =C<! $+ F GHHIJ 2'
KKK > J +- ' (- E 7 / P
P E $ 4 :J JL9
:<<J J9 GGG 0 J= . :<<G 6C &
( ? ( E $8 . H 2' KKK >
* # 5 ' ' / ( /
( ? + N / 2 ( 5
0 5 ' ' .
'
Resumo
* 3 ' / + # 5 '
, ' '2 '2 #
+ 7 5 ! / 5 & '
'2 # + ' ,
! 2 (- ' (
' / (- O ' #
/
* 0 , ( ( (- !
! / 4 ( ( !
! 8 H ' 5 ' ' H ' 5 ' 3
# '
(-( ( ! ' ! 8 +
' ! 79I<
# & 2 /
( ( # ' * +
+ 0 '
(-! ! '2 '2
! ( # !
' ! O 0 '
, (- 7 / 3 ' ! /
N ( ' ( 0 , (
(-' '2 '2 # + 4
2' " & / # 0 0 ,
( (- ! ' ! 5 '
6 ' ' ' ' ' ' ' , '
' > * 0 ' ' ! (
# ! &/ E , ( 0
P 2 / 2, ' # < 9 "
'2 , 0 '
7 3 ' 5 +
'
5 , ' '2 0 N 5 ' ,
( (- ' ' 5 '
' / 3 ' 2 , ( 2'
3 ? ( ,
3 & ' ( 2' 3
' !' E , ( ,
' ! '2
5 ( '2 + 8 0 (
' 0 ( +
/ , ( 5 (
(- ! ! H , '2 5 ( + !
+! ( ,
(- ( # ' '2 5
( + ! + , '2 5
'2 # +
3 ' 2 + / , ,
! / 5 & ' 2 2
'2 ,
, 0 * ! / 5 &
' + 2' N
2 ' E ' ( 0
0 / ' '2 #
' 5 ( E ( !
' ' ( 2 2
' N ' ( ' ( ( 5 '
/ 5 7 ' , '
N 2 ' J; ,
0 ' 2 ( !
! 5 0 , ( , ' '
' , ' + (
2 ' ' 5=
E 2 ( # /
, 0 2' N # ' '0 (
(- ! ( + +
'
= . ( ' ( 0 , (
(-! / 5 & '
'2 '2 # +
: . ' 5 ' (- !
' ' 5 ' ' N
'2 ' O
(-! !
J . ( ' ( #
' / ( 4 '2 5
'2 + 8 ( + !
9 . (- O ' /
0 6, ' , ' >
N 2 ' E 0 # 0
( ! ! , O
(-Abstract
+ / + F @ F F + '
+ D + , D + ' D +
D ' + F @ / + / /
+ 5 ' + '
+ / + F / + /5
+ D '
+ + / / 4 / 5
D8 D + H + /+ 5 ' DH F 5 ' ' DH
F + F F + /+ /5 +
F ' D8 D + /
+ + ' + D + 79I<
D D + + + D ' + D
/ D + + / / + +
F @ F + + / 5 5 ' ' D +
+ / F+ + + + '
+ / / + D + D ' + + @
+ D + '
, + ' + / + F @ + + ,
' + ' ' + +
D 7+ /D + D + + +
, + ' 6 ' ' '
' ' ' ' , ' ' > + + F
D + / / + /
+ D ' + , +
+ /+ , + / +D / < 9 " D , D
D ' / D + 5 ' 5 '
' D ' F ' / F + +
' D F ' + /+ D + 5 ' ' D + /
+ + / / / + + /+ 5 '
+ + + F + / / F /+ + D 3 D
+ ' $ + '
3 +
+ 5 D + ' + '
+ + + @ ' D + / + F @ F
// + + D ' ' + 5 +
+ /+ ' ' + @ '
5 D 5 F + +
+ + / / + 5
+ D ' 5 +
T+ D + + 5 / F +
D + 5 ' + 5 /
D + D + ' F + + /+5 D
+ $ F ' + + '
+ D + 5 +
' D ' ' +
' /5 F5 ' + F + + /
F ' / + F + + +
F @ + + + F + + ' + /+5 D
+ ' J; + ? ' + +
+ ' + ' F + + /+
, D + /+5 D + + /+ , D + F
' + ' F + ' D +
D ' D + 5=
+ + + + +
+ / / ' + + F @
+ @ F / D4
= . ' / / + + , 5
' + + ' D
+ D '
: D / 5 ' ' D ' +
+ /+ ' D F ' D + ' D +
J . / + + / / '
/ 4 + ' 5 D + '
D 8
9 / /5 ' D ' 6, '
, ' > + /+ D + J D
/5 / + + / /
Índices
Conteúdos
Lista de Abreviaturas 1
Introdução geral 3
Os fármacos anti-retrovirais e o ciclo de replicação viral 3
A terapêutica anti-retroviral 4
A monitorização terapêutica de fármacos anti-retrovirais 6 Ciclo geral do medicamento e factores implicados na variabilidade farmacocinética 7 Curvas concentração vs. tempo – parâmetros farmacocinéticos 12
Características farmacológicas do efavirenz 14
Critérios para a monitorização terapêutica de fármacos e aplicabilidade ao efavirenz 17 Limitações da aplicabilidade da monitorização terapêutica de fármacos 24 Potenciais cenários da aplicabilidade da monitorização terapêutica ao efavirenz 27
Objectivos 29
Objectivos geral 29
Objectivos específicos 29
Capítulo 1 30
Desenvolvimento, optimização e validação de métodos para a quantificação de fármacos anti-retrovirais
1.1 Introdução 30
1.2 Enquadramento e Objectivos 31
1.3 Métodos e Resultados 31
1.4. Discussão 35
1.5. Conclusão 38
Capítulo 2 39
Estudo da variabilidade inter-individual das concentrações plasmáticas de efavirenz
2.1 Introdução 39
2.2 Enquadramento e Objectivos 39
2.3 Métodos 40
2.4 Resultados 40
2.5 Discussão 48
2.6 Conclusão 54
Capítulo 3 55
Estudo da variabilidade intra-individual das concentrações plasmáticas de efavirenz
3.1 Introdução 55
3.3 Métodos 56
3.4 Resultados 57
3.5 Discussão 60
3.6 Conclusão 64
Capítulo 4 65
Concentrações de efavirenz em indivíduos co-infectados pelos VHB/C sem alteração da função hepática
4.1 Introdução 65
4.2 Enquadramento e Objectivos 67
4.3 Métodos 67
4.4 Resultados 68
4.5 Discussão 71
4.6 Conclusão 73
Capítulo 5 74
Estudo da alteração dos níveis de HDL-c ao longo de 36 meses em doentes medicados com efavirenz
5.1 Introdução 74
5.2. Enquadramento e Objectivos 77
5.3 Métodos 78
5.4 Resultados 78
5.5 Discussão 85
5.6 Conclusão 91
Capítulo 6 92
Actividade PON-1 em indivíduos medicados com efavirenz
6.1 Introdução 92
6.2 Enquadramento e Objectivos 93
6.3 Métodos 93
6.4 Resultados 95
6.5 Discussão 97
6.6 Conclusão 100
Considerações finais 101
Referências bibliográficas 103
Figuras
Figura 1 Ciclo biológico do vírus da imunodeficiência humana e possíveis locais de acção para os fármacos
anti-retrovirais. 3
'
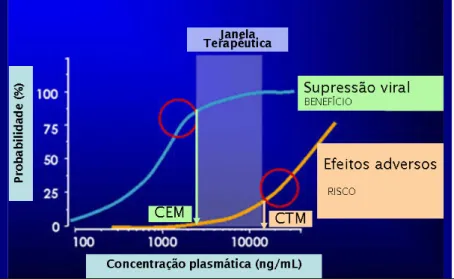
Figura 3 Conceito de janela terapêutica. 7
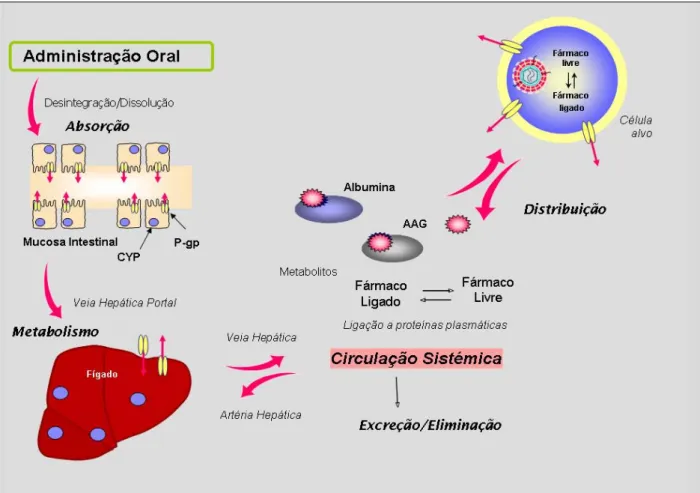
Figura 4 Esquema ilustrativo do percurso dos anti-retrovirais de administração oral no organismo e principais factores responsáveis pela variabilidade nas concentrações de fármaco disponíveis na célula alvo.
8
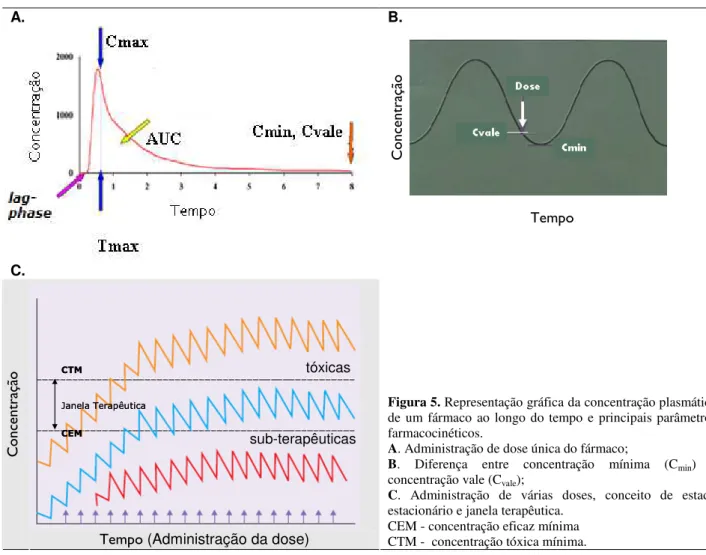
Figura 5 Representação gráfica da concentração plasmática de um fármaco ao longo do tempo e principais parâmetros
farmacocinéticos. 12
Figura 6 Cromatograma-tipo obtido a partir de soluções padrão para a quantificação de anti-retrovirais.
33
Figura 7 Resultados anuais da avaliação externa da qualidade.
34
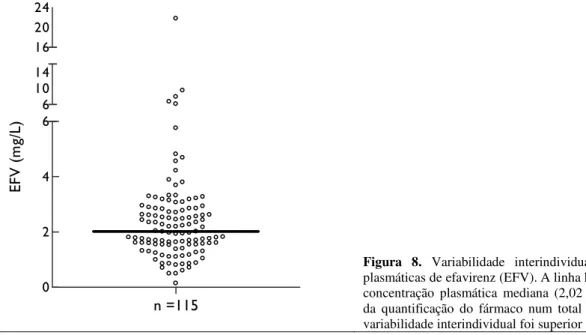
Figura 8 Variabilidade inter-individual das concentrações plasmáticas de efavirenz. 41
Figura 9 Concentrações plasmáticas de efavirenz quantificadas em amostras obtidas entre as 8 e 16 horas pós toma do
fármaco. 42
Figura 10 Concentrações plasmáticas de efavirenz quantificadas em homens e mulheres. 42
Figura 11 Concentrações plasmáticas de efavirenz em amostras obtidas entre as 8 e 16 horas pós toma de efavirenz sem
ou com ingestão de alimentos. 42
Figura 12 Concentrações plasmáticas de efavirenz quantificadas em indivíduos sem e com experiência anti-retroviral
prévia. 43
Figura 13 Concentrações plasmáticas de efavirenz em amostras obtidas entre as 8 e 16 horas pós toma de efavirenz em
indivíduos Caucasianos ou Negros. 43
Figura 14 Efeito da duração do tratamento com efavirenz nas concentrações do fármaco. 43
Figura 15 Efeito da idade dos indivíduos nas concentrações plasmáticas de efavirenz. 44
Figura 16 Efeito do peso dos indivíduos nas concentrações de efavirenz. 44
Figura 17 Variabilidade inter-individual nas concentrações de efavirenz – influência dos fármacos anti-retrovirais
concomitantes. 46
'
Figura 19 Variabilidade intra-individual nas concentrações plasmáticas de efavirenz. 59
Figura 20 Influência do índice de massa corporal na concentração plasmática de efavirenz. 60
Figura 21 Concentrações plasmáticas de efavirenz ao longo do tempo, em indivíduos mono-infectados pelo vírus da imunodeficiência humana e em indivíduos co-infectados pelos vírus da hepatite B e/ou C.
70
Figura 22 Efeito da infecção pelo vírus da imunodeficiência humana no transporte reverso de colesterol.
75
Figura 23 Frequência de indivíduos com valores recomendados, pelo NECP (National Cholesterol Education Program, 2001), de colesterol, total e associado as lipoproteínas de baixa e elevada densidade, e de triglicéridos.
80
Figura 24 Variação nos valores de colesterol, total e associado às lipoproteínas de elevada e de baixa densidade, e os valores de triglicéridos ao longo do tempo de terapêutica anti-retroviral com efavirenz.
81
Figura 25 Efeito ao longo do tempo da terapêutica anti-retroviral com efavirenz no colesterol associado às lipoproteínas de alta densidade médio e estratificado por valor basal. 81
Figura 26 Dependência do valor basal observada na variação dos valores de colesterol associado às lipoproteínas de elevada densidade aos 12 meses de terapêutica com efavirenz. 82
Figura 27 Correlação entre variação dos valores de lipoproteínas de elevada densidade (HDL-c) e do índice aterogénico
colesterol total:HDL-c 83
Figura 28 Correlação entre as concentrações plasmáticas de efavirenz e as alterações nos valores de colesterol associado às lipoproteínas de alta densidade. 84
'
Tabelas
Tabela 1 Resumo dos resultados obtidos em diferentes ensaios clínicos relativos à percentagem de indivíduos cujo primeiro esquema terapêutico incluiu Efavirenz (EFV) e que apresentaram carga viral < 50 cópias/mL num
determinado período do tratamento. =I
Tabela 2 Resumo de estudos aleatorizados que visaram avaliar o benefício da monitorização terapêutica de fármacos
anti-retrovirais que incluiram efavirenz :I
Tabela 3 Resumo das características das diferentes metodologias desenvolvidas para a quantificação das
concentrações plasmáticas de fármacos anti-retrovirais. J:
Tabela 4 Combinações de retrovirais que em adição ao efavirenz constituíram o esquema terapêutico
anti-retroviral dos indivíduos incluídos. 99
Tabela 5 Comparação da frequência de concentrações tóxicas e sub-terapêuticas classificadas com base nos diferentes valores propostos na literatura para a concentração eficaz mínima e concentração tóxica mínima.
9;
Tabela 6 Comparação da variabilidade inter-individual encontrada entre diferentes grupos de indivíduos e frequência de concentrações tóxicas e sub-terapêuticas de efavirenz. 9G
Tabela 7 Características dos doentes e coeficientes de variação observados durante 3 anos no índice de massa corporal e tempo entre a toma de efavirenz e a colheita da amostra. IG
Tabela 8 Comparação entre os resultados obtidos em cada ano do estudo: concentração de efavirenz, variabilidade intra e inter-individual e percentagem de concentrações tóxicas e sub-terapêuticas.
IM
Tabela 9 Resumo dos principais trabalhos publicados que descrevem concentrações e efavirenz na co-infecção e suas
principais conclusões. ;;
Tabela 10 Marcadores bioquímicos utilizados na avaliação da função hepática. ;G
Tabela 11 Associação entre o aumento da razão AST:ALT e o progresso no desenvolvimento de insuficiência hepática.
;G
Tabela 12
Comparação entre os marcadores de integridade do hepatócito e colestase entre o co-infectado pelo vírus da hepatite B e/ou C e o grupo mono-infectado pelo vírus da imunodeficiência humana no início do estudo e após dois anos de terapêutica com efavirenz. L<
Tabela 13 Alterações no valor de colesterol associado às lipoproteínas de elevada densidade em indivíduos medicados com efavirenz como primeiro esquema anti-retroviral ou como substituição de inibidores de protease.
LL
Tabela 14
Comparação entre variáveis demográficas e clínicas entre os grupos de indivíduos, sem tratamento e tratados com efavirenz.
M;
Tabela 15
Comparação a actividade da Paraoxonase (PON-1) e razão activitidade PON-1:HDL-c entre indivíduos sem tratamento e tratados com efavirenz.
=
Lista de Abreviaturas
U
!
"
#
$
#
%
&
'
(
)
*
+,
-'
'
./
0
%1
2.
+,
(
2 #
#
3
.
+,
45
5
+,
5
+,
/
/
+
+,
+,
6#
&
(
#718
7
2
/
9
2$
2
(
2
$
2
γ
:
%
:9
;
:
/9
/
>>
!"
#$
9
;
5
#
?
4
.9%
"
"
$
% /
,
4
% /
4
/
#
!9
@
# #
#
#9
$
"
#/
/
#>
$
3
#!
#
5
%
%
&9
9
,
&2.
2
,
3
&
"
&
&
& #
%
"
&%
%
&A
& <
BC
9$
9.
.
( +,
=
3
5
<
3
+,
5
:
D
:
D
/:
=
D
-J
Introdução geral
Os fármacos anti-retrovirais e o ciclo de replicação viral
* '2 '2 # + 6E $>
, & ! 5 ' 6 CE> *
( E $ ' CE 6 / => ,
( , 4 ' 5
, ! / & 6?C > & 6 ' . > 5 &
6??C > 5 67 > / % , ' 5
/ / 5 CI 6 ' ' T @
:<<LH @ :<<GH :<<GH $ :<<G>
( E $ 0 .9Q ' 6 ? >
Figura 1. Ciclo biológico do vírus da imunodeficiência humana (VIH) e possíveis locais de acção para os diferentes fármacos anti-retrovirais (ARV). Os fármacos ARV actualmente disponíveis inibem a actividade dos enzimas transcriptase reversa, protease, integrase e os passos de fusão e entrada inibindo, consequentemente, o ciclo de replicação viral. As células infectadas pelo VIH são células CD4
+
9
/ & / / O ' 2/
A terapêutica anti-retroviral
# 5 ' ' ! 6$ C 5 " " A # " A>
( ! # CE 6 @
:<<GH :<<GH $ :<<G> N $ C
( ( 2' ! C? ' 6 / ' >
2 , ( 0 2' 6 I< & C?
E $8 " 9<< & C? E $8 "> ? # 5 '
E $ , ' 0 ' ' ( ' 6 +
:<<<> ( 0 6 ' 7
:<<J>4 # / - '2 5
& ( 6 0 ? 2 > ( / '
! ( ' & 0 .9Q & , 3
E $ / 2
# & / & '
. , ( 0 2' 3 ' # 5 '
2' / + , ' '2 ,
' 6 / ' I< & C? E $8 ">
3 ( ! 2' ! 2'
3 ' 0 ' ' #
' 8 ! (- # ,
( 2 E $ '
( 2 / & 6"D> .9Q / '
6 @ :<<GH $ :<<GH
:<<G> 2 (- #
'2 3 2 0 , ' ' / !
' , CE , + /
, + ( 8 2 0 !'
, ( 3 (
/ ( # (- ! /
I
, $ C + 0 ,
'2 0 2 ?C 3 ??C
7 ' 6C E> 6 @ :<<GH :<<GH $
:<<G> ? P ( 7 C E 0 #
&
' 2 $ C / ' / "D .9Q
# 6 :<<G> # / '
N , ( ' 0 ,
= /=< 6=< ' > & , $ C / ' 2'
! !' 6/ I< & 8 "> N :9 6$
:<<G> ' / ' / ' '
' / 6 J 9 > ' (- '
# ' &/
' / ' & '
/ !' 6 & >
6 # ' &/ >
* 2' / ' ( ' , ' (- N
$ C 0 ' !' 4 ( ' 9<< & 8 " ( 9
' 0 # 6 :<<G> *
=I< & 8 " 6B + :<<M> I<
& 8 " 6 @ :<<G> '2 # +! ;
( E $ N
# 7 5 , #
P ' / #
( , &
(-* 0 / , ' ,
# ' ' ' '2 #
# / , ! 6 @ :<<=>
, ' '
0 67S> CE N # (
# (- ! 6 . > / '
;
A monitorização terapêutica de fármacos anti-retrovirais
? ( / / 5 ' ' / &/
. 7 5 , ,
CE ( . + , '
( E E ( + ' '
2 , ( / / ,
A monitorização terapêutica de um fármaco (TDM) é uma estratégia multidisciplinar, baseada em medições repetidas das suas
concentrações associadas a uma resposta farmacodinâmica, que visa a optimização da resposta à terapêutica e fornecer, a um clínico,
informação para um tratamento individualizado (Back e col, 2002; Ivanovic e col, 2008).
( 6 ( > ! ! 8 0
2 / * / , (
6 ( > 0 O 67.> V ( 7.
( ! ! # 6 / :>
( '0 3
' ( (- & 7 , !
# P 0 ! , ( 2 6 E 5
( 3 > 3 N ( &
2 6 5 ( , / & > 6 / J> 6 @
:<<:> * ' (- N + ! 8 , 0
E , (- & 0
3 #
Figura 2. Curvas concentração–resposta (adaptado de Back e col, 2002). A análise de curvas concentração-resposta permite a definição de um intervalo de concentrações óptimas.
EC50 Concentração que permite uma resposta
máxima em 50% dos indivíduos.
TC50 Concentração responsável por reacções
L
* / N 7. 0 7S % / " 6 ! > Q
D 6 ' > % , ' / ! '
! / E O 5
/ ( ( ( 6 >
( ! 6 / 9> E ,
' O 7S
Ciclo geral do medicamento e factores implicados na variabilidade farmacocinética
' ' ! ' /
' ' ' 2/ ( 0
6 / 9> 5 ( ! * ! ,
& ( 0 6 (
! 79I< 5 W7> ' P (
6 / 2 57 % 75/7>
. ! 2/ ( '
& / 2/ 0 ' ? 2/ !'
( ( (
, ! , / ( 0 E (
/ ! , 0 ' / (
0 / '0 / 2/ 0
/
G
V / ( / 2 ! ' 2 '
/ / ( 0 ( ! 0
/ / ( &
N # 3 6 + 5 !
! > ! / 2 6 N ! >
? U=5/ 2 ! 6 > O
5 ( ! / N 2 , 2 ' 2' (
' ' , ( / 0 ' '
(- / , 2
0 / ' ?
/ ' ( / & (
( ( 3 / # ' !
/ 0 / , 2 ( / 8 ' (
! . ' + ! 2
7 0 (- ! ' 6 ' / >
Figura 4. Esquema ilustrativo do percurso dos anti-retrovirais (ARV) de administração oral no organismo e principais factores responsáveis pela variabilidade nas concentrações de fármaco disponíveis na célula alvo. Após a toma da dose prescrita é atingida uma determinada concentração do fármaco no plasma que depende principalmente do efeito de primeira passagem. Uma vez no plasma, o ARV circula associado a proteínas como albumina e a α1-glicoproteína ácida (AAG). O fármaco é posteriormente distribuído pelos diferentes tecidos. No local de acção farmacológica, o ARV (onde a sua acção vai depender do transporte do fármaco livre para, e no, interior da célula e, nos NRTI, também da activação intracelular) vai permitir a inibição da replicação viral, o que se traduz num decréscimo das cargas virais plasmáticas e um aumento no número de células CD4
+
M
* ! ' ' 2 #
& / / * (
/ 5
( +! / ! / 0
/ 2 / ( 2 !
&/ , 4 / 0 / ' !' N /
! / ( ( # /
! 0
( ' (
! / ? ( ! ( ,
( , 2 5, 2
&/ ' 5 4 /
! ' ' ( 7
( 8 ' ( / '
( 7 5 , ' '
, ! , , ' '
! '
(-! E # /
( ' ' & / ,
#
/ ' 3 #
( ' 2 0
6 ! 0 > 0 !
' ! % (
! 5 & ( 2
! ( / ( 6 , > *
! & 5
? ( ! !
' ( % (
! ' 5 ! / (
2 ' (
! % ( 5 '
(- ' ' ( ( ( /
6 (- > ' N ( 3 / /
6 (- > ' ( !
' ' (- ( ( + & 3 / ( * W7 0 2
! ' ' ( O E
+
=<
( 6 ' ' T / @ :<<G> ? $
/ =G 2 9: 5 2 IM / ' E
2 = 9 M<X (- !
W7J 9 6I<X> / W7:.; 6J<X> 6 '
' T / @ :<<G> C ' N + !
W7 J 9 O , ' 69<X P ' >.
* CE 0 W7 CE 5
!' (
! 6 ' ' T :<<L> ? !
0 C E * 2 ( C E 0 (
! , & , 0
(- ! '
/ ' / ( &/ C E 7 0 P
, / ( ! (
8 P ! # ( 6 D
@ :<<=> E ( / / ( +
E ( C E (
/ 7 +! (- , ' ' ( 3
2 7 ' /
(- ! / 5 * C E 0 W7J 9
( ( ' ( ' 6 > 6 /
I > ( ' 7S C E4
/ ( + ! 6 @ :<<:> C 0
& C E W7:.; C E + &
! & W7= : W7: ; W7: M W7: =M
!' / 3 / ( (- ,
==
7 2 $) & 6 > 6 " >
( ( ( !
. 2 + 0 75/7 2 $) &
6 > 0 5= : = 6 .C5=>
/ 2/ + 5 ! /
& 6B :<<= >
( / CE
(-( 0 ' ( ! '
6B :<<= H :<<9> W7 0
5 ' 6 Y :<<:H + :<<JH T
:<<L> 75/7 0 '2 '
'2 6 :<<9>
E & 5 ' ' 2' (- CE
'O .
E ( ( ( 0 / ,
! / 4 5 ( 2 ! (
2 ! / / !
! 0 * (
! / ( ( 5 ,
' ! / , 3
(
. 3 N ' (- /
! / ! / 0 6C / :<<;H D "
:<<L> &/ # + ! 6 D :<<;H
:<<G> ( 8 ( E $ 5 (- 6" =MMJH :<<<H
C :<<9H 7 ' :<<L> ' !' &/ (
(- ! + + H ( 50
6 3 :<<9H + @ :<<9H C / :<<;H C+
:<<G> E (- !
, 6 ' T :<<LH
=:
Curvas concentração vs. tempo – parâmetros farmacocinéticos
( ! ! , / 0
' + N / I * 6 # " > 2 '
! ( ( !
0 ( ! ?
! ! ? , '
' 2 3 / 0 /
( ! 6 > , 0 +
! 6 > 6 / I > ' 2
' ( ! ( ! (
' ( 0 ! , ' ( 5 2
! 7 0 ! , 0
( ! 6 2 5
( > / 0 ( (
( ( !
A. B.
+,
C.
tóxicas
sub-terapêuticas
B #
B #
+,
(Administração da dose)
Figura 5. Representação gráfica da concentração plasmática de um fármaco ao longo do tempo e principais parâmetros farmacocinéticos.
A. Administração de dose única do fármaco;
B. Diferença entre concentração mínima (Cmin) e
concentração vale (Cvale);
C. Administração de várias doses, conceito de estado estacionário e janela terapêutica.
=J
( ! / 0 / , !
! ( 0
N ( 6 0 ( > *
O 7S , 0 5' 6 =8:> ! *
=8: ! I<X ! /
? ' / N / & 0 /
( ' 6 ' > , ( 2 6 > 6 / I >4
0 ( ! ' / ' 0
( ! /
E ' / # ( ' ,
( & /
' / & . ' ! ( 0
! + ' ' / ' ,
, ' ' 0 ' ,
0 ! + P , ' , 3
! ' ( ! ' 6 >
( ! ' / & P
(- 7S / (
* 7S 0 + & ( P &
( P 6 / I > & (
! , 0 / , ( ! 0 '
( / 5 , 0 / ! ,
& =8: O 5 ' !
, + . ' 2
=8: '2 , & ( &
( 7 ! 3 0 '
' , +! ( ( ! , 2 *
0
' '2 !' ' + ! *
' ( , ( 6$ =MMM E
=MMM> O . CE 6" 7
:<<;H B + :<<M> . ' !
' 2 ! ' !
3 ' ( ! ! E
=9
Características farmacológicas do efavirenz
* ' 6E E> ' 5E $5= E $5: C '
E $5= CE
E 0 2 ' ' 6 + ? 3 :<<L>
/ I<X '2
6$ :<<;> ? ' &/ E E +
6 :<<JH :<<9>
E ( ! ?C E E 0 CE ( , $ C
+ , + ??C 6 @ :<<GH :<<GH $
:<<G> ? / , E E
+ 6 :<<GH B + :<<M>
, $ C + E E '!
2 E , $ C E E ,
6 // :<<JH . B :<<9H :<<9H ' " + :<<9 H / H :<<9H D :<<IH @ :<<;H :<<GH C
:<<G> ? = 5 ' (
, '2 E E ( / /
'2 , # / ' Z I< &
05 6 9G > 6 =>
'2 ??C ! 6T / :<<I>
/ 0 E E 0 3! , P ( / ,
' E $5= # 2
S=<J? 0 6 @ ? =MMGH + :<<<> * #
E E 0 CE ' 6?E7> 6 # 5 >
6 :<<:> 0 + (- ,
# ?C P (- #
=I
Tabela 1. Resumo dos resultados obtidos em diferentes ensaios clínicos relativos à percentagem de indivíduos cujo primeiro esquema terapêutico incluiu Efavirenz (EFV) e que apresentaram carga viral < 50 cópias/mL num determinado período do tratamento.
@ #
E F
/
G18 4 B EHF
? 97I
E 3 B F
: %
C7 7J K8 11 2$ I I '9
9 L M
C887
C1 7J NO C8O 2$ I I
D M
C887 788 7J K8 N8 2$ I I 7
. ? M
C881 J7 7J NN JJ 2$ I I
CNJ N8 KN 1 2$ I /I$
& M
C8879
CJ1 N8 17 C8 2$ I /I 7
% M
C88J2 C18 ON JO C 8 2$ IC % /
COO 77 NJ CN 2$ I I 9$
M
C887$
8 77 N CJ 2$ I I 7
C7 77 N7 CK 2$ I'9 B
M C88J
C77 77 KN C 2$ I$ B 9$
P M
C88N: JC OC J1 8 2$ I'9 B
3TC: Lamivudina. ABV: abacavir. d4T: estavudina. ddI: didanosina. HAART: esquema antiretroviral. FCT emtricitabina. NRTI: análogo nucleósido inibidor da transcriptase reversa. TDF: tenofovir. ZDV: zidovudina. 1 Resultado de análise intent-to-treat.
Falência virológica: A: 6% no grupo ABV e 4% no grupo ZDV; B: 15,7%;. C: 10%; D: falência virológica: 4% no grupo FCT e 12% no grupo d4T. E: 24%; F: 16% no grupo TDF e 16% no grupo ZDV G: 6% no grupo ZDV/3TC e 3% FCT/TDF e H: 26%.
* E E 0 CE (- ' ? ' 6 / :<<;>
(- E + 8
! / & E
5 & 6 =<X ' ' !'
> ( / # ( +
/ ' (- 6= =<X '2 > 6 @ ? =MMGH
=;
:<<M> . , '! + &
+ 5 , 3 '2
E !' 9 =<X ( CE
6 // :<<L> / 6 0
:<<IH [ 5 :<<M> E : 9
( ! 0 5 '!
'! ,
'2 6" + :<<JH 0 :<<IH // :<<LH [ 5 :<<M>
* (- ' , 5 6 =<X '2 > "
O ! (- 2 2 ' (
6 :<<<H S . + :<<JH 5 :<<JH B D
:<<9H S + :<<IH ? :<<IH C ' :<<L>
( E E / !' 0 6. :<<:H @
:<<GH :<<GH $ :<<G>
( P ! 6*.> ;<< /
, ! ! ; =< /
! 6 + :<<=> E ' ! !' E E 6
9 = /8"> ! 0 J I + & ' 0
= G /8" IG = /8" + ' 6 @ ? =MMG>
E E /
( '
* E E / N 2 + 6\MMX> N *
! 0 2 6 + =MMMH D :<<=>
( ! 5 ( 6
:<<I> , ( ! 0 ( 5
* =8: ! ! '2 !' 0 I: L; + & P 9<
II + & ( / 5 ' 5 ( 6 +
:<<=> ? =8: ! '2 E $Q
6 3@ :<<J>
* ! 0 2/
=L
+ ' ' 6 =MMMH + :<<=> ,
/ 3 / *
=X ! 6 =MMMH + :<<=>
, 3 '2 (
* E E 0 ' W7: M W7: =M W7J 9 ? 0
' 0 ' 5 (
' W7J 9 6 + :<<=> E 0
6 // :<<L> ( !
2/ 6$ :<<9> 6 D :<<:> , #
& (- 7S
/ ' 2 ' 6 ' ' :<<I>
. , E E 0 75/7 6 Y :<<:H
:<<IH . :<<;> E &
+ , # / ,
N # E E * 0 J9JI
/ & ( 67 5
/ S :<<9> ' (- 6?
:<<JH T :<<I> / & ' +
E E 6 D :<<: $ :<<J>
2' ! 6 D :<<:> ?
, ( ! 0
& 2
0 E E 5/7 0 ' 4
6 :<<I> 6 + :<<J T :<<G>
6 + :<<L>
Critérios para a monitorização terapêutica de fármacos e aplicabilidade ao
Efavirenz
* 0 , 3 . ! N ( #
' ( ? ( 5 0
5 / , 2 ' O .
=G
1. Relação PK/PD A concentração do fármaco (PK) está associada com o seu efeito (PD) que pode
ser eficácia ou toxicidade.
7 ! CE 0 + 3 , ( ( !
! , ' E , ( !
! ' 6 ' ' " 7 :<<;>
E ( #
5 / ' ' # (
! ( '2 K # A ,
# 0 ( 4
'2 0 # ! ! N
# ! !
(- &
* E $ E E 0 ( 2'
! 5 # = /8" 6 :<<=> E
( ! CE P # /
=J< '2 + G :< + & ! '
: =G & 2 E E ::;
( + / , :JI
'2 L=M + 2 :G 6 3@
:<<J> : '2 G<< E E / *. ;<<
/ *. ' 6 ]9<< & 8 "> / ;LX '2
* ' # ( ( ! / '
6 ^< <<J ^< =9> ' E :<<=
" / 6:<<:> (- ! E E JJ
'2 # CE 6 J , $ C > J
? / , ( E E + G :< +
& ( ! ! '2 , '
' 6 / ' _:< & 8 "> 6L:X> : =;G /8" * / ,
P ( = /8" ' # #
=M
* ' P # ' = =
/8" 6E " + :<<;>
' ;G '2 699 + 0 9<`M >
' / ( (- ! E E 2 6 a+
:<<9> + =< :9 + & E E * '2
' : / 5 4 0 / ' bI<
& 8 " 5 ( L c 8" 6: : /8"> E E
( ! 6 _< <I> 6J< 9I '2 +
(- : : /8"> 6=< =J '2 +
(- : : /8"> * / ' : : /8" E
! C , 6:<<9> '
9G '2 , , $ C ?E7 ?E7
2 E E , : ?C / '
(- ! E E 6 + =: + &
! > J / ? 5/ JI '2
/ 2 , GJX ' (- ,
# ??C * , 3 ' #
/ 6, / ' = /=< / ' I< & 8 ">
9JX '2 H ' , # (- ( !
! 6J ; /8"> 6 ^< <:L> 6: L
/8"> E '2 ' (- , #
??C , # '2
(-E (-E J /8" 6LIX> ' , ,
(-J /8" 6::X> E ,
O ( ! (
(-, # E E / 0
( ! E E ' (
(-2' ? ' 6 :<<=H ?P[
:<<=H 3@ :<<JH / :<<9H $ :<<9H a+ :<<9H :<<IH P :<<IH 0 :<<IH S + :<<IH + :<<;H & :<<LH @ + + :<<L>
:<59<X '2 E E ! 2'
? 2' ! ' 6 9 < /8"> ! 6
:<
+ 3@ 6:<<J> ?
, , ( (- ! !
' (- = 9 /8" 3 # E E
/ / :<<= 6 :<<=>
0 ?P[ 6:<<=> '2 E E ,
' P 2' ? (- ! !
? / '2 ' ( 0 E E 69 M /8"> , #
' ( b J I /8" 6GLX> '2
E E 6 0 J L /8" 9LX
( bJ I /8"> * / , (- bJ I /8"
' ' 2' ?
? / / 6:<<9> / & =J =G '2
E E +! =: ? / ( !
! 69 J`: M /8"> =: + & N
'2 6: L`< L /8"> * 2 , 3 E E
' ( ! 9 < /8"
P N (
6:<<I> 2 / :9
, ;X '2 E E &/ (
( ( E E E ( '
6 ^< <9>
P 6:<<I> , # , !
( (- ! E E , , (
N 2 0
6:<<I> / 6=G > '2 / ' I<
& 8 " '2 =L , 2
( ! =< '2 ,
(-, ! 6I =<`: =I /8"> 6 ^< <:I> ,
6: LM`= J= /8"> * 2 , '2 (- E E '
# ' 2' ? / 5 /
( ' . P '2 ,
'
'0 6 3@ :<<JH a+ :<<9H P :<<IH S +
:<<IH & :<<L> ' 5 , / 5
+ + 3 ' 6 ! :<<IH
(-:=
'2 (- ! E E '
(-6:<<L> / ?
' '2 (- ! E E
; /8" ' + ' ?
( E / / (
/ 0 7S87.4 '2 , (
W7: ; ' (- ! E E '
(-& 2' ?
(-* :?? ;I ' :<<< B + :<<=
3 ' ! / ( , ?E7 E E
' 6 9 > Q ' 6J > 6S + :<<IH ' " + :<<;>
? ( ( E E ! ?
A janela terapêutica do fármaco deve estar definida e ser um intervalo estreito, ou seja, deve
existir uma diferença pequena entre a CEM e CTM.
? ( . ( '2 0 '
' # 63 # > 3 # !
/ '2 ( ( & &
! ' '
(-' 6:<<=>
(- ! E E /
' ! , 2
' ( % ! ( 5 3 # =59
/8" '0 , ' E
0 3 #
(-. CE 6S + :<<9H " 7 :<<;>
E! ' , ' + O . ??C 7
, # ' 5 # 6=:5J<X> 6 :<<JH
:<<JH & :<<LH C :<<L> ? & 6:<<L>
/ , J;X
L;X 3 !' 6 :<<J>
E '2 / ' !' ' 5 #
::
E . ( & N ( ??C
:9X 6. / :<<9> J;X 6C & :<<9> + ( '
, # (- CE 3 # ' :;X 6. /
:<<9> J:X 6 & :<<L> ??C 69GX> , 7 6=9X> 6 & :<<L>
3. A variabilidade interindividual nas concentrações do fármaco deve ser maior que a janela
terapêutica.
# / ' (- ! (
'2 & ( ! ! /
( . CE 6 @ :<<:> ( !
, '2 CE ' =< '
6 @ :<<:H :<<JH & :<<LH ' ' :<<G> . ,
' (- '2 '
' # 0 ( '2
' ' (- E E ,
/ 3 ( 6 2 :>
4. Variabilidade intra-individual nas concentrações do fármaco: se a concentração de um fármaco
no mesmo indivíduo varia sem motivo aparente, torna-se pouco exequível o ajuste da dose com
base numa única medição, pelo que, para um fármaco em estado estacionário, se espera que a
variação intra-individual nas concentrações seja baixa.
' 5 ' ' ' '
(-6 ! ! ! >
(-! - ( + P !
7 / ! CE
/ ' (- +
7S ' / 6 @ :<<:> ' 5 '
(- ! 0 7 699 9GX S+ :<<;H ?
:<<;> , ??C 6:IX S+ :<<;H ? :<<;>
* ' 5 ' (- E E 3
:J
5. Não existem outros parâmetros clínicos ou laboratoriais de quantificação mais simples que
permitam o acesso ao efeito.
( ( 0 2 2 ( 2 , #
N $ C ( ? , N !
# / ' / "D .9Q /
# 4 2 (- ( / '
P "D .9Q /
2 ( , / &
' &/ &/ * '2 $ C '
/ ' / "D .9Q ' / E
(- , 4 ' , #
( ! d
. ' ( &
/ / '2 N # 3
( 5& ' & 3 0 ! '
? ( 0 ' ( 7
, 6 # > 3 '
* / ' / "D .9Q
/ / ( !
0 / ' 6" /
:<<J> ? / '2 (- 5&
, # , # 6" /
:<<J> E & , / /
( # 3
(-! E ' ( 0 P E (
' ' # ( #
' ' '
(- &
6. Possibilidade de intervenção: a capacidade de intervir em casos de concentração insuficiente ou
excessiva é essencial.
* E E 5 ! I< / :<< / ;<< /
:9
7. Métodos analíticos para a quantificação das concentrações de ARV por técnicas standard e
na matriz desejada, rápidos e sem custos excessivos são necessários para a realização da TDM.
A qualidade dos resultados obtidos por estes métodos deverá ser assegurada por um programa de
Avaliação Externa da Qualidade realizado por entidades reconhecidas e acreditadas.
* 2 = ( ' ' ' ( 0
, ( ( ! CE
Limitações da aplicabilidade da monitorização terapêutica ao Efavirenz
. E E + 3 / 2 6 /
:<<;H W :<<;H :<<GH B + :<<M> /
' (- 'O ,
* ?C &5 ! 4 (
' ?C 0 ( (- !
! &
! N ' ( ' (
N 0 E
(-(- ! 6 / :<<:> , O , (
P / / 2 6 +
:<<<> * 2 . (- ?C /
'! 0 ( 2'
6 + :<<<> ( ( E E N
# / , ( P ,
$ C +
! 0 ( / , # * !
2' ( / ( N 2 !
" # $ % $
& $ E + #
(-& * P '2 E E 2 0
+ + 3 ' ' 2 . E E
* (- #
:I
7 @ =MM=> E ( , '2
(- '2 3
(- ' (- '
7 ' '2 2
/ (- '
? + + 3 ' ' 2 .
N # E E4 , 2 '2
CE 6 :> - !
3 CE 2 * P '2 E E 0
(- ' O 7S ' !' 6 :>
Tabela 2. Resumo de estudos aleatorizados que visaram avaliar o benefício da monitorização terapêutica (TDM) de fármacos anti-retrovirais e que incluíram Efavirenz (EFV).
Q
25 =
Q
2$ I 9.
2.
2$ E B F
.
2$ E B F
# " #>
M C887
7 & 7 M N
C D
4 2$ E CF
M C881
C 8 & N CMC 2
>D M C88N
CC , 1 MC 7
D 7 D
4 R
4 ,
+, N D
M
C88K OO , 7 CM 2
M C 7
:;
E 2 + '
2 . CE N # E :<<:
:<<L '! 2 4 $ 6 / :<<JH D :<<I> (
6 ' /+ :<<:H :<<9> E 0 6 + :<<:H
:<<L> ! 6 :<<I>
? N '2
+ 0 ( (- ! ( 3
# O 7S
3 # O 7S
( # CE . ' @ :<<J E
7S87. '2
' * ( 3 # '2 # CE
0' + 3
E , ' 2 . N #
6 ' /+ :<<:H :<<9> 3
( . 6W :<<;> 2 2
' ' ( =:
' 0 2 ' N #
2 / / 2 ' &/ ?
0 '2 ' . 2 =:
, . 2 , 3!
' ( ! 2
* ' !' . 6 + :<<:H / :<<J>
'2 $ C ' 7 ' 6 .E>
' 6? E> , , 2 C E &
# CE 0 ' ( , , ' (
+ . , / ,
2 S+ 6:<<;> P =<<< '2 !
2 2 . E P
' J<X '2 (- 3!' ,
( 0 =<<X '2 , 2 N
( 3 0 LIX
2 N (- ' ( . 0
( * / # 6S+ :<<;> 5
:L
? 6 :<<L> (- /
2 L;X JIX 6 ' /+ :<<:H
:<<9H :<<IH S+ :<<;> E P '2 ,
(- 5& N ( ! '
(- ' N !
' ! . 2
( ( . CE
E # 2 .
'0 ( (- (
(-' 6 :<<LH / :<<LH S :<<LH C
:<<L> * E + '2
, (- 3 # E E
7 ' '2 '
(- 3!' 6 :<<L>
Potenciais cenários de aplicabilidade da monitorização terapêutica de
fármacos ao Efavirenz
, - ( 2 . E E 5 /
( ( 0 / (- 4
' $ E (
. ! ( 6' $ / :<<;H C :<<L> 0 5/
'2 ( + ! 5 ( !
6S :<<L> * '2 ( + ! + ! '
' 2 2 0 +
E E '2 7 =8J '2 E $
' 5 '2 + 6E$ > ( '2 0
( + ! ( + ! (- '
' ' ! 6 D :<<;> , '
' ' , ' ( E
! 2 I (
$ ( ) ($ '2 ' N # ,
! ,
:G
# (- / 2
+ & , ! C , 6:<<9>
, ( ( CE 0
, ' ! 0 ' (- 5&
E E 0 W7: ; J 9
& 6 @ ? =MMGH + :<<=H T :<<J> E
;<X (- ! 6T /
@ :<<G> , (- / ' 6
:<<IH T :<<L> / (- '
! ( 6 ' ' :<<G>
(- 6? :<<J> *
(-' (-' / 5 & ' +
'2 ( / ! ( , 6B
:<<;>
! $ * ,
$ C ' ' ' (- ! ,
, ' '2
# 6 :<<:> 5 ' ( #
' 2 # (- 5 # 0
, N ! 0 ( ' /
( ' /
'2 ! . 0 '
N # ' ( ! ( 6$ /
:<<:> ? . ' / 0 + ,
( / , !
'2 , ' (
! N # /
67 @ :<<G> (- !
7S ' 0 , ' (
:M
Objectivos
Objectivo geral
* 3 ' / + N # 5
' , ' '2 E $ 7 5
??C E E , ! 2
(- ' ( ' /
(- O E E # /
Objectivos específicos
= ( ' ( 0 , ( (- 7 ??C
'2 E $ ' N (
: 7 ' ( # E E /
/ '2 ' / , ' 5 '
(- ! E E ! ' , 3
' ( 3 # !
J E (- O E E / E $
' ( (- ! !
J<
Capítulo 1
Desenvolvimento, optimização e validação de métodos para a
quantificação de fármacos anti-retrovirais
1.1 Introdução
( 7S CE . !
' ' N 5 ! * ' , (
(- ! 2 P
(- + D 6=MMM>4
$ # )" A <+;#L F " ; : A ?
L , & #
5 I<J / ;: '
-$ E " 4 ;9< =M< / '
? ( / ' 0 , 3 . ! CE
# E E E / 5 2 4 0 !
0 2' ' ,
, , ' (
* 0 ' , ( O ! , E E E
'2 # # 0' '
' (- , / : 7 = 7 Q = ??C
, $ C , "7E8C E Q E E 7
' ( (- 7 7 Q??C 5 ,
P $7" / (- 0
! ! ' . P
(- ! 2' 0
, (- ! 7 ??C &
J=
( / ?C , ' ( (
' 5E $ 5 (
, ( 0 ' ' 0 2' .
1.2 Enquadramento e Objectivos
E 2 ( / ' ' '
, ( (- 7 ??C '2 E $
0 ' N ' / ( 2
, 7S , . , ' '0
, ' ( & , '
, !
1.3 Métodos e Resultados
* + 2 ' ' 0
, ( (- ! CE / 2, '
# 6$7" >4 => , ( E EH :> , ( ?E7 J> , ( 7 4 ' 6 7E> .E C E "7E , ' 6 VE> ? E ?
:<<I ' ' 0 , , ( 7 ??C
N ' 7 ' 6 e> M !
P 2
J ( ! ( /
O / ! / , O
( ' ' ' " & /
E / 6 2 : ;>
. 0
, ' ( '2 , ;< f + *
- ( ' ! !'
(- D ( ! E 0
' / 0 '
(- 6 + + =MM=> ? / ;
/ 5 ! 0
/ ;
J:
Tabela 3. Resumo das características das diferentes metodologias desenvolvidas no presente trabalho para a quantificação das
concentrações plasmáticas de fármacos anti-retrovirais.
$
#
E
F
# 3
$
4
9
+,
E
F
E
F
2$ 8MC1 # +, E F 2 +,E C 88HM 78 Q F
+,
C S 7 1 D
J 9 , C157 # 1 T / M1 B
>:C#!718 . :
KM1 18S18 E B F
C7N 8 # /9 % !# &A $ 8M7 25 +, < <
E : F
ED 5 F
2 +,
E C 88HM 78 Q F
+,
C S 7 D
J 9 , 185 MO # 1 T M8 B
>:C#!7C1 . :
NMK
C 8 CJ
#
8MC
# +,
E* 4 M1HF
+,
C S C
D J 9 , 185 MO # 1 T / M8 B
>:C#!7C1 . :
NM8 C8SJ8 E B F
CJC K # 2$ # /9 ' % !# &A $ 8M7 25 +, < <
E : F
ED 5 F
2 +,
E C 88HM 78 Q F
+,
C S 7 D
J 9 , 185 MO # 1 T M8 B
>:C#!7C1 . :
NM7 C 8 7J
JJ
A
A
B
B
C
C
J9
/ ' ( 6 / L>
+ 6SS > / /
+ + & A M A ( )" <+;
+ , :<<= =L & / I< &
B + :<<G ? / L " &
/ ' ( , SS :<<:
E E :<<I e :<<J ! * 3 '
/ , ( CE
( 0 5 2 , ( !
( & 7 J
( + ! (
( 0 ( '
/ E 5 5
' ( 0 ? / L 0 2' '
' 0 , ( , ( O M CE
:<<I
C88 C88C C88 C887 C881 C88N C88K C88J
78 N8 J8 88 C8 78 N8 A H 5 ,
C88 C88C C88 C887 C881 C88N C88K C88J
78 N8 J8 88 C8 78 N8 B
C88 C88C C88 C887 C881 C88N C88K C88J
78 N8 J8 88 C8 78 N8 C
C88 C88C C88 C887 C881 C88N C88K C88J
78 N8 J8 88 C8 78 N8 D H 5 ,
C88 C88C C88 C887 C881 C88N C88K C88J
78 N8 J8 88 C8 78 N8 E
C88 C88C C88 C887 C881 C88N C88K C88J
78 N8 J8 88 C8 78 N8 F
C88 C88C C88 C887 C881 C88N C88K C88J
78 N8 J8 88 C8 78 N8 G H 5 ,
C88 C88C C88 C887 C881 C88N C88K C88J
78 N8 J8 88 C8 78 N8 H
C88 C88C C88 C887 C881 C88N C88K C88J
78 N8 J8 88 C8 78 N8 I
Figura 7. Resultados anuais da avaliação externa da qualidade desde de 2002: Cada barra de erro representa a média e o erro padrão da média relativa a 6 concentrações-teste de cada fármaco quantificadas na avaliação anual. A linha a tracejado representa 100% de exactidão e as linhas a cheio definem o intervalo considerado válido pela entidade avaliadora KKGT (80 a 120%). A.
JI
1.4 Discussão
? / , (- '
(- CE ? & / ' ' ' 0
+$ , - 5 : ??C L 7 %
$7" # . * ! 2 , , !
2' ' ( , E 0 /
! . !
05 , . 0 ' ' '
/ * 0 ! $
0 1 2 '2 E 0 ( O &
$% $ ' 0 , ( '
* 0 ' ' N ' ' /
/ $7" 2'
& + 6 + ( O ' > ?
P 0 I< & /
/ & ,
(-/ ! , ( !
, ( , CE ' E
0 ' 3 3! , $% ! $ !
'2 , ! 7
. , !' N :: f
, ' ' /
! ( 6 / ;.> (
( ! / 5 ,
( ( E ( (
/ / !5 /
! , ,
* '2 E $ ' '
' ( , ;< f
0 ' ( '2 6 ' ' :<<= >
/ # , / ( '
-N (- ' ( N '2
* 05 0 ' ' ' 2 4 '
J;
( ( ' /O E
, # ( 0 (
+ ' * 2 ' / + 0
2 &' 3 ( $7" ' / + 0 !
/ (
( 6:=< > , , # ( '
( / 0 ! ( 4
, ( ! 0
' ( / $ '
0 . ! &
, &' 0 !' *
0 ' / , ( /
' + $7" ' /
( E ' / '
(
N '! 5:< f
'! G< f 7 J
/ ( 8 / ( / '
(- D !' '!
' / ( $7" !
0 ( . CE4 '
' ' !'
, ( , / / , * , ,
' 0 / ' / 0 ' ,
, 2
( 0 / ' / 2'
(
? , ' / 0 0 ,
/ ( 7 ' (
& " D 2' +
( ) ! ! (
0 '
' , ' ( 0 /
2' 3 +
' 0 ! '! ' ( + ,
JL
0 ( ' ' /
, # (
( ' !
0 ( 05 3 2 05
+ O , 2
/
0 :<<9 : 0 2' , , '
$7" P CE + ( ! ; 7 :
??C ? , ( " A , 2 +
2' 6 :<<:H :<<:> 3 0
' ( e + , (
O , 3! / ' e / :<<I 67 :<<I> E 0
' ( ' / ,
G 6 ' ? E> 05 %
' / ' /O N !
/ ! ' / 5
( ! ;< ' < I "
. / , 0 ' ( '
& /# 0 ( 0
(- 6 + + =MM=>
' ( 0 6 ' 5 0 '
, ( 5 (
(- > 3 (
7 , ' 0 0 ,
' / ' ( , 5
/ , , (- , 'O
' ( ' (
( ( 0 '0 !
/ ' ( , E
- 2 SS &
? :f / :<<= = =L & + J
(- 6 :<<= > ? Jf
/ J :L & 6. :<<:> ? P ' ( B + :<<G
I; & I= E E4 :G
, $7" ( ' 0 0 '
ML =<9X ' :J :G:X
JG
1.5. Conclusão
? + ' ' ' 0 , , ( :
??C L 7 . 7S E , ( 0
P 2 < 9 " '2 ,
JM
Capítulo 2
Estudo da variabilidade interindividual das concentrações
plasmáticas de efavirenz
2.1 Introdução
' ' ' 0 5 ! E E 3 ' / +
' ' (- ! CE
' (- ! '2 0 , /
'2 (
? ' ( 0 ' 6 ' '
:<<G> 7 ! 3 #
'2 / (- #
. ( * 3 ' '
(-! ' , 3 # '2
(- 5& & ? 3 '
! . (
(- 3 # !
E ' !' , ' '
(- ! CE , + / N
# 5 ( 7S '2 N #
(-2.2 Enquadramento e Objectivos
E 0 8 , ( . E E
3 ' + 2 '
(- ! E E '2 ( 2' ,
9<
2.3 Métodos
& ( 2 '2
E $ / # $ " 6. >
/ 0 4 '2 , $ C , 2 E E
;<< / *. 3 # + 2 +! #
N # ' '0 , ! !'
+ E (- '2 2
? / / 4 ( # E EH +
P E E + + / H E E + +
/ H ( '2 H ,
# $ C # 5 ' 0' ( E E
, / 0 2
7 ' ' ( E E /8" c 8" J =L
7 ! / , " g
' 9 6, " K + ($ ' $> ( /
(- ' !' / ' '
_< <I ' ' ' ( 6 E>
/ 6X>
2.4 Resultados
! "
E ==I '2 (- ! E E ' < =9
/8" := G9 /8" ( / G * ' (
! 6 ' 5, > : <: 6= I95: GI> /8" E '
==I '2 MJX ' ' 6:= G9 /8">
;JX 6 / G>
# ! $ ! !
! "
* / '2 + ' G =;
+ & E E 6 > (- !
9=
'2 2 6 ^GG> '
( / ' (- E E + 6 : =M /8">
:; + 6= G: /8"> 6 / =<>
* '2 , + E E ( 6 ^9= = L; /8">
(- , / E E 6 ^LJ : :J
/8"> 6 / ==> (- + '2 $ C
' 6 ^II : =L /8"> # # 6 ^9I : <= /8"> 6 / =:>
V (- ! '2 6 ^M;
= ML /8"> ? / 6 ^=G : =I /8"> ( / '
N ( 6 / =J> ? ' 2 ! 6:= G9 /8">
, + ( ? /
( # E E ' = =<G 6 6 VC> =J 695:G>
> '2 ( E E (
! 6 / =9>
* '2 2 + =G ;L 6 JM 6JJ59G> > *
# '2 (- ! E E
' ( ' 6 / =I> E ( ' 5 /
'2 , /
6 ^;I ^< J:<L ^< <<M:>
* '2 ' 9< =<I @/ 6;J 6II5LI> S/> , ,
( '2 ( E E 6 / =;>
U
1
8 C 7 N N 8 7 N C8 C7
2
$
E
B
F
9:
K
J
O
8
C
7
1
N
K
8-8
C-1
1-8
K-1
8-8
4
2$ EDF
2
$
E
B
F
Figura 9. Concentrações plasmáticas de efavirenz (EFV) quantificadas em amostras obtidas entre as 8 e 16 horas pós toma do fármaco.
: . D
8-8 C-1 1-8 K-1 8-8
2
$
E
B
F
Figura 10. Concentrações plasmáticas de efavirenz (EFV) quantificadas em homens (n=88) e mulheres (n=26). As concentrações não diferem entre homens e mulheres.
8-8 C-1 1-8 K-1 8-8
2
$
E
B
F
9J
25 = 3
8-8 C-1 1-8 K-1 8-8
2
$
E
B
F
Figura 12. As concentrações plasmáticas de efavirenz (EFV) quantificadas em indivíduos sem (controlo, n=55) e com experiência anti-retroviral prévia (n=45)não foram significativamente diferentes.
8-8
C-1
1-8
K-1
8-8
2
$
E
B
F
Figura 13. Concentrações plasmáticas de efavirenz (EFV) em amostras obtidas em indivíduos Caucasianos (n=96) ou de Negros (n=18).
8 C1 18 K1 88
8-8 C-1 1-8 K-1 8-8
U 8M87
& U 8MC ON
2$ E
F
2
$
E
B
F
99
K
CK
K
7K
1K
NK
8-8
C-1
1-8
K-1
8-8
U 8M8 CO
&
U 8MC C1
/
E
F
2
$
E
B
F
Figura 15. Efeito da idade dos indivíduos nas concentrações plasmáticas (n=102) de efavirenz (EFV).
1
71
11
N1
K1
J1
O1
81
1
8-8
C-1
1-8
K-1
8-8
#
E> F
2
$
E
B
F
Figura 16. Efeito do peso dos indivíduos (n=92) nas concentrações de efavirenz (EFV).
? 9 5 ! CE , 3 E E 2
, $ C '2 ( e ' 6 e > J
' 6 9> J ! '2 6' / =L>
? # ! CE (- E E
, ' ( '
% & '
* ' (- ! E E +
3 # 6 I>
E ' = < J < /8" 6 I hE E 6 /8">i> , #
'2 (- 5 # + 6' 9
h 6X> '2 i> ' E ' == G<X
7 ( 6' I>
9I
Tabela 4. Combinações de anti-retrovirais que em associação ao efavirenz constituíram o esquema terapêutico HAART dos indivíduos incluídos (n = 102).
+,
Abacavir + Emtricitabina = < 1
Abacavir + Didanosina + Lamivudina + Lopinavir/r = < 1
Abacavir + Didanosina + Estavudina = < 1
Abacavir + Didanosina+ Lopinavir/r = < 1
Abacavir + Atazanavir/r = < 1
Abacavir + Estavudina = < 1
Abacavir + Lamivudina ; 6
Abacavir + Lamivudina + Zidovudina = < 1
Abacavir + Lamivudina + Indinavir/r = < 1
Abacavir + Tenofovir = < 1
Abacavir + Tenofovir + Lopinavir/r = < 1
Abacavir + Indinavir/r = < 1
Abacavir + Amprenavir/r = 9
Didanosina + Estavudina = < 1
Didanosina + Lamivudina M < 1
Didanosina + Tenofovir : 2
Didanosina + Tenofovir + Lopinavir/r = < 1
Emtricitabina + Tenofovir =M 18
Emtricitabina + Tenofovir + Amprenavir/r = < 1
Emtricitabina + Estavudina + Tenofovir + Amprenavir/r = < 1
Estavudina+ Tenofovir + Lopinavir/r = < 1
Estavudina + Tenofovir = < 1
Estavudina + Lamivudina J 3
Estavudina+ Indinavir/r : 2
Lamivudina + Tenofovir ; 6
Lamivudina + Zidovudina J: 30
Lamivudina + Zidovudina + Tenofovir : 2
Tenofovir + Lopinavir/r = < 1
Tenofovir+ Lopinavir/r + Saquinavir = < 1
Lopinavir/r + Saquinavir = < 1
9;
Tabela 5. Comparação da frequência de concentrações tóxicas e sub-terapêuticas classificadas com base nos diferentes valores propostos na literatura para a concentração eficaz mínima (CEM) e concentração tóxica mínima (CTM).
R =
2$
E B F EHF
. ( M C88 M8 E F
D M C88N M N E 7F
& VD M C887 CMC NC E17F
2.
$ < = +W =
# M C88N M8 J8 EJ8F
. ( M C88 7M8 8 EOF
.
$ < =
+W 45 @X ( M C88 M1 E F
Salvo excepções indicadas, o número total de indivíduos incluídos foi 115. Para o cálculo foram consideradas apenas as amostras colhidas entre as 8 e as 12 horas pós toma (n=101).
7 / ' 9$ # $ /9 % #
8-8 C-1 1-8 K-1 8-8
2
$
E
B
F
9L
# ! $ !
7 # ' ' ' O
(- / 5 *
? ; 5 ' '
(-5/ , # (- & 5 #
' !' 3 # (- !
' ' 6' O > / CE
E E , $ C 4 9<X e "7E8 H I<X
' 6 E> 9 , C E & &A ;<X
6 > J 6 > + / L<X . 6 ^< <<:>
+ M =: + & 5 E E GIX P
V ' /
5 (- & 5 # 6 ;>
' + N / 6 ;> E
+ 6 ^;I> , (- 6 ^< <=;9
#C" A> '2 9< 6 ^J: E ;GX = LI
/8" ;LX (- : : /8" JX (- 9 <
/8"> ' '2 6 ^JJ E ;<X
: 9G /8" J;X (- : : /8" =IX (- 9 <
/8"> 6 / =G>
G 78 ≥78
8-8 C-1 1-8 K-1 8-8
Y
/ E F
2
$
E
B
F
9G
Tabela 6. Comparação da variabilidade interindividual encontrada entre diferentes grupos de indivíduos e frequência de concentrações tóxicas (superiores a 4 mg/L) e sub-terapêuticas (inferiores a 2,2 mg/L) de efavirenz (EFV).
& 2$
E B F EHF
+W =
EHF
+W 45
EHF
#
O K MKJ KC 8 E1OF E F
8 C7 CM N NO E7NF C E F
C CM 1 71 8 E7KF ECF
: D
C N MK1 N7 C E1OF E1F
: JJ CM O N7 71 E1 F K E F
& 5
. D CN MJ1 18 K EN1F C E7F
8M87
E " F
, KC CMC 1N N E18F 1 EOF
2$ I
% +, & 7 MKN KN CN EN F 7 E1F
, 11 CM K 1N CO E1JF N E F
25 =
% # 3 & 71 CM8 NO CN E1JF EKF
& ON MOK N7 1 E11F J EJF
, J CM 1 7 O E77F ENF
8M817
E " F
ZN8 > J CM88 7J C E11F C E1F
N K8 > C7 CM 7 11 E7NF C EJF
#
[K8 > CMCK 11 1E7JF E 8F
ARV: anti-retroviral. n: número de indvíduos ns: não significativo. CV: coeficiente de variação.
2.5 Discussão
' ' ' (- ! E E
# '2 (- ! 3 # ,
( . ! 4 , E E ;<< /
*. / '2 2 :<X
(-' ( ' ' #
(- 5& !
9M
' ' 2 * / 3 #
/ 0 9 ' N E ,
! ! $ 3- & $ ) 4
($
' E
' ' ' (- ! 0
' , , , , 3 ( E ,
'2 (- & 5 #
E E ' ( ! ? !
, ( 0 , ' ' 6E =MMM>
+ ' (
0 2' . ( ' !
(- ' 2' ? E E 0 , (
3 N , (- ' !
E N ( ' :9 + /
' ' ,
' ( (- ! O 7S '
E ( ! O !
, - ' 4 ( / (
-( 3 # ? O
6' " + :<<;> + ' =:
+ 6 + G :< + & H :<<=> =9 + 6=<
:9 + & H a+ :<<9> =; + 6 & :<<L> :< + 6 9
+ & Y+ H :<<G> / :9 + ' (
6 / :<<;>
. / ' E 4 = < /8"
+ G :< + & :<<=>H = = /8" 6' " + :<<;>H : : /8" + =< :9 + & 6 a+
:<<9> ( :<<; . CE + " 7
, (- =: + & ( E E '
5 J /8"
? + 5 ' ! 6
( > 2 # ' !' '
' GIX + ' 9 + 6M 6 M> =:
6 =:> + & > ' ' M =< == =:
I<
( ? ' ! +
0
* ' ' ' E 6X>
==I 0 ' 6==GX
:<<=H IIX 3@ :<<JH G9X a+ :<<9>
? ! (- , ' ( . ' 5 ,
' 5 (- .
N ( ( ' &/ 5
& , , ' (
! ' 7 , +! (
'2 2 , '2
? + + ! P
'2 N ! E (
! 0 (
(-' N , P (- 5 # ' ,
, ! ' ( . . ,
(- + 6
:<<JH & :<<L> 0 (- 0
P (- &
!. $ . ($
3- ! * ( #
( ! / , ,
# + (- , O
(- # , '2 , + + N
# (- &
* + / / '
'2 (- ! ! !. $ 4 !
$ 5
3-# 6 2 6 >
/ 2 > ( (- ! E E !
6"& 5 0 :<<:H 3@
I=
. # N ( ? / (- E E 6$
:<<9 / :<<;> ? + ' := JG /8"
+ ( ? / E ' ,
J (- E E , ' :<
/8"
? 2 E E /
! ? / ' +
' + 6 :<<:> ? N (
( 0 ' / ! ,
P '2 ' ( ( E E
/ 7 6:<<J> $ 6:<<9> S + 6:<<I> / / 0
' / ( / 0 E E 0 !
( ! 2 / / 6 ' ' S /
:<<G> * / B , D 6:<<:> /
' , ' ' / 0 CE E E 0
' ' !
' ' ,
( !
* ' ' E E W7: ;
'O W7J 9 6T :<<J> *
# & ! 6 D
" :<<L> , # (
O W7: ; (
;X P + ! W7 + ' '
/ P ! ' W7J 9 W7:.;
? ( ' 7S E E
2 / 0 W7: ;
$ 3 =<< A " 6 ?7> W7 : ;
( ?7 P /
+ 6e / :<<L ' ' T / @ :<<G>
* W7 : ;j= 0 K # A 5 (- 0 8 4
$ O 6ILX> 6I< IIX> ! 6J< L<X> 69<X> 5 6J< 9IX> 6 + D :<<9H S :<<IH C / :<<L >
I:
* W7 : ;j9 6 ?7 LGI \ > 0 4 $ O 6=9X> ! 6 G X>
6 9 X> ( ( ? / 6 + D
:<<9 S :<<I C / :<<L > 0 E E
K # A 4 JL = c/ +8 " 6C / :<<L >
* W7 : ;jI 6=9IM \ > 5 , # =:X
5 $ O ! 6 + D :<<9H $ :<<IH
S :<<IH C / :<<L >H 2' 2 6" /
:<<=H " :<<J> 0 E E '2 '
99 M I: I c/ +8 " 6$ :<<IH C / :<<L >
' (- / # '
' (- E E 6 / :<<;>
* I=; \ W7 : ;j; 6I=; \ LGI \ > W7
: ;jL 6=9IM \ LLL \ I=; \ > 6$ :<<9 :<<IH
+ D :<<9H C 2/ 5?&' :<<IH S :<<IH C / :<<I :<<L H / :<<L> C 2/ 5?&' 6:<<I>
=<< '2 , # / &
( E E4 K # A 6I:X = L= /8"> 69JX : ; /8"> 6IX
J IL /8"> / C / 6:<<I> '
(-! / & (
(-+ : J ' ,
$ 6:<<9 :<<I> ( E E 2'
? E ( ' :9
, 3 6J =<
> * ' (
(-( I=; W7: ; , ' , # '2 ( ? /
6:<X> , 6JX>4 (- E E , K # A
6 ^< <J;> E ! # #
0 / "D .9Q * 2 , ( !
E E (- I=;
V I=; , 0 (
(- ( 6$ :<<9> + ( '
+
* : ;j:; 9MM \ 3 # 6 / :<<L>
O ( : ;j;
I=; 0 + , '2 + /& I=;
IJ
* W7: ; MGJ \ ( ? /
6S :<<IH C / :<<L H TD :<<G> 0
(- E E
* W7 : ;j=; j=G j:L j:G j:M * !
' ! GIX
( E E 6C / :<<L > * : ;j:L j:G '2
? / 6< ;X , # > j:M P
E / E E (- ! 5 ! 5/ ( 7S
. W7: ; 0 6C / :<<L >
E ( E E ' ' W7 '
? / ' ' !
/ 0 CE ( / 0 2 /
! 2 E ' 7S ,
( .
. ' / 6:<<;> ' ( (- !
! 6 + > N ( 6 ? / > /
, '2 6 +
, + > /
( ! ' ? ! '
( (- E E , /
( ' + 5 + = :9 + &
# + +
(- E E / + # ' 5 ,
+ (- ;<X '
, + ( ' (- '
/ 2
' ( .
, 3 . P (- &
(- 5 #
+ , '
(-! / (
' !' O . ' (
'2 , 5/ / ' !'
( (- 6 # '2
> ' 0 / ' ? + /
I9
5 # (- ! CE ?
( ' (- 0 5
/ ! * ' 9< ' W7 9<
3! =;X 6 =MML>
' ' (- ! !
+ '
( ( ' +
, 3 # (- ' =<
? + , ' 4 0
+ + / . $
! 4$ %
k + , /
' !' + ' ' ( , '2 !
( / ! ' N (
# # / ( ,
' 5 , 0/ !
(-! E E
2.6 Conclusão
? + ' !' ( & ' (
(-! E E 2' 3 ' !'
, ' ( ( ! '2 3 ,
3 # ' ' (- ! E E
II
Capítulo 3
Estudo da variabilidade intra-individual das concentrações
plasmáticas de efavirenz
3.1 Introdução
? 2 5 , ' ' '
(- ! E E , (- & 5
# / '2 * 3 ' E E .
( ' 5 ' '
/ , , ( P ( ! '
' 3 3 7 (- P
( ! '! 2' ! 2
' , ' 5 ' / &
' ( ' &/ ( 6 / :<<9> 5 , '
5 ' ' ! / & # #
? # N ' 5 '
(-! E E , ' J<X '
. ! 6 :<<=H 3@ :<<JH a+
:<<9H 0 :<<IH ? :<<;> E ' ' 5
' + 3 +
' ( ! . 4
(-! '2 ' #
# # / 5
3.2 Enquadramento e Objectivos
* ' 5 ' 0 0 8 , (
. ! ? + 5 ' 5 '
(- ! E E / 5 + (
I;
' (- ! E E '2 /
' E E + /
3.3 Métodos
* 2 + '2 E $Q ,
$ C E E # 7 ,
'0 , !
!' + * '2
/ J; + ( ' N (- ! E E
/ ' / "D .9Q J`= 3
E E 6;<< / *.> * P J 9 (- + , 0
! P 2 J , (- ' ( ,
' 5 ' / 7 , 0
' ( 6 / '
"D .9Q> ! (- '2 $
(- E E '2 , N
+ + G =; + & E E
6' 2 :> . ! N $ C
2
* ( N ' 5 ' 0
4 + E E + / 5 (
'2 + 6E$ > 8 E$ 9< 5 ( ' (
'2 , / / ' I< & 8 " &
# , & ( / ' !' 2
!' : - ' # #
' (- ! 0 ` ' 6 .>
0 6 ' > ' (- ! E
6X> V ' I<X 5
6 ' , > * 2
/ 4 ( / '2 6' X
' ( > ! ' O 6 ?*E > & 5
(- P 5 (