UNIVERSIDADE FEDERAL DO CEARÁ CENTRO DE TECNOLOGIA
DEPARTAMENTO DE ENGENHARIA METALÚRGICA E DE MATERIAIS MESTRADO EM ENGENHARIA E CIÊNCIA DE MATERIAIS
NATÁLIA DANTAS GOMES DE SOUZA
OBTENÇÃO DE NANOBIOCOMPÓSITOS MAGNÉTICOS CONSTITUÍDOS DE GALACTOMANANA, GLICEROL E FERRITA DE NÍQUEL E ZINCO
NATÁLIA DANTAS GOMES DE SOUZA
OBTENÇÃO DE NANOBIOCOMPÓSITOS MAGNÉTICOS CONSTITUÍDOS DE GALACTOMANANA, GLICEROL E FERRITA DE NÍQUEL E ZINCO
Dissertação de mestrado apresentada ao Programa de Pós-Graduação em Engenharia e Ciências de Materiais, da Universidade Federal do Ceará, como requisito parcial para obtenção do título de mestre em Engenharia e Ciências de Materiais. Área de concentração: propriedades físicas e mecânicas dos materiais.
Orientador: Prof. Dr. Pierre Basílio Almeida Fechine.
NATÁLIA DANTAS GOMES DE SOUZA
OBTENÇÃO DE NANOBIOCOMPÓSITOS MAGNÉTICOS CONSTITUÍDOS DE GALACTOMANANA, GLICEROL E FERRITA DE NÍQUEL E ZINCO
Dissertação de Mestrado apresentada ao Programa de Pós-Graduação em Engenharia e Ciências de Materiais, da Universidade Federal do Ceará, como requisito parcial para a obtenção do grau de Mestre.
Aprovada em: ___/___/______.
BANCA EXAMINADORA
______________________________________________________________ Prof. Dr. Pierre Basílio Almeida Fechine (Orientador)
Universidade Federal do Ceará (UFC)
______________________________________________________________
Prof. Dr. Ricardo Emilio Ferreira Quevedo Nogueira
Universidade Federal do Ceará (UFC)
______________________________________________________________
Prof. Dr. Karlo David Alves Saboia
A Deus.
AGRADECIMENTOS
Primeiramente, minha gratidão vai ao único, maravilhoso, conselheiro e príncipe daăpazănossoă“Deus Pai”. A Ele toda honra e toda glória pelo que Ele é e pelo seu cuidado e amor. Nunca me deixou desviar o caminho, me confortando nos momentos difíceis, através do seu Espírito Santo, e me alegrando com suas promessas e benções infinitas.
Aos meus pais, Damião e Mariza, pela vida e por todo amor, carinho, respeito, educação, exemplo, enfim, por existirem em minha vida. Aos meus irmãos Rafael e Kamylla, pelo carinho e amor sempre muito presentes.
Ao meu querido e amado esposo, David Souza, neguinho lindo, amor da minha vida, pai do meu filho, a quem tenho grande orgulho e admiração por tudo que representa em minha vida. Devo a ele minhas maiores e menores conquistas, pois foi e é meu maior incentivador. Agradeço, principalmente, pela vida do Natanael, nosso presente de Deus, que ainda está no meu ventre, te amo meu filho. Aos meus sogros Moacyr e Edna pelo incentivo e oração. A minha vozinha, Laura, que sempre intercede com orações e louvores a Deus por minha vida.
Ao meu querido professor, amigo e orientador Pierre Basílio a quem devo a concretização desse trabalho. Foi um gentleman em todas as horas, sempre com entusiasmo, delicadeza e paciência. Ao Rafael Freire um agradecimento especial, pelo acompanhamento sempre a pronto para me ajudar com muito carinho e dedicação. Um exemplo de aluno, homem, filho, pai e esposo.
RESUMO
Nos últimos anos, um grande interesse na associação de materiais magnéticos e biológicos tem sido relatado na literatura. A obtenção de novos compósitos constituídos de galactomanana (GM), nanopartículas magnéticas (MNPs) de NiZn e glicerol (GL) foram produzidos em diferentes proporções com finalidade de potencializar as características individuais de cada material para futuras aplicações. Sendo assim, as propriedades estruturais, magnéticas e dielétricas dos nanobiocompósitos foram investigadas por Difração de Raios-X (DRX), Espectroscopia de Absorção na Região de Infravermelho (FTIR), Análise Térmica (TG), Calorimetria Exploratória Diferencial (DSC), Microscopia Eletrônica de Varredura (MEV), Microscopia Eletrônica de Transmissão (TEM), Medidas Magnéticas e Medidas Dielétricas. A estrutura de espinélio da ferrita de NiZn foi confirmada por DRX e TEM e a amostra GMGL apesar de ser um material amorfo apresentou em seus nanobiocompósitos picos caracteristicos da fase de NiZn. As bandas características para as amostras foram confirmadas por FTIR. Estas por sua vez seguiram um perfil de degradação de acordo com as quantidades de NiZn incorporados, confirmados nos termogramas de DSC. A caracterização por MEV foi importante para avaliação da morfologia. Os resultados das medidas dielétricas apresentaram baixas perdas dielétricas e das medidas magnéticas mostraram comportamento magnético para todos os nanobiocompósitos. Portanto, os resultados da caracterização dos nanobiocompósitos foram satisfatórios para possíveis aplicações como biomaterias, dispositivos eletrônicos ou em áreas afins.
ABSTRACT
In recent years, a great interest in the association of magnetic and biological materials has been reported in the literature. New composite consisting of galactomannan (GM), magnetic nanoparticles (NPs) of NiZn and glycerol (GL) were produced in different proportions with the purpose of enhancing the individual characteristics of each material for future applications. Thus, the structural, magnetic and dielectric properties of nanobiocomposites were investigated by Absorption Spectroscopy in the Region of Infrared (FTIR), X-Ray Diffraction (XRD), Thermal Analysis (TG), Differential Scanning Calorimetry (DSC), Electron Microscopy (SEM), Transmission Electron Microscopy (TEM), Magnetic Measurements and Dielectric Measurements. The structure of spinel NiZn ferrite was confirmed by XRD and TEM. Sample GMGL despite being an amorphous material presented in their nanobiocomposites characteristic peaks of phase NiZn. The characteristic bands in the samples were confirmed by FTIR. These in turn followed a degradation profile in accordance with the amounts of NiZn incorporated, which was confirmed in the DSC thermograms. The characterization by SEM was important to assess the morphology. The results of dielectric measurements showed low dielectric loss and magnetic measurements showed magnetic behavior for all nanobiocomposites. Therefore, the results of the characterization of nanobiocomposites were satisfactory for potential applications as biomaterials, electronic devices or related areas.
LISTA DE ILUSTRAÇÕES
Figura 1 - Estrutura do monossacarídeo, dissacarídeo/oligossacarídeo e polissacarídeo ... 17
Figura 2 - Estrutura da galactomanana comăunidadesădeămanoseăemăligaçãoăβ-(1-4) e unidades deăgalactoseăemăligaçãoăα-(1-6)...19
Figura 3 - Folha, flores, vagem e sementes de Caesalpinia ferrea.. ...21
Figura 4 - Estrutura do glicerol. ... 22
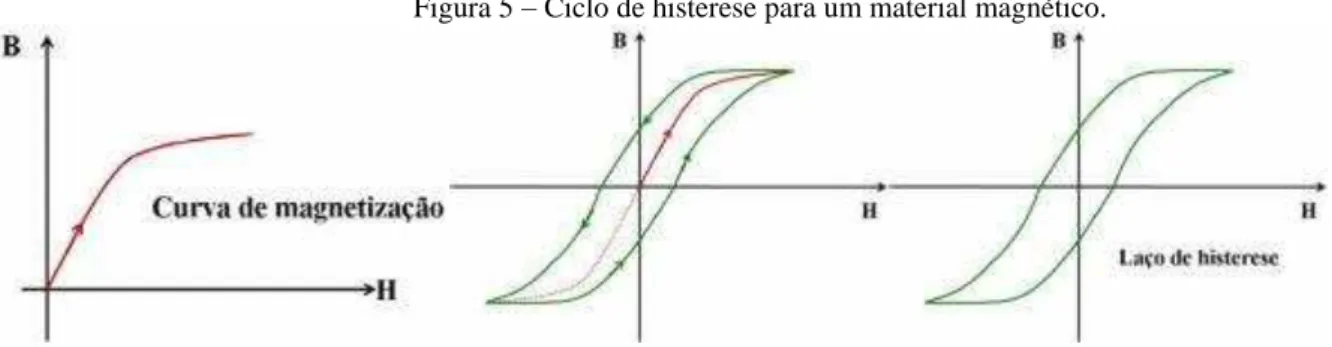
Figura 5 - Ciclo de histerese para um material magnético.. ... 24
Figura 6 - Representação da estrutura de Espinélio (AB2O4)...26
Figura 7 - Bandas de absorção na região do infravermelho de GM...36
Figura 8 - Perfil de degradação da amostra GM. ... 38
Figura 9 - Termograma por DSC da amostra GM. ... 39
Figura 10 - Micrografias da amostra GM com ampliação 120x (a) e 600x (b). ... 40
Figura 11 - DRX da amostra NiZn. ... 41
Figura 12 - Bandas de absorção na região do infravermelho de NiZn.. ... 43
Figura 13 - Curva de magnetização da amostra NiZn. ... 44
Figura 14 - Micrografia da amostra NiZn com ampliação em uma dada região.. ... 45
Figura 15 - Filmes de GMGL nas proporções 90/10, 80/20 e 70/30 com a massa fixa de 0,1g de NiZn. ... 46
Figura 16 - DRX dos nanobiocompósitos 0,06NP, 0.14NP, 0,20NP, GMGL e NiZn...47
Figura 17 - Bandas de absorção na região do infravermelho do NiZn, GMGL e dos nanobiocompósitos. ... 48
Figura 18 - Perfil de degradação das amostras GMGL, NiZn e dos nanobicompósitos. ... 51
Figura 19 - Curvas de DSC da amostra GMGL e dos nanobiocompósitos ... 53
Figura 20 - Micrografias das amostras GMGL (a), 0,06NP (b), 0,14NP (c) e 0,20NP (d) ... 55
Figura 21 - Curvas de magnetização das amostras NiZn, 0,06NP, 0,14NP e 0,20NP.. ... 56
LISTA DE TABELAS
Tabela 1- Classificação taxonômica da Caesalpinia ferrea. ... 21 Tabela 2 - Principais vantagens do método hidrotérmico ... 28 Tabela 3 - Valores de massa bem como as proporções em percentual utilizada nos testes de composição para GM e GL ... 32 Tabela 4 - Bandas de absorção na região do infravermelho da amostra GM ... 37 Tabela 5 - Bandas de absorção na região do infravermelho e suas respectivas atribuições ... 49 Tabela 6 - Bandas de absorção na região do infravermelho e suas respectivas atribuições ...50 Tabela 7 - Eventos relativos à degradação das amostras NiZn, 0,20NP, 0,14NP, 0,06NP e GMGL...52
Tabela 8 - Eventos térmicos ocorridos nas curvas de DSC para as amostras GMGL, 0,06NP, 0,14NP e 0,2NP...54
LISTA DE ABREVIATURAS E SIGLAS
CFC Cúbica de Face Centrada
DSC Calorimetria Exploratória Diferencial
FTIR Infravermelho com Transformada de Fourier H Campo magnético externo aplicado
Hc Coercividade GL Glicerol
GM Galactomanana
MET Microscopia Eletrônica de Transmissão MEV Microscopia Eletrônica de Varredura MNPs Nanopartículas magnéticas
Mr Magnetização remanescente Ms Magnetização de Saturação NPs Nanopartículas
TG Termogravimetria
RWP Concordância entre os perfis calculado e observado S Progresso do Refinamento
SUMÁRIO
1. INTRODUÇÃO ... 13
2. OBJETIVOS ... 15
2.1 Objetivo Geral ... 15
2.2 Objetivos Específicos ... 15
3. REVISÃO BIBLIOGRÁFICA ... 16
3.1 Polissacarídeos ... 16
3.1.1 Galactomananas ... 18
3.2 Glicerol ... 22
3.3 Materiais Magnéticos ... 24
3.3.1 Ferritas: estrutura e propriedades ... 26
3.4 Biocompósitos ... 29
4. MATERIAIS E MÉTODOS ... 30
4.1 Materiais e reagentes ... 30
4.2 Extração e purificação das Galactomananas ... 30
4.3 Síntese das nanopartículas magnéticas ... 31
4.4 Síntese dos Nanobiocompósitos ... 32
4.5 Técnicas de caracterização ... 33
4.5.1 Difração de Raios-X ... 33
4.5.2 Espectroscopia na região do Infravermelho ... 33
4.5.3 Análise Térmica... 34
4.5.4 Calorimetria Exploratória Diferencial ... 34
4.5.5 Microscopia Eletrônica de Varredura ... 34
4.5.6 Microscopia Eletrônica de Transmissão ... 34
4.5.7 Medidas dielétricas ... 35
4.5.8 Medidas magnéticas ... 35
5 RESULTADOS E DISCUSSÃO ... 35
5.1 Caracterização da Galactomanana ... 35
5.1.1 Espectroscopia de Absorção na Região do Infravermelho ... 35
5.1.2 Análise Térmica ... 37
5.1.3 Calorimetria Exploratória Diferencial ... 38
5.1.4 Microscopia Eletrônica de Varredura ... 39
5.2.1 Difração de Raios-X ... 40
5.2.2 Espectroscopia Vibracional na Região do Infravermelho ... 42
5.2.3 Medidas Magnéticas ... 44
5.2.4 Microscopia Eletrônica de Transmissão ... 45
5.3 Caracterizações dos nanobiocompósitos ... 46
5.3.1 Características macroscópicas dos filmes ... 46
5.3.2 Difração de Raios-X ... 47
5.3.3 Espectroscopia de Absorção na Região do Infravermelho ... 48
5.3.4 Análise Térmica ... 50
5.3.5 Calorimetria Exploratória Diferencial ... 53
5.3.6 Microscopia Eletrônica de Varredura ... 54
5.3.7 Medidas Magnéticas ... 56
5.3.8 Medidas Dielétricas ... 57
6 CONCLUSÃO ... 61
7 PERSPECTIVAS ... 63
1. INTRODUÇÃO
Estudos envolvendo materiais biológicos e magnéticos têm sido investigados devido suas aplicações em vários segmentos da indústria [1]. Sendo assim, materiais naturais como os polissacáridos, que podem ser encontrados com abundância na natureza em animais, plantas e microrganismos são bastante empregados na obtenção de novos materiais por suas propriedades físico-químicas. Dentre suas vantagens, podemos citar: biodegradabilidade, abundância na natureza, por possuírem ação sinérgica com outros polissacarídeos, além de geralmente serem atóxicos [2].
Os polissacarídeos são gomas naturais encontrados em sua maioria em plantas superiores obtidas de exsudatos de tronco de árvore, atuando como mecanismo de proteção da planta, sementes, frutos, tubérculos, algas ou por fermentação microbiológica. Os polissacarídeos quando em água fria ou quente podem formar dispersões coloidais, ou seja, soluções altamente viscosas ou até mesmo géis, o que apresenta uma alternativa bastante viável em suas aplicações. Na biomedicina, eles são aplicados em engenharia de tecidos, imobilização de enzimas, biossensores, e como veículo de liberação de fármacos etc [3]. Os polissacarídeos também podem formar filmes como, por exemplo, temos a quitosana, galactomananas e carboximetilcelulose vêm sendo usados para fins variados [4-6]. Galactomanana e quitosana são usados na fabricação de filmes finos que tem importantes funções na imobilização de biomoléculas e no desenvolvimento de biossensores [7].
Neste contexto, a busca por novas fontes de galactomananas constitui uma tarefa de grande importância, uma vez que essa goma pode representar uma alternativa barata, renovável e natural de matérias primas para a indústria [8]. Alguns componentes são importantes na formação dos filmes, como os plastificantes, que são substâncias que quando adicionadas a outros materiais, provocam mudanças nas suas propriedades físicas, químicas e mecânicas [9]. Pesquisas revelam que filmes constituídos de galactomanana e glicerol podem ser usados como revestimentos comestíveis em alguns frutos, melhorando sua qualidade de conservação [10].
volume. O uso desses materiais pode proporcionar alta reatividade, diferentes propriedades magnéticas, condutividade, dentre outras [11]. Devido a estas características únicas proporcionadas pelo tamanho reduzido, os mesmos podem ser usados em diversas áreas, como engenharia, medicina, tecnologia da informação etc. Na área da biomedicina, as nanopartículas magnéticas são bastante estudas para aplicações com fins terapêuticos e de diagnóstico [12].
Dentre as nanopartículas magnéticas podemos destacar as ferritas mista de
NiZnFe2O4 que apresentam 50% dos íons Zn2+ substituídos pelos cátions Ni2+ para a formação
2. OBJETIVOS
2.1 Objetivo Geral
O presente trabalho tem como objetivo geral a obtenção de novos nanobiocompósitos magnéticos constituídos de galactomanana, glicerol e ferritas de NiZn e avaliar suas propriedade físico-químicas, magnéticas e dielétricas para possíveis aplicações nas áreas biológicas e tecnológicas.
2.2 Objetivos Específicos
Extrair e purificar a galactomanana das sementes de Caesalpinia ferrea;
Síntese da nanopartícula magnética de Ni0,5Zn0,5Fe2O4 (ferrita de NiZn).
Obtenção dos novos compósitos constituídos de galactomanana, glicerol e ferrita de
NiZn.
Caracterização dos materiais investigados por:
Difração de Raios-X (DRX)
Espectroscopia de Absorção na Região do Infravermelho (FTIR)
Análise Térmica (TG)
Calorimetria Exploratória Diferencial (DSC)
Microscopia Eletrônica de Varredura (MEV)
Microscopia Eletrônica de Transmissão (TEM)
Medidas Magnéticas
3. REVISÃO BIBLIOGRÁFICA
3.1Polissacarídeos
Polissacarídeos são macromoléculas naturais encontradas em todos os organismos vivos, constituindo um grupo de compostos dos mais abundantes e importantes da biosfera. Pode-se citar, como exemplo, celulose e amido nas plantas e glicogênio nos animais [13]. São polímeros naturais, constituídos de unidades básicas chamadas de monossacarídeos unidas por ligações glicosídicas. Essas unidades diferem entre si na unidade, no grau de ramificação, tipo de ligações que as unem e no comprimento de suas cadeias, apresentando diferentes composições e funções. São classificados como homopolímeros ou heteropolímeros [14].
Os homopolímeros possuem um único tipo de unidade monomérica, como por exemplo, amido e glicogênio, os quais servem como forma de armazenamento de glucose, celulose e quitina. Estes atuam como elementos estruturais das paredes das células vegetais e de exoesqueletos de animais. Os heteropolímeros contêm duas ou mais unidades monoméricas diferentes, como os peptidoglicanos, que fazem parte da camada rígida da parede celular das células bacterianas e fornecem um suporte extracelular para os organismos de todos os reinos naturais [15].
Essas macromoléculas são constituídas de glícidos que de acordo com a sua complexidade podem ser agrupados em três tipos principais: os monossacarídeos, os oligossacarídeos e os polissacarídeos. Os glícidos mais simples são os monossacarídeos (oses), que quimicamente são poliálcoois que contêm um grupo aldeído ou um grupo cetónico. Os monossacarídeos mais importantes são os que contêm cinco átomos de carbono, denominados pentoses (ribose e desoxirribose), e seis átomos de carbono, chamados hexoses (glicose ou glucose, frutose e galactose). Os oligossacarídeos são glícidos hidrolisáveis que resultam da ligação glicosídica de dois, os dissacarídeos, sacarose, maltose e lactose, a dez monossarídeos.
osmótico celular [16]. A Figura 1 representa a cadeia estrutural do monossacarídeo, dissacarídeo/oligossacarídeo e polissacarídeo, respectivamente.
Figura 1 - Estrutura do monossacarídeo, dissacarídeo/oligossacarídeo e polissacarídeo.
Fonte: [17].
O uso de polímeros naturais para aplicações diversificadas têm sido de vital importância nos avanços das ciências e apresentam várias vantagens como ser de fácil obtenção, ser biocompatível, biodegradável, abundante na natureza e geralmente atóxico [18]. Outras vantagens da utilização de biopolímeros estão em processos biológicos que incluem as características seguintes: não-carcinogênica, mucoadesividade, alta capacidade de encapsulamento e liberação do fármaco de forma prolongada e a estabilidade térmica [19].
microbiológica [20]. Os polissacarídeos de sementes podem ser divididos em de reservas ou estruturais. Os de reservas são os mais utilizados industrialmente e incluem galactomananas, xiloglucanas, glucanas e mananas. Dentre esses as galactomananas e xiloglucanas se destacam em aplicações na indústria [21] [22]
Os principais polissacarídeos de reserva em plantas são o amido, os frutanos e os polissacarídeos de reserva de parede celular. Estes últimos ocorrem principalmente em sementes e podem ser classificados de acordo com suas estruturas em três grupos: mananas, que inclui as mananas puras, galactomananas e glucomananas, xiloglucanas e galactanas. Esta classificação é baseada essencialmente na estrutura química desses polímeros. Os polissacarídeos podem ser chamados de gomas e, em sentido amplo, são conhecidos pela indústria por ser materiais que podem, quando hidratados em água fria ou quente, formar dispersões coloidais, soluções altamente viscosas em baixas concentrações ou até mesmo géis [23, 24].
As gomas solúveis em água são também conhecidas como hidrocoloides e na indústria de alimentos são largamente utilizadas como ingredientes funcionais atuando como modificadores de textura, agentes gelificantes, espessantes, estabilizadores, emulsionantes, agentes de revestimento, fibras dietéticas e filmes comestíveis [25, 26]. Atividades biológicas como, por exemplo, antivirais, antitumorais, antioxidantes, anticoagulantes e antitrombóticas também vêm sendo investigadas para polissacarídeos extraídos de diversas fontes [27, 28].
A principal importância dessas macromoléculas está na habilidade de controlar características reológicas de sistemas aquosos por meio de estabilização de emulsões, suspensão de partículas, histerese e controle de cristalização [29, 30].
3.1.1 Galactomananas
As galactomananas são polissacarídeos neutros, comumente encontrados no endosperma de sementes onde desempenham papel de reserva. São normalmente catabolizados para fornecer energia e esqueletos de carbono da planta, durante a germinação [31-33].
Esses biopolímeros são assim denominados por apresentarem como estrutura
genérica uma cadeia linear de resíduos de manose unidas por ligações glicosídicas -(14), a
qual os resíduos de galactose estão unidos por ligações do tipo -(16) em graus de
substituição variados, dependendo da espécie [21, 35, 36]. A Figura 2 representa a estrutura genérica da galactomanana.
Figura 2 –Estruturaădaăgalactomananaăcomăunidadesădeămanoseăemăligaçãoăβ-(1-4) e unidades de galactoseăemăligaçãoăα-(1-6).
Fonte: [37].
Sendo uma das maiores famílias do reino vegetal, as leguminosas possuem um número elevado de espécies estudadas. As propriedades físico-químicas e a conformação das galactomananas estão estreitamente relacionadas com a razão manose/galactose e a distribuição estatística das unidades de galactose ao longo da cadeia de manose que varia de espécie para espécie e três subfamílias das leguminosas (Caesalpinioideae, Mimosoideae e Faboideae) podem ser diferenciadas por esta razão e ocupam um papel importante na composição do polímero [38, 39].
A razão M/G são fatores extremamente importantes para estabelecer uma relação entre a estrutura do polímero e suas propriedades em solução, principalmente quanto à sua capacidade de solubilização e interação molecular [40].
Há uma tendência ao aumento de solubilidade em água com o aumento de galactose, mas devido às grandes interações internas (ligações de hidrogênio), isso normalmente não é verificado. Assim, a eficiência de extração aquosa depende da composição das galactomananas e seu rendimento pode variar como método de extração e como tempo envolvido no processo. Devido à sua estrutura, as galactomananas são hidrofílicas e formam soluções de alta viscosidade [43].
As galactomananas mais comuns são as de alfarroba (goma de alfarroba), a tara (goma tara) e a de guar (goma de guar), que possuem razões de M/G com pequenas variações, já que a razão M/G depende do tipo de planta e das condições de extração [44].
As diversas aplicações da galactomanana decorem de suas propriedades reológicas em solução aquosa, formando soluções de alta viscosidade em baixas concentrações (0,5 a 1%) o que as torna comercialmente úteis principalmente como agentes espessantes, estabilizantes, emulsificantes, floculantes e inibidores sinérgicos o que os fazem um material de escolha em indústrias alimentícias, cosméticas, farmacêuticas, têxteis e para fins de liberação oral controlada de fármacos [37, 45, 46].
Todas essas propriedades são diretamente dependentes das características químicas, físicas e estruturais de cada polímero: como peso molecular, configuração anoméricaă (αă eă β),ă conformaçãoă (linear,ă ramificada,ă helicoidal,ă agregaçãoă entreă cadeias),ă presença de grupos funcionais (carboxila, aminas e sulfatos, por exemplo), grau de substituição dos monômeros e a posição das ligações glicosídicas entre as unidades. Dessa maneira, a caracterização química é necessária para o direcionamento de suas aplicações industriais [47-50].
A família Leguminoseae ou Fabaceae é a terceira maior entre as angiospermas. Ocorre em todos os continentes, exceto Antártica, e em diversos habitats, exceto marinho e epifítico [51]. A família é representada por 19.325 espécies, reunidas em 727 gêneros e 36 tribos [52]. No Brasil, há 2.100 espécies reunidas em 188 gêneros e tem importância econômica, principalmente na indústria de fármacos e na construção civil [53, 54]. Sua casca é muito usada na medicina popular, tendo propriedades antiinflamatórias e analgésicas, anti-cancerígenas e anti-úlceras [55-57].
Tabela 1 – Classificação taxonômica da Caesalpinia ferrea.
Taxonomia
Divisão Magnoliophyta (Angiospermae)
Classe Magnoliopsida (Dicotiledonae)
Subclasse Rosidae
Ordem Fabales
Família Caesalpiniaceae (Caesalpinioideae, Leguminosae)
Espécie Caesalpinia ferrea Martius ex Tulasne var. ferrea
Fonte: [58].
As árvores da Caesalpeinia ferrea atingem de 10 a 15 m de altura, com tronco curto de 40 a 60 cm de diâmetro. Folhas compostas bipinadas de 15 a 19 cm de comprimento, com 5 a 11 pinas opostas; folíolos em número de 8-24 por pina. Fruto/legume na forma de vagem indeiscente (não se abre quando maduro), muito duro e de cor escura [59].
As árvores crescem em grande parte do Brasil, apresentando três variedades. A variedade ferrea (sinônimo: Caesalpinia ferrea var. cearensis) tem ocorrência predominante na Região Nordeste, sendo mais comum em regiões da Caatinga, onde é conhecida principalmente por Jucá. As outras duas variedades, parvifolia e leiostachya, são formas características da Mata Atlântica, onde é espontânea no Rio de Janeiro [60, 61]. Folha, vagem e semente estão representadas na Figura 3.
Figura 3 – Folha, flores, vagem e sementes de Caesalpinia ferrea.
A busca de novas fontes de galactomananas constitui uma tarefa de grande importância, uma vez que essa goma pode representar uma alternativa barata, renovável e natural de matéria primas para a indústria [63]. Países tropicais, como o Brasil, apresentam grande potencial como produtores de recursos renováveis que ainda não foram suficientemente explorados, tendo vastas regiões apropriadas ao cultivo de leguminosas [21].
Comercialmente, as galactomananas se destacam devido à sua facilidade de obtenção e industrialização. Embora muitas galactomananas tenham sido isoladas nos últimos anos, somente as sementes de goma-guar (Cyamopsis tetragonolobus, manose/galactose 2:1), deă alfarrobaă ouă “locust bean”ă (Ceratonia siliqua, manose/galactoseă 2:1)ă eă deă gomaă “tara”ă (Caesalpinia spinosa, manose/galacose 3:1) são utilizadas comercialmente [64].
As galactomananas podem ser aplicada na industria como matéria-prima em produtos alimentícios, cosméticos, sequestrantes de metais e sistemas farmacêuticos, a partir de diferentes fontes vegetais, com a vantagem da disponibilidade das sementes o ano todo, considerando que a produção (sazonalidade) é diferente para cada espécie e local [65].
3.2 Glicerol
A estrutura química do glicerol, representada na Figura 4, tem como nome comum o composto orgânico 1,2,3-propanotriol, comercialmente é conhecido como glicerina.
Figura 4 – Estrutura do glicerol
Dentre as características físico-químicas do glicerol destacam-se as propriedades de ser um líquido oleoso, incolor, viscoso e de sabor doce, solúvel em água e álcool em todas as proporções e pouco solúvel em éter, acetato de etila e dioxano e insolúvel em hidrocarbonetos [66].
Na natureza, o glicerol existe em vegetais (soja, mamona, babaçu, girassol, palma, algodão, coco, dendê, pinhão manso) e animais em formas combinadas de glicerina com ácidos graxos. O glicerol é o principal subproduto gerado na produção de biodiesel, correspondendo a aproximadamente 10 % do volume total de biodiesel produzido correspondem a glicerol [67].
Devido à combinação de propriedades físico-químicas, como não toxicidade, ausência de cor e odor, o glicerol é uma substância com grande variedade de aplicações. Na indústria química, farmacêutica, alimentícia, têxtil, aplicações terapêuticas e etc. Na indústria de alimentos o glicerol é utilizado como aditivo alimentar em função de suas propriedades estabilizantes, antioxidantes, sequestrantes, emulsificantes e umectantes [68].
O glicerol também pode ser usado como plastificante, onde possui a função de diminuir as forças intermoleculares entre as cadeias, melhorando, assim, a flexibilidade, a força tensil e as propriedades de adesão do filme formado. Essa melhor coalescência é atribuída à capacidade dos plastificantes em reduzir a temperatura de transição vítrea (Tg) dos polímeros a eles associados, o que aumenta, como consequência, a mobilidade das cadeias poliméricas, melhorando a propriedade mecânica dos filmes [69].
Na produção dos filmes a base de polímeros, geralmente é adicionada materiais plastificantes como o glicerol, a fim de melhorar as propriedades físicas, químicas e mecânicas dos compósitos obtidos [70]. Sendo assim, a incorporação de plastificante em biopolímeros é uma ótima alternativa para resolver problemas como: baixa elasticidade, pouca resistência, que o deixa quebradiço, pois modifica a organização molecular tridimensional da rede polimérica, diminuindo as forças de atração intermoleculares e aumentando o volume livre do sistema. Consequentemente, melhora a flexibilidade e extensibilidade dos filmes [9].
3.3 Materiais Magnéticos
O magnetismo é o fenômeno que está relacionado com a força de atração ou repulsão que atua entre os materiais magnéticos. Os materiais podem pertencer magneticamente ao grupo dos materiais diamagnéticos, paramagnéticos e ferromagnéticos. Além destes, o ferrimagnetismo e o antiferromagnetismo são consideradas subclasses do ferromagnetismo [71, 72]. Os materiais ferromagnéticos e ferrimagnéticos possuem magnetização espontânea, ou seja, eles apresentam magnetização não nula, mesmo na ausência de campo externo aplicado. Essa classificação está associada à resposta magnética do material a um campo aplicado que tem seus dipolos atômicos orientados na direção desse campo [71-73].
A Perda por histerese é proporcional à área do laço, por exemplo, em materiais magnéticos duros, o laço de histerese e largo, enquanto em materiais magnéticos macios, o laço de histerese é estreito. A Figura 5 representa a curva de magnetização, o efeito da variação de sentido do campo magnético e o laço de histerese, respectivamente.
Figura 5 – Ciclo de histerese para um material magnético.
Fonte: [74].
A curva começa na origem e à medida que o valor de H aumenta, campo externo aplicado, M, magnetização, aumenta até alcançar um valor máximo que é chamado de magnetização de saturação (Ms), onde retorna quando atinge a magnetização de saturação máxima reduzindo H até o valor nulo inicial, observando-se que os valores de magnetização obtidos não coincidem com os valores iniciais da curva (M=0), ou seja, existirá um magnetismo remanescente (Mr). Um efeito de histerese é produzido, onde o campo M se defasa em relação ao H aplicado, ou diminui a uma taxa mais baixa [71, 72].
sistemas de conversão eletromecânica (eletrodomésticos, automóveis, aviões), eletrônicos e de telecomunicações, transdutores, sensoriamento, prospecção geológica, informática, automação industrial, medicina e a engenharia biomédica [71, 75, 76]. Como exemplo de materiais magnéticos pode-se citar o ferro, alguns aços e a magnetita, onde toda substância é influenciada, em maior ou menor grau, pela presença de um campo magnético[71].
Nas últimas décadas, nanopartículas magnéticas têm sido alvo de extensivos estudos devido sua interação com um campo magnético externo. Tal propriedade as torna um material atrativo para aplicações que exijam um direcionamento, como em operações de transporte e separação [77].
Esses materiais ganharam destaque nas aplicações biológicas, onde diferentes formas de óxido de ferro para procedimentos diagnósticos, como ressonância magnética nuclear (RMN), carreador magnético de drogas e hipertermia magnética tem ganhado ampla aceitação em vários tipos de práticas, embora as aplicações terapêuticas ainda estejam sob investigação. Tais aplicações exploram as duas maiores vantagens dos óxidos de ferro: sua baixa toxicidade em seres humanos e a possibilidade de se controlar sua magnetização [78, 79].
A eficácia das nanopartículas magnéticas de óxido de ferro como agente de contraste em vários tecidos depende de suas propriedades físico-químicas, tais como, tamanho, carga e revestimento. E pode ser aumentada através de modificações na superfície por substancias biológicas ativas (antibióticos, polissacarídeos, ligantes receptores, proteínas e etc) [80].
Materiais magnéticos podem ser classificados de acordo a interação intrínseca destes com um campo magnético externo. Uma propriedade característica utilizada para tal fim é a susceptibilidade magnética [81]. Os valores encontrados para susceptibilidade magnética servem de parâmetro para avaliar o comportamento magnético do material bem
como para classificá-lo em diamagnético, paramagnético, ferromagnéticos,
antiferromagnético ou ferrimagnético [12]. Materiais com estrutura de espinélio, como as ferritas, são um grande exemplo de partículas com este comportamento magnético [82].
comportamento superparamagnético se manifesta quando o tamanho da partícula é comparável ao tamanho do domínio magnético.
3.3.1 Ferritas: estrutura e propriedades
Ferritas são materiais cerâmicos que apresentam em sua composição óxido de
ferro (Fe2O3) combinado com outros metais. Genericamente, a estrutura de espinélio pode ser
representada pela fórmula AB2O4, onde A é o metal com estado de oxidação 2+ e B é o metal
com estado de oxidação 3+. O cristal deste material também pode ser representado por
MFe2O4, onde M geralmente é um metal de valência 2+, como por exemplo, Ni2+, Mn2+, Zn2+
etc [81]. A célula unitária de uma ferrita do tipo espinélio está representada na Figura 6 com os átomos de oxigênio formando uma estrutura Cúbica de Face Centrada (CFC) [85].
Figura 6 – Representação da estrutura de Espinélio (AB2O4).
Fonte: [86].
posição dos cátions na rede cristalina, a estrutura espinélio é definida como normal. No caso de M2+[Fe3+]O4 e inversa, no caso de Fe3+[M2+Fe3+]O4 [82].
Para um espinélio do tipo normal, o sítio tetraédrico é ocupado por um cátion de valência 2+, enquanto que o sítio octaédrico é ocupado pelo cátion com valência 3+, por exemplo, podemos citar a ferrita ZnFe2O4 [87]. No caso de um espinélio inverso ocorre o
contrário, ou seja, cátions 2+ ocupam sítios octaédricos e cátions 3+ ocupam os sítios
tetraédricos. Um exemplo é a ferrita NiFe2O4 [88].
Os materiais com estrutura de espinélio também podem apresentar uma mistura entreă asă estruturasă normală eă inversa.ă Alémă dasă ferritasă “puras”,ă também é possível obter ferritasă “misturadas”,ă ouă seja,ă ferritasă naă quală aă estruturaă éă formadaă poră doisă cátionsă
divalentes. Sendo assim, materiais tais como MnZnFe2O4 e NiZnFe2O4 podem ser
classificadosăcomoăferritasăă“mistas”.ăOsămesmosăapresentamă50%ădosăíonsăZn2+ substituídos pelos cátions Mn2+ e Ni2+ para a formação da estrutura de espinélio. No caso da ferrita
NiZnFe2O4, os cátions Zn2+ presentes na estrutura ocupam os sítios tetraédricos, enquanto que
80% dos cátions Ni2+ ocupam os sítios octaédricos e apenas 20% sítios tatraédricos [82].
As ferritas apresentam propriedades extrínsecas e intrínsecas [89]. As intrísecas são definidas como as propriedades elétricas e magnéticas que dependem somente da estequiometria, tais como magnetização de saturação, anisotropia magnetocristalina, magnetoestricção, temperatura de Curie. Já as extrínsecas dependem do tamanho e contorno de grão, porosidade e densidade. Devido a essas propriedades extrisnsecas se fez necessário o desenvolvimento de vários métodos de obtenção de ferritas com o intuito de controlar variáveis tais como tamanho de grão, porosidade etc [81]. Estas por sua vez podem ser frequentemente empregados em indutores de alta frequência, transformador de núcleos de dispositivos eletrônicos, como gravação magnética, barras para antenas, componentes de micro-ondas, dispositivos magnéticos permanentes, gravação de alta velocidade e disquetes, entre outros [81, 90-92].
A capacidade para produzir nanopartículas ultrafina de ferrita resulta em novas aplicações, devido às propriedades únicas destes materiais magnéticos que dependem de vários fatores, tais como o método de preparação, a composição, a temperatura de sinterização, o tempo de sinterização, atmosfera de sinterização, etc [93].
[100], dente outros. Esses métodos foram desenvolvidos, visando trazer contribuições valiosas na otimização dos processos de fabricação e das propriedades de tais materiais.
As ferritas, materiais com estrutura de espinélio, são amplamente estudadas por apresentarem propriedades estruturais, magnéticas e elétricas que dependem do processo de fabricação, composição química e microestrutura tornando-se importantes para aplicações principalmente na tecnologia de materiais nanoestruturados [101].
No devido trabalho, utilizou-se a síntese hidrotérmica devido as suas vantagens como, por exemplo, obter principalmente o controle da homogeneidade química, morfológica e granulométrica dos pós, garantindo, assim, o controle da microestrutura e propriedades finais do material [102].
A síntese de materiais cerâmicos envolvendo processos hidrotérmicos baseia-se no aquecimento da suspensão formada pelos precursores metálicos sob condições de elevadas temperatura e pressão. O termo hidrotérmico implica a ocorrência de reações em meio aquoso submetidas a elevadas temperaturas (T > 25°C) e pressões (P > 100 kPa) [103]. Desta forma, os processos de nucleação e crescimento são conduzidos a formarem partículas com tamanho reduzido além do controle da forma [104].
Nessas condições, podemos ter materiais cerâmicos com elevada cristalinidade com uma série de vantagens sobre métodos convencionais e não-convencionais devidos a sua versatilidade no preparo, sendo possível regular a taxa e a uniformidade da nucleação, crescimento e envelhecimento, para promover o controle do tamanho e morfologia do cristal, além de reduzir os níveis de agregação dos mesmos [105].
As principais vantagens do método hidrotérmico, em detrimento das outras tecnologias de preparo de materiais, estão mostradas na Tabela 2.
Tabela 2 – Principais vantagens do método hidrotérmico.
Fonte: [102].
Principais Vantagens
Pó formado diretamente em solução
Pó sintetizado pode ser anidro, cristalino ou amorfo
Controle do tamanho da partícula
Controle da forma da partícula Controle de composição e estequiometria
As nanopartículas magnéticas de óxido de ferro foram desenvolvidas como agente de contraste para MRI e aumentaram a sensibilidade e a especificidade dos diagnósticos, devido às modificações do tempo de relaxação dos prótons. Esses agentes de contraste têm uma vantagem de produzir um aumento na relaxação dos prótons em MRI em comparação com os paramagnéticos. Consequentemente, doses em quantidades menores destes agentes de contraste com nanopartículas de óxido de ferro magnéticas são necessárias no corpo humano do que as paramagnéticas [80, 106, 107]. Tais aplicações exploram as duas maiores vantagens dos óxidos de ferro: sua baixa toxicidade em seres humanos e a possibilidade de se controlar sua magnetização [108].
A nanotecnologia biomédica, que se baseia na construção de nanopartículas puras ou na combinação de materiais inorgânicos e orgânicos, está assumindo um papel de grande importância para aplicações em diagnóstico, terapêutica, biologia molecular e bioengenharia [109].
3.4 Biocompósitos
Os biocompósitos são materiais heterogêneos formados por dois ou mais constituintes distintos, combinando diferentes biomateriais para produzir um único dispositivo com desempenho superior à de seus componentes formadores. Os biomateriais são definidos como qualquer substância ou combinação de substâncias, naturais ou sintéticas, metais, cerâmicas, macromoléculas naturais e compósitos que são utilizados em aplicações biomédicas e que interagem com sistemas biológicos [110].
A combinação entre cerâmicas e polímeros tem sido muito usada nas últimas duas décadas para produzir compósitos de elevado desempenho. Sendo assim, tendo em vista as propriedades inerentes dos materiais envolvidos, onde estão fundamentalmente ligadas à estrutura básica destes materiais, como ligações químicas primárias e arranjo atômico, é que dentro deste contexto, os materiais cerâmicos, híbridos cerâmico-polímeros e compósitos cerâmico-cerâmicos apresentam grande versatilidade no desenvolvimento de novos materiais com aplicações biotecnológicas [109].
Filmes de polissacarídeos podem ser obtidos a partir de derivados hidrossolúveis de celulose, amido, pectina, alginatos, carragena, dextrinas e outras gomas. São exemplos de biomateriais, metais, cerâmicos, polímeros, compósitos e semicondutores [112].
A busca por um material que possa funcionar como uma interface entre o biológico e o eletrônico é um grande incentivo para o estudo de novos compósitos [113]. Uma blenda polimérica é uma mistura de polímeros, cuja finalidade é a obtenção de um material que apresente características físicas, químicas e físico-químicas diferenciadas, combinadas de modo a conservar as vantagens de cada polímero [114-117].
Para solucionar as desvantagens das cerâmicas e polímeros, novos estudos têm sido realizados no intuito de desenvolver nanobiocompósitos que possuam propriedades satisfatórias para aplicações em diversas áreas [110].
4. MATERIAIS E MÉTODOS
4.1 Materiais e reagentes
Todos os reagentes e materiais utilizados no procedimento com o objetivo de isolar e purificar a galactomanana foram os seguintes: sementes de Jucá e álcool etílico
comercial (CH3CH2OH, Cequimica, 96%).
Na síntese da nanopartícula de NiZn, todos os reagentes foram de grau analítico sendo: cloreto de ferro III hidratado (FeCl3.6H2O, Dinâmica, 97%), cloreto de níquel II
hidratado (NiCl2.6H2O, Vetec, 97%), cloreto de zinco II (ZnCl2, Dinâmica, 97%) e hidróxido
de sódio (NaOH, Cinética Química, 97%). Na preparação dos nanobiocompósitos,
acrescentou-se o glicerol (C3H8O3, Vetec, 96%) utilizado como plastificante na formação dos
filmes.
4.2 Extração e purificação das Galactomananas
Uma amostra de 112g de sementes de jucá da espécie Caesalpinia ferrea foi
posteriormente uma amostra de 10g foram liofilizados. A referida coleta se deu através de separação manual do tegumento a partir do embrião. Tal procedimento evita as principais impurezas nas galactomananas, eliminando as substâncias presentes nos revestimentos da semente e do embrião como proteínas, lipídios, fibras brutas, xilose e pentoses. Após a obtenção dos endospermas, estes foram submetidos a quatro extrações aquosas com 900 mL de água milli-Q por 4 horas, a 80°C, sobre agitação constante. Ao final de cada extração uma solução viscosa era retirada e reservada. Posteriormente, a referida solução oriunda do procedimento anterior, foi adicionada uma solução aquosa de álcool etílico na proporção 1:3 (v/v). Um precipitado foi observado após a adição obtendo, assim, a galactomanana. Esta, por sua vez, foi retirada e resolubilizada em 900 mL de água milli-Q e liofilizada [8, 118]. Ao final do processo verificou-se um rendimento de 59,5% (m/m) de galactomanana, valor consideravelmente favorável em escala maior de produção A amostra de galactomanana obtida neste trabalho foi nomeada GM.
4.3 Síntese das nanopartículas magnéticas
Neste trabalho, utilizou-se o método de reações hidrotérmicas, uma vez que este possibilita um pequeno tamanho de grão, homogeneidade e em alguns casos a eliminação do processo de calcinação. A síntese das nanopartículas ocorreu em meio básico de acordo com a reação (1).
0,5Ni2+ + 0,5Zn2+ + 2Fe3+ + 8OH- Ni0,5Zn0,5Fe2O4 + 4H2O (1)
As nanopartículas foram sintetizados de acordo com Freire et al [119]. As quantidades estequiométricas dos precursores metálicos foram dissolvidos em água destilada
obedecendo a relação molar de 0,5Ni2+ + 0,5Zn2+: 2Fe3+, ou seja, na proporção 1 : 2 para os
precipitado foi lavado seguidas vezes com água destilada e metanol. O produto resultante foi colocado em uma mufla a 100°C, por 3, horas para secagem. Posteriormente, o produto seco foi macerado em cadinho de porcelana para a obtenção da nanopartícula magnética de fórmula Ni0,5Zn0,5Fe2O4. Esta amostra foi denotada NiZn.
4.4 Síntese dos Nanobiocompósitos
Os nanobiocompósitos constituídos de galactomanana (GM), glicerol (GL) e
nanopartícula magnéticas (MNPs) de NiZn foram preparados em proporções diferentes a fim
de encontrar a melhor composição para os mesmos. Desta forma, em um primeiro momento, somente as composições de GM e GL foram testadas. Todas as massas utilizadas bem como as proporções em percentual são mostradas na Tabela 3.
No intuito de produzir filmes de aspectos relativamente homogeneios foram realizados testes com os materiais galactomanana e glicerol. Sendo assim, as composições de GM e GL foram preparadas com as seguintes porcentagens: 90/10, 80/20 e 70/30 (GMGL). As massas de GM e GL foram pesadas conforme mostrado na Tabela abaixo. Foram adicionados 50 mL de água mili-Q e as amostras permaneceram sob agitação até a total solubilização.
Tabela 3 - Valores de massa bem como as proporções em percentual utilizada nos testes de
composição para GM e GL.
GM GL
GMGL
Massa (mg) Percentual (%) Massa (mg) Percentual (%)
4,5x10-4 90 0,5x10-4 10 90/10
4,0x10-4 80 1,0x10-4 20 80/20
3,5x10-4 70 1,5x10-4 30 70/30
Fonte: Próprio autor.
Inicialmente, quantidades de GM e GL foram pesadas na proporção escolhida. Foram adicionados 50 mL de água mili-Q e o sistema permaneceu em agitação até total solubilização. Com GM e GL devidamente solubilizadas, acrescentou-se requerida quantidade de NiZn para cada amostra preparada. Essas soluções foram homogeneizadas utilizando o aparelho Sonifier W450D Branson nas seguintes condições: 50% de amplitude por 5 minutos, variando 2s de pulso ON e 1s de pulso OFF sob banho de gelo para que não ocorra a degradação do polímero. Após o término do procedimento anterior, as soluções foram colocadas em placas de Petri e mantidas em temperatura ambiente por cinco dias para secagem dos filmes.
4.5 Técnicas de caracterização
4.5.1 Difração de Raios-X
As análises de difração de Raios-X (DRX) foram realizadas em um aparelho
Rigaku (Laboratório de Raio-X / Departamento de Física – UFC) equipado com tubo de
CuKαă(λ=ă1,54056Å),ăutilizandoăvoltagemădeă40ăkVăcomăumaăcorrenteădeă25mA.ăOsăfilmesă foram fixados sobre uma placa de vidro recortadas retangularmente, com medidas de 2,0 cm x 1,5 cm e a análise para o pó da nanoparticula de Ni-Zn foi realizada para determinação dos valores de tamanho de partícula, parâmetros de rede e as fases. Estes foram calculados a partir do tratamento matemático do difratograma obtido através do refinamento de materiais cristalinos utilizando o Método de Rietveld.
4.5.2 Espectroscopia na região do Infravermelho
Os dados de Espectroscopia na região do Infravermelho (FTIR) foram obtidos em um aparelho Espectrômetro Perkin Elmer FTIR (Departamento de Química Orgânica e
Inorgânica – UFC). As amostras de GM, NP e seus respectivos filmes foram analisados
utilizando pastilha de KBr misturada e triturada ao material. Os espectros foram coletados na
faixa 4000–400 cm-1. A espectroscopia na região do infravermelho é uma das técnicas
4.5.3 Análise Térmica
As amostras foram submetidas à análise termogravimétrica (TG) em equipamento modelo TGA Q50 V20.13 Build 39 da TA Instruments. As amostras foram colocadas em cadinhos de platina na faixa de temperatura usada foi de 0 a 700°C. A razão de aquecimento
de 10°C.min-1 em atmosfera de N2 e vazão de 25 mL.min-1. As medidas foram realizadas em
colaboração com o Laboratório de Análises Térmicas, no Departamento de Química Orgânica e Inorgânica na Universidade Federal do Ceará.
4.5.4 Calorimetria Exploratória Diferencial
As curvas DSC foram obtidas no equipamento DSC Q20 V24.9 Build 121, sob
atmosfera dinâmica de nitrogênio, com vazão de 50 mL.min-1, em cadinhos herméticos de
alumínio, razão de aquecimento de 10ºC.min-1 até atingir 400ºC. As medidas foram realizadas
no laboratório de Análises Térmicas, no Departamento de Química Orgânica e Inorgânica na Universidade Federal do Ceará.
4.5.5 Microscopia Eletrônica de Varredura
As análises de microscopia eletrônica de varredura foram realizadas em um equipamento TM3000 Tabletop Microscope. As amostras dos filmes foram colocadas sobre uma superfície adesiva de carbono, sem a necessidade de recobrimento da amostra por outro metal. As analises foram realizadas em colaboração com o laboratório de analise de MEV no departamento de Geologia, Universidade Federal do Ceará.
4.5.6 Microscopia Eletrônica de Transmissão
A análise de Microscopia Eletrônica de Transmissão foi realizada para amostra da
nanoparticula de NiZn em um equipamento Jeol JEM – 1011 operando em 100 kV e equipado
4.5.7 Medidas dielétricas
As medidas dielétricas foram realizadas abrangendo um intervalo de frequência entre 0,4 e 7,0GHz, a temperatura ambiente de 300K. No aparelho Agilent E4991A (RF Impedance / MaterialAnalyzer). As amostras foram analisadas através do contato dos eletrodos do aparelho.
4.5.8 Medidas magnéticas
As medidas magnéticas foram realizadas por J. C. Denardin (Departamento de Física, Universidad de Santiago de Chile) a temperatura ambiente com magnetômetro (vibrating sample magnetometer - VSM) previamente calibrado com um fio de níquel. Após a medida da massa de cada amostra, a magnetização foi dada em emu/g.
5 RESULTADOS E DISCUSSÃO
5.1 Caracterização da Galactomanana
5.1.1 Espectroscopia de Absorção na Região do Infravermelho
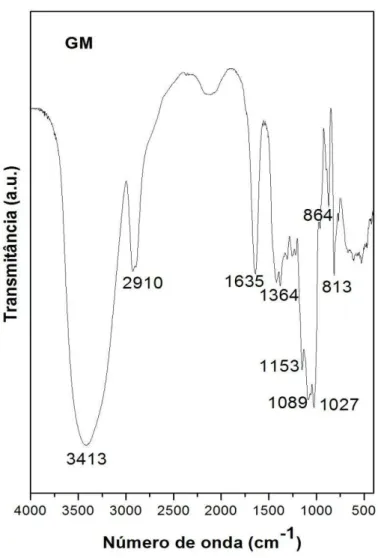
Figura 7- Bandas de absorção na região do infravermelho de GM.
Fonte: Próprio autor.
Na região anomérica, frequências entre 950 e 700 cm-1, exibiram absorções
característica da galactomanana. Bandas evidenciadas em 864 e 813 cm-1 podem ser
atribuídas àă presençaă deă unidadesă α-D-galactopiranoseă eă unidadesă deă β-D-mannopiranose,
respectivamente [4, 120]. A banda em 1027 cm-1 pode ser atribuída ao alongamento
vibracional do CH2, enquanto que a banda em 1089 cm-1 surgiu a partir do estiramento do
álcool primário CH2OH presente na estrutura [121]. Outra banda em 1153 cm-1 também foi
observada. Esta, por sua vez, podeăserăatribuídaăàăligaçãoăvibracională (C-O) devido ao anel
de piranose [4]. A região entre 1364 e 1450 cm-1 está relacionada a deformações simétricas
dos grupos COH e CH2. A banda em 1635 cm-1 refere-se ao estiramento do anel de galactose
e de manose. Em 2910 cm-1, pode estar relacionada ao grupamento CH, em especial do grupo
CH2. Bandas acima de 3000 cm-1 tais como a observada em 3413 cm-1 fazem referência ao
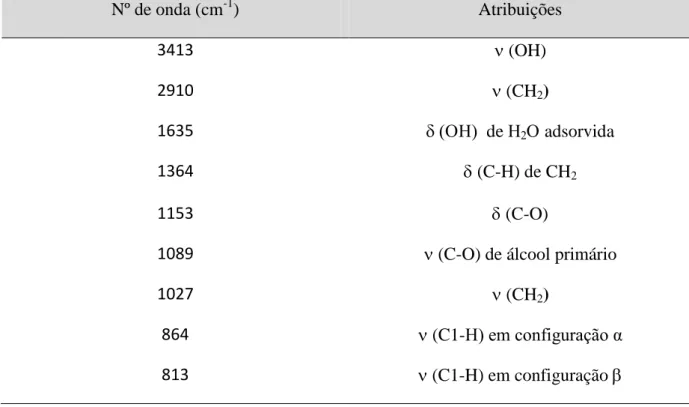
As principais atribuições das bandas de absorção da amostra GM estão representadas na Tabela 4.
Tabela 4 - Bandas de absorção na região do infravermelho da amostra GM.
Nº de onda (cm-1) Atribuições
3413 (OH)
2910 (CH2)
1635 de adsorvida
1364 (C-H) de CH2
1153 (C-O)
1089 (C-O) de álcool primário
1027 (CH2)
864 (C1-H)ăemăconfiguraçãoăα
813 (C1-H) em configuração
Fonte: Próprio autor
5.1.2 Análise Térmica
Figura 8 – Perfil de degradação da amostra GM.
Fonte: Próprio autor.
O resultado do perfil de degradação de GM mostrado na Figura 8 está de acordo com dados encontrados na literatura para galactomanana [126-128]
5.1.3 Calorimetria Exploratória Diferencial
Figura 9 – Termograma por DSC da amostra GM
Fonte: Próprio autor.
O termograma mostra duas transições para a amostra GM. A primeira, entre 160 e 165°C, resulta da desidratação da amostra com evento endotérmico exibindo um evento em 164,57°C e entalpia de 184.6 J/g. O segundo evento, corresponde à decomposição do material orgânico em transição exotérmica com evento em 309,95 °C, gerando uma entalpia de 105.5 J/g.
5.1.4 Microscopia Eletrônica de Varredura
polissacarídeos. As microscopias da amostra GM com ampliação 120X (a) e 600X (b) estão representadas na Figura 10. Nesta amostra visualizou-se uma malha constituída basicamente por fibras. Ou seja, observou-se nas duas micrografias o comportamento fibrilar com um padrão interno de polimerização heterogêneo. Tal fato torna-se mais evidente quando a amostraăéăampliadaăemă“b”.ăSendoăassim,ăduasăregiõesăsãoăobservadas, uma com superfícies lisas e a outra com fibras entrelaçadas.
Figura 10 - Micrografias da amostra GM com ampliação 120X (a) e 600X (b).
Fonte: Próprio autor.
5.2 Caracterização da nanopartícula NiZn
5.2.1 Difração de Raios-X
Figura 11 - DRX da amostra NiZn
Fonte: Próprio autor.
Os picos de difração observados em 29,9°, 35,3°, 42,8°, 53,3°, 56,7° e 62,2°
podem ser atribuídos à fase cúbica (JCPDS n° 086-1355) das ferritas com grupo espacial Oh7,
indicando a formação da estrutura espinélio. Além disso, nenhum vestígio de NaCl foi encontrado evidenciando o excelente processo de lavagem realizado. O difratograma mostra que não há a presença de picos associados a frase secundária. Os dados estruturais provenientes do DRX da amostra NiZn foram tratados com o auxílio do programa DBWTools, versão 2.3 [130], através do método de Rietveld, onde foram obtidos alguns parâmetros como: tamanho de partícula, parâmetro de rede, quantificação das fases etc. Neste método, alguns dos parâmetros mais importantes a serem avaliados são o Rwp (porcentagem de erro obtido) e o S (razão do erro previsto pelo erro esperado), uma vez que estes se referem à concordância e ao progresso do refinamento [131]. Desta forma, foram observados alguns dados estruturais obtidos pelos ajustes, bem como parâmetro de rede, Rwp e S.
10 nm. Os parâmetros Rwp e S apresentaram valores de 17,56 (%) e 1,05, respectivamente. Tais valores demonstram a boa qualidade do refinamento, pois valores na faixa 10 a 20 % para Rwp e menores que 1,3 para S evidenciam um refinamento confiável de caráter satisfatório [98].
5.2.2 Espectroscopia Vibracional na Região do Infravermelho
O espectro de FTIR da amostra NiZn está representado na Figura 12 e permite
identificar a presença de grupos OH- e H2O adsorvida na superfície das nanopartículas, uma
vez que foi possível observar bandas em 3436 e 1632 cm-1, respectivamente. A formação da
estrutura de espinélio também foi evidenciada através de bandas observadas entre 750 e 400
cm-1 e estas podem ser atribuídas às vibrações de íons metálicos em sítios com determinadas
Figura 12 – Bandas na região do infravermelho de NiZn.
Fonte: Próprio autor.
Observou-se uma banda em 586 cm-1 que pode ser atribuída a vibração do metal
no sítio tetraédrico, ou seja, oriunda de um sítio com simetria Td e que contribui com 1 dos 5
modos T1u que são ativos na região do infravermelho. Outra banda em 450 cm-1 foi
identificadaăeăéăcaracterísticaădaăvibraçãoădoămetalănoăsítioă“octaédrico”,ăpoisăapareceăentreă 385 a 450 cm-1. Essa banda é proveniente de um sítio com simetria D3d que contribui com
mais 1 modo T1u. De acordo com a literatura, é previsto a aparição de 5 modos vibracionais T1u. Entretanto, a faixa de número de onda estudada, somente foi possível observar 2 modos. As demais bandas correspondentes aos outros modos vibracionais aparecem em números de
5.2.3 Medidas Magnéticas
A susceptibilidade magnética em materiais depende da temperatura e também do campo, fornecendo uma curva com forma sigmoidal característica onde é possível investigar as propriedades magnéticas das nanopartículas. Materiais magnéticos, de maneira geral, apresentam curvas abertas de M-H, chamadas de laços (loops) de histerese. A Figura 13 apresenta a curva de magnetização para amostra NiZn que foi realizada a temperatura ambiente.
Figura 13 – Curva de magnetização da amostra NiZn
Fonte: Próprio autor.
O perfil de magnetização sugere a obtenção de um material com caráter superparamagnético, pois não se observou histerese na curva de magnetização obtida. Logo, a amostra estudada apresentou coercividade nula com bastante susceptibilidade a um campo
magnético externo atingindo sua magnetização de saturação (Ms) com a aplicação de campos
magnéticos relativamente pequenos. O valor Ms para a amostra NiZn foi registrado em torno
de 56 emu/g.
5.2.4 Microscopia Eletrônica de Transmissão
A imagem obtida no Microscópio Eletrônico de Transmissão para a amostra NiZn com ampliação em uma dada região está representada na Figura 14.
Figura 14 – Micrografia da amostra NiZn com ampliação em uma dada região.
Fonte: Próprio autor.
Através da micrografia mostrada acima foi possível determinar o tamanho médio da partícula. O valor encontrado foi aproximadamente 10,8 nm. Tal valor confirma o resultado encontrado por DRX. Além do referido parâmetro retirado da micrografia. O TEM também pode ser empregado para avaliar a morfologia da partícula. Para este trabalho, tal fator merece destaque uma vez que o processo de síntese aplicado para a síntese da amostra pode resultar em partículas com diferentes morfologias dependendo das condições aplicadas
realizado durante a síntese da amostra NiZn, foi possível verificar pela micrografia ampliada dentro da Figura sua morfologia cúbica.
5.3 Caracterizações dos nanobiocompósitos
5.3.1 Características macroscópicas dos filmes
Na busca de preparar nanobiocompósitos com aspectos satisfatórios foi realizado um teste para avaliar a melhor composição de GM e GL nas seguintes proporções mássicas: 90/10, 80/20 e 70/30 de GMGL com massa fixa de 0,1g de NiZn.
A imagem dos filmes nas proporções 90/10, 80/20 e 70/30 com a massa fixa de 0,1g de NiZn está apresentada na Figura 15, onde a massa fixa de NPs foi adicionada para identificar sua magnetização incorporada nos filmes. Estes, por sua vez foram analisados quanto as suas características macroscópicas referentes à homogeneização.
Figura 15 - Filmes de GMGL nas proporções 90/10, 80/20 e 70/30 com a massa fixa de 0,1g de
NiZn.
Fonte: Próprio autor.
5.3.2 Difração de Raios-X
O padrão e as fases cristalinas dos picos característicos da amostra NiZn, GMGL e os respectivos nanobiocompósitos estão mostradas na Figura 16.
Como relatado anteriormente, os dados estruturais provenientes do DRX para a amostra NiZn foram tratados com o auxílio do programa DBWTools, versão 2.3 [130], através do método de Rietveld, e foi evidenciado somente a presença da estrutura de espinélio sem qualquer impureza.
Figura 16 - DRX dos nanobiocompósitos 0,06NP, 0.14NP, 0,20NP, GMGL e NiZn
Com a amostra de NiZn devidamente refinada foi possível comparar os difratogramas das amostras. A amostra contendo Galactomanana e glicerol foi chamado no texto de GMGL e as nanoparticulas magnéticas de NP. Observa-se que o difratograma da amostra GMGL não indica nenhuma fase cristalina, já que este não apresenta NPs e dispõem de uma quantidade maior da galactomanana que é um material amorfo. No entanto, mesmo sendo um material amorfo, as fases cristalinas referentes a ferrita de NiZn foram evidenciadas nos difratogramas dos nanobiocompósitos, 0,2NP, 0,14NP e 0,06NP, confirmando a presença de NiZn compósitos sintetizados.
5.3.3 Espectroscopia de Absorção na Região do Infravermelho
Os espectros de FT-IR da amostra de NiZn, GMGL e dos nanobiocompóstios estão representados na Figura 17.
Figura 17 – Bandas de absorção na região do infravermelho do NiZn, GMGL e dos
nanobiocompósitos.
Como relatado anteriormente, o espectro da amostra NiZn permite identificar a
presença de grupos OH- e H2O adsorvida com bandas em 3436 e 1632 cm-1, respectivamente.
Além disso, a formação da fase de espinélio com bandas de absorção entre 750 – 400 cm-1 também foi evidenciada [98, 132].
Por outro lado, o compósito GMGL apresenta bandas de absorção em 3400 e 1651 cm-1 características de glicosídicos relativos aos grupos OH- e H2O adsorvida [106, 135].
Outras bandas detectadas em 2924, 1429 e 1040 cm-1 indicam, respectivamente, o estiramento
dos grupos CH2, CH e CO presentes na estrutura dos polissacarídeos [123, 136]. Atribuições
das principais bandas de absorção das amostras de GMGL e NiZn estão representadas na Tabela 5.
Tabela 5 - Bandas de absorção na região do infravermelho e suas respectivas atribuições.
Amostras Nº de onda (cm-1) Atribuição
GMGL
3400 (OH)
2924 (CH2)
1651 de adsorvida
1429 (C-H) de CH2
1040
872
(C-O) de álcool primário
(C1-H)ăemăconfiguraçãoăα
818 (C1-H) em configuração
NiZn
3436 (OH)
1632 de adsorvida
586 (Fe-O)
450 (Fe-O)
De acordo com as bandas características apresentadas para as amostras de NiZn e GMGL podemos verificar através dos espectros dos nanobiocompósitos (0,06NP, 0,14NP e 0,2NP) a incorporação das nanopartículas de NiZn na matriz GMGL. Os espectros mostraram também que houve a homogeneização dos compósitos e um aumento de intensidade da banda
observada em 586 cm-1, de acordo com o esperado para as proporções de NPs. Ou seja, existe
um aumento na intensidade da referida banda à medida que há um aumento na massa de nanopartícula. A Tabela 6 representa as bandas de absorção das amostras dos nanobiocompósitos e suas respectivas atribuições.
Tabela 6 - Bandas de absorção na região do infravermelho e suas respectivas atribuições.
Nº de onda (cm-1)
Atribuições
0,06NP 0,14NP 0,20NP
3410 3391 3408
(OH)
2924 2920 2923 (CH2)
de adsorvida
(C-H) de CH2
(C-O) de álcool primário
(Fe-O)
1651 1651 1639
1432 1400 1397
1032 1047 1047
586 586 586
υă- estiramento,ă ă- deformação angular. Fonte: Próprio autor.
Portanto, de acordo com os espectros de FT-IR pode-se confirmar a presença de NiZn nos nanobiocompósitos atribuídos ao processo de extração, purificação e síntese dos materiais envolvidos, bem como a homogeneização dos mesmo pelo processo de preparação.
5.3.4 Análise Térmica
anteriormente discutida. Isso se devi ao maior número de cadeias formadas na incorporação do glicerol ao compósito.
Já a amostra GMGL apresenta maior perda de massa no 2° evento quando comparada aos nanobiocompósitos e a amostra NiZn maior quantidade de resíduo. Não foram identificados eventos significativos em NiZn já que materiais cerâmicos apresentam-se bastante resistentes a temperaturas elevadas [137].
Figura 18 – Perfil de degradação das amostras GMGL, NiZn e dos nanobicompósitos
Fonte: Próprio autor.
As amostras GMGL e 0,20NP apresentaram somente dois eventos enquanto que as amostras 0,06NP e 0,14NP três eventos. Os eventos de degradação tiveram comportamento semelhante para todas as amostras com exceção de NiZn. Tal fato pode ser explicado por sua alta estabilidade térmica. Para GMGL e os nanobiocompósitos, pode-se afirmar que o experimento revelou curvas de degradação cujos comportamentos estão de acordo com os dados da literatura [138].
evento de degradação para a amostra 0,06NP foi observado na temperatura entre 80 e 200°C com perda de massa de 17,43%. No entanto, o 3º evento da amostra 0,06NP e os 2º eventos das amostras GMGL, 0,14NP e 0,20NP apresentaram perdas de massa semelhantes em 46,32%, 75,44%, 56,46% e 63,16% respectivamente. Contudo ainda foi observado um 3º evento da amostra 0,14NP entre 500 e 700°C com perda de massa de 15,53%. Esses valores de perda de massa estão associados à incorporação das NPs ao polímero com diferentes magnitudes de interação. Isto, por sua vez, explica o aparecimento de novos eventos de perda de massa nos compósitos quando comparados somente a amostra GMGL. Dessa forma, os resultados mostram que a adição de NPs pode aumentar a estabilidade térmica da matriz polimérica. A Tabela 7 apresenta os dados relativos às perdas de massa e as temperaturas em que ocorreram os eventos de degradação, bem como a massa residual.
Tabela 7 – Eventos relativos à degradação das amostras NiZn, 0,20NP, 0,14NP, 0,06NP e GMGL
Amostras
1º evento 2° evento 3º evento Massa
residual MR (%) TE (°C) MP (%) TE (°C) MP (%) TE (°C) M
P
(%)
NiZn 100 – 200 8,0 - - - - 92,0
0,20NP 50 – 200 10,41 175 - 700 63,16 - - 20,90
0,14NP 50 – 150 8,963 200 – 500 56,48 500 - 700 15,53 19,02
0,06NP 50 – 100 11,22 80 - 200 17,43 500 - 700 46,32 15,34
GMGL 50 – 150 10,04 150 - 650 75,44 - - 13,45
TE – Temperatura do evento, MP– Perda de massa, MR– Massa residual.
Fonte: Próprio autor.