UNIVERSIDADE
CATÓLICA DE
BRASÍLIA
PRÓ-REITORIA DE PÓS-GRADUAÇÃO E PESQUISA
STRICTO SENSU EM EDUCAÇÃO FÍSICA
Doutorado
EFEITOS DO TREINAMENTO RESISTIDO SOBRE A COMPOSIÇÃO CORPORAL, PERFIL LIPÍDICO, FORÇA E HIPERTROFIA MUSCULAR EM
HIV-SOROPOSITIVOS COM E SEM LIPODISTROFIA
Autor: Ciro José Brito
Orientador: Prof. Dr. Cláudio Olavo de Almeida Córdova
Co-orientador: Dr. Otávio de Toledo Nóbrega
CIRO JOSE BRITO
EFEITOS DO TREINAMENTO RESISTIDO SOBRE A COMPOSIÇÃO CORPORAL, PERFIL LIPÍDICO, FORÇA E HIPERTROFIA MUSCULAR EM
HIV-SOROPOSITIVOS E OU SEM LIPODISTROFIA
Tese apresentada ao Programa de Pós-Graduação Stricto Sensu em Educação Física da Universidade Católica de Brasília (UCB) como requisito parcial para obtenção do título de doutor em Educação Física
Orientador: Dr. Cláudio Olavo de Almeida Córdova Co-orientador: Dr. Otávio de Toledo Nóbrega
Folha de Aprovação
Tese de autoria de Ciro José Brito, intitulada efeitos do treinamento resistido sobre a composição corporal, perfil lipídico, força e hipertrofia muscular em HIV-soropositivos com ou sem lipodistrofia, apresentada como requisito parcial para obtenção do grau de Doutor em Educação Física, no Programa de Pós-Graduação em Atividade Física e Saúde da Universidade Católica de Brasília, em 10 de dezembro de 2010, defendida e aprovada pela banca examinadora abaixo assinada:
__________________________________________________ Prof. Dr. Cláudio Olavo de Almeida Córdova
Orientador – Universidade Católica de Brasília (UCB)
__________________________________________________ Prof. Dr. Otávio de Toledo Nóbrega
Co-orientador – Universidade de Brasília (UnB)
__________________________________________________ Prof. Dr. Jonato Prestes
Membro interno – Universidade Católica de Brasília (UCB)
__________________________________________________ Prof. Dr. Ricardo Moreno
Membro externo – Universidade de Brasília (UnB)
__________________________________________________ Prof. Dr. Francisco Andreotti Prada
DEDICATÓRIA
Dedico este trabalho a memória de minha mãe Rosa Inácio da Silva que tanto me incentivou a seguir nos estudos e sempre desejou em ter um filho doutor.
Ao meu pai Amaury Cesar de Brito pelo incentivo e companhia fiel de todos estes anos.
AGRADECIMENTOS
Ao meu orientador e amigo Cláudio Córdova por sempre me apontar a direção correta.
Ao meu amigo Edmar Lacerda Mendes pela ajuda nos momentos difíceis e amizade ao longo dos anos.
A minha família pelo apoio e incentivo nos estudos.
Ao médico Martinho Menezes pela oportunidade e confiança no meu trabalho.
Aos médicos Fernanda Neves Rosa, Mario Antonio Nogueira e Flávio Faria pelas trocas de conhecimento.
A enfermeira Sonia Albuquerque por sempre acreditar neste projeto.
A professora Nerildes Martins pelo apoio, amizade, carinho, dedicação e paciência.
Aos pacientes que se voluntariam e toda equipe de apoio do Centro de Promoção da Saúde da Cidade de Conselheiro Lafaiete.
Aos professores Sérgio Rodrigues de Paula e Otávio de Toledo Nóbrega pelos conselhos imprescindíveis.
Aos meus amigos na UCB Aparecido Pimentel e Renato Andre pela fiel companhia ao longo dos meus anos no Distrito Federal.
RESUMO
Introdução: a proposta terapêutica “High Active Antiretroviral Therapy” (HAART), terapia
antirretroviral de alta atividade, proporcionou grande aumento na sobrevida de pacientes infectados pelo vírus da imunodeficiência humana (HIV). Entretanto, HIV-soropositivos submetidos à HAART podem desenvolver síndrome lipodistrófica do HIV (SLHIV) que caracteriza-se pela redistribuição da gordura corporal e alterações antropométricas associadas com doenças cardiovasculares, diabetes mellitus tipo 2 entre outras. Por outro lado, o treinamento resistido (TR) é citado como intervenção não-medicamentosa para o controle da glicemia e redução da resistência a insulina e obesidade central. Ademais, não é de nosso conhecimento estudos que tenham controlado a ingestão de macro e micronutrientes a fim de dirimir fatores de confundimento relacionados com a expressão do fenótipo composição corporal em HIV-soropositivos. Objetivo: investigar os efeitos do TR sobre variáveis antropométricas, bioquímicas, imunitárias, força e qualidade de vida em indivíduos HIV-soropositivos com ou sem SLHIV. Materiais e métodos: trata-se de um desenho quase-experimental com pré e pós-testes. Participaram deste estudo 45 soropositivos (39,4±11,0 anos) de ambos os gêneros, os quais foram aleatoriamente alocados em 4 grupos: i) Lipodistrofia mais exercício (LE, n = 12); ii) Ausência de lipodistrofia mais exercício (SLE, n = 11); iii) Lipodistrofia sem exercício (LSE, n = 11); iv) Ausência de lipodistrofia sem exercício (SLSE, n = 11). Os grupos LE e SLE realizaram 3 sessões de exercícios semanais, sendo realizadas 10 repetições a 80% de uma repetição máxima (1RM). Em todas as sessões realizaram-se exercícios de supino, agachamento, pulley costas, mesa flexora, rosca bíceps, tríceps e cadeira extensora. Resultados: observou-se que as medidas de pré-teste sobre as variáveis colesterol total (211,7±24,3 vs. 192,4±25,5 mg/dL), lipoproteína de baixa densidade (131,3±23,2 vs. 119,5±17,1 mg/dL), triglicérides (175,5±50,1 vs. 142,4±33,3 mg/dL), glicemia de jejum (100,7±19,9 vs. 84,4±9,7 mg/dL), gordura subcutânea total (140,6±52,3 vs. 122,5±31,6 cm) e central (111,6±44,9 vs. 82,7±22,9 cm) e circunferência de cintura (90,5±12,7 vs. 78,9±11,5 cm) foram significativamente (P≤0,05) mais elevadas nos grupos
com lipodistrofia (LE e LSE) quando comparados aos demais. No entanto, estas variáveis apresentaram redução significativa (P≤0,05) pós-intervenção no grupo LE sugerindo efeito
protetor do TR na manifestação de co-morbidades associadas ao uso contínuo da HAART. Verificou-se aumento significativo (P≤0,05) na força muscular e área muscular do braço
isenta de massa óssea (AMB) dos grupos LE, SLE, o mesmo não foi observado para os grupos. Ademais, constatou-se melhora significativa (P≤0,05) em todos os indicadores de
qualidade de vida nos grupos LE e SLE, o que não foi observado nos demais grupos. Conclusão: os resultados sugerem que 24 semanas de TR contribuem significativamente para controlar os efeitos adversos do uso continuo da HAART e, provavelmente, reduzem a manifestação destas alterações em pacientes sem redistribuição da gordura corporal.
ABSTRACT
Purpose:The therapeutic proposal Highly Active Antiretroviral Therapy (HAART), provided large increase the survival of patients infected with human the immunodeficiency virus (HIV). However, individuals undergoing therapy (HAART) may develop HIV lipodystrophy syndrome (SLHIV) which is characterized by the redistribution body fat and anthropometric changes associated with diseases cardiovascular disease, type 2 diabetes among others. On the other hand, the resistance training (RT) is quoted as non-medication intervention for glycemic control and reducing insulin resistance and central obesity. Furthermore, it is our knowledge further studies have controlled intake macro and micronutrients in order to remove the confounding related to the phenotypic expression of body composition in HIV-seropositive. Aim: Investigate the effects of variables in TR anthropometric, biochemical, immunological, strength and quality of life in HIV-seropositive individuals with or without SLHIV. Methods: it is a quasi-experimental with pre and post-tests. Participated in this study 45 HIV positive
(39.4 ± 11.0 years) of both sexes, which were randomly allocated into four groups: i) Lipodystrophy which exercise (LE, n = 12), ii) absence of lipodystrophy which exercise (SLE, n = 11), iii) Lipodystrophy without exercise (LSE, n = 11), iv) absence of lipodystrophy without exercise (SLSE, n = 11). The LE and SLE groups held three sessions weekly exercise, being carried out 10 repetitions at 80% of one maximum repetition (1MR). In all sessions were held exercises in supine, squat, lat back, leg curl, biceps, triceps and chair extension. Results: There was that measures of pre-test on variables total cholesterol (211.7 ± 24.3 vs. 192.4 ± 25.5 mg/dL), lipoprotein low density (131.3 ± 23.2 vs. 119.5 ± 17.1 mg/dL), triglycerides (175.5 ± 50.1 vs. 142.4 ± 33.3 mg/dL), fasting glucose (100.7 ± 19.9 vs. 84.4 ± 9.7 mg/dL), total subcutaneous fat (140.6 ± 52.3 vs. 122.5 ± 31.6 cm) and central (111.6 ± 44.9 vs. 82.7 ± 22.9 cm) and waist circumference (90.5 ± 12.7 vs. 78.9 ± 11.5 cm) were significantly (P <0.05) higher in groups with lipodystrophy (LE and LSE) compared to the others. However, these variables A significant reduction (P <0.05) after intervention in group LE suggesting a protective effect of TR in the manifestation of co-morbidities associated with continuous use of HAART. There was a significant increase (P <0.05) in force muscle and Bone-free upper arm muscle area (AMA) group LE SLE, the same was not true for the groups. Moreover, there was improvement significant (P <0.05) in all indicators of quality of life in groups LE and SLE, which was not observed in other groups. Conclusion: The results suggest that 24 weeks of RT significantly contribute to control adverse effects of the continued use of HAART and probably reduce manifestation of these abnormalities in patients without fat redistribution body.
LISTA DE FIGURAS
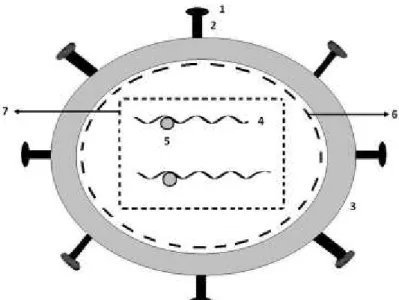
Figura 1. Estrutura física do HIV.
Figura 2. O ciclo de replicação do HIV-1.
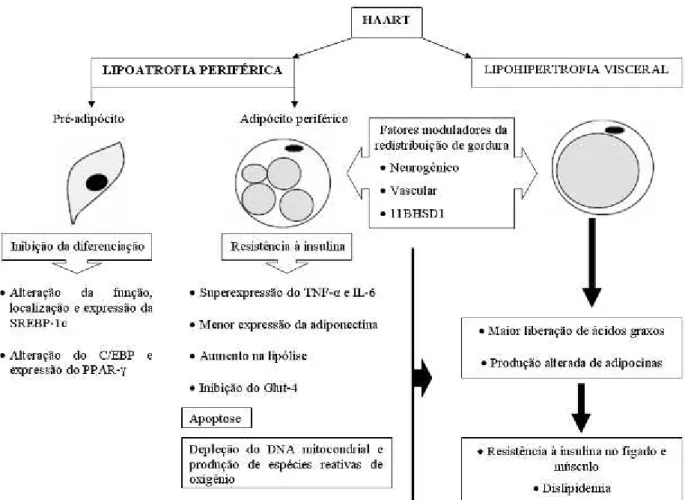
Figura 3. Modelo patofisiológico para a Síndrome Lipodistrófica do HIV.
Figura 4. Diagrama de seleção de amostra-montagem dos grupos. Figura 5. Topografia da gordura para os grupos LE, SLE, LSE, SLSE.
LISTA DE TABELAS
Tabela 1. Medicamentos recomendados pela Organização Mundial de Saúde.
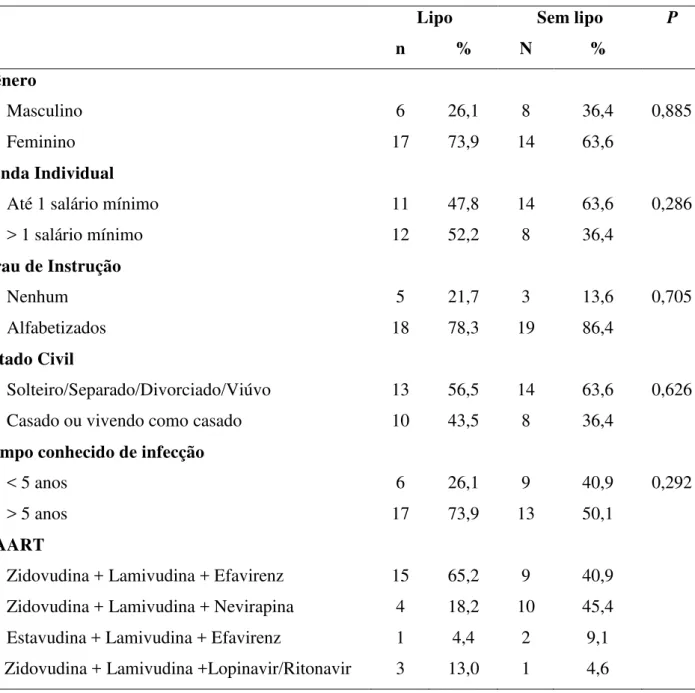
Tabela 2. Distribuição da amostra em valores absolutos e percentuais segundo características sócio-demográficas e epidemiológicas.
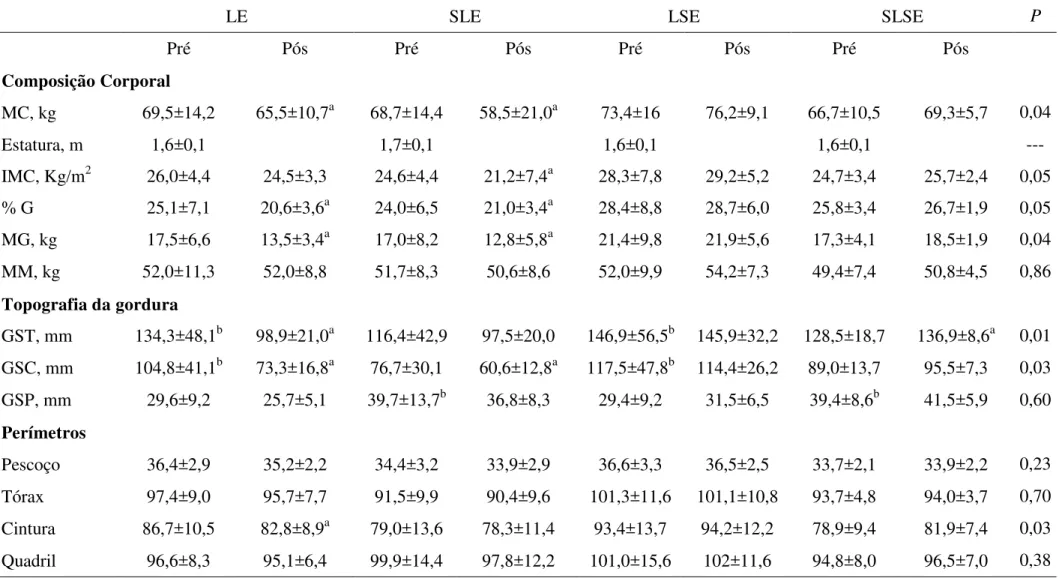
Tabela 3. Valores de linha de base e após 24 semanas para os grupos LE, SLE, LSE, SLSE nas variáveis relativas à composição corporal e antropometria.
Tabela 4. Valores de linha de base e após 24 semanas para os grupos LE, SLE, LSE, SLSE nas variáveis relativas ao perfil lipídico, glicemia de jejum e as variáveis hemodinâmicas.
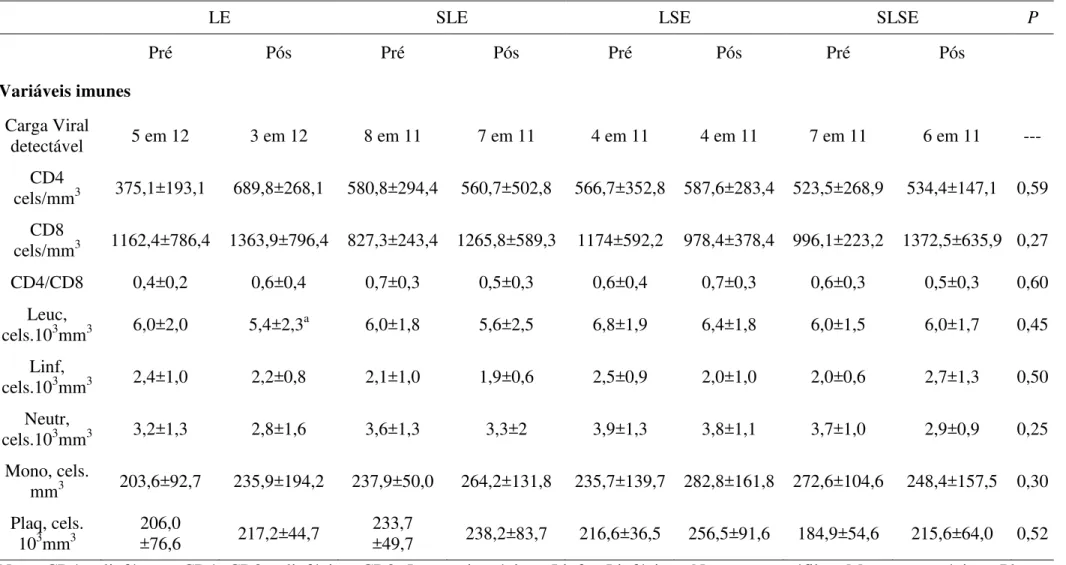
Tabela 5. Valores de linha de base e após 24 semanas para os grupos LE, SLE, LSE, SLSE nas variáveis relativas à imunidade.
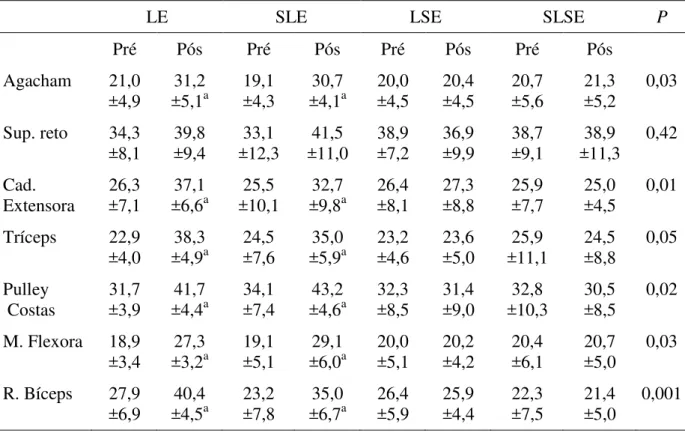
Tabela 6. Valores de linha de base e após 24 semanas para as medidas de força muscular em Kgs.
LISTA DE ABREVIAÇÕES %G – percentual de gordura;
11 HSD1 – 11- -Hidroxiesteroide hidrogenase Tipo I;
3TC – lamivudina; ABC – abacavir;
ACC – acetil CoA carboxilase;
ACSM – American College Sports Medicine; Agacham – agachamento;
AMB – área muscular do braço isenta de massa óssea; AMP-c – adenosina monofosfato cíclico;
AZT – zidovudina; Cad – cadeira;
CC – circunferência de cintura;
CPS – Centro de Promoção da Saúde; CT – colesterol total;
d4T – estavudina; Ddl – didanosida;
DMO – densidade mineral óssea; DOM1 – domínio físico;
DOM2 – domínio psicológico;
DOM3 – domínio nível de independência; DOM4 – domínio relações sociais; DOM5 – domínio meio ambiente; DOM6 – domínio espiritualidade; EFV – efavirenz;
GSC – gordura subcutânea central; GSP – gordura subcutânea periférica; GST – gordura subcutânea total; HDL – lipoproteína de alta densidade;
HDL – lipoproteína de alta densidade;
HIV – vírus da imunodeficiência humana; IDV – idinavir;
IL-6 – interleucina-6;
IMC – Índice de Massa Corporal; IP – inibidores de protease;
IPAQ – questionário internacional de atividade física;
IR – resistência a insulina;
LDL – lipoproteína de baixa densidade;
LE – presença de lipodistrofia com exercício;
Leuc – leucócitos; Linf – linfócitos;
LPV/r – lopinavir/ritonavir;
LSE – presença de lipodistrofia sem exercício;
M – mesa;
MG – massa corporal gorda; MM – massa corporal magra; Neutr – neutrófilos;
NFV – nelfinavir; NVP – Nevirapina;
OMS – Organização Mundial de Saúde;
PAS – pressão arterial sistólica;
Plaq – plaquetas;
PPAR- – receptor- proliferador ativado de peroxissoma; QV – Qualidade de vida;
R – rosca;
RM – repetição máxima; RNA – ácido ribonucléico; RPM – rotações por minuto; RTV – ritonavir;
SIV – vírus da imunodeficiência em símios;
SLE – ausência de lipodistrofia com exercício;
SLHIV – síndrome lipodistrófica do HIV;
SLSE – ausência de lipodistrofia sem exercício;
SQV – saquinavir; Sup – supino;
SUS – Sistema Único de Saúde;
TCLE – termo de consentimento livre e esclarecido;
TG – triglicerídeos;
TNF-α – fator de necrose tumoral-α;
TR – treinamento resistido;
Trigl – triglicérides;
UCB – Universidade Católica de Brasília;
SUMÁRIO
1 INTRODUÇÃO 15
2 OBJETIVOS 17
2.1 Objetivo geral 17
2.2 Objetivos específicos 17
3 REVISÃO DE LITERATURA 18
3.1 A epidemiologia da infecção pelo vírus HIV no Brasil 18
3.2 Características estruturais do HIV, mecanismos de infecção e evolução da doença 19
3.3 Impacto da infecção do vírus HIV na saúde 23
3.4 A terapia antirretroviral de alta atividade 25
3.5 Efeitos adversos da terapia antirretroviral fortemente ativa 27
3.6 Patofisiologia da lipodistrofia 30
3.7 Influência da atividade física na saúde e qualidade de vida de HIV-soro-positivos 33
3.8 O treinamento resistido 36
3.9 Importância do treinamento resistido para HIV-soro-positivos 39
4 MATERIAIS E MÉTODOS 41
4.1 Casuística 41
4.2 Protocolo de treinamento resistido 43
4.3 Definições conceituais e operacionais para as variáveis do estudo 44
4.3.1 Medidasantropométricas 44
4.3.2 Medidas bioquímicas 45
4.3.3 Indicadores de qualidade de vida 46
4.3.4 Variáveis hemodinâmicas 46
4.3.5 Controle nutricional 47
5 RESULTADOS 49
6 DISCUSSÃO 58
7 CONCLUSÃO 63
8 REFERÊNCIAS BIBLIOGRÁFICAS 64
9 ANEXOS 82
9.1 Comprovante de submissão de manuscrito à Revista Brasileira de Ciência e Movimento 82
9.2 Comprovante de submissão do estudo de caso ao Journal of Medical Case Report 83
9.3 Comprovante de submissão de manuscrito original à Revista Clinics 86
9.4 Comprovante de submissão de manuscrito original à Revista Motriz 88
9.5 Versão resumida do questionário de qualidade de vida da Organização Mundial de
Saúde – WHOQoL-HIV (versão resumida) 89
9.6 Recordatório alimentar habitual 92
9.7 Folha de aprovação do Comitê de Ética em Pesquisa 93
9.8 Carta de apresentação e Termo de Consentimento Livre e Esclarecido. 94
9.9 Fotos relativas ao treinamento resistido em soropositivos no Centro de Promoção da
1 INTRODUÇÃO
O vírus da imunodeficiência humana (HIV) está presente em todos os continentes,
com maior prevalência de infecção na África subsaariana, onde alcança status de pandemia.
De acordo com os dados apresentados pela Organização Mundial da Saúde, há um milhão e
meio de soropositivos na América Latina, dos quais seiscentos mil são brasileiros. No ano de
2007, ocorreram cerca de cem mil infecções e aproximadamente cinqüenta e oito mil mortes
na América Latina associadas à infecção pelo HIV (UNAIDS, 2008). Estas estatísticas
demonstram a importância em se estabelecer programas de tratamento desta epidemia.
A terapia antirretroviralde alta atividade (HAART) tem proporcionado melhora na
qualidade de vida e aumento na sobrevida aos soropositivos mediante supressão do HIV
(COUZIGOUet al., 2007). Entretanto, tem sido reportado que soro-positivos submetidos a
esta terapia podem desenvolver síndrome lipodistrófica por infecção pelo HIV (SLHIV)
(DELL'ISOLAet al., 2006; DUONG et al., 2006). A SLHIV é reconhecida como efeito
adverso associado a todos inibidores de protease em terapia de longa duração (DUONGet al.,
2006). Outra categoria de drogas associada ao tratamento, definida como inibidores de
transcriptase reversa (ITR), relaciona-se também às alterações lipodistrotóficas do tipo
lipoatrofia (DELL'ISOLAet al., 2006) e toxicidade mitocondrial, contribuindo negativamente
para a elevação da acidose lática (KOHLER; LEWIS, 2007).
A SLHIV caracteriza-se pelo aumento da gordura visceral, presença de gibosidade
dorsal, ginecomastia e aumento da mama em mulheres, perda da gordura subcutânea da face e
das extremidades (TERRY et al., 2006). Carr et al. (1998) descreveram com detalhes a
associação entre antirretrovirais e lipodistrofia, resistência à insulina, problemas hepáticos
(ARENAS-PINTO et al., 2003), dislipidemia, hipertensão arterial (ROBINSON et al., 2007)
Outra indesejável alteração decorrente da infecção pelo HIV consiste na progressiva
redução da massa corporal magra (MM) (MACERA, 2007), que por sua vez associa-se à
redução da capacidade do sistema músculo-esquelético em gerar força (O'BRIENet al., 2004).
Uma vez que a HAART per se não exibe aumento da MM em portadores de HIV (CADEet
al., 2007), novas metodologias devem ser empregadas com o propósito de elucidar
prescrições acuradas de TR visando efeitos positivos na constituição da MM e ganho de força
em pacientes HIV-soropositivos (SATTLER et al., 2002; SOUZA et al., 2008).
Resultados de estudos têm sugerido a inserção de exercícios físicos aeróbios
(ROBINSON et al., 2007) e anaeróbios (LINDEGAARD et al., 2008; SAKKAS et al., 2009)
como terapia auxiliar ao tratamento da infecção pelo HIV (ROBINSONet al., 2007), uma vez
que estes minimizam os efeitos adversos das terapias tradicionais (GRINSPOONet al., 2000).
Nesta perspectiva, torna-se importante a adoção de estratégias que beneficiem a qualidade de
vida destes indivíduos (BARRIOS et al., 2002). Embora diversos estudos tenham investigado
a influência do exercício na saúde e qualidade de vida de pacientes soropositivos, a literatura
tem sugerido limitações como, ausência de grupo controle (SOUZA et al., 2008), amostras
pequenas (RØGE et al., 2002; SOUZA et al., 2008) e reduzido período de intervenção
(LINDEGAARD et al., 2008; SAKKAS et al., 2009). Ademais, não é de nosso conhecimento
trabalhos que realizaram prescrição nutricional em soropositivos submetidos à atividade
física. É importante ressaltar que aspectos nutricionais devem ser considerados para a
verificação dos efeitos do TR sobre a síntese de proteínas e reconstituição do glicogênio
2 OBJETIVOS
2.1 Objetivo geral
Verificar os efeitos de 24 semanas de treinamento resistido (TR) sobre o perfil lipídico, resposta imunitária, níveis de força, composição corporal e qualidade de vida em pacientes soropositivos com ou sem lipodistrofia.
2.2 Objetivos específicos
Realizar um levantamento do perfil sócio-demográfico e composição corporal em pacientes soro-positivos com ou sem lipodistrofia atendidos pelo centro de promoção da saúde da cidade de Conselheiro Lafaiete.
Verificar o efeito do TR de alta intensidade nas seguintes variáveis:
Concentrações plasmáticas de triglicérides, colesterol total, lipoproteína de alta densidade, lipoproteína de baixa densidade e glicemia de jejum;
Pressão arterial sistólica, diastólica e frequência cardíaca de repouso;
Percentual de gordura, massa corporal, massa corporal gorda, massa corporal magra, gordura subcutânea total, periférica e central;
Força muscular e área muscular do braço direito isenta de massa óssea.
Contagem global e sub-populações leucocitárias, assim como, carga viral e;
3 REVISÃO DE LITERATURA
O referencial teórico do presente trabalho foi escrito por meio de revisão bibliográfica
com as palavras ―AIDS‖, ―HIV e exercise‖, ―HIV e variability”, “HIV epidemiology”,
―pathophysiology e HIV‖, ―HAART‖, ―HAART e exercise‖ nas seguintes bases de dados em
saúde: MEDLINE (base de dados de literatura internacional, produzida pela US National
Library of Medicine – NLM), LILACS (Literatura Latino-Americana y del Caribe en
Ciencias de la Salud), SciELO (Scientific Electronic Library Online), Periódicos da Capes,
além de sites da Internet e livros da área.
3.1 A epidemiologia da infecção pelo HIV no Brasil
O vírus da imunodeficiência humana (HIV), disseminado em todo o mundo, é o agente
responsável pela síndrome da imunodeficiência adquirida (AIDS). A exata origem do vírus e
o início de sua infecção na humanidade ainda são desconhecidos. No entanto, acredita-se que
tenha evoluído da contaminação por seres humanos a partir do vírus da imunodeficiência em
símios (SIV). Povos africanos apresentavam o costume de caçar e se alimentar de macacos.
Além disso, geograficamente, a disseminação dos HIV e SIV é semelhante (PINTO e
SCHINEIDER, 2006).
Ao contrário de muitos países da África subsaariana, que possuem infecção do tipo
generalizada, no Brasil a prevalência de infecção é concentrada. De acordo com dados
publicados pela Organização das Nações Unidas (ONU), no ano de 2007, estima-se que o
Brasil apresente cerca de 600 mil infectados, dos quais 180 mil utilizam antirretrovirais.
Apesar das campanhas de prevenção, 30 mil novos casos são registrados a cada ano, sendo
No último relatório da ONU o Brasil foi elogiado por estratégias de prevenção e
tratamento da epidemia de AIDS (UNAIDS, 2008). Segundo Brito et al. (2000), a propagação
da infecção no Brasil apresenta caráter multidimensional. Inicialmente, observou-se maior
prevalência em homossexuais. Atualmente, a relação sexual desprotegida entre homens é
responsável por 50% das infecções por HIV no Brasil (DOURADO et al., 2006). No entanto,
verificaram-se alterações nas classes de transmissão, com maior incidência entre
heterossexuais e mulheres. De acordo com dados publicados em 2005, a epidemia cresceu
nove vezes entre as mulheres jovens ou casadas com relacionamento estável, sem
comportamento de risco, e que contraíram o vírus do parceiro (AMARO, 2005). Por outro
lado, a transmissão vertical (mãe para filho) reduziu para 4%. E, por drogas injetáveis,
declinou em cidades onde foram realizadas campanhas de conscientização (UNAIDS, 2008).
3.2 Características estruturais do HIV, mecanismos de infecção e evolução da doença
O HIV é um membro do gênero Lentivirus da família Retroviridae e compreende os
sorotipos HIV-1 e HIV-2 (YAMAMOTO et al., 2006), sendo o HIV-1 o principal responsável
pela pandemia mundial (PINTO e SCHINEIDER, 2006). Ambos os sorotipos possuem
proteínas estruturais em genoma de RNA protegido pelo envelope viral. O envelope viral é
constituído de proteína complexa denominada env. A proteína env possui glicoproteínas
importantes para a infecção como a gp41 e gp120. No interior do HIV evidencia-se uma
proteína matriz (p17), que circunda o capsídio, composto pela proteína p24. A p24 guarda a
estrutura mais importante do vírus como a transcriptase reversa (p51), a protease (p11) e a
Figura 1. Estrutura física do HIV: 1. gp120, 2. gp41, 3. bicamada lipídica, 4. RNA, 5. transcriptase reversa, 6. p17, 7. p24.
O HIV possui notável capacidade de mutação e se adaptação às novas condições
ambientais. Uma grande incidência de erros ao nível transcricional do genoma resulta em
alterações nas bases genéticas durante o ciclo replicativo (Figura 2), sendo que a elevada
variabilidade genômica do HIV apresenta importantes implicações para o diagnóstico,
tratamento e prevenção, bem como nas investigações epidemiológicas (DAN CRISTEA et al.,
2005). Por exemplo, as glicoproteínas de superfície podem apresentar variação gênica
próximo a 10% em um paciente e de 50% em grupos, o que dificulta o desenvolvimento de
vacinas (RAMBAUT et al., 2004). Até o presente momento, uma vacina desenvolvida por
pesquisadores brasileiros e franceses parece a mais promissora na eliminação do vírus,
Figura 2. O ciclo de replicação do HIV-1. A infecção produtiva inicia com a adsorção viral à célula e suas interações com os receptores clusterofdifferentiation (CD) 4 (passo 1). No caso
do HIV, a entrada viral (passo 2) se dá por um processo independente de Ph que ocorre seguindo a fusão das membranas viral e celular e resulta na descapsidação viral (passo 3). A transcrição reversa ocorre dentro da partícula subviral no citoplasma da célula infectada (passos 4 e 5). O produto DNA fita-dupla é transportado ao núcleo (passo 5) onde integração ao DNA genômico (passo 7) é mediado pela integrase que é codificada pelo vírus, um componente pertencente ao complexo de pré-integração subviral. O DNA viral integrado serve como um molde para o DNA dependente de RNA polimerase (Pol II) e coordena a produção de mRNAs que são traduzidas em proteínas virais no citoplasma das células infectadas (passos 8-11). O envelope e as poliproteínas Gag e Gag/Pol (passo 12) são transportadas por vias independentes em direção à membrana plasmática, onde a progênie da partícula viral inicia o brotamento (passo13) a partir da célula infectada e são lançadas como partículas imaturas (passo 14). A subsequente proteólise pela protease, enzima codificada pelo vírus, gera partículas maturas (passo 15) contendo um núcleo condensado característico.
Do início da infecção, ao surgimento da AIDS, até os estágios finais da doença (AIDS
wasting) o vírus passa por diversas mutações no organismo (FOUCHIER et al., 2002).
Atualmente existem 3 grupos de classificação do HIV-1: majoritário (M), outros (O) e novos
(N). O grupo M possui os subtipos A1, A2, B, C, D, F1, F2, G, H, J e K. Além destes, existem
16 formas recombinantes como a número 2 (CRF02_AG) e número 1 (CRF01_AE)
(OSAMANOV et al., 2000). O HIV-1 possui, aproximadamente, 10000 pares de base (pb). A
presença de diferentes RNA recombinantes, no envelope viral, é que determina a resistência
Os subtipos virais apresentam diferentes características quando se trata da
manifestação da doença. Em relação à capacidade de infecção, as variantes B, C e CRF01_AE
são as mais efetivas (ESSEX, 1999). No tocante à evolução da doença, o subtipo D
desenvolve mais rapidamente a AIDS quando comparado ao subtipo A (KALEEBU et al.,
2001), enquanto o subtipo C possui menor capacidade de se replicar dentro do linfócito CD4
(BALL et al., 2003). Em relação à distribuição geográfica destes subtipos, o subtipo C é o
mais prevalente, mundialmente; o B, na Europa e Brasil. Ademais, o subtipo F (em pequena
proporção) e o subtipo C são muito encontrados na região Sul do Brasil (BRIGIDO, 2009;
DIAS et al., 2009).
A infecção pelo HIV é caracterizada por uma fase aguda e um período de latência. A
infecção aguda é transitória (entre uma e quatro semanas de duração). Os sintomas
observados são febre alta por um ou dois dias, suores, linfadenomegalia transitória,
esplenomegalia, fadiga, falta de apetite, depressão, úlceras na pele, boca e genitais (NIU et al.,
1993). O monitoramento destes sintomas é importante, uma vez que o indivíduo pode infectar
outras pessoas, sem saber se é soropositivo (MINISTÉRIO DA SAÚDE, 2008).
O período de latência é aquele no qual a doença vai se desenvolvendo. Este dura, em
média, 10 anos e culmina com o aparecimento da AIDS (BACHETTI e MOSS, 1989).
Durante esta fase, enquanto a contagem de células CD4 estiver acima de 350 cel./mm3, as
infecções mais bacterianas, como tuberculose, por exemplo, na medida em que a doença
progredir, podem ocasionar outros sintomas como: febre baixa, sudorese noturna, fadiga,
diarréia crônica, cefaléia, alterações neurológicas, pneumonia, sinusite, bronquites, diarreia
crônica e leucoplasia oral pilosa.
Ademais, a AIDS é caracterizada pela instalação de doenças oportunistas como
pneumonia, toxoplasmose do sistema nervoso central, tuberculose pulmonar, meningite
nao-Hodgkin e câncer de colo do útero) e danos a outros órgãos e tecidos (miocardiopatia,
nefropatia e neuropatias) (MINISTÉRIO Da SAÚDE, 2008). O estágio final da doença (AIDS
wasting) é caracterizado por rápida redução da massa corporal (>10%), diarréia e fadiga
crônicas e febre documentada (≥ γ0 dias intermitentes ou constantes) na ausência de doenças
concorrentes (CDC, 1987).
3.3 Impacto da infecção do vírus HIV na saúde
O Centro de controle de doenças dos Estados Unidos elegeu uma série de indicadores
da severidade da infecção denominada wasting, ou seja, perda de peso superior a 10%
associada à diarréia ou fadiga crônicas e febre documentada por um período igual ou superior
a 30 dias intermitente ou constante na ausência de doenças concorrentes (CDC, 1987). Na
medida em que se eleva a carga viral e reduz a concentração de células CD4 e CD8, o
indivíduo tende a manifestar sintomas da imunodeficiência. Além dos sintomas acima,
descritos no tópico anterior, a imunodeficiência diminui as resistências orgânicas,
aumentando as chances de infecções oportunistas.
Estas são assim denominadas porque, dificilmente, afetam pessoas saudáveis, mas em
um sistema imunitário comprometido, pode ser letal. Dentre as principais infecções
oportunistas, destacam-se: candidíase, citomegalovirose, meningite, criptocose, hepatites B e
C, herpes, pneumonia, sarcoma de karposi, toxoplasmose e tuberculose (MINISTÉRIO DA
SAÚDE, 2003).
A tuberculose é a principal infecção oportunista que acomete pacientes soropositivos,
aproximadamente 1,4 milhões de pessoas no mundo, sendo que 40% estão na África
subsaariana (RAVGLIONE et al., 2005). Antiretrovirais e medicamentos tuberculostáticos
A infecção do HIV limita a extração/utilização do O2 na musculatura periférica por
reduzir a atividade de enzimas oxidativas (CADE et al., 2003; DUONG et al., 2007). A
menor capacidade de utilização do oxigênio,advinda da toxicidade mitocondrial, afeta
diretamente a aptidão física, e consequentemente, a disposição do individuo à realização de
atividades cotidianas, pois a dificuldade em utilização do oxigênio pelas células musculares e
hepáticas resulta em aumento da produção de acido lático no repouso, causando acidose lática
(níveis de lactato <5mmol/L), em casos mais graves hiperlactacidemia (acúmulo de lactato
≥5mmol/L).
A acidose lática esta associada a todos os tipos de antirretrovirais, em especial, os ITR,
pois, esta classe de medicamento interfere diretamente na atividade do DNA mitocondrial
(TOLOMEO et al., 2003). Apesar da baixa prevalência (entre 9 a 16% dos pacientes
submetidos à HAART) (ARENAS-PINTO et al., 2003) a acidose lática é gravíssima, pois
resulta em maior propensão à fadiga no repouso e menor aptidão física (TOLOMEO et al.,
2003). A incapacidade do individuo em realizar atividades físicas pode concorrer com o
desenvolvimento da depressão(LIMA et al., 2007), cujos sintomas estão associados à alta
mortalidade em portadores de HIV.
HIV-soropositivos estão mais propensos a infecções no trato gastrintestinal (TGI).
Segundo Hill e Balkin (2009), as adversidadesTGI mais frequentes em HIV-soropositivos
incluem diarreia, náusea, vômito, disfagia, perda de massa corporal, dores abdominais,
sangramento e tumores como sarcoma de Kaposi e linfoma não-Hodkin. Possivelmente, as
infecções e doenças no TGIestão associadas àdepleção na concentração linfócitos CD4 no
intestino decorrentes da progressão da doença (Aproximadamente 60% dos linfócitos
intestinais são CD4). Esta redução na concentração de linfócitos aumentam as chances de
avium. Ademais a infecção pelo HIV reduzas concentrações de bactérias benéficas à saúde
intestinal como lactobacilos e bífidobactérias (HILL e BALKIN, 2009).
O menor número de linfócitos CD4 está associado à infecção pelo HIV e ao dano
oxidativo no timo. Em soropositivos, é menor a quantidade de receptores para a formação de
linfócitos e de pré-linfócitos T (CD34+) que chegam ao estágio final da maturação
(GOUGEON. 2003). A interferência do estresse oxidativo no timo é danosa para a saúde do
paciente soropositivo, pois a grande quantidade de linfócitos CD4 infectada deve ser
eliminada por linfócitos citolíticos (CD8). Portanto, a manutenção das concentrações de CD4
fica afetada, uma vez que a reposição no timo apresenta-se reduzida.
A infecção pelo HIV também aumenta a concentração de algumas citocinas
pró-inflamatórias como o fator de necrose turomal-α (TNF-α). A elevada produção de TNF- α
torna o ambiente mais propícioa replicação viral dentro do CD4 através da ativação do fator
nuclear κ-B (MAHLKNECHT et al., 2000).
3.4 A terapia antirretroviral de alta atividade – HAART
Ao final da década de 80, adotou-se a monoterapia (Zidovudina – AZT) para
tratamento da infecção pelo HIV, porém, o efeito não era duradouro. Atualmente, a
monoterapia é utilizada com o propósito de impedir a transmissão vertical do HIV
(MINISTÉRIO DA SAÚDE, 2003). A partir de 1995, adotou-se o uso de combinado de
medicamentos inibidores de transcriptase reversa análogos de nucleotídeos (INTR). Apesar de
evoluir em relação à monoterapia, os efeitos também eram breves. Posteriormente, o
tratamento evoluiu para a terapia com 3 medicamentos, de duas classes distintas, denominada
HAART (COUZIGOU et al., 2007).
Embora a cura da AIDS esteja distante, a HAART é o tratamento mais eficiente para a
transcriptase reversa não-análogos de nucleotídeos (INNTR) e inibidores de protease (IP). A
Tabela 1 apresenta exemplos de medicamentos recomendados pela OMS.
Tabela 1. Medicamentos recomendados pela OMS.
INTR INNTR Inibidores de Protease
Zidovudina (AZT) Nevirapina (NVP) Saquinavir (SQV) Didanosina (ddl) Efavirenz (EFV) Ritonavir (RTV)
Estavudina (d4T) Indinavir (IDV)
Lamivudina (3TC) Nelfinavir (NFV)
Abacavir (ABC) Lopnavir/ritonavir (LPV/r)
Nota. INTR – inibidores de transcriptase reversa análogos de nucleotídeos, INNTR–
inibidores de transcriptase reversa não-análogos de nucleotídeos (INTR). Fonte: Ministério da Saúde (2003).
Os ITR’s são os medicamentos mais utilizados na HAART, sendo recomendados
como terapia inicial 2 INTR e 1 INNTR (AZT + 3TC + EFV) (MINISTÉRIO DA SAÚDE,
2008). Embora os propósitos sejam os mesmos, estes medicamentos possuem mecanismos de
ação diferenciados. Os INTR’s incorporam a cadeia de DNA a ser transcrita e impedem a
cópia do RNA viral; já os INNTR afetam diretamente a atividade da enzima transcriptase
reversa.
Anterior à prescrição da HAART, o médico deve avaliar o estado imunológico do
paciente. Neste sentido, o linfócito CD4 é o principal marcador, iniciando-se o tratamento
quando as concentrações deste estão entre 200 e 350 células/mm3. No entanto, devem-se realizar exames adicionais, pois a contagem de células pode reduzir, independente da infecção
pelo vírus. Quando a contagem de CD4 não está disponível, a medicação pode ser prescrita se
o paciente apresentar contagem de linfócitos inferior a 1.200 células/mm3. A carga viral é outro bom indicador, uma vez que estando elevada (acima de 100.000 copias/mL) pode
da AIDS, a HAART deve ter início, independente da contagem de CD4, linfócitos, ou carga
viral (MINISTÉRIO DA SAÚDE, 2008).
Além dos ITR’s e IP’s, outros dois medicamentos podem ser utilizados para controle
da infecção, como é o caso dos inibidores de fusão, que impedem que o vírus infecte o
linfócito CD4. Esta terapia é muito utilizada para impedir a transmissão vertical do HIV. No
entanto, é uma droga de alto custo, elevada toxicidade e de administração intramuscular, o
que dificulta a adesão ao tratamento (BRENNAN-BENSON et al., 2006). Os inibidores de
integrase impedem que a integrase viral insira o DNA vírus no DNA hospedeiro. É uma boa
terapia, pois bloqueia o surgimento de vírus mais resistentes. Pois, assim como os inibidores
de fusão, é uma droga de custo elevado. Caso este medicamento venha ser utilizado,
cotidianamente, por pacientes que serão atendidos pelo SUS, o governo terá que investir mais
de mil dólares paciente/dia (MINISTÉRIO DA SAÚDE, 2008).
3.5 Efeitos adversos da HAART
Sem dúvida, a HAART representa um avanço em termos de tratamento para o
soropositivo (HACKER et al., 2007). Chen et al. (2007) lançaram um trabalho revisando 10
anos da HAART. Os autores destacam a eficiência dessa terapia em reduzir a carga viral e
aumentar a concentração de linfócitos CD4, o que reduz a morbidade e mortalidade. No
entanto, efeitos adversos são observados pelo uso da HAART por longo período, dentre eles a
SLHIV.A SLHIV compreende a lipoatrofia periférica e lipohipertrofia visceral (BAUER et
al., 2004, HACKER et al., 2007).
Esta pode ser caracterizara pelo aumento da gordura visceral, presença de gibosidade
dorsal (acúmulo de gordura na região cervical), ginecomastia masculina e aumento da mama
em mulheres, perda da gordura subcutânea da face e das extremidades (TERRY et al.,
cardiovasculares e dislipidemia (CARR et al., 1999; TERRY et al., 2006). Segundo Fève et
al. (2004), apesar do aumento na sobrevida e melhora da qualidade de vida, os efeitos
colaterais contribuem para a baixa aderência ao tratamento. Na tentativa de reduzir os efeitos
adversos da HAART, Van Wljk et al. (2005) observaram que o uso concomitante dos
hipoglicemiantes orais roseglitazona e metformina reduz o estoque de gordura visceral,
melhora o perfil lipídico sanguíneo, a função endotelial e reduz a lipoatrofia periférica.
O primeiro estudo a detectar a redistribuição de gordura corporal, em paciente
infectado por HIV, associada à terapia antirretroviral foi publicado na literatura especializada
em 1997 (HENGEL et al., 1997). Um ano após, Carr et al. (1998) descreveram, em detalhes,
a associação entre a terapia e a síndrome da lipodistrofia periférica, RI, dislipidemia,
hipertensão arterial (ROBBINSON et al., 2007) e, consequentemente, maior risco de doença
cardiovascular (FISCHER et al., 2006). Um dos estudos mais representativos sobre alterações
orgânicas resultantes da SLHIV foi desenvolvido por Grunfield et al. (2006), que
investigaram 1183 soropositivos por 4 anos. Os resultados deste estudo revelaram que a
SLHIV expõe o paciente a risco cardiovascular similar àquele observado em tabagistas. Nesta
linha, outro estudo populacional, com 23468 voluntários, evidenciou que, a cada ano de
exposição à HAART, há aumento em até 1,26 vezes para o risco de infarto do miocárdio
independente de outros fatores (FRIIS-MØLLER et al., 2003).
A SLHIV tem sido associada a todos IP’s, particularmente à combinação terapêutica
envolvendo estavudina, efavirenz, ritonavir e saquinavir em terapia de longa duração
(DUONG et al., 2006). Outra abordagem associada ao tratamento da infecção, baseada em
inibidores de transcriptase reversa análogo de nucleosídeos (IsTRN), está relacionada a
alterações lipodistrotóficas do tipo lipoatrofia (DELL'ISOLA et al., 2006) e toxicidade
Há associação direta entre a infecção pelo HIV, doenças oportunistas, HAART e
menor atividade mitocondrial nas células (DE LA ASSUNCIÓN et al.; 2004). Opii et al.
(2007) demonstraram que o uso contínuo dos medicamentos reduz a concentração de DNA
polimerase- , enzima responsável pela replicação das mitocôndrias. De La Assunción et al.
(2004) verificaram associação entre o uso do AZT, aumento da peroxidação lipídica e radicais
livres. O dano causado a cada indivíduo depende do tipo de célula afetada (uma célula
muscular resulta em perda de massa magra e redução do gasto energético).
Dentre os antirretrovirais, os IP’s são aqueles que causam maior perturbação na
homeostasia da glicose (GEMINARIO et al., 2000). Van Vonderen et al. (2009) verificaram
que a combinação zidovudina+lamivudina+Lopinavir/Ritonavir (1 INTR, 1 INNTR e 1 IP)
produz maior resistência à insulina periférica e aumenta a lipólise basal quando comparado
nevirapina+ Lopinavir/Ritonavir (1 INNTR e 1 IP). Além disso, a segunda combinação
medicamentosa melhora a sensibilidade à insulina hepática. A reduzida produção de
adiponectina, pelo tecido adiposo, resulta em aumento da RI e arteriosclerose. Minami et al.
(2009) verificaram que o tipo de antirretroviral interfere na produção de adiponectina e, de
acordo com este estudo, o efavirenz e o ritonavir reduziram a liberação de adiponectina pelo
tecido adiposo. Em 88 pacientes utilizando INNTR e acompanhados por 24 meses, Zannou et
al. (2009) verificaram que 8% desenvolveram diabetes, 35% hipercolesterolemia e 13%
desenvolveram síndrome metabólica.
A osteopenia e consequente osteoporose também são complicações metabólicas
associadas ao uso da HAART, sendo a cabeça do fêmur a parte mais comprometida (HUANG
et al., 2001). Sugere-se que a redução da densidade mineral óssea (DMO) esteja relacionada
com a degeneração da matriz mineral óssea (TEBAS et al., 2000). Carr et al. (2001)
verificaram em seu estudo que a osteopenia foi prevalente em 22% de uma amostra de
infecção pelo HIV, associada à HAART, reduz a DMO em mulheres de meia-idade. Em um
estudo com 214 voluntários (79% homens), divididos em dois grupos (uso intermitente do
antirretroviral e uso contínuo), Grund et al. (2009) observaram que o uso contínuo do
antirretroviral está diretamente associado à redução da DMO.
Em curto prazo, os antirretrovirais reduzem a incidência de infecções no TGI, no
entanto, longo período de exposição da HAART, principalmente dos IP’s, apresentam efeito
contrário (BRAGA NETO et al., 2010). Neste sentido, dados de estudos indicaram que
aproximadamente 60% dos indivíduos que utilizam IP’s são acometidos de diarreia. Os
mecanismos associados a estes efeitos colaterais foram vagamente elucidados. Estudos in
vitro indicaram que os IP’s reduzem a resistência transepitelial, afetam o balanço de minerais
importantes para o equilíbrio osmolítico intestinal como o cálcio e cloro e induzem a massiva
apoptose tecidual (BRAGA NETO et al., β010). Já os ITR’s induzem a menor perturbação GI,
sendo observados apenas casos de náuseas e vômitos (HILL e BALKIN, 2009).
3.6 Patofisiologia da lipodistrofia
Em duas coortes prospectivas, observou-se que a prevalência da SLHIV situa-se entre
20% (GALLI et al., 2002) e 84% (CARR et al.; 1999). Os fatores que determinam o
desenvolvimento da SLHIV ainda não foram completamente esclarecidos. Entretanto
postula-se que postula-sejam de ordem multifatorial, ou postula-seja, o próprio vírus, a constituição genética do
indivíduo, o tipo de medicamento utilizado e fatores que controlam os estoques de gordura
corporal como a RI, leptina e dieta (FÈVE et al., 2004).
Conforme descrito, a SLHIV é um efeito adverso associado a todos os antirretrovirais
e entender os mecanismos pelos quais a HAART causa a SLHIV pode auxiliar na elaboração
de novos medicamentos. Deve-se ressaltar, no entanto, que a HAART é uma intervenção
Para se entender tais mecanismos deve-se, primeiramente, conhecer a fisiologia do
tecido adiposo. Os adipócitos são células de origem mesodérmica oriundas de várias
linhagens adipoblásticas. Resumidamente, possuem três funções: síntese e acúmulo de
triglicerídeos através da ação das enzimas acetil-CoA carboxilase (ACC) e ácido graxo
sintetase (FAS); hidrolisar triglicerídeos em ácidos graxos e glicerol pelo estímulo das
catecolaminas e adenosina monofosfato cíclico (AMP-c) e liberar adipocinas como leptina,
fator de necrose tumoral-α (TNF-α), interleucina-6 (IL-6), resistina e adiponectina. O
desempenho correto das funções do adipócito depende de uma série de transcrições. Três
tipos de enzimas regulam as atividades dos adipócitos: esterol regulatório ligante da
proteína-1c (SREBP-proteína-1c), receptor- proliferador ativado de peroxissoma (PPAR- ) e CCAAT/proteína
ativadora (C/EBP) (FÈVE et al.,2004).
Embora os IP’s estejam fortemente associados ao desenvolvimento da SLHIV, os
ITRN’s e ITRNN’s também promovem alterações na composição corporal e metabolismo.
Resultados de estudos in vitro evidenciaram vários mecanismos pelos quais estes tipos de
medicamentos podem levar à SLHIV. As linhagens mais utilizadas em estudos com HIV são
os pré-adipócitos 3T3-L1 e 3T3-F442A(FÈVE et al.,2004).
Um dos prováveis mecanismos pelos quais os IP’s e ITRN’s levam à redistribuição da
gordura está no desempenho anormal de células adiposas. Possivelmente a inibição do
SREBP-1c seja o alvo dos IP’s, uma vez que foram observadas baixas concentrações de
RNAm SREBP-1c em soropositivos tratados com este medicamento (BASTARD et al.,
2002). Ademais, os IP´s reduzem a forma natural dos SREBP-1c (DOWELL et al., 2000) e
sua capacidade de transcrição (MISEREZ et al., 2002). Apenas dois estudos verificaram
redução na expressão do PPAR- e da C/EBP associado ao uso dos IP’s (DOWELL et al.,
Em relação aos ITRN’s, poucos estudos foram realizados e as respostas não são
consistentes. Por exemplo, Brinkman et al. (1999) hipotetizaram que os INTR’s reduzem o
DNA mitocondrial (mtDNA). Possivelmente, a depleção do mtDNA resultaria na lipoatrofia
periférica. No entanto, estes efeitos adversos são observados pelo uso crônico do
medicamento (FÈVE et al., 2004). Já os INNTR’s foram associados ao aumento nos níveis de
LDL e desregulação da atividade do SREBP-1c (HADRI et al., 2004).
Outro distúrbio no tecido adiposo associado à HAART é a necrose do tecido adiposo
subcutâneo, possivelmente associado ao aumento na produção de TNF-α e IL-6 nas células
adiposas (BASTARD, 2004). Este processo é responsável pelo surgimento da lipoatrofia
periférica. É curioso, porém, o comportamento antagônico entre o tecido adiposo periférico
(lipoatrofia) e visceral (lipohipertrofia). Fliers et al. (2003) propuseram que a lipoatrofia
periférica é uma neuropatia autonômica. O sistema nervoso autônomo pode estar associado ao
antagonismo funcional dos tecidos adiposos periférico e central, uma vez que atividade
simpática ativa a lipólise e a parassimpática o anabolismo (KREIER et al., 2002). Cabe
ressaltar também que o tecido adiposo visceral é mais vascularizado; neste sentido, o tecido
adiposo subcutâneo está mais propenso à hipoxia quando comparado ao visceral (FÈVE et al.,
2004).
Abordando o metabolismo da glicose em soropositivos, Hadigan et al. (2001)
observaram que 35% dos pacientes com SLHIV apresentavam RI. No entanto, não se pode
afirmar que a SLHIV esteja associada ao desenvolvimento do diabetes. Sabe-seque os IP’s
podem gerar RI, independente da presença de SLHIV (NOOR et al., 2002), e o indinavir inibe
a expressão do Glut4 (BEN-ROMANO et al., 2004). Possivelmente, a RI seja resultado da
alteração na produção de citocinas. Em soropositivos, foi observado o aumento das adipocinas
TNF-α, IL-6 e menor liberação de adiponectina. Sugere-se ainda, que o aumento na liberação
(11-HSD1), enzima importante para a atividade do cortisol. Portanto, quanto maior a liberação
de 11- HSD1, maior a liberação de ácidos graxos livres na corrente sanguínea e,
consequentemente, maior RI (FÈVE et al., 2004). Um modelo teórico que ilustra as possíveis
vias metabólicas associadas à patofisiologia SLHIV é apresentado na Figura 3.
Figura 3. Modelo patofisiológico para a Síndrome lipodistrófica do HIV.
3.7 Influência da atividade física na saúde e qualidade de vida de soropositivos
Não se sabe ao certo a associação entre a lipodistrofia e propensão à aterosclerose.
(MOOSER et al., 2006), embora estudos mais recentes indiquem associação direta entre as
duas (MAGGI et al., 2006; LORENZ et al., 2007). Jiang et al. (2007) verificaram que a
HAART induz à disfunção mitocondrial o que leva a concomitante aumento de espécies
mitocondrial pode ser um importante fator culminante da disfunção endotelial devido ao
aumento nas concentrações plasmáticas de radicais livres (APOSTOLOVA etal., 2010).
Neste contexto, sugere-se que, a prática de exercícios seja benéfica para o paciente
soropositivo que utiliza HAART. Veljkovic et al. (2009) observaram que a atividade aeróbia
aumenta a expressão do peptídeo NTM1, responsável pela apoptose do HIV. Assim, o
exercício torna-se importante estratégia não-medicamentosa para o tratamento. Quanto maior
a resistência orgânica ao vírus, maior o período que o paciente permanecerá sem iniciar a
HAART, evitando assim, as co-morbidades e toxidades associadas à terapia.
Entretanto, períodos breves de exercício (8-12 semanas) não influenciam a carga viral
e a contagem de CD4, tanto exercícios de natureza anaeróbia (ROUBENOFF et al., 1999a)
quanto aeróbia (SMITH et al., 2001). Neste sentido, faz-se necessária a adoção da prática
regular de longa duração, a fim de se observar alterações importantes em variáveis associadas
à saúde e qualidade de vida (QV)de soropositivos, dentre elas MM, Densidade Mineral Óssea
e perfil lipídico. Segundo Ciccolo et al. (2004), a HAART transformou a infecção pelo HIV
em uma doença crônica e, deste modo, programas de exercício devem ser incorporados ao
tratamento desta população.
O aumento da gordura central decorrente da HAART aumenta o risco para o
desenvolvimento de doenças cardiovasculares (DE SAINT MARTINet al., 2006). Por outro
lado, não é recente a prescrição de exercícioscomo tratamento não medicamentoso para a
prevenção de cardiopatias (SHIMADA et al., 2007). É provável que o exercício atenue a
lipodistrofia, pois a atividade física de caráter aeróbio resultou maior expressão da proteína
SREBP-1c (IKEDA etal., 2002). De Saint Martin et al. (2006) recomendam que um programa
de prevenção de doenças cardiovasculares deva fazer parte do tratamento de portadores de
HIV. Cabe ressaltar que a eficiência do tratamento só poderá ser alcançada com a adoção de
meses de exercício aeróbio, não foi observada redução no colesterol total. Além disso,
observou-se aumento significativo do nível de triglicerídeos.
Um dos fatores que contribuem para o agravo da doença reside no afastamento do
portador do HIV de suas atividades cotidianas (ROBENOFF, 2000b). Sendo assim, a inserção
em um programa de atividade física melhora a QV do portador de HIV nos campos físico,
psicológico e social. Em um estudo envolvendo suplementação protéica (whey protein) e
treinamento resistido para ganho de massa muscular em portadores de HIV, Agin et al. (2001)
observaram que, embora tenha acorrido aumento de massa muscular em ambos os grupos,
evidenciaram-se alterações significativas na QV apenas para o grupo exercitado. Da mesma
forma, em 12 semanas de treinamento resistido ou aeróbio foram observadas melhoras na
sensação de bem-estar (LOX et al., 1995), na auto-estima (LOX et al., 1996) e redução dos
sintomas relativos ao estresse (LOX et al., 1995).
Investigando a influência da dieta e do exercício na QV de mulheres obesas portadoras
de HIV, Engelson et al. (2006) verificaram que a implementação de um programa de
treinamento e controle dietético por 12 semanas reduziu a adiposidade subcutânea e visceral.
No entanto, apesar da redução da massa corporal, melhora na força, aptidão física e QV não
se observaram alterações benéficas em variáveis metabólicas relativas ao risco de diabetes e
doenças cardiovasculares. Em outro estudo, com a mesma duração, observou-se redução dos
sintomas de depressão (NEIDIG et al., 2003).
Utilizando o questionário de QV da Organização Mundial de Saúde para pacientes
soropositivos (WHO-QoL-HIV), Mutimura et al. (2008a) observaram que, após seis meses,
houve melhoras nos domínios relacionados à independência, relações sociais, auto-estima e
imagem corporal em pacientes com SLHIV. Cabe ressaltar, no entanto, que nem todos os
estudos com exercício em soropositivos resultaram em melhora na QV. Terry et al. (1999)
de exercício aeróbio de moderada (55 a 60% do VO2máx) e alta intensidade (75 a 85% do
VO2máx). Outro estudo utilizando as mesmas intensidades de atividade aeróbia não observou
melhora nos índices de QV de pacientes soropositivos (MACARTHUR et al., 1993).
3.8 O treinamento resistido
O treinamento resistido (TR) é uma das modalidades de atividade física recomendadas
para a melhora da aptidão física. Dentre os principais benefícios do TR para a saúde e
desempenho esportivo, sugere-se o aumento da massa muscular/óssea (BAKER et al., 2006;
BURD etal., 2010; JOVINE et al., 2006; KEMPER et al., 2009), taxa metabólica basal
(BAKER et al., 2006; BURD et al., 2010), força máxima (JOVINE et al., 2006; LINNAMO,
2005), resistência de força (DE AZEVEDO et al., 2007), flexibilidade (VALE et al., 2006),
redução da gordura corporal total (DE AZEVEDO et al., 2007; STRASSER e
SCHORBERBERGER, 2011), gordura central (STRASSER e SCHORBERBERGER, 2011)
e contribui para o desenvolvimento de um perfil benéfico de mediadores inflamatórios
(CALLE e FERNANDEZ, 2010).
Diversos estudos observaram efeitos positivos do TR para melhora do desempenho
esportivo (CHANDLER e BROWN, 2009; LINNAMO, 2005; AAGAARD e ANDERSEN,
2010). Por exemplo, os efeitos ergogênicos do TR na impulsão vertical, horizontal e
velocidade de sprint (PETERSON et al., 2006), resistência de corredores de longa distância
(AAGAARD e ANDERSEN, 2010), desempenho de nadadores (BREED e YOUNG, 2003) e
jogadores de handebol (HERMASSI et al., 2010). Ademais, os benefícios do TR foram
observados na saúde e qualidade de vida (CONTE et al., 2009; CALLE e FERNANDEZ,
2010), bem como no controle de doenças crônicas não-transmissíveis como o diabetes tipo II
2006; KEMPER et al., 2009) hipertensão arterial (KURU et al., 2009) e obesidade
(STRASSER e SCHORBERBERGER, 2011).
Quanto ao planejamento do programa de treinamento, a anamnese deve informar o
profissional de educação física sobre a condição física e eventuais limitações do aluno. Neste
sentido, questões relacionadas ao número de articulações envolvidas no exercício, séries,
freqüência semanal, intervalo, número de repetições e carga devem ser previamente definidos.
De acordo com o AmericanCollegeofSportsMedicine exercícios multiarticulares devem iniciar
a sessão, uma vez que proporcionam menor fadiga localizada (KRAEMER et al., 2002).
Quanto à ordem dos exercícios, Chandler e Brown (2009) recomendam a alternância de
exercícios para membros superiores/inferiores e quando possível alternar entre agonistas e
antagonistas.
O volume de treinamentopode ser manipulado pelo número de séries pelas repetições e
quantidade de carga(CHANDLER e BROWN, 2009). No entanto, dependendo da ênfase, o
programa de TR pode proporcionar diferentes adaptações fisiológicas. Por exemplo, em
estudo com 32 sedentários, Campos et al. (2002) observaram que o treinamento com elevado
número de repetições proporciona ganho na resistência muscular, quando comparado ao
treinamento com moderadas e baixas repetições. Por outro lado, o treinamento com baixas
repetições foi mais eficiente que o de elevadas repetições em aumentar a força máxima (1RM)
e hipertrofiar. Em oposição, o estudo recente de Burd et al., (2010) sugerem que o
treinamento com elevadas repetições é mais eficiente para induzir a hipertrofia quando
comparado ao treinamento com baixas repetições e carga elevada (90% de 1RM até a fadiga).
Em relação à frequência de treinamento, os estudos têm sido consensuais em afirmar
que, para um mesmo volume de treinamento, a maior frequência tem se mostrado mais
eficiente para ganhos de força e hipertrofia (KRAEMER et al., 2002). Neste sentido, Kelly et
realizou-se treinamento isovolumétrico em três sessões semanais quando comparado a sessão
única. Segundo Chandler e Brown (2009) além de melhorar o desempenho, o maior número
de sessões semanais permite a realização de maior número de combinações de exercícios por
grupo muscular.
Quanto à velocidade de execução, o treinamento superlento (5 segundos para a fase
concêntrica e 5 segundos para a excêntrica) tende a resultar em menores ganhos de força
quando comparado com execuções mais rápidas (2 a 5 segundos para a realização das duas
fases do exercício). Hatfield et al. (2006) observaram em 9 homens treinados que o
treinamento superlento comparado a velocidade auto-sugerida produz menor força absoluta e
potência muscular. Em contrapartida, Pereira e Gomes (2007) não observaram diferenças
entre o treinamento superlento e rápido em aparelho isocinético.
Para o intervalo entre séries, García-López et al. (2007) evidenciaram que o intervalo
não interfere na resistência muscular. Entretanto, o intervalo de curta duração (1minuto) é
mais vantajoso do que o longo intervalo (4 minutos) por resultar em maior quantidade de
repetições até a fadiga e manutenção da velocidade de execução. Após seis meses de
treinamento, Ahtiainen et al. (2005) não observaram diferença significativa na força máxima
quando compararam o treinamento de curto intervalo (2 minutos) e longo intervalo (5
minutos). Por outro lado, o intervalo longo resultou em maior força isométrica. Bottaro et al.
(2009) observaram que o intervalo de curta duração (30 segundos) libera maior quantidade de
hormônio do crescimento quando comparado aos intervalos de 60 e 120 segundos. Já
Robinson et al. (1995) observaram maior força absoluta (1RM) no grupo que realizou
intervalo mais longo (180 segundos) quando comparados aos grupos que realizaram intervalo
3.9 Importância do treinamento resistido para soropositivos
O treinamento resistido pode prevenir ou tratar a sarcopenia, promover a hipertrofia
muscular e, consequentemente, a MM em portadores de HIV (ROBINSON et al.,
2007).Ademais, atenua os efeitos adversos em variáveis metabólicas em portadores de HIV
submetidos à terapia anabólica pelo uso concomitante de testosterona e exercício
(GRINSPOON et al., 2000). Boop et al. (2003) sugeriram que o programa de treinamento
deve ser iniciado com atividades aeróbias de acordo com a capacidade funcional do paciente.
De acordo com Mooney e Vergel (2009), o ganho de massa muscular associado ao
treinamento resistido, auxilia no controle de triglicérides plasmáticos de pacientes
soropositivos. Já Roubenoff (2000) observou que o treinamento resistido reduz a gordura
visceral. Terryet al. (2006) observaram em 30 pacientes lipodistróficos e dislipidêmicos que
12 semanas de treinamento resistido resultaram em redução da massa corporal total,
percentual de gordura e relação cintura-quadril. Os resultados não revelaram alterações na
imunidade.
Segundo o consenso do American College of Sports Medicine(ACSM), a variação de
carga do treino (volume e intensidade) deve ser estabelecida de acordo com o nível de aptidão
física do indivíduo. Para iniciantes, recomendam-se mais repetições e menos carga (8-12
repetições máximas – RM); intermediários e avançados, menos repetições e mais carga (1-6
RM). Em relação ao período mínimo de treino, seis a sete semanas são recomendadas para a
observação dos efeitos hipertróficos (ACSM, 2009). Nesse sentido, Roubenoff et al. (1999a)
verificaram que oito semanas de treinamento resistido progressivo elevaram a massa magra e
a força em pacientes portadores de HIV. Resultado similar foi observado em 16 semanas
utilizando o treinamento concorrente dividido em 20 minutos de exercício aeróbio e uma hora
Dentre os principais benefícios do treinamento resistido, pode-se citar o aumento da
massa magra e densidade mineral óssea (KRAEMER et al., 2002). Neste sentido, é altamente
recomendada a inserção do treinamento resistido no tratamento do HIV, pois homens
soropositivos tendem a apresentar redução da densidade mineral óssea e baixa massa corporal
(CARR et al., 2001). Uma vez que a sarcopenia está diretamente associada à progressão da
doença, a combinação de estratégias envolvendo nutrição e atividade física parece surtir
4 MATERIAIS E MÉTODOS
4.1 Casuística
Trata-se de uma amostra de conveniência constituída por portadores de HIV/AIDS
registrados no Centro de Promoção da Saúde (CPS) da cidade de Conselheiro Lafaiete – MG
– Brasil e submetidos à HAART por no mínimo 1 ano (n=150). Do total, 64 pacientes não
desejaram participar do estudo. Ademais, foram excluídos aqueles que não completaram as
etapas previstas ou desejaram abandonar o estudo (n = 4); apresentaram antecedentes de
hipertensão (n = 4); doenças cardíacas ou diabetes (n = 2); fumantes, consumidores de
bebidas alcoólicas ou de fármacos de ação diurética (n = 13); sob tratamento com corticóides,
esteróides anabolizantes ou hormônio do crescimento (n = 2); presença de doenças
oportunistas (infecções ou tumores) nos três meses que antecederam o experimento (n = 5); e
que realizaram alguma cirurgia como liposucção ou lipoescultura seis meses antes do
experimento (n = 1). Portanto, a amostra foi constituída por 45 pacientes.
O estudo foi previamente aprovado pelo comitê de ética para pesquisas em seres
humanos da Universidade Federal de Viçosa – MG, em acordo com a declaração de Helsinki
(protocolo 052/2008). Os voluntários foram informados sobre os objetivos do estudo e
assinaram um termo de consentimento livre e esclarecido. Todos os voluntários mantiveram a
HAART seguindo recomendações médicas e foram monitorados por médicos, nutricionista e
profissional de educação física durante a investigação. Para determinação de presença de
lipodistrofia, adotou-se a metodologia descrita por Lichtenstein et al. (2001).
Os critérios antropométricos para determinação da lipodistrofia validados por
Lichtenstein et al. (2001) graduam as alterações corporais associadas a SLHIV por meio de
escalas do tipo Likert. As avaliações consideram medidas subjetivas (reportada pelo paciente)
e objetivas (exame médico). Os sinais para lipoatrofia periférica ou lipohipertrofia central são