UNIVERSIDADE
FEDERAL
DE SANTA
CATARINA
Programa
de
Pós-Graduação
em
Engenharia Ambiental
Departamento
de
Engenharia
Sanitária eAmbiental
GILBERTO
N
ICOLAI
AVALIAÇÃO
DAs
CONCENTRAÇÓES
DE NITRATos
NA
ÁGUA
SUBTERRÂNEA
Do
MUNIci1>Io
DE
CHAPECÓ
-
sc
- Dissertação apresentada à Universidade
Federal de Santa Catarina, para obtenção
do
título de Mestreem
EngenhariaAmbiental.
Orientador: Prof. Dr.
Henry
Xavier CorseuilAVALIAÇÃO
DAS CONCENTIIAÇÕES DE NITRATO
NA
ÁGUA
SUBTERRÃNEA
DO
MUNICIPIO
DE
CHAPECO
-
sc.
GILBERTO
NICOLAI
Dissertação submetida ao corpo docente
do Programa
dePós
-Graduação
em
EngenhariaAmbiental da Universidade Federal de Santa Catarina
como
parte dos requisitos necessários para obtençãodo
grau deMESTRE
EM
ENGENHARIA AMBIENTAL
na
Área
de Tecnologias deSaneamento
AmbientalAprovado
por:fifl
lProf. Pa `o Belli Filho, Dr.
PrO`í.`.§I~acir Dalmagro, Dr
Í I
/
I- Í
V
PÍOÍÍ Henry Xavier Corseuil, Dr./,
(Orientador)
Prof. Flávio Rubens Lapolli, Dr.
(Coordenador)
FLORIANÓPOLIS,
sc -
BRASIL
Não
é
o
desafio
com
que
nos
deparamos
que
determina
quem
somos
eo
que
estamos nos
tornando,
mas
a maneira
com
que respondemos ao
desafio,
somos
combatentes
idealistas,mas
plenamente
conscientes,pois
0
terconsciência
não
nos obriga
a
termos
teoria:só
nos obriga
a
sermos
conscientes.Problemas
para
vencer,liberdade
para
provar,
e,enquanto acreditarmos
em
nosso
sonho,
nada
é
por
acaso.
AGRADECIIVIEN
TOS
Gostaria de estender
meus
agradecimentos a todas as pessoas envolvidas direta eindiretamente neste trabalho e
em
especial:Ao
prof.Hemy
Corseuil, pela oportunidade queme
concedeu
de ingressarno
mestrado, e suas orientações seguras durante o transcorrer da pesquisa.
Ao
Sr.Mariano
Smaniotto, pessoa a qual devo muito.Sua
dedicação e incentivonos
momentos
mais necessários, foram excencias para a conclusão desse trabalho.Não
tenho palavras para expressar omeu
agradecimento.Ao
SrChico
fimcionário daLeão
poços, que conheceChapecó
como
poucos, pelagrande auxilio
na
coletado
material.A
Marilde,Marcio
e Alexandredo
REMAS,
pela paciência, incentivo, e o grandeauxílio na recepção e análise das amostras
Aos
colegas, Clarice, Viviane, Cleide,Decio
e Adaiane, pela amizade, e palavras deincentivo neste dois anos
do
cursoAo
amigo
José Carlos Kroth, obrigado.Ao
amigo Moacir Wagner,
pela ajudana
elaboraçãodo
trabalho, pelacompanhia
eamizade.
Aos meus
irmãos Dario, Elton e Dirson,sem
a ajuda, compreensão, apoio moral e financeiro, não seria possível a realizaçãodo
curso de mestrado. VAos meus
pais, quemesmo
não
estando mais conosco, tenho a certeza queme
SUMÁRIO
LISTA
DE
FIGURAS
... ..LISTA
DE
TABELAS
... ..RESUMO
... ..ABSTRACT
... ..1.0
n×ITRoDUÇÃo
... ..1.1
O
Oestedo
Estado de Santa Catarina-Visão
Geral1.2
O
município deChapecó
... ..2. O
REVISÃO
BIBLIOGRÁFICA
... ..2.1
ONitrogênio
... ..2.2
O
Ciclodo
Nitrogênio ... ..2.3
Nimficaçâo
.... ... ..2.3.1 Fatores que afetam a nitrificação ... ..
2.3.2 Efeitos da nitrificação ... ..
2.4 Nitrato ... ... ..
2.4.1 Nitrato
na
água subterrânea ... ..2.5 Fontes potenciais de nitrato na água subterrânea .... ..
2.5.1 Dejetos de suínos ... ..'
... _.
2.5.2
Saneamento
in situ ... ..2.5.3 Fertilizantes agrícolas ... ..
2.6
Doenças
causadas pela ingestão de nitratos ... ..372.6.1
Metahemoglobina
... ..372.6.2 Carcinogênese ... ..40
2.7 Tratamento para eliminação de Nitratos., ... .. 41
3.0
MATERIAIS
E
MÉTODOS...
... ..443.1 Geologia ... ..
44
3.2 Procedimento para seleção e coleta das amostras de água ... ..46
3.3 Analise ... ..
47
3.4 ' Localização dos poços
-
interior ... .. 503.5 Localização dos poços
-
zona urbana ... ..534.0
RESULTADOS
E DISCUSSÃO
... ..564.1 Resultados
da
águana zona
rural ... ..574.2 Resultados dos poços
na
zona urbana ... .. 594.3 Nitrito ... .. 61
4.4 Nitrato ... ..62
5.0
coNcLUsÕEs
E
RECOMENDAÇÕES
... ..vo
6.0
REFERÊNCLAS
BIBLIOGRÁFICAS
... ._ 73z
LISTA
DE
FIGURAS
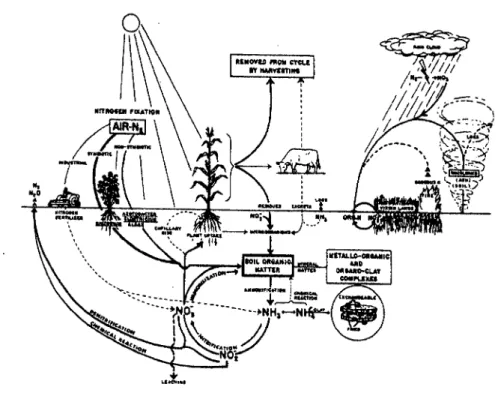
Figura 1
O
ciclodo
Nitrogêniodo
Solo(STEVENSON,
1982IN
ELDOR
&
CLARK,
1996 ... ._ 1 1
Figura 2
O
Ciclo Biológicodo
Nitrogênio(POSTGATE,
1987) ... .. 12Figura 3
O
Ciclodo
Nitrogênio(LEHNINGER,
1991) ... ..l3 Figura 4A
Reciclagem do
Nitrogênio da Biosfera(LEHNIN
GER,
1991) ... .. 16Figura 5 Fontes e Trajetórias
do
Nitrogêniona
Subsuperñcie(ALLAN,
1979) ... ..24Figura 6 Perfil esquemático ilustrando as zonas dos diferentes compostos nitrogenados
na
pluma
... ..33Figura 7
Comportamento
dapluma
contaminanteno
período de seca ... ..34Figura 8
Comportamento
dapluma
contaminanteno
período dechuva
... ..34Figura 9
Mapa
geológicodo
Brasil ... ..44Figura 10
Mapa
do
Brasil e Santa Catarina indicando a localizaçãodo
município deChapecó
... ..46Figura 11
Esquema
ilustrativoda
perfuração deum
poço
artesiano e localonde
as coletasforam
realizadas ... ..49Figura 12
Modelo
de cromatógrafo iônicomarca
DIONEX
~
DX
120 utilizado nas análises das amostras de água ... ..48Figura 13
Mapa
do
município deChapecó
com
a localização dos poços coletados nazona
ruraldo
município ... ..52ii
Figura 15
Gráfico
de resultadosdo
cromatógrafoiônico
DIONEX
-
DX
120... ..56
Figura 16
Gráfico
demonstrativo de poçoscom
NO3
-
N
e sua distribuição de acordo
com
as concentrações-
zona
urbana... ..63
Figura 17
Gráfico
demonstrativo de poçoscom N03-N
na zona
rural e sua distribuiçãode acordo
com
as suas concentrações... ..64
Figura 18
Gráfico
demonstrativo-
cidade e interior-
e suas respectivas
concentrações
... ..65
Figura 19
Gráfico
de resultados das análises zona urbana... ..66
Figura
20 Gráfico
de resultados das análiseszona rural ... ..66
Figura 21
Gráfico
comparativo entre as análises de 1998e
2000
...Tabela l
Tabela 2
Tabela3
Tabela 4
Tabela 5
LISTA
DE TABELAS
Principais
Organismos
Envolvidosno
Processo de Nitrificação(PAUL E
CLARK,
1996) ... ..18Localização e profundidade dos poços coletados na zona rural
do
Município deChapecó
... ..50Localização e profimdidade dos poços coletados
na zona
urbanado
município deChapecó
... ..53Demonstrativo de resultados obtidos para nitrito e nitrato nas análises
da
água de poços artesianosna zona
ruraldo
município deChapecó
... ..57RESUMO
O
nitrato é o poluente mais freqüente nas águas subterrâneas.Em
concentraçõessuperiores a 10 mg/l
NO3_N,
pode
causarmetahemoglobina
e câncer.Além
do
uso defertilizantes agrícolas e criação de animais, os sistemas de saneamento in situ, quer por
tanques sépticos
ou
fossas sedimentares, constituem importantes fontes de nitrato naságuas subterrâneas.
No
presente trabalho procurou-se avaliar a concentração de nitratose nitritos
na
água subterrâneado
município de Chapecó, oestedo
Estado de SantaCatarina, através da coleta e análise de 100 amostras de água provenientes de poços
situados
no
interior ena zona
urbana.Os
resultadosmostraram
quedo
total de poços 19apresentaram nitrito.
Desse
total 13 poços estão situadosna
zona urbana e 6no
interior,sendo que apenas
um
apresentou valoracima do
permitido pela legislação (1 mg/1N02-
N).
O
aspectoem comum
é a profundidade, todoscom
mais de 100 metros, situadosem
todas as regiõesdo
município.Com
relação ao nitrato apenasum
não
apresentou concentração.Do
total de poços nazona
urbana (52 poços) amostrascom
até 1 mg/1NO3"N
foram
30 (57,69%).De
1 até 2 mg/1NO3_`N
12 poços (23,07%), e poçoscom
níveis
acima
de 2 mg/1 10 (19,23%).Nenhum
poço
ultrapassou omáximo
exigido porlei para o nitrato na zona urbana.
No
interior (44 poços analisados) poçoscom
até 1mg/1
NO3_N
totalizaram 33 (75%), poçoscom
1 a 2 mg/1NO3"N
10 (22.72%), e poçoscom
niveisacima
de 2 mg/l l (2.27%).Na
zona rural, aexemplo da zona
urbana,nenhum
poço
excedeu omáximo
exigido por lei. Pode-se observar que a maioria dospoços, tanto da zona rural
como
urbana ainda não atingiu 1 mg/1NO3_N. Os
níveis denitrato são baixo
na
maioria deles,mas
esta denunciandouma
poluição,que
tende a seagravar.
As
práticas agrícolas, o aproveitamentoou
não aproveitamentoadequado
dedejetos de suínos e aves, a aglomeração de pessoas
com
sistema deficiente de captação etratamento de esgoto, são as causas principais da poluição desse manancial.
Os
valorescorrespondentes à zona urbana são maiores e mais freqüentes devido a falta de
um
sistema de captação e tratamento de esgoto, que na fala deste é
armazenado
em
fossasnegras
ou
sépticas. Para o interior o afastamento das fontes poluidoras (chiqueiros etc.)ABSTRACT
Nitrate is the
more
frequent pollutant in the underground waters. Inconcentrations
up
to 10 mg/lN03'
-N
can causemetahemoglobina
and cancer. Besidesthe use of agricultural fertilizers
and
creation of animals, the system of sanitation in situ,by
septic tanks or sedimentary sewages, are important sources of nitrate in theunderground waters. This
work
tries to evaluate the concentrationsof
nitretesand
nitritos in the underground water of the city of Chapeco, west of the state of Santa
Catarina,
by
collectingand
analysing 100 samples of water extractedfrom
wells int the country sideand
in the urban área.The
resultsshowed
that 10 wells presented nitrito, 13of
those placed in the urban áreaand
6 in the countryside,and
just one presented valueup
to the allowedby
the legislation (1 mg/1N02-N).
The
aspect incommon
is the depht, all withmore
than 100 meters, located in all área of the city. Related to nitrate,just onewell didn”t present concentration.
Of
the total of well int the urban área (52 wells)sample
withup
to 1 mg/1NO;-N
ware 30
(57,69%).Of
up
to 2 mg/lNO;-N
12 wells(23,07%),
and
wells vvith levels above 2 mg/1 10 (19,23%).No
well crossed themaximum
demanded
by law
for the nitrate in the urban área. ln the countryside (44analyzed wells) wells with
up
to 1 mg/lNO3-N
were
33 (75%), wells with l to 2 mg/lNO;-N
10 (22,72%),and
wells with levels above 2 mg/l l (2,27%). In the rural área,just like the urban área,
no
well exceded themaximum
demanded
by
law. It can beobserved that
most
of the wells, in all the city, the concentration still didn”t reach l mg/lNO;-N. The
levels of nitrate arelow
inmost
of them,but they areshowing
pollution,that tends to
become
worse.The
agricultural practices, the appropriated or vvrong use ofdejections of swine
and
birds, the gathering of peoples with deficient system receptionand
sewer treatment, are themain
causes ofthe pollution.The
valuesconespondig
tothe urban área are larger
and
more
frequent due to the absence of a reception systemand
sewer treatment, thatinthe speech of this is stored at black or septics sewages. In the
coimtryside the removal of the pollutant sources (pigsties etc.)
makes
possible a better1-INTRoDUÇÃo
A
água
como
um
bem
econômico
eum
recurso finito e vulnerável, essencialpara a sustentação da vida, requer
uma
gestão efetiva através de ações integradas eparticipativas que protejam os ecossistemas naturais, e ao
mesmo
tempo
propiciem odesenvolvimento social e econômico,
com
a proteção dos ecossistemas naturais.A
história mostra que
sempre
existiuum
dominador
eum
dominado. Estamesma
históriaconta
que
países que possuíamuma
agricultura fortesempre
dominavam
ou
atéexterminavam
os seus adversários, por não teremuma
agricultura compatível.Na
nossahistória mais recente, os grandes dominadores
do
nossomundo
foram
o Egito,Roma,
Grécia, Turquia e, nos últimos séculos, França, Inglaterra, Rússia,
Alemanha. Hoje
é osEstados Unidos.
Nos
próximos 30
anos, odominador do
mundo
seráquem
tiverágua
potável.
A
água
cobre a maior partedo
planeta,porém
tunapequena
parcela dessa águapode
e é utilizada paraconsumo humano
e animal.A
distribuição dela é deforma
desigual,
ñcando
a maior parteno
oceanos.A
água doce
disponível encontra-se nascalotas polares, lençóis subterrâneos, rios e lagos.
De
acordocom
ABRÃO,
2000, aágua cobre
75%
do
globo terrestre,com
Luna carga de 1,4 bilhão deKm3,
dessa águatotal,
97,3%
estão nos oceanos.2,7%
de água doce assim distribuidos:79%
nas calotaspolares e geleiras,
20,64%
são água subterrâneas, e0,33%
de água doce superficial.Desta água,
temos
53% em
rios e lagos,38%
deumidade do
solo,8%
de vaporatmosférico e
1%
de água nos organismos vivos.O
Brasil possui24%
da
água líquidado mundo. Dessa
água66%
estão nas bacias hidrográficas da região amazônica,onde
vive
5%
da
população brasileira.V
SANTA CATARINA
(1997).
O
estado de Santa catarina possui, atualmente,L:
água no
estado,vem
apresentadouma
aumento
constanteem
ftmção de diversosfatores.
Além
do
crescimento vegetativoda
população, cerca de1,5%
a.a.,na
últimadécada
em
Santa Catarina,há
de se considerartambém
oaumento
decorrentedo
maiorconsumo
per cápita da população, fato quetem
como
principal causa a concentraçãoda
população urbana
no
período.Da
mesma
forma, a elevação da atividade industrialno
estado e 0
emprego
de novas tecnologias na agricultura (uso de irrigação por exemplo)contribuíram significativamente para o
aumento
total da demanda.As
água superficiaisem
Santa Catarinaconforme
estudosdo
mesmo
diagnosticogeral
SANTA CATARINA
(1997) (p. 81) estão contaminadas. Para a região oesteespecificamente “as águas tanto superficiais quanto subterrâneas, apresentam-se
deterioradas pelo uso intenso de agrotóxicos, pelo processo de erosão dos solos e
principalmente pela concentração e
manejo
inadequado de dejetos de suínos.”De
acordo
com
levantamentos feitos pelaFundação do
Meio
Ambiente
-
FATMA
-na
década de 1980 a região apresentava
230
atividades empresariais, das quais 138 foramconsideradas poluidoras (hospital, pocilgas, madeireiras, abatedouros/matatouros,
olaria, indústria de ração, indústria extrativa de Óleo, chiqueirões, aviários e esgoto
sanitários.
A
carga poluidora recebidana
época era equivalente aum
despejo diário de300
mil habitantesA
região oeste catarinense apresenta a maior concentração de suínos porkm2
do
país. Este fato, aliado ao alto grau de confinamento, traz
como
conseqüênciaum
grandeaumento do volume
euma
grave concentração de dejetos de suínos.De
acordocom
aEPAGRI,
84%
das fontes e pequenos mananciais da área estão contaminados porcoliformes fecais.
(SANTA
CATARINA,
1997)Visto que a maioria
do
mananciaisdo
oestedo
estado de Santa Catarina estãocontaminados por agrotóxicos e despejo constante de dejetos de suínos, as atenções
estão se voltado para a água subterrânea,
no
entanto os estudo relativos a esta área sãodeficientes.
SANTA CATARINA
(1997) “Dentre as deficiências básicasno
estadoFace às necessidades crescentes das última décadas, o
número
de perfurações depoços profundos para utilização de água subterrânea
tem
apresentadoum
considerável crescimento, notadamenteem
algumas regiõesdo
estado. Estes poçosvisam
tanto supriro abastecimento urbano industrial quanto ao
meio
rural.Além
do
aspecto necessidade, outros fatorestem
contribuído para isso.Como
se sabe, a utilização de águassubterrâneas
normalmente
apresenta vantagensquando
comparada
à de água desuperfícies, particularmente
no
que se refere a custos de tratamento, prazos de execuçãoe proteção dos mananciais.
O
fatorem
desvantagemfica
por conta, quase sempre,do
elevado investimento exigido
em
máquinas
e equipamentos de perfuração, fato quelimita a ação
do
poder público.De
acordocom
informações fornecidas pelaCompanhia
deÁguas
eSaneamento
de Santa Catarina
-
CASAN
-
e pelaCompanhia
Integrada de DesenvolvimentoAgrícola de Santa Catarina
-
CIDASC
-
0 estado possui atualmente quase dois milpoços profundos perfurados por estas duas companhias,
além
de alguns implantados naregião oeste pela extinta Sudesul.
Não
foram incluídosno
levantamento os poçosartesianos de propriedade da iniciativa privada, os quais representam
mn
número
considerável
no
estado.Segundo
levantamento efetuado pelaCASAN,
1995 e pelaCIDASC
1996, a região extremo oeste emeio
oeste possui 765 poços profundoscom
uma
vazão total de 5.617,00 e tuna vazãomédia da
regiãoem
14,20m3/h.(SANTA
CATARINA,
1997)A
nível de estado, Santa Catarina apresenta urna situação delicadacom
relação aqualidade dos seus recursos hídricos.
De
acordocom
aCASAN,
(citado por Oliveira,1992), o sistema de abastecimento caracteriza-se por utilizar
82%
da captação a partirde mananciais superficiais,
15%
nos lençóis subterrâneos e apenas3%
em
outro tipo demananciais.
A
extensãodo
problema, resultado
fato de que80%
dos recursos hídricosdo
território catarinense, encontrarn-se seriamentecomprometidos
em
decorrência dosimpactos ambientais gerados pelo lançamento de efluentes de esgoto urbano, de
animais, industriais, uso inadequado de agrotóxicos e erosão
(FATMA,
citado porOliveira, 1992).
Os
principais fatores determinantesdo
grau de entropia dos mananciaispresença de
compostos
orgânicosem
cursos d”água, proporcionando riscos de contaminação por patógenos, a intensa eutrofização verificada atualmente pela quasetotalidade dos rios catarinenses, fornecendo desta
forma
disponibilidade alimentar para0 desenvolvimento dos simollídeos (borrachudo) e o risco de contaminação por nitratos
nas águas subterrâneas
que
são os principais fatores determinantesdo
grau de entropiados mananciais catarinenses
(SILVA,1996)
Os
impactos provocados pelos dejetos de suínos oriundos da fração nitrogenada,possivelmente sejam os que
determinem
maiores danos, pois 'além de ser elementoessencial
no
processo de síntese causando floração das águas superficiais, o nitrogênioem
contatocom
águas subterrâneasinduza
formação de nitratos, estecomposto quando
ingeridos consequentemente
em
meio
anaeróbio é reduzido a nitrito 'no organismo, elemento conhecidamente cancerígeno(PICOT,
1992)1.1 -
O
OESTE
DO
ESTADO
DE SANTA CATARINA
-
VISÃO
GERAL
A
região oestedo
estado écomposta
pelas baciasdo
riosChapecó
e Irani, estaregião
vem
apresentadoum
grande crescimento socioeconômico nas última duas décadas.A
população rural representa47%
(l80.4l4 habitantes) da total (386.4l4habitantes).
O
relevo se apresenta acidentado na sua maior parte, o que contribui paraoagravamento da erosão.
Da
mesma
fonna, a cobertura vegetalda
região se apresentadegradada,
com
apenas17%
de vegetação primaria e sectmdária e1%
da
área reflorestada.A
aptidão agrícolada
maior parte dos solos esta enquadradana
classe 3 e4(uso
com
restrições), oque não impede
que seja a primeiraem
produção de grãos euma
das primeirasdo
estado na produção de suínos, aves e leite.(SANTA CATARINA,
1997)
Como
conseqüência da intensa atividade agropecuária, constata-se o agravamento da erosãodo
solo e o assoreamento dos rios,além da
grandecontaminação dos mananciais por dejetos de suínos e por agrotóxicos,
no
oestedo
1985, citado por Oliveira et. al.,
apud
SILVA,
1996), proporcionandouma
produçãoem
tomo
de25000
m3/dej/mês praticamente isentos de quaisquer tratamentos.Quando
confrontada a disponibilidade de
água
com
os diversos usos, verifica-se quehá
uma
relativa normalidade na maior parte das sub-bacias da região.
Em
algumas
delas,contudo,
há
escassezcomo
é o casodo
no
Chalanana
foz,próximo
de Chapecó. Nestecontexto,
vem
aumentado
a perfuração de poços profundos na área,sem
um
processoO
1.2 -
o
MUNICIPIO
DE
CHAPECÓ
O
municipio deChapecó
está situadono
oestedo
Estadode
Santa Catarim, a689
metrosacima do
mar. Possuiuma
área ruralde
594,71
km2,
euma
área urbanade
67,00km2.
Com
clima superúmido
mesotérmico
seusolo é latossolo roxo distrófico,
terra roxa estrutura eutrófica e
distrófica
com
temperaturamédia
anualde
20,17 graus centigrados.A
estruturaftmdiaria conta
com
2.800 propriedadescom
um
totalde
imóveis territoriaisde
33.498.,sendo 12.103 desocupados e 21.395 ocupados.
O
município possui urna população totalde
136.878 habitantes(AMOSC/98),
sendo 123.060
(88%)
urbana e 16.818(12%)
rural,com
uma
densidadedemográfica de
223,59 Hab/1<m2, sendo
d
densidade urbanade
1.3ós,o3Hab/Km*
zmai
de
31,39Hab/km2.
No
mmúdrpid
existem 36.467 zdifiedçõzs.A
cAsAN
possui 525.342ligações.
Não
existe estação de tratamentode
esgoto.A
massa
de residuos sólidosrecolhida diariamente é
de
70
toneladas,além
disso,o
município de possuium
plantelde
383.385 bovinos, 745.574 suínos e 1.654.100 aves(IBGE, 1996
www.ibge.gov.br)O
Municipiode
Chapecó, foi selecionado para estetrabmo,
facea
grande produção agropecuária, suinícula, ea
exploração intensivada água
subterrânea, tantono
interior
do
municípiocomo
na zona
urbana, eem
facea
quase inexistênciade
estudoságua
são deboa
qualidade, sendo classificadacomo
bicarbonatada alcalina, queapresentou,
no
entanto índices de nitrato quemerecessem
maior atenção.Desta forma, o objetivo principal deste trabalho foi avaliar a presença de
nitratos e nitritos
na
água subterrâneado
município deChapecó
-SC
através da coletaeanálise de 100 poços artesianos localizados
na
zona rural e nazona
urbanado
município.
Neste contexto partimos
da
premissa de que a água jácontém
níveis de nitratosem
virtude de resultados anteriores terem demonstrado isso, e temoscomo
objetivosespecíficos:
- Detectar possíveis variações das concentrações entre a
água
dos poçosdo
interior e
da
cidade;- Observar variações
na
concentração de nitratos entre as análises de 1998(NICOLAI,
1998) e atuais; i- Estabelecer possíveis fontes de contaminação;
- Elaborar
um
quadro completo,no que
diz respeito a contaminação porO
2-
REVISAO
BIBLIOGRÁFICA
2.1
_
o
N1TRoGÊN1o
O
nome
desse elementoprovém
do
grego e signiñca “formador de nitron”,onde
“nitron” se refere ao nitrato de potássio,
KNO3.
Em
francês, onome
para o nitrogênio éazoto,
que
significa“sem
vida”. (O
pioneiro francês A.L.Lavoisier observouque
urnrato
morreu quando
mantidoem
atmosfera de nitrogênio.)Os
sais deamônio
e osnitratos
eram
conhecidos dos primeiros alquimistas, quetambém
prepararam o quedeveria ser o ácido nítrico.
(RUSSEL,
1994)O
nitrogênio ocorrena
terracomo
o principal constituintedo
ar(~78%
em
volume).
Compostos
inorgânicosdo
nitrogênionão
sãocomumente
encontradoscomo
minerais, porque a maioria deles é solúvel
em
água.O
nitrogênio é encontradoem
compostos
orgânicosem
todos os seres viventes, animais e plantas. Proteínas, sãomoléculas gigantes, cujas peças constituintes são compostos contendo nitrogênio
chamados
aminoácidos.(RUSSEL,
1994) .O
nitrogênio éum
elemento extremamente importantena
síntese de proteínas pelas plantas epode
vir a serum
fator limitantena
produção de alimentos. Entretanto, onitrogênio,
como
todo o nutriente,pode
causar problema de superprodução de algas noscorpos receptores de estações de tratamento que
não
forem capazes de retirar ou, aomenos,
reduzir a quantidade desse elemento.Nos
esgotos o nitrogêniopode
aparecer dediversas formas, desde nitrogênio orgânico, amônia, até fomias mais oxidativas
como
nitrito e nitrato.
(PAGANINI,
1997).Pode-se conhecer a presença e estimar o grau de estabilização
da
matéria orgânica pela verificaçãoda fonna
como
estão presentes os compostos de nitrogêniona
água
residuária.O
nitrogênio presenteno
esgoto fresco está quasesempre
todo_/
biológica transformam o nitrogênio presente primeiramente
em
amônia, depoisem
nitrito e depois
em
nitrato.A
concentraçãocom
que o nitrogênio aparece sob estasvárias formas indica a idade
do
esgotoou
sua estabilizaçãoem
relação àdemanda
de oxigêmo.(JORDÃO
&
PESSOA,
1995).Pode-se dizer que na
decomposição
da matéria orgânica, o nitrogênio presentenas proteínas passa por
uma
fase amoniacal(NHÍ),
convertendo-se daíem
nitrato(NO3`). Nesta forma, ele
pode
ser absorvido pelos vegetais,chegando
até os outrosorganismos vivos, fechando o ciclo.
A
presença na água doscomposto
nitrogenadospode
indicar o tipo, freqüência e distância da contaminação orgânica(OPAS,
1987)O
nitrogênio albuminóide é aquele resultante da morte dos seres vivos.Sua
transformação
em
NHÍ
(nitrogênio amoniacal) indica o início da oxidação, queproduzirá
NOz
(nitrito) e,em
seguidaNO3
(nitrato).Um
resultado de análise de águaonde
o nitrogênio albuminóide apareceem
concentrações maiores que o nitrogênioamoniacal indica presença de matéria não decomposta.
Caso
o resultado seja o contrário, isto é, a concentração de nitrogênio amoniacalseja maior
do
que o de nitrogênio albuminóide, admite-se que a matéria orgânicapresente
na água
já encontra-seem
processo de decomposição.Como
a transfonnaçãoN-albiuninóide
- N-
amoniacal é mais rápidaquando
a matéria orgânicaprovém
deexcretas animais
do
queem
vegetais (folhas e galhos,) esse resultado indica que a águateve contato recente
com
excretas.(OPAS,
1980)A
presença de nitritos (NOz`)em
concentrações elevadas indicaque
a matéria orgânica presentena
água encontra-se apouca
distânciado
pontoonde
foi feita a coletapara análise.
Os
nitiitos sãouma
forma transitória, sendo rapidamente oxidada à nitratoNO3. Sua
persistência indica despejo contínuo de matéria orgânica.Os
nitratos são o último estágioda
oxidaçãodo
nitrogênio. Resultados de análisecom
altas concentraçõesde nitratos indicam que a matéria orgânica que entrou
em
contatocom
a águaencontrava-se totalmente decomposta. Esse fato não significa que a água esteja isenta de
1U
2.2 -
o
CICLO
no
N1TRoGÊN1o
O
Nitrogênio (N) é nutriente mineral encontrado freqüentementeem
pouca
quantidade para a nutrição das plantas e o quarto elemento mais
comum
nacomposição
destas, perdendo apenas paro o carbono (C) , hidrogênio (H) e oxigênio (O).
O
átomo
de nitrogênio existe
em
diferentes estados de oxidação e estados ñsicos.As
alteraçõesentre elas são
comumente
mediadas por organismosno
solo.A
facilidadecom
que as alteraçõesocorrem
nos estados de oxidação resulta na formaçãode
diferentes formasinorgânicas
que
desaparecem rapidamentedo
ecossistema.A
fonna N03'
é solúvelem
água
e, destemodo,
sujeita a lixiviação e ao transporte pela água.As
fonnas NI-If eNH;
estão sujeitas à volatilização e a fixação tanto pelas argilacomo
pela matéria orgânicado
solo(MOS).
A
escassez de nitrogênio, portanto,com
freqüência limita aprodutividade das plantas.
Além
disto, as fases gasosa e solúvel deste nutrientelevam
à poluição ambiental(ELDOR
&
CLARK,
1996).O
nitrogênio é essencial à vida e é inncomponente
de proteínas e ácidos nucléicosem
células de micróbios, animais e plantas.É
irônico que o gás nitrogênioseja o gás
mais
abundante(79%
da
atmosferada
terra)(BITTON,
1994)no
arque
nósrespiramos e ainda é
um
nutriente limitadoem
ambientas aquáticos eem
terrasagrícolas, conduzindo à deficiência de proteinas que é experimentada por milhões de
pessoas
em
paísesem
desenvolvimentoSegundo
PAUL
&
CLARK,
1996, o conceito deum
ciclo foi formulado por Lohnis (1913), seguido da identificação das fomiasdo
N
no
solo e o papel dos microorganismosno
movimento
do
N
deuma
forma
para outra. Ele representou oNz
como
central ao ciclo e reconheceu as formas proteina, amida,NH3, N02'
e NO3`.1.1.
É:
'Í
/Í/
Ê
`;O___`z¿":,' _ /,.« ~._`: ”".=`? zíš '
'Ã
'*1
' 'z=f~â e ‹ ' ; .Í'Qi
_.-,H ~, \\`É
\\_\ _ ¡>›‹/I \\`{` Í,.ffmf^›‹^ s.. flkr/ / IÍIOVII IYIMRVII1 /' ,__/, ‹ ---~<
GITWI 1 ` ___" _ _ _;~' _'-z'f'>S
^` . zw-. , .›>( /, _ _ 1
"~ ବ*>
A
- ._:€T.jl>
_ _;9
nunca uma 1.1
am.. » 1
' -=
za :-f›:¡;.;f:;-,'i,z'‹<_='¿'-,
°-.'.~.:^~' .
'
=- -~
una»-anuutc
uma onwwcur
°"'_' comuna
-` -_ âunurmvmlvaä ` mu,--NI-í£==‹ «t
,M
/
QE' Q É
Õ.
'°v‹
V
Llxlll
FIGUR E B. 1 Ninogen cycle in soil. (From Stnwcnson. l982.)
Figura
01. Ciclodo
Nitrogêniono
solo.(STEVENSON,
1982 inELDOR
&
CLARK,
1996)O
ciclono
nitrogêniopode
ser esboçado de outras maneiras, (figura 02 efigura
O3) Essenciahnente ela simboliza as transformações por que passa o elemento
nitrogênio (N) neste planeta através
da
ação dos seres vivos.O
lado esquerdo e o setorinferior
da
fig
02
mostram
a síntese de matéria viva nitrogenada (principalmenteproteinas) a partir de compostos nitrogenados inorgânicos (íons nitrato, nitrito e amônia)
durante o crescimento das plantas e o seu
consumo
por animais, seguido por sua voltaao solo
como
resultado dadecomposição
e putrefação de material vegetal e animal.O
setor superior mostra a perda de nitrogênio, para a atmosfera, de nitratos e seu
retomo
IL
umarsäsenao
O
*ZH
*ty
'N
A5%
AMomHcàcAo _nc
,mnms
~MOM
<::::_-_-:i '°'°"j«Í
.
um
Wii:-CV
'““**i::.::::>
'°Ê3'‹='Ã'- `š
4/
mm
I
NÍTRITÔS
~
OA
~e*°`°$
Figura 02
-
Ciclo Biológicodo
Nitrogênio(POSTAGE,
1987)é”
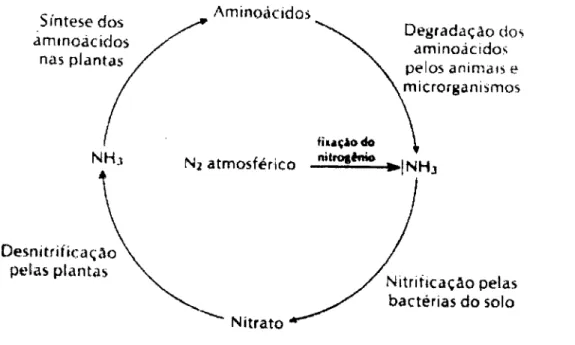
De
a acordocom
LEHNINGER,
1991, a primeira etapano
ciclodo
nitrogênio éa
fixação do
nitrogênio atmosférico por organismos fixadores de nitrogênio para produzir amônia.A
amônia pode
ser usada pela maioria dos organismos vivos.Entretanto,
há
algumas importantes bactériasdo
solo que retiram a sua energiada
oxidação da
amônia
a nitrito eno
fim
a nitrato. Pelo fato destes organismos seremextremamente
abundantes e ativos, praticamente toda aamônia
que atinge o solotoma-
se oxidada a nitrato, processo conhecido
como
nitrificação.As
plantas e muitas*bactérias
podem
facilmente reduzir o nitrato de volta aamônia
pela ação da nitratoredutase. Este processo é conhecido
como
desnitrificação.A
amônia formada pode
sertransformada
em
aminoácidos, pelas plantas, que são então utilizadas pelos animaisComo
uma
fonte de aminoácidos, essenciais e não essenciais, para sintetizar asproteínas animais.
Com
a morte dos animais, a degradação microbiana de suas proteínasretoma
aamônia
ao solo,onde
as bactérias nitrificadoras convertem-naem
nitritos1.3
Biblioteca
Universitária
,uFscs
aí
942
S.. t d _
Aminoácidos
_ “ 95?
9*
Degradaçao
dosammoacidos
¿,m¡n0¿C¡d0Snas p|'3m~¿'5 pelos animais e
microrganismos
iinçáo do
NH.: N; atmosférico
~|NH3
Desnitriíicação
pen”
plantasNitrificaçào pelas bactérias
do
solo\
Nmaro
Figura 03
-O
Ciclono
Nitrogênio.(LEHNINGER,
1991)O
conceito de ciclodo
nitrogênio abrange o conjunto de transferências etransformações que sofre este elemento, e que
tem
lugar por diferentes vias,como
o ar,o solo, a água, os microrganismos, as plantas, os animais e o
homem.
(DIAZ,
1985.)O
constante intercâmbio e transformaçõesdo
nitrogênio seproduzem
através deprocessos
como
a fixação, amonificação, nitrificação e desnitrificação.O
processo de conversão de nitrogênio gasoso auma
forma combinada
sedenomina fixação do
nitrogênio, e se produz pela ação de uns poucos organismos, e
em
menor
medida
devidoa certos processos atmosféricos.
A
fixação
atmosférica acontececomo
conseqüência defenômenos
de ionizaçãocomo
tomientas elétricas, radiação cósmica etc.que
cedem
energia necessária para que se produza acombinação
de nitrogêniocom
o oxigênio e ohidrogênio,
formando compostos
solúveisna
água dachuva
que se incorporam ao solo.14
A
fixação
biológicado
nitrogêniopode
ser realizada por algumas algas e bactérias de vidaautônoma (DIAS,
1985). Relativamente poucos organismos sãocapazes de usar (fixar) o nitrogênio gasoso (Nz)
que
representa perto de80%
da nossaatmosfera.
Como
a crosta terrestrecontém
muitopouco
nitrogênio na forma de saisorgânicos solúveis, todos os organismos vivos
dependem
em
última instânciado
nitrogênio atmosférico e dos organismos fixadores de nitrogênio.
O
nitrogêniopode
serfixado
pelas cianobactériasou
pelas algas verdesou
azuis; elas são células totalmente auto suficientes pois são completamente autotróficas. Elaspodem
fixar
o nitrogênio atmosférico etambém
realizar a fotossíntese, obtendo assim todo o carbono quenecessitam
do
dióxido de carbono atmosférico.(LEHNINGER,
1991)Muitas outras espécies de bactérias fixadoras de nitrogênio
ocorrem no
solo.Algumas
delasvivem
simbióticamenteem
nódulos de raízes de certas plantas,especialmente de
membros
da família das leguminosas.(LEHNINGER,
1991).Como
resultado
do
processo defixação
apareceno
soloamoníaco ou
íonamônio que
são absorvidos pelas plantas através de seu sistema radicular incorporando-se o nitrogênio,posteriormente nos aminoácidos e proteínas. Através da ingestão de vegetais, os animais
incorporam o nitrogênio
em
novas proteínas, e defonna
semelhante se incorpora nas proteínas humanas.(DIAZ,
1985)O
processo deamonificação compreende
o conjunto de reações que, partindo da degradação doscompostos
orgânicosdo
nitrogênio,conduzem
a formação de íonamônio.
Em
um
meio
oxidante, o íonamônio
produzido, seja por processo de fixaçãoou
amonificação, se converteem
seguidaem
nitrito eem
nitrato pelo processo denitriñcação. Este é
um
processo de oxidação biológico que seproduzem
em
duas fases,devido a ação de dois grupos de microrganismos distintos:
O
grupo das Nitrosomas,Nitrosococus, Nitrosospira, Nitrosocystis e Nitrosogloes que convertem
o
amônio
a íonnitrito , e
o
grupo Nítrobacter, que oxida o íon nitrito a íon nitrato.Ambas
são bactériasautotróficas, que utilizam a energia das reações quírnicas inorgânicas.
(DELWICHE,
1.)
2.3 -
NITRIFICAÇÃQ
A
nitrificação converteNH4+
em
N02'
eN02'
em
NO3`. Resultana
produçãodo
que
era historicamente conhecidocomo
salitre(KNO3)
A
primeira fonte reconhecida desalitre foi
mn
sal eflorescentefonnado
sobre pedrasou
tijolos expostos a NI-13. Estaeflorescência é descrita
na
bíblia (levítico 14:34-53).A
pólvora feita usando-se salitre foi desenvolvida pelos chinesesno
século X.Na
Europa, plantaçõescom
salitre foramdescritas por
um
escritoralemão no
séculoXVI.
Terra, estrume e caleram
misturadosem
barracões e regadoscom
urina e esgoto.Os
montes eram
mantidos aerados e osalitre era extraído
com
água quente. Acreditava-seque N03'
fosseformado
através deuma
reação química envolvendo NI-If e Oz,com
solo argilosocomo
catalisadorquímico.
(PAUL
&
CLARK,
1996.)Por volta de 1870, Pasteur postulou
que
a formação deNO3`
era microbiológicae análoga à conversão de álcool a vinagre.
A
primeira evidência experimental de que anitrificação era biológica foi
dada
por Schloesing eMuntz
em
1877. Eles adicionaramefluente de esgoto e
um
tubo longo, cheiocom
areia esterilizada eCaCO3. Depois
de20
dias,
NH4+
havia desaparecido eN03'
estava presente. Warington,em
1878,em
Rothamsted,
no Reindo
Unido, descobriu que a nitrificação eramn
processo de duasetapas envolvendo dois grupos de microrganismos.
Um
grupo exidavaNHÍ
a NOz`, eum
outro oxidavaN02'
a NO3`. Entretanto ele não isolou os organismos responsáveis.Winogradsky
é reconhecidocomo
sendo o primeiro a isolar os nitrificantes.(PAUL
&
CLARK,
1996.)Os
microrganismos responsáveis pela nitrificação são as bactérias nitrificantesque
são divididosem
dois grupos principais:Nitrosomonas
éum
gênero tipico dos seisque
oxidam amônia
a nitnto; Nitrobacter representaum
número menor
de gêneros queoxidam
nitrito a nitrato. (tabela 01)Do
ponto de vista ecológico elastem
duas funçõesimportantes,
uma
benéfica
e outra deletéria.A
amônia embora
sejaum
nutriente vegetaladequado, é
menos
eficiente que o nitrato, preferido pela maioria das plantas.As
bactérias nitrificantes
desempenham
uma
função útil aotomarem
o nitrogênio daLU
retida pelo solo, enquanto os nitratos são rapidamente levados, de sorte que a
nitrificação
pode
resultarem
perda de nitrogênio.(POSTGATE,
1987).A
figura 04
representa a reciclagemdo
nitrogênio da biosfera pela ação debactérias nitrificantes.
Bactérias nitrificantes
Nitratos
N
Bactérias _atmostšéflcø f¡¡adO¡¿,5'de
-›Amôma
Plantasnitrogênio
Aminoácidos
Animais
Figura 04
-A
reciclagemdo
nitrogênio da biosfera(LEHNINGER,
1991)A
nitriñcação é a conversão deamônia
a nitrato através da ação deIl'l1Cl'O1'g3.I1l SITIO S.
1
-
Conversão
de NI-If a NOz`.Nitrosomonas
(por ex. N. europaea. N.oligocarbogenes). Outros oxidante de
amônio
são Nitrospira, Nitrosococcus e Nitrosolobus(FOCHT E VERSTRAETE,
1977,apud
BITTON,
1994).2NH..*
+ oz
->
2NH2oH
+
2H*
NH4* +1.5oz
-->
Noz'+2H*+H,o+2751‹J
2
-
A
conversão deN02'
paraN03'
Nitrobacter (por exemplo, N. agilis, N.winogradski) converte nitrito para nitrato:
NOz` +
0.5Oz
-%
NO3` +
75 klll
Essas bactérias,
além
de sua importânciaem
agricultura,como
agentes danitrificação dos solos
(uma
vez que os vegetaisem
geral, não são capazes de assimilaramônia ou
nitritos,mas
apenas nitratos)merecem
ainda a atenção especial poruma
razão análoga: elas realizam a transformação da amônia, resultante
da
degradação das proteínasou
aminoácidos existentesno
esgoto,em
nitratos, que constituemum
dos maisimportantes fatores limitantes
no
crescimento de algas.(BRANCO,
1986)Além
disso, são as bactériasdo
gênero Nitrosomonas, as responsáveis pelapresença de nitritos
em
muitas águas, o que constitui importante indício químico de contaminação por esgotosou
outra fonte de matéria orgânica.Sendo
os nitritos instáveisem
água contendo oxigênio, graças principalmente à presença de Nitrobacter, o seuaparecimento é
sempre
transitório, somente se veriñcandono
momento
em
que se dá a degradação de matéria orgânica; entretanto,nem
sempre
revela a presença de esgoto, pois a formaçãodo húmus, ou decomposição
de restos vegetais, leva igualmente àformação
de nitritos.(BRANCO,
1986.) ^A
oxidação deNH]
aN02'
e então paraN03'
éum
processoque
rende energia.Microrganismos utilizam a energia gerada para assimilar COz. Exigências de carbono
para nitrificadores são satisfeitas por gás carbônico, bicarbonato,
ou
carbonatos.A
nitrificação é favorecida pela presença de oxigênio e alcalinidade eficiente paraneutralizar os íons de hidrogênio produzidos durante 0 processo de oxidação.
(BITTON,
1994).
A
intensificaçãoda
nitrificação dá-seem
condições aeróbias;em
solos inigados,porém
drenados, as condições serão tanto melhores quanto maioresforem
as condiçõesde aeração
do
solo.Em
solos inundados a nitrificação-ocorre nos primeiros milímetrosda
superflcie de contatocom
o ar, indo ao limite dacamada
aeróbia-anaeróbia da lâminad”agua/solo.
Assim
a nitrificação dependetambém
da
profundidadeda
lâmina d'água,do
tempo
de permanência damesma
sobre o solo, dos períodos de rega eda
estruturado
solo, já que a difusão
do
oxigênio faz-se 104 vezes mais rápida pelo ardo
que pelamassa
líquida.(PAGANIN1,
1997)A
tabela 01 demonstra os principais microrganismos envolvidosno
processo de-10
Tabela
01 - Principais microrganismos envolvidosno
processo de nitiiñcação.(PAUL
&
CLARK,
1996)GENERO
ESPÉCIE
Oxidam
NHÍ
aN02'
Nitrosomonas
Europeae
Nítrosospira Briensis
Nitrosococcus Nitrosus
Oceanus
Mobilus
N
itrosovibrioT
enuisNitrosolobus Multzformus
Oxidam
N02'
aN03'
Nitrobacter Winogradskí
Hamburgensis
Vulgaris
N
itrococcus MobilusNitrospina Gracil us
Nitrospira
Marina
2.3.1
-
Fatoresde
Afetam
a Nitrificação_A._gi_dg
-
A
produção deN03'
está relacionadacom
o solo ecom
os valores depH
da
solução. Valores ideais depH
podem
variar de 6,6 a 8,0. Geralmente, as taxas denitrificação
em
solos agrícolasdiminuem
abaixo depH
6,0 etomam-se
irrelevantesabaixo de 4,5. Valores altos de
pH
inibem a transfonnação deNOz`
a NO3`.Quase
todos os solos ácidos de florestasproduzem N03' quando
distúrbios,como
fogoou
derrubadas, resultamem
maiores taxas de mineralização doque
imobilizaçãodo
N.1/
nitrificação
em
solos florestaisnão
é tão sensível à acidez quanto aquelaque
ocorreem
solos agrícolas.'
O
pH
ótimo para Nitrosomonas e Nítrobactérias está entre 7.5 e 8.5(EPA
norte-americano, 1975
apud
BITTON,
1994)A
mtrificação cessa apH
igualou
menor
que6.0.
(PAINTER,
1970;PAINTERE
LOVELESS,
1983,apud
BITTON,
1994).Aeração
-
Como
oOz
éum
requisito obrigatório para todas as espécies, a aeração é essencial para a nitrificação.A
difusão deOz no
solo e, destemodo,
a aeração, é controlada por fatorescomo
aumidade
e estruturado
solo.'
Umidade
e Temperatura-
A
umidade
afeta o regime de aeraçãodo
solo; porisso o estado da
água do
solotem
influênciana
produção de NOz`.A
saturaçãocom
água
limita a difusão de Oz, e a nitrificação é suprimida.No
outro extremo, a proliferação bacteriana é retardada pela insuficiência de água.As
reações gerais demineralizaçâo
que
produzem
NHÂ'
sãomenos
sensíveis a seca e temperatura baixa; porisso
NH4+
acumula-seem
solos secosou
frios.A
nitrificação.Embora
lenta abaixo de5°C, ocorre debaixo da capa de neve
em
muitos solos.Também
é lentaacima
de 40°C.A
temperatura ideal está entre30
e 35°C.A
interaçãoda
temperatura, umidade, aeração e outros fatorescompõem
o efeito sazonal.Em
áreas temperadas, a nitrificação é maiorna
primavera e outono emenor
no
verão e invemo.A
taxa de crescimento de nitrificadores é afetada atravésda
temperaturano
alcance de 8
-
30°C.A
temperatura ótima informada foi ao redor de 30°C.(HITDLEBAUGH
&
MOLEIRO,
1981apud
BITTON,
1994).Inibição Tóxica
-
Nitrificadores estão sujeitos a inibição de substrato e produtose
também
são bastante sensíveis a váriascombinações
tóxicas presentes nas águaimprópria.
(BITTON,
1983;BITTON
et al., 1989apud
BITTON,
1994) Parece quemuitas dessas
combinações
são mais tóxicas as Nitrosomonasque
as Nitrobactérias.Material orgânico
em
água impróprianão
é diretamente tóxico a nitrificadores.A
LV
combinações
mais tóxicas para nitrificadores são cianeto, fenóis, anilinas e metaispesados (prata, mercúrio, níquel, cromo, cobre e zinco.
(BITTON,
1994)2.3.2
-
Efeitosda
NitrificaçãoComo
as plantas assimilam rapidamente NO3`, e obom
crescimento égeralmente considerado dependente deste processo, a nitrificação biológica é usada
como
um
indicador da fertilidadedo
solo.A
nitrificaçãotambém
pode
levar aconseqüência indesejáveis.
O
amônio
éum
cátion, adsorve os colóidesdo
solo e é relativamente estacionário.O
nitrato, por outro lado, emn
ânion que émóvel na
soluçãodo
solo.Sob
certas condições, particularmenteem
solos arenosos, sujeitos a chuvasfortes,
ou
onde
excessiva irrigação é praticada,NO3`
será lixiviado para longeda
regiãoda raiz.
(PAUL
&
CLARK,
1996)O
excesso deN03'
lixiviadodo
solo acaba indo para a água subterrânea, lagose correntes. Esta envolvido em: 1) crescimento excessivo das plantas e algas
(eutrofização); 2) problemas de saúde
como
metahemoglobinemia
e; 3) formação denitrosaminas cancerígenas pela reação
com
outros compostos nitrogenados.Os
intermediários gasososda
nitrificaçãopoluem
a atmosfera.(PAUL
&
CLARK,
1996)2.4
-
NITRATO
O
nitrato éum
íon resultante dacombinação
deum
átomo
de nitrogêniocom
trêsátomos
de oxigênio (NO3`).Nas
análises de águapode
ser referido ao íon nitratoou
aonitrogênio.
(CETESB,
1978)É
um
dos íons mais encontradosem
águas naturais, geralmente ocorrendoem
baixos teores nas água superficiais,mas
podendo
atingir altas concentraçõesem
águasL1
efeitos adversos à saúde: a indução à metahemoglobinemia, especialmente
em
crianças,e a
fonnação
potencial de nitrosaminas e nitrosamidas carcinogênicas.(NISCHIHARA
,1998)
O
nitrato constitui o produto final da estabilização aeróbicado
nitrogênioorgânico
(CARVAJAL
et al 1980).O
resultado da degradação microbiana desubstâncias orgânicas nitrogenadas,
como
proteínas, a íons deamônia
(NHÍ)
(LEWWIS
et al 1982).O
nitrato é aforma
mais oxidadado
nitrogênio. Provavelmente é o ânion maisestável nas condições existentes nas águas superficiais.
Devido
à sua estreita relaçãocom
o cicloda
vida, as concentrações de nitrato são fortemente influenciadas pelasatividades das plantas e dos animais.
As
bactériaspossuem
um
papel importantena
relação dos nitratos
na
água.(BATALHA,
1977)O
nitrato é atualmenteuma
das maiores preocupações mundiais, quer seja pelouso indiscriminado de agrotóxicos, quer seja pela grande produção de dejetos de suínos,
aves etc., quer seja pela grande produção de efluentes líquidos
humanos,
e o nãotratamento
do
mesmo.
Salvo paises que são exceção à regra, a maioria não faz otratamento dos efluentes, que são jogados indiscriminadamente
em
rios e córregos,ou
através de fossas sépticas.
A
grande produção desses efluentes, faz surgir o aparecimento de nitratos, quelixiviados
alcançam
os rios e principalmente a água subterrânea.O
nitrato é aforma
mais persistente emóvel do
nitrogênio nas águassubterrâneas,
em
ambientes oxidantes.Além
de constituirum
contaminantesquando
excedam
a 10 mg/lN03'
-N,
étambém,
por suas características ñsico-químicas,um
excelente indicador de contaminação antrópica. Estudos
(RITTER,
1990)tem
mostradocorrelações entre a presença de nitrato e de pesticidas,
em
áreas agrícolas nosEUA.
Segundo
FERREIRA
&
HIRATA
(1993), o nitrato, procedido pela condutividadeelétrica e pelos cloretos, é muito mais eficiente e preciso
na
indicaçãoda
contaminaçãopor sistemas de saneamento in situ, comparativamente às bactérias colifonnes, devido à
_._._._._.-___
T
1 i1
Até
1984 as concentrações aceitáveis de nitratona
água aceitas pelaOMS
(organizaçãoMundial
da Saúde) estavam entre 50 e 100 mg/1. Concentraçõesacima
de100 mg/1
não eram
recomendadas.Em
1984 devido aos informesda
incidência demetehemoglobinemia
infantil, aOMS
reduziu os índicesrecomendados
a 10 mg/1N03'
-
N
ou
(45 mg/1 NO3`).(GRAY,
1994)A
poluição deágua
subterrânea e de superficie por nitrato setomou
um
dos problemas ambientaisem
várias partesdo
mundo.
O
uso excessivo de fertilizantes denitrogênio
em
agricultura intensiva e descarga de detritos domésticos e de animais são O onsideradas as principais causas queagravam
o problema.(VOLOKITA
et al., 1996).Preocupações
com
possíveis conseqüências para a saúdetem
levado à adoção deum
valor de diretriz (10
mg
N03'
- N/1)em
água
par oconsumo
humano
(WHO,
1984)No
Brasil os níveismáximos
de nitratosem
água paraconsumo
sãoregulamentados pelo decreto n° 14.250 de 05 de junho de 1981, e estabelecem os teores
máximos
para o nitrato de 10 mg/1 deN03'
-N
e par o nitrito de 1,0 mg/1 deN02'
-N
(SANTA
CATARINA,
1998).gz'
Nos
EstadosUnidos
o padrão é regulado pela Environrnental ProtectionAgency
(EPA)
e fixoucomo
padrãomáximo
de contaminação da água por nitratosem
10 mg/1N03'
-N
e aEuropa
fixou
os níveismáximos
em
12 mg/l.(GLASS
&
SILVERSTEIN,
1997)
Na
maion`a dos solos,NHK,
liberado durante adecomposição da
matéria orgânica, e que não é usado imediatamente pelos organismos é rapidamentetransformado
em
NO3`.N
de fertilizantes adicionadoscomo
uréia,NHÍ
ou na forma
deNH3,
estátambém
sujeito à nitrificação.Assim
queN03'
éformado no
solo,ou
adicionado por deposição
úmida ou
seca, está sujeita aos seguintes destinos: 1)pode
sofrer redução por microrganismos, resultando