Bu tez çalışmasının amacı, daha önce çiçekli ve çiçeksiz sarımsak genotiplerinde diferansiyel olarak eksprese edildiği saptanan XTG_MCG_13, XCT_MGT_7, XCT_MGC_6, XTG_MGA_10 kodlu EST genlerinin ekspresyon düzeylerinin qRT-PCR analizi ile belirlenmesidir. XCT_MGC_6 için kodlanan genin, diğer genotiplere kıyasla çiçek G2 genotipinin bitki gelişim aşamalarında önemli ölçüde yukarı eksprese edildiği bulundu. Bu tez çalışmasının amacı, daha önce çiçekli ve çiçeksiz sarımsak genotiplerinde diferansiyel olarak eksprese edildiği saptanan XTG_MCG_13, XCT_MGT_7, XCT_MGC_6, XTG_MGA_10 kodlu EST genlerinin ekspresyon düzeylerinin qRT-PCR analizi ile belirlenmesidir. Sarımsak soğanları 4 ℃ ve 20 ℃ olmak üzere iki farklı sıcaklıkta 12 hafta süreyle depolanmıştır.
qRT-PCR analizlerinde, XCT_MGT_7 EST ve XTG_MCG_13'ü kodlayan EST genlerinin, bitki gelişim evrelerinde çiçekli G2 ve G3 sarımsak genotiplerinde, çiçeksiz G4 ve G5 sarımsak genotiplerine göre daha yüksek ifade edildiği belirlendi. TÜBİTAK-TOVAG proje tesisi 1050551 bünyesinde cDNA-AFLP analizleri ile belirlenen XCT_MGT_7 EST geninin 2007 ve 2008 yetiştirme sezonlarında G1 ve G2 genotiplerinin çiçeklenmesinden alınan yaprak örneklerinde ok işaretli.

GİRİŞ
Soğan ve pırasa gibi yeterli tohum veren çeşitlerin geliştirilmesi, sarımsağın daha pratik ve ekonomik olarak yetiştirilmesini sağlayabilir (İpek, 2011). Son yıllarda sarımsağın anavatanı sayılan Orta Asya'da tohum üreten sarımsak türleri bulunmuş ve bunlar Avrupa, Asya ve ABD'de gen bankalarında koruma altına alınmıştır. Ekonomik değeri olan bir diğer Allium türü olan soğanda (A. cepa L.) hibrit tohumların başarılı bir şekilde üretilmesi ve kullanılması bu beklentileri pekiştirmektedir.
Islah çalışmalarında bu genotiplerden daha güçlü çiçek sapına sahip hatların geliştirilmesi, çiçek sürgününde daha az veya hiç diş olmaması, polen canlılığı ve tohum üretiminin yüksek olması sarımsakta ticari hibrit tohumların üretilmesini sağlayacaktır. Sarımsakta çiçeklenme mekanizmasının tam olarak aydınlatılması, sarımsakta çiçeklenme ve tohum üretimi ile ilgili genetik problemlerin çözülmesine yardımcı olabilir. Bu genin uzun ve kısa olmak üzere iki farklı mRNA'ya sahip olduğunu ve kısa mRNA'nın her iki sarımsak genotipinin tüm aşamalarında ifade edildiğini, uzun mRNA'nın ise normal çiçek açan genotipte sadece çiçeklenme sırasında ifade edildiğini bulmuşlardır.
Araştırmacılar, sarımsakta çiçeklenmedeki bu farkın, mRNA olgunlaşması sırasında meydana gelen alternatif modifikasyonların (alternatif ekleme) etkinliği ile ilgili olabileceğini öne sürüyorlar. Bu çalışmada Arabidopsis bitkisinde tanımlanan LEAFY/FLO geninin homologu sarımsakta incelenmiş ancak sarımsakta çiçeklenme ile ilişkili diğer genler için gen ekspresyon çalışması yapılmamıştır. Daha önce tamamlanmış olan TÜBİTAK-TOVAG 1050551 "Sarımsakta (Allium sativum L.) Gen Ekspresyon Profilinin (mRNA) Analizi ve Çiçeklenmeyi Kontrol Eden Aday Genlerin Saptanması" projesi çerçevesinde, "Sarımsakla İlgili Farklı Şekilde Eksprese Edilen 35 Aday Gen- cDNA-AFLP yöntemiyle ilk kez sarımsakta spesifik çiçeklenme "Expressed sequence taqs" (EST) tespit edildi, ancak bu EST'lere ait genlerin sarımsakta ekspresyon seviyeleri ile çiçeklenme arasındaki ilişkisi henüz doğrulanmadı.
Bu tez önerisinin amacı, daha önce çalışılan "Sarımsakta (Allium sativum L.) Gen İfade Profilinin (mRNA) Analizi ve Çiçeklenmeyi Kontrol Eden Aday Genlerin Belirlenmesi" başlıklı TÜBİTAK-TOVAG 1050551 numaralı proje kapsamında belirlenmiştir. , ve sarımsak genotiplerinde farklı gelişim dönemlerinde belirlenmiştir. Eksprese çiçeklenme ile ilişkili bazı aday genlerin ekspresyon seviyelerinin qRT-PCR analizi ile belirlenmesi ve karakterizasyonu.
KAYNAK ARAŞTIRMASI
- Sarımsağın Tüketim Şekilleri
- Sarımsağın Sağlık Yönünden Faydaları
- Sarımsağın Morfolojik ve Çiçek Özellikleri
- Bitkilerde ve Sarımsakta Çiçeklenme Mekanizması
- qRT-PCR ve Referans Genler (“Housekeeping” Genler)
Sarımsak klonları çiçek özelliklerine göre genel olarak "sapsız/sapsız" ve "sapsız" olmak üzere iki gruba ayrılır. Sap üreten sarımsak klonları (gövde/düzenli çiçeklenme), uygun ekolojik koşullar sağlandığında güçlü bir anaç oluşturur. Geç dikim yapıldığı ve soğutma ihtiyacının karşılanmadığı durumlarda çiçeklenme görülmez veya çiçek sapı gelişimi zayıf olur.
Çiçek sapı oluşturmayan (sapsız/çiçeksiz) sarımsak klonlarında ise ekolojik şartlar sağlansa bile genellikle çiçeklenme görülmez veya nadiren görülür (İpek, 2011). Bu üçüncü gruptaki klonlar, "kısmen çiçekli" klonlar olarak tanımlandı, çünkü bunlar düzenli olarak çiçek açmazlar ve klon içinde ekolojik koşullara bağlı olarak gövde üretimi ve gövde uzunluğunda değişiklik gösterirler. Morfolojik olarak, "kısmi çiçek açan" klonları düzenli çiçek sapları üreten klonlardan ayırmak bazen mümkün olmayabilir.
Rotem ve ark. (2007), düşük sıcaklığın apikal meristemin farklılaşmasını ve gövde uzamasını desteklediğini, ancak çiçek sürgününün morfolojisi üzerinde hiçbir etkisinin olmadığını bildirdi. PCR tabanlı yöntemler arasında qRT-PCR kullanılarak gen ekspresyonunun tespiti diğerlerine göre daha kısa sürede ve doğrudan sonuç odaklı olarak belirlenebilmektedir. Bu yöntemin genel araştırma prensibi, mRNA'dan ters transkripsiyon ile elde edilen cDNA'nın florokrom prob veya cybergreen varlığında incelenen gene özgü primerler kullanılarak RT-PCR cihazı ile çoğaltılması ve ortaya çıkan sinyalin qRT- sırasında tespit edilmesidir. ölçüldü. PCR işlemi.
Ayrıca sarımsak bitkilerinin tuz stresi altındaki qRT-PCR analizlerinde en uygun referans geni belirlemek için yapılan bir çalışmada, "TAP42-interacting protein (TIP41)", "ökaryotik translasyon başlatma faktörü 4α (eIF-4α)", " actin (ACTIN)", "gliseraldehit-3-fosfat dehidrojenaz (GAPDH)", "tubulin β-7 (TUB7)", "uzama faktörü 1 alfa (EF-1α)",.
MATERYAL VE YÖNTEM
- Bitki Materyali
- RNA İzolasyonu
- RNA Miktarı Belirleme
- cDNA sentezi
- Gerçek Zamanlı PCR
- qRT-PCR Sonuçlarının Analizi
- İstatistiksel Analiz
2) 1.5 ml'lik tüpler, her tüpte 35 ul RA1 veya RAP solüsyonu ve 3.5 ul merkaptoetanol ile hazırlandı. 14) 70 µl RNAz içermeyen su ilave edilip 1-2 dakika bekletildikten sonra 11000g'de 1 dakika santrifüj edildi ve RNA örnekleri analiz edilmek üzere -85°C'de derin dondurucuda saklandı. Ters transkripsiyonel reaksiyonlar, DNAz veya RNAz enzimi içermeyen suyla 20 kat seyreltildi, ardından buz üzerine yerleştirildi ve gerçek zamanlı PCR (qRT-PCR) analizi ile devam edildi.
Gerçek zamanlı PCR reaksiyonları (qRT-PCR), aktin geninin (gi|56159166|gb|AY821677.1) dizilerinden referans olarak türetilir ve cDNA Primer3 bantları XTG_MCG_13, XCT_MGT_7, XCT_MGC_6, XCT_MGC_10'un dizileri referans olarak alınır. bir önceki proje kapsamında TÜBİTAK-TOVAG 1050551 ile geliştirilen primerler kullanılarak gerçekleştirilmiştir (Tablo 3.1). Her numune için her primer kombinasyonu için ayrı ayrı hazırlanan SYBR Green Mix; 5 µl Mastermix, 0.5 µl ileri primer, 0.5 µl primer geri, 0.1 µl DYE ve 1 µl ultra saf su kullanılarak hazırlandı ve karışımdan 7 µl, 3 µl cDNA içeren PCR plakasının her bir oyuğuna dağıtıldı. Hesaplama seçeneği ile her örneğin CT (threshold cycle, threshold cycle) değerleri ve ΔΔCT yöntemi ile hesaplanan normalizasyon değerleri elde edilmiştir.
BULGULAR VE TARTIŞMA
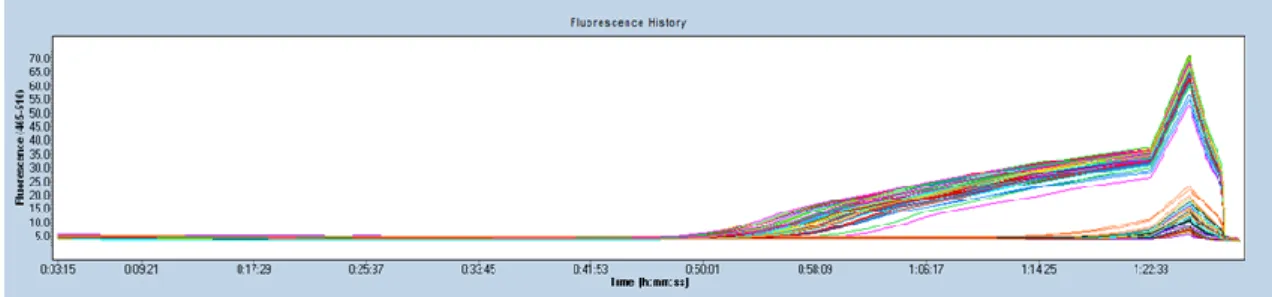
Gerçek zamanlı PCR (qRT-PCR)
7-8 çiçek yaprağı, 6 6 yapraklı meristem, 4-5 yapraklı meristem, 2-3 yaprak meristeminde 21 ℃'de depolama sonrası, 4 ℃'de depolama sonrası ve ön depolamada gen ekspresyon düzeyi en düşük bulunmuştur. G2 genotipinde, XTG_MGA_10 gen ekspresyon seviyesi, tüm aşamalardaki yaprak ve meristem örneklerinde genel olarak düşüktü. Bu genin G2 genotipinde en yüksek ekspresyonu 2-3 yapraklı meristem örneklerinde ve 21°C'de muhafaza edildikten sonra, en düşük ekspresyon ise 6 yapraklı meristem örneklerinde saptanmıştır.
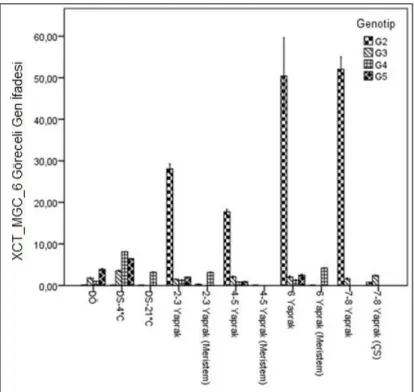
En yüksek gen ekspresyonu yaprak örneklerinde 2-3 yaprak aşamasında (259,85), en düşük ise 7-8 yaprak aşamasında (14,99) yaprak örneklerinde bulundu. G3 genotipinde XCT_MGT_7 geninin ekspresyon düzeyi yaprak örneklerinde 2-3 yaprak, 4-5 yaprak ve 6 yaprak evresinde en yüksek, en düşük ise 7-8 yaprak evresinde belirlendi. Aynı genotipte, XCT_MGC_6 geni, 4°C'de depolamadan sonra meristem numunesinde en yüksek ifadeye sahipti, ardından 7-8 yaprak aşamasında çiçek sürgünü numunesi geldi.
XCT_MGC_6 geninin en yüksek ekspresyon seviyesi, depolamadan önce meristem numunesinde tespit edildi ve genin nispi ekspresyon seviyesi, diğer gelişim aşamalarındaki meristem numunelerinde %50'den fazla azaldı. Aynı genotipteki XTG_MGA_10 geninin ekspresyon seviyesi, XCT_MGC_6 geninin ekspresyon seviyesine benzerdi. G5 genotipinde, XCT_MGT_7 geninin ekspresyon seviyesi 2–3 yaprak aşamasında en yüksek 0,30 seviyesindeydi ve depolama öncesi ve sonrasında meristem örneklerinde gen ekspresyonu tespit edilmedi.
G5 genotipinde XCT_MGC_6 geninin en yüksek ekspresyon seviyesi 4 ℃'de depolama sonrası meristem numunesinde (6,45) ve depolama öncesi meristem numunesinde XTG_MGA_10 geninin en yüksek ekspresyon seviyesi (1,33) belirlendi.

Çiçeklenen ve Çiçeklenmeyen Sarımsak Genotipleri Arasında cDNA-AFLP EST
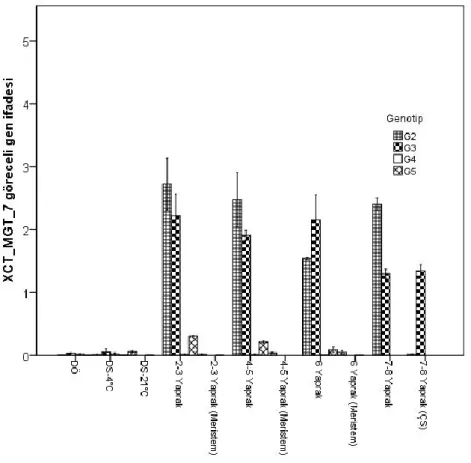
TÜBİTAK-TOVAG projesi 1050551'de cDNA-AFLP analizleri ile belirlenen XTG-MCG-13 EST gen bandı G1 ve G2 çiçeklenme gibi genotiplerin farklı gelişme dönemlerinden elde edilen yaprak örneklerinde gözlenirken, depolama örneklerinde gözlenmedi. faz. 2007 ve 2008 yetiştirme sezonlarında G1 ve G2 çiçekli genotiplerinden alınan yaprak örneklerinde TÜBİTAK-TOVAG proje tesisi 1050551 bünyesinde cDNA-AFLP analizleri ile XTG-MCG-13 EST geninin ok işaretli bant profili belirlenmiştir. XCT_MGT_7 EST geninin; çiçekli genotipler G2 ve G3'ün yaprak örneklerinde ifade edilir, ancak çiçeksiz sarımsak genotipleri G4 ve G5'te ifade edilmez.
XCT_MGT_7 EST geninin en yüksek ekspresyon düzeyi, çiçekli genotipin 2-3 yaprak-yaprak (2.47) ve 7-8 yaprak (2.41) dönemlerinde alınan yaprak örneklerinde olmuş, ancak bu üç dönem arasında istatistiksel olarak bir fark görülmemiştir. Bu tez çalışmasında, XCT_MGT_7 EST geninin ekspresyon düzeyi, daha önce tamamlanan TÜBİTAK-TOVAG projesi 1050551'de cDNA-AFLP analizi ile belirlenen bant profili ile uyumludur. TÜBİTAK-TOVAG 1050551 projesinde XCT-MGT-7 EST gen bandı, çiçekli genotip G1 ve G2'nin farklı gelişim dönemlerinden elde edilen yaprak örneklerinde saptanmış, çiçeksiz G3'ün yaprak örneklerinde ise saptanmamıştır. genotip (bu projede G4 olarak kodlanmıştır) (Şekil 4.5).
2007 ve 2008 yetiştirme sezonlarında çiçekli genotip G1 ve G2'den elde edilen yaprak örneklerinde TÜBİTAK-TOVAG projesi 1050551 kapsamında okla gösterilen cDNA-AFLP analizleri ile belirlenen XCT_MGT_7 EST gen bandı profili. XCT_MGT_7 EST geni ve NCBI gen bankaları, veri tabanındaki diğer türlerde tanımlanan genlerle benzerlikler bulmadı. XCT_MGT_7 EST geni için 1502 nükleotit uzunluğunda bir cDNA dizisi, NCBI veri tabanında sarımsak ve diğer Allium türlerinin EST'leri ile BLAST analizlerinde saptandı.
1050551 numaralı TÜBİTAK-TOVAG projesinin sonuçları ve Zhu vd. (2017) ve bu tez çalışmasının sonuçları, XCT_MGT_7 EST geninin çiçekli ve çiçeksiz sarımsak genotiplerinin yapraklarında, depolama aşamalarında ve meristem dokularında diferansiyel olarak eksprese edilen bir gen olduğunu göstermektedir.

SONUÇ 26
Dikim öncesi sıcaklık uygulamaları sırasında karbonhidratların diferansiyel gen ekspresyonu, meristem sonlandırmasını ve sarımsağın tomurcuklanmasını kontrol eder. Sarımsak çeşitliliği değerlendirmesi ve germplazm koleksiyonlarındaki varsayılan kopyaların saptanması için AFLP'lerin, RAPD işaretçilerinin ve izozimlerin karşılaştırılması. Sarımsakta tiamin biyosentezinde görev alan THIC geninin depolama süresince ekspresyon düzeyindeki değişimin belirlenmesi (tez çalışması, Bursa Uludağ Üniversitesi (Türkiye)).
Reproductive development and phenotypic differences in garlic are associated with expression and cleavage of LEAFY homologue gaLFY. Effect of nutrient, growth regulator and temperature on in vitro growth and organogenesis of excised tops of garlic (Allium sativum L.) cloves.