Avaliação da combinação de silibinina e benznidazol na atividade anti-Trypanosoma cruzi in vitro [manuscrito] / Arthur Marques Nascimento. Avaliação da combinação das drogas silibinina e benznidazol sobre a atividade de a -Trypanosoma cruzi in vitro Membros do comitê. Neste trabalho, a atividade in vitro de SLB e SLB associado a BZ (SLB+BZ) foi avaliada contra um isolado da cepa Y de T.
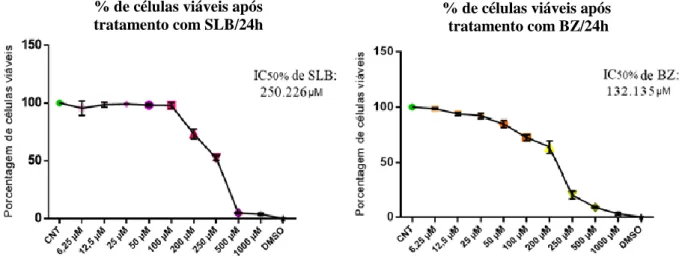
Neste estudo, a atividade in vitro de SLB e SLB ligada a BZ (SLB + BZ) contra T. 26 Figura 4: Desenho experimental para avaliação da atividade citotóxica e anti-T.cruzi de SLB, BZ e ligação SLB + BZ em diferentes concentrações in vitro usando células VERO e cepa Y. 289 Figura 5: Porcentagens (%) de viabilidade celular de células VERO após tratamento com SLB e BZ no ensaio MTT.
Portanto, este trabalho busca investigar o potencial farmacoterapêutico da combinação de um produto natural, SLB, com BZ em teste in vitro em diferentes doses.
REVISÃO DA LITERATURA
- A doença de Chagas e o Trypanosoma cruzi
- Sintomatologia e diagnóstico
- Quimioterapia
- Novos horizontes para o tratamento da doença de Chagas
- Produtos naturais: a silibinina
Segundo Zingales (2017), a criação e evolução natural da DCh depende de uma série de fatores, incluindo os aspectos imunológicos do próprio hospedeiro e as características genéticas do parasita. Além disso, podem ser observadas pequenas alterações no eletrocardiograma (ECG), alta frequência de arritmias, bradicardia, edema e até morte súbita (PRATA, 2001). Desde o final dos anos 60 e início dos anos 70, duas drogas têm sido utilizadas no tratamento da DC: o nifurtimox (NF) e o benznidazol (BZ) (COURA & CASTRO, 2002) que foram introduzidos empiricamente na terapia (URBINA , 2002). .
Além disso, os inúmeros efeitos colaterais contribuem para o abandono do tratamento, além de questionar o uso desses compostos com o mesmo esquema terapêutico entre a fase aguda e crônica (MUÑOS, MURCIA E SEGOVIA, 2011). Essa droga ideal, porém, ainda não existe e é objeto de muitas pesquisas na quimioterapia da CDh. Segundo Coura e Castro (2002), o grande desafio no tratamento da DCh concentra-se na busca de medicamentos e terapias que tenham a capacidade de promover a cura parasitológica em indivíduos tratados nas diferentes fases da doença, com baixa toxicidade. atividade oral em pequenas doses e baixa probabilidade de desenvolver resistência do parasita.
Dentre os planos de novas terapias, alguns tópicos podem ser considerados, como: o desvio de medicamentos como o uso de inibidores da biossíntese de ergosterol (IBE), um tipo de colesterol essencial para a membrana de fungos e tripanossomatídeos (FIUZA, 2018), a busca de novas drogas entre substâncias naturais, ou terapia combinada, onde as drogas existentes são associadas a BZ e NF. Dentre as propostas terapêuticas, a reorientação medicamentosa é promissora, pois consegue trazer novas aplicações para medicamentos já conhecidos (COURA, 2009), acelerando o processo de chegada do medicamento à população-alvo. A terapia combinada de medicamentos para o tratamento da DCh é cada vez mais defendida.
A combinação de drogas de diferentes classes químicas pode ser capaz de reduzir as doses e a duração do tratamento, resultando em menor incidência de efeitos colaterais. 25 Segundo Coura (2009), o controle de doenças como tuberculose, hanseníase e AIDS só era possível por meio do tratamento com associações de medicamentos com diferentes mecanismos de ação. Além disso, uma combinação eficaz de drogas pode aumentar a ação de diferentes compostos terapêuticos (sinérgicos) e prevenir o desenvolvimento de resistência ao tratamento do parasita.
Também é importante relatar que os dados da literatura confirmam muitos estudos que incluem combinações de drogas como uma opção para quimioterapia ChD, como BZ e cetoconazol (ARAÚJO et al., 2000), cetoconazol e terbinafina (MALDONADO et al., 1993) , BZ e aspirina, NF e aspirina (LOPEZ-MUÑOZ et al., 2009), BZ e diamidinas aromáticas (BATISTA et al, 2011). Assim, ao inibir a Pg-p, o SLB pode aumentar ou manter a concentração de drogas dentro das células por mais tempo (JABINI et al, 2015).
JUSTIFICATIVA
OBJETIVOS
Objetivos específicos
MATERIAIS E MÉTODOS
- Fármacos
- Silibinina
- Benznidazol
- Cepa de T. cruzi
- Linhagem celular
- Estudos da eficácia in vitro
- Estudo da atividade citotóxica de SLB e BZ por MTT
- Avaliação da atividade anti-T.cruzi de SLB e BZ sobre formas epimastigotas de cepa Y
- Estudo da atividade anti-T. cruzi sobre formas amastigotas
Para a preparação das placas de teste, as células contidas nos frascos de cultura de 75 cm2 foram lavadas com PBS estéril, seguida da adição de 3 mL de Tripsina e incubadas por 5 minutos a 37°C. Ao conteúdo por tripsinização foram adicionados 6 ml de meio DMEM F12, seguido de centrifugação a 1700 rpm por 10 minutos em temperatura ambiente. 30 em câmara de Neubauer usando Trypan® Blue, o número de células VERO plaqueadas (10.000 células por poço) foi determinado de acordo com a metodologia padronizada do Laboratório de Doença de Chagas (LADOC) baseada em Mosmann (1983).
O teste de citotoxicidade in vitro MTT é o teste padrão ouro utilizado pelo FDA (U.S. Food and Drug Administration) com base nos padrões propostos pela International Organization for Standardization, ISO para a avaliação biológica de dispositivos médicos (FDA, 2012). 31 A partir da porcentagem de inibição de cada concentração de droga, o IC50 (concentração de droga que reduz a viabilidade celular em 50%) foi calculado usando o programa CompuuSyn. O IC50 (concentração do fármaco inibitório que causa 50% do efeito analisado, inibição da proliferação celular) foi calculado a partir do percentual de inibição das concentrações individuais do fármaco utilizando o programa CompuSyn.
Um total de 1,0 x 104 células VERO foram semeadas em lamínulas circulares de 13 mm de diâmetro, colocadas em placas de 24 poços e incubadas por 24 horas a 37ºC, 5% de CO2 e posteriormente infectadas com tripomastigotas derivados da cultura da cepa Y. em Células VERO, na proporção de 20:1 parasitas/células. A cada poço foi adicionado meio de cultura fresco, contendo ou não substâncias SLB e BZ em diferentes concentrações (conforme descrito e indicado no desenho experimental, figura), ajustado para um volume final de 1 ml/poço. Lamelas contendo células foram lavadas com PBS 1x estéril, fixadas com metanol e então coradas com solução de Giemsa (10% em água destilada).
Para determinar o efeito do tratamento de células infectadas tratadas com diferentes concentrações de compostos SLB e BZ, o índice endocítico (IE) foi calculado. Utilizando estes dados, calculou-se a percentagem de inibição da infecção das células tratadas relativamente às células infectadas e não tratadas. Essa porcentagem de inibição foi então usada para construir curvas dose-efeito e calcular o IC50 usando o software Graph Pad Prism 6 e CompuSyn.

RESULTADOS
Estudo de citotoxicidade em células VERO utilizando o MTT
Avaliação da atividade anti- T. cruzi em formas epimastigotas
Os resultados mostram que o BZ foi capaz de eliminar um maior número de epimastigotas em concentrações menores que o SLB.
Avaliação anti-T. cruzi em formas amastigotas em células VERO
Houve diferença na porcentagem (%) de amastigotas entre o controle não tratado e os grupos tratados com as drogas SLB e BZ a partir das menores concentrações (6,25uM para SLB e 2,5uM para BZ). As maiores concentrações de SLB (100 e 25 µM) que garantiram 99% de sobrevivência das células VERO (conforme teste de citotoxicidade item 6.1) induziram inibição de 23,28 e 56,85% respectivamente de amastigotas em células VERO se for considerado o índice endocítico percentual. inibição (% média de células infectadas x número médio de amastigotas por célula infectada). O 36-drug BZ apresentou um percentual de inibição de amastigotas em células VERO de 23,61% em sua maior concentração testada, 10 µM (o que também garantiu uma média de 99% de viabilidade celular no teste de citotoxicidade).
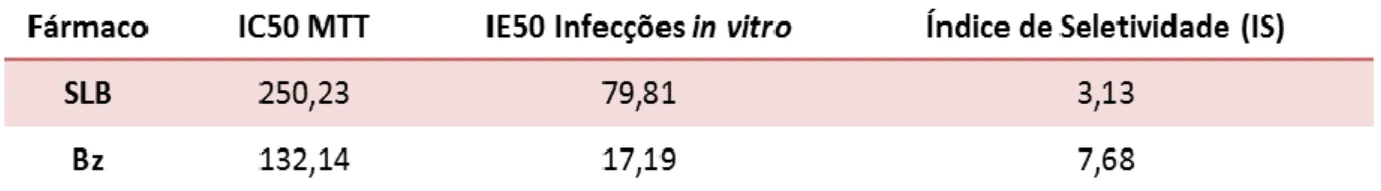
De acordo com o teste com as drogas em associação, observou-se que todas as diferentes associações apresentaram alguma atividade anti-T. A associação SLB100+BZ10 µM foi a que deu o melhor resultado, superior às outras associações e aos medicamentos . SLB e BZ em monoterapia, resultando em 91,44% de inibição de amastigotas em comparação com CNT. Os índices de seletividade (IS - razão do IC 50 obtido no teste de citotoxicidade MTT, dividido pelo IC 50 obtido de cada composto (SLB e BZ) em amastigotas após 24 h de incubação) foram calculados a seguir.
DISCUSSÃO
Portanto, neste estudo procuramos avaliar testes in vitro do produto natural, SLB, isolado e também combinado com o medicamento de referência BZ, enquanto investigamos a estratégia de combinação de medicamentos. Nos últimos anos, o número de pesquisas sobre as atividades biológicas do SLB tem aumentado devido à grande variedade de importantes efeitos farmacológicos associados a esse composto (DE OLIVEIRA et al, 2015). A atividade antifúngica do SLB torna-se interessante para DCh porque, semelhante aos antifúngicos da classe IBE (itraconazol, cetoconazol, posaconazol, etc.)
39 Além dessas possibilidades, o SLB também possui atividade anti-inflamatória (GREENLEE, 2007), o que pode contribuir para a melhora dos danos teciduais causados pelo T. Este estudo começou avaliando a toxicidade in vitro do composto silibinina em células VERO com o método MTT. Em relação ao SLB IC50 encontrado neste estudo, o resultado foi superior ao do grupo de Elhag et al. (2015) que encontraram valores de SLB IC50 como 40 μM para a linhagem A127 e 200 μM para LN229.
Após o estudo de citotoxicidade pelo método MTT, o efeito tripanocida do SLB sobre parasitas foi avaliado in vitro. Isso pode levar a pensar que a estratégia de combinação dessas drogas pode alcançar resultados positivos na atividade anti-T. Finalmente, com base nos resultados do experimento de citotoxicidade do MTT, as concentrações de SLB e BZ a serem utilizadas no ensaio em células infectadas. com amastigotas de T.
Por outro lado, o BZ em sua maior concentração, que manteve 100% de viabilidade celular (10 µM), apresentou uma redução percentual de infecção de 23,61%, o mesmo observado na concentração de 25 µM de SLB. Segundo Mazzeti (2014), não se pode esperar que estudos de terapia combinada in vitro determinem a eficácia de uma determinada combinação em tratamentos clínicos futuros. Por outro lado, os efeitos e interações observados in vitro suportam os estudos pré-clínicos in vivo.
CONSIDERAÇÕES FINAIS
CONCLUSÃO
Suscetibilidade e resistência natural de cepas de Trypanosoma cruzi a drogas utilizadas clinicamente na doença de Chagas. Identificação de novos compostos que inibem a síntese de ergosterol como potenciais drogas para a terapia da doença de Chagas. Cumarinas isoladas de Calophyllum brasiliense produzem alterações ultraestruturais e afetam a infectividade in vitro do Trypanosoma cruzi.
Evaluation of in vitro anti-Trypanosoma cruzi activity of medications benznidazole, amiodarone hydrochloride, and their combination. Rationale and design of a randomized placebo-controlled trial assessing the effects of etiological treatment in Chagas' cardiomyopathy: the Benznidazole evaluation for the interruption of trypanosomiasis (BENEFIT). Trypanosoma cruzi benznidazole susceptibility in vitro does not predict therapeutic outcome of human Chagas disease.
The urgent need to develop new drugs and devices for the treatment of Chagas disease.