Este trabalho apresenta uma proposta de experimento de cromatografia em coluna utilizando materiais alternativos, de fácil acesso e baixo custo, para ser implementado em aulas introdutórias de Química Orgânica. Normalmente, o que é abordado nas aulas que envolvem cromatografia é a cromatografia em papel, por ser o tipo de cromatografia de menor custo.
Considerações Gerais
A cromatografia em coluna é considerada uma das principais técnicas de separação, portanto, para o sucesso da implementação desta técnica, é fundamental que nas aulas de química orgânica haja pelo menos uma atividade experimental que explore este tema e que o aluno consiga manipular e compreender, de forma eficaz. na prática, como funciona esse método. Este trabalho apresenta a técnica clássica de cromatografia em coluna do ponto de vista qualitativo, utilizando materiais alternativos de fácil acesso e baratos, e a utilização desses materiais não reduz a qualidade do processo.
Misturas e técnicas de separação
Cromatografia
Técnicas cromatográficas
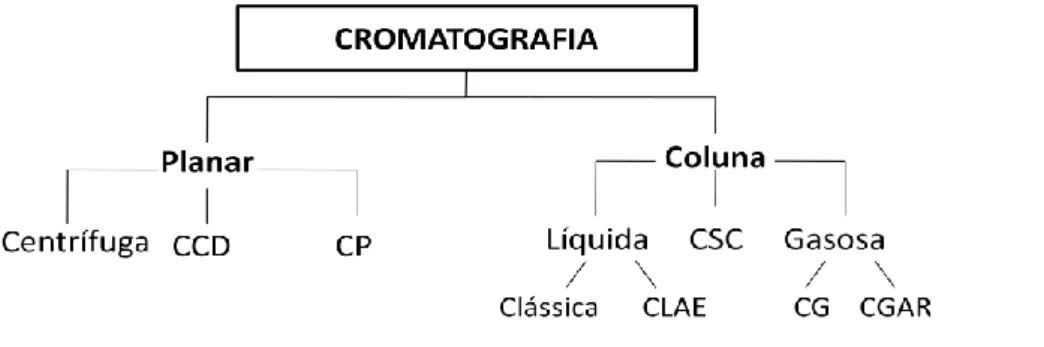
Vários tipos de cromatografia são possíveis, dependendo da natureza das fases envolvidas: métodos de cromatografia sólido-líquido (coluna, camada fina e papel), líquido-líquido (líquido de alto desempenho) e gás-líquido (vapor) são comuns (ENGEL et al., 2012; CAZES, 2002). CCD- cromatografia em camada delgada; CP- Cromatografia em Papel; HPLC - Cromatografia Líquida de Alta Eficiência; Cromatografia supercrítica CSC; GC- cromatografia gasosa; CGAR - cromatografia gasosa de alta resolução).
Cromatografia em coluna
À medida que cada uma dessas bandas passa pelo fundo da coluna, ela é coletada (ENGEL et al., 2012). Alguns parâmetros que influenciam na separação são a escolha dos adsorventes (fase estacionária) dos solventes (fase móvel) e o tamanho da coluna.

Experimentação e Contextualização no ensino de Química
O objetivo básico do ensino de Química para formar cidadãos inclui a abordagem de informações químicas básicas que possibilitem ao aluno participar ativamente da sociedade tomando decisões com consciência de suas consequências. No ensino de química, a experimentação pode ser considerada um método/ferramenta eficaz para criar situações-problema que busquem questionamentos dos alunos, onde eles possam relacionar o conhecimento prévio ao conhecimento contextualizado (apud. NASCIMENTO, 2013). O uso da contextualização no ensino de química é orientado pelos parâmetros curriculares nacionais para o ensino médio quando propõem (BRASIL, 1999) a utilização de experiências e fatos do cotidiano dos alunos, da tradição cultural para a construção do conhecimento químico, permitindo leituras repetidas do mundo (SILVA; MARCONDES, 2010).
Segundo a teoria de David Ausubel, a dicotomia teoria-prática e o conhecimento prévio do aluno devem caminhar juntos para a aprendizagem significativa e cognitiva do aluno (MOREIRA; MASINI, 2001). Diante disso, além de uma proposta de aula experimental de química orgânica com materiais alternativos, com direcionamento e abordagem para o ensino superior, mas também facilmente adequada para o ensino médio, a escolha direcionada de corantes alimentícios como amostra foi pensada com o objetivo de realizar uma abordagem contextualizada com suas estruturas químicas, durante o experimento e a explicação do método, com a teoria estudada, já que o assunto das disciplinas acadêmicas são funções orgânicas.
Corantes alimentícios
Corantes orgânicos artificiais
Quando um corante azo (vermelho escarlate) foi injetado sob a pele da orelha de um coelho, foi observado crescimento celular atípico sob a pele.
Objetivo geral
Objetivos específicos
Experimentos com materiais alternativos e sua relevância
Cromatografia com materiais alternativos
Dados os referenciais teóricos estudados, a utilização de fases estacionárias alternativas, como açúcar, fécula de batata, entre outras, requer principalmente solventes apolares, como Hexano e Éter de Petróleo. Neste caso, embora a fase estacionária utilizada seja alternada, a fase móvel não o é, o que foge ao objetivo do trabalho. Assim, para este trabalho, o método mais adequado à amostra a ser cromatografada foi o de Celeghini e Ferreira (1998), em que utilizaram areia e etanol comercial como fases estacionárias e móveis, respectivamente.
A decisão pela utilização da areia como fase estacionária deveu-se à sua fácil localização tanto no litoral (areia de praia) quanto no interior (areia de rio), que também pode ser obtida em canteiros de obras ou em lojas de materiais de construção, e principalmente por conter sílica em sua composição. A utilização da areia como fase estacionária possibilita a utilização de fases móveis polares como etanol e água, pois a escolha desses solventes está diretamente relacionada à amostra escolhida, conforme mostrado na discussão apresentada posteriormente.
Adequação da fase estacionária
A areia de praia utilizada nestes testes veio da Praia de Pituaçú, em Salvador-Ba, e a areia de rio foi fornecida por uma casa de material de construção da cidade de Amargosa-Ba. Primeiramente, a areia foi peneirada (peneira de cozinha) para retirar pedras maiores e outros materiais indesejados. Em seguida, foram lavados com água e deixados em solução de ácido sulfúrico 6 M, ou solução de bateria comercial, por 24 horas para remoção de possível matéria orgânica.
Em seguida foram lavados com água em abundância até que o pH da água de lavagem ficasse entre 6,0 e 7,0 e por fim foram secos em estufa a 100 ºC por 4 horas.
Adequação da fase móvel
Preparação da coluna
Estudos das fases estacionárias
Peneiração
Microscopia eletrônica de varredura- MEV
Separação cromatográfica
Os resíduos deste experimento são compostos por: areia, que pode ser lavada com água e reaproveitada após secagem; etanol e água, que podem ser separados por destilação, e corantes, que podem ser jogados na pia, pois são comumente usados como alimento.
Amostra
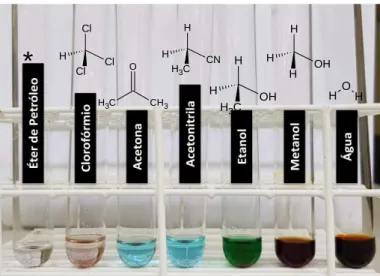
Solubilidade dos corantes
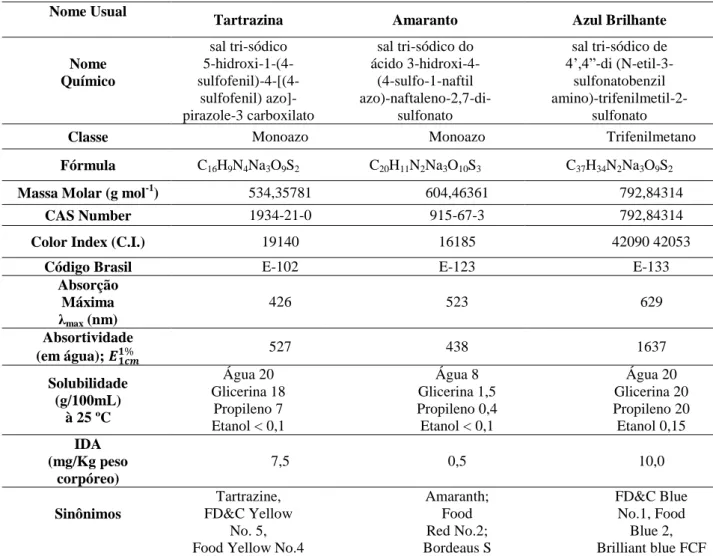
Caracterização da amostra
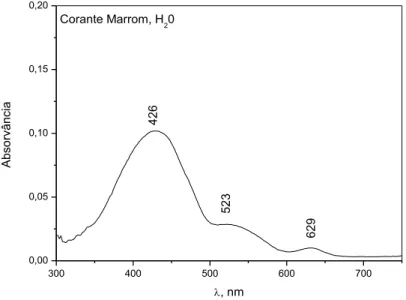
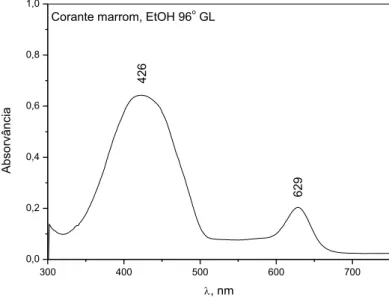
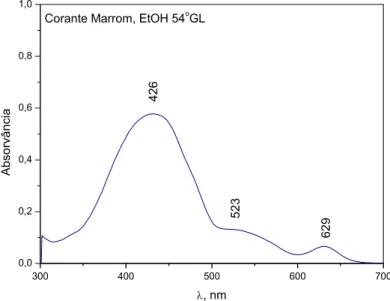
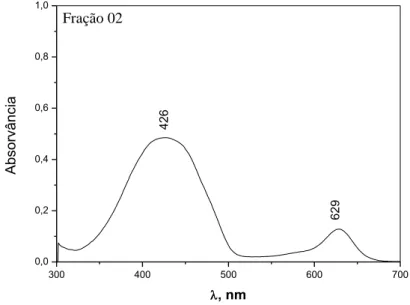
A acetona e a acetonitrila seriam bons solventes para separar o azul brilhante da tatrazina, evitando assim a presença da segunda fração esverdeada, que é o único contaminante, além do metanol, que por ser muito polar, dissolveria o corante Amaranto como a água . Pode-se observar que ao retirar a presença de água do solvente utilizando etanol 96ºGL (Figura 6), a banda de absorção do Amaranto (comprimento de onda máximo de absorção em 523 nm) desaparece do espectro, restando a tartrazina e a luz azul (λ máx. em 426nm). e 629 nm) (PRADO; GODOY, 2003).
Ensaios cromatográficos
A fase móvel utilizada foi Etanol 96ºGL para remoção dos corantes Azul Brilhante e Tartrazina, e Etanol 54ºGL para remoção do Amaranto. Com base nisso, foi considerada uma terceira possibilidade, a utilização da areia de praia como fase estacionária, por apresentar grãos menores que a areia de rio. Assim, a cromatografia foi realizada utilizando 100% areia de praia (ensaio 04), e a fase móvel utilizada foi a mesma dos ensaios anteriores.
Outros testes foram realizados com a mesma fase estacionária (100% areia de praia), pois esta deu os melhores resultados. Assim, o teste 04, com 100% areia de praia como fase estacionária, e Etanol 96 ºGL como fase móvel (que pode ser substituído pelo Etanol da estação), e Etanol 54 ºGL foi o teste com melhores resultados, e o mesmo seria utilizado como proposta para aulas experimentais.

Análise das fases estacionárias estudadas
Amido
Diante desta análise, o tamanho do grânulo de amido é da ordem de grandeza em micrômetros (µm), ou seja, bem menor em relação aos demais tipos de grânulos utilizados nesta pesquisa. Embora a eficiência do método cromatográfico esteja relacionada à compactação, nem sempre ele é viável. Os resultados experimentais utilizando peneira estão compilados na Figura 11 para todas as fases estacionárias utilizadas.
Com estes resultados pode-se confirmar que o tamanho do grão do amido é, em sua maior parte, menor que 170 mesh, ou seja (88 µm). Assim, embora a eficiência da coluna esteja relacionada ao empacotamento, a alta compressão muitas vezes não é viável.
![Figura 10- A) Estrutura da amilose [polímero linear composto por D-glicoses unidas em (1-4)]](https://thumb-eu.123doks.com/thumbv2/123dok_br/19675037.0/38.892.196.795.226.456/figura-estrutura-amilose-polímero-linear-composto-glicoses-unidas.webp)
Areias (Rio e Praia)
Embora a areia de praia seja muito semelhante em tamanho de grão à areia de rio, foi realizada uma análise de Microscopia Eletrônica de Varredura, analisando o tipo de superfície dos grãos (Figura 12). Na Figura 12 é possível observar o comportamento irregular da areia de rio, com poros, diferentemente da areia de praia e da sílica, que apresentam regularidade em suas superfícies. Na Figura 12a (areia de rio) há um aumento de 100 vezes para poder observar um grão inteiro, na Figura 12b (areia de praia) há um aumento de 1000 vezes, isso justifica que a areia da praia seja cerca de 10 vezes menor que a de um rio, garantindo maior compactação e maior eficiência na coluna.

Separação cromatográfica
Para potenciar a discussão com os alunos é fundamental saber analisar a influência que a estrutura química dos corantes tem na fase móvel. Portanto, os únicos solventes utilizados neste trabalho foram Etanol 96ºGL (ou Etanol Estacionário), Etanol 54ºGL e Água. O corante Tartrazina (C16 H9N4Na3O9S2) (Figura 19) possui um grupo menos sulfonado que o Amaranto e um grupo carboxilato adicional, o que lhe confere uma polaridade menor (ROSA; SCHELEDER, 2016), portanto sua solubilidade em água é menor (20g/100mL a 25ºC) (PRADO; GODOY, 2003), fazendo com que a polaridade do etanol seja suficiente para retirá-lo da coluna.
Nos testes realizados no presente trabalho, o corante Azul Brilhante (C37H34N2Na3O9S3) (Figura 20a) foi o primeiro a ser retirado da coluna. No teste realizado por Rosa e Scheleder (2016), destacam que a retirada do corante Fast Green (Figura 20b), da primeira coluna, se deve ao número de carbonos e à sua estrutura mais complexa.
Coluna cromatográfica
Possui grandes semelhanças com outro corante, Fast Green (Figura 20b), que foi utilizado no trabalho de Rosa e Scheleder (2016). Sua semelhança se deve à quantidade de carbono, em sua estrutura mais complexa, nos grupos sulfonados e no grupo imínio quaternário. Embora existam grupos sulfonados, sua estrutura mais complexa, com cadeia de carbono mais longa e grupo imínio quaternário, pode neutralizar um grupo SO3.
O resultado deste teste foi promissor, pois nada muda em termos de tempo, quantidade de material ou eficiência do método, em comparação com a coluna de vidro. Assim, além de utilizar a fase móvel e estacionária com materiais alternativos, a própria coluna passou a ser feita com materiais da mesma natureza.
Aula experimental
Havia um total de 6 alunos na turma, que foram divididos em 2 grupos que realizaram o mesmo procedimento mas com duas colunas diferentes, uma coluna convencional (de vidro) e uma coluna feita de materiais alternativos. A Química é uma ciência experimental, portanto os estudantes de Química precisam aprender, conhecer e aprimorar tanto conhecimentos teóricos quanto experimentais, sendo que estes últimos são muito difíceis de desenvolver seja por falta de recursos ou de oportunidades. Os objetivos do trabalho foram alcançados, pois a técnica proposta foi desenvolvida com sucesso com materiais alternativos.
O procedimento adotado foi adaptado ao modelo de uma aula experimental tradicional e a opinião do professor sobre este procedimento foi positiva, o que torna a adoção deste procedimento promissora para futuras aulas de Química Orgânica Experimental. Aplicação de aulas experimentais de química com materiais alternativos provenientes de resíduos e materiais domésticos no ensino de jovens e adultos (EJA).