Síntese, caracterização e estudo das propriedades magnéticas
de ortoferritas de lantânio dopadas com manganês
Andréia Cavalcante de Lima
_______________________________________
Tese de Doutorado
Natal/RN, dezembro de 2010
UNIVERSIDADE FEDERAL DO RIO GRANDE DO NORTE
CENTRO DE CIÊNCIAS EXATAS E DA TERRA
SÍNTESE, CARACTERIZAÇÃO E ESTUDO DAS PROPRIEDADES MAGNÉTICAS DE ORTOFERRITAS DE LANTÂNIO DOPADAS COM MANGANÊS
Tese apresentada ao Programa de Pós-Graduação em Química da Universidade Federal do Rio Grande do Norte, em cumprimento às exigências para obtenção do título de Doutora.
Orientadora: Profa. Dra. Dulce Maria de Araújo Melo
Co-orientador: Prof. Dr. José Humberto de Araújo
Divisão de Serviços Técnicos
Catalogação da Publicação na Fonte. UFRN / Biblioteca Setorial do Instituto de Química
Lima, Andréia Cavalcante de.
Síntese, caracterização e estudo das propriedades magnéticas de ortoferritas de lantânio dopadas com manganês / Andréia Cavalcante de Lima. Natal, RN, 2010
154 f.
Orientadora:Dulce Maria de Araújo Melo. Co-Orientador: José Humberto de Araújo
Tese (Doutorado em Química) - Universidade Federal do Rio Grande do Norte. Centro de Ciências Exatas e da Terra. Programa de Pós-Graduação em Química.
1. Inorganica– Tese. 2. Ortoferritas – Tese. 3. Método Pechini – Tese. 4. Reação de combustão – Tese. 5. Ferromagnetismo fraco – Tese. I. Melo, Dulce Maria de Araújo. II. Araújo, José Humberto de. III. Universidade Federal do Rio Grande do Norte. IV. Título.
Dedico esta conquista aos meus pais, irmãos e ao meu sobrinho querido.
Aos meus avós (in memorian) que não puderam compartilhar comigo esta vitória. Agradeço por tudo que fizeram por mim.
A Deus, por estar ao meu lado nas horas difíceis e me permitir a concretização de mais uma etapa importante na minha vida.
A Profa. Dra. Dulce Maria de Araújo Melo pela orientação, paciência, confiança e contribuição para o desenvolvimento do trabalho.
Ao Prof. Dr. José Humberto de Araújo pela co-orientação, incentivo, amizade e ajuda com relação ao refinamento pelo método Rietveld e histereses magnéticas.
As Professoras, Dra. Joana D´arc Gomes da Silva e Dra. Sibele Berenice Castelã Pergher, pelas valiosas sugestões dadas durante o exame de qualificação para o melhoramento da tese.
Aos Professores, Dr. Francisco das Chagas Dantas de Lemos e Dr. Artur da Silva Carriço, por aceitarem participar da banca de defesa da tese. Em especial ao Professor Artur pelo estímulo e confiança depositados.
Ao pesquisador Dr. Juan Alberto Chavez Ruiz por aceitar participar da banca de defesa, pelas análises de RTP realizadas no Centro de Tecnologias do Gás e Energias Renováveis (CTGAS-ER) e, principalmente pela atenção, paciência e ajuda com a interpretação dos resultados.
Ao Prof. Dr. Ademir Oliveira da Silva pela amizade e colaboração na realização das análises termogravimétricas.
Aos técnicos, Érico e Artejose, dos laboratórios de Difratometria de Raios X e Microscopia Eletrônica de Varredura do Núcleo de Estudos em Petróleo e Gás Natural (NEPGN) pela realização das respectivas análises.
Aos amigos do Laboratório de Análise Térmica e Materiais (LATMAT), Ana Paula, Danielle Karinne, Valdelice, Patrícia, Rosane, Moisés, Letícia, Daliane, Felipe e Juliana, pela ótima convivência no ambiente de trabalho e pelas horas de descontração. Um agradecimento em especial as minhas amigas Klécia, Ana Paula, Danielle Karinne e Valdelice, que sempre me deram força e incentivaram nos momentos difíceis.
Aos amigos do Laboratório de Magnetismo e Materiais Magnéticos (LMMM), Armando, Rodolfo, Raquel e Kaliane, por terem me recebido de braços abertos, pela amizade e ótima convivência.
“O homem se torna muitas vezes o que ele
próprio acredita que é. Se insisto em repetir para mim mesmo que não posso fazer uma determinada coisa, é possível que acabe me tornando realmente incapaz de fazê-la. Ao contrário, se tenho a convicção de que posso fazê-la, certamente adquirirei a capacidade de realizá-la, mesmo que não a tenha no começo.”
Ortoferritas AFeO3 (A = terra rara) constituem uma importante classe de óxidos perovskita que exibem ferromagnetismo fraco. Estes materiais encontram inúmeras aplicações como sensores químicos, catodos para células a combustíveis e na área de catálise, o que os fazem interessantes do ponto de vista científico e tecnológico. Suas propriedades estruturais, elétricas e magnéticas são dependentes de vários fatores tais como: o método de preparação, condições do tratamento térmico, composição química e substituição de cátions nos sítios A e/ou B. Neste trabalho, ortoferritas do tipo LaFe1-xMnxO3 (0 ≤ x ≤ 1) foram preparadas pelo método Pechini e pela reação de combustão assistida por microondas com a finalidade de avaliar a influência da rota de síntese na formação do óxido, assim como o efeito da substituição parcial do ferro por manganês e do tratamento térmico nas propriedades magnéticas. Os pós precursores foram calcinados a 700°C, 900°C, 1100°C e 1300°C por 4 horas e caracterizados através das técnicas: Análise termogravimétrica (TG), Difração de raios X (DRX), Refinamento pelo método de Rietveld, Microscopia eletrônica de varredura (MEV), Redução a temperatura programada (RTP) e Medidas de histerese magnéticas realizadas à temperatura ambiente. De acordo com os difratogramas, a formação da fase perovskita com estrutura ortorrômbica foi observada para os sistemas onde 0 ≤ x ≤ 0,5 e, romboédrica para x = 1. Os resultados também mostraram uma diminuição dos parâmetros de rede com a substituição parcial do ferro por manganês e, conseqüentemente uma redução do volume da célula unitária. As curvas de histerese exibiram ferromagnetismo fraco para os sistemas preparados por ambos os métodos de síntese. Entretanto, uma dependência da magnetização em função do teor de dopante foi observada para as amostras produzidas pelo método Pechini. Já para os sistemas preparados por reação de combustão, verificou-se que as fases secundárias exercem forte influência no comportamento magnético.
Orthoferrites AFeO3 (A = rare earth) are an important class of perovskite oxides that exhibit weak ferromagnetism. These materials find numerous applications as chemical sensors, cathodes for fuel cells and catalysis, which make them interesting from the standpoint of science and technology. Their structural, electrical and magnetic properties are dependent on many factors such as the preparation method, heat treatment conditions, chemical composition and replacement of cations in sites A and/or B. In this paper, LaFe1-xMnxO3 (0 ≤ x ≤ 1) orthoferrites-type was prepared by Pechini method and Microwave-assisted combustion reaction in order to evaluate the influence of synthesis route on the formation of oxide, as well as the effect of parcial replacement of iron by manganese and heat treatment on the magnetic properties. The precursor powders were calcined at 700°C, 900°C, 1100°C and 1300°C for 4 hours and they were characterized by the techniques: Thermogravimetric analysis (TGA), X ray diffraction (XRD), Refinement by Rietveld method, Scanning electron microscopy (SEM), Reduction temperature programmed (RTP) and Magnetic hysteresis measurements performed at room temperature. According to the XRD patterns, the formation of perovskite phase with orthorhombic structure was observed for the systems where 0 ≤ x ≤ 0.5 and rhombohedral for x = 1. The results also showed a decrease of lattice parameters with the parcial replacement of iron by manganese and consequently a reduction in cell volume. The hysteresis curves exhibited weak ferromagnetism for the systems prepared by both synthesis methods. However, a dependence of magnetization as a function of dopant content was observed for samples produced by Pechini method. As for the systems prepared by combustion reaction, it was found that the secondary phases exert a strong influence on the magnetic behavior.
Figura 2.1 - Representação dos movimentos dos elétrons: (a) movimento orbital ao redor do núcleo e (b) movimento spin em torno do próprio eixo... 22
Figura 2.2 - Tipos de magnetismo encontrados nos materiais... 26
Figura 2.3 - Esquema (A) parede de domínios e (B) ordenação dos
momentos em uma parede de domínios adjacentes... 27
Figura 2.4 - Curva de magnetização para um material ferromagnético inicialmente desmagnetizado. As configurações de domínios estão representadas durante os vários estágios de magnetização até a magnetização de saturação... 28
Figura 2.5 - Curva de histerese magnética típica de um material Ferromagnético...
30
Figura 2.6 - Variação da coercividade com o tamanho da partícula... 31
Figura 2.7 - Configuração de spin na superfície de uma nanopartícula... 33
Figura 2.8 - Representação da estrutura ideal cúbica da perovskita... 35
Figura 2.9 - Estrutura perovskita com distorções: (a) romboédrica e (b)
Ortorrômbica... 36
Figura 2.10 - Representação geométrica dos orbitais s, p e d... 39
Figura 2.11 - Projeção dos orbitais (a) dxy e (b) dx2-y2, e dos orbitais p dos íons oxigênio, no plano xy... 40
Figura 2.12 - Efeito do campo cristalino em um octaedro... 41
Figura 2.13 - Diagrama de energia dos orbitais d de um metal de transição (a) livre, (b) em um octaedro perfeito e (c) com deformação Jahn Teller...
42
Figura 2.14 - Representação da ligação M-O mostrando a comparação entre a troca direta e a indireta (super troca). A super troca estabiliza o antiferromagnetismo. A troca direta é comumente
ferromagnética... 43
Figura 2.15 - Representação esquemática do mecanismo de dupla troca (a) antes e (b) depois do elétron de condução trocar de íon
manganês... 44
Figura 4.1 - Fluxograma da síntese e caracterização do sistema LaFe1-xMnxO3 (0 ≤ x ≤ 1) preparado pelo método Pechini... 67
Figura 4.2 - Fluxograma da síntese e caracterização do sistema LaFe1-xMnxO3 (0 ≤ x ≤ 1) preparado pela reação de combustão
assistida por microondas... 69
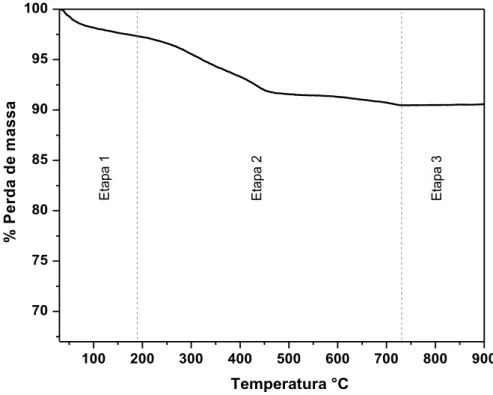
Figura 5.1 - Curva TG do pó precursor do sistema LF preparado pelométodo Pechini e tratado a 300°C por 4h... 78
Figura 5.2 - Curvas TG dos pós precursores dos sistemas LFM1, LFM3 e LFM5 preparados pelo método Pechini e tratados a 300°C
por4h... 78
Figura 5.3 - Curva TG do pó precursor do sistema LM preparado pelo
método Pechini e tratado a 300°C por 4h... 79
Figura 5.4 - Curva TG do pó precursor do sistema LF preparado pela reação
de combustão assistida por microondas... 81
Figura 5.5 - Curvas TG dos pós precursores dos sistemas LFM1, LFM3 e LFM5 preparados pela reação de combustão assistida por
microondas... 82
Figura 5.6 - Curva TG do pó precursor do sistema LM preparado pela
reação de combustão assistida por microondas... 82
Figura 5.7 - Padrões de Difração de raios X do sistema LaFe1-xMnxO3
(0 ≤ x ≤ 1) preparado pelo método Pechini e tratado a 700°C por
4h. ▲ = LaMnO3, ❖ = LaFe0,5Mn0,5O3, ■ = LaFe0,7Mn0,3O3, ● =
LaFe0,9Mn0,1O3, ♦ = LaFeO3, ▽ = Fe2O3... 85
Figura 5.8 - Padrões de Difração de raios X do sistema LaFe1-xMnxO3
(0 ≤ x ≤ 1) preparado pelo método Pechini e tratado a 900°C por 4h. ▲ = LaMnO3, ❖ = LaFe0,5Mn0,5O3, ■ = LaFe0,7Mn0,3O3, ● =
LaFe0,9Mn0,1O3, ♦ = LaFeO3, ▽ = Fe2O3... 89
Figura 5.9 - Padrões de Difração de raios X do sistema LaFe1-xMnxO3
(0 ≤ x ≤ 1) preparado pelo método Pechini e tratado a 1100°C
por 4h. ▲ = LaMnO3, ᄋ= Mn2O3, ❖ = LaFe0,5Mn0,5O3, ■ =
por 4h. ▲ = LaMnO3, ❖ = LaFe0,5Mn0,5O3, ■ = LaFe0,7Mn0,3O3, ●
= LaFe0,9Mn0,1O3, ♦ = LaFeO3, ▽ = Fe2O3... 95
Figura 5.11 - Padrões de difração de raios X do sistema LaFe1-xMnxO3
(0 ≤ x ≤ 1) preparado pela reação de combustão assistida por
microondas e tratado a 700°C por 4h. ▲ = LaMnO3, ❖ = LaFe0,5Mn0,5O3, ■ = LaFe0,7Mn0,3O3, ☐ = La(OH)3, ● =
LaFe0,9Mn0,1O3, ♦ = LaFeO3, ▽ = Fe2O3... 98
Figura 5.12 - Micrografias do sistema LaFe1-xMnxO3 preparado pelo método Pechini e tratado a 700°C por 4h. (a) LF, (b) LFM1, (c) LFM3,
(d) LFM5 e (e) LM... 102
Figura 5.13 - Micrografias do sistema LaFe1-xMnxO3 preparado pelo método Pechini e tratado a 900°C por 4h. (a) LF, (b) LFM1, (c) LFM3,
(d) LFM5 e (e) LM... 104
Figura 5.14 - Micrografia do sistema LaFe1-xMnxO3 preparado pelo método Pechini e tratado a 1100°C por 4h. (a) LF, (b) LFM1, (c) LFM3,
(d) LFM5 e (e) LM... 106
Figura 5.15 - Micrografia do sistema LaFe1-xMnxO3 preparado pelo método Pechini e tratado a 1300°C por 4h. (a) LF, (b) LFM1, (c) LFM3,
(d) LFM5 e (e) LM... 107
Figura 5.16 - Micrografia do sistema LaFe1-xMnxO3 preparado pela reação de combustão assistida por microondas e tratado a 700°C por 4h.
(a)LF, (b) LFM1, (c) LFM3, (d) LFM5 e (e) LM... 109
Figura 5.17 - Perfil de RTP do sistema LFM3 preparado pelo método Pechini
e tratado a 900°C por 4h... 111
Figura 5.18 - Perfis de RTP do sistema LFM5 preparado pelo método Pechini
e tratado em diferentes temperaturas... 113
Figura 5.19 - Perfil de RTP do sistema LFM5 preparado pela reação de
combustão assistida por microondas e tratado a 700°C por 4h.... 114
Figura 5.20 - Curvas de histerese do sistema LaFe1-xMnxO3 (0 ≤ x ≤ 1)
preparado pelo método Pechini e tratado a 700°C por 4h... 116
Figura 5.21 - Curvas de histerese do sistema LF preparado pelo método
Pechini e tratado em diferentes temperaturas... 118
Figura 5.22 - Curvas de histerese do sistema LFM1 preparado pelo método
Pechini e tratado em diferentes temperaturas... 123
Figura 5.24 - Curvas de histerese do sistema LFM5 preparado pelo método
Pechini e tratado em diferentes temperaturas... 126
Figura 5.25 - Curvas de histerese do sistema LM preparado pelo método
Pechini e tratado a 700°C e 900°C por 4h... 128
Figura 5.26 - Curvas de histerese do sistema LM preparado pelo método
Pechini e tratado a 1100°C e 1300°C por 4h... 129
Figura 5.27 - Curvas de histerese dos sistemas LF e LFM1 preparados pela reação de combustão assistida por microondas e tratados a
700°C por 4h... 130
Figura 5.28 - Curvas de histerese dos sistemas LFM3 e LFM5 preparados pela reação de combustão assistida por microondas e tratados
a 700°C por 4h... 131
Figura 5.29 - Curva de histerese do sistema LM preparado pela reação de
Tabela 4.1 - Nomenclatura do sistema LaFe1-xMnxO3 (0 ≤ x ≤ 1)... 64
Tabela 4.2 - Reagentes usados na síntese do sistema LaFe1-xMnxO3
(0 ≤ x ≤ 1)... 65
Tabela 5.1 - Dados percentuais da decomposição térmica dos pós precursores do sistema LaFe1-xMnxO3 (0 ≤ x ≤ 1) preparado pelo método Pechini... 80
Tabela 5.2 - Dados percentuais da decomposição térmica dos pós precursores do sistema LaFe1-xMnxO3 (0 ≤ x ≤ 1) preparado pela reação de combustão assistida por microondas... 84
Tabela 5.3 - Valores de 2θ do pico principal do sistema LaFe1-xMnxO3
(0 ≤ x ≤ 1) preparado pelo método Pechini e tratado a 700°C por 4h... 86
Tabela 5.4 - Dados obtidos através do refinamento pelo método de Rietveld do sistema LaFe1-xMnxO3 (0 ≤ x ≤ 1) preparado pelo método Pechini e tratado a 700°C por 4h... 87
Tabela 5.5 - Volume da célula unitária do sistema LaFe1-xMnxO3 (0 ≤ x ≤ 0,5)
preparado pelo método Pechini e tratado a 700°C por 4h... 88
Tabela 5.6 - Dados obtidos através do refinamento pelo método Rietveld do sistema LaFe1-xMnxO3 (0 ≤ x ≤ 1) preparado pelo método Pechini e tratado a 900°C por 4h... 90
Tabela 5.7 - Volume da célula unitária do sistema LaFe1-xMnxO3 (0 ≤ x ≤ 0,5) preparado pelo método Pechini e tratado a 900°C por 4h... 91
Tabela 5.8 - Dados obtidos através do refinamento pelo método Rietveld do sistema LaFe1-xMnxO3 (0 ≤ x ≤ 1) preparado pelo método Pechini e tratado a 1100°C por 4h... 93
Tabela 5.9 - Volume da célula unitária do sistema LaFe1-xMnxO3 (0 ≤ x ≤ 0,5) preparado pelo método Pechini e tratado a 1100°C por 4h... 94
Tabela 5.10 - Dados obtidos através do refinamento pelo método Rietveld do sistema LaFe1-xMnxO3 (0 ≤ x ≤ 1) preparado pelo método Pechini e tratado a 1300°C por 4h... 96
Tabela 5.11 - Volume da célula unitária do sistema LaFe1-xMnxO3 (0 ≤ x ≤ 0,5)
(0 ≤ x ≤ 1) preparado pela reação de combustão assistida por microondas e tratado a 700°C por 4h... 99
Tabela 5.13 - Dados obtidos através do refinamento pelo método Rietveld do sistema LaFe1-xMnxO3 (0 ≤ x ≤ 1) preparado pela reação de combustão assistida por microondas e tratado a 700°C por 4h.... 100
Tabela 5.14 - Volume da célula unitária do sistema LaFe1-xMnxO3 (0 ≤ x ≤ 0,5)
preparado pela reação de combustão assistida por microondas
e tratado a 700°C por 4h... 100
Tabela 5.15 - Parâmetros magnéticos do sistema LaFe1-xMnxO3 (0 ≤ x ≤ 1) preparado pelo método Pechini... 116
Tabela 5.16 - Parâmetros magnéticos do sistema LF preparado pelo método
Pechini... 118
Tabela 5.17 - Parâmetros magnéticos do sistema LFM1 preparado pelo
método Pechini... 121
Tabela 5.18 - Parâmetros magnéticos do sistema LFM3 preparado pelo
método Pechini... 124
Tabela 5.19 - Parâmetros magnéticos do sistema LFM5 preparado pelo método Pechini... 126
Tabela 5.20 - Parâmetros magnéticos do sistema LM preparado pelo método
Pechini... 129
Tabela 5.21 - Parâmetros magnéticos do sistema LaFe1-xMnxO3 (0 ≤ x ≤ 1)
B Indução Magnética
CTGAS – ER Centro de Tecnologias do Gás e Energias Renováveis Dc Diâmetro Crítico da Partícula
Dm Diâmetro Médio de Cristalito
DM Dzialoshinskii-Moriya DRX Difração de Raios X
E Energia de anisotropia magnética
H Campo Magnético
Hc Campo Coercivo
ICSD Do Inglês: Inorganic Crystal Structure Database
JCPDS Do Inglês: Joint Committee on Powder Diffraction Standards K Constante Magneto-cristalina
LATMAT Laboratório de Análise Térmica e Materiais
LMMM Laboratório de Magnetismo e Materiais Magnéticos
M Magnetização
MAUD Do Inglês: Materials Analysis using Diffraction MAV Magnetômetro de Amostra Vibrante
MEV Microscopia Eletrônica de Varredura mI Número Quântico Magnético do Elétron
Mmáx Magnetização em Campo Máximo Aplicado
Mr Magnetização Remanente
Ms Magnetização de Saturação
NEPGN Núcleo de Estudos em Petróleo e Gás Natural RTP Redução à Temperatura Programada
Sig, Rw Índices de Qualidade do Refinamento
t Fator de Tolerância
Tc Temperatura de Curie
TG Termogravimetria
TM Transição Morin
TN Temperatura de Néel
B Magnéton de Bohr
1 INTRODUÇÃO... 18
2 REVISÃO BIBLIOGRÁFICA... 21
2.1 INTRODUÇÃO AO MAGNETISMO... 21
2.1.1 Tipos de comportamento magnético... 24
2.1.2 Domínios magnéticos... 27
2.1.3 Curva de magnetização... 29
2.1.4 Anisotropia magnética... 31
2.1.5 Efeitos de superfície em nanopartículas... 32
2.2 PEROVSKITAS... 33
2.2.1 Estrutura ABO3... 34
2.2.2 Campo cristalino... 38
2.2.3 Efeito Jahn-Teller... 41
2.2.4 Interações de troca... 43
2.2.5 Ortoferritas... 45
2.2.5.1 LaFeO3... 46
2.2.5.1.1 Dopagem no sítio do lantânio... 50
2.2.5.1.2 Dopagem no sítio do ferro... 52
2.3 MÉTODOS DE PREPARAÇÃO DE ÓXIDOS PEROVSKITAS... 56
2.3.1 Método Pechini... 57
2.3.2 Reação de combustão... 59
2.3.2.1 Reação de combustão assistida por microondas... 61
3 OBJETIVOS... 63
3.1 OBJETIVO GERAL... 63
3.2 OBJETIVOS ESPECÍFICOS... 63
4 METODOLOGIA EXPERIMENTAL... 64
4.1 NOMENCLATURA DO SISTEMA LaFe1-xMnxO3 (0 ≤ x ≤ 1)... 64
4.2 MATERIAIS E MÉTODOS... 64
4.2.1 Síntese do sistema LaFe1-xMnxO3 (0 ≤ x ≤ 1) pelo método Pechini... 65
4.2.2 Síntese do sistema LaFe1-xMnxO3 (0 ≤ x ≤ 1) pela reação de combustão assistida por microondas... 68
4.3 CARACTERIZAÇÃO DO SISTEMA LaFe1-xMnxO3 (0 ≤ x ≤ 1)... 70
4.3.3 Refinamento pelo método de Rietveld... 72
4.3.4 Microscopia Eletrônica de Varredura (MEV)... 73
4.3.5 Redução a Temperatura Programada (RTP)... 74
4.3.6 Medidas magnéticas... 75
4.3.6.1 Magnetômetro de Amostra Vibrante (MAV)... 75
5 RESULTADOS E DISCUSSÃO... 77
5.1 ANÁLISE TERMOGRAVIMÉTRICA (TG)... 77
5.2 DIFRAÇÃO DE RAIOS X (DRX)... 84
5.3 MICROSCOPIA ELETRÔNICA DE VARREDURA (MEV)... 101
5.4 REDUÇÃO A TEMPERATURA PROGRAMADA (RTP)... 110
5.5 MEDIDAS DE MAGNETIZAÇÃO (MAV)... 115
6 CONCLUSÕES... 134
1 INTRODUÇÃO
A síntese e o estudo de materiais magnéticos constituem uma importante linha de pesquisa envolvendo a química e a física do estado sólido, cuja relevância no campo científico e tecnológico está relacionada à alta funcionalidade e aplicação destes materiais em diversas áreas da ciência.
Dentre as inúmeras aplicações dos materiais magnéticos, podemos citar seu uso como ímãs permanentes, discos rígidos, dispositivos de microondas, sensores, transformadores e indutores de alta freqüência, aparelhos de telecomunicações, absorvedores de radiação eletromagnética, entre outras.
Atualmente, em virtude do avanço da tecnologia moderna, há uma crescente necessidade de se produzir novos materiais magnéticos ou melhorar suas características em função da possibilidade de redução nas dimensões dos equipamentos quanto a peso e tamanho, permitindo a miniaturização de dispositivos, e à limitação a saturação e perdas elétricas e magnéticas.
Nesse sentido, os óxidos mistos com estrutura perovskita têm sido bastante investigados por possuírem potenciais aplicações tecnológicas (KIM et al., 2005; ZHU; YE, 2004; HUR et al., 2004; KIMURA et al., 2003; DHO et al., 2004), tais como rádio, televisão, microondas, comunicação via satélite, dispositivos de memória, etc., resultantes da combinação de suas propriedades elétricas e magnéticas.
Estes óxidos abrangem diferentes características físicas podendo se comportar desde isolantes até semicondutores (RAYCHAUDHURI, 1995), como cristais ferroelétricos (AUCIELLO; SCOTT; RAMESH, 1998), supercondutores em altas temperaturas (BEDNORZ; MÜLLER, 1986), apresentarem propriedade de magnetoresistência gigante (variação da resistência elétrica de um material quando submetido a um campo magnético) (JIN et al., 1994; VON HELMOLT et al., 1993), entre outras.
Uma classe de óxidos com estrutura perovskita que vêm recebendo especial atenção é aquela onde o metal de transição apresenta valência mista, em razão da forte interação existente entre suas propriedades estruturais, magnéticas e eletrônicas. Um exemplo são as ortoferritas AFeO3 (A = Terra rara) que podem ser usadas para a maioria das aplicações eletrônicas por causa de sua condutividade mista.
A presença de defeitos iônicos e eletrônicos (CHERRY; ISLAM; CATLOW, 1995) faz destes materiais potenciais candidatos para o desenvolvimento de células a combustível (BIDRAWN et al., 2008), catalisadores para oxidação ou redução de gases poluentes (PECCHI et al., 2008; FAYE et al., 2009), membranas permeáveis de oxigênio (SHAULA et al., 2005), sensores químicos (LIU et al., 2006) entre outras aplicações. Quanto às propriedades magnéticas, as ortoferritas são classificadas como materiais antiferromagnéticos. Entretanto, estes podem exibir ferromagnetismo fraco em função do acoplamento antiferromagnético dos íons Fe3+ com spin canting (EIBSCHÜTZ; SHTRIKMAN; TREVES, 1967). A substituição parcial por cátions bivalentes no sítio A destes materiais resultam em sistemas do tipo A1-xA’xFeO3
(A = terra rara; A’ = cátions bivalentes), que dependendo principalmente da diferença
do raio iônico entre os íons A e A’, bem como do método de síntese empregado,
geram duas conseqüências possíveis: o ferro pode estar em um estado de valência mista Fe3+ e Fe4+, onde o teor de Fe4+ cresce com o aumento de x (BLASCO et al., 2008) e, o ferro pode permanecer no estado trivalente, e com isso, ocorrer uma deficiência de oxigênio na rede para compensar o balanço de cargas (LI et al., 1993). Tanto o estado de valência mista quanto a concentração de vacâncias de oxigênio exercem papel fundamental nas propriedades magnéticas destes compostos.
2 REVISÃO BIBLIOGRÁFICA
Neste capítulo será feita uma revisão dos principais conceitos relacionados ao magnetismo e aos óxidos tipo perovskita, que serão necessários para uma melhor compreensão do trabalho desenvolvido durante o período de doutoramento.
2.1 INTRODUÇÃO AO MAGNETISMO
Os materiais na natureza são formados a partir dos elementos químicos que se encontram distribuídos na tabela periódica. Cada elemento químico é único sendo composto de um núcleo constituído por prótons e nêutrons, que está envolto por camadas de elétrons, onde apenas os prótons e os elétrons possuem cargas elétricas. O magnetismo pode-se dizer é uma propriedade cuja natureza é de origem elétrica, estando relacionado com uma carga em movimento. Seus princípios e mecanismos básicos são complexos, todavia, sua origem encontra-se na estrutura eletrônica dos átomos (PAULO, 2006; CULLITY; GRAHAM, 2009).
O momento magnético associado a um elétron é denominado magnéton de
Bohr ( B) e sua magnitude é de 9,27 x 10-24 A.m2. O momento magnético de spin, para cada elétron em um átomo, é de + B (sinal positivo - spin e negativo – spin
), sendo a contribuição do momento magnético orbital igual a ml B, onde mI representa o número quântico magnético do elétron (CALLISTER, 2002).
As propriedades magnéticas de um material são determinadas pelas interações que ocorrem entre um campo magnético externo e os momentos de dipolo magnéticos dos átomos constituintes. O momento magnético líquido ou global de um átomo é o resultado da soma das contribuições dos momentos magnéticos de cada um dos elétrons, incluindo o cancelamento dos momentos de spin e orbital dos pares eletrônicos.
O momento magnético resultante será nulo quando dois elétrons encontram-se emparelhados no mesmo orbital, pois como conencontram-seqüência da regra de Hund, estes elétrons terão spins invertidos. Assim, para o cálculo do momento magnético líquido de um átomo são considerados apenas os elétrons desemparelhados. Deste modo, materiais compostos por átomos que possuem camadas eletrônicas totalmente preenchidas não são capazes de serem magnetizados permanentemente (CALLISTER, 2002).
Fonte: GOMES, 2009
As propriedades magnéticas de uma substância são geralmente descritas por três grandezas físicas: indução magnética (B), campo magnético (H) e magnetização (M). A indução magnética é o campo proveniente da própria magnetização do material e do campo externo aplicado. A relação entre eles é dada pela Equação 2.1 (CULLITY; GRAHAM, 2009):
B = 0 (H + M) (2.1)
Onde 0 é a permeabilidade no vácuo.
A magnetização M pode ser definida pela relação M = m/V = n B/V, onde m é o momento magnético total, que corresponde ao número total de átomos n que possuem elétrons desemparelhados multiplicado pelo momento magnético elementar B (magnéton de Bohr), dividido pelo volume V que ele ocupa (CULLITY; GRAHAM, 2009; JILES, 1991).
O comportamento magnético dos materiais pode ser descrito também por outras propriedades importantes como a susceptibilidade (χ) e a permeabilidade magnética ( ), conforme visto na Equação 2.2. A susceptibilidade magnética é a
medida da efetividade com que um campo magnético externo induz o dipolo magnético no material. Já a permeabilidade magnética é definida como a razão entre a indução magnética e a intensidade do campo magnético (CULLITY; GHAHAN, 2009).
χ = M/H = B/H (2.2)
2.1.1 Tipos de comportamento magnético
Os materiais, em sua grande maioria, exibem magnetismo reduzido e, somente quando estão na presença de um campo magnético externo é possível classificá-los quanto aos tipos de interação e alinhamento entre os seus momentos de dipolo magnéticos. Diante da resposta que apresentam quando submetidos a aplicação de um campo magnético externo, os materiais podem ser classificados em cinco tipos principais: Diamagnéticos, Paramagnéticos, Ferromagnéticos, Antiferromagnéticos e Ferrimagnéticos (JILES, 1991; CAMILO, 2006; CULLITY; GHAHAN, 2009).
Diamagnéticos – São materiais cujos átomos possuem camadas eletrônicas totalmente preenchidas nos quais os momentos estão emparelhados e se cancelam, não apresentando magnetização resultante. Quando na presença de um campo magnético externo, eles são fracamente magnetizados no sentido oposto do campo magnético aplicado. Isto se deve ao surgimento de pequenas correntes localizadas no interior do material criando seu próprio campo magnético em oposição ao campo aplicado. Estes materiais apresentam valores de susceptibilidade magnética pequenos e negativos. Exemplos: vários metais (ex: Cu, Ag, Hg, Bi, Au); a maioria dos não metais (ex: B, Si, P); gases nobres; muitos íons (ex: Na+, Cl- e seus sais); moléculas diatômicas (ex: H2, N2); água e a maioria dos compostos orgânicos (JILES, 1991; PAULO, 2006; CAMILO, 2006; CULLITY; GHAHAN, 2009).
Ferromagnéticos – São materiais que têm momentos de dipolo magnéticos permanentes que interagem entre si causando alinhamento paralelo. Ou seja, apresentam magnetização espontânea na ausência de campo externo. Quando estão sob a influência de um campo externo, seus momentos de dipolo magnéticos se alinham na direção e sentido do campo aplicado, podendo seguir orientados mesmo após sua remoção. Um material ferromagnético atinge a máxima magnetização chamada de magnetização de saturação (Ms), quando todos os dipolos magnéticos estão alinhados com o campo magnético aplicado. Acima de uma temperatura crítica denominada de temperatura de Curie (Tc), este alinhamento é destruído e o material comporta-se como paramagnético. Seus valores de susceptibilidade magnética são altos e positivos. Exemplos: metais de transição (ex: Fe, Co, Ni); terras raras (ex: Gd, Tb, Dy, Ho, Er e Tm); ligas de elementos ferromagnéticos e algumas ligas de Mn (ex: MnBi) (JILES, 1991; PAULO, 2006; CAMILO, 2006; CULLITY; GHAHAN, 2009).
Antiferromagnéticos – São materiais que têm momentos de dipolos magnéticos alinhados em sentido antiparalelo, levando a uma magnetização nula. Quando expostos a um campo magnético externo, os momentos se orientam na direção do campo. Acima de uma temperatura crítica, chamada de temperatura de Néel (TN), o alinhamento antiparalelo desaparece e o material passa a se comportar como paramagnético. Seus valores de susceptibilidade magnética são pequenos e positivos. Exemplos: compostos de metais de transição (ex: MnO, FeO, CoO, NiO, MnS, CuCl2) (JILES, 1991; PAULO, 2006; CAMILO, 2006; CULLITY; GHAHAN, 2009). Um aspecto bastante interessante observado para alguns materiais antiferromagnéticos é o aparecimento de uma pequena magnetização resultante, fazendo com que deixem de ser totalmente antiferromagnéticos e passem a exibir um ferromagnetismo fraco. Tal fenômeno é explicado em função da interação de troca Dzialoshinskii-Moriya, na qual ocorre a formação de um pequeno campo molecular devido a uma inclinação dos spins (spin canting) que compõe a rede cristalina do material, resultando numa magnetização não nula. Alguns óxidos
Em particular, a hematita é um óxido com acoplamento antiferromagnético por toda a sua estrutura romboédrica em baixas temperaturas. A -8ºC, verifica-se que este apresenta uma transição magnética denominada de transição Morin (TM). Nesta temperatura, o material passa a ter um ordenamento ferromagnético fraco devido ao
“spin canting” resultante da interação de troca Dzialoshinskii-Moriya, conforme discutido anteriormente. No entanto, uma dependência da temperatura da TM com o tamanho de partículas é observada, onde esta se desloca para temperaturas maiores quando o tamanho da partícula aumenta. Para partículas muito pequenas
(≤ 20 nm), a transição desaparece (BESSER; MORRISH; SEARLE, 1967; MORRISH, 1994; BENGOA et al., 2010).
Ferrimagnéticos – São materiais que apresentam alinhamento semelhante aos antiferromagnéticos, porém seus momentos de dipolos magnéticos são de magnitudes diferentes, fazendo com que possuam uma pequena magnetização espontânea. Seus valores de susceptibilidade magnética são altos e positivos. A magnetita (Fe3O4) e ferritas M2+O.Fe2O3 (M = Fe, Ni, Co, Cu, Mn, Mg) são alguns exemplos destes materiais (JILES, 1991; PAULO, 2006; CAMILO, 2006; CULLITY; GHAHAN, 2009). Na Figura 2.2 são ilustrados os tipos de magnetismo encontrado nos materiais com suas orientações de dipolo magnéticos.
Figura 2.2 - Tipos de magnetismo encontrado nos materiais.
2.1.2 Domínios magnéticos
Materiais, ferromagnéticos e ferrimagnéticos, que se encontram a uma temperatura abaixo da temperatura de Curie (Tc), são compostos por regiões de pequeno volume onde existe um alinhamento mútuo de todos os momentos magnéticos na mesma direção. Tais regiões são denominadas de domínios e cada domínio está magnetizado até a sua magnetização de saturação. Estes domínios são separados dos domínios adjacentes por uma parede denominada de Bloch (CALLISTER, 2002), como ilustrado na Figura 2.3.
Em geral, os domínios possuem dimensões microscópicas podendo cada grão de uma amostra policristalina consistir em mais de um domínio. Assim, em um material com dimensões macroscópicas existirá um grande número de domínios, onde todos poderão ter diferentes orientações de magnetização. As orientações dos domínios variam em função do campo H aplicado, enquanto que seu tamanho é determinado por diferentes fatores incluindo as propriedades intrínsecas do material e a sua microestrutura (CALLISTER, 2002; CULLITY; GHAHAN, 2009).
A avaliação das estruturas de domínios é muito importante, pois permite um melhor entendimento dos mecanismos de magnetização e de histerese em materiais ferromagnéticos e ferrimagnéticos. Estruturas de domínios esquemáticas estão representadas em vários pontos ao longo da curva M x H na Figura 2.4.
Figura 2.3 - Esquema (A) parede de domínios e (B) ordenação dos momentos em uma parede de domínios adjacentes.
No processo de magnetização de uma amostra, à medida que um campo H é aplicado, os domínios que estão orientados favoravelmente (ou que estejam praticamente alinhados) na direção do campo, crescem à custa daqueles que estão orientados de maneira desfavorável. Esse processo continua com o aumento da força do campo até a amostra macroscópica se tornar um único domínio com todos os seus spins alinhados na direção do campo, que é quando o material atinge sua magnetização de saturação (Ms). Deste modo, pode-se dizer que o processo de magnetização de uma amostra consiste em convertê-la de um estado de multidomínios ferromagnéticos pela aplicação de um campo magnético externo, para um estado no qual há um único domínio na mesma direção do campo aplicado (CALLISTER, 2002; FERRI, 2007).
Figura 2.4 - Curva de magnetização para um material ferromagnético inicialmente desmagnetizado. As configurações de domínios estão representadas durante os vários estágios de magnetização até
a magnetização de saturação.
2.1.3 Curva de magnetização
A curva de magnetização também conhecida como curva ou ciclo de histerese serve para caracterizar magneticamente um material, pois através dela são obtidas informações sobre sua magnetização de saturação, remanência e coercividade. Tais parâmetros permitem avaliar a adequação do material para uma determinada aplicação.
Para obtê-la, o material é inicialmente exposto a um campo magnético onde à medida que o campo aumenta, a magnetização cresce até atingir um patamar constante, em que todos os momentos magnéticos estão apontando na mesma direção do campo aplicado. Ou seja, o material atinge sua magnetização de saturação (Ms). Em seguida, o campo magnético é reduzido a partir do valor da magnetização de saturação, fazendo com que este decresça lentamente. Porém, a curva de desmagnetização não acompanha a curva de magnetização inicial, e o material ainda permanece magnetizado, pois seus momentos magnéticos não perdem totalmente o alinhamento. Esse valor residual de magnetização também chamado de magnetização remanente (Mr) é obtido quando o campo magnético é totalmente retirado (H = 0). Para neutralizar a Mr, aplica-se o campo no sentido inverso até que a magnetização seja reduzida a zero. O campo necessário para atingir esse valor é denominado de campo coercivo (Hc). Por fim, continuando a variar o módulo do campo, o material alcança novamente o valor de saturação. O ciclo é repetido no sentido inverso até se obter a curva fechada chamada de histerese.
Dentre os parâmetros magnéticos obtidos através do ciclo de histerese, a coercividade é a propriedade mais importante variando em função do tamanho das partículas. Uma relação de dependência entre a coercividade e o tamanho das partículas magnéticas é mostrada de forma esquemática na Figura 2.6. É possível verificar que quando a partícula tem o seu tamanho reduzido, a coercividade aumenta até atingir um valor máximo e, então tende a zero.
De acordo com o gráfico da Figura 2.6 podem ser identificadas três regiões: (1) Abaixo de um diâmetro crítico (ds), as partículas encontram-se em regime de monodomínio e o momento magnético é instável e, portanto, Hc = 0. Nesta região, as partículas são chamadas de superparamagnéticas; (2) Para diâmetros intermediários, acima do limite superparamagnético e abaixo do diâmetro crítico (d0), as partículas encontram-se ainda em regime de monodomínio, sendo o momento magnético estável com a coercividade alcançando um máximo; por fim, (3) Para diâmetros maiores que d0 (acima de vários m), o regime é de multidomínio e a
coercividade cai (CULLITY; GRAHAN, 2009).
Figura 2.5 - Curva de histerese magnética típica de um material ferromagnético.
A partir do ciclo de histerese do material pode-se extrair informações quanto a sua dureza magnética, o que permite classificá-lo como magneticamente duro ou mole. Materiais magnéticos duros são aqueles que apresentam largas curvas de histerese, altos valores de magnetização remanente e coercividade.
Estes materiais encontram ampla aplicação em dispositivos de memória magnética como disquetes, HD de computadores e tarja de cartões bancários. Já os materiais magnéticos moles apresentam ciclo de histerese estreito, baixos valores de magnetização remanente e coercividade, sendo usados em dispositivos que necessitam trabalhar com altas freqüências como aparelhos de comunicação, radares, chip de computadores (GOMES FILHO, 2009).
2.1.4 Anisotropia magnética
A maioria dos materiais possui algum tipo de anisotropia que afeta o comportamento da magnetização. A anisotropia magnética é o fenômeno de orientação preferencial da magnetização espontânea (Ms) ao longo de certas direções características de cada material. A energia de anisotropia magnética é aquela associada à orientação da magnetização ao longo de um eixo cristalográfico (eixo de fácil magnetização) do material magnético. Para um sistema uniaxial, a energia de anisotropia magnética (E) pode ser definida pela Equação 2.3.
Figura 2.6 - Variação da coercividade com o tamanho da partícula.
(1) (2) (3)
Onde K é a constante magneto-cristalina, θ corresponde ao ângulo entre a magnetização de saturação (Ms) e o eixo fácil de magnetização e V é o volume da partícula.
Uma alta energia de anisotropia indica que a magnetização será mais fácil em uma determinada direção. Existem várias formas de anisotropia, porém as mais importantes são a cristalina, a de forma e a de tensão. Dentre estas, a anisotropia cristalina é intrínseca do material, ou seja, independe de sua microestrutura. (LESLIE-PELECKY; RIEKE, 1996; RIBEIRO, 2008).
2.1.5 Efeitos de superfície em nanopartículas
A superfície desempenha um importante papel no comportamento magnético das nanopartículas. Os efeitos de tamanho dominam as propriedades magnéticas destes materiais, tornando-se mais significativos quando as partículas são muito pequenas. Com a diminuição do tamanho da partícula, aumenta-se a concentração de átomos na superfície e, estes por terem o número de coordenação (número de átomos vizinhos próximos) incompleto, contribuem para um momento magnético líquido devido a não compensação dos spins na superfície do material.
Tal comportamento pode ser compreendido em termos de um modelo denominado de spin gigante, que assume que todos os spins participam de um único domínio, e que a energia magnética é determinada pelo volume e forma das partículas (KODAMA; BERKOWITZ, 2005). Na Figura 2.7 é ilustrada uma representação esquemática dos spins na superfície de uma nanopartícula.
2.2 PEROVSKITAS
Desde a descoberta do mineral perovskita “CaTiO3”, que na temperatura ambiente apresenta estrutura cristalina distorcida tipo ortorrômbica, o estudo de compostos que cristalizam com a estrutura tipo perovskita tem sido bastante intensificado, em função da ampla diversidade de suas propriedades possibilitarem inúmeros desenvolvimentos tecnológicos.
Os compostos do tipo perovskita possuem composição química ABX3, sendo A e B cátions metálicos, onde A é o maior deles, enquanto que X é geralmente um ânion formado por membros da família dos halogênios, como flúor, cloro, bromo ou oxigênio (PEREZ, 2000). Os óxidos de estrutura ABO3 são os compostos mais numerosos dessa classe apresentando vasto campo de aplicações tecnológicas. A larga aplicabilidade destes materiais se deve a variações estruturais e diferentes propriedades, tais como ferroeletricidade (LaCoO3), piezoeletricidade (BaTiO3, PbTiO3), supercondutividade (Ba1-xKxBiO3 e BaBi1-xPbxO3), magnetoresistência colossal (La1-xSrxMnO3), condutividade iônica e eletrônica (LaFeO3) entre outras.
Figura 2.7 - Configuração de spin na superfície de uma nanopartícula.
Grande parte das propriedades exibidas por estes materiais estão relacionadas a pequenos desvios na estrutura e composição ideal dos óxidos. Entretanto, ainda faz-se necessário uma compreensão melhor dos mecanismos responsáveis por estas mudanças. Por esta razão, uma investigação mais aprofundada com o objetivo de revelar maiores detalhes sobre o comportamento destes materiais torna-se extremamente essencial.
2.2.1 Estrutura ABO3
Nos óxidos de estrutura perovskita ABO3, os cátions A e B diferem consideravelmente em tamanho. Normalmente, o sítio A é ocupado por um cátion com raio iônico grande tal como os metais alcalinos, os alcalinos terrosos, as terras raras e outros íons grandes como Pb2+ e Bi3+ com número de coordenação 12. Já o sítio B é ocupado por um cátion com raio iônico menor como os metais de transição 3d, 4d e 5d, possuindo número de coordenação 6 (KOPONEN et al., 2005; LIMA et al., 2009).
Para manter a estabilidade da estrutura perovskita é necessário que o cátion do sítio B tenha preferência pela coordenação octaédrica e possua uma carga iônica elevada, e o cátion do sítio A tenha um tamanho adequado e ocupe as vacâncias dodecaédricas. Ou seja, o cátion A deve possuir raio iônico maior que 0,9 Å e o cátion B, maior que 0,51 Å (SPINICCI et al., 2001; MELO, 2007).
A eletroneutralidade é outra condição fundamental para estabilizar a estrutura. As cargas dos íons A e B devem somar 6. Assim, as distribuições das cargas nos óxidos podem ocorrer de diferentes formas: A1+B5+O3, A2+B4+O3 ou A3+B3+O3. Porém, as estruturas mais comuns são aquelas em que A é um cátion de um elemento terra rara e B é um metal de transição, ambos estando no estado de oxidação trivalente (TEJUCA; FIERRO, 1992; SOARES, 2005).
Um aspecto interessante da estrutura perovskita é sua flexibilidade estrutural devido a possibilidade de substituição de cátions nos sítios A e/ou B. Na maioria dos casos, a substituição parcial de um ou mais íons na rede cristalina da perovskita gera um grupo numeroso de compostos conhecidos como perovskitas duplas cuja
fórmula geral é AA’BB’O6.
Figura 2.8 - Representação da estrutura ideal cúbica da Perovskita.
Quando tais substituições acontecem, o sítio pode ser ocupado pelos íons de uma maneira ordenada ou aleatória. Se eles adotam um arranjo ordenado, a simetria e em muitos casos, o tamanho da célula unitária muda (WOODWARD, 1997; SOARES, 2005).
Os óxidos do tipo perovskita se comportam como isolantes elétricos quando cristalizam com estrutura ideal cúbica, em razão das fortes ligações iônicas que fazem com que a mobilidade dos elétrons pelo cristal seja muito pequena. Poucos materiais apresentam a estrutura ideal à temperatura ambiente, apesar de muitos assumirem a simetria cúbica em temperaturas mais elevadas.
Esses óxidos, em sua grande maioria, possuem estrutura ligeiramente deformada, apresentando distorções que resultam na formação de redes hexagonais, tetragonais, romboédricas e ortorrômbicas (MAGYARI-KOPE et al., 2001; STOKES et al., 2002; MELO, 2007). As duas últimas são as distorções mais comuns e suas estruturas estão ilustradas na Figura 2.9.
Figura 2.9 - Estrutura perovskita com distorções: (a) Romboédrica e (b) Ortorrômbica.
(a) (b)
As distorções ocorridas na estrutura podem estar associadas a três prováveis mecanismos: distorção dos octaedros ocasionada pelo efeito Jahn-Teller, a inclinação ou rotação dos octaedros em função da substituição de íons no sítio A por outros de raio iônico diferente e, por último, deslocamento de íons no sítio B. Estes diferentes tipos de distorções podem ocorrer separadamente ou em combinação (PEREZ, 2000; SILVA, 2004; VILLEGAS, 2006; MELO, 2007). A magnitude da distorção é medida pelo fator de tolerância t (Equação 2.4) introduzido por GOLDSCHMIDT (1926):
Onde dA-O e dB-O representam a menor distância dos sítios ao oxigênio mais próximo. Estas distâncias ou comprimentos de ligação dependem da estequiometria do composto, que varia com substituições nos sítios A e B ou através da indução de vacâncias. GOLDSCHMIDT (1926) estabeleceu que para a estrutura cúbica da
perovskita ser estável, o fator de tolerância t deve estar no intervalo 0,8 ≤ t ≤ 0,9.
Porém, estruturas perovskitas podem ainda ocorrer para valores no intervalo 0,89 ≤ t ≤ 1,02 (COEY; VIRET; VON MOLNAR, 1999).
Para a perovskita ideal cúbica, t = 1 e o ângulo da ligação B-O-B é 180°. Quando t < 1, o ângulo da ligação B-O-B diminui, levando a uma mudança no grupo espacial de Pm3m (cúbica) para R3c (romboédrica). Esta mudança ocorre devido à rotação ou inclinação cooperativa dos octaedros. Logo, o ângulo da ligação B-O-B varia linearmente com o fator de tolerância t. Para valores ainda menores de t, ocorre a mudança do grupo espacial Pm3m para Pnma (ortorrômbica). No caso da estrutura ortorrômbica, esta pode assumir duas formas: (1) “O-ortorrômbica”,
caracterizada por uma relação de parâmetros de rede (c/a) > , e (2) “O”
-ortorrômbica”, com (c/a) < Este último arranjo é resultado de uma sobreposição da distorção Jahn-Teller na estrutura perovskita (TEJUCA; FIERRO; TASCÓN, 1989; ATTFIELD, 2002; MELO, 2007).
2.2.2 Campo Cristalino
Na teoria do campo cristalino, os metais de transição 3d quando íons livres, possuem cinco orbitais degenerados em energia que são dxz, dyz, dxy, dx2
-y2 e dz2, cada um com formas e orientações diferentes. Na mesma condição, o oxigênio 2p possui três diferentes orbitais px, py e pz, também degenerados em energia, conforme ilustrado na Figura 2.10. A degenerescência dos orbitais d é quebrada quando os metais de transição estão situados no centro de um octaedro formado por seis íons O2- (complexo octaédrico), como no caso dos óxidos de estrutura perovskita.
Este desfavorecimento energético pode ser melhor visualizado na Figura 2.11, onde a projeção dos orbitais dxy e dx2
-y2 no plano xy, bem como os orbitais p dos íons oxigênio é observada. Nesta condição, os orbitais d do metal de transição são divididos em dois grupos com energias distintas: os triplamente degenerados de mais baixa energia conhecidos como t2g (dxz, dyz, dxy) e os duplamente degenerados de maior energia conhecidos como eg (dx2
-y2, dz2), conforme mostrado na Figura
2.12.
Figura 2.10 - Representação geométrica dos orbitais s, p e d.
Os orbitais t2g possuem uma energia de 2∆/5 a menos que no caso do íon
livre, enquanto que os orbitais eg possuem uma energia de 3∆/5. Esta diferença energética (∆) entre os subgrupos de orbitais denomina-se desdobramento do campo cristalino. Os ligantes que provocam apenas um pequeno grau de desdobramento do campo cristalino são designados ligantes de campo fraco. Já os que provocam um grande desdobramento são denominados ligantes de campo forte (LEE, 1999; CAVALCANTE, 2009).
Tomando-se como exemplo o íon Fe3+, na presença de um ligante de campo fraco, os cinco elétrons 3d seriam distribuídos nos orbitais da seguinte forma: os três primeiros elétrons iriam preencher os orbitais t2g com spins paralelos e os outros dois iriam preencher os orbitais eg, também paralelamente, de acordo com a regra de Hund. Deste modo, teríamos cinco elétrons desemparelhados e a configuração seria dita de alto-spin. Para a situação de um ligante de campo forte, os cinco elétrons estariam ocupando apenas os orbitais t2g, enquanto os orbitais eg estariam desocupados. Nesse caso, haveria apenas um elétron desemparelhado e a configuração seria dita de baixo-spin.
Figura 2.11 - Projeção dos orbitais (a) dxy e (b) dx2-y2, e dos orbitais p dos íons oxigênio, no plano xy.
2.2.3 Efeito Jahn-Teller
A forma dos complexos dos metais de transição é influenciada pela maneira como os orbitais d estão preenchidos, ou seja, se estão preenchidos simétrica ou assimetricamente. Num complexo octaédrico, a repulsão entre os elétrons do metal de transição central e dos seis ligantes desdobra os orbitais d em dois subníveis t2g e eg. Se os elétrons d estiverem dispostos simetricamente, a repulsão sentida por todos os seis ligantes será a mesma. A estrutura será, portanto, um octaedro perfeitamente regular. Caso os elétrons d estejam distribuídos assimetricamente, eles repelirão com maior intensidade alguns ligantes do complexo que outros. Deste modo, a estrutura do complexo será distorcida, pois o preenchimento assimétrico dos orbitais eg implica que alguns dos ligantes serão mais fortemente repelidos que outros. Isso provoca uma distorção significativa da forma octaédrica. Conforme discutido, os orbitais eg sofrem um aumento de energia devido à vizinhança em forma de octaedro, de maneira que os íons ligados procuram diminuir a energia total do sistema, alterando suas posições iniciais e provocando distorções. Esse processo que remove a degenerescência dos orbitais eg é conhecido como efeito Jahn-Teller. (LEE, 1999; REIS JUNIOR, 2003).
Figura 2.12 - Efeito do campo cristalino em um octaedro.
Um caso particular de distorção Jahn-Teller ocorre quando o octaedro se alonga em uma determinada direção, fazendo com que os octaedros vizinhos sejam comprimidos na mesma direção, e assim por diante. Este fenômeno é conhecido como efeito Jahn-Teller cooperativo.
Estas distorções implicam em severas conseqüências às propriedades magnéticas, elétricas e estruturais dos óxidos do tipo perovskita. Certas
deformações podem alterar o ângulo θ da ligação B-O-B, diminuindo, conseqüentemente a mobilidade eletrônica entre os íons de transição. Na Figura 2.13 é ilustrado um resumo dos conceitos discutidos neste parágrafo.
Figura 2.13 - Diagrama de energia dos orbitais d de um metal de transição (a) livre (b) em um octaedro perfeito e (c) com deformação Jahn-Teller.
2.2.4 Interações de troca
Nos óxidos de estrutura perovskita, as interações de troca indireta (que são intermediadas pelo íon oxigênio) são dominantes e podem ocorrer via mecanismo de super troca ou dupla troca.
Na interação de super troca, há uma superposição dos orbitais d do metal de transição com os orbitais p do íon oxigênio, fazendo com que na região de superposição destes orbitais só seja permitido, de acordo com o princípio da exclusão de Pauli, um único elétron de cada spin. Assim, somente o acoplamento antiparalelo de spins é favorecido nos extremos das ligações M-O-M (M = metal de transição), localizando os elétrons. Este tipo de configuração resulta em um ordenamento antiferromagnético de longo alcance dos momentos magnéticos de spin, levando o material a um comportamento isolante, ou seja, um isolante de Mott. Além disso, o acoplamento antiferromagnético estabiliza o sistema em um estado de mais baixa energia. Um número de sólidos iônicos, incluindo alguns óxidos e fluoretos, são antiferromagnetos acoplados por interação de super troca. Na Figura 2.14 é ilustrada uma representação das interações de troca direta e indireta (BLUNDELL, 2001; CARNEIRO, 2005).
Figura 2.14 - Representação da ligação M-O mostrando a comparação entre a troca direta e a indireta (super troca). A super troca estabiliza o antiferromagnetismo. A troca direta é comumente
ferromagnética.
No caso da interação de dupla troca, esta ocorre entre os diferentes estados de oxidação do íon metálico também intermediado pelo íon oxigênio. Esse tipo de interação favorece o acoplamento ferromagnético. As manganitas são exemplos de compostos cujas interações ferromagnéticas ocorrem via mecanismo de dupla troca. No sistema La1-xCaxMnO3, a substituição de La3+ por Ca2+ implica no aparecimento de um estado de valência mista, no qual coexistem pares de íons Mn3+ e Mn4+. Esse estado de valência mista permite que um elétron, antes localizado em um íon Mn3+ seja transferido para posição do íon vizinho Mn4+. Este fenômeno é denominado de dupla troca devido à transferência simultânea de elétrons, ou seja, a dupla troca ocorre via transferência de um elétron do Mn3+ para o orbital p do íon O 2-simultaneamente com a transferência de um elétron deste íon O2- para o orbital vazio do íon Mn4+ (BLUNDELL, 2001; CARNEIRO, 2005). Na Figura 2.15 têm-se uma representação esquemática do mecanismo de dupla troca.
Figura 2.15 - Representação esquemática do mecanismo de dupla troca (a) antes e (b) depois do elétron de condução trocar de íon manganês.
Para haver saltos que possibilitem o movimento do elétron entre os dois íons de Mn ao longo da ligação Mn-O-Mn, os spins destes íons de Mn devem estar alinhados. Com base nessa teoria, ZENER (1951) demonstrou que uma interação indireta pode dar origem ao ferromagnetismo e, mostrou sua relação com a condutividade elétrica. Se os spins dos íons de Mn forem antiparalelos, ou se o ângulo da ligação Mn4+-O-Mn3+ for desviado significativamente de 180°, a transferência eletrônica é dificultada entre os sítios e a condutividade elétrica diminui.
2.2.5 Ortoferritas
Ortoferritas de fórmula geral AFeO3 (A = terra rara) pertencem a uma relevante classe de materiais ferromagnéticos fracos com interessantes propriedades magnéticas e magneto-óticas (DIDOSYAN et al., 2003). Estes materiais encontram inúmeras aplicações como sensores químicos (LIU et al., 2006), catodos para células a combustível (BIDRAWN et al., 2008) e na área de catálise (MERINO et al., 2006). A estrutura e propriedades destes materiais são fortemente influenciadas pelo tipo e quantidade do íon dopante, assim como pelo método de síntese empregado na preparação dos pós precursores.
Nos últimos anos, vários pesquisadores têm buscado em seus estudos aprimorar o método de preparação destes pós a fim de melhorar suas propriedades e conseqüentemente seu desempenho. Dentre os métodos usados para preparação de ortoferritas podemos citar: reação do estado sólido (AHMED; EL-DEK, 2006), moagem de alta energia (CRISTÓBAL et al., 2009), método Pechini (POPA; FRANTTI; KAKIHANA, 2002), método da combustão (WANG et al., 2006), método dos citratos precursores (SHABBIR; QURESHI; SAEED, 2006) entre outros.
As ortoferritas cristalizam com uma estrutura perovskita distorcida, na qual a célula unitária é ortorrômbica. A principal distorção está relacionada à inclinação do octaedro FeO6. A estrutura magnética desses compostos é constituída por duas subredes pseudocúbicas de face centrada onde cada íon Fe3+ está cercado por seis íons O2- formando o octaedro FeO6. O acoplamento entre essas subredes resulta num ordenamento antiferromagnético. Entretanto, o alinhamento dos momentos magnéticos dos íons ferro não é estritamente antiparalelo, possuindo uma leve inclinação que resulta numa pequena magnetização no material. Como conseqüência, um comportamento ferromagnético fraco pode ser observado (MATHUR et al., 2004). Dependendo do tamanho do cátion terra rara, o octaedro FeO6 pode variar seu ângulo de inclinação, levando o material a apresentar diferentes momentos magnéticos resultantes (MATHUR et al., 2002; MATHUR et al., 2004; CRISTÓBAL et al., 2009).
2.2.5.1 LaFeO3
A ortoferrita de lantânio (LaFeO3) é a mais conhecida dessa classe de óxidos cerâmicos, apresentando estrutura distorcida tipo ortorrômbica com todos os íons ferro no estado de oxidação trivalente. É um material isolante antiferromagnético com temperatura de Néel de 477°C. A sua temperatura de Néel é a mais alta dentre as ortoferritas de terras raras, a qual está relacionada à alteração no ângulo da ligação Fe-O-Fe que passa de 180° para 155° induzindo a ortorrombicidade da célula unitária (LYUBUTIN; DMITRIEVA; STEPIN, 1999).
Na literatura, trabalhos recentes envolvendo o estudo das propriedades magnéticas de ortoferritas produzidas por diferentes métodos são encontrados e discutidos abaixo.
HUI, JIAYUE e ANHUA (2010) investigaram as propriedades magnéticas de ortoferritas AFeO3 (A = Y, La e Gd) preparadas pelo método da combustão. Os difratogramas dos materiais calcinados em diferentes temperaturas mostraram que somente a fase LaFeO3 ortorrômbica foi obtida direto da reação de combustão sem precisar passar por etapa de tratamento térmico. Já para as amostras YFeO3 e GdFeO3, a formação da fase ortorrômbica foi observada após os pós sofrerem tratamento térmico a 800°C. Quanto a morfologia, evidenciou-se a formação de aglomerados com tamanhos de grãos entre 70-85nm, 25-50nm e 50-70nm para as amostras YFeO3, LaFeO3 e GdFeO3, respectivamente. As curvas de magnetização exibiram ferromagnetismo fraco somente para as amostras LaFeO3 e YFeO3, enquanto que um comportamento paramagnético foi observado para GdFeO3.
Figura 2.16 - Curva de magnetização do LaFeO3 à temperatura ambiente.
No caso das amostras LaFeO3 e YFeO3, os autores justificam o resultado em função da ausência de interação entre os íons Fe3+ e A3+ (A = La; Y), uma vez que estes últimos possuem configuração eletrônica completa (La3+ = [Xe]; Y3+ = [Kr]), sendo não magnéticos e, por isso, a magnetização é dada apenas pelos momentos magnéticos dos íons ferro (Fe3+ = [Ar] 3d5). Já para o composto GdFeO3, existe tanto a contribuição ferromagnética dos íons Fe3+ quanto a paramagnética do íon Gd3+ (Gd3+ = [Xe] 4f7). Entretanto, esta última é a que predomina no composto.
CRISTÓBAL et al. (2009) prepararam a ortoferrita de lantânio (LaFeO3) por um método mecanoquímico utilizando diferentes óxidos de ferro (Fe3O4 e Fe2O3) como precursores, a fim de estudar o efeito da rota de síntese e dos materiais de partida nas propriedades magnéticas. Diferentes tempos de moagem, assim como o tratamento térmico em temperaturas entre 600°C e 1000°C foram utilizados como parâmetros de investigação. De acordo com os resultados de DRX, a completa formação do óxido LaFeO3 ocorreu após 3h de moagem, independente do tipo de óxido de ferro utilizado. Os tamanhos de cristalitos obtidos foram de ~ 15 nm para as amostras ativadas, e de ~ 60 nm quando calcinadas a 1000°C. Segundo os autores, esse efeito era esperado uma vez que a estrutura cristalina do composto é deteriorada e o tratamento térmico promove novamente sua recristalização. Os difratogramas das amostras ativadas por 3h e calcinadas a 1000°C mostraram apenas a fase LaFeO3 bem cristalizada. Com base nas curvas de histerese, o comportamento magnético das amostras foi verificado, onde uma diminuição na magnetização de saturação com o aumento do tempo de moagem foi observado nas amostras produzidas a partir da magnetita (Fe3O4). Já a coercividade mostrou um aumento após meia hora de ativação com posterior diminuição após decorrido 1h. Os autores relatam que tal comportamento é consistente com a reação que ocorre dentro do moinho de bolas. O consumo da magnetita e surgimento do composto LaFeO3 antiferromagnético produz uma notável queda da magnetização de saturação.
Em relação ao aumento do campo coercitivo nos primeiros estágios da ativação, a explicação se dá em razão da redução do tamanho de domínio da magnetita, que é a principal fase. Com o aumento do tempo de ativação, ocorre um aumento na formação do LaFeO3, e com isso, uma diminuição da coercividade. Para a amostra sem ativação obtida a partir da hematita (Fe2O3), a curva de histerese mostrou comportamento típico de material antiferromagnético "canting", à temperatura ambiente, acima da transição Morin (TM). Uma diminuição na magnetização de saturação após meia hora de ativação é observada, seguido por um aumento da propriedade em tempos maiores de ativação. Esse fato também é explicado em função da formação da ortoferrita de lantânio, que nesse caso tem Ms maior que a hematita. Os resultados revelaram que independente do tipo de óxido de ferro utilizado na síntese, a similaridade entre os valores de Ms e Hc obtidos para as amostras com ativação de 3h, indicam que ambas apresentam a fase perovskita com estrutura antiferromagnética distorcida (CRISTÓBAL et al., 2009).
Um estudo avaliando o efeito do tratamento térmico nas amostras de ambas as séries ativadas por 3h também foi realizado. Resultados similares foram observados. Com o aumento da temperatura de calcinação, a magnetização de saturação diminui, em conseqüência da evolução da estrutura magnética distorcida do LaFeO3 para um ordenamento antiferromagnético. Porém, as histereses para as amostras calcinadas a 1000°C exibiram respostas diferentes. A amostra produzida a partir da magnetita exibiu ainda comportamento ferromagnético fraco, enquanto que uma estrutura completamente antiferromagnética foi obtida usando a hematita. Tal fato sugere uma influência da natureza do óxido de ferro usado na rota de síntese em torno das propriedades magnéticas da ortoferrita de lantânio (CRISTÓBAL et al., 2009).
Um gráfico da magnetização versus temperatura também foi construído e, a partir deste, observou-se que todas as ortoferritas exibem o mesmo comportamento magnético que persiste até a temperatura de -233°C. Os autores relatam que o ferromagnetismo fraco observado nas amostras se deve essencialmente ao
“canting” originado do alinhamento das duas redes acopladas antiferromagneticamente na estrutura perovskita distorcida.
2.2.5.1.1 Dopagem no sítio do Lantânio
A substituição parcial de cátions bivalentes ou monovalentes no sítio do lantânio forma compostos do tipo La1-xAxFeO3 (A = Ca, Sr, Na), onde os íons ferro podem estar presentes na estrutura em um estado de valência mista (Fe4+/ Fe3+). Outra provável conseqüência com a dopagem é a indução de vacâncias de oxigênio no composto para neutralizar o balanço de cargas e manter o ferro no estado de oxidação trivalente. Tanto o estado de valência mista do metal de transição quanto à concentração de vacâncias de oxigênio constituem defeitos estruturais, os quais têm um papel determinante nas propriedades magnéticas das ortoferritas. Em busca de uma maior compreensão sobre a influência das modificações estruturais sobre as propriedades magnéticas destes materiais, trabalhos relatados na literatura investigam uma correlação existente entre estrutura e propriedade.
BELLAKKI et al. (2009) observaram um aumento da magnetização e da contribuição ferromagnética com o aumento da concentração de dopante. Os autores estudaram a influência do sódio nas propriedades magnéticas e estruturais do sistema La1-xNaxFeO3 ( 0 ≤ x ≤ 0,3) produzido pelo método da combustão. A