UNIVERSIDADE FEDERAL DE MINAS GERAIS
DEPARTAMENTO DE FISIOLOGIA E BIOFÍSICA PÓS-GRADUAÇÃO EM CIÊNCIAS BIOLÓGICAS:
FISIOLOGIA E FARMACOLOGIA
DESENVOLVIMENTO E CARACTERIZAÇÃO DE LIPOSSOMAS
CONTENDO GABA PARA INTERVENÇÃO A LONGO PRAZO NO
SISTEMA NERVOSO CENTRAL
Gisele Cristiane Vaz
Orientador: Marco Antônio Peliky Fontes
Coorientador: Frédéric Frézard
Coorientador: Kaushik Patel
UNIVERSIDADE FEDERAL DE MINAS GERAIS
DEPARTAMENTO DE FISIOLOGIA E BIOFÍSICA PÓS-GRADUAÇÃO EM CIÊNCIAS BIOLÓGICAS:
FISIOLOGIA E FARMACOLOGIA
DESENVOLVIMENTO E CARACTERIZAÇÃO DE LIPOSSOMAS
CONTENDO GABA PARA INTERVENÇÃO A LONGO PRAZO NO
SISTEMA NERVOSO CENTRAL
Gisele Cristiane Vaz
Orientador: Marco Antônio Peliky Fontes
Coorientador: Frédéric Frézard
Coorientador: Kaushik Patel
Belo Horizonte
Outubro de 2014
Aos meus sobrinhos
João Guilherme, Lucas e Maria Alice,
AGRADECIMENTOS
Ao meu orientador Marco Antônio Peliky Fontes pela oportunidade, pelo
aprendizado e pela excelente convivência durante todos esses anos.
Ao meu coorientador Frederic Frezard por toda assistência e
aprendizado durante o desenvolvimento deste projeto.
Ao Dr. Kaushik Patel por me receber em seu laboratório, por todos os
ensinamentos e oportunidades.
À todos que de alguma forma contribuíram para o desenvolvimento
deste projeto, em especial os professores Fabrício Moreira e Robson Santos.
Às professoras Maria José Campagnole-Santos e Andréa Haibara por
todo aprendizado e ótima convivência no Laboratório de Hipertensão.
Ao Zezé, Marilene, Nayara Kesia, Cyntia, Nilda e Rodner por toda ajuda
e disponibilidade.
Aos colegas do departamento de Fisiologia e Biofísica, do Laboratório
de Hipertensão e do Laboratório de Biofísica dos Sistemas Nanoestruturados,
Aos amigos da University of Nebraska Medical Center, em especial
Neeru Sharma, Hong Zheng, Xuefei Liu, Bo Xu, Tamra Lewellyn e Lirong Xu,
por terem sido minha família enquanto eu estava em Omaha.
Aos meus queridos amigos Érica Mário, Nívia Santiago, Daniel Lima,
Priscila Guimarães, Flávia Ribeiro, Carlos Xavier, Danielle Ianzer, Ana Paula
Côrrea, Letícia Cordeiro, Natália Machado e Tiago Coelho por fazerem tudo
ficar mais fácil. Por serem a extensão da minha família.
Ao Vinícius por estar sempre perto, não importando a distância física,
por todo amor e paciência.
À minha família com quem aprendo todo dia o verdadeiro sentido do
amor. Aos meus pais Ademir e Edna por todo apoio, por sempre estarem ao
meu lado. Aos meus irmãos Josiane e Adriano pelo amor incondicional.
À Deus, por sua presença constante em minha vida, sempre atendendo
as minhas orações e me dando a força necessária para enfrentar as
adversidades e nunca desistir dos meus objetivos. Por permitir que eu
RESUMO
Lipossomas são vesículas esféricas formadas por uma ou várias bicamadas
concêntricas de lipídios, que isolam um ou vários compartimentos aquosos
internos do meio externo, apresentando como maior vantagem o fato se serem
biocompatíveis. O ácido-γ-aminobutírico (GABA) é o principal neurotransmissor
inibitório do sistema nervoso central (SNC). A literatura mostra claramente o
envolvimento deste neurotransmissor na regulação cardiovascular, em
condições normais ou patológicas. O objetivo do presente estudo foi
desenvolver, caracterizar e testar lipossomas contendo GABA. Lipossomas
GABA (LG) foram preparados pelo método do
congelamento-descongelamento, utilizando os seguintes lipídios: DSPE, CHO e DSPE-PEG.
Os LG foram testados em ratos Wistar: 1) Sobre o controle autonômico
cardiovascular central em preparação com animais anestesiados. Onde foi
observado que após dois dias da microinjeção intracerebroventricular (ICV) de
LG ocorreu uma atenuação no aumento da atividade simpática do nervo renal
(ASNR) dos animais que receberam bicuculina metiodide (BMI) no mesmo
local. 2) Frente ao estresse emocional. Após dois e cinco dias da microinjeção
ICV de LG foi verificada uma atenuação da taquicardia quando os animais
eram submetidos ao estresse por jato de ar. 3) Ao teste de ansiedade no
labirinto em cruz elevado. Observou-se que os animais que receberam LG ICV
após dois dias, apresentaram uma diminuição do comportamento de
ansiedade. LG foram também microinjetados no núcleo paraventricular do
hipotálamo (PVN) de animais Sprague-Dawley (SD) com insuficiência cardíaca
(IC). Verificou-se nestes animais um aumento na expressão do receptor GABAA
na norepinefrina urinária. Células neuronais NG108-15 tratadas com LG
apresentaram alteração na expressão do GABAAR e da nNOS. Os resultados
indicam que os LG são uma ferramenta com potencial para ser utilizada em
ABSTRACT
Liposomes are spherical vesicles formed by one or several concentric lipid
bilayers that isolate one or more internal aqueous compartments of the external
environment, their major advantage is to be biocompatible. The γ-aminobutyric
acid (GABA) is the major inhibitory neurotransmitter in the central nervous
system (CNS). The literature clearly shows this neurotransmitter involvement in
cardiovascular regulation in normal or pathological conditions. The aim of this
study was to develop, characterize and test liposomes containing GABA. GABA
liposomes (GL) were prepared by the freeze- thawing method using the
following lipids: DSPE, DSPE-PEG CHO. The GL was tested in Wistar rats: 1)
On the central autonomic cardiovascular control in preparation with
anesthetized animals. We observed that after two days of
intracerebroventricular (ICV) GL microinjection occurred an attenuation of the
increased sympathetic renal nerve activity (RSNA) in animals that received
bicuculline methiodide (BMI) in the same location. 2) Front emotional stress.
After two and five days of ICV GL microinjection we observed an attenuation of
tachycardia when the animals were subjected to air jet stress. 3) The anxiety
test in the elevated plus maze. It was observed that the animals that received
ICV LG microinjection, showed after two days a decrease in anxiety behavior.
LG have also been microinjected in the paraventricular nucleus of the
hypothalamus (PVN) of animals Sprague-Dawley (SD) with heart failure (HF).
There was an increase in GABAA receptor (GABAAR) and neuronal nitric oxide
synthase (nNOS) expression, these animals also showed a decrease in urinary
the expression of GABAAR and nNOS. The results indicate that LG is a
SUMÁRIO
1 INTRODUÇÃO ... 14
1.1 Lipossomas como ferramenta utilizada na liberação de drogas .. 14
1.1.1 Estruturas e características biofísicas dos lipossoma ... 16
1.1.2 Microinjeção de lipossomas no sistema nervoso central ... 18
1.2 GABA e sua importância nas regiões centrais envolvidas na regulação cardiovascular ... 19 1.3 Insuficiência cardíaca congestiva ... 23
1.3.1 Interação entre GABA e óxido nítrico no PVN de animais com insuficiência cardíaca congestiva ... 24 1.4 Justificativa ... 25
2 OBJETIVOS ... 26
2.1 Objetivo geral ... 26
2.2 Objetivos específicos ... 26
3 MATERIAL E MÉTODOS ... 27
3.1 Lipossomas ... 27
3.1.1 Preparo de lipossomas ... 27
3.1.2 Desenvolvimento e caracterização dos lipossomas ... 29
3.2 Experimentos in vivo ... 31
3.2.1 Animais ... 31
3.3 Experimento in vitro ... 35
3.4 Protocolos experimentais ... 36
3.4.1 Ratos wistar submetidos ao registro da ASNR (anestesiados) 36 3.4.2 Ratos Wistar submetidos ao estresse por jato de ar ... 36
3.4.3 Ratos Wistar submetidos ao labirinto em cruz elevada ... 37
3.4.4 Ratos Wistar que receberam lipossomas marcados com DiI ... 38
3.4.5 Ratos SD com insuficiência cardíaca ... 39
3.4.6 Células NG108-15 ... 40
3.5 Análise estatística ... 43
4 RESULTADOS ... 44
4.1 Caracterização dos lipossomas ... 44
4.2 Experimentos com ratos wistar ... 48
4.3 Experimentos com ratos SD que apresentam ICC ... 58
4.4 Experimentos com células NG108-15 ... 64
5 DISCUSSÃO ... 78
6 CONCLUSÃO ... 89
ABREVIATURAS
ASNR - atividade simpática do nervo renal
BMI - bicuculina metiodide
CHO - Colesterol
CREB-P - fator de transcrição elemento responsivo a ligação de cAMP
fosforilado
FC - frequência cardíaca
DiI - 1,1’dioctadecil-3,3,3’,3’-tetrametil-indocarbocianina perclorato
DAF-FM - 4-amino-5metilamino-2’, 7’-difluorofluoresceina diacetato
DMH - hipotálamo dorsomedial
DSPC - Diestearoil-fosfatidilcolina
DSPE-PEG2000 - Diestearoil-fosfatidiletanolamina-polietileno glicol 2000
GAPDH - gliceraldeído-3-fosfato desidrogenase
GABA - ácido-γ-aminobutírico
GAD - descarboxilase do ácido glutâmico
GABAAR - receptores GABAA
GABA-T - GABA-transaminase
ICC - insuficiência cardíaca congestiva
ICV - intracerebroventricular
i.p. - intraperitoneal
LG - lipossoma GABA
LV - lipossoma vazio
NO - óxido nítrico
nNOS - óxido nítrico sintase neuronal
NTS - núcleo do trato solitário
PIN - proteína de inibição da nNOS
PVDF - difluoreto de polivinilideno
SD - ratos Sprague-Dawley
SG - solução GABA
SNC - sistema nervoso central
SHR - ratos espontaneamente hipertensos
SSADH - semi aldeído succínico desidrogenase
SUV - vesícula unilamelar pequena
Tc - temperatura de transição de fases
PAG - substância cinzenta periaqueductal
PAM - pressão arterial média
PEG - polietileno glicol
PVN - núcleo paraventricular do hipotálamo
RVLM - bulbo rostroventrolateral
VGAT - transportador vesicular de GAB
1 - INTRODUÇÃO
Apesar do enorme progresso feito pela neurociência nas últimas
décadas, o desenvolvimento de uma metodologia apropriada para estudo das
ações crônicas de diferentes drogas no sistema nervoso central (SNC) continua
sendo um desafio (Frezard et al., 2011).
Ao longo dos anos muitas técnicas vêm sendo utilizadas na para
elucidar o funcionamento de populações neuronais específicas. Dentre estas,
destaca-se o uso de lesões químicas e eletrolíticas, a estimulação elétrica, a
estimulação química e a bomba osmótica. Apesar destas técnicas terem
permitido um grande avanço na compreensão do funcionamento de
grupamentos neuronais, elas também apresentam algumas desvantagens. A
maioria delas não permite o estudo do efeito crônico de fármacos nos núcleos
cerebrais, com exceção da bomba osmótica. Esta permite a liberação crônica
de fármacos no cérebro, no entanto, apresenta como principal limitação o
volume liberado, muitas vezes alto para o estudo de núcleos cerebrais
específicos.
Uma alternativa interessante para a liberação crônica de drogas no SNC
poderia ser utilização de lipossomas. Ao longo dos anos estes carreadores de
fármaco tornaram-se objeto de vários estudos, mostrando inúmeras aplicações
práticas.
Lipossomas são vesículas esféricas microscópicas, constituídas de uma
ou várias bicamadas concêntricas de lipídios, que isolam um ou vários
compartimentos aquosos internos do meio externo (Frezard et al., 2005). Eles
podem encapsular substâncias hidrofílicas e/ou lipofílicas no compartimento
aquoso interno e na membrana, respectivamente (Figura 1) (Batista et al.,
2007). Uma grande vantagem no uso de lipossomas, com relação a outros
sistemas transportadores de fármacos é a sua elevada biocompatibilidade
(Frezard et al., 2005), baixos toxicidade e efeito colateral (Ulrich, 2002). Além
disso são sistemas altamente versáteis cujo tamanho, lamelaridade, superfície,
composição lipídica, volume e composição do meio aquoso interno podem ser
manipulados em função dos requisitos farmacêuticos e farmacológicos
(Frezard et al., 2005).
Estas vesículas foram descritas pela primeira vez na década de
sessenta, quando Banghan et al., (1965) observaram que fosfolipídios em
solução aquosa poderiam formar uma estrutura fechada em bicamada. Os
lipossomas foram utilizados inicialmente como modelo de membrana celular
devido a semelhança com a mesma. Somente na década de 70 sua
capacidade em armazenar drogas (Gregoriadis et al., 1971, Gregoriadis and
Ryman, 1972) e seu uso como carreador de fármacos (Gregoriadis, 1976)
foram explorados. A partir de então observou-se um grande avanço no
desenvolvimento e nas técnicas de preparo dos lipossomas, com a aprovação
de várias drogas, produtos e tecnologias baseadas na sua utilização (Torchilin,
2005).
1.1.1 - Estruturas e características biofísicas dos lipossomas
Lipossomas podem ser obtidos a partir de qualquer substância anfifílica
formadora de fase lamelar (Frezard et al., 2005). Os lipídios mais utilizados são
os que apresentam uma forma cilíndrica como os fosfolipídios (fosfatidilcolinas,
fosfatidilserina, fosfatidilglicerol e esfingomielina), que tendem a formar uma
bicamada estável na solução aquosa. Os fosfolipídios são caracterizados por
uma temperatura de transição de fases (Tc), na qual a membrana passa de
uma fase gel, onde a cadeia hidrocarbonada do lipídio está em estado
ordenado, para uma fase cristal-líquido, onde as moléculas ficam com
movimentos mais livres e os radicais hidrofílicos agrupados tornam-se
completamente hidratados. O comprimento e a saturação da cadeia lipídica
quando a temperatura ambiente é menor que a Tc dos lipossomas (Batista et
al., 2007). A adição de lipídios com carga efetiva negativa ou positiva podem
também ser incluídos na composição da membrana o que pode influenciar a
taxa de incorporação das substâncias, impedir a agregação/fusão das
vesículas lipídicas e modular seu destino no organismo (Frezard et al., 2005).
Um componente lipídico importante que entra muitas vezes na composição dos
lipossomas é o colesterol. Este aumenta a rigidez das membranas no estado
de cristal-líquido e reduz a rigidez e os defeitos estruturais das membranas na
fase gel (Frezard et al., 2005).
Lipossomas convencionais são compostos por fosfolipídios e colesterol.
In vivo, os lipossomas convencionais são reconhecidos pelo sistema fagocitário
mononuclear, sendo então rapidamente removidos da circulação (Vemuri and
Rhodes, 1995, Batista et al., 2007). Lipossomas de longa duração in vivo
podem ser obtidos por diferentes métodos, incluindo o revestimento da
superfície lipossômica com componentes hidrofílicos como os polietilenoglicóis
(PEG) (Torchilin, 2005, Batista et al., 2007). A camada hidrofílica superficial
destes polímeros aumenta o tempo de circulação dos lipossomas prevenindo o
reconhecimento e consequente associação com as opsoninas do plasma.
Desta forma, inibindo o processo de captura pelas células do sistema
fagocitário mononuclear, principalmente as células de Kupffer do fígado
(Needham et al., 1992, Batista et al., 2007).
O tamanho médio dos lipossomas varia de 20 a 5000 nm (Frezard et al.,
2005). Eles podem conter uma única bicamada lipídica ou bicamadas múltiplas
em torno do compartimento interno, sendo classificados em unilamelar ou
ou grandes, sendo caracterizados como lipossomas unilamelares pequenos
(SUVs - small unilamellar vesicles) e lipossomas unilamelares grandes (LUV -
large unilamellar vesicles) (Batista et al., 2007).
Várias características devem ser observadas no preparo dos
lipossomas. A definição do objetivo do estudo e o conhecimento das
características da substância a ser encapsulada são pontos importantes.
Deve-se considerar ainda a maximização da taxa de encapsulação do fármaco
encapsulado (Frezard et al., 2005). Associado a estes fatores torna-se também
importante a escolha de um método adequado para o preparo dos lipossomas.
Existem diversos métodos para o preparo de lipossomas, dentre eles
destaca-se o método de hidratação do filme lipídico destaca-seguida de etapas de
congelamento-descongelamento. Ele foi descrito pela primeira vez por Mayer et
al., (1985), sendo um método interessante para encapsular substâncias
hidrofílicas, uma vez que, aumenta o volume da solução no interior do
lipossoma (Sriwongsitanont and Ueno, 2011).
1.1.2 - Microinjeção de lipossomas no sistema nervoso central
Trabalhos prévios já demonstraram a viabilidade de encapsular
peptídeos em lipossomas para microinjeção dos mesmos no sistema nervoso
central. Estudos de Silva-Barcellos et al., (2001) mostraram o efeito da
microinjeção de lipossomas contendo angiotensina Ang-(1-7) no bulbo
rostroventrolateral (RVLM), um importante núcleo envolvido nas respostas
cardiovasculares (Dampney et al., 2003). A liberação crônica unilateral de
durante período noturno. Nenhum destes efeitos foi observado em animais que
receberam lipossomas vazios. É importante observar ainda que os lipossomas
foram preparados com fosfolipídios que apresentam elevada Tc, incluindo um
lipídio acoplado com polietilenoglicol. Os animais apresentaram efeitos
cardiovasculares até 5 dias após a microinjeção dos lipossomas contendo
Ang-(1-7). Através de estudo de liberação in vitro, foi possível demonstrar a
habilidade dos lipossomas em reter o peptídeo encapsulado. Após 5 dias, 98%
da Ang-(1-7) ainda apresentava-se retida dentro do lipossoma. Em outro
estudo, Silva-Barcellos et. al. (2004) demonstraram a importância das
características do lipossoma contendo Ang-(1-7) nos efeitos cardiovasculares
produzidos pela sua microinjeção unilateral na RVLM. Diversas variáveis como
o emprego ou não de lipídios acoplados ao polietilenoglicol, o aumento na
concentração de Ang-(1-7) encapsulada, a calibração ou não das vesículas,
foram exploradas na produção dos lipossomas. Observou-se que os
lipossomas de tamanho calibrado e de membrana rígida recoberta com
polietilenoglicol provocaram efeitos mais duradouros quando microinjetados na
RVLM.
1.2 - GABA e sua importância nas regiões centrais envolvidas na regulação cardiovascular
O ácido-γ-aminobutírico (GABA) é o neurotransmissor inibitório mais
prevalente no SNC de mamíferos. Estima-se que 40 a 50% de todo SNC utilize
GABA como neurotransmissor primário (Beleboni et al., 2004). Embora ele
só foi descrita 40 anos depois (Awapara et al., 1950, Roberts and Frankel,
1950, Florey and Mc, 1959). Após a década de 50, o interesse no seu potencial
neuroquímico cresceu significativamente. No entanto, apenas no início da
década de 70 foi demonstrado que o GABA preenchia todos os critérios
clássicos para ser considerado um neurotransmissor (Krnjevic, 1974, Bowery
and Smart, 2006).
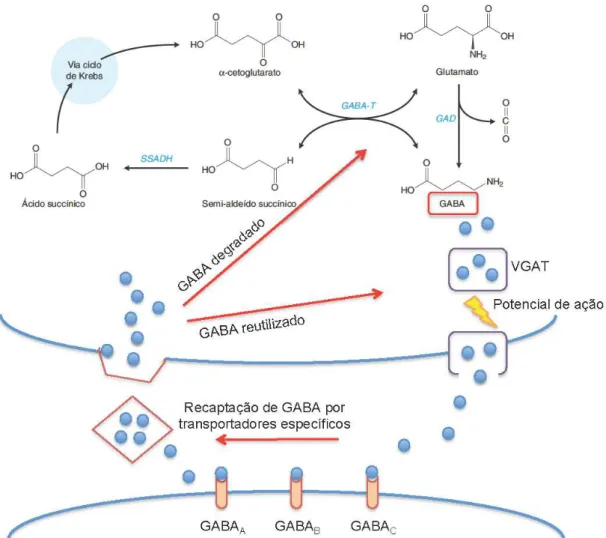
A principal via de formação do GABA envolve a descarboxilação do
L-glutamato em L-glutamato pela enzima descarboxilase do ácido glutâmico (GAD).
A quantidade de GABA no tecido esta diretamente relacionada com a presença
da GAD. O GABA é acondicionado em vesículas pré-sinápticas por um
transportador (VGAT). Em resposta a um potencial de ação, ocorre liberação
de GABA na fenda sináptica por fusão das vesículas contendo GABA com a
membrana pré-sináptica. A ação do GABA na fenda sináptica é finalizada
através da captação do neurotransmissor por transportadores específicos
localizados na superfície dos terminais pré-sinápticos e nas células gliais. A
maioria do GABA recaptado é reutilizado, a outra parte é degradada. No interior
das células a enzima mitocondrial GABA-transaminase (GABA-T) catalisa a
conversão do GABA em semi-aldeído succínico que é oxidado a ácido
succínico pela semi aldeído succínico desidrogenase (SSADH), entrando a
seguir no ciclo de Krebs, onde é transformado em α-cetoglutarato. A seguir, a
GABA-T regenera glutamato a partir do α-cetoglutarato (Figura 2) (Beleboni et
al., 2004).
As ações inibitórias desse neurotransmissor são mediadas por três
neurotransmissão gabaérgica pode ser dividida em rápida e lenta. Os
receptores GABAB produzem uma inibição lenta, uma vez que são acoplados
indiretamente a canais de cálcio e potássio, via proteína-G. Já os receptores
GABAA (GABAAR) e GABAc são diretamente acoplados a canais de cloro,
gerando uma inibição rápida (Beleboni et al., 2004, Vithlani et al., 2011).
Após uma exposição breve a altas concentrações de GABA (milimolar),
a ativação dos GABAAR localizados nos sítios sinápticos move o potencial de
membrana para longe do limiar de disparo, o que é chamado de inibição fásica.
Em contraste, baixas concentrações de GABA (submicromolar) presentes no
ambiente extracelular pode de forma persistente ativar receptores
extra-sinápticos gerando uma inibição tônica (Vithlani et al., 2011).
Diversos estudos já mostraram o envolvimento do GABA na regulação
autonômica. Este neurotransmissor exerce uma influência inibitória importante
em núcleos envolvidos na manutenção do tônus simpático. Trabalhos
demonstraram que a microinjeção intracerebroventricular (ICV) do agonista de
GABAAR, muscimol provocou uma diminuição na pressão arterial média
(PAM), frequência cardíaca (FC) e atividade simpática do nervo renal (ASNR)
em gatos (Antonaccio et al., 1978) e diminuição da PAM e FC em ratos
espontaneamente hipertensos (SHR) (Unger et al., 1984). De forma contrária,
injeções ICV do antagonista de GABAAR, bicuculina metiodide (BMI), aumentou
a PAM, FC e ASNR (DiMicco, 1982, Schmidt and DiMicco, 1984) (Karson et al.,
1999). A ativação sítio específica dos GABAAR também diminui a ASNR e a
PAM (Allen, 2002, Dampney et al., 2003) além de atenuar a resposta ao
Estudos anteriores, já demonstraram a viabilização do preparo de
lipossomas contendo GABA encapsulado. Loeb et al., 1982, 1986 utilizaram a
injeção intraperitoneal de lipossomas preparados apenas com fosfatidilserina
contendo GABA encapsulado, no tratamento da epilepsia induzida por injeção
intraperitoneal de penicilina em ratos. Os autores observaram uma diminuição
na atividade epilética, indicando um possível efeito do GABA no SNC.
1.3 - Insuficiência cardíaca congestiva
Atualmente a insuficiência cardíaca congestiva (ICC) é considerada uma
epidemia global, com aumento da prevalência em países em desenvolvimento.
Apesar de todo avanço terapêutico na área médica a morbidade e mortalidade
desta doença continuam em níveis altíssimos (May et al., 2013). A ICC pode
ser caracterizada por uma ativação neuro-humoral em resposta a diminuição
do débito cardíaco e consequente diminuição na perfusão tecidual (Watson et
al., 2006). A curto prazo, os mecanismos compensatórios desencadeados são
benéficos para manter a homeostase, mas a ativação crônica leva a uma
deterioração da função cardíaca e progressão da ICC (Pyner, 2014).
Já está bem estabelecido que pacientes e modelos de animais
experimentais para insuficiência cardíaca congestiva (ICC) apresentam o tônus
simpático aumentado (Xu et al., 2012). A longo prazo, a simpatoexcitação e
alta concentração da noradrenalina plasmática causam dano ao miocárdio e
apoptose, diminuindo a contratilidade do mesmo (Li and Patel, 2003). Sabe-se
que o aumento da simpatoexcitação que ocorre nesta condição é originado no
SNC. Em particular, o núcleo paraventricular do hipotálamo (PVN) tem se
destacado por apresentar um papel importante na integração da resposta
simpatoexcitatória na ICC (Sharma et al., 2011). O PVN é um núcleo pré-motor
simpático que está diretamente envolvido na regulação do tônus simpático e no
controle cardiovascular (Dampney et al., 2002, da Silva et al., 2011, Gomes da
1.3.1 - Interação entre GABA e NO no PVN de animais com insuficiência
cardíaca congestiva
O PVN é um núcleo envolvido na coordenação das respostas
neuro-humorais. Ele é dividido em diversos grupos neuronais, sendo os principais os
magnocelulares (que sintetizam vasopressina e ocitocina para serem liberados
na hipófise posterior em resposta a determinado estímulo, incluindo
hiperosmolaridade) e os neurônios parvocelulares neuroendócrinos que
secretam hormônios hipofisiotróficos e neurônios parvocelular pré-autonômicos
que controlam a atividade simpática (Stern, 2004, Pyner, 2009, 2014).
Diversos neurotransmissores/neuromoduladores são encontrados no
PVN. Entre eles, glutamato (Bains and Ferguson, 1997a, b) e angiotensina II (Li
and Ferguson, 1996) que geralmente exercem efeitos excitatórios nos reflexos
cardiovasculares (Miyawaki et al., 1996). Enquanto o GABA (Schmidt and
DiMicco, 1984) e óxido nítrico (NO) (Bredt et al., 1990) são mediadores
inibitórios que influenciam a atividade simpática no PVN (Li and Patel, 2003).
Especula-se que a interação entre os neurotransmissores excitatórios e
inibitórios neste núcleo possam influenciar a regulação do tônus simpático. O
equilíbrio destas interações parece apresentar um papel importante na
disfunção simpática observada na ICC. Estudos demonstraram que uma
redução nas ações inibitórias do NO e/ou GABA pode contribuir para o
aumento das ações de neurotransmissores/neuromoduladores excitatórios
como o glutamato e angiotensina II no PVN. Este desequilíbrio poderia
1.4 - Justificativa
Considerando a capacidade dos lipossomas de permitir a liberação de
fármacos de maneira crônica e a importância do GABA na regulação
cardiovascular central torna-se relevante a encapsulação do GABA em
lipossomas. Esta formulação poderá ser útil não somente no estudo da
influência crônica de GABA em diversas regiões cerebrais, como também no
melhor entendimento dos muitos estados patológicos que estão relacionados
7 - REFERÊNCIAS BIBLIOGRÁFICAS
Allen AM (2002) Inhibition of the hypothalamic paraventricular nucleus in
spontaneously hypertensive rats dramatically reduces sympathetic
vasomotor tone. Hypertension 39:275-280.
Antonaccio MJ, Kerwin L, Taylor DG (1978) Reductions in blood pressure, heart
rate and renal sympathetic nerve discharge in cats after the central
administration of muscimol, a GABA agonist. Neuropharmacology
17:783-791.
Awapara J, Landua AJ, Fuerst R, Seale B (1950) Free gamma-aminobutyric
acid in brain. The Journal of biological chemistry 187:35-39.
Bains JS, Ferguson AV (1997a) Nitric oxide regulates NMDA-driven GABAergic
inputs to type I neurones of the rat paraventricular nucleus. J Physiol 499
( Pt 3):733-746.
Bains JS, Ferguson AV (1997b) Reduced NMDA receptor sensitivity may
underlie the resistance of subpopulations of PVN neurons to
excitotoxicity. Neuroreport 8:2101-2105.
Banghan AD, Standish MM, Watkins JC (1965) Diffusion of univalent ions
across the lamellar swollen phospholipids. J Mol Biol.
Batista CM, Carvalho CMBd, Magalhães NSS (2007) Lipossomas e suas
aplicações terapêuticas: Estado da arte. Brazilian Journal of
Pharmaceutical Sciences.
Beleboni RO, Carolino RO, Pizzo AB, Castellan-Baldan L, Coutinho-Netto J,
aspects of GABAergic neurotransmission: pathological and
neuropsychobiological relationships. Cell Mol Neurobiol 24:707-728.
Bowery NG, Smart TG (2006) GABA and glycine as neurotransmitters: a brief
history. Br J Pharmacol 147 Suppl 1:S109-119.
Bredt DS, Hwang PM, Snyder SH (1990) Localization of nitric oxide synthase
indicating a neural role for nitric oxide. Nature 347:768-770.
Chebib M, Johnston GA (1999) The 'ABC' of GABA receptors: a brief review.
Clin Exp Pharmacol Physiol 26:937-940.
da Silva AQ, Fontes MA, Kanagy NL (2011) Chronic infusion of angiotensin
receptor antagonists in the hypothalamic paraventricular nucleus
prevents hypertension in a rat model of sleep apnea. Brain Res
1368:231-238.
Dampney RA, Coleman MJ, Fontes MA, Hirooka Y, Horiuchi J, Li YW, Polson
JW, Potts PD, Tagawa T (2002) Central mechanisms underlying short-
and long-term regulation of the cardiovascular system. Clin Exp
Pharmacol Physiol 29:261-268.
Dampney RA, Horiuchi J, Tagawa T, Fontes MA, Potts PD, Polson JW (2003)
Medullary and supramedullary mechanisms regulating sympathetic
vasomotor tone. Acta physiologica Scandinavica 177:209-218.
DiMicco JA (1982) Blockade of forebrain gamma-aminobutyric acid (GABA)
receptors and reflex activation of the cardiac vagus in anesthetized cats.
J Pharmacol Exp Ther 223:654-661.
Florey E, Mc LH (1959) The effects of factor I and of gamma-aminobutyric acid
Frezard F, dos Santos RA, Fontes MA (2011) Liposome-encapsulated
neuropeptides for site-specific microinjection. Methods Mol Biol
789:343-355.
Frezard F, Schettini DA, Rocha OG, Demicheli C (2005) Lipossomas:
propriedades físico-farmacológicas, aplicações à base de antimônio.
Química Nova 28:511-518.
Gomes da Silva AQ, Xavier CH, Campagnole-Santos MJ, Caligiorne SM,
Baltatu OC, Bader M, Santos RA, Fontes MA (2012) Cardiovascular
responses evoked by activation or blockade of GABA(A) receptors in the
hypothalamic PVN are attenuated in transgenic rats with low brain
angiotensinogen. Brain Res 1448:101-110.
Gregoriadis G (1976) The carrier potential of liposomes in biology and medicine
(second of two parts). The New England journal of medicine
295:765-770.
Gregoriadis G, Leathwood PD, Ryman BE (1971) Enzyme entrapment in
liposomes. FEBS letters 14:95-99.
Gregoriadis G, Ryman BE (1972) Fate of protein-containing liposomes injected
into rats. An approach to the treatment of storage diseases. European
journal of biochemistry / FEBS 24:485-491.
Karson AB, Aker R, Ates N, Onat F (1999) Cardiovascular effects of
intracerebroventricular bicuculline in rats with absence seizures. Epilepsy
research 34:231-239.
Krnjevic K (1974) Chemical nature of synaptic transmission in vertebrates.
Li YF, Patel KP (2003) Paraventricular nucleus of the hypothalamus and
elevated sympathetic activity in heart failure: the altered inhibitory
mechanisms. Acta physiologica Scandinavica 177:17-26.
Li Z, Ferguson AV (1996) Electrophysiological properties of paraventricular
magnocellular neurons in rat brain slices: modulation of IA by angiotensin
II. Neuroscience 71:133-145.
May CN, Yao ST, Booth LC, Ramchandra R (2013) Cardiac sympathoexcitation
in heart failure. Auton Neurosci 175:76-84.
Mayer LD, Hope MJ, Cullis PR, Janoff AS (1985) Solute distributions and
trapping efficiencies observed in freeze-thawed multilamellar vesicles.
Biochimica et biophysica acta 817:193-196.
Miyawaki T, Minson J, Arnolda L, Chalmers J, Llewellyn-Smith I, Pilowsky P
(1996) Role of excitatory amino acid receptors in cardiorespiratory
coupling in ventrolateral medulla. Am J Physiol 271:R1221-1230.
Needham D, McIntosh TJ, Lasic DD (1992) Repulsive interactions and
mechanical stability of polymer-grafted lipid membranes. Biochimica et
biophysica acta 1108:40-48.
Pyner S (2009) Neurochemistry of the paraventricular nucleus of the
hypothalamus: implications for cardiovascular regulation. Journal of
chemical neuroanatomy 38:197-208.
Pyner S (2014) The paraventricular nucleus and heart failure. Experimental
physiology 99:332-339.
Roberts E, Frankel S (1950) gamma-Aminobutyric acid in brain: its formation
Schmidt B, DiMicco JA (1984) Blockade of GABA receptors in periventricular
forebrain of anesthetized cats: effects on heart rate, arterial pressure,
and hindlimb vascular resistance. Brain Res 301:111-119.
Sharma NM, Zheng H, Mehta PP, Li YF, Patel KP (2011) Decreased nNOS in
the PVN leads to increased sympathoexcitation in chronic heart failure:
role for CAPON and Ang II. Cardiovasc Res 92:348-357.
Silva-Barcellos NM, Caligiorne S, dos Santos RA, Frezard F (2004) Site-specific
microinjection of liposomes into the brain for local infusion of a short-lived
peptide. J Control Release 95:301-307.
Sriwongsitanont S, Ueno M (2011) Effect of freeze-thawing process on the size
and lamellarity of PEG-lipid liposomes. The Open Colloid Science
Journal 4:1-6.
Stern JE (2004) Nitric oxide and homeostatic control: an intercellular signalling
molecule contributing to autonomic and neuroendocrine integration?
Progress in biophysics and molecular biology 84:197-215.
Stotz-Potter EH, Willis LR, DiMicco JA (1996) Muscimol acts in dorsomedial but
not paraventricular hypothalamic nucleus to suppress cardiovascular
effects of stress. J Neurosci 16:1173-1179.
Torchilin VP (2005) Recent advances with liposomes as pharmaceutical
carriers. Nature reviews Drug discovery 4:145-160.
Ulrich AS (2002) Biophysical aspects of using liposomes as delivery vehicles.
Bioscience reports 22:129-150.
Unger T, Becker H, Dietz R, Ganten D, Lang RE, Rettig R, Schomig A, Schwab
muscimol in spontaneously hypertensive rats. Role of the
sympathoadrenal axis. Circulation research 54:30-37.
Vemuri S, Rhodes CT (1995) Preparation and characterization of liposomes as
therapeutic delivery systems: a review. Pharmaceutica acta Helvetiae
70:95-111.
Vithlani M, Terunuma M, Moss SJ (2011) The dynamic modulation of GABA(A)
receptor trafficking and its role in regulating the plasticity of inhibitory
synapses. Physiological reviews 91:1009-1022.
Watson AM, Hood SG, May CN (2006) Mechanisms of sympathetic activation in
heart failure. Clin Exp Pharmacol Physiol 33:1269-1274.
Xavier CH, Nalivaiko E, Beig MI, Menezes GB, Cara DC, Campagnole-Santos
MJ, Fontes MA (2009) Functional asymmetry in the descending
cardiovascular pathways from dorsomedial hypothalamic nucleus.
Neuroscience 164:1360-1368.
Xu B, Zheng H, Patel KP (2012) Enhanced activation of RVLM-projecting PVN
neurons in rats with chronic heart failure. Am J Physiol Heart Circ Physiol