Aplicação de tecnologias eletroquímicas (oxidação
via radicais hidroxila, oxidação mediada via cloro ativo
e eletrocoagulação) para o tratamento de efluentes reais ou sintéticos
Dayanne Chianca de Moura
____________________________________________
Tese de Doutorado
Natal/RN, outubro de 2014
CENTRO DE CIÊNCIAS EXATAS E DA TERRA
INSTITUTO DE QUÍMICA
APLICAÇÃO DE TECNOLOGIAS ELETROQUÍMICAS
(OXIDAÇÃO VIA RADICAIS HIDROXILA, OXIDAÇÃO
MEDIADA VIA CLORO ATIVO E ELETROCOAGULAÇÃO)
PARA O TRATAMENTO DE EFLUENTES REAIS OU
SINTÉTICOS
Tese apresentada ao Programa de Pós-Graduação em Química da Universidade Federal do Rio Grande do Norte, em cumprimento às exigências para obtenção do título de Doutor em Química.
Orientador: Prof. Dr. Carlos Alberto
Martínez-Huitle
NATAL - RN
Divisão de Serviços Técnicos Catalogação da Publicação na Fonte. UFRN
Biblioteca Setorial do Instituto de Química Moura, Dayanne Chianca de.
Aplicação de tecnologias eletroquímicas (oxidação via radicais hidroxila, oxidação mediada via cloro ativo e eletrocoagulação) para o tratamento de efluentes reais ou sintéticos / Dayanne Chianca de Moura. – Natal, RN, 2015.
Natal, RN, 2014. 164 f. : il.
Orientador: Carlos Alberto Martínez-Huitle.
Tese (Doutorado em Química) - Universidade Federal do Rio Grande do Norte. Centro de Ciências Exatas e da Terra. Programa de Pós-Graduação em Química.
1.Processos eletroquímicos – Tese. 2. Tratamento de Efluentes - Tese. 3. Efluente real da UFRN - Tese. 4. Corantes - Tese. 5. Oxidação Eletroquímica - Tese. 6. Materiais Eletrocatalíticos – Tese. I. Martínez-Huitle, Carlos Alberto II. Universidade Federal do Rio Grande do Norte. III. Título.
Dedico esta grande vitória aos meus pais, que nunca hesitaram
em abrir mão de seus próprios sonhos em favor de suas filhas.
A Deus, pelo dom da vida, por sua infinita bondade, graça, misericórdia e sua
presença tão real em meu viver... Meu Senhor muito obrigada!
Ao meu orientador, Prof. Dr. Carlos Alberto Martínez-Huitle, pelo crédito e pela
oportunidade não só de trabalhar em seu grupo de pesquisa, mas também de alcançar
esse objetivo. Obrigada mesmo pela confiança, orientação e, sobretudo, por ter sido um
orientador-amigo que sempre se mostrou disposto a me ouvir. As sérias e descontraídas
"charlas" sempre surtiram efeito. Jamais esquecerei das primeiras palavras de ânimo que
me dirigiu no dia em que fui acolhida, palavras que me trouxeram um alívio e renovou
um sonho.
Agradezco también a lo Prof. Dr Marco Antonio Quiroz de la Universidad de
Las Américas-Puebla por me haber recibido, por la bienvenida muy fraterna en mi
estancia de doctorado por allá y, principalmente por la amistad. No podría dejar de
agradecer también a todos del Laboratorio de Electroquímica y especialmente a la
Profa. Dra. Mónica Cerro-López por su atención y cuidado.
À Cynthia Kérzia pela dedicação, paciência, responsabilidade e cumplicidade;
uma pessoa que me acompanhou em quase todos os momentos de experimento. À
Elisama pela disponibilidade em ensinar como dar os primeiros passos no laboratório;
sua ajuda foi fundamental. À Martha Gallegos, Izabelle e Mariana pela grandiosa ajuda
nos trabalhos experimentais. Obrigada mesmo pelo apoio!
A todos os colegas do Laboratório de Eletroquímica Ambiental e Aplicada, os
momentos de agradável convivência, de sérias conversas e não há como esquecer
também dos momentos de grande descontração. Todos eles foram valiosos!
Agradeço à equipe da Química Tecnológica - professores, Reunis, técnicas de
laboratório e monitores - obrigada pela respeitosa convivência e principalmente, por
fazerem parte da formação na docência assistida.
Também não poderia deixar de registrar um agradecimento especialíssimo à
Aline Felipe e Danielle Maia: conseguiram enxergar o que eu, num determinado
momento, não podia ver. Como vocês foram importantes!
À minha família por estarem sempre de forma tão intensa em minha vida. Aos
meus pais Pedro e Valda e às minhas irmãs Daniella e Darlenne por sofrerem e
vibrarem cada conquista. Ah, e a Clarinha obrigada pelos sorrisos que tanto alegram
um obstáculo.
Aos que fazem parte do Instituto de Química, professores e funcionários.
À CAPES, pelo suporte financeiro concedido.
A todas as pessoas que, de alguma forma, participaram e contribuíram para a
“Se não puder voar, corra. Se não puder correr, ande. Se não puder andar, rasteje,
mas continue em frente de qualquer jeito.”
Martin Luther King Jr
“Tudo é possível ao que crê.”
Neste trabalho foi estudada a degradação de efluentes reais e sintéticos utilizando processos eletroquímicos, como oxidação via radicais hidroxila, oxidação mediada via cloro ativo e eletrocoagulação. O efluente real utilizado foi coletado no tanque decantador da Estação de Tratamento de Efluentes da Universidade Federal do Rio Grande do Norte (ETE-UFRN) e o outro, um efluente do corante têxtil Azul Ácido113 (AB 113) foi sintetizado em laboratório. No processo eletroquímico, os efeitos do material anódico, da densidade de corrente, da presença e da concentração de cloreto assim como das espécies de cloro ativa geradas in situ foram avaliados. Eletrodos de diferentes composições, Ti/Pt, Ti/Ru0,3Ti0,7O2, DDB, Pb/PbO2 e Ti/TiO2
-nanotubos/PbO2 foram utilizados como ânodos. Esses eletrodos foram submetido à
análises eletroanalíticas com o objetivo de verificar como acontecem os processos anódicos e catódicos frente as concentrações de NaCl e eletrólito suporte utilizado. Os potencias de desprendimento de oxigênio também foram verificados. O efeito das espécies de cloro ativo formadas sob a eficiência do processo foi avaliado através da remoção da matéria orgânica do efluente UFRN. O tratamento do efluente ETE-UFRN usando os eletrodos Ti/Pt, DDB e Ti/Ru0,3Ti0,7O2 foi avaliado, obtendo boas
performances. A degradação eletroquímica do efluente ETE-UFRN foi capaz de promover a diminuição da concentração de COT e DQO em todos os ânodos testados. Entretanto, Ti/Ru0,3Ti0,7O2 apresentou uma degradação considerável devido as espécies
de cloro ativa geradas in situ. Os resultados obtidos com o processo eletroquímico na
presença de cloreto foram mais satisfatórios do que aqueles obtidos na ausência. A adição de 0,021 M NaCl resultou em remoções mais rápidas da matéria orgânica. Num segundo momento, foi preparado e caracterizado o eletrodo Ti/TiO2-nanotubos/PbO2 de
acordo com o que reporta a literatura, entretanto sua preparação foi para um disco (10 cm de diâmetro) com área superficial bem superior ao descrito pelos mesmos autores, visando aplicação ao efluente do corante têxtil AB 113. Imagens de MEV foram tomadas a fim de se observar o crescimento dos nanotubos de TiO2 bem como confirmar
a eletrodeposição do PbO2. Também foi utilizado um microscópio de Força Atômica
para comprovar a formação desses nanotubos. Além disso, foi testada e constatada uma alta estabilidade eletroquímica do eletrodo Ti/TiO2-nanotubos/PbO2 para aplicações a
longo prazo indicando como um ótimo material eletrocatalítico. A oxidação eletroquímica do AB 113 utilizando Ti/Pt, Pb/PbO2, Ti/TiO2-nanotubos/PbO2 e Al/Al
(eletrocoagulação) também foi estudada. Entretanto, as melhores remoções de cor e decaimento de DQO foram obtidas quando Ti/TiO2-nanotubos/PbO2 foi utilizado como
ânodo, removendo até 98% de cor e 92,5% de decaimento de DQO. Análises de CG/EM foram realizadas a fim de se identificar os possíveis intermediários formados na degradação do AB 113.
In this work the degradation of real and synthetic wastewater was studied using electrochemical processes such as oxidation via hydroxyl radicals, mediated oxidation via active chlorine and electrocoagulation. The real effluent used was collected in the decanter tank of the Federal University of Rio Grande do Norte (ETE-UFRN) of Effluent Treatment Plant and the other a textile effluent dye Ácido Blue 113 (AB 113) was synthesized in the laboratory. In the electrochemical process, the effects of anode material, current density, the presence and concentration of chloride as well as the active chlorine species on site generated were evaluated. Electrodes of different compositions, Ti/Pt, Ti/Ru0,3Ti0,7O2, BDD, Pb/PbO2 and Ti/TiO2-nanotubes/PbO2 were
used as anodes. These electrodes were subjected to electroanalytical analysis with the goal of checking how happen the anodic and cathodic processes across the concentrations of NaCl and supporting electrolyte used. The potential of oxygen evolution reaction were also checked. The effect of active chlorine species formed under the process efficiency was evaluated by removing the organic matter in the effluent-ETE UFRN. The wastewater treatment ETE-UFRN using Ti/Pt, DDB and Ti/Ru0,3Ti0,7O2 electrodes was evaluated, obtaining good performances. The
electrochemical degradation of effluent-UFRN was able to promote the reduction of the concentration of TOC and COD in all tested anodes. However, Ti/Ru0,3Ti0,7O2 showed a
considerable degradation due to active chlorine species generated on site. The results obtained from the electrochemical process in the presence of chloride were more satisfactory than those obtained in the absence. The addition of 0.021 M NaCl resulted in a faster removal of organic matter. Secondly, was prepared and characterized the electrode Ti/TiO2-nanotubes/PbO2 according to what the literature reports, however
their preparation was to disk (10 cm diameter) with surface area and higher than that described by the same authors, aiming at application to textile effluent AB 113 dye. SEM images were taken to observe the growth of TiO2 nanotubes and confirm the
electrodeposition of PbO2. Atomic Force Microscope was also used to confirm the
formation of these nanotubes. Furthermore, was tested and found a high electrochemical stability of the electrode Ti/TiO2-nanotubes/PbO2 for applications such as long-term
indicating a good electrocatalytic material. The electrochemical oxidation of AB 113 using Ti/Pt, Pb/PbO2 and Ti/TiO2-nanotubes/PbO2 and Al/Al (electrocoagulation) was
also studied. However, the best color removal and COD decay were obtained when Ti/TiO2-nanotubes/PbO2 was used as the anode, removing up to 98% of color and
92,5% of COD decay. Analysis of GC/MS were performed in order to identify possible intermediates formed in the degradation of AB 113.
KEY WORDS: Effluent Treatment. Real Effluent UFRN. Dyes. Electrochemical
Figura 1.1 - Distribuição da água no planeta... 18
Figura 2.1 - Estrutura química de um azo corante... 26
Figura 2.2 - Exemplos de métodos de tratamento de efluentes... 29
Figura 2.3 - Conceito do sistema convencional de tratamento de esgotos... 33
Figura 2.4 - Valo de oxidação da ETE-UFRN. ... 35
Figura 2.5 - Tanque decantador da ETE-UFRN. ... 36
Figura 2.6 - Representação esquemática da oxidação eletroquímica de compostos orgânicos em ânodos de óxidos metálicos (MOX), formando superóxido (MOx+1). ... 43
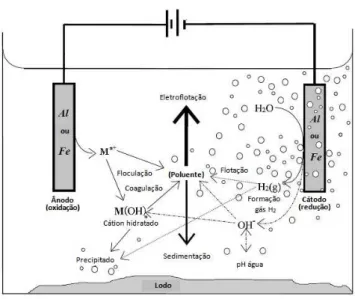
Figura 2.7 - Mecanismo durante coagulação eletroquímica... 50
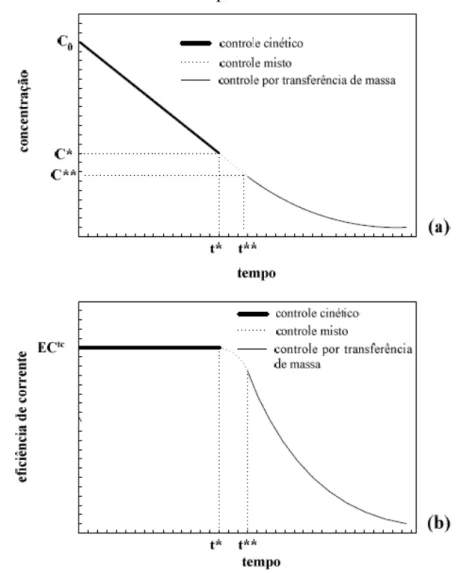
Figura 2.8 - a) Concentração em função do tempo; b) eficiência de corrente em função do tempo. ... 57
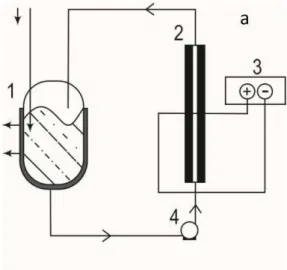
Figure 3.1 - Electrochemical flow cell configuration for the oxidation experiments at Ti/Pt and BDD anodes: (1) thermoregulated reservoir; (2) electrochemical flow cell; (3) power supply and (4) pump. ... 78
Figure 3.2 - Current density-potential curves for the Pt electrode in the presence of different amounts of NaCl on (a) Pt/Ti and (b) BDD anodes. Na2SO4 as supporting electrolyte; scan rate: 5 mV s−1 and 25°C. ... 81
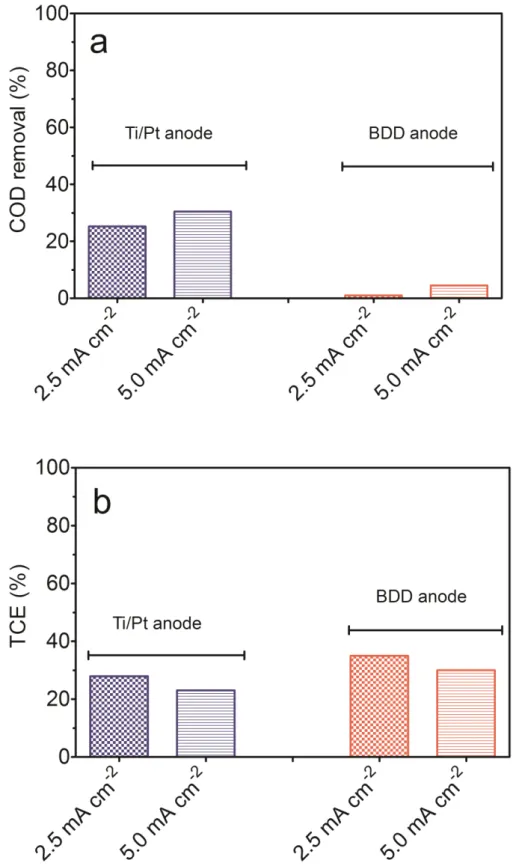
Figure 3.3 - (a) % of COD removal and (b) %TCE, as a function of applied current density (2.5 and 5.0 mA cm−2), during direct electrochemical oxidation of real effluent by using Ti/Pt and BDD anodes... 83
Figure 3.4 - (a) % of COD removal and (b) %TCE, as a function of applied current density (2.5 and 5.0 mA cm−2), during Cl- mediated oxidation of real effluent by using Ti/Pt and BDD anodes………. 85
Figure 4.1 - Diagram of the one-compartment electrochemical cell used
for studying active chlorine production as well as Cl- mediated
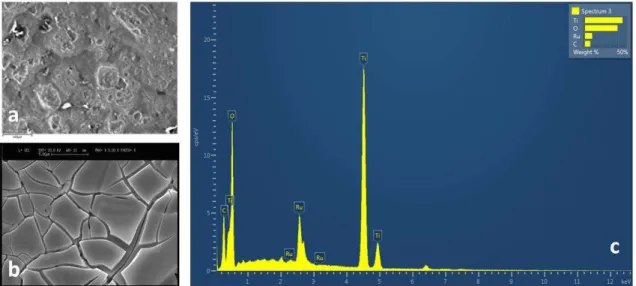
oxidation of real effluent: C, counter, R, reference, and W,
electrocatylitic material used (c, EPMA spectrum), as anode, for
studying active chlorine production as well as Cl- mediated
oxidation of real effluent... 99
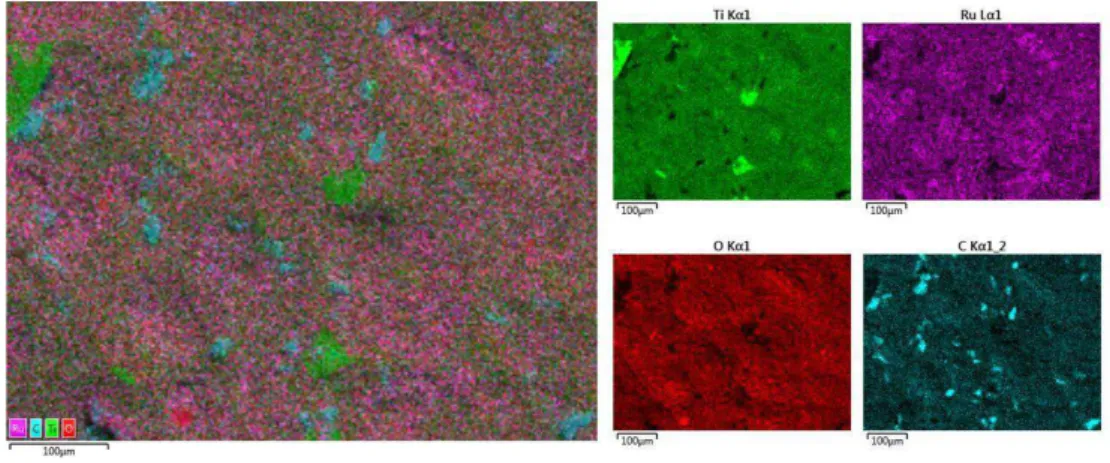
Figure 4.3 - EDS layered image as evidence of the dispersion/distribution of
each one of the components of anode used……… 100
Figure 4.4 - Cyclic voltammetric curves obtained at Ti/Ru0.3Ti0.7O2
electrode in absence (Na2SO4 0.01 mol L-1) and in the presence
of NaCl (1.5; 2.5; 3.5 g L-1) recorded at 10 mV s-1……… 100
Figure 4.5 - Linear polarization curves recorded at Ti/Ru0.3Ti0.7O2 electrode
in absence (Na2SO4 0.01 mol L-1) and in the presence of NaCl
(1.5; 2.5; 3.5 g L-1), scan rate 10 mV s-1……….. 103
Figure 4.6 - Active chlorine concentrations assessed in the course of the
electrolysis of a solution containing with 2.5 g L-1 of NaCl by
applying 25, 50 and 75 mA cm-2 at 25 °C……….. 105
Figure 4.7 - TOC removal efficiency as a function of applied current density
(25; 50 and 75mA cm-2) after 10 min of electrochemical
treatment of real effluent by Cl- mediated oxidation……….. 107
Figure 4.8 - Profile of pH behavior, as a function of time at different current densities (25; 50 and 75 mA cm-2), during electrochemical treatment of real effluent collected from biological-physical chemical treatment station at UFRN... 110
Figure 5.1 - (a) SEM image of anodized Ti/TiO2-nanotubes. The inset (b) and
(c) are the SEM images of the magnified orderly arranged
nanotubes. (d) EDS spectrum regarding the composition analysis,
showing that it corresponds to TiO2... 120
Figura 5.2 - (a) SEM images of PbO2 deposit into Ti/TiO2-nanotubes and the
magnified orderly arranged PbO2-tetragonal crystals. (c) EDS
spectrum regarding the composition analysis, showing that the
thin film corresponds to PbO2... 120
Figura 5.3 - Electrochemical measurements obtained in H2SO4: a) CV curves
curves for both electrodes...
Figure 5.4 - Electrochemical treatment of synthetic dye effluent using a disk
Ti/TiO2-nanotubes/PbO2 anode with 65 cm2 of geometrical area
by using electrochemical flow cell. Color decay, as a function of
electrical charge passed, by applying different current densities.
The inset is the percentage of COD removal, as a function of
applied current density. ... 123
Figure 6.1 - Design of the electrochemical flow cell. 1a) Different
compartments of the cell: A) anodic compartment, B) electrolysis
compartment and C) Cathodic compartment. 1b) Electrolysis
compartment: One inlet and outlet section. 1c) Electrolyte
distribution in the central compartment toward electrode
surfaces... 136
Figure 6.2 - (a) SEM image of anodized Ti/TiO2-nanotubes, (b) magnification
of anodized Ti/TiO2-nanotubes (c) SEM image of the magnified
orderly arranged PbO2-tetragonal crystals and (d) SEM image of
PbO2 deposit into Ti/TiO2-nanotubes. ... 138
Figure 6.3 - Polarization curves at different electrodes obtained in 1 M H2SO4
with a scan rate of 50 mV s-1. Electrode area: 4 cm2……….. 139
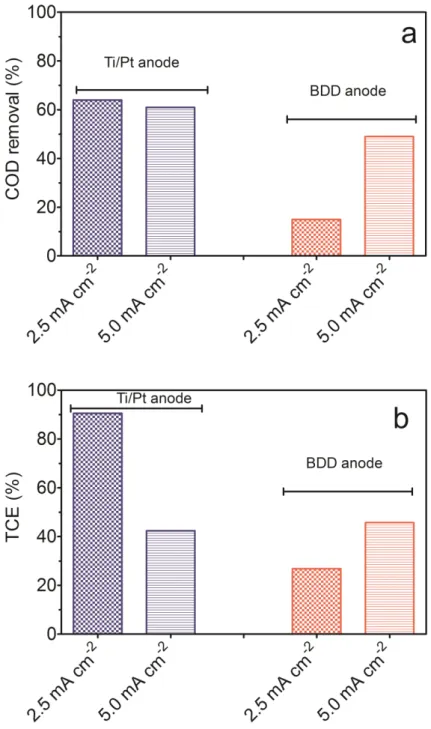
Figure 6.4 - Graphs with values in percentage of colour removal during the
electrochemical treatment EC and EO, depending on the
electrical charge passed (Q), current density and process…………... 142
Figure 6.5 - Graphs with values in percentage of chemical oxygen demand
(COD) after electrochemical treatment…………...……… 142
Figure 6.6 - Chromatogram of a sample collection at the end of
electrooxidation time when the Ti/TiO2-nanotubes/PbO2
Table 3.1 - Energy consumption calculated from Eq. (13), per volume of
treated effluent during direct and mediated oxidation of a real
effluent... 87
Table 4.1 - Percentage of color and COD decays and energy consumption
for the indirect electro-oxidation with active chlorine of organic
pollutants in chloride solutions using undivided cells with
DSA-type anodes. ... 95
Table 4.2 - Operating potential (E), energy consumption and cost for the
electrochemical treatment by Cl- mediated oxidation... 110
Table 5.1 - The characteristics of Acid Blue 113 (AB 113)... 119
Table 6.1 - Percentage of color and COD removals and energy cost for the
electrochemical oxidation of selected dyes solutions using PbO2
and Pt anodes... 131
Table 6.2 - The characteristics of Acid Blue 113 (AB 113)……... 134
Table 6.3 - Values color removal, COD decay in percent, energy cost and
consumption, per volume of treated effluent during anodic
oxidation of AB 113 for: (i) different applied current densities
and (ii) several anodes. [AB]0 =250 mg dm-3, electrolyte: Na2SO4
A - Ampere.
AB 113 - Corante Azul Ácido.
ADE - Ânodo Dimensionalmente Estável (em inglês Dimensionally Stable
Anodes, DSA).
DDB - Diamante Dopado com Boro (em inglês Boron Doped Diamond,
BDD).
CG/EM - Cromatografia Gasosa acoplada a Espectrometria de Massa (em inglês
Gas Chromatography Mass Espectrometry, GC/MS).
Cl- - Íons Cloreto.
CI - Color Index.
CONAMA - Conselho Nacional do Meio Ambiente.
COT - Carbono Orgânico Total (em inglês Total Organic Carbon, TOC).
DQO - Demanda Química de Oxigênio (em inglês Chemical Oxygen Demand,
COD).
EC - em inglês Electrocoagulation.
EDX - Espectroscopia de Difração de Raios X (em inglês X-Ray
Diffractometer, XRD).
ETE - Estação de Tratamento de Efluentes.
J - Densidade de corrente.
kWh - Kilowatt hora.
kWh m-3 - Kilowatt hora por metro cúbico.
mA cm-2 - Miliampere por centímetro quadrado.
MEV - Microscopia Eletrônica de Varredura (em inglês Scanning Electron
Microscope, SEM).
MFA - Microscopia de Força Atômica (em inglês Atomic Force Microscopy,
AFM).
OE - Oxidação eletroquímica (em inglês Electrochemical Oxidation, EO).
POAs - Processos Oxidativos Avançados (em inglês Advanced Oxidation
Processes, AOP).
RDO - Reação de Desprendimento de Oxigênio (em inglês Oxygen Evolution
Reaction, OER).
Ti/Pt - Platina suportada em Titânio.
CAPÍTULO 1 1.I INTRODUÇÃO... 18
CAPÍTULO 2 ASPECTOS TEÓRICOS... 23
2.1 PROBLEMA AMBIENTAL... 23
2.2 LEGISLAÇÃO AMBIENTAL... 24
2.3 CONTAMINAÇÃO DA INDÚSTRIA TÊXTIL... 24
2.4 CORANTES TÊXTEIS E SUA CLASSIFICAÇÃO... HPAs... 25 2.5 TRATAMENTOS DE EFLUENTES... HPAs... 28 2.5.1 Tratamento Biológico... HPAs... 30 2.5.2 Tratamento Físico-Químico... 30
2.5.3 Tratamento Químico... HPAs... 31 2.6 ESTAÇÕES DE TRATAMENTO DE EFLUENTES (ETE)... 33
2.6.1 ETE – UFRN... 34
2.7 TECNOLOGIAS ELETROQUÍMICAS... 37
2.7.1 Oxidação Eletroquímica... 39
2.7.1.1 Reações nos Eletrodos... 42
2.7.1.2 Eletrodos Utilizados... 45
2.7.2 Eletrocoagulação... 49
2.7.2.1 Reações de Eletrocoagulação com Eletrodos de Alumínio... 51
2.8 DENSIDADE DE CORRENTE LIMITE... 55
2.9 MÉTODOS ANALÍTICOS PARA QUANTIFICAR MATÉRIA... ORGÂNICA 58 2.9.1 Demanda Química de Oxigênio (DQO)... 58
2.9.2 Carbono Orgânico Total (COT)... 59
REFERÊNCIAS... 62
CAPÍTULO 3 CL- MEDIATED ELECTROCHEMICAL OXIDATION FOR TREATING AN EFFLUENT USING PLATINUM AND DIAMOND ANODES………. 73
3.1 INTRODUCTION……… 74
3.2 MATERIALS AND METHODS……….. 77
3.2.4 Electro-oxidation Experiments……….. 77
3.2.5 Analytical Methods……….……… 78
3.3 RESULTS AND DISCUSSION... 80
3.3.1 Polarization Curves in the Presence of Halide Ion………... 80
3.3.2 COD Removal by Electrochemical Treatment………. 82
3.3.3 Effect of NaCl Dissolved in the Effluent……… 84
3.3.4 Energy Consumption Estimation………... 87
3.4 CONCLUSIONS... 88
CAPÍTULO 4 ACTIVE CHLORINE SPECIES ELECTROGENERATED ON Ti/Ru0.3Ti0.7O2 SURFACE: ELECTROCHEMICAL BEHAVIOR, CONCENTRATION DETERMINATION AND THEIR APPLICATION………. 92
4.1 INTRODUCTION………. 93
4.2 EXPERIMENTAL……… 96
4.2.1 Reagents………... 96
4.2.2 Surface Analysis...………... Analysis………... 96 4.2.3 Electrochemical Measurements………. 97
4.2.4 Active Chlorine Species………... 97
4.2.5 Electro-oxidation Experiments……….. 98
4.2.6 Characteristics of the Wastewater Effluent Generated by UFRN 99 4.3 RESULTS AND DISCUSSION………... 99
4.3.1 Surface Morphology……… 99
4.3.2 Electrochemical Measurements………. 100
4.3.3 Electrolysis of Chloride Solutions………...…... Solutions………... 104 4.3.4 Electrochemical Treatment of Actual Effluent………. 107
4.3.5 Energy Consumption and Cost……….. 110
4.4 CONCLUSIONS………... 111 CAPÍTULO 5
LARGE DISK ELECTRODES OF Ti/TiO2-NANOTUBES/PbO2
5.1 INTRODUCTION………...
..
116
5.2 EXPERIMENTAL………....
...
117
5.2.1 Preparation of Ti/TiO2-nanotubes and Ti/TiO2-nanotubes/PbO2 117
5.2.2 Surface Characterization……… 6.2.3 Electrochemical measurements 118 5.2.3 Electrochemical Experiments………. 118
5.3 RESULTS AND DISCUSSION... 119
5.4 CONCLUSIONS………... 124
CAPÍTULO 6 ELECTROCHEMICAL DEGRADATION OF ACID BLUE 113 BY USING DIFFERENT ELECTRODE MATERIALS……….... 129
6.1 INTRODUCTION………... .. 130 6.2 EXPERIMENTAL……….... ... 133 6.2.1 Chemicals and Dye Solution………... 133
6.2.2 Electrodes………... 134
6.2.3 Surface Analysis of Ti/TiO2-nanotubes/PbO2………... 135
6.2.4 Electrochemical Measurements………. 135
6.2.5 EO and EC Experiments……… 135
6.2.6 Analytical Methods………. 136
6.2.7 Gas Chromatography-Mass Spectrometry (GC/MS) Analysis…... 137
6.3 RESULTS AND DISCUSSION………... 138
6.3.1 Surface Analysis of Ti/TiO2-nanotubes/PbO2………... 138
6.3.2 Electrochemical Measurements………. 139
6.3.3 Colour Removal and COD Decay……….. 140
6.3.4 Energy Consumption Estimation………... 143
6.3.5 Final by-Products Identification……… 143
6.4 CONCLUSIONS………... 144
CAPÍTULO 7 CONSIDERAÇÕES FINAIS………... 150
CAPÍTULO 8 PRODUÇÃO CIENTÍFICA………... 153
CAPÍTULO 1
1 INTRODUÇÃO
A água é um bem precioso e insubstituível. Além de ser um elemento vital para
a existência da própria vida na Terra, a água é um recurso natural que pode propiciar
saúde, conforto, riqueza ao homem, etc. Não sendo utópico sem ela toda a vida acabaria
pois ela exerce grande importância para a manutenção da vida de todas as espécies do
planeta. Exemplo disso, 80% do nosso organismo é composto por água. Muitas pessoas,
sabendo da maior parte da composição do nosso planeta, afirmam categoricamente que
ele não deveria se chamar “Terra”, e sim “Água”, uma vez que cerca de 70% de sua
superfície é composta por essa substância. Cerca de 97,5% da água disponível no
mundo está nos oceanos e apenas 2,5% é água doce. A Figura 1.1 apresenta o panorama
geral da distribuição de água no planeta.
Figura 1.1 Distribuição da água no planeta.
Fonte: Revista Galileu, 2014.
Apesar da proporção reduzida de água potável disponível, ainda assim o volume
de água é muito grande. No entanto, o seu mau uso vem reduzindo drasticamente a
qualidade desse recurso natural e, consequentemente, sua disponibilidade. O lançamento
de efluentes industriais (óleo, corantes, etc), agrícolas (pesticidas e fertilizantes
químicos), de lixo e de esgoto doméstico são os principais responsáveis pela poluição
das águas. Poluição é uma alteração ecológica provocada pelo ser humano, que
prejudique, direta ou indiretamente, a vida ou o bem-estar, como danos aos recursos
naturais como a água e o solo e impedimentos a atividades econômicas como a pesca e a
de matéria orgânica, o que levam ao aumento da quantidade de nutrientes disponíveis
nos cursos hídricos, fenômeno denominado eutrofização. A eutrofização é um processo
normalmente de origem antrópica (provocado pelo homem), ou raramente de ordem
natural, tendo como princípio básico a gradativa concentração de matéria orgânica
acumulada nos ambientes aquáticos. Durante esse processo, a quantidade excessiva de
minerais (fosfato e nitrato) induz a multiplicação de micro-organismos (algas) que
habitam a superfície da água, formando uma camada densa, impedindo a penetração da
luminosidade. Esse fato implica na redução da taxa fotossintética nas camadas
inferiores, ocasionando o déficit de oxigênio suficiente para atender a demanda
respiratória dos organismos aeróbios (peixes e mamíferos aquáticos), que em virtude
das condições de baixo suprimento, não conseguem sobreviver, aumentando ainda mais
o teor de matéria orgânica no meio.
Em consequência, o número de agentes decompositores também se eleva
(bactérias anaeróbias facultativas), atuando na degradação da matéria morta, liberando
toxinas que agravam ainda mais a situação dos ambientes afetados, comprometendo
toda a cadeia alimentar, além de alterar a qualidade da água, também imprópria ao
consumo humano.
Diante do grande problema relacionado à poluição e consequentemente escassez
da água no planeta, as entidades governamentais em todo o mundo têm despertado seus
interesses em discutir essa questão através de conferências e fóruns criando protocolos e
legislações com o objetivo de minimizar os efeitos causados pela intervenção antrópica
no meio ambiente. É exatamente neste momento que pesquisadores veêm a
oportunidade de aliar seus conhecimentos científicos aos grandes desafios oriundos dos
mais diversos problemas ambientais que o homem tem causado ao longo do tempo.
Com isso a necessidade de se desenvolver tecnologias cada vez mais limpas, torna-se
desenfreado o trabalho desta parcela tão importante da sociedade. Apesar dos
governantes de alguns países não considerarem primordiais, pesquisadores e empresas
preocupados com a sustentabilidade buscam dia a dia alternativas que visam contribuir
para conservação do nosso bem comum, o meio ambiente que desejamos para as
gerações futuras.
Indubitavelmente, de todas as crises sociais e naturais que os seres humanos
devem enfrentar, a dos recursos hídricos é a que mais afeta a nossa sobrevivência. Essa
que a mesma possa ser reutilizada. Atualmente, diversas metodologias têm sido
utilizadas para este fim. Entretanto, o surgimento de novas técnicas torna-se um desafio
tendo em vista o aumento da necessidade de se tratar efluentes cada vez mais diversos e
que atendam aos limites estabelecidos pelas legislações ambientais no Brasil e no
mundo.
Com isso, as tecnologias eletroquímicas têm alcançado um destaque onde não
apenas são comparáveis com outras tecnologias em termos de custo, mas são, também,
mais eficientes e compactas. Para algumas situações, as tecnologias eletroquímicas
podem ser a etapa indispensável para tratar efluentes que contenham poluentes
resistentes (CHEN, 2004).
Dentro da temática relatada nesta introdução, o Capítulo 2 apresenta os aspectos
teóricos que permeiam, isto é, fundamentam esta Tese. Assuntos como contaminação,
remediação, tipos de tratamento e uma ênfase às tecnologias eletroquímicas
(mecanismos, tipos de eletrodos, reações, etc.) foram abordados.
Um dos métodos mais populares de tratamento de efluentes e desinfecção de
água utilizados no mundo é a eletrocloração. Baseado nisto, investigou-se a produção de
espécies de cloro ativo, assim como, espécies reativas de oxigênio com aplicação ao
tratamento de um efluente real, aqui denominado de efluente ETE-UFRN. Os resultados
dessa investigação estão apresentados no Capítulo 3 e teve como objetivo estudar o
papel da relação de cloreto na reação de desprendimento de oxigênio utilizando os
ânodos de Ti/Pt e DDB. Estes resultados foram escritos na forma de artigo e publicado
no Journal Electroanalytical Chemistry.
A fim de se verificar quais espécies são formadas no processo de Oxidação
Indireta (neste caso, mediada por cloreto) e suas respectivas concentrações, decidiu-se
estudar a influência da adição de uma pequena concentração de NaCl frente ao eletrodo
Ti/Ru0.3Ti0.7O2 classificado como ADE (Capítulo 4). A escolha deste eletrodo pode ser
justificada pelas suas características: apresentam elevada estabilidade, alta produção de
espécies oxidantes levando a eficiências de corrente de 81% a 93%. O tratamento do
efluente ETE-UFRN foi realizado via essas espécies de cloro ativo eletrogeradas onde
obtivemos valores consideráveis de remoção de matéria orgânica com publicação no
Journal of Water Process Engineering.
Já o Capítulo 5, que gerou o terceiro artigo desta Tese, também já se encontra
preparação de um novo eletrodo. Isto foi possível graças a uma experiência realizada na
Universidad de Las Américas Puebla (UDLAP), México, sob a orientação do Prof Dr.
Marco Antonio Quiroz. A caracterização deste eletrodo (Ti/TiO2-nanotubos/PbO2)
apontam-o como um material promissor para a degradação de orgânicos. Com isso,
decidiu-se trabalhar com um efluente contendo o corante têxtil Azul Ácido 113,
sintetizado em laboratório.
A degradação do corante através do eletrodo Ti/TiO2-nanotubos/PbO2
apresentou ótimas eficiências e a partir daí decidiu-se comparar com outros tipos de
materias anódicos, como Ti/Pt e Pb/PbO2, assim como Al/Al através do método de
eletrocoagulação (Capítulo 6). Também escrito na forma de artigo, pretende-se
submeter ao Environmental Nanotechnology, Monitoring and Management.
A pesquisa objetivou também estimar o consumo de energia elétrica e calcular o
custo do tratamento por litro de efluente tratado visando sua utilização em amostras
CAPÍTULO 2
2 ASPECTOS TEÓRICOS
2.1 PROBLEMA AMBIENTAL
As preocupações com a temática dos recursos hídricos que permeia um dos
maiores problemas ambientais no mundo atual tem se potencializado e despertado o
interesse da comunidade científica levando ao desenvolvimento de inúmeras pesquisas,
sobretudo para o desenvolvimento de técnicas adequadas visando o enquadramento às
legislações vigentes que se apresentam cada vez mais rigorosas, devido a pressão da
sociedade por políticas ambientais responsáveis.
Até o fim do século passado, a água era tida como um recurso praticamente
inesgotável, infelizmente esta ideia se tornou equivocada, pois constantes variações
geoclimáticas vêm alterando a disponibilidade de água potável, sendo essas mudanças
decorrentes do trabalho humano (desmatamento, emprego indiscriminado de defensivos
agrícolas, assoreamento de rios e nascentes, impermeabilização dos solos, poluição da
atmosfera, ocupação de mananciais, etc) (PEREIRA e FREIRE, 2005).
O avanço industrial e o aparecimento de novas tecnologias evidenciados nos
últimos anos fizeram com que o homem começasse a se preocupar com esses problemas
ambientais. Não só o crescimento tecnológico deve ser compatível com a preservação
ambiental como também o surgimento de novas técnicas de tratamento de efluentes se
fazem necessárias, com a finalidade de unir baixos custos à eficiência da preservação
ambiental e da saúde pública.
O impacto do custo financeiro cada vez mais alto tem levado a maioria das
empresas à conclusão de que é vantajoso tomar a iniciativa de gerenciar e tratar
adequadamente os seus resíduos. As políticas industriais de minimização da geração de
resíduos, por sua vez, têm levado à produção de efluentes com novas características.
Várias tecnologias foram desenvolvidas para o tratamento de efluentes industriais. A
seleção da tecnologia depende das características do efluente e da qualidade que se
deseja para o produto final, além de custo e facilidade de operação do processo.
Portanto, um dos maiores desafios da indústria no novo milênio é conviver
pacificamente com o meio ambiente em tempos de escassez de recursos hídricos. A
geração de uma enorme quantidade de efluentes industriais, acompanhada da
tem obrigado a indústria a adotar novas políticas ambientais (AL-READHWAN et al.
2005).
2.2 LEGISLAÇÃO AMBIENTAL
A legislação ambiental brasileira constituída pela Lei 6.938/1981, e Resolução
001/1986 do Conselho Nacional do Meio ambiente (CONAMA) conceituou as águas
interiores, as superficiais e as subterrâneas como um recurso ambiental, e a degradação
da qualidade ambiental, por sua vez, como qualquer alteração adversa desse recurso
(BRASIL, 1981; 1986).
No Brasil não há leis ou resoluções que determinem a prática de reúso na
indústria, contudo, existe a obrigatoriedade de tratamento antes do descarte, prevista na
Resolução 430/2011 do CONAMA – Conselho Nacional do Meio Ambiente, que
estabelece os parâmetros de qualidade para lançamento do efluente em corpos
receptores além de complementar a Resolução do CONAMA 357/2005. Ela determina
que efluentes de qualquer fonte poluidora somente poderão ser lançados diretamente
nos corpos receptores após o devido tratamento e desde que obedeçam às condições,
padrões e exigências dispostos nesta Resolução e em outras normas aplicáveis. Seu
artigo 27 dispõe que as fontes potencial ou efetivamente poluidoras dos recursos
hídricos deverão buscar práticas de gestão de efluentes com vistas ao uso eficiente da
água, à aplicação de técnicas para redução da geração e melhoria da qualidade de
efluentes gerados e, sempre que possível e adequado, proceder à reutilização (BRASIL,
2011).
2.3 CONTAMINAÇÃO DA INDÚSTRIA TÊXTIL
A indústria têxtil tem causado uma enorme preocupação em estudiosos. Forgacs
et al. 2004 afirmam que a utilização de corantes sintéticos têm se tornado um dos
problemas ambientais mais relevantes devido ao seu uso extensivo em muitos campos
da tecnologia até os dias atuais, bem como em vários ramos da indústria têxtil, como
por exemplo na produção de papel, na indústria alimentícia, no curtimento de couro, na
pesquisa agropecuária, em células foto-eletroquímicas e também em tingimento de
cabelos. Devido sua produção ser feita em grande escala e aplicação extensiva, os
fatores que põem em risco a saúde humana. Se não forem tratados adequadamente antes
de lançados nos corpos receptores, os efluentes provenientes da indústria de corantes ou
de processos envolvendo tintura têxtil podem alterar o ecossistema e por em risco a
saúde da população.
O efluente descartado sem tratamento adequado afeta diretamente o meio
ambiente causando danos, que em alguns casos são irreparáveis. Isso se dá pelo fato de
que alguns corantes e seus intermediários apresentam alta aromaticidade e são de baixa
biodegradabilidade (ARSLAN et al. 2000 e SAUER et al. 2002) e ainda, por serem
coloridos, alteram a qualidade da água, provocando a redução da penetração da luz e,
consequentemente, interferindo no processo de fotossíntese, afetando, então, a
oxigenação dos corpos aquáticos e, com isso, os seres vivos de tal habitat e os que deles
se alimentam (NEAMTU et al. 2002). Além disso, certas classes de corantes, assim
como seus subprodutos, podem ser carcinogênicos e/ou mutagênicos. Estudos indicam
que a poluição colorida de cursos d’água começa a ser observável a concentrações a partir de 1 mg L-1 (CATANHO et al. 2006).
Em razão disso, vários estudos têm buscado encontrar formas de solucionar essa
problemática de contaminação por parte da indústria têxtil. Dentre as várias
metodologias utilizadas para tratar efluentes têxteis pode-se citar, adsorção em carvão
ativado, biodegradação utilizando micro-organismos, métodos físico-químicos (como
precipitação, juntamente com adição de agentes complexantes), ou seja, métodos
tradicionais de tratamento de efluentes industriais e, a oxidação eletroquímica. Nesse
sentido, técnicas eletroquímicas têm sido propostas para o tratamento de efluentes
diversos. Nesses processos, compostos aromáticos podem ser convertidos em produtos
biodegradáveis ou, eventualmente, em CO2 e H2O onde são denominados de combustão
eletroquímica (COMNINELLIS, 1994).
2.4 CORANTES TÊXTEIS E SUA CLASSIFICAÇÃO
A remoção ou a descoloração de corantes de águas residuárias constitui-se em
uma grande preocupação da indústria têxtil, antes do descarte, devido à rigorosa
legislação vigente (PASCHOAL e TREMILIOSI-FILHO, 2005). Em geral, a maior
preocupação com relação aos efluentes têxteis está associada à ampla utilização de
corantes sintéticos da família dos azocorantes, os quais possuem caráter carcinogênico e
O uso de corantes vem desde a antiguidade, quando os pigmentos eram extraídos
das plantas. São definidos como substâncias orgânicas utilizadas para colorir
parcialmente fibras têxteis, couros, papéis, etc e podem ser classificados de acordo com
a estrutura química do seu grupo cromóforo (responsável pela cor que absorve a luz
solar) ou de acordo com o grupo funcional (que permite a fixação nas fibras do tecido).
Existem vários tipos de grupos cromóforos, tais como antraquinona, nitro e azo. No
entanto, o grupo mais largamente usado pertence à família dos azocorantes (60 %) que
são formados, principalmente, por dois ou mais grupamentos azo (-N=N-) ligados a
anéis aromáticos. A Figura 2.1 apresenta a estrutura de um corante do tipo azo. Eles
constituem cerca de 70% de todos os corantes sintéticos (KUSIC et al. 2007) devido à
facilidade de obtenção e à variedade de produtos que através deles (tipo azo) podem ser
obtidos.
Figura 2.1 - Estrutura química de um azo corante.
Fonte: Autor, 2014.
Alguns dos principais grupos de corantes, de acordo com o modo de fixação, são
apresentados a seguir (ALCÂNTARA e DALTIN, 1996):
a) Corantes Ácidos: são aqueles onde o grupo cromóforo é um ânion (normalmente
sulfonatos orgânicos do tipo RSO2O-). Estes substituintes tornam o corante solúvel em
água e têm grande importância no método de aplicação do corante em fibras protéicas
b) Corantes Básicos: são aqueles onde o grupo cromóforo é um cátion (normalmente um
sal de amina ou um grupo imino ionizado); ligações iônicas são formadas entre o cátion
da molécula do corante, e os sítios aniônicos na fibra. São usados para colorir também
lã e seda, embora tenham moderada aderência a esses materiais.
c) Corantes Diretos: são solúveis em água e possuem alta afinidade com algodão e
outras fibras de celulose. São aplicados diretamente de um banho neutro contendo NaCl
ou Na2SO4.
d) Corantes Dispersos: insolúveis em água e são aplicados em fibras de celulose e em
outras fibras hidrofóbicas através de suspensão. Durante o processo de tintura, o corante
sofre hidrólise e a forma insolúvel é lentamente precipitada na forma dispersa
(finamente divida) sobre acetato de celulose, nylon, poliéster e poliacrinonitrila.
e) Corantes Reativos: são corantes contendo um grupo eletrofílico (reativo) capaz de
formar ligação covalente com grupos hidroxila das fibras celulósicas, com grupos
amino, hidroxila e tióis das fibras protéicas e também com grupos amino das
poliamidas. Existem numerosos tipos de corantes reativos, porém os principais contêm a
função azo e antraquinona como grupos cromóforos e os grupos clorotriazinila e
sulfatoetilsulfonila como grupos reativos. Neste tipo de corante, a reação química se
processa diretamente através da substituição do grupo nucleofílico pelo grupo hidroxila
da celulose.
f) Corantes Azóicos: são compostos coloridos, insolúveis em água, que são sintetizados
sobre a fibra durante o processo de tingimento. Nesse processo a fibra é impregnada
com um composto solúvel em água, conhecido como agente de acoplamento (naftol)
que apresenta alta afinidade por celulose. A adição de um sal de diazônio (RN2+)
provoca uma reação com o agente de acoplamento já fixado na fibra e produz um
corante insolúvel em água. O fato de usar um sistema de produção do corante
diretamente sobre a fibra, através da combinação de um corante precursor sem grupos
sulfônicos e a formação de um composto solúvel, permite um método de tingimento de
fibras celulósicas (especificamente alongadas) com alto padrão de fixação e alta
g) Corantes de Enxofre: É uma classe de corantes que após a aplicação se caracterizam
por compostos macromoleculares com pontes de polissulfetos (-Sn-), os quais são
altamente insolúveis em água. Em princípio são aplicados após pré-redução em banho
de ditionito de sódio que lhes confere a forma solúvel, são reoxidados
subsequentemente sobre a fibra pelo contato com ar. Estes compostos têm sido
utilizados principalmente na tintura de fibras celulósicas, conferindo cores preto, verde
oliva, azul marinho, marrom, apresentando boa fixação. Entretanto, estes corantes
usualmente apresentam resíduos altamente tóxicos.
h) Corantes Branqueadores: são substâncias que quando aplicadas em tecidos brancos
proporcionam alta reflexão de luz, inclusive de comprimento de onda não visíveis que
são transformados em visíveis por excitação e retorno de elétrons aos níveis normais.
Estes corantes apresentam grupos carboxílicos, azometino N=CH-) ou etilênicos
(-CH=CH-) aliados a sistemas benzênicos, naftalênicos, pirênicos e anéis aromáticos.
A geração de uma enorme quantidade de efluentes industriais, acompanhada da
conscientização das conseqüências do descarte destes efluentes nos recursos naturais,
tem obrigado a indústria a adotar novas políticas ambientais (AL-READHWAN et al.
2005). Dependendo das substâncias que são utilizadas, diferentes tecnologias e
processos são aplicados em vários setores industriais. Com isso, conviver pacificamente
com o meio ambiente em tempos de escassez de recursos hídricos tem se tornado um
dos maiores desafios da indústria no novo milênio.
2.5 TRATAMENTOS DE EFLUENTES
As atividades humanas do dia-a-dia bem como as decorrentes da revolução
industrial têm influenciado o fluxo e armazenamento de água e a qualidade da água
doce disponível.
O estudo de tratamento de efluentes, sejam domésticos ou industriais, tem
ganhado bastante força nos últimos anos e um dos principais fatores que mais
impulsionam este tipo de estudo reside na escassez crescente de água potável existente
no globo terrestre bem como a alta estabilidade dos poluentes orgânicos que são
extremamente resistentes à luz e a agentes oxidantes moderados. Estes fatores têm
poluentes, cada vez mais rigorosos e o desenvolvimento de tecnologias adequadas para
o tratamento de efluentes.
A Figura 2.2 apresenta alguns dos processos utilizados assim como os métodos
eletroquímicos que têm sido considerados como uma alternativa inovadora por se tratar
de tecnologias que oferecem prevenção ou remediação ambiental.
Figura 2.2 - Exemplos de métodos de tratamento de efluentes.
Fonte: Adaptado de SANTOS et al, 2014.
A oxidação biológica é, certamente, o processo mais econômico, porém uma de
suas desvantagens é por requerer uma grande área para construção de tanques de
armazenamento de efluentes onde o volume a ser tratado permanece dias até completar
o tratamento através das bactérias facultativas que são as responsáveis pela degradação
da matéria orgânica. Os Métodos físico-químicos (filtração, coagulação, adsorção e
floculação), a oxidação química (uso de cloro, ozônio, peróxido de hidrogênio, a
oxidação do ar úmido) e os processos oxidativos avançados, mais comumente
conhecidos como POAs (reação de Fenton, ozônio + radiação UV, fotoquímica) são
Por causa das características extremamente diversas desses efluentes, que
normalmente contém uma mistura de compostos orgânicos e inorgânicos, nenhuma
estratégia universal de recuperação é viável. Por isso, aremoção de poluentes orgânicos
constitui um dos maiores objetivos do tratamento de efluentes. Entretanto, devido a sua
diversidade, não existe uma fórmula pronta e/ou adequada para utilização em qualquer
situação. Para atingir o objetivo, existem vários processos de tratamento, baseados em
fenômenos ou princípios físicos, químicos ou biológicos, ou ainda, em suas
combinações.
2.5.1 Tratamento Biológico
Processos biológicos são aqueles que dependem da ação de microrganismos
presentes nos efluentes. Geralmente constitue a alternativa mais econômica quando
comparado com outros processos químicos e físicos (SESHADRI et al. 1994 e
FORGACS et al. 2004 ). Alguns métodos de biodegradação são freqüentemente
aplicados para tratamento de efluentes, pois muitos microrganismos como bactérias,
algas e fungos são capazes de acumular e degradar diferentes poluentes. Entretanto, suas
aplicações são geralmente restritas. O tratamento biológico requer uma grande extensão
de área e é limitado pela sensibilidade das variações climáticas, bem como pela
toxicidade de alguns produtos químicos. Uma vantagem do tratamento biológico sobre
outros métodos de tratamentos físicos e químicos é que grande parte do material
orgânico presente, que é medido por testes de Demanda Química de Oxigênio (DQO),
pode ser convertido em material sólido (CRINI, 2005).
2.5.2 Tratamento Físico-químico
Os processos físicos são caracterizados por operações que removem substâncias
fisicamente separáveis dos líquidos ou que não se encontram em dissolução. Exemplos de
processos físicos: remoção de sólidos grosseiros; remoção de sólidos decantáveis; remoção
de sólidos flutuantes; remoção da umidade do lodo; filtração dos efluentes; incineração do
lodo; diluição dos efluentes; homogeneização dos efluentes e floculação.
Diferentes métodos físicos são também amplamente usados para a remoção de
cor, tais como processos de filtração com membrana (MO et al. 2008) (nanofiltração,
osmose reversa, eletrodiálise), troca iônica e técnicas de adsorção por carvão ativado,
inconveniência do processo de membrana é o custo de instalação do processo e o custo
de reposição periódica da membrana, inviabilizando economicamente muitas vezes sua
utilização.
De acordo com informações na literatura, adsorção em fase líquida é um dos
métodos mais populares e eficientes para remoção de poluentes de efluentes. O processo
de adsorção sólido-líquido explora a habilidade que certos sólidos têm de concentrar na
sua superfície substâncias específicas presentes em soluções aquosas. Dessa forma, os
componentes das soluções aquosas podem ser separados.
2.5.3 Tratamento Químico
Os processos químicos, como seu próprio nome já diz, são processos nos quais
ocorre adição de produtos químicos. São utilizados de forma auxiliar aos processos
físicos e biológicos, ou até mesmo complementando-os. Alguns métodos químicos de
tratamento de efluentes incluem coagulação ou floculação (GOLOB et al. 2005),
combinados com flotação e filtração, ozonização (OGUZ et al. 2005; JÓZWIAK et al.
2007), processos eletroquímicos (CRINI, 2005), oxidação química, cloração,
neutralização ou correção do pH e métodos de oxidações convencionais por agentes
oxidantes (JÓZWIAK et al. 2007). O processo químico de oxidação para remoção de
orgânicos é freqüentemente o mais usado devido ao seu manejo simples. Pode-se citar
como exemplo o efluente da indústria têxtil onde são constituídos de corantes sintéticos
que são resistentes a condições moderadas de oxidação, como ocorre em sistemas de
tratamento biológico. Então, uma remoção de cor adequada deve ser realizada por
agentes oxidantes mais poderosos, como por exemplo (OGUZ et al. 2005; JÓZWIAK
2007), ozônio ou até mesmo pelo processo de decomposição oxidativa utilizando
processo Fenton (JÓZWIAK et al. 2007).
O tratamento eletroquímico de efluentes coloridos é considerado um processo
moderno e um método poderoso de controle de poluição, oferecendo boa eficiência de
remoção. Em alguns casos, este processo não requer nenhum tipo de produto químico
adicional. Os equipamentos necessários e a operação são geralmente simples. Porém,
são processos que podem promover a formação de subprodutos indesejáveis que podem
ser mais nocivos do que as espécies iniciais do processo (GUARATINI e ZANONI
Outra metodologia bastante conhecida são os Processos Oxidativos Avançados
(POAs) que despertam grande interesse para o tratamento de efluentes, águas
superficiais e subterrâneas contaminadas. Os resultados de trabalhos experimentais com
diferentes substratos e amostras de águas contaminadas foram tão interessantes que
parcerias foram estabelecidas com indústrias em projetos de ampliação de escala.
Porém, para o desenvolvimento de tais técnicas, é muito importante a escolha do
processo, a construção e modelo da unidade fotoquímica, bem como a sua otimização
(BRAUN e OLIVEROS, 1997).
Apesar dos POA serem constituídos por diferentes sistemas reativos, todos têm a
mesma característica química: a produção de radicais hidroxilas (•OH) por um oxidante,
com exceção da fotólise da água com radiação Ultravioleta (UV) (BRAUN e
OLIVEROS, 1997). Os radicais •OH são espécies extraordinariamente reativas que
atacam a maioria das moléculas orgânicas com constantes de reação, usualmente, da
ordem de 106-109 m-1s-1. Estes processos também são caracterizados pela baixa
seletividade do ataque, o que é uma característica muito importante para um oxidante
utilizado no tratamento de efluentes. A versatilidade dos POAs é realçada pelo fato de
existirem diversas possibilidades para a produção dos radicais hidroxilas, o que permite
a escolha do método mais adequado de acordo com o tratamento necessário
(ANDREOZZI et al. 1999).
No entanto, todos estes métodos apresentam alguns inconvenientes importantes,
isto é, desvantagens. Por exemplo, filtração e adsorção nem sempre são suficientes para
atingir os limites de descarga (BOUSHER et al. 1997); coagulação e flotação geram
uma grande quantidade de sedimentos; oxidações químicas têm baixas taxas de
capacidade e precisam de transporte e armazenamento de reagentes perigosos; e os
POAs exigem elevados custos de investimento.
Como os regulamentos ambientais se tornam cada vez mais rigorosos são
necessários novos e promissores processos para o tratamento eficiente de vários tipos de
águas residuais com custos de operação relativamente baixos. Neste contexto, os
pesquisadores estão tentando vários processos alternativos, como a técnica
eletroquímica, oxidação úmida, ozonização, método fotocatalítico para a degradação de
compostos orgânicos.
As políticas industriais de minimização da geração de resíduos, por sua vez, têm
desenvolvidas para o tratamento de efluentes industriais. A seleção da tecnologia
depende das características do efluente e da qualidade que se deseja para o produto
final, além de custo e facilidade de operação do processo.
2.6 ESTAÇÕES DE TRATAMENTO DE EFLUENTES (ETE)
As estações de tratamento de efluentes (ETE) em geral são constituídas de
diversas unidades, usualmente na forma de tanques, cada qual desempenhando
isoladamente uma ou mais funções específicas. Entretanto, cada unidade é operada de
maneira integrada com as demais, formando um sistema de tratamento para atingir o
objetivo comum que é a remoção de determinados constituintes do esgoto,
principalmente para a recuperação da água. A Figura 2.3 mostra esquematicamente a
composição de uma estação de tratamento completa convencional, até a desinfecção
final.
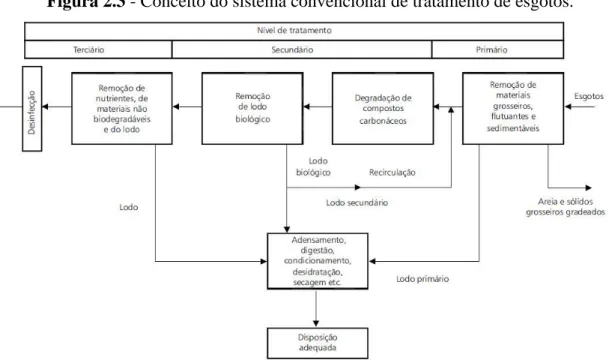
Figura 2.3 - Conceito do sistema convencional de tratamento de esgotos.
O tratamento de efluentes é usualmente classificado de acordo com os seguintes
níveis: preliminar; primário; secundário e terciário. O tratamento preliminar objetiva
apenas a remoção dos sólidos grosseiros, enquanto o tratamento primário visa a
remoção de sólidos sedimentáveis e parte da matéria orgânica. Em ambos predominam
os mecanismos físicos de remoção de poluentes. Já no tratamento secundário, no qual
orgânica e eventualmente predominantes, nitrogênio e fósforo. O tratamento terciário
objetiva a remoção de poluentes específicos (usualmente tóxicos ou compostos não
biodegradáveis) ou ainda, a remoção complementar de poluentes não suficientemente
removidos no tratamento secundário. O tratamento terciário é bastante raro no Brasil.
O grau de remoção, desempenho ou eficiência de uma ETE é avaliado
comparando-se essas quantidades ou concentrações presentes no afluente e efluente.
Além do efluente líquido tratado, com qualidade compatível com o seu lançamento em
corpos receptores ou possível reuso, são gerados ainda no processo de tratamento,
subprodutos sólidos ou gasosos, os quais podem necessitar de posteriores tratamentos
específicos. Por isso, a busca de técnicas que minimizem essa geração torna-se um dos
principais atrativos existentes, quando de novas técnicas a serem empregadas.
2.6.1 ETE - UFRN
A estação de tratamento de esgoto da UFRN tem como objetivo destinar
adequadamente os efluentes sanitários gerados no Campus Central, eliminando os
sistemas de fossas sépticas e sumidouros que contaminam o solo e o lençol freático que
abastece o Campus.
O sistema de esgotamento sanitário do Campus Central é composto por
aproximadamente 7,0 km de rede coletora, Estação de Tratamento de Esgotos (ETE) e
reuso do efluente tratado. O projeto da ETE foi elaborado no final da década de 70,
iniciando sua operação em 1981.
Diariamente cerca de 400.000 litros de efluentes chegam às instalações da
ETE. O tratamento é realizado em valo de oxidação com decantação secundária. A
escolha por essa concepção de tratamento baseou-se nas seguintes vantagens: pequena
área para implantação, custo inferior aos sistemas convencionais, elevada eficiência na
remoção de DBO e sólidos em suspensão, lodo mineralizado que dispensa a digestão
anaeróbica, fácil operação e manutenção e dispensa decantação primária. O efluente
tratado é utilizado na irrigação das áreas verdes da ETE e dos campos de futebol do
Campus Central.
Tratamento Preliminar: Visa à remoção de sólidos grosseiros e de areia que podem
danificar os conjuntos motor-bomba, bem como controlar a vazão afluente. Nessa etapa,
o efluente bruto percorre seguidamente as seguintes unidades:
Grade: espaçamento de 2,5 cm e inclinação de 45º em relação a horizontal;
Caixas de Areia: retenção de partículas de areia com dimensões igual ou
superior a 0,2 mm;
Calha Parshal: dispositivo de medição de vazão na forma de um canal aberto
com dimensões padronizadas. Outra finalidade da calha é controlar o nível de água na
caixa de areia e na grade.
Tratamento Secundário: Visa à remoção da matéria orgânica e dos sólidos em
suspensão. É composto pelas seguintes unidades:
Valo de Oxidação: nesta unidade ocorre a oxidação biológica da matéria
orgânica, isto é, a conversão da matéria orgânica em matéria inorgânica por bactérias
aeróbicas. Para tanto, dois aeradores mecânicos, como mostra a Figura 2.4, insuflam
oxigênio na massa líquida.
Figura 2.4 - Valo de oxidação da ETE-UFRN.
Fonte: Portal de Meio Ambiente da UFRN.
Decantador Secundário: após sair do valo de oxidação, o esgoto segue para o
gravidade (Figura 2.5). Esses sólidos formam o lodo que será recirculado em parte para
que seja mantida uma concentração de 4000 mg/L de sólidos em suspensão no valo de
oxidação, sendo o excesso encaminhado para o leito de secagem.
Figura 2.5 - Tanque decantador da ETE-UFRN.
Fonte: Portal de Meio Ambiente da UFRN.
Leito de secagem: recebe o lodo do decantador quando não é necessária sua
recirculação para o valo de oxidação. O lodo é disposto em células formadas por
camadas de tijolo branco, brita e areia por onde a parte líquida percola. O resíduo (lodo)
fica submetido a incidência solar. Após seco é raspado e encaminhado ao aterro
sanitário.
Tratamento Terciário: Destina-se a remoção de patógenos. A desinfecção, com cloro
gasoso, do efluente tratado é feita em um tanque com chicanas horizontais, forçando o
efluente a percorrer todo esse trajeto em cerca de 30 minutos, promovendo um maior
contato e, consequentemente maior ação do agente desinfectante.
Todo o efluente tratado é armazenado em um tanque de onde é bombeado para a
2.7 TECNOLOGIAS ELETROQUÍMICAS
O uso da eletricidade para tratamento de água foi sugerido, pela primeira vez,
em 1889 na Inglaterra. Os processos de tratamento eletroquímico de efluentes
promovem a remoção ou a destruição de espécies poluentes, direta ou indiretamente,
por meio de reações de oxidação e/ou redução em células eletroquímicas, sem a adição
de grandes quantidades de produtos químicos.
Nesse sentido, as tecnologias eletroquímicas têm sido propostas para o
tratamento de diversos efluentes por oferecerem uma solução alternativa, como por
exemplo, controle e/ou remediação ambiental por meio de reações redox, seja através
das reações diretas entre as espécies poluentes e as superfícies dos eletrodos ou do
sinergismo desses processos com o poder de espécies oxidantes geradas in situ
(ROCHA et al. 2009). Configuram-se como técnicas bastante versáteis, em que o único
reagente envolvido é o elétron, que é um regente limpo e, portanto, não são necessários
reagentes extras, reduzindo assim, a possibilidade de volatilização e descarga de
resíduos não tratados. São técnicas facilmente automatizáveis que permitem trabalhar à
temperatura ambiente e pressão atmosférica, e a otimização do processo se dá, por
exemplo, através do controle da intensidade de corrente e da diferença de potencial
entre os eletrodos, variáveis que são facilmente mensuráveis e atuantes. Além dos
parâmetros de operação, a taxa de degradação do poluente depende do material do
ânodo. Em geral, podemos citar algumas vantagens dos tratamentos eletroquímicos de
efluentes:
Versátil: são aplicáveis a uma grande variedade de meios, concentrados ou
diluídos, e poluentes, biológicos ou não, encontrados em gases, líquidos e
sólidos. Além disso, os tratamentos eletroquímicos podem ser adaptados a
diferentes projetos, visando a otimização do espaço físico disponível para as
instalações de tratamento, permitindo o tratamento de pequenas quantidades
(microlitros) até grandes volumes (milhões de litros).
Boa eficiência energética: operam em temperaturas inferiores aos seus
equivalentes não eletroquímicos, como a incineração térmica. Os eletrodos e as
da queda ôhmica, da distribuição irregular de corrente e da presença de reações
paralelas.
Fácil automação: as variáveis inerentes aos processos eletroquímicos, como a
diferença de potencial entre eletrodos, a distância entre eles e a corrente aplicada
à célula são facilmente operáveis. Além disso, o parâmetro densidade de
corrente limite pode ser encontrado permitindo a otimização do processo,
evitando assim desperdício energético.
Custo/benefício: essa relação é atingida quando a construção de células e
reatores eletroquímicos são projetados com materiais eficientes e ao mesmo
tempo de baixo custo.
Compatibilidade ambiental: reagentes livres de produtos químicos.
Há algumas décadas, um grande número de empresas tem comercializado
dispositivos eletroquímicos para a remoção de íons metálicos, recuperação de metais,
tratamento de efluentes contendo cromo dissolvido, dessulfurização de gases de
combustão e dessalinização. No entanto, até agora, o papel das tecnologias
eletroquímicas para o tratamento de poluentes orgânicos em grande escala tem sido
relativamente pequeno. Mas hoje em dia, graças a investigações intensivas visando
otimizar a atividade eletrocatalítica como a estabilidade dos materiais eletródicos
(metais, óxidos metálicos, polímeros, carbono, etc.) e a geometria do reator, as
tecnologias eletroquímicas chegaram a um estado promissor de desenvolvimento e
podem ser efetivamente utilizadas para a desinfecção e purificação de águas residuais
poluídas com compostos orgânicos (MARTÍNEZ-HUITLE e FERRO, 2006;
MARTÍNEZ-HUITLE e BRILLAS, 2008 e 2009; CHEN, 2004; PANIZZA e
CERISOLA, 2009; BRILLAS et al. 2009; COMNINELLIS e CHEN, 2010; SIRÉS et
al. 2014 ).
O uso das tecnologias eletroquímicas objetiva a conversão dos poluentes
orgânicos, entre eles os compostos aromáticos, em produtos biodegradáveis ou, até, em
CO2 e H2O, processo denominado de combustão eletroquímica (COMNINELLIS,
1994). Além dos parâmetros de operação já citados, a taxa de degradação do poluente
depende do material do ânodo. Neste quadro, a oxidação eletroquímica dos substratos
modelo tem sido investigado em vários materiais anódicos, geralmente óxidos de metal,