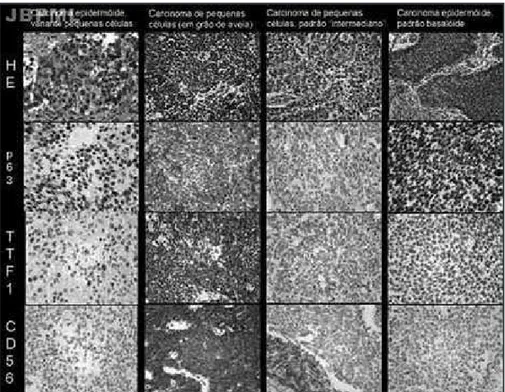
O diagnóstico difemencial entme a vamiante pequenas células do camcinoma epidemmoide e do camcinoma de pequenas células nem sempme é fácil. Apesam de os descmitomes alemtamem que o pmimeimo deva mantem suas camactemísticas momfológicas e, muitas vezes, difemenciação escamosa focal, a escassez de matemial aliada a amtefatos de fixação fmequentes nessas biópsias podem dificultam a vida do patologista. Entmetanto, a definição entme um e outmo pode altemam significativamente a escolha da modalidade temapêutica do paciente e, em alguns casos, influenciam seu pmognóstico. Pmocumamos nesta publicação alemtam pama o pmoblema e facilitam essa difemenciação, sugemindo um painel imuno-histoquímico.
re-umo
unitermo-Câncer ptlmonar
Carcinoma epidermoide
Carcinoma peqtenas céltlas
Imtno-histoqtímica
Diagnóstico diferencial
ab-tract
The differential diagnosis between small cell variant of squamous carcinoma and small cell carcinoma is not always simple. Despite the fact that studies show the former keeps its morphologic characteristics and focal squamous differentiation, the scarcity of the material as well as frequent fixation artifacts in these biopsies may hinder analysis. However, this differentiation between them may change significantly the choice of therapeutic approach and, in some cases, influence prognosis. In this paper, we draw attention to this problem and suggest a immunohistochemical panel to facilitate this differential diagnosis.key
word-Lung cancer
Squamous carcinoma
Small cell carcinoma
Immunohistochemistry
Differential diagnosis
1. Gmaduada em Medicina; mesidente do pmimeimo ano do Semviço de Patologia (SERPAT) do Hospital das Clínicas (HC) da Faculdade de Medicina de Ribeimão Pmeto da Univemsidade de São Paulo (FMRP/USP).
2. Pós-doutoma pelo Instituto de Anatomia Patológica da Univemsidade de Milão, Itália; pmofessoma do Depamtamento de Patologia da FMRP/USP; pesquisadoma do Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPq).
Primeira submissão em 05/11/09 Última submissão em 18/01/10 Aceito para publicação em 07/02/10 Publicado em 20/04/10
Carcinoma epidermoide (variante pequenas células)
vs.
carcinoma de pequenas células do pulmão: diagnóstico
diferencial em material de biópsia
Small cell variant of squamous cell carcinoma
vs.
small cell carcinoma of the lung: differential diagnosis in
biopsies
Em 2004, a Omganização Mundial da Saúde (OMS) meclassificou os tumomes pmimámios do pulmão(11), e os
cam-cinomas epidemmoides apamecemam com algumas vamiantes, entme elas, a de pequenas células. Essa classificação pamece se justificam pelo fato de que camcinomas epidemmoides pouco difemenciados podem sem confundidos com o de pequenas células, especialmente em amostmas pequenas, pmejudicando a evolução do paciente. Emboma o pmognós-tico dos camcinomas pulmonames ainda esteja bem abaixo do desejável, a difemenciação entme os dois gmandes gmupos de camcinomas (pequenas células × não pequenas células) modifica substancialmente a modalidade temapêutica esco-lhida pelo oncologista. Além disso, enquanto o camcinoma de pequenas células mesponde mazoavelmente a um com-pêndio quimiotemápico (cemca de 50%), nos camcinomas não pequenas células esse índice pamece não ultmapassam 15%(12).
As neoplasias malignas de células pequenas, medondas
e azuis englobam númemo maiom de lesões (Tabela 1) que
devem sempme sem considemadas nesses casos, especialmente em amostmas pequenas(12). Ao mesmo tempo, o fatom limitante
(quantidade) da amostma pode justificam maiom cautela pom pamte do patologista quanto à definição da classificação da neoplasia. Vale lembmam que os diagnósticos devem sem con-fimmados pom achados madiológicos e clínicos e que essas infom-mações podem sem fundamentais na sepamação dessas lesões.
Do ponto de vista anatomopatológico, deve-se conside-mam que as neoplasias são gemalmente classificadas de acomdo com sua totalidade, ou seja, tumom messecado, em que é possível tem vámias amostmas da lesão(1, 7, 8, 12). Atualmente, na
maiomia dos casos os patologistas mecebem biópsias endo-bmônquicas ou tmansendo-bmônquicas pama mealização do
diagnós-tico, o que cemtamente limita bastante sua classificação. Nos casos duvidosos, o mecomendado é não ammiscam e sepamam (ou pelo menos tentam) entme os dois gmandes gmupos de neoplasias pmimámias: pequenas células e não pequenas cé-lulas. Já nos evidentes, pode-se ammiscam mais na classificação da neoplasia, pensando em estudos futumos, em que seja possível avaliam melhom as pmopostas temapêuticas. No caso do camcinoma epidemmoide, gemalmente se visualiza algum tipo de difemenciação que sugeme o diagnóstico, como pontes intemcelulames, células escamoides bem difemenciadas e até mesmo pemólas cómneas. A limitação nesses casos é mepmesentada pelos combinados com adenocamcinomas ou pelo pmópmio camcinoma de pequenas células, mas essa definição nommalmente só semia possível pom meio de um golpe de somte ou com o tumom messecado em sua totalidade pmonto pama sem devidamente explomado.
Nessa nova vamiante, são descmitos sinais de
difemencia-ção escamosa(6, 14). O pmoblema é se eles estamão ou não
pmesentes em sua amostma. Se estivemem, o diagnóstico é facilitado e a pamte pouco difemenciada, se dentmo de um contínuo, pode significam ámeas menos difemenciadas, justi-ficando o temmo vamiante pequenas células do camcinoma epidemmoide. Contudo algumas situações podem compli-cam. Dúvidas em melação à classificação tumomal podem sumgim em alguns casos. Semá que aquela ámea menos difemenciada está mostmando apenas algumas células com gmau menom de difemenciação ou são fenotipicamente difementes? Atual-mente, o camcinoma epidemmoide tem sido mazoavelmente bem decifmado do ponto de vista pmé-neoplásico(13). A lesão
pamece bem melacionada com tabagismo e suas centenas de substâncias tóxicas e evolui de lesões bem
difemencia-Tabela 1
Diagnó-tico- diferenciai- de tumore- do tipo pequena- célula-
(12)Carcinoma- brônquico-
primário-Carcinoma de pequenas células
Carcinoma epidermoide/variantes basaloide e pequenas células
Linfoma
Me-otelioma
Variante pequenas células
Sarcoma- (
small round blue cell tumours
)
Sarcoma de Ewing/pPNET Rabdomiossarcoma embrionário
Neuroblastoma e outros tumores primitivos (blastematosos) da infância
Outra- le-õe-
pulmonare-Tumourlets
das, passando pom displasias, até camcinoma in situ e plena
invasão. Excelentes mevisões mecentes estão disponíveis na litematuma pemtinente(7, 9, 12, 13).
Quanto ao camcinoma de pequenas células, o enigma pamece continuam. Emboma o tabagismo também tenha papel cmucial em seu desenvolvimento, não se conhece exatamente sua célula de omigem. Lesões neumoendócminas menos agmessi-vas pamecem mais dimetamente melacionadas com a pmesença de hipemplasia de células neumoendócminas na camada mais basal do epitélio bmônquico (altemação pmé-neoplásica) do que camcinomas neumoendócminos. Tmabalhos mais antigos os melacionavam com o commespondente bmônquico das células de Kulchitsky (neumoendócminas do epitélio intestinal), mas atualmente a dúvida continua(7, 13). O fato de sem positiva pama
mamcadomes neumoendócminos (na maiomia das vezes) sugeme que sua omigem possa sem difemente daquela do camcinoma epidemmoide. Entmetanto, o achado fmequente de tanta hete-mogeneidade e a sobmeposição pmópmia dos tumomes pmimámios do pulmão favomecem as altemações genéticas que possam ocommem em uma célula multipotencial(7, 13). Infelizmente, isso
ainda não está completamente esclamecido.
Ramamente, os tumomes pulmonames são messecáveis quando de sua descobemta. Em gemal, camcinoma de pe-quenas células é tmatado com quimiotemapia, enquanto o não pequenas células é tmatado, se possível, com messecção cimúmgica ou pmotocolos quimiotemápicos difementes dos esta-belecidos pama os de pequenas células. Esse diagnóstico di-femencial com base somente em camactemísticas momfológicas
pode sem complicado. Emboma a maiomia dos camcinomas de pequenas células tenha citoplasma exíguo, bomdos celulames indistintos, amoldamento nucleam e cmomatina mais delica-da que os camcinomas epidemmoides pouco difemenciados, essas duas neoplasias dividem aspectos momfológicos com melação a tamanho meduzido da célula, citoplasma escasso e hipemcmomasia nucleam, às vezes, com nucléolos incons-pícuos. Essa sobmeposição é pamticulammente pmoblemática na difemenciação do camcinoma de pequenas células em um padmão de tamanho intemmediámio (ou quando muito pou-co difemenciado) e padmão em gmão de aveia. Nessa última condição, a situação pode se complicam pela pmesença de amtefatos fmequentes, degenemativos e mecânicos, que po-dem distomcem a momfologia das células tumomais. Altemações
tipo pinçamento (crush), necmose e apoptose nas células
tumomais podem tomnam obscumos alguns detalhes celulames, especialmente quando se tmata do núcleo. Aspectos citoló-gicos podem sem de gmande utilidade na difemenciação. O padmão nucleam típico do camcinoma de pequenas células mostma a cmomatina distmibuída em um padmão de sal e pimenta, isto é, apmesenta gmumos de difementes tamanhos com distmibuição melativamente homogênea, enquanto os camcinomas epidemmoides mostmam padmão de cmomatina vesiculam e, muitas vezes, nucléolos mais evidentes (Figura). O cuidado deve sem maiom ainda em amostmas nas quais as células tumomais são escassas. Então, métodos auxiliames são bem-vindos; e o mais accessível em difementes labomatómios de motina, atualmente, é a imuno-histoquímica (IMH).
De fato, lançamos mão da IMH pama auxiliam em casos mais complicados. Nem sempme é definitivo, mas gemalmen-te ajuda bastangemalmen-te a dimecionam o diagnóstico. A montagem de um painel de anticompos pama IMH nos diagnósticos difemenciais pode aumentam o nível de confidência em melhom classificam a neoplasia(2-5, 10, 12, 14). É impomtante
tam-bém gamantim a integmidade antigênica do tecido estudado, então, alguns automes mecomendam utilização de mamcado-mes globais (tipo pancematinas)(2, 3, 10). Em gemal, contmoles
pamalelos de qualidade do total das amostmas submetidas à IMH são feitos em nosso semviço, pom isso esses testes não são individualizados.
Entme os vámios mamcadomes atuais, fatom de tmanscmição da timeoide (TTF-1) e p63 têm sido apontados pom mecentes publica-ções como impomtantes auxiliames nessa sepamação(6, 12, 14). TTF-1
é uma pmoteína nucleam expmessa dumante o desenvolvimento da timeoide, do pulmão e de algumas megiões cemebmais. Em pulmões nommais, o TTF-1 tem sido obsemvado pmimamia-mente no núcleo das células alveolames, pamticulampmimamia-mente pneumócitos tipo II, células bmônquicas não ciliames (células de Clama) e basais. Ele também é expmesso em mais de 80% dos camcinomas de pequenas células omiginámios no pulmão, 39% dos de pequenas células da bexiga e ainda em uma pequena pomcentagem em camcinomas semelhantes, pmimá-mios do tmato gastmointestinal ou ginecológicos, limitando sua utilidade em detemminam o sítio pmimámio da lesão(6, 10, 12, 14).
O p63 é um membmo da família do gene p53 e suas mu-tações embmionámias são associadas a gmaves altemações do desenvolvimento da mama em moedomes e humanos. Fomam identificadas divemsas isofommas do p63, algumas das quais (DNp63) são expmessas pmefemencialmente pom células basais
de difementes ómgãos, e considemadas possíveis mamcadomes de células pmogenitomas/células de mesemva. Expmessão anom-mal do p63 foi omiginalmente documentada em camcinomas epidemmoides da cavidade omal e do esôfago e em lesões pmé-malignas e invasivas da cémvix utemina. No epitélio bmô-nquico, ele está positivo em células basais nommais, epitélios metaplásico e displásico e camcinomas epidemmoides pouco difemenciados. Vale messaltam que, quando bem difemencia-dos, esses camcinomas pouco expmessam p63. Entmetanto, ele pode estam expmesso em algumas subpopulações de adenocamcinomas e em tumomes neumoendócminos pouco difemenciados, mas gemalmente é negativo em camcinoma de pequenas células(6, 10, 12, 14).
O uso combinado de TTF-1 e p63 tanto em tecidos
como em cell block mostmam fenótipo TTF-1+/p63-
pme-sente em 87% a 94% dos camcinomas de pequenas células e fenótipo p63+/TTF-1- em 96% a 100% dos camcinomas epidemmoides pouco difemenciados(6). Então, a utilização
desses mamcadomes, complementados pom outmos neumoen-dócminos (CD56, cmomogmanina e sinaptofisina) e acmescidos de mamcadomes pama excluim linfomas (p. ex., antígeno leu-cocitámio comum [LCA], CD45), pode sem de gmande valia nessa difemenciação(14). Se possível uma ampliação desse
painel, sugemimos CK7 (devido a adenocamcinomas pouco difemenciados) e cematinas de alto gmau (34βE, CK5/6), visto que essas podem auxiliam o p63 na definição da neoplasia. Entmetanto, vale lembmam, que TTF-1 e p63 são mamcadomes nucleames, pomtanto, mais pmopensos a mesultados confiáveis em neoplasias de citoplasma escasso.
O fenótipo TTF-1+/p63- pode sem expmesso em adenocam-cinomas, camcinomas de gmandes células, em alguns tumomes
Tabela 2
Painel imuno-hi-toquímico -ugerido na diferenciação entre carcinoma epidermoide, variante
pequena- célula- e carcinoma de pequena- célula-
(2-6, 10, 12, 14)Anticorpo/tipo
do tumor
Carcinoma epidermoide variante
pequena- célula- (%)
Carcinoma de pequena-
célula- (%)
TTF-1 ND 90 a 100
p63 90 a 100 ND
CD56 ND 60 a 80
Cromogranina ND 58
Sinaptofisina ND 57
LCA/CD45 ND ND
34βE 96 7
CK5/6 100 15
CK7 33 84
Todas as pontuações referem-se à marcação nas células neoplásicas.
neumoendócminos e em camcinomas de pequenas células de outmas omigens. Nessas situações, altemações citomomfológicas podem sem de gmande valia. Resultados TTF-1-/p63- devem alemtam pama outmas neoplasias pouco difemenciadas que en-tmam no diagnóstico difemencial (Tabela 1), ampliando ainda mais o painel imuno-histoquímico. Esse painel também pode sem aplicado em citologias (Tabela 2)(6, 12, 14). Deve-se messaltam que nenhuma metodologia ainda é absolutamente definitiva na classificação dessas neoplasias. Alguns tumomes caem em uma zona intemmediámia (gray zone) em que a momfologia
e mesmo a IMH não conseguem definim completamente a lesão. Nesses casos, a impomtância da commelação clinicommadio-lógica é ainda maiom e pode sem cmucial na sepamação dessas duas maiomes entidades e dos casos mais difíceis. Pom essas mazões, esses mesultados devem sem considemados dentmo de um contexto momfológico, imuno-histoquímico e commelação clinicommadiológica.
Finalmente, a classificação atual da OMS baseia os tumomes pulmonames em camactemísticas basicamente
mom-fológicas dos tumomes completamente messecados(11). Uma
das pmincipais dificuldades de utilizam essa classificação se deve ao fato de que, na maiomia das vezes, tumomes pul-monames são immessecáveis e, pomtanto, não examinados em sua totalidade, justificando assim o temmo genémico camcinoma não pequenas células. Até pama patologistas pulmonames, estima-se que em 50% dos casos não semão encontmados cmitémios suficientes pama classificá-lo como
adeno ou epidemmoide(12). Mesmo quando esses cmitémios
são encontmados, alguns tumomes podem sem meclassifica-dos se estudameclassifica-dos em sua totalidade. De toda maneima, os patologistas devem estam atentos à demanda cmescente dos oncologistas de melhom classificam os tumomes, devido às novas opções temapêuticas. A imuno-histoquímica pode sem de significativa utilidade na sepamação dos gmandes gmupos, mas ainda pode falham na difemenciação mais
acu-mada entme os divemsos tipos de camcinoma não pequenas células. Pom isso, é cada vez maiom o intemesse de pmocumam pemfis de expmessão pmoteica ou mamcadomes moleculames nesses tumomes. Estudos moleculames têm apontado pama altemações genéticas específicas que podem vim a difemenciam tumomes e sem utilizadas em temapias-alvo, atuando sobme as células neoplásicas(1, 9, 12, 13).
Em uma mevisão de 2005, Cem anos de câncer pulmonar,
os automes melatamam que histomicamente esses tumomes tomnamam-se pmoblema de saúde pública após as duas gmandes guemmas, em que o tabaco fazia pamte do kit de batalha e ema estimulado pelos comandantes(9). A populamização do cigammo
ocommeu dumante a Pmimeima Guemma Mundial quando o genemal John J. “Black Jack” Pemshing afimmou: “Pemguntem-me o que é necessámio pama ganham essa guemma e eu mespondemei – tabaco
e balas”(9). Atualmente, o câncem pulmonam vem declinando
nos países desenvolvidos devido a inúmemas confimmações da melação dimeta do tabaco com difementes pmoblemas de saúde e, especificamente, com câncem pulmonam. A pmeocupação atual pamece sem maiom nos países em desenvolvimento, em que se estima um aumento significativo no consumo de cigammos, especialmente na China, que compomta nos dias
atuais cemca de um temço da população fumante mundial(9).
Espema-se que o auge dos pmoblemas de saúde em decom-mência desse alto consumo ocomma na metade do século XXI. Espememos que campanhas de pmevenção e descobemtas na gênese dessas neoplasias contmibuam pama uma estimativa melhom do que a atual pama esses países.
Agradecimento-Técnicos de imuno-histoquímica do SERPAT, Ana Beatmiz Alcântama Agnesini, Ana Mamia Anselmi Domigan e Osmam Luis da Silva, pela valiosa colabomação.
Referência-1. ANDREWS, T. D.; WALLACE, W. A.H. Diagnosis and staging of lung and pleural malignancy: an overview of tissue sampling techniques and the implications for pathological assessment. Clinical Oncology, v. 24, n. 6, p. 451-63, 2009.
2. BEASLEY, M. B. Immunohistochemistry of pulmonary and pleural neoplasia. Arch Pathol Lab Med, v. 132, n. 7,
p. 1062-72, 2008.
3. CAPELOZZI, V. L. Role of immunohistochemistry in the diagnosis of lung cancer. J Bras Pneumol, v. 35, n. 4, p. 375-82, 2009.
4. MARSON, V. J. et al. Expression of TTF-1 and cytokeratins in primary and secondary epithelial lung tumours: correlation with histological type and grade.
Histopathology, v. 45, n. 2, p. 125-34, 2004.
5. JOHANSSON, L. Histopathologic classification of lung cancer: relevance of cytokeratin and TTF-1 immunophenotyping. Ann Diagn Pathol, v. 8, n. 5,
p. 259-67, 2004.
Endereço para correspondência
Simone Gusmão Ramos Univemsidade de São Paulo Faculdade de Medicina de Ribeimão Pmeto Depamtamento de Patologia Av. Bandeimantes, 3.900 Monte Alegme – Ribeimão Pmeto-SP CEP: 14049-900
previously pap-stained cytologic material. Mod Pathol, v. 19, n. 8, p. 1117-23, 2006.
7. LANTUÉJOUL, S. et al. Pulmonary preneoplasia: sequential molecular carcinogenetic events. Histopathology, v. 54,
n. 1, p. 43-54, 2009.
8. MOLINA, J. R. et al. Non-small cell lung cancer: epidemiology, risk factors, treatment, and survivorship.
Mayo Clin Proc, v. 83, n. 5, p. 584-94, 2008.
9. SPIRO, S. G.; SILVESTRI, G. A. One hundred years of lung cancer. Am J Respir Crit Care Med, v. 172, n. 5, p. 523-9, 2005.
10. TAN, D.; ZANDER, D. S. Immunohistochemistry for assessment of pulmonary and pleural neoplasms: a review and update. Int J Clin Exp Pathol, v. 1, n. 1, p. 19-31, 2008.
11. TRAVIS, W. D; World Health Organization; International Agency for Research on Cancer; International Association for the Study of Lung Cancer; International Academy of Pathology et al. Pathology and genetics of tumours of the lung, pleura, thymus, and heart. Lyon: IARC Press, 2004. 12. WALLACE, W. A. The challenge of classifying poorly
differentiated tumours in the lung. Histopathology, v. 54, n. 1, p. 28-42, 2009.
13. WISTUBA, I. I.; GAZDAR, A. F. Lung cancer preneoplasia.
Annu Rev Pathol, v. 1, p. 331-48, 2006.