www.jped.com.br
ARTIGO
ORIGINAL
Serum
phenylalanine
in
preterm
newborns
fed
different
diets
of
human
milk
夽
,
夽夽
Débora
M.
Thomaz
a,
Paula
O.
Serafin
a,
Durval
B.
Palhares
a,b,
Luciana
V.M.
Tavares
a,ce
Thayana
R.S.
Grance
a,∗aUniversidadeFederaldeMatoGrossodoSul(UFMS),CampoGrande,MS,Brasil
bCaseWesternReserveUniversity---RBCH,Cleveland,EstadosUnidos
cUniversidadeCatólicaDomBosco(UCDB),CampoGrande,MS,Brasil
Recebidoem20dejunhode2013;aceitoem10defevereirode2014
KEYWORDS
Serumphenylalanine; Humanmilk;
Humanmilkfortifier; Bankedhumanmilk; Pretermnewborns
Abstract
Objective: Toevaluatephenylalanineplasmaprofileinpretermnewbornsfeddifferenthuman milkdiets.
Methods: Twenty-fourvery-lowweightpretermnewbornsweredistributedrandomlyinthree groupswithdifferentfeedingtypes:GroupI:bankedhumanmilkplus5%commercialfortifier withbovineprotein,GroupII:bankedhumanmilkplusevaporatedfortifierderivedfrom modi-fiedhumanmilk,GroupIII:bankedhumanmilkpluslyophilizedfortifierderivedfrommodified humanmilk.Thenewbornsreceivedthegroupdietwhenfulldietwasattainedat15±2days. Plasmaaminoacidanalysiswas performedonthefirst andlastday offeeding. Comparison amonggroupswasperformedbystatisticaltests:onewayANOVAwithTukey’spost-testusing SPSSsoftware,version20.0(IBMCorp,NY,USA),consideringasignificancelevelof5%. Results: Phenylalaninelevelsinthefirstandsecondanalysis were,respectively,inGroup I: 11.9±1.22and29.72±0.73;inGroupII:11.72±1.04and13.44±0.61;andinGroupIII:11.3
±1.18and15.42±0.83mol/L.
Conclusion: Theobservedresultsdemonstratedthathumanmilkwithfortifiers derivedfrom humanmilkactedasagoodsubstratumforpreterminfantfeedingbothintheevaporatedor thelyophilizedform,withoutsignificantincreasesinplasmaphenylalaninelevelsincomparison tohumanmilkwithcommercialfortifier.
©2014SociedadeBrasileiradePediatria.PublishedbyElsevierEditoraLtda.Allrightsreserved.
DOIserefereaoartigo:http://dx.doi.org/10.1016/j.jped.2014.02.003
夽 Comocitaresteartigo:ThomazDM,SerafinPO,PalharesDB,TavaresLV,GranceTR.Serum phenylalanineinpretermnewbornsfed
differentdietsofhumanmilk.JPediatr(RioJ).2014;90:518---22.
夽夽EstudoconduzidonaUniversidadeFederaldeMatoGrossodoSul(UFMS),CampoGrande,MS,Brasil.
∗Autorparacorrespondência.
E-mail:thayanagrance@yahoo.com(T.R.S.Grance).
PALAVRAS-CHAVE Fenilalanina plasmática; Leitehumano; Aditivoparaleite humano;
Leitehumano debanco; Recém-nascido pré-termo
Fenilalaninaplasmáticaemrecém-nascidospré-termoalimentadoscomdiferentes dietasdeleitehumano
Resumo
Objetivo: Avaliaroperfilplasmáticodoaminoácidofenilalaninaemrecém-nascidospré-termo alimentadoscomdiferentesdietasdeleitehumano.
Métodos: Foramestudados24recém-nascidospré-termodemuitobaixopeso,distribuídosem trêsgruposcomdiferentesdietas:GrupoI:leitehumanodebancocom5%deaditivocomercial paraleitehumanocomproteínadeorigembovina(LHB-AC);GrupoII:leitehumanodebanco comaditivodeleitehumanomodificadoevaporado(LHB-E);eGrupoIII:leitehumanodebanco comaditivodeleite humanomodificadoliofilizado(LHB-L). Osrecém-nascidosreceberam a dietadefinidaparaogrupoquandoalcanc¸aramdietaplenapor15±2dias.Aanálisedo ami-noácidoplasmáticofoifeitanoprimeiroeúltimodiasdadieta.Acomparac¸ãoentreosgruposfoi realizadapormeiodotesteANOVAdeumavia,seguidopelopós-testedeTukey,utilizando-seo softwareSPSS(IBMCorp,NY,EUA),versão20.0,econsiderandoumníveldesignificânciade5%. Resultados: Asconcentrac¸õesplasmáticasdoaminoácidofenilalaninanaprimeira esegunda análisesforam, respectivamente,noGrupo I(LHB-AC)11,9±1,22e29,72±0,73;noGrupoII (LHB-E)11,72±1,04e13,44±0,61;enoGrupoIII11,3±1,18e15,42±0,83umol/L.
Conclusão: Osresultadosencontradosdemonstramqueoleitehumanocomaditivosdopróprio leite humano comportou-se como um bom substrato para alimentac¸ão do recém-nascido pré-termo, tanto naformaevaporada como liofilizada, semlevara aumentossignificativos na concentrac¸ão plasmática de fenilalanina em comparac¸ão ao leite humano com aditivo comercial.
©2014SociedadeBrasileiradePediatria.PublicadoporElsevierEditoraLtda.Todososdireitos reservados.
Introduc
¸ão
A superioridade do leite humano (LH) na alimentac¸ão de recém-nascidos pré-termo (RNPT) já está bem documen-tada.OLHtemimpactoimportantenocrescimentocerebral enodesenvolvimento,mesmoquandonãopromovegrande ganhodepeso,reforc¸andooconceitodequeoótimo cres-cimentopós-nataldeRNPTaindanãoéconhecido.1---5
Quanto ao aporte de proteínas, não só a quantidade, mastambémaqualidadeéimportanteparaocrescimento adequado. A composic¸ão de aminoácidos das fórmulas e aditivosdeleitehumanocomproteínabovinatemsua quali-dadecomprometidaemrelac¸ãoàdoLH,consideradapadrão ouro.6---9
Afrac¸ãoproteicadoleitedevacatempredominânciade caseína,quepossuialtoteordoaminoácidofenilalanina.10 Embora seja um aminoácido essencial, em crianc¸as rece-bendo proteína de leite bovino, o nível plasmático desse aminoácido é elevado (próximo àqueles associados com defeitosdometabolismo).11---13
Com oaumentodaingestãoedaconcentrac¸ão plasmá-ticadefenilalaninaocorreainibic¸ãodaenzimatirosinase, econversão,pelahidroxilac¸ão,dafenilalaninaemtirosina, aumentando a disponibilidade de tirosina. Este aumento pode ocasionar um efeito deletério no desenvolvimento cerebral, levando a consequências como distúrbio do sono, déficit de memória, dificuldade de atenc¸ão e de concentrac¸ão.14---17
Enquantonãosesabeoqueéótimoemnutric¸ãodeRNPT, osneonatologistasdevemestarcompromissadoscomoque pareceserideal,quenãocausealterac¸õesemcurtoprazo equetragamelhordesenvolvimentoemlongoprazo.Neste contexto,suplementaroLHcomaditivocontendoproteína
homólogaàdoLHpareceumaalternativaapropriadapara oaporteproteico,mantendoumaconcentrac¸ãoplasmática seguradefenilalanina.18---20
Considerandoestahipótese,pretendeu-seanalisar com-parativamente a concentrac¸ão plasmática de fenilalanina em RNPT alimentados com leite humano de banco (LHB) acrescido de aditivo comercial FM85® (Fortified Milk 85,
Nestlé, São Paulo, Brasil), e em RNPT alimentados com LHBacrescidocomumaditivooriundodopróprioLH,com retiradadegorduraelactosenasformasevaporadaou lio-filizada.
Métodos
Após a aprovac¸ão do Comitê de Ética em Pesquisas (Res. 17/2006) da Universidade Federal do Mato Grosso do Sul (UFMS),foirealizado,noperíodode2008a2010,umensaio clínicorandomizado,nãocego,nosetordeneonatologiado NúcleodoHospitalUniversitário(NHU)daUFMS (Universi-dade Federal de Mato Grossodo Sul,Campo Grande, MS, Brasil).
Asdietasoferecidasacadagrupoforam:
Grupo I: RNPT alimentados com leite humano de banco deleite,acrescidocom5%doaditivoFM85® (Nestlé,São
Paulo,Brasil),determinadopelasigla:LHB-AC;
GrupoII:RNPTalimentadoscomleitehumanodebancode leitesuplementadocomleitehumanomodificado:100ml deLHdesnatado,evaporadoa20%,comextrac¸ãode lac-tose,adicionadoem80mldeleitehumanoepasteurizado, determinadopelasigla:LHB-E;
Grupo III: RNPTalimentadoscomleite humanodebanco de leite, suplementado com leite humano modificado: 70ml de LHdesnatado, evaporado a 20%, com extrac¸ão delactose, liofilizado,reconstituídoem100mldeLHB e pasteurizado,determinadopelasigla:LHB-L.
Osaditivosdeoriginadosdeleitehumano foram elabo-radosconformeametodologiadescritaporThomazetal.21 Dos24RNPT,dezpertenciamaoGI,cincoaoGIIenove ao GIII. Estes foram alimentados, nesta ordem, em dife-rentesmomentos. Emboraa selec¸ãonãotenha sido cega, foramselecionadostodososRNPTinternadosnoNHU-UFMS noperíododoestudo,equeseadequavamaoscritériosde inclusão.
ForamincluídososRNPTcomidadegestacionalinferior a34semanas,compesodenascimentoigualouinferiora 1.500kg,adequadosounãoparaaidadegestacional, está-veisclinicamenteesemqualquer malformac¸ãocongênita, cujospais,apósseremesclarecidosdanaturezadoestudo, assinaram o termo de consentimento informado, livre e esclarecido.
ForamexcluídosRNPTcommáformac¸ãocongênita, dis-túrbiosmetabólicos,anemia,qualquerdoenc¸aematividade (distúrbiosrespiratórios,manifestac¸õesdosistemanervoso centralegastrointestinal),hemorragiaperiventricular,grau maiorouiguala2eaquelescujasmãestinhamleite sufici-enteparaalimentarseusfilhos.
Durante o estudo foram substituídos os RNPT que apresentaram condic¸ões clínicas desfavoráveis ao desen-volvimentodapesquisa.Estas condic¸õesestavam,em sua totalidade,relacionadascompioradoníveldeinfecc¸ão.
OsRNPT receberam a dieta específicado grupo a que iriam pertencer somente quando atingiram a dieta ente-ral plena (100ml/kg) e com boa tolerância; portanto, os prematurosfizeram parte dos grupos assim que iniciaram aalimentac¸ãoplenaporsondagástrica.
Os RNPT foram acompanhados desde que iniciaram a alimentac¸ãodosleitesmodificadospor15±2dias.
Foi feita a análise não cega do aminoácido fenilala-nina plasmático. Para isso foi colhida uma amostra de sangue venoso pré-prandial (2h30min à 3h após a última mamada)porpunc¸ãopercutâneacomseringacontendotrês gotas de heparina (efeito anticoagulante), acondicionada emtubodemicrocentrífuga(EppendorfdoBrasilLtda,São Paulo, Brasil), sendo o plasma devidamente separado por centrifugac¸ão(2.500rotac¸õesporminutodurante10min), identificadoecongeladoa-20◦Cparaposterioranálisede aminoácidos,porCromatografiaLíquidadeAltaEficiência. Acoletadosangue foirealizada emcada crianc¸adostrês gruposparaacomparac¸ãodoperfildoaminoácidono pri-meirodia,antesdeacrianc¸ainiciaradieta específicado grupoenoúltimodiarecebendoestadieta.
Aavaliac¸ãodaassociac¸ãoentreasdietasofertadasaos RNPTcomasvariáveissexo,classificac¸ãopeso/idade gesta-cional,SDRfoirealizadapormeiodotestedoQui-quadrado. Jáaassociac¸ãoentreasdietasofertadaseasvariáveisidade gestacional, peso ao nascimento, início da alimentac¸ão, volume, calorias, início da nutric¸ão enteral mínima, dias deventilac¸ãomecânicaeconcentrac¸ãoplasmáticade feni-lalanina foi realizada por meio do teste ANOVA de uma via, seguido pelo pós-teste de Tukey. Os resultados das demais variáveis avaliadasneste estudo foram apresenta-dosnaformadeestatísticadescritivaounaformadetabela egráfico.Aanáliseestatísticafoirealizadautilizando-seo software SPSS, versão 20.0 (IBM Corp,NY, USA), conside-randoumníveldesignificânciade5%.
Resultados
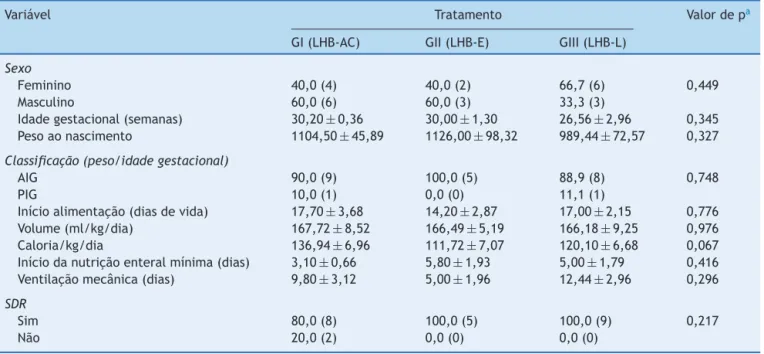
As características dos três grupos quanto ao sexo, idade gestacional, peso ao nascer, adequac¸ão do peso para a idade gestacional, início da alimentac¸ão enteralmínima, início da alimentac¸ão enteral plena, uso de ventilac¸ão mecânica,SíndromedoDesconfortoRespiratório,volumee caloria média diária de dieta recebida estão expostas na
tabela1.
Quantoaestascaracterísticas,osgruposnão apresenta-ramdiferenc¸asestatisticamentesignificantes(tabela1).
Osníveisplasmáticosdoaminoácidofenilalanina(média + EPM) na primeira e segundaanálises foram, respectiva-mente, no grupo I (LHB-AC) 11,9±1,22 e 29,72±0,73; no grupo II (LHB-E) 11,72±1,04 e 13,44±0,61; e no grupo III 11,3±1,18e15,42±0,83umol/L.Osresultadosreferentesà concentrac¸ãodoaminoácidoessencialfenilalaninadogrupo I,IIeIIIestãoilustradosnafigura1.
Nãohouve diferenc¸a entreos tratamentos em relac¸ão àconcentrac¸ãoplasmáticadefenilalaninanoprimeirodia da alimentac¸ão enteral plena (teste ANOVA de uma via, p = 0,931). Por outro lado, os tratamentos foram dife-rentes entre si no momento 15 dias após o início da alimentac¸ão (teste ANOVA de umavia, p < 0,001), sendo
Concentração plasmática de
fenilalanina (
μ
mol/L)
35
30
25
20
15
10
5
0
1 15
Momento (dias)
LHB-AC LHB-E LHB-L
Tabela1 Resultadosreferentesàsvariáveisavaliadasnesteestudo,deacordocomaalimentac¸ãoofertadaaosrecém-nascidos pré-termo
Variável Tratamento Valordepa
GI(LHB-AC) GII(LHB-E) GIII(LHB-L)
Sexo
Feminino 40,0(4) 40,0(2) 66,7(6) 0,449
Masculino 60,0(6) 60,0(3) 33,3(3)
Idadegestacional(semanas) 30,20±0,36 30,00±1,30 26,56±2,96 0,345 Pesoaonascimento 1104,50±45,89 1126,00±98,32 989,44±72,57 0,327
Classificac¸ão(peso/idadegestacional)
AIG 90,0(9) 100,0(5) 88,9(8) 0,748
PIG 10,0(1) 0,0(0) 11,1(1)
Inícioalimentac¸ão(diasdevida) 17,70±3,68 14,20±2,87 17,00±2,15 0,776 Volume(ml/kg/dia) 167,72±8,52 166,49±5,19 166,18±9,25 0,976 Caloria/kg/dia 136,94±6,96 111,72±7,07 120,10±6,68 0,067 Iníciodanutric¸ãoenteralmínima(dias) 3,10±0,66 5,80±1,93 5,00±1,79 0,416 Ventilac¸ãomecânica(dias) 9,80±3,12 5,00±1,96 12,44±2,96 0,296
SDR
Sim 80,0(8) 100,0(5) 100,0(9) 0,217
Não 20,0(2) 0,0(0) 0,0(0)
Osresultadosestãoapresentadosemmédia±erro-padrãodamédiaouemfrequênciarelativa(frequênciaabsoluta).SDR,síndromedo desconfortorespiratório;AIG,Adequadoparaaidadegestacional;PIG,Pequenoparaaidadegestacional.
a ValordepnotesteANOVAdeumavia(idadegestacional,pesoaonascimento,iníciodaalimentac¸ão,volume,calorias,inícioda
nutric¸ãoenteralmínimaeventilac¸ãomecânica)ounotestedoQui-quadrado(sexo,classificac¸ãopeso/idadegestacional,SDR).
queaconcentrac¸ãoplasmáticadefenilalaninanogrupode RNPTLHB-ACfoimaiordoqueaquelaparaosgruposLHB-Ee LHB-L(pós-testedeTukey,p<0,05),porém,semdiferenc¸a significativaentreosdoisúltimosgrupos(0>0,05).
Discussão
Este estudosugere que,paraanálise doperfilde aminoá-cidos,asamostrasdesanguedevemsercolhidas imediata-menteantesdaalimentac¸ão,poisassimépossívelanalisar o perfildeaminoácidos commenor interferênciadadieta ofertada.Estaevidênciajustificaaescolhadefazeracoleta desanguepré-prandialparaaanálisedeaminoácidos.22
Ao comparar a concentrac¸ão do aminoácido fenilala-ninaentreosRNPTalimentadoscomasdiferentesdietas, verificou-sequeaquelesalimentadoscomaditivocomercial tiveramíndicesplasmáticosmaioresdesteaminoácido,com diferenc¸a extremamente significativa em relac¸ão àqueles alimentadoscomosaditivosevaporadoeliofilizado.
Considerandoqueosgruposeramsemelhantesquantoàs característicasexpostasnatabela1eosíndicesplasmáticos defenilalaninaeramsemelhantesnostrêsgruposnoinício doestudo,estadiferenc¸ana concentrac¸ãodefenilalanina aofinaldomesmopareceestarrelacionadaàqualidadeda proteínadoaditivoutilizadonaalimentac¸ãodecadagrupo eàmenorcapacidadededegradac¸ãodesteaminoácidopelo RNPT,emrelac¸ãoaorecém-nascidoatermo.Adiferenc¸anão deveestarrelacionadaàquantidadetotaldeproteína con-sumida,porqueoteormédiodeproteínadadietadogrupo LHB-AC(1,96±0,01g/dL)éintermediárioaosdasdietasdos gruposLHB-E(1,81±0,01g/dL),LHB-L(2,38±0,03g/dL).21
Embora o valor calóricodoLHB-AC 81,65±0,87kcal/dL seja maior que o do LHB-E 67,78±2,01 e do LHB-L
72,27±2,56kcal/dL, um estudo clínico ainda não publi-cadoobservouqueo ganhodepeso edecomprimentofoi semelhante nos três grupos, com vantagem no aumento do perímetro cefálico no grupo LHB-L em relac¸ão aos outrosgrupos.21 Estas características de crescimento evi-denciamumbom aproveitamentodas proteínas ofertadas pelosaditivoshomólogosemcomparac¸ãoaoaditivo comer-cialcomumenteutilizado.
Estudos que avaliaram o perfil de aminoácidos sanguí-neodeRNPTalimentados comLHacrescidocom oaditivo comercialFM85®observaramquehánecessidadedemelhor
adequac¸ão da proteína ofertada por este suplemento. Oaditivo de origemheteróloga resultou em modificac¸ões dosmacronutrientesbioquímicospodendointerferirno neu-rodesenvolvimentodascrianc¸as.23,24
Em análise de fenilalanina plasmática em grupos de recém-nascidosatermosaudáveisaosseismesesdeidade alimentadoscomleitematerno,fórmularegular,doistipos defórmulas com caseína hidrolisadae fórmulas com pro-teínasdo sorohidrolisadas, o grupoalimentado comleite maternoapresentouamenorconcentrac¸ãodoaminoácido,25 oquepareceocorrer,mesmoemrecém-nascidosatermo, devidoaomaiorteordefenilalaninanasfórmulasàbasede leitedevaca.
OmesmoresultadofoiencontradoemRNPTalimentados com LH com três diferentes aditivos: proteína do LH, proteínadosorodeleitedevacaeumamisturadeproteína do soro de leite de vaca, peptídeos e aminoácidos com uma composic¸ão de aminoácidos parecida com a do LH. A concentrac¸ão de fenilalanina foi maior no grupo que recebeuo LHcomaditivo deproteínadosorodeleitede vaca.Entreosoutrosdoisgruposnãohouvediferenc¸a.26
fórmulas com proteínas do leite de vaca com diferen-tes teores e proporc¸ão de proteínas do soro/ caseína, aqueles alimentados com leite humano tiveram a menor concentrac¸ãoplasmáticadefenilalanina.27
Por outro lado, um estudo que ofereceu a RNPT leite humanodebanco,leitehumanodebancoevaporadoa70% ou leite humano de banco com aditivo comercial FM85®
nãoencontroudiferenc¸asignificativanos níveisde fenila-laninaplasmática. Nesse caso, nem a quantidade,nem a qualidadedaproteínaoferecidainterferiunosníveisséricos desseaminoácido.23
Outroestudoqueavaliouofluxodosaminoácidosglicina, leucinae fenilalanina em RNPT em alimentac¸ão parente-raleenteralobservouqueofluxodoaminoácidoglicinaé maisafetado pela via deadministrac¸ão, o doaminoácido leucinaépouco afetado eo doaminoácidofenilalanina é maisafetadopeloaporteoferecido.28
Apesardoaumentosignificativodefenilalanina plasmá-tica, não foi observada qualquer repercussão metabólica importantenosbebêsalimentadoscomproteínadeorigem bovinanodecorrerdesteestudo,masemlongoprazopode serumfatorruimnodesenvolvimentocognitivo.Portanto, aindasãoquestionadososníveisplasmáticosideaisde fenila-laninaafimdeevitarosefeitosnocognitivoemlongoprazo. As investigac¸õesrealizadas demonstram que o LHcom aditivosdeleprópriocomportou-secomoumbomsubstrato paraalimentac¸ãodoRNPT,sejanaformaevaporadaou liofi-lizada,semlevaraaumentossignificativosnaconcentrac¸ão plasmáticadefenilalaninaemcomparac¸ãoaoleitehumano comaditivocomercial.
Financiamento
BolsadepesquisadaFundac¸ãodeApoioaoDesenvolvimento doEnsino,CiênciaeTecnologiadoEstadodoEstadodeMato GrossodoSul(FUNDECT).
Conflitos
de
interesses
Osautoresdeclaramnãohaverconflitosdeinteresse.
Referências
1.CockerillJ,UthayaS,DoréCJ,ModiN.Acceleratedpostnatal headgrowthfollowspretermbirth.ArchChildFetalNeonatal. 2006;1:184---7.
2.SinghalA,FarooqiIS,O’RahillyS,ColeTJ,FewtrellM,LucasA. Earlynutritionandleptinconcentrationinlaterlife.AmJClin Nutr.2002;75:993---9.
3.SinghalA, FewtrellM,ColeTJ,LucasA. Lownutrientintake andearlygrowthforlaterinsulinresistanceinadolescentsborn preterm.Lancet.2003;361:1089---97.
4.HalesCN,OzanneSE.Thedangerousroadofcatch-upgrowth. JPhysiol.2003;547:5---10.
5.ChanGM,LeeML,RechtmanDJ.Effectsofahumanmilk-derived humanmilkfortifierontheantibacterialactionsofhumanmilk. BreastfeedMed.2007;2:205---8.
6.MartinezFE,CameloJuniorJS.Alimentac¸ãodorecém-nascido pré-termo.JPediatr(RioJ).2001;77:32---40.
7.PalharesDB,JorgeSM,Gonc¸alvesAL,MartinezFE.Aminoácidos plasmáticosderecémnascidospré-termoalimentadoscomleite humanodebancodeleiteoufórmuladosleitedevaca.JPediatr (RioJ).1990;66:188---92.
8.LucasA.Influenceofneonatalnutritiononlong-termoutcome. In: SalleBL, SwyerPR,eds. Nutrition of the very-low-birth--weightinfant.NestléNutritionWorkshopSeries,32.NewYork: RavenPress;1993.p.183---96.
9.PereiraGR,NiemanL.Métodosdenutric¸ãoporviaenteralem recém-nascidopré-termo.In:PereiraGR,LeoneCR,Navantino AF,editors.TrindadeOF.Nutric¸ãodorecém-nascidopré-termo. RiodeJaneiro:Medbook;2008.p.31---43.
10.PencharzPB,BallRO.Aminoacidneedsforearlygrowthand development.JNutr.2004;134:1566---8.
11.RäihäNC.Biochemicalbasisfornutritionalmanagementof pre-terminfants.Pediatrics.1974;53:147---56.
12.HayJrWW.Strategiesforfeedingthepreterminfant. Neona-tology.2008;94:245---54.
13.VazFA,LauridsenE,TrosterEJ.Alimentac¸ãodorecém-nascido pré-termo:considerac¸õesatuais.Pediatria.1985;7:3---7.
14.Cie´slaJ,Fr˛aczykT,RodeW.Phosphorylationofbasicaminoacid residuesinproteins:importantbuteasilymissed.ActaBiochim Pol.2011;58:137---48.
15.KilaniAR,ColeFS,BierDM.Phenylalaninehydroxylaseactivity inpreterminfants:istyrosineaconditionallyessentialamino acid?AmJClinNutr.1995;61:1218---23.
16.DenneSC,KarnCA,AhlrichsJA,DorotheoAR,WangJunying, LiechtyEA.Proteolysisandphenylalaninehydroxylationin res-ponse to parenteral nutrition in extremely premature and normalnewborns.JClinInvest.1996;97:746---54.
17.ShortlandGJ, Walter JH, FlemingPJ, Halliday D. Phenylala-ninekineticsinsickpretermneonateswithrespiratorydistress syndrome.PediatrRes.1994;36:713---8.
18.LucasA,LucasPJ,ChavinSI,LysterRL,BaumJD.Ahumanmilk formula.EarlyHumDev.1980;4:15---21.
19.SantosMM, Martinez FE, Sieber VM, Pinhata MM, Ferlin ML. Acceptability and growth of VLBW --- infants fed with own mother’milkenrichedwithanaturalorcommercialhumanmilk fortifier.PediatricResearch.1997;41:231.
20.Camelo Junior JS, Martinez FE. Lactoengenharia do leite humano.In:PereiraGR,LeoneCR,AlvesFilhoN,TrindadeFilho O,editors.Nutric¸ãodorecém-nascidopré-termo.São Paulo: Medbook;2008.p.11---29.
21.ThomazDM, Serafim PO, PalharesDB, MelnikovP, Venhofen L, Vargas MO. Comparison between homologous human milk supplementsandacommercialsupplementforverylowbirth weightinfants.JPediatr(RioJ).2012;88:119---24.
22.Graham-ThiersPM,BowenLK.Effectofproteinsourcenitrogen balanceand plasmaaminoacidsinexercisinghorses.JAnim Sci.2011;89:729---35.
23.SantosSC, Figueiredo CM, Andrade SM,PalharesDB. Plasma amino acids in preterm infants fed different human milk diets from a human milk bank. Eur J Clin Nutr. 2007;2: 51---6.
24.PalharesDB, ThomazDM,TavaresLV,SerafinP.Effectofdiet onserumaminoacidprofileinvery-low-birthweightneonates. AdvancesinMedicineandBiology.2011:31.
25.Olle H, Lõnnerdal BO. Nutritional evaluation of protein hydrolysate formulasin healthy term infants: plasmaamino acids,hematology,and traceelements.AmericanJClinNutr. 2003;78:296---301.
26.Boehm G, Borte M, Bellstedt K, Moro G, Minoli I. Protein quality of human milk fortifier in low birth weight infants: effectsongrowthandplasmaaminoacidprofiles.EurJPediatr. 1993;152:1036---9.
27.RassinDK,GaullGE,RaihäNC,HeinonenK.Milkprotein quan-tity and quality in low-birth weight infants: IV: Effects on tyrosine and phenylalanine in plasma and urine. J Pediatr. 1977;90:356---60.