ANA ISABEL BATISTA DA MOTA BAÍA
DESCOLORAÇÃO DE CORA TES AZO EM REACTORES
A AERÓBIOS TERMÓFILOS
Dissertação apresentada para a obtenção do
grau de Mestre no ramo de Química pela
Universidade da Beira Interior
Orientador: Professora Doutora Isolina Maria Silva Cabral Gonçalves
2
Todo o estudo sientifico é simples aproximação à verdade, nunca o seu esgotamento:
“Face à realidade, o que julgamos saber claramente ofusca o que deveríamos saber”
3
4
Agradecimentos
À Professora Doutora Isolina Gonçalves pela orientação, rigor científico e dedicação manifestadas ao longo do trabalho, fundamentais para a sua conclusão.
À Professora Doutora Maria José Pacheco pelo testemunho de trabalho, pela incondicional disponibilidade e sobretudo pela coragem transmitida.
À D. Ana Brás, D. Isabel Aibéu e a todos os funcionários do Departamento de Química, Universidade da Beira Interior, que directa ou indirectamente colaboraram na realização deste trabalho.
À Fitecom SA, na pessoa do Exmo. Eng.º João Carvalho, pela compreensão evidenciada face à necessidade de alteração do meu horário de trabalho, a fim de poder concretizar este estudo.
A todos, muito obrigado!
5
Resumo
O presente trabalho centra-se no desempenho dos reactores termófilos no tratamento de efluente têxtil simulado. Foi avaliada a influência de um bioadsorvente (dreche) na descoloração anaeróbia de corantes azo. Dois reactores UASB operaram a uma temperatura de 55 ± 2ºC, com um tempo de retenção hidráulico de 7 horas, alimentados com glucose, o substrato. O reactor termófilo, RT, foi inoculado com biomassa anaeróbia mista e no outro foi incorporada dreche, RT-DC, na razão de 1:4 bioadsorvente / biomassa anaeróbia mista (v/v). Os resultados indicam, no global, uma melhor performance para o RT-DC relativamente ao RT. Em média a taxa de remoção de CQO foi de 3,8 ± 1,6 e de 4,3 ± 1,7 g CQO removido/L.d, para uma concentração de corante de 60 mg/L, no RT e RT-DC respectivamente. A percentagem de remoção de cor foi, para o corante Reactive Orange 16, de 76 ± 1% no RT e para o corante Acid Orange 7 foi de 81 ± 1% no RT-DC.
Embora se tenham obtido bons resultados foi registada alguma instabilidade no sistema, causada sobretudo por variações no caudal e no pH de alimentação, conduzindo a um decréscimo na taxa de remoção de CQO. Ambos os corantes foram removidos, contudo algumas aminas aromáticas geradas como metabolitos anaeróbios continuam presentes na descarga dos reactores. Estes resultados foram confirmados através de espectros de UV-visível. A presença da dreche no RT-DC parece também contribuir para a eliminação de, pelo menos, um dos metabolitos do AO7, o 1-amino-naftol, pois não foi detectada a sua presença nos cromatogramas de HPLC. Sob condições termófilas o agente liposomal (fosfolípidos) foi testado como alternativa de co-substrato à glucose. Em ambos os reactores registaram-se aumentos das taxas de remoção de CQO e de remoção de cor. A integração do adsorvente anaeróbio no reactor (RT-DC) parece contribuir para um aumento dos parâmetros de eficiência, tais como CQO, COT e remoção da cor. Assim, a dreche (um resíduo da indústria cervejeira) pode ser aplicada na condição de agente modificador e adsorvente em reactores anaeróbios, representando um papel importante na performance do sistema. Seria importante a realização de estudos complementares neste tipo de degradação, para se compreender melhor a descoloração anaeróbia nestas circunstâncias.
6
Abstract
The present work is focused on the performance of thermophilic anaerobic reactors treating a simulated textile effluent. The influence of a biosorbent (spent brewery grains) on anaerobic decolourization of azo dyes was evaluated. Two upflow anaerobic sludge blanket reactors operating at 55 ± 2ºC, with a hydraulic retention time of 7h and fed with glucose as co-substrate were followed. The thermophilic reactor, TR, was inoculated with mixed anaerobic biomass and the integrated biosorption-anaerobic thermophilic reactor, TR-B, was inoculated with a 1:4 biosorbent /mixed anaerobic biomass ratio (v/v). Results indicate an overall better performance for the TR-B system relatively to TR. In average a COD removal rate of 3.8 ± 1.6 and 4.3 ± 1.7 g COD removed/L.d for a dye concentration of 60 mg/L could achieved for TR and TR-B respectively. The percentage of colour removal was in average, for dye Reactive Orange
16, of 76 ± 1 % in TR and for the dye Acid Orange 7 of 81 ± 1 % in the TR-B system. Although these good results have been obtained, some instability of both systems were
registered, caused mainly by flowrate and pH feed variations, leading to a decrease of the COD removal rates. Both dyes were removed, however some aromatic amines generated as anaerobic metabolites still remained in the out of the reactors. These results were checked by UV-visible spectra. The presence of spent brewery grains in the reactor TR-B seems also to contribute for the elimination of, at least, one of the AO7 metabolites, the 1-amino-naphtol, since its presence was not detected in the HPLC chromatograms. Under thermophilic regime a liposome agent (phospholipids) tested as an alternative co-substrate to glucose in both reactors for decolourization tests depicted an increase of both COD and colour removal rates. The integrated anaerobic-biosorption reactor (TR-B) seems to display an improvement of the efficiency parameters, such as COD, TOC and colour removal. This shows that spent brewery grains (a by-product of brewery industry) could be applied as a conditioning along with as an adsorvent agent in anaerobic reactors, playing an important role in the performance of the system. Some complementary studies on its degradation are also necessary in order to have a better understanding of the anaerobic decolourization under these circumstances.
7
Abreviaturas
AO7 C.I. HPLC RO16 rpm RT RT-DC SBG SBR SS SSV TRH UASB UV Acid Orange 7 Colour ÍndexCromatografia líquida de alta
Reactive Orange 16
Rotações por minuto Reactor termófilo
Reactor termófilo com dreche
Spent Brewer’s Grains Sequential Batch Reactor
Sólidos suspensos
Sólidos suspensos voláteis Tempo de retenção hidráulico
Upflow Anaerobic Sludge Blanket
8
Índice
1. Introdução ... 1
2. Revisão bibliográfica ... 4
2.1 Aspectos da Indústria Têxtil ... 4
2.2 A cor no efluente têxtil ... 5
2.3 Processos de tratamento ... 11
2.3.1 Processos físicos ... 12
2.3.2 Processos químicos ... 13
2.3.3 Processos biológicos ... 13
2.4 Tratamento anaeróbio ... 13
2.4.1 Química e bioquímica do processo ... 16
2.4.2 Processos Termófilos ... 18
2.4.3 Tratamento Anaeróbio Aplicado à Remoção de Corantes Azo ... 20
2.4.4 Tratamento Anaeróbio na Europa ... 21
2.5 Valorização da dreche cervejeira ... 21
2.5.1 Processo de obtenção ... 22
2.5.2 Composição química e propriedades físico-químicas ... 23
2.5.3 Aplicações ... 24
2.5.4 Vias de metabolismo anaeróbio de componentes associados à Dreche ... 30
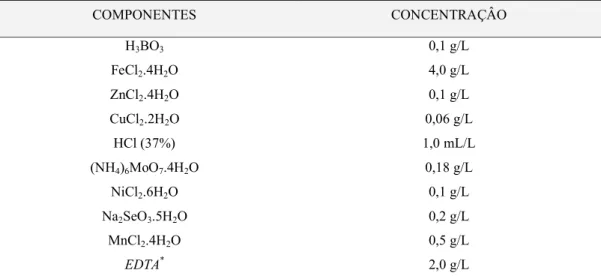
3. Material e métodos ... 32 3.1 Inóculo ... 32 3.2 Meio de cultura ... 32 3.3 Corantes ... 34 3.4 - Métodos analíticos... 35 3.5 - Metodologia experimental ... 36
9
4. Degradação do corante por tratamento anaeróbio ... 38
4.1 - Fase de adaptação dos reactores ... 38
4.2 - Remoção de CQO ... 38
4.3 Descoloração ... 42
4.4 Remoção de COT ... 44
4.5 Comparação do comportamento do leito dos reactores ... 48
4.6 Influência do substrato principal no funcionamento do RT e RT-DC ... 52
5. Conclusões e sugestões de trabalho futuro ... 55
Descoloração de Corantes Azo em Reactores Anaeróbios Termófilos
1
1. Introdução
Nas últimas décadas, os problemas ambientais têm-se tornado cada vez mais críticos e frequentes devido, principalmente, ao desmedido crescimento populacional e ao aumento da actividade industrial. As alterações na qualidade do solo, do ar e da água têm atingido proporções catastróficas. Sem dúvida que a contaminação das águas naturais tem sido um dos grandes problemas da sociedade moderna. Neste contexto, a economia da água em processos produtivos deve receber especial atenção devido ao valor que se associa a este bem de primeira necessidade (Kunz et al., 2002).
No sector têxtil, em particular os processos húmidos geram elevados volumes de efluentes, os quais não sendo correctamente tratados, podem causar sérios problemas de contaminação ambiental (Kunz et al., 2002).
Historicamente, a indústria têxtil sempre se localizou na proximidade de rios e ribeiras, que disponibilizavam a água necessária para o processo produtivo, recebendo em troca os efluentes gerados. Esta indústria caracteriza-se por requerer elevadas quantidades de água e de produtos químicos, produzindo assim, efluentes de grande variabilidade quanto ao volume e quanto á composição (Vandevivere et al., 1998). O maior inconveniente da descarga indiscriminada destes resíduos, reside no facto destes conterem substâncias orgânicas e inorgânicas de difícil degradação, mesmo a longo prazo.
Os problemas ambientais associados à indústria têxtil derivam, entre outros, do uso de corantes orgânicos. Um grande número destes compostos é recalcitrante e apresenta carácter carcinogénico e mutagénico (Soares, 2000). Tendo em conta que a maioria dos resíduos são lançados em recursos naturais, sem qualquer tipo de tratamento, tornou-se urgente aprofundar a investigação nesta área. Estas visam a elaboração de métodos eficazes e económicos para a eliminação destes compostos dos rios de forma integral. Como processos de remoção deste tipo de compostos podem referir-se processos biológicos e físico-químicos como a coagulação – floculação, tecnologias de membrana em associação com processos de oxidação, nomeadamente electroquímica, oxidação avançada incluindo fotocatálise e ozonólise, entre outros. Nas últimas décadas tem-se assistido ao avanço significativo dos processos biotecnológicos, na remediação dos
Descoloração de Corantes Azo em Reactores Anaeróbios Termófilos
2
ecossistemas. Neste âmbito, os fungos, as leveduras e microrganismos têm sido investigados na remoção da carga poluente têxtil. Relativamente aos bioprocessos, a sua aplicação na degradação de corantes azo tem sido efectuada quer por via anaeróbia, quer aeróbia. De acordo com a literatura os corantes, de uma maneira geral, são biodegradados. A susceptibilidade destes compostos à degradação biológica depende do tipo de grupo substituinte associado aos anéis aromáticos presentes na sua estrutura química (Camargo, 2002;Corso, 2002).
Em geral a quebra da ponte azo efectua-se por um processo redutivo, originando aminas aromáticas, as quais poderão ser posteriormente eliminadas por diferentes vias metabólica. Neste contexto, a integração de bioprocessos parece constituir uma alternativa viável à mineralização de corantes. Os produtos da descoloração resultantes de bioprocessos redutivos poderão ser eliminados via metabólica anaeróbia, desde que se desenvolva no sistema uma maior diversidade microbiológica, o que pode ser conseguido por adição de substratos mais complexos. Estes poderão simultaneamente funcionar nas suas diferentes etapas de degradação, como bioadsorventes e como transportadores de electrões, complementando as vias metabólicas associadas à descoloração e mineralização destes compostos. A adição de bioadsorventes à biomassa anaeróbia, pode ser conseguida valorizando-se um subproduto ou um resíduo de outro processo instalado, como a dreche resultante da produção cervejeira. Sendo a dreche constituída basicamente por celulose, arabinoxileno, lenhina, proteínas e lípidos, a bioeliminação simultânea desta permitirá obter, não apenas ganhos energéticos (produção de metano e hidrogénio), como também remover compostos xenobióticos como os corantes. Para além da poluição estética, estes podem contribuir para a carência química de oxigénio nas águas, contaminação de solos e originar mutações genéticas em espécies dos ecossistemas, sendo a sua eliminação uma preocupação pertinente e actual dos investigadores nesta área (Camargo, 2002;Corso, 2002).
Neste trabalho procurou desenvolver-se um processo integrado anaeróbio no qual se incorporou um bioadsorvente, dreche cervejeira, com o intuito de avaliar a sua aplicação na bioeliminação de corantes azo. Mais especificamente, pretendeu-se contribuir para o estudo de processos alternativos aos reactores anaeróbios térmófilos convencionais “UASB - upflow anaerobic sludge blankt” .
A influência do tipo de corante azo, ácido e reactivo no sistema integrado anaeróbio – biosorção operado em regime termófilo, bem como da presença do bioadsorvente no
Descoloração de Corantes Azo em Reactores Anaeróbios Termófilos
3
processo de descoloração está descrita nos capítulos 3 e 4. Estes capítulos seguem-se ao capítulo 2, no qual se apresenta o estado da arte relativo à bioremoção de corantes têxteis. No último capítulo, capítulo 5, efectuou-se uma análise global à viabilidade do processo, tendo por base os resultados parciais obtidos na preparação da presente dissertação.
Descoloração de Corantes Azo em Reactores Anaeróbios Termófilos
4
2. Revisão bibliográfica
2.1 Aspectos da Indústria Têxtil
Estima-se que o sector têxtil tenha um consumo de água da ordem dos 90.000 a 800.000 m3/ano, o que representa uma utilização de cerca 50 a 250 m3 por tonelada de produto têxtil (APT, 2000).
Os efluentes têxteis podem apresentar elevadas cargas orgânicas, principalmente os provenientes da lavagem das lãs, com valores entre 30 a 150 g/L expressos em CQO (carência química de oxigénio). Este tipo de efluentes é essencialmente constituído por gorduras, sujidades orgânicas e inorgânicas, detergentes, álcalis, pesticidas (organofosfatos) e insecticidas. Apresentam uma razão CQO/CBO5 (carência
bioquímica de oxigénio) entre 2,5 e 3, elevado teor de sólidos suspensos (SS), entre 18 e 80 g/L e valores de pH entre 8 e 10 (Brás, 2003).
A ultimação têxtil engloba o conjunto de operações a que um “tecido” é submetido após a sua fabricação até estar pronto para a sua confecção. Essas operações, às quais se pode aplicar também a designação de enobrecimento têxtil, podem ser subdivididas da seguinte forma:
- Tratamento prévio ou preparação, conjunto de operações necessárias para preparar o material para ser tingido, estampado ou receber um dado acabamento; estas operações são por vezes designadas genericamente apenas por branqueamento.
- Tingimento, operação de coloração uniforme do material têxtil.
- Acabamentos propriamente ditos, efectuados sobre o tecido já branqueado, tingido ou estampado, conforme o caso, de forma a torná-lo mais adequado para o fim em vista (Araújo e Castro, 1986).
Nas fases de ultimação têxtil intervém como matérias-primas não só o material têxtil como também diversos produtos, desde a água, resinas, corantes, detergentes, entre outros. A água é, em termos de quantidade, a principal matéria-prima na ultimação
Descoloração de Corantes Azo em Reactores Anaeróbios Termófilos
5
têxtil. É um factor determinante na localização de fábricas: em locais onde a água é mole e na proximidade de cursos de água (Araújo e Castro, 1986).
Estima-se que mais de 50% do corante utilizado, dependendo do tipo, é rejeitado no efluente durante o processo de tingimento. Este tipo de efluentes industriais deveria ser tratado antes da descarga para o meio ambiente (Supaka et al., 2004).
Os efluentes provenientes do processo de enobrecimento têxtil apresentam um pH que pode variar desde valores ácidos a alcalinos, dependendo do tipo de fibra, do tipo de corante utilizado e da quantidade de base usada nas operações de ultimação (Brás, 2003).
2.2 A cor no efluente têxtil
A cor é um dos factores de sucesso comercial dos produtos têxteis. Cada vez mais os consumidores exigem produtos de elevada qualidade. Consequentemente, estes produtos têm de apresentar, entre outras características, solidez à luz e à lavagem. Assim, para além da optimização dos processos, os corantes usados devem ser estáveis, para resistirem aos vários tratamentos usados no processo têxtil, sendo para isso utilizadas substâncias cada vez mais difíceis de degradar (Soares, 2000). As moléculas de corante e alguns produtos resultantes da sua degradação podem ser tóxicos ou conter metais pesados que, uma vez libertados, podem inibir a actividade biológica (Brás, 2003).
A cor é o primeiro sintoma de contaminação visível no efluente. A remoção de cor nos efluentes têxteis é hoje uma prioridade, constituindo um sério desafio à indústria têxtil e a organismos e empresas dedicadas ao tratamento de águas residuais (Soares, 2000).
A fracção de corante rejeitada nas águas residuais têxteis, depende do tipo de fibra processada, do tipo de corante aplicado e da tecnologia de tingimento. A tabela 2.1, apresenta os valores médios para os diferentes parâmetros que constituem um efluente após tingimento.
Descoloração de Corantes Azo em Reactores Anaeróbios Termófilos
6
Tabela 2.1 Características de um efluente após processo de tingimento (adaptado de Figueiredo, 2006).
Até meados do século XIX apenas eram utilizados corantes naturais, cujo nome estava relacionado com a planta (ou animal ou mineral) donde eram extraídos. Com o aparecimento dos corantes sintéticos, a nomenclatura começou a complicar-se; os inúmeros nomes comerciais existentes encontram-se sistematizados no conhecido “Colour Index” (C.I.), espécie de dicionário dos corantes editado pela Society of Dyes
and Coulorists e pela Americ Association of Textile Chemists and Clorists (Araújo e
Castro, 1986).
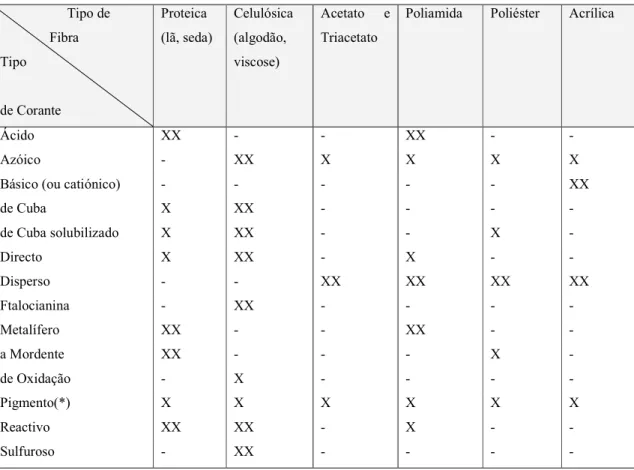
Relativamente à classificação dos corantes, se para os químicos interessa fundamentalmente a constituição química, para os têxteis interessa mais o seu comportamento tintorial, relacionado com as condições de aplicação. Na tabela 2.1 encontram-se, por ordem alfabética, os diferentes tipos de corantes, de acordo com a classificação por utilização, bem como a sua aplicação às diferentes fibras têxteis.
Parâmetro Valores Médios Unidades
CQO 1100 – 4600 mg O2/L CBO5 10 – 1800 mg O2/L ST 500 – 14100 mg/L STD ≈ 50 mg/L pH 5 – 10 Cor 1450 – 4750 mg/L Água 8 - 300 L/Kg
Descoloração de Corantes Azo em Reactores Anaeróbios Termófilos
7
Tabela 2.2 Corantes de acordo com a sua aplicação às diferentes fibras (Araújo e Castro, 1986). Tipo de Fibra Tipo de Corante Proteica (lã, seda) Celulósica (algodão, viscose) Acetato e Triacetato
Poliamida Poliéster Acrílica
Ácido XX - - XX - -
Azóico - XX X X X X
Básico (ou catiónico) - - - XX
de Cuba X XX - - - - de Cuba solubilizado X XX - - X - Directo X XX - X - - Disperso - - XX XX XX XX Ftalocianina - XX - - - - Metalífero XX - - XX - - a Mordente XX - - - X - de Oxidação - X - - - - Pigmento(*) X X X X X X Reactivo XX XX - X - - Sulfuroso - XX - - - - xx Muito adequado x Adequado
(*) Não pode ser considerado um verdadeiro corante – pigmentos
Os corantes também podem ser classificados de acordo com a sua estrutura química, tendo em conta o grupo cromóforo responsável por lhe conferir cor. A cor resulta da absorção de radiação visível pela molécula de corante, devida à presença desses mesmos grupos. Estes são constituídos por um sistema de electrões com ligações duplas conjugadas, e do grupo funcional ou auxocromo, que é um substituinte, doador ou aceitador de electrões que intensifica a cor do cromóforo, alterando a energia global do sistema de electrões. Os grupos cromóforos mais frequentes são: -C=C-; -C=N-; -C=O-; -N=N-; -NO2; os grupos auxocromos são: -NH3; -COOH; -SO3H e –OH (Correia et al.,
Descoloração de Corantes Azo em Reactores Anaeróbios Termófilos
8
Esta classificação define um grande número de classes estruturais diferentes de corantes e pigmentos. À classe mais importante pertencem os corantes azo (monoazo, diazo, triazo e poliazo, consoante o número de ligações azo, -N=N-, existentes na molécula do corante). Este grupo de corantes constitui cerca de dois terços dos corantes orgânicos listados. Os corantes antraquinónicos possuem um grupo cromóforo antraquinónico, podendo este estender-se a outras estruturas policíclicas de quinonas. Os corantes triarilmetanos constituem a classe comercial mais representativa, vulgarmente aplicados em meio ácido, básico e a mordente (Kunz et al., 2002).
Em seguida descrevem-se de forma mais pormenorizada as diferentes classes de corantes em função do grupo cromóforo.
Corantes Antraquinónicos – dentro desta classe de corantes encontram-se corantes ácidos, mordentes, dispersos, básicos, directos, reactivos, entre outros.
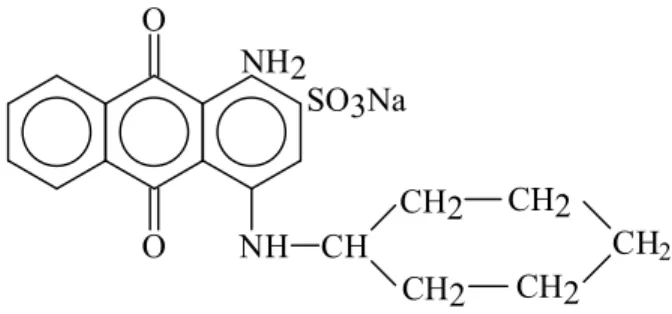
Os corantes reactivos possuem um grupo electrófilo capaz de formar uma ligação covalente com grupos hidroxilo das fibras celulósicas, com grupos amino, hidroxilo e tióis das fibras proteicas e com grupos amino das poliamidas. Com este tipo de corantes, a reacção química processa-se directamente através da substituição do grupo nucleofílico pelo grupo hidroxilo da celulose. Como exemplo temos o Reactive Orange 16 (figura 2.1). Considerando os corantes dispersos, insolúveis em água, aplicam-se geralmente no tingimento de fibras celulósicas e outras fibras hidrofóbicas através de suspensão. Durante o processo de tingimento, o corante hidrolisa-se e a forma, inicialmente, insolúvel precipita lentamente na forma dispersa sobre o acetato de celulose. Normalmente, estes processos ocorrem na presença de agentes dispersantes, com longas cadeias, que estabilizam a suspensão do corante, facilitando assim, o contacto entre o corante e a fibra (Guaratini, 1999; Zanoni, 1999).
Figura 2.1 Corante antraquinónico, Reactive Orange 16. O O NH CH SO3Na NH2 CH2 CH2 CH2 CH2 CH2
Descoloração de Corantes Azo em Reactores Anaeróbios Termófilos
9
Corantes Triarilmetanos - são corantes aniónicos portadores de um ou mais grupos sulfónicos.
Estes grupos substituintes ionizáveis tornam o corante solúvel em água; aplicam-se no tingimento de fibras proteicas (lã, seda) bem como em fibras de poliamida sintética. Após neutralização do corante, este liga-se à fibra através de uma troca iónica que envolve o par de electrões livre dos grupos amino e carboxilato das fibras proteicas na forma não protonada (Guaratini, 1999; Zanoni, 1999).
Importantes no tingimento de fibras proteicas e poliamida. Têm a característica de possuir um grupo hidroxilo ou carboxilo na posição orto relativamente ao cromóforo azo, permitindo a formação de complexos com iãos metálicos. Neste caso, o processo de tingimento explora a capacidade de interacção entre o metal e os grupos funcionais portadores de pares de electrões livres, como os que se encontram nas fibras proteicas (Guaratini, 1999; Zanoni, 1999).
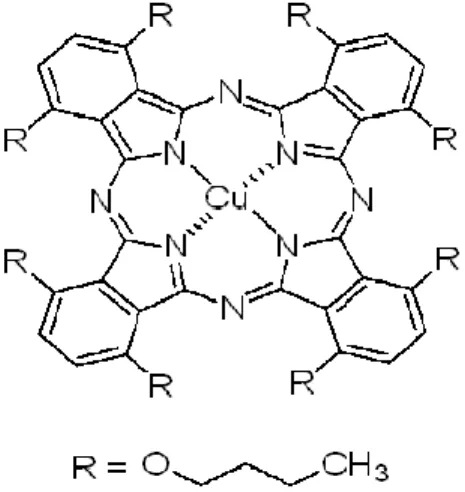
Corantes Ftalocianinas – corantes direccionados para o tingimento de fibras de celulose (algodão, viscose, etc), através de interacções de Van der Waals.
A afinidade do corante pela fibra aumenta pela presença de electrólitos, pela planaridade da configuração da molécula do corante ou pela dupla ligação conjugada, que permite um aumento da adsorção do corante sobre a fibra. Este grupo de corantes contém, normalmente, mais do que um grupo azo (Guaratini, 1999; Zanoni, 1999).
Figura 2.2 Corante Ftalocianina, Copper(II)
Descoloração de Corantes Azo em Reactores Anaeróbios Termófilos
10
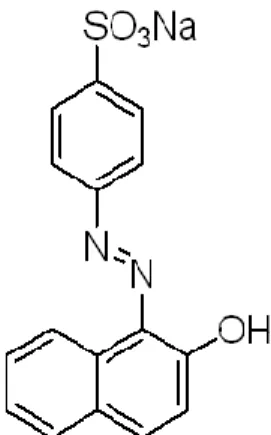
Corantes azo – os corantes azo constituem o maior grupo de corantes usados mundialmente, representando cerca de 50% da produção total (Eropean IPPC, 2002).
Quimicamente são caracterizados por um ou mais grupos azo (-N=N-). Em conjunto com as estruturas aromáticas adjacentes formam um sistema conjugado de electrões, que facilita a sua deslocalização das orbitais π, possibilitando a absorção de diferentes níveis de energia, na zona do visível.
A reacção de síntese destes corantes, mais generalizada, é denominada de diazotação: consiste no acoplamento de um sal de diazónio, resultante de uma amina aromática diazotada, com um anel de benzeno ou naftaleno, substituído por grupos aceitadores ou dadores de electrões, como os grupos amino, hidroxilo, cloro, nitro, metilo e sulfónico. Jogando com o número de grupos azo, tipo de anel aromático e tipo de posição dos substituintes, conseguem sintetizar-se muitos corantes azo, com uma enorme variedade de cores e intensidades. Estas características e o facto de serem moléculas quimicamente estáveis, sintetizadas com relativa facilidade, tornam estes corantes os mais usados industrialmente. Estima-se que existam mais de 10000 corantes azo comercializados, não só na indústria têxtil, mas na indústria do papel, alimentar e farmacêutica (Brás, 2003).
Pela sua elevada diversidade ao nível de cores e intensidades, os corantes azo têm a particularidade de poderem ser aplicados nos mais diversos materiais: fibras têxteis (naturais como a lã, seda, algodão e não naturais, viscose, poliésteres, polivinílicos e outras); plásticos; papel; curtumes; óleos minerais; ceras; alimentos; cosméticos; produtos farmacêuticos (Figueiredo, 2006).
Descoloração de Corantes Azo em Reactores Anaeróbios Termófilos
11
2.3 Processos de tratamento
As técnicas de tratamento baseadas em processos de coagulação, seguidos de separação por flotação ou sedimentação, apresentam uma elevada eficiência na remoção de partículas materiais. No entanto, a remoção de cor e a remoção de compostos orgânicos dissolvidos, apresenta algumas deficiências. Os processos de adsorção em carvão activado são mais eficientes, contudo, sendo a superfície química do carvão positiva, a adsorção de corantes de carácter catiónico torna-se uma limitação. Tendo em conta alguns destes inconvenientes, a utilização de processos que realmente degradem as substâncias de interesse, tem vindo a aumentar. Dentro destes processos destrutivos, os processos biológicos têm particular interesse, principalmente por causa da relativa facilidade que se encontrou na implementação de sistemas que operam em grande escala. Os processos biológicos utilizados mais frequentemente são os sistemas de lamas activadas: agitação dos efluentes na presença de microrganismos e ar, durante o tempo necessário para metabolizar e, ao mesmo tempo, flocular grande parte da matéria orgânica. Mas este processo têm um grande inconveniente, para além de ser bastante susceptível à composição do efluente, produz um grande volume de lamas (Kunz et al., 2002). Na tabela 2.3 encontram-se exemplos de tecnologias físico-químicas que podem ser aplicadas, quer como tratamento primário e/ou secundário, quer como afinação na depuração das águas residuais têxteis.
Descoloração de Corantes Azo em Reactores Anaeróbios Termófilos
12
Tabela 2.3 – Tecnologias físico-químicas utilizadas na remoção de corantes das águas residuais têxteis (adaptado de Figueiredo, 2006).
Tecnologia Características
Filtração por membrana • Necessita de tratamento posterior relativamente ao concentrado.
• Custos de implementação elevados.
Adsorção • Aplicação de carvão activado como adsorvente.
• Custos elevados relativamente ao carvão activado (dificuldade de desorção do corante).
Coagulação/Floculação • Aplicação como tratamento primário. • Aplicação como tratamento secundário. • Aplicação como tratamento de afinação. • Obtenção de elevado volume de lamas químicas. Troca iónica • Aplicação baseada na adsorção electrostática.
• Remoção efectiva de corantes reactivos.
• Custos elevados associados à regeneração do permutador iónico.
Processos electroquímicos • Possibilidade de formação de subprodutos desconhecidos.
• Formação de espumas.
• Elevados custos associados ao processo.
2.3.1 Processos físicos
Os processos físicos têm como principal função separar os sólidos em suspensão existentes nas águas residuais. Estes sólidos são eliminados por ordem crescente de tamanho. As operações mais importantes que fazem parte deste tipo de tratamento são: flotação, coagulação, floculação, sedimentação, filtração e centrifugação (Alonso et al., 2004).
Descoloração de Corantes Azo em Reactores Anaeróbios Termófilos
13
2.3.2 Processos químicos
Os processos químicos procuram a eliminação da matéria orgânica não metabolizada totalmente, após a aplicação de um processo biológico, ou que não é biodegradável. Estes processos incluem operações de oxidação química, adsorção, permuta iónica, processos de membrana (microfiltração, ultrafiltração, nanofiltração, osmose inversa, etc), entre outros (Alonso et al., 2004).
2.3.3 Processos biológicos
O principal objectivo do tratamento biológico é eliminar a matéria orgânica biodegradável presente nos efluentes. Criam-se as condições necessárias para que um grupo de microrganismos seja capaz de assimilar o substrato orgânico, transformando-o em dióxido de carbono e água, no caso de microrganismos aeróbios, ou dióxido de carbono e metano, quando se trata de microrganismos anaeróbios. Este tipo de tratamentos supõe a aplicação dos processos naturais de auto-depuração, levados a cabo em condições controladas. Ao reduzir a matéria orgânica consegue-se baixar a carência de oxigénio, tanto biológica como química, bem como a toxicidade da vida aquática dos efluentes. Também se incluem nestes processos biológicos, aqueles processos cujo principal objectivo é a eliminação de nutrientes (nitrogénio e fósforo) (Alonso et al., 2004).
Como tecnologia de tratamento os bio-reactores anaeróbios têm sido dos mais implementados no tratamento de efluentes industriais. Estes sistemas apresentam uma elevada diversidade de aplicação, operando quer em regime termófilo, quer mesofilo (Alonso et al., 2004).
2.4 Tratamento anaeróbio
Foi em 1977, na Holanda, que surgiu o primeiro reactor anaeróbio em grande escala. Com a capacidade de 1000 m3 este reactor de manto de lamas e fluxo ascendente ou reactor UASB (Upflow Anaerobic Sludge Blanket), era utilizado no tratamento de efluentes provenientes da produção de açúcar de beterraba (Lettinga et al., 1980). Este
Descoloração de Corantes Azo em Reactores Anaeróbios Termófilos
14
reactor foi o principal impulsionador da digestão anaeróbia como processo de tratamento de efluentes líquidos industriais.
Este tipo de reactor possibilita a obtenção de uma biomassa anaeróbia de morfologia granular, de baixo índice volumétrico de lamas, consequentemente, boas propriedades de sedimentação, sem necessidade da presença de um suporte inerte (Lettinga et al., 1980; Van Lier et al., 2001).
Os reactores UASB, conseguem operar a baixos tempos de retenção hidráulico, praticamente independentes do tempo de retenção de sólidos, pois possuem uma elevada capacidade de retenção de biomassa sem necessitar de reciclagem externa. Estas características hidrodinâmicas permitem a diminuição do volume do reactor, ou seja, há uma redução de custos de implementação e manutenção. Para além disso, conseguem depurar cargas orgânicas na ordem dos 10 a 15 Kg CQO/(m3.d) (Lettinga., 1992). Comparando-os com os sistemas anaeróbios convencionais, toleram melhor os compostos tóxicos ou inibitórios, pois a biomassa presente em elevada concentração está protegida pela estrutura granular (Dolon et al., 1997).
Calcula-se que estejam em funcionamento mais de 1000 reactores UASB em todo o mundo, utilizados no tratamento de efluentes industriais e municipais. A formação e a estabilidade dos grânulos da biomassa, com elevada actividade biológica e boas propriedades de sedimentação, são características que determinam e justificam o sucesso de aplicação destes reactores. O mecanismo e a velocidade de granulação bem como as características da lama granular formada dependem das espécies dos microrganismos envolvidos. Ou seja, dependem das suas velocidades de crescimento e de morte, da afinidade pelo substrato e da sua capacidade para produzir polímeros específicos e das condições de operação de cada reactor. Estudos anteriores propõem um modelo para a distribuição estrutural das espécies de microrganismos nos grânulos. Estes são constituídos por três camadas concêntricas: a camada externa contém uma grande variedade de bactérias anaeróbias facultativas tais como acidogénicas, sulfatoredutoras e metanogénicas hidrogenotróficas; a segunda camada ou intermédia, contém bactérias acetogénicas e metanogénicas hidrogenofílicas; na terceira camada e última, no centro do grânulo, existem bactérias metanogénicas acetoclásticas. Este modelo pode representar a conformação geral de um grânulo com actividade metabólica em condições nutricionais óptimas para todos os grupos de bactérias presentes. Nesta estrutura os microrganismos acidotróficos dominam a região interna dos grânulos e
Descoloração de Corantes Azo em Reactores Anaeróbios Termófilos
15
utilizam metabolitos produzidos pelas espécies acidogénicas (Buitton, 1994; Fang et al., 1994).
Nas últimas duas décadas foi extensa a bibliografia publicada por vários autores relacionada com a viabilidade de aplicação do reactor UASB no tratamento de uma vasta variedade de efluentes (McCarty, 2001), na remoção de alguns componentes tóxicos presentes em efluentes industriais, mais especificamente na remoção de sulfatos aos quais estão associados fenómenos de competição entre bactérias sulfatoredutoras e metanogénicas, por substratos orgânicos e à toxicidade do produto resultante da sua redução, o sulfureto (Lens et al., 1998).
Investigações recentes demonstram que alguns compostos orgânicos não biodegradáveis sob condições aeróbias são transformados por via anaeróbia. Estes sistemas apresentam benefícios ecológicos e económicos globais muito favoráveis relativamente a tecnologias alternativas, como é o caso dos tratamentos aeróbios ou físico-químicos. Para além dos custos operacionais serem reduzidos, os custos de investimento são também inferiores devido à menor dimensão do equipamento (Figueiredo, 2006).
A digestão anaeróbia é um processo fermentativo que tem por objectivos a remoção da matéria orgânica, a formação de biogás e a produção de biofertilizantes ricos em nutrientes. Assim constitui uma alternativa de tratamento para determinados efluentes industriais e sanitários. A baixa produção de lamas, a baixa necessidade de nutrientes, o facto de poder trabalhar com altas e baixas taxas orgânicas, são algumas das vantagens que caracterizam este tipo de sistemas.
Um digestor anaeróbio é um reactor biológico, onde a biomassa é mantida ao abrigo do ar e da luz. A metabolização anaeróbia é assegurada por biomassa bacteriana complexa (Edeline, 1988). Durante algum tempo, a digestão anaeróbia era aplicada no tratamento de resíduos industriais concentrados e da forma mais simples possível. Um pouco mais tarde, uma reestruturação do processo permitiu o desenvolvimento de reactores com outras configurações, bem como o tratamento de águas ou suspensões mais diluídas (Edeline, 1988).
Descoloração de Corantes Azo em Reactores Anaeróbios Termófilos
16
2.4.1 Química e bioquímica do processo
De uma forma simplificada, pode dizer-se que o processo anaeróbio ocorre em quatro etapas. Numa primeira etapa, a matéria orgânica complexa é transformada em compostos mais simples (aminoácidos, açúcares), pela acção de microrganismos que a hidrolisam. Na segunda etapa, as bactérias acidogénicas transformam, por sua vez, os aminoácidos e os açúcares em compostos mais simples (ácido acético, hidrogénio e dióxido de carbono). Estes produtos são transformados novamente, numa terceira etapa, por acção de bactérias acetogénicas. Finalmente, os microrganismos acetogénicos transformam estes substratos em CH4 e CO2.
Hidrólise
–
o primeiro passo da degradação anaeróbia, consiste na hidrólise ou liquefação dos biopolímeros, por meio de enzimas extracelulares, dado que as bactérias não têm capacidade para assimilar material orgânico na forma particulada. É normalmente um processo lento, sendo os lípidos, no geral, hidrolisados mais lentamente que as outras macromoléculas. A velocidade da hidrólise é afectada por um grande número de factores, entre os quais a superfície específica e varia com o tipo de substrato. Embora no caso de um substrato complexo e heterogéneo a cinética de hidrólise possa ser considerada de 1ª ordem, outras cinéticas podem descrever mais adequadamente a hidrólise de substratos simples e homogéneos. No caso de substratos complexos esta etapa pode limitar a velocidade do processo de degradação anaeróbia (Alves, 1998).Fermentação - os substratos utilizados no processo fermentativo são os monómeros resultantes da hidrólise que, após serem transportados através da membrana celular para o interior da célula, são transformados numa variedade de produtos, entre os quais acetato, propionato e butirato. Geralmente, a população fermentativa representa cerca de 90% da população bacteriana total dos digestores anaeróbios. O número e a diversidade das espécies bacterianas fermentativas envolvidas no processo depende largamente da composição do substrato e o comportamento da fase acidogénica afecta a metanogénese. Estudos microbiológicos da população fermentativa (ou acidogénica) em digestores anaeróbios mostram que a maioria das bactérias fermentativas são anaeróbias obrigatórias, sendo algumas anaeróbias facultativas. Estas últimas permitem manter o
Descoloração de Corantes Azo em Reactores Anaeróbios Termófilos
17
potencial redox do meio em níveis baixos, consumindo o oxigénio que, de alguma forma, possa entrar no digestor. As bactérias fermentativas têm tempos de duplicação curtos, verificando-se que a fermentação nunca é limitante no processo global da degradação anaeróbia (Alves, 1998).
Acetogénese e Metanogénese - Durante esta etapa, os produtos da fermentação são
transformados em acetato, dióxido de carbono e hidrogénio por acção das chamadas bactérias sintróficas ou produtoras obrigatórias de hidrogénio. Exemplo de uma transformação acetogénica:
CH3CH2COO- + 3H2O → CH3COO- + 3H2 + HCO3- + H+ (2.1)
As bactérias metanogénicas, que têm uma elevada afinidade para o hidrogénio transformam-no, juntamente com o dióxido de carbono, em metano, de acordo com a seguinte estequiometria:
HCO3- + 4H2 + H+ → CH4 + 3H2O (2.2)
A metanogénese, a etapa final do processo e responsável directa pela produção de metano constitui, em muitos casos, o passo controlador do processo. As bactérias metanogénicas pertencem ao reino das Arqueabactérias. São anaeróbias estritas requerendo para o seu desenvolvimento um potencial redox entre -250 e -300 mv. Possuem coenzimas e cofactores específicos e degradam apenas um número limitado de substratos com baixo número de carbonos: acetato, metanol, metilaminas, formato e hidrogénio + dióxido de carbono. As equações a seguir apresentadas exemplificam algumas das transformações que ocorrem durante esta etapa:
4H2 + CO2 → CH4 + 2H2O (2.3)
CH3COO- + H+ → CH4 + CO2 (2.4)
Descoloração de Corantes Azo em Reactores Anaeróbios Termófilos
18
De salientar que, em digestores anaeróbios tenta-se maximizar a conversão directa de metanol a metano relativamente às transformações acetogénicas, uma vez que a estas está associada menor remoção de carência química de oxigénio (CQO) (Alves, 1998).
2.4.2 Processos Termófilos
Foi em 1776 que Volta reconheceu que os processos biológicos anaeróbios resultavam na conversão da matéria orgânica em metano (Barker, 1956). Mais tarde, Metcalf e Eddy (1915) descrevem um sistema anaeróbio híbrido construído em 1890 por Moncrieff. Este consistia num tanque com um espaço vazio em baixo e um leito de pedra em cima. Um dos primeiros filtros anaeróbios descritos foi um leito de areia na estação experimental de Massachusetts, que se deduz ter começado a operar em 1887, com um tempo de retenção de 8 dias (McCarty, 2001).
Em Inglaterra, em 1895, Donald Cameron implementa com grande sucesso um outro processo anaeróbio, o tanque séptico. Este sistema, amplamente utilizado no tratamento de efluentes domésticos, transportava no efluente de saída matéria sólida não digerida. Facto que levantava problemas aos sistemas de tratamento a operar a jusante. A solução encontrada, estruturada por W. O. Travis em 1904, consistia num processo de tratamento composto por duas fases em que os sólidos suspensos sedimentavam num tanque, à qual deu o nome câmara de hidrólise, para fermentação autónoma. Por forma a optimizar a separação da matéria sólida do efluente, Karl Imhoff introduziu alterações neste sistema. Segundo Imhoff a matéria sólida permanecia no tanque de hidrólise por um período de tempo que ia de algumas semanas até vários meses, sendo posteriormente retirada e acondicionada (Metcalf e Eddy, 1915). Apesar de resolver alguns problemas o processo de Imhoff não mostrou ser a solução adequada para o tratamento completo de efluentes. A resolução do problema surgiu quando foi instalado em Essen-Rellinghausen o primeiro sistema aquecido de digestão de lamas num tanque de digestão em separado (McCarty, 2001). O sucesso deste sistema adveio da elevada eficiência de tratamento e do crescente reconhecimento do valor energético do metano que, para além de ser utilizado no aquecimento de digestores, foi também usado em outras aplicações (Imhoff, 1938).
Descoloração de Corantes Azo em Reactores Anaeróbios Termófilos
19
As primeiras experiências desenvolvidas com vista à aplicação de processos anaeróbios no tratamento de efluentes industriais são atribuídas a Arthur Buswell na década de 20 (McCarty, 2001). As suas pesquisas centraram-se no estudo dos processos anaeróbios e na sua aplicação ao tratamento de efluentes industriais e resíduos agrícolas. Um passo igualmente importante para o desenvolvimento dos processos anaeróbios foi dado por G. J. Stander que, ao separar as bactérias anaeróbias da corrente de saída, mantendo-as no sistema, concluiu que o tempo de retenção hidráulico podia ser reduzido até 2 dias, em vez das duas semanas ou mais utilizadas nos digestores convencionais. Esta alteração consistia num tanque de sedimentação colocado sobre o tanque de digestão, na base do qual o fluente era alimentado. Esta disposição, ao contrário da usada por Imhoff, permitia a sedimentação das bactérias entre outros sólidos, que continuamente eram reintroduzidos no tanque de digestão por gravidade, aumentando o tempo de retenção dos microrganismos no sistema. Esta evolução foi validada por aplicações à escala real, nomeadamente no tratamento de efluentes resultantes da produção e tratamento de vinho, tornando-se numa mais valia para a redução do tamanho dos reactores (Frankin, 2001).
O reactor de leito de lamas de fluxo ascendente (UASB), concebido por G. Lettinga (1980), tornou-se no reactor anaeróbio de aplicação mais bem sucedida em tratamento de efluentes industriais e municipais. As suas primeiras publicações descreviam este tipo de reactor através de duas ideias básicas. A primeira determinava que a agitação mecânica no reactor devia ser mínima para optimizar a sedimentação dos sólidos biológicos e a segunda determinava que o sistema de separação do biogás, bem como a sedimentação de sólidos, deveria ser instalado no topo do reactor (McCarty, 2001). Considerando que os efluentes têxteis são descarregados a elevadas temperaturas (40-70ºC), a opção por processos anaeróbios termófilos parece ser promissora, pois estes para além de serem eficazes na biodescoloração de corantes azo, favorecem a produção de biogás como fonte de energia. O metabolismo anaeróbio associado ao consórcio microbiano apresenta velocidades de reacção mais elevadas do que a dos processos mesofilos, tendo-se obtido velocidades de descoloração até seis vezes mais elevadas do que a observada em processos mesófilos (Santos, 2006).
Descoloração de Corantes Azo em Reactores Anaeróbios Termófilos
20
2.4.3 Tratamento Anaeróbio Aplicado à Remoção de Corantes Azo
De uma forma geral é assumido pela maioria dos investigadores que os corantes azo são resistentes à degradação bacteriana por via aeróbia (Shaul et al., 1991; Ganesh et
al., 1994; Pagga e Taeger, 1994). Nestas condições o mecanismo predominante de
bioeliminação está dependente da adsorção do corante à biomassa (Laing, 1991; Churchley et al., 1997). A degradação anaeróbia dos corantes azo ocorre por quebra redutiva da ligação azo, tendo sido propostos diversos mecanismos, nomeadamente por via enzimática, por vias metabólicas envolvendo transportadores de electrões e por via química directa entre outros (Haug et al., 1991; Bumpus, 1995; Delée et al., 1998). Por redução da ligação azo geram-se como produtos intermediários, aminas aromáticas, que são geralmente compostos de baixa coloração, excepto algumas aminas com grupos substituintes hidroxil e carboxil (Razo-Flores et al., 1997). Dependendo do tipo de grupo substituinte presente no anel aromático, as aminas são mais ou menos susceptíveis à mineralização por via anaeróbia ou por via aeróbia. Deste modo, vários dos mecanismos propostos na literatura para o metabolismo dos corantes azo por via bacteriana envolvem duas etapas. A primeira refere-se à redução da ligação azo com formação das aminas aromáticas e a segunda permite a mineralização dessas aminas por processos oxidativos ou redutivos.
Desta forma, a aplicação de sistemas anaeróbios combinados, sequenciais ou em fase, poderá ser a solução para a resolução dos problemas ambientais causados pela descarga directa dos corantes nos ecossistemas (Lourenço et al., 2001; Lourenço et al., 2003).
O processo de redução da ponte azo pode ser representado pela seguinte equação:
2e + 2H+
2e + 2H+
R1 – N = N – R2 → R1 – NH – NH – R2 → R1 – NH2 + R2 – NH2 (2.6)
R1 e R2 são os substituintes e, geralmente, correspondem a derivados de fenil e naftol
(Sangaleti et al., 1995).
Descoloração de Corantes Azo em Reactores Anaeróbios Termófilos
21
2.4.4 Tratamento Anaeróbio na Europa
Atendendo à crescente utilização das tecnologias anaeróbias existem estudos detalhados relativos à quantidade e tipo de sistemas anaeróbios a operar em todo o mundo aplicados ao tratamento de efluentes industriais (Frankin, 2001). De acordo com este autor, num total de 2000 unidades de tratamento de efluentes cerca de 1215 unidades referem-se ao tratamento de efluentes por via anaeróbia, o que corresponde a aproximadamente 60% do total.
Nos anos 70, a preocupação com a energia permite uma alteração dos antigos digestores anaeróbios, transformando-os em reactores de alto desempenho, tendo como principal objectivo a produção de gás, bem como a diminuição da poluição.
Actualmente, como método de tratamento de efluentes, a digestão anaeróbia oferece um número de vantagens significativas, como já foi referido, tornando-se numa tecnologia de grande interesse para grande parte da indústria química. Os sistemas de tratamento anaeróbios modernos, em associação com processos biológicos e físico-químicos, são sistemas que se apresentam bastante flexíveis permitindo tratar cargas orgânicas baixas e elevadas; podem ainda operar a diferentes temperaturas, desde o regime psicrófilo (0 – 20ºC) até ao regime termófilo (50 – 70ºC), possibilitando a degradação desde os substratos mais simples aos mais complexos (Lettinga, 2001). De salientar a degradação de compostos xenobióticos e persistentes efectuada por bactérias metanogénicas, as quais se julgava serem mais sensíveis a este tipo de poluentes comparando com as bactérias aeróbias.
2.5 Valorização da dreche cervejeira
Actualmente existe uma grande pressão política e social, para reduzir a poluição proveniente das diversas actividades industriais. Quase todos os países em crescimento tentam adaptar-se a esta realidade, modificando os processos, de forma a reciclar os resíduos. Consequentemente, a maioria das empresas jamais deveria considerar os resíduos como desperdícios, mas sim como matéria-prima para outros processos.
A fabricação da cerveja gera grande quantidade de resíduos, contudo, a maioria destes produtos agrícolas pode ser reutilizada. Assim, comparando com outras indústrias, a fabricação da cerveja “cuida” do meio ambiente. O spent grain (grão da
Descoloração de Corantes Azo em Reactores Anaeróbios Termófilos
22
cevada), contribui em média para 31% do peso do malte original, aproximadamente 20Kg por 100L de cerveja produzida. A sua produção em elevadas quantidades ocorre ao longo de todo o ano, a um custo moderado, não só em grandes cervejeiras como também nas pequenas (Mussatto et al, 2006).
2.5.1 Processo de obtenção
A cevada é o cereal mais importante no mundo, depois do trigo, milho e arroz. É usado principalmente em alimentos para animais ou como matéria-prima na produção de cerveja. O grão da cevada é rico em amido e proteínas e é composto por três partes principais: germe (embrião); endosperma (inclui o aleurona e o endosperma amiláceo) e o invólucro da semente. Este último pode dividir-se em três fracções: o tegumento (interior das camadas que rodeiam o aleurona); o revestimento do tegumento (camada do pericarpo) e a própria casca. O pericarpo é um pouco parecido com cera e é ligeiramente à prova de água e o tegumento actua como uma membrana semi-permeável. A interface pericarpo-tegumento define efectivamente o exterior e o interior da parte central, ou seja, do núcleo. As paredes da célula são compostas, principalmente, por linhocelulose mas também contém pequenas quantidades de proteínas, resinas e taninos (Mussatto et al, 2006).
Na preparação da fabricação da cerveja, após a colheita, a cevada é limpa e escolhida classificando-se conforme o seu tamanho. Após um período de descanso de 4 -6 dias, a cevada torna-se malte, num processo controlado de germinação que proporciona o aumento do conteúdo enzimático do grão. O processo de formação do malte inclui três etapas fundamentais: impregnação, germinação e secagem. A figura 2.4 é uma representação esquemática, não só do processo de obtenção do malte como também da produção do “grão cervejeiro” (SBG – Spent Brewery Grain).
O processo de fabrico da cerveja é selectivo, removendo apenas aqueles nutrientes do malte necessários para produzir a cerveja não fermentada: desperdícios lavados, proteínas insolúveis em água e os resíduos das paredes das células da casca (Mussatto et al, 2006).
Descoloração de Corantes Azo em Reactores Anaeróbios Termófilos
23 CEVADA ↓ Limpeza/Selecção ↓ Impregnação (água 5-18 ºC/ 48 h) ↓ Germinação (humidade do ar 15-21 ºC/ 6-7 dias) ↓ Secagem ↓ Armazenagem ↓ MALTE DA CEVADA ↓ Moagem ↓ Mistura (água + calor) ↓
Filtração → Fracção líquida/ Cerveja ainda Fracção sólida ↓ não fermentada
SBG
Figura 2.4 - Representação esquemática do processo de obtenção da SBG a partir da cevada (adaptado de Mussatto et al, 2006).
2.5.2 Composição química e propriedades físico-químicas
Os principais componentes do grão seco são a casca, o pericarpo e o tegumento. Este conjunto é rico em celulose, polissacáridos não – celulósicos e lenhina; também pode conter algumas proteínas e lípidos. A casca contém consideráveis quantidades de sílica e muitos dos compostos polifenólicos do grão da cevada. Estima-se que 25% dos minerais presentes na cevada apresentam-se como silicatos.
A composição química do grão varia de acordo com a variedade da cevada, a altura da colheita, as condições em que ocorre a formação do malte e com a quantidade e o tipo de complementos adicionados no processo de fabrico da cerveja. O grão da cevada seco é considerado um material linhocelulósico rico em proteína e fibra, cerca de 20% e 70% da sua composição, respectivamente. Examinação microscópica mostrou a presença de numerosos tecidos fibrosos oriundos da superfície das camadas do grão de cevada original. Os principais constituintes destes tecidos fibrosos são: arabinoxileno,
Descoloração de Corantes Azo em Reactores Anaeróbios Termófilos
24
lenhina (macro molécula polifenólica) e celulose (um homopolímero linear composto por unidades de glucose). Na tabela 5.1 encontram-se os principais constituintes químicos do SBG (Mussatto et al., 2006).
Tabela 2.4 Composição química da dreche (Mussatto et al., 2006)
COMPONENTE SBG (% peso seco) Celulose 16,8 Arabinoxileno 28,4 Lenhina 27,8 Proteínas 15,2 Lípidos Nd Cinza 4,6
A dreche contém, além destes constituintes, minerais, vitaminas e aminoácidos. O cálcio, o cobalto, o cobre, o ferro, o magnésio, o fósforo, o potássio, o selénio, o sódio são alguns dos minerais que fazem também parte da sua composição e estão presentes em concentrações abaixo de 0,5% (Mussatto et al, 2006).
2.5.3 Aplicações
Embora a dreche seja o principal desperdício no processo de fabrico da cerveja, tem recebido pouca atenção como um produto vendável. Este tipo de resíduos é, frequentemente, um problema ambiental. Contudo, devido à sua composição química pode ter valor como matéria-prima noutros processos. De seguida citam-se alguns sectores de actividade que podem incorporar a dreche para valorização.
Alimentação animal - até agora, a principal aplicação do grão seco da cevada tem sido na alimentação animal (principalmente para gado) devido ao elevado teor de proteínas e fibra. Alguns estudos demonstraram que o grão seco é um excelente ingrediente na alimentação de ruminantes, desde que combinado com uma fonte de nitrogénio barata, tal como a ureia, fornecendo todos os aminoácidos essenciais. Sendo
Descoloração de Corantes Azo em Reactores Anaeróbios Termófilos
25
um suplemento com elevado valor nutricional, estimula o aumento da produção de leite, sem afectar a fertilidade animal.
Se o grão seco é incorporado nas dietas alimentares do gado, o conteúdo total sólido de leite e a gordura aumentam. Contudo, a concentração de glucose, proteína, albumina, ureia, triglicerídeos, colesterol, fosfolípidos, sódio, potássio, cálcio, fósforo e magnésio, no plasma sanguíneo, não é afectada.
Até há algum tempo, o principal mercado para a dreche cervejeira era a alimentação do gado leiteiro, como já foi referido. No entanto, o facto de ser uma fonte de proteínas, fibras e energia, alargou o seu consumo para uma série de animais, incluindo aves domésticas, porcos e peixes.
Alguns investigadores avaliaram o SBG como uma possível substituição do farelo de arroz no regime alimentar dos peixes e observaram que aqueles que se alimentavam com farelo de arroz e 30% de grão de cevada tinham um aumento do peso corporal, quando comparados com aqueles que apenas ingeriam o farelo de arroz. De acordo com estes autores, o melhor desempenho no crescimento deveu-se ao aumento do conteúdo de proteínas e aminoácidos essenciais, fornecidos pelo grão seco da cevada (Mussatto et al, 2006).
Alimentação humana - devido ao seu relativo baixo custo e elevado valor nutritivo, o grão de cevada seco tem sido alvo de estudo por parte de empresas de flocos, biscoitos e aperitivos. Contudo, o grão é demasiado granular para adição directa na alimentação, sendo por isso necessário converte-lo primeiro a farinha. Farinha com elevado teor de proteína, preparada a partir do grão seco da cevada, foi incorporada, com êxito, num grande número de produtos de padaria, incluindo pão, bolos, biscoitos, mistura de cereais, etc. A adição do grão seco da cevada melhora o valor nutricional do pão. A adição de 10% do grão seco aumenta o teor de proteínas e de aminoácidos essenciais em 50 e 10%, respectivamente, e duplica o conteúdo de fibra relativamente aos valores obtidos para o pão tradicional, sem o grão seco da cevada. Estes pães têm menos 7% de calorias. A densidade calórica é cerca de metade da maioria dos cereais.
A ingestão do grão de cevada seco, ou produtos derivados, pode trazer benefícios para a saúde, como por exemplo, propiciam a diminuição de pedras vesiculares.
Quando se adicionou o grão seco da cevada à dieta dos ratos verificou-se uma diminuição da prisão de ventre e da diarreia. Estes resultados foram atribuídos ao
Descoloração de Corantes Azo em Reactores Anaeróbios Termófilos
26
conteúdo de proteína rica em glutamina e ao elevado conteúdo de polissacarídeos não celulósicos (arabinoxileno 20-47%) (Mussatto et al, 2006).
Produção de energia - outro importante sector de utilização da dreche, ou grão seco de cevada, é na produção de energia, efectuada ou por combustão directa, ou por fermentação. No processo de combustão, a dreche sofre desumidificação para que o teor de humidade seja inferior a 55%. Durante a combustão há emissão de poeiras, gases tóxicos que contêm óxidos de azoto e SO2.
O biogás é uma mistura de metano, 60-70%, dióxido de carbono e pequenas quantidades de nitrogénio e monóxido de carbono, que se pode recolher através da fermentação anaeróbia da semente da cevada. Divide-se em duas etapas, uma etapa hidrolítica e outra metanogénica. A primeira etapa ou seja, a hidrólise do material da fibra da dreche é em geral o passo controlador do metabolismo da degradação da dreche. A hidrólise é facilitada por um tratamento alcalino, conseguindo-se uma conversão de 86% de matéria seca, para um tempo de retenção no reactor de 8 dias. Pode ainda ser melhorada por um tratamento químico e térmico, com solução 0,2 M NaOH a 700C, ou por tratamento enzimático com fungos produtores de celulases, ou simplesmente por moagem.
Ezeonu e Okaka (1994) avaliaram o processo cinético e a eficiência da digestão anaeróbia, após a fermentação da dreche e obtiveram um rendimento total de 3476 cm3 de biogás /100g de dreche cervejeira, após 15 dias de digestão. Durante a etapa fermentativa e metanogénica, os organismos acidogénicos convertem macromoléculas complexas em ácidos gordos voláteis: acetato, butirato, propionato e álcoois. Posteriormente, as bactérias metanogénicas convertem estes compostos em metano (Mussatto et al, 2006).
A produção de biogás, permite a sua utilização nos processos industriais, como fonte de energia. Devido à crise energética mundial, a utilização de dreche na produção de biocombustíveis, constitui uma alternativa considerável, visto que é uma fonte de energia renovável. O metano, o seu principal constituinte, tem a propriedade de ser combustível e ter baixa solubilidade em água (Ezeonu, 1994; Okaka, 1994).
Bioadsorção – A dreche cervejeira pode funcionar como adsorvente, num mecanismo no qual ocorre transferência de massa de um composto de uma fase fluida
Descoloração de Corantes Azo em Reactores Anaeróbios Termófilos
27
(adsorvato), para uma sólida (adsorvente). Neste caso o adsorvido pode ser retido à superfície do sólido por interacções moleculares, nomeadamente forças de van der Waals e forças hidrofóbicas, dando-se a adsorção física. Se as interacções envolverem uma ligação química entre as moléculas do adsorvido e as moléculas da superfície do sólido, a adsorção ocorre por via química (Nunes, 2004).
Os adsorventes são normalmente utilizados na forma de pó ou de pequenos grânulos, de modo a proporcionarem uma elevada área específica de adsorção e consequentemente uma maior capacidade de remoção do adsorvato. Sendo a dreche um adsorvente de baixo custo, têm sido feitas investigações sobre a possibilidade de utilização quer na adsorção de metais pesados, quer de corantes (Low et al., 2000; Nunes, 2004).
As experiências mais utilizadas em adsorção relacionam a quantidade de adsorvato adsorvido por grama de adsorvente (q) e a concentração de equilíbrio de adsorvato (C), a temperatura constante (Kennedy e Cabral, 1993). Quando o equilíbrio termodinamico (da concentração de adsorvato) entre a solução e o adsorvente é alcançado não ocorre mais adsorção. Este equilíbrio é definido pelas concentrações de adsorvente e adsorvato no sistema tendo em conta as condições de temperatura e pH (Proctor e Toro-Vasquez, 1996).
De seguida são apresentados os dois modelos mais utilizados na explicação do processo de adsorção isotérmica, o modelo de Freundlich e o modelo de Langmuir. O primeiro modelo é empírico enquanto o segundo apresenta uma expressão teórica resultante do pressuposto de que as moléculas de adsorvato formam uma monocamada (Nunes, 2004).
Isotérmica de Langmuir – com o objectivo de interpretar o fenómeno de adsorção de gases Langmuir propôs um modelo baseado nos seguintes pressupostos (Atkins, 1986; Geankoplis, 2001):
• Todos os locais de adsorção são equivalentes entre si e a superfície é uniforme;
• As moléculas adsorvidas estão localizadas em locais específicos ou seja só se observa a formação de uma monocamada;
Descoloração de Corantes Azo em Reactores Anaeróbios Termófilos
28
• A capacidade de uma molécula ser adsorvida num determinado local é independente da ocupação dos locais vizinhos;
• No equilíbrio, a velocidade de adsorção é igual à velocidade de desorção.
Então, o equilíbrio dinâmico é dado por: Ka
A + S AS (2.7)
Kd
Ka representa a constante de velocidade para a adsorção e Kd representa a constante
de velocidade para a desorção. A velocidade de adsorção é proporcional à pressão parcial (p) de A e ao número de locais vagos N(1-Ɵ), em que N é o número total de locais e Ɵ designa a fracção de posições ocupadas na superfície.
dƟ/dt = Ka p >(1-Ɵ) (2.8)
A velocidade de modificação de Ɵ na desorção é proporcional ao número de locais ocupados, NƟ:
dƟ/dt = - Kd >Ɵ (2.9)
No equilíbrio a velocidade de adsorção é igual à velocidade de desorção, assim, resolvendo a equação resultante desta soma resulta a expressão da isotérmica de Langmuir (Atkins, 1986):
Ɵ = Kp / (1 + Kp) em que K = Ka / Kd (2..10)
Como se trata da adsorção de uma substância em solução a equação anterior assume a forma (Geankoplis, 2001):
q = (qmáx C)/(K + C) (2.11)
Descoloração de Corantes Azo em Reactores Anaeróbios Termófilos
29 onde:
q – concentração de soluto adsorvido por unidade de massa de adsorvente qmáx – concentração máxima de soluto adsorvido
C – concentração de equilíbrio do soluto em solução K – constante de equilíbrio para a adsorção
Após tratamento matemático da equação (2.11) obtém-se a expressão,
1/q = (K/CqMax ) + (1/qmáx) (2.12)
Esta expressão permite construir o gráfico 1/q versus 1/C de forma a obter-se o coeficiente angular e a ordenada na origem que permite determinar qmáx e K. Estes
parâmetros indicam, respectivamente, a área superficial do adsorvente e a intensidade do adsorvente (Nunes, 2004).
A isotérmica de Langmuir representa a adsorção ideal. Pois é bastante frequente os casos em estudo distanciarem-se desta equação. Tendo em conta as condições dadas para a aplicação deste modelo, a mais importante visa o facto de se poderem formar várias camadas de adsorção e os locais de adsorção serem energeticamente heterogéneos. Contudo, o modelo assume a existência da saturação do adsorvente, o que realmente parece acontecer na prática (Kennedy e Cabral, 1993).
Isotérmica de Freundlich – em 1924, Freundlich descreveu a adsorção de um adsorvato numa solução aquosa como sendo um equilíbrio reversível quando este era estabelecido em poucos segundos ou minutos a uma determinada temperatura (Proctor e Toro-Vasquez, 1996). A isotérmica de Freundlich é derivada da equação (2.10) por modificação das suposições de Langmuir:
Ɵ = Kf pn (2.13)
Kf e n são constantes empíricas e p é a pressão parcial do adsorvato. O parâmetro n