O papel da membrana celular na terapia do cancro com novos compostos de ruténio
Texto
Imagem
![Figura 6. Fórmula estrutural dos complexos de Ruténio (III): NAMI-A (trans-[RuCl 4 (DMSO)(Im)]ImH, KP1019 (trans-[RuCl 4 (Ind) 2 ]IndH) e o NKP-1339 (Na[trans-[RuCl 4 (Ind) 2 ]IndH]) – adaptado de [21]](https://thumb-eu.123doks.com/thumbv2/123dok_br/15216063.1019928/24.892.110.783.715.1020/figura-fórmula-estrutural-complexos-ruténio-nami-trans-adaptado.webp)
![Figura 7. Fórmula estrutural do complexo OR6 e dos seus ligandos pbt e bpy – adaptado de [25]](https://thumb-eu.123doks.com/thumbv2/123dok_br/15216063.1019928/25.892.172.692.866.1108/figura-fórmula-estrutural-complexo-or-seus-ligandos-adaptado.webp)
![Figura 8. Fórmula estrutural do complexo S8 e S10 e dos seus ligandos Salan-4-MeO e Salan-5-MeO, respetivamente, e do PPh 3 – adaptado de [25]](https://thumb-eu.123doks.com/thumbv2/123dok_br/15216063.1019928/27.892.125.767.653.1012/figura-fórmula-estrutural-complexo-ligandos-salan-respetivamente-adaptado.webp)
Documentos relacionados
O 6º ano do Mestrado Integrado em Medicina (MIM) é um estágio profissionalizante (EP) que inclui os estágios parcelares de Medicina Interna, Cirurgia Geral,
Realizar a manipulação, o armazenamento e o processamento dessa massa enorme de dados utilizando os bancos de dados relacionais se mostrou ineficiente, pois o
Por meio dos registros realizados no estudo de levantamento e identificação de Felinos em um remanescente de Mata atlântica, uma região de mata secundária
confecção do projeto geométrico das vias confecção de projeto de drenagem, dimensionamento e detalhamento de 20 lagos de retenção, projeto de pavimentação e
Nesse contexto, a análise numérica via MEF de vibrações sísmicas induzidas por detonações se mostra como uma metodologia que pode contribuir significativamente
To demonstrate that SeLFIES can cater to even the lowest income and least financially trained individuals in Brazil, consider the following SeLFIES design as first articulated
Fonte: elaborado pelo autor. Como se pode ver no Quadro 7, acima, as fragilidades observadas após a coleta e a análise de dados da pesquisa nos levaram a elaborar
Ao analisar o conjunto de empresas de dois segmentos da BM&FBOVESPA –Energia Elétrica e Bancos –, verifi cando as métricas fi nanceiras de rentabilidade e risco Nunes, Nova
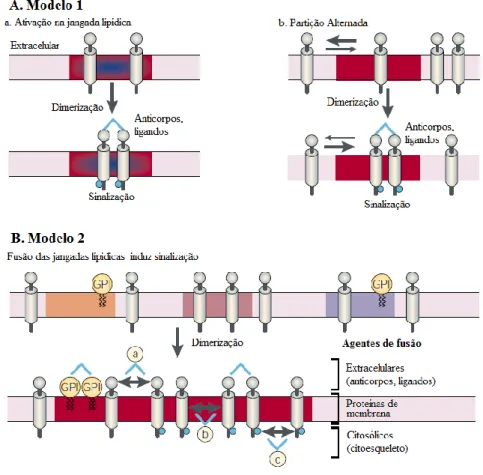
![Figura 9. Diagramas esquemáticos de modelos de estrutura de membranas biológicas. (A) Modelo do Mosaico Fluido e (B) modelo do mosaico fluido modificado – adaptado de [29]](https://thumb-eu.123doks.com/thumbv2/123dok_br/15216063.1019928/28.892.152.759.630.890/diagramas-esquemáticos-estrutura-membranas-biológicas-mosaico-modificado-adaptado.webp)
![Figura 11. Fórmula estrutural dos glicerofosfolípidos utilizados neste trabalho: DOPC, POPC, DPPC e POPE (adaptado de [34])](https://thumb-eu.123doks.com/thumbv2/123dok_br/15216063.1019928/30.892.113.751.259.432/figura-fórmula-estrutural-glicerofosfolípidos-utilizados-neste-trabalho-adaptado.webp)
![Figura 14. Representação das fases lamelares mais comuns: fase gel, fase liquido-desordenado (L d ) e fase liquido-ordenado (L o ), em que representa o colesterol – adaptado de [37]](https://thumb-eu.123doks.com/thumbv2/123dok_br/15216063.1019928/33.892.147.743.110.274/figura-representação-lamelares-desordenado-ordenado-representa-colesterol-adaptado.webp)
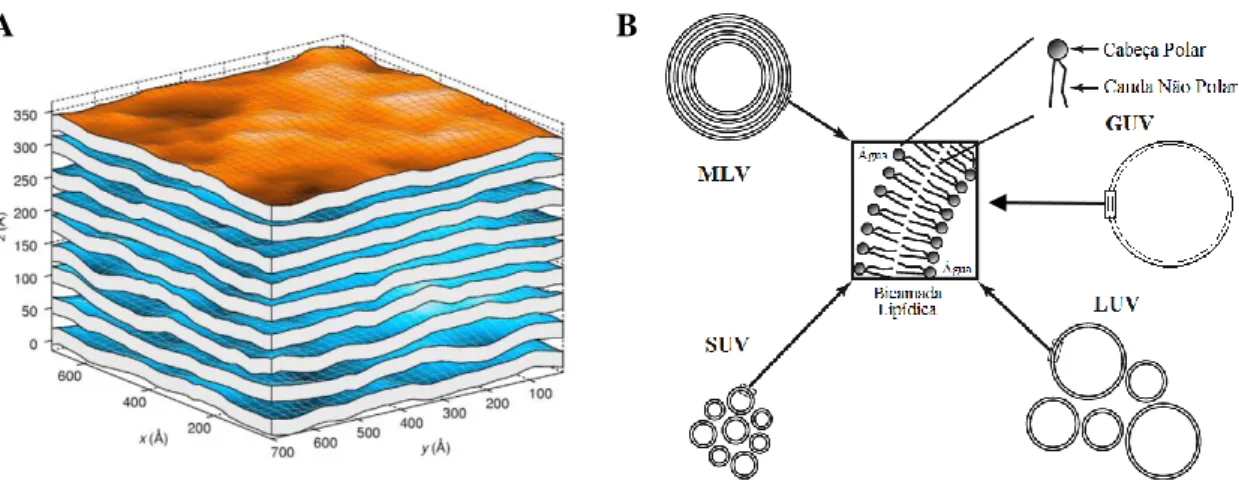
![Figura 18. Representação da complexidade da membrana celular e dos sistemas modelo que mimetizam as características da membrana celular – adaptado de [58]](https://thumb-eu.123doks.com/thumbv2/123dok_br/15216063.1019928/39.892.127.772.239.483/representação-complexidade-membrana-sistemas-mimetizam-características-membrana-adaptado.webp)