DEPARTAMENTO DE F´ISICA
PROGRAMA DE P ´OS-GRADUAC¸ ˜AO EM F´ISICA
KEILLA FAC¸ ANHA SILVA
ESTUDO DO POLIMORFISMO E DESENHO DE COCRISTAIS DOS ANTI-HELMINTICOS RICOBENDAZOL E ALBENDAZOL
ESTUDO DO POLIMORFISMO E DESENHO DE COCRISTAIS DOS ANTI-HELMINTICOS RICOBENDAZOL E ALBENDAZOL
Disserta¸c˜ao de Mestrado apresentada ao Pro-grama de P´os-Gradua¸c˜ao em F´ısica da Uni-versidade Federal do Cear´a, como requisito parcial para a obten¸c˜ao do T´ıtulo de Mes-tre em F´ısica. ´Area de Concentra¸c˜ao: F´ısica da Mat´eria Condensada.
Orientador: Prof. Dr. Alejandro Pedro Ayala.
Biblioteca Universitária
Gerada automaticamente pelo módulo Catalog, mediante os dados fornecidos pelo(a) autor(a)
S58e Silva, Keila Façanha.
Estudo do polimorfismo e desenho de cocristais dos anti-helminticos Ricobendazol e Albendazol / Keila Façanha Silva. – 2016.
79 f. : il.
Dissertação (mestrado) – Universidade Federal do Ceará, Centro de Ciências, Programa de Pós-Graduação em Física, Fortaleza, 2016.
Orientação: Prof. Dr. Alejandro Pedro Ayala.
ESTUDO DO POLIMORFISMO E DESENHO DE COCRISTAIS DOS ANTI-HELMINTICOS RICOBENDAZOL E ALBENDAZOL
Disserta¸c˜ao de Mestrado apresentada ao Pro-grama de P´os-Gradua¸c˜ao em F´ısica da Uni-versidade Federal do Cear´a, como requisito parcial para a obten¸c˜ao do T´ıtulo de Mes-tre em F´ısica. ´Area de Concentra¸c˜ao: F´ısica da Mat´eria Condensada.
Aprovada em 15 / 12 / 2016 .
BANCA EXAMINADORA
Prof. Dr. Alejandro Pedro Ayala (Orientador)) Universidade Federal do Cear´a (UFC)
Prof. Dr. Jos´e Alves de Lima Junior Universidade Federal do Cear´a (UFC)
meu namorado e a todos que acreditaram e contribu´ıram para
A Deus, por todas as bˆen¸c˜aos que tenho recebido em minha toda vida, inclusive a concretiza¸c˜ao desse trabalho.
Aos meus familiares: pai, m˜ae e irm˜aos, que mesmo longe sempre estiveram comigo em pensamento. Sendo que tudo que fa¸co ´e por eles.
Ao meu namorado por est´a ao meu lado em todos os momentos, j´a se v˜ao mais de 5 anos de muito companheirismo e muitas conquistas, pessoa mais que especial que Deus colocou na minha vida.
Ao professor Dr. Alejandro Pedro Ayala, pela maravilhosa orienta¸c˜ao, incen-tivo e apoio durante todas as etapas do Mestrado. Agrade¸co pela constante paciˆencia e disposi¸c˜ao ao longo desses dois anos. Melhor orientador n˜ao existe, ´e minha grande inspira¸c˜ao de profissional e de ser humano, foi uma honra trabalhar com vocˆe e uma satisfa¸c˜ao enorme dizer que fui sua orientanda, muit´ıssimo obrigada.
Aos colegas de grupo de pesquisa por estarem sempre dispostos a ajudarem e compartilhar seus conhecimentos, a come¸car pelo Bruno Sousa que sempre esteve disposto a me ajudar nos laborat´orios e nas d´uvidas quotidianas, sentirei muita falta de sua amizade e de nossas conversas na sala 8, foram dois anos de muita aprendizagem e muitas alegrias, o levarei sempre como uma maravilhosa lembran¸ca de Fortaleza.
A Yara Santiago, por sempre carinhosamente me ajudar em tudo que fosse necess´ario e pela pessoa especial e iluminada que ´e, uma pessoa que facilmente pode-se atribuir muitas qualidades, aprendi demais com vocˆe, muito obrigada por sua amizade. Mais uma boa lembran¸ca de Fortaleza.
A J´essica Fonseca, que me acolheu t˜ao bem, n˜ao s´o no grupo, mas em tudo, basicamente me ensinou a usar todos os equipamentos e as atividades do laborat´orio de crescimento, agrade¸co por todos os ensinamentos e pela amizade, a levarei para sempre comigo.
A Laura Vidal por seu aux´ılio em muitos momentos no laborat´orio, por tirar algumas d´uvidas no ˆambito da farm´acia e pela pessoa especial que se tornou para mim.
Agrade¸co tamb´em pela maravilhosa acolhida em sua casa, jamais esquecerei, nunca fui t˜ao bem recebida em uma casa que n˜ao fosse a dos meus pais, me senti como se fosse da fam´ılia, meus sinceros agradecimentos.
A Silmara Alves por tirar algumas d´uvidas de qu´ımica e por tornarem os nossos dias mais alegres e radiantes com sua presen¸ca. Gostaria de deixar um agradecimento especial a Luciana Nogueira pela pessoa encantadora que ´e, e que esteve comigo nos primeiros momentos no laborat´orio e por compartilhar o que sabia comigo.
Agrade¸co pela amizade de Beatriz Bezerra, Anacl´ecia e F´abio Medeiros, foi bom conhecer vocˆes
Agrade¸co a todos do grupo de pesquisa pelas pessoas especiais que s˜ao, e pelos momentos maravilhosos que passamos juntos, vocˆes s˜ao pessoas inesquec´ıveis e peculiares. N˜ao poderia deixar de agradecer ao Gelson Rodrigues por seu grande apoio e incentivo em muitos momentos. Ao Rodrigo Almeida, companheiro ao longo desses 6 anos de amizade, ao Raul que ajudou durante o processo de sele¸c˜ao do mestrado, foi uma ajuda de extrema importˆancia, ao Stanley que ´e uma esp´ecie de “Google da F´ısica”.
valia na minha vida, sem ela n˜ao teria feito F´ısica e consequentemente n˜ao teria chegado at´e aqui. O que vocˆe fez por mim h´a 6 anos jamais ser´a esquecido.
Agrade¸co a minha madrinha que sempre me desejou o melhor e por ter come-morado e acompanhado cada conquista da minha vida.
Agrade¸co a universidade de Limerick na Irlanda pela parceria, no qual possi-bilitou a realiza¸c˜ao de uma parte do trabalho.
A universidade de Ros´ario na Argentina, por ter cedido as amostras no qual trabalhei.
Ao departamento de F´ısica da Universidade Federal do Cear´a (UFC) pela maravilhosa receptividade. N˜ao existe lugar melhor para estudar.
A Coordena¸c˜ao de Aperfei¸coamento de Pessoal de N´ıvel Superior (CAPES) pela bolsa que foi de grande importˆancia durante esses dois anos de Mestrado.
As caracter´ısticas f´ısico-qu´ımicas dos f´armacos est˜ao diretamente relacionadas `a sua efic´acia terapˆeutica, e estas, por sua vez, est˜ao vinculadas ao arranjo estrutural apre-sentado pelo f´armaco, o qual ´e oriundo das diferentes conforma¸c˜oes e/ou intera¸c˜oes intra e intermoleculares que definem o empacotamento cristalino das mol´eculas nas diferentes formas s´olidas. Desta forma, conhecer e controlar estas caracter´ısticas ´e de fundamental importˆancia na ´area farmacˆeutica. Neste contexto, o presente trabalho aplicou diferentes estrat´egias envolvendo a engenharia de cristais, visando a melhora das propriedades bio-farmacˆeuticas dos f´armacos ricobendazol e albendazol. No caso do ricobendazol, cristais foram obtidos a partir da t´ecnica de evapora¸c˜ao lenta e fazendo uso da difra¸c˜ao de raio X de monocristal a estrutura cristalina do f´armaco foi elucidada, bem como uma cuida-dosa caracteriza¸c˜ao no estado s´olido foi realizada. O ricobendazol cristaliza no sistema monocl´ınico pertencente ao grupo espacial P21/c. A estrutura cristalina ´e composta por quatro mol´eculas por cela unit´aria (Z=4), acomodando uma mol´ecula na unidade as-sim´etrica (Z’ =1), e possuindo os seguintes parˆametros de rede: a = 7.5960(16) ˚A, b = 9.3047(18) ˚A, c= 18.726(4) ˚A e β = 82,198(5)o
. J´a para o albendazol o objetivo foi investigar as formas polim´orficas reportadas na literatura, bem como buscar novas fases cristalinas do f´armaco. Uma vez que encontra-se reportada duas formas polim´orficas, as formas I e II que est˜ao enantiotropicamente relacionadas. Entretanto, conclu´ımos que h´a trˆes formas cristalinas para o albendazol, no qual a forma I refere-se ´a forma comercial-mente distribu´ıda que, quando recristalizada em metanol, obt´em-se um terceiro polimorfo, a forma III. Sendo assim, realizamos a caracteriza¸c˜ao das formas polim´orficas do albenda-zol, fazendo um estudo comparativo entre os polimorfos o que nos permitiu investigar sua estabilidade termodinˆamica. Outra estrat´egia aplicada aos f´armacos abrangeu o desen-volvimento de cristais multicomponentes com diversos coformadores. Ou seja, realizamos uma busca por co-cristais para ambos os f´armacos atrav´es das t´ecnicas de moagem as-sistida por solvente e slurry, usando uma variedade de coformadores. Resultados promis-sores foram obtidos com ´acido ox´alico, ´acido salic´ılico, ´acido 2,6-dihidroxibenzoico, ´acido 3,5-dihidroxibenzoico e ´acido 3,5- dinitroxibenzoico. Deste modo, obtivemos poss´ıveis co-cristais para o ricobendazol e o albendazol, sendo estes resultados in´editos para os referidos f´armacos.
The physico-chemical properties of drugs are directly related to their therapeutic efficacy, and these, in turn, are linked to the structural arrangement presented by the drug, which comes from the different conformations and/or intra and intermolecular interactions that define the crystalline packing of molecules in the different solid forms. In this way, knowing and controlling these characteristics is of fundamental importance in the pharmaceutical area. In this context, the present work applied different strategies involving crystal en-gineering, aiming at the improvement of the biopharmaceutical properties of the drugs: ricobendazole and albendazole. In the case of ricobendazole, crystals were obtained from the slow evaporation technique and, making use of single crystal x-ray diffraction, the crystalline structure of the drug has been clarified, as well as a careful characterization in the solid state was performed. Ricobendazole crystallizes in a monoclinic system belon-ging to P21/c space group. The crystalline structure is composed of four molecules per unit cell (Z = 4), accommodating a molecule in the asymmetric unit (Z = 1), and posses-sing the following lattice parameters: a = 7.5960 (16) ˚A, b = 9.3047 (18) ˚A, c = 18,726 (4) ˚
A, andβ = 82.198 (5)o
. For albendazole the objective was to investigate the polymorphic forms reported in the literature, as well as seek new crystalline phases of the drug. There are reported two polymorphic forms, forms I and II, which are enantiotropically related. However, we found that there are three crystalline forms for albendazole, where form I refers to the commercially distributed form, which, when recrystallized in methanol yields a third polymorph, form III. Therefore, the characterization of the polymorphic forms of albendazole was performed, making a comparative study between polymorphic crystal structures which allowed us to investigate their thermodynamic stability. Another stra-tegy applied to drugs covered the development of multi-component crystals with several coformers. Thus, we do a search for co-crystals for both drugs through the solvent-assisted milling and slurry techniques, using a variety of coformers. Promising results were ob-tained with oxalic acid, salicylic acid, 2.6-dihydroxybenzoic acid, 3.5- dihydroxybenzoic acid and 3.5- dinitroxybenzoic acid. In this way, we obtained possible co-crystals for ricobendazole and albendazole, being these unpublished results for these drugs.
Figura 1 – Diferentes empacotamentos da mol´ecula do f´armaco na estrutura cristalina. 18
Figura 2 – Forma¸c˜ao de solvatos de compostos farmacˆeuticos. . . 19
Figura 3 – F´armaco carregado mais ´ıon reagente, formando sais farmacˆeuticos. . . . 20
Figura 4 – F´armaco mais mol´ecula neutra, formando co-cristais farmaˆeuticos. . . 21
Figura 5 – Mol´eculas de APIs distribu´ıdas de formas aleat´orias, caracterizando um material amorfo. . . 21
Figura 6 – Estrutura molecular do albendazol e do sulf´oxido de albendazol. . . 30
Figura 7 – Representa¸c˜ao da cela unit´aria do Ricobendazol. Formando, assim, agre-gados moleculares ao longo da rede. . . 31
Figura 8 – Representa¸c˜ao ORTEP da unidade assim´etrica do RBZ mostrando os ´atomos rotulados e 50% de probabilidade de elipsoides. . . 31
Figura 9 – Intera¸c˜oes intramolecular e intermolecular descritas na tabela 2, com des-taque para o d´ımero formado. . . 33
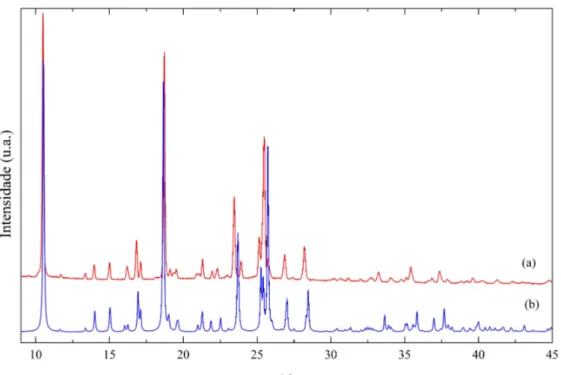
Figura 10 –Difratogramas referentes `as amostras de RBZ: (a) padr˜ao experimental e em (b) padr˜ao calculado. . . 35
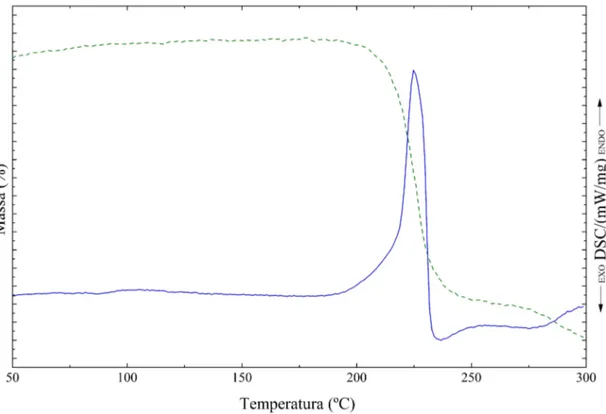
Figura 11 –Comportamento t´ermico do RBZ recristalizado em metanol. . . 36
Figura 12 –Espectro de IR do ricobendazol. . . 37
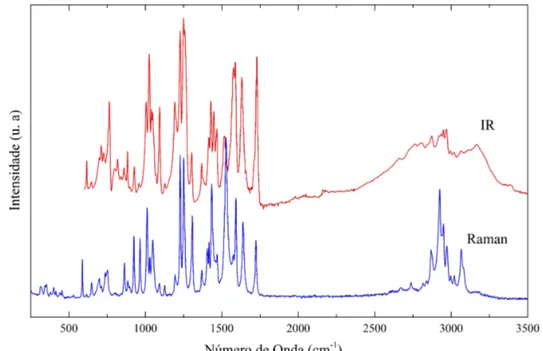
Figura 13 –Compara¸c˜ao dos espectros FTIR e FT-Raman referentes `a amostra de ricobendazol. . . 37
Figura 14 –Imagens referentes ao cristal de RBZ via microscopia ´optica. . . 38
Figura 15 –Fotomicrografias obtidas por MEV referentes `a amostra RBZ. . . 38
Figura 16 –Estrutura qu´ımica do Albendazol. . . 40
Figura 17 –Diagrama de Energia Livre versus Temperatura para um Sistema Enan-tiotr´opico. G representa a energia livre de Gibbs e H ´e a entalpia. Adap-tado de [12] . . . 42
Figura 18 –Diagrama de Energia Livre versus Temperatura para um sistema Mo-notr´opico. . . 43
Figura 19 –Unidade assim´etrica da forma descrita por [49]. . . 44
Figura 20 –Unidade assim´etrica da forma II descrita por [32]. . . 44
Figura 21 –Vista ao longo do eixo b dos empacotamentos cristalinos das duas formas (a) BOGFRZ e (b) SUTWIU. . . 44
calculado e em c) forma I. Figura retirada de Pranzo et al, 2011. . . 46 Figura 24 –Curvas de DSC que demonstram a transforma¸c˜ao polim´orfica da forma
III para a forma I. . . 48 Figura 25 –Formas polim´orficas do albendazol. Forma I (Vermelha), no qual a mesma
corresponde a nossa mat´eria prima e por sua vez a forma III (azul) ´e a recristaliza¸c˜ao em metanol. . . 48 Figura 26 –An´alise em microscopia de hot-state realizada na forma III mostrando
que ocorre uma nova fus˜ao seguida de uma recristaliza¸c˜ao come¸cando em 190o
C, cujo o processo ´e dado em cima das seguintes temperaturas, em 190o
C in´ıcio da fus˜ao, em 216o
C a recristaliza¸c˜ao total e em seguida
come¸ca o processo de decomposi¸c˜ao do composto. . . 49 Figura 27 –Compara¸c˜ao das curvas de DSC/TG entre os dois polimorfos do
alben-dazol, evidenciando a distin¸c˜ao entre ambas. . . 49 Figura 28 –Curvas de DSC das formas polim´orficas mostradas por Pranzo. Em a)
forma I, em b) recristaliza¸c˜ao em DMF e em c) recristaliza¸c˜ao em meta-nol, ambas correspondentes `a forma II. Figura retirada de Pranzo, 2011.. 50 Figura 29 –Espectro de FTIR das formas I e III do albendazol. . . 51 Figura 30 –Espectro FTIR das formas I e III do albendazol. Regi˜ao ampliada, na
faixa entre 2400 a 3500cm−1. . . 52 Figura 31 –Espectro FTIR das formas I e III do albendazol. Regi˜ao ampliada, na
faixa entre 1500 a 1800 cm−1. . . 53 Figura 32 –Espectro FTIR das formas I e III do albendazol. Regi˜ao ampliada, na
faixa entre 1200 a 1500 cm−1. . . 54 Figura 33 –Espectro FTIR das formas I e III do albendazol. Regi˜ao ampliada, na
faixa entre 2400 a 2450 cm−1. . . 55 Figura 34 –Sele¸c˜ao de coformadores a partir do software ConQuest 1.18 da CSD. . . 58 Figura 35 –Difratogramas comparando as amostras obtidas pela t´ecnica de moagem
assistida por solvente e os insumos de partida. Onde temos em a) ´acido glut´arico, em b) albendazol e em c) podemos observar a mistura de fase ap´os a moagem. . . 60 Figura 36 –Difratogramas comparando as amostras obtidas pela t´ecnica de moagem
de moagem assistida por solvente e os insumos de partida. Onde temos em a) RBZ: ´Acido ox´alico-mistura f´armaco/conformador, em b) ´acido
ox´alico e em c) amostra de ricobendazol. . . 62 Figura 38 –Difratogramas comparando as amostras obtidas por cristaliza¸c˜ao em
sus-pens˜ao e os isumos de partida. Ou seja, na parte superior da figura s˜ao os cocristais formados, f´armaco + coformador, no meio s˜ao os coformadores
no casso, SAA, 2,6DBA e 3,5DTA e na parte inferior o ricobendazol na forma pura. . . 64 Figura 39 –Curvas DSC comparando as amostras obtidas por slurry e os insumos de
partida. Onde temos na parte superior as misturas RBZ + conformador
processados, no meio os conformadores, ou seja, SAA, 2,6DBA e 3,5DTA e em baixo a amostra de ricobendazol. . . 66 Figura 40 –Espectro de infravermelho para os co-cristais de ricobendazol. Na parte
de cima da figura s˜ao os sistemas cristalinos ap´os processamento, isto ´e,
RBZ+coformadores, no meio os coformadores usados no processamento, novamente SAA, 3,5 DTA e 2,6 DBA e logo abaixo apenas ricobendazol. 67 Figura 41 –Difratrogramas da amostra obtida por meio da mistura de ABZ:3,5DTA.
Onde temos em a) 3,5-DTA, em b) ABZ e em c) a mistura f´armaco
coformador. . . 68 Figura 42 –Curvas de DSC da amostra obtida por meio de ABZ:3,5DTA. . . 69 Figura 43 –Espectro de infravermelho da amostra obtida por meio da mistura entre
Tabela 1 – Parˆametros cristalogr´aficos do RBZ . . . 32 Tabela 2 – Liga¸c˜oes de hidrogˆenio que contribuem para o arrajamento
1 INTRODUC¸ ˜AO . . . 15
1.1 Anti-Helm´ınticos Benzimidaz´olicos . . . 16
1.2 A Importˆancia do Estudo das Formas S´olidas na Ind´ustria Far-macˆeutica . . . 17
1.3 Formas Cristalinas de F´armacos . . . 18
1.3.1 Polimorfo . . . 18
1.3.2 Solvatos/Hidratos . . . 19
1.3.3 Sais . . . 19
1.3.4 Co-cristais . . . 20
1.3.5 Amorfo . . . 21
2 M´ETODOS EXPERIMENTAIS . . . 23
2.1 Difra¸c˜ao de Raio X . . . 23
2.1.1 Difra¸c˜ao de Raio X de P´o (DRXP) . . . 23
2.1.2 Difra¸c˜ao de Raios X de Monocristal (DRXM) . . . 24
2.2 An´alise T´ermica . . . 24
2.2.1 Termogravimetria e Calorimetria Explorat´oria Diferencial . . 24
2.3 Espectroscopia Vibracional . . . 25
2.4 Microscopia ´Optica . . . 27
2.5 Ativa¸c˜ao Mecanoqu´ımica . . . 27
3 RICOBENDAZOL . . . 29
3.1 Processo de cristaliza¸c˜ao . . . 30
3.2 Descri¸c˜ao da Estrutura Cristalina . . . 30
3.3 Caracteriza¸c˜ao em estado s´olido do Ricobendazol . . . 34
3.3.1 Difra¸c˜ao de Raio X de P´o . . . 34
3.3.2 Calorimetria Explorat´oria Diferencial e Termogravimetria . . 35
3.3.3 Espectroscopia Vibracional Raman e Infravermelho (IR) . . . 36
3.3.4 Microscopia ´Optica e Microscopia Eletrˆonica de Varredura . . 38
4 POLIMORFISMO DO ALBENDAZOL . . . 40
4.1 Classifica¸c˜ao dos Polimorfos . . . 41
4.2 Descri¸c˜ao dos polimorfos do Albendazol . . . 43
4.3 Caracteriza¸c˜ao dos polimorfos do Albendazol . . . 47
5.1 Materiais e M´etodos . . . 57
5.2 S´olidos obtidos via t´ecnica de moagem assistida por solvente (MAS) . . . 59
5.3 Caracteriza¸c˜ao no estado s´olido obtido via cristaliza¸c˜ao por sus-pens˜ao (slurry) . . . 63
5.3.1 Co-cristais do Ricobendazol . . . 64
5.3.2 Co-cristal do Albendazol . . . 67
6 CONCLUS ˜OES . . . 71
7 ANEXO A . . . 74
1 INTRODUC¸ ˜AO
Pode-se dizer que um dos fatores que definem as propriedades farmacol´ogicas de um f´armaco ´e o arranjo estrutural que ele apresenta. Assim, t˜ao importante quanto a s´ıntese de novos f´armacos ´e a sua caracteriza¸c˜ao estrutural, j´a que sua conforma¸c˜ao pode estar diretamente relacionada a propriedades f´ısico-qu´ımicas, tal como a solubilidade e biodisponibilidade. A partir desse conhecimento torna-se necess´ario que caracter´ısticas como, distˆancias interatˆomicas, ˆangulos de liga¸c˜ao, ˆangulos de tor¸c˜ao, configura¸c˜ao re-lativa da mol´ecula, entre outros aspectos importantes da geometria molecular, sejam revelados e analisados. Devido a importˆancia desse tipo de estudo, mais pesquisas nesse sentido precisam ser realizadas, com o intuito de correlacionar estrutura e a¸c˜ao, e assim ampliar o campo de vis˜ao.
Nesse contexto, o presente trabalho tem por objetivo estudar dois f´armacos da classe dos anti-helm´ınticos, Ricobendazol (RBZ) e Albendazol (ABZ), ambos deriva-dos benzimidaz´olicos de largo espectro. Os anti-helm´ınticos, tamb´em conhecideriva-dos como verm´ıfugos, constituem uma classe de f´armacos utilizados na preven¸c˜ao e tratamento de diferentes parasitoses, sendo o albendazol largamente empregado para tratamento de verminoses, e o ricobendazol, tamb´em chamado de sulf´oxido de albendazol por ser um me-tabolito ativo do albendazol, um f´armaco amplamente utilizado em medicina veterin´aria. Inicialmente, a ideia deste trabalho consistiu na determina¸c˜ao da estrutura cristalina do ricobendazol, uma vez que n˜ao se encontra reportada na literatura, bem como a caracteriza¸c˜ao de propriedades f´ısico-qu´ımicas relevantes. Portanto, objetivou-se a obten¸c˜ao de um monocristal que possibilitasobjetivou-se a completa elucida¸c˜ao estrutural do f´armaco pela t´ecnica de difra¸c˜ao de raios X de monocristal (DRXM), sendo os mono-cristais obtidos a partir da recristaliza¸c˜ao do ricobendazol em solventes como metanol, com caracteriza¸c˜ao adicional realizada por t´ecnicas de difra¸c˜ao de raios x de p´o (DRXP), an´alise t´ermica e espectroscopia vibracional.
polimorfo foi encontrado para o RBZ. No caso do albendazol encontram-se reportadas na literatura duas formas polim´orficas, e um dos objetivos deste trabalho foi evidenci´a-las, comprov´a-las e caracteriz´a-las. Entretanto, durante nossas buscas foi obtida uma nova fase cristalina, tornando-se dessa forma o principal sujeito de investiga¸c˜ao para o ABZ.
Uma proposta em andamento neste trabalho ´e a busca por co-cristais, onde destaca-se a importˆancia desse diagn´ostico, devido a obten¸c˜ao de co-cristais apresentar-se como alternativa para produ¸c˜ao de novas formas s´olidas vi´aveis. A co-cristaliza¸c˜ao ´e uma t´ecnica que permite a cristaliza¸c˜ao de dois ou mais compostos em ´unica fase cristalina, propiciando oportunidades no desenvolvimento de medicamentos por modificar proprie-dades como a solubilidade e a estabilidade de f´armacos. Esta t´ecnica enquadra-se como forma racional de otimiza¸c˜ao de ativos farmacˆeuticos com baixa biodisponibilidade pelo aperfei¸coamento de suas propriedades f´ısico-qu´ımicas [1]. Adequados a estes prop´ositos, o ricobendazol e o albendazol, representam modelos para estes estudos, uma vez que apresentam reduzida solubilidade aquosa. Nesse sentido, foi realizada uma busca por co-cristais para ambos os f´armacos e consequentemente a caracteriza¸c˜ao dos s´olidos obtidos. Dessa forma, o presente trabalho pretende fornecer informa¸c˜oes que permitam a melhor compreens˜ao estrutural e das propriedades f´ısico-qu´ımicas alusivas aos compos-tos estudados. Visando uma melhor compreens˜ao, a disserta¸c˜ao foi dividida em cinco cap´ıtulos. Na qual a revis˜ao da literatura est´a apresentada ainda neste cap´ıtulo, ou seja, no cap´ıtulo I. O cap´ıtulo II exp˜oe sobre todas as t´ecnicas experimentais usadas durante o trabalho. J´a o cap´ıtulo III apresenta a elucida¸c˜ao da estrutura cristalina do ricobendazol, bem como sua caracteriza¸c˜ao. No cap´ıtulo IV abordamos o polimorfismo do albendazol. E por fim no cap´ıtulo V trataremos da busca feita por cristais multicomponentes para ambos os f´armacos.
1.1 Anti-Helm´ınticos Benzimidaz´olicos
1.2 A Importˆancia do Estudo das Formas S´olidas na Ind´ustria Farmacˆeutica Segundo a Lei no
5.991, de 17 de dezembro de 1973, que disp˜oe sobre o Controle Sanit´ario do Com´ercio de Drogas, Medicamentos, Insumos Farmacˆeuticos e Correlatos, os medicamentos consistem em produtos farmacˆeuticos que s˜ao utilizados com finalidade profil´atica, curativa, paliativa ou para fins de diagn´ostico. Para que um medicamento chegue ao mercado ´e necess´ario que se apresentem `as agˆencias regulat´orias dados de seguran¸ca e efic´acia [4].
Os medicamentos em sua maioria s˜ao compostos por f´armacos e excipientes. Por defini¸c˜ao, os f´armacos s˜ao substˆancias que possuem algum efeito farmacol´ogico, sendo assim usados nos medicamentos, por sua vez, os excipientes farmacˆeuticos s˜ao substˆancias inclu´ıdas em um sistema de libera¸c˜ao de f´armacos para auxiliar durante o processo de manufatura, o qual pode proteger algumas de suas propriedades tal como a estabilidade e tamb´em aumentar a aceitabilidade do paciente, ocorrendo dessa forma a seguran¸ca e o efeito terapˆeutico do f´armaco durante seu uso e estoque[5].
As formas farmacˆeuticas mais difundidas no meio farmacˆeutico s˜ao as s´olidas, devido a sua estabilidade, facilidade de manuseio, elevada ades˜ao por parte dos pacientes, economia na formula¸c˜ao e f´acil distribui¸c˜ao [6]. Entendemos como s´olidos cristalinos aque-les que possuem uma estrutura ordenada em virtude dos arranjos regulares de ´atomos, mol´eculas ou ´ıons que as constituem, onde estes elementos est˜ao dispostos em posi¸c˜oes fixas no espa¸co, arranjados de uma forma peri´odica em trˆes dimens˜oes, cujas posi¸c˜oes ocu-padas seguem uma ordena¸c˜ao que se repete para longas distancias. Em contrapartida nos s´olidos amorfos ou s´olidos n˜ao cristalinos, seus ´atomos, mol´eculas ou ´ıons n˜ao apresentam uma organiza¸c˜ao de longo alcance.
A efic´acia terapˆeutica de cada f´armaco est´a diretamente ligada com suas ca-racter´ısticas no estado s´olido. Dessa forma, uma compreens˜ao completa das rela¸c˜oes entre as estruturas f´ısicas e as propriedades dos s´olidos farmacˆeuticos ´e extremamente importante no processo de desenvolvimento de um novo f´armaco. Os compostos far-macˆeuticos podem apresentar numerosas formas s´olidas, as quais possuem diferentes pro-priedades f´ısico-qu´ımicas, entre elas a solubilidade, estabilidade e biodisponibilidade [7]. No entanto, a grande maioria destes compostos n˜ao possuem propriedades moleculares altamente desej´aveis, ou seja, n˜ao possuem potencial m´aximo de desempenho em suas atividades biol´ogicas.
uma substˆancia incluem, cor, solubilidade, forma cristalina, absor¸c˜ao de ´agua e proprie-dades de n˜ao absor¸c˜ao, tamanho de part´ıcula, dureza, caracter´ısticas secantes, fluxo e a capacidade de ser filtrada, compressibilidade e densidade. As diferentes formas s´olidas po-dem ter pontos de fus˜ao, propriedades espectrais, e estabilidade termodinˆamica diferentes. Em um f´armaco, varia¸c˜oes dessas propriedades podem conduzir `as diferentes velocidades de dissolu¸c˜ao, absor¸c˜ao oral e biodisponibilidade. No qual, a ´ultima refere-se `a quantidade absorvida de um f´armaco, a partir de sua forma farmacˆeutica, e `a velocidade pela qual esse processo ocorre [8].
A maioria dos f´armacos existem em diferentes formas s´olidas como polimorfos, solvatos, hidratos, sais e co-cristais. Escolher a melhor forma cristalina de um f´armaco ´e um passo essencial do desenvolvimento de um medicamento, uma vez que esta pode impactar significativamente na sua performance [6]. Assim ´e de fundamental importˆancia entender cada uma dessas formas s´olidas.
1.3 Formas Cristalinas de F´armacos
Como descrito anteriormente, os ingredientes farmacˆeuticos ativos (active phar-maceutical ingrediente, API) ou f´armaco, podem existir em diversas formas s´olidas. Deste modo, os s´olidos amorfos e cristalinos podem ser classificados como monocompetentes, quando possuem apenas uma substˆancia, ou s´olidos multicomponentes, quando possuem mais de uma substˆancia [9]. Dentre os multicomponentes apresentaremos as formas mais comumente encontradas de compostos farmacˆeuticos no estado s´olido.
1.3.1 Polimorfo
O polimorfismo ´e a capacidade que alguns compostos qu´ımicos possuem de apresentarem diferentes formas cristalinas. Em suma, polimorfos s˜ao fases s´olidas de uma mesma substˆancia com disposi¸c˜oes arquitetˆonicas distintas de seus arranjos cristalinos. Como mostra a figura abaixo:
Figura 1 – Diferentes empacotamentos da mol´ecula do f´armaco na estrutura cristalina.
medicamentos, al´em da possibilidade de ocasionar desvios da qualidade durante o pro-cesso produtivo [10].
Dentre todas as propriedades f´ısico-qu´ımicas que s˜ao afetadas pelo polimor-fismo, destacaremos a solubilidade, que ´e um fator determinante para a libera¸c˜ao e ab-sor¸c˜ao do f´armaco, apresentando um importante papel na biodisponibilidade [11]. ´E poss´ıvel que um s´olido farmacˆeutico, com boa solubilidade em determinada forma po-lim´orfica, possa apresentar uma solubilidade reduzida para as demais formas que o f´armaco possa exibir, e o resultado disso ´e a perda da atividade farmacol´ogica, ou at´e mesmo a toxidade no organismo para casos em que a solubilidade seja superior [8].
1.3.2 Solvatos/Hidratos
Produz-se um solvato durante um processo de cristaliza¸c˜ao de um determinado f´armaco com um solvente qualquer, nesse procedimento ocorre a captura de mol´eculas de solvente, ou seja, o solvente ´e capaz de empacotar-se e cristalizar-se juntamente com o f´armaco fazendo parte da estrutura cristalina. Ele pode associar-se ao s´olido atrav´es de intera¸c˜oes intermoleculares, como as liga¸c˜oes de hidrogˆenio, liga¸c˜oes de Van der Waals ou dipolo-dipolo.
Durante um processo de cristaliza¸c˜ao se o solvente que for incorporado `a es-trutura cristalina do f´armaco for a ´agua, ser˜ao formados os hidratos. Essa nomenclatura diferenciada ocorre devido a ´agua ser um dos solventes com maior capacidade de formar liga¸c˜oes de hidrogˆenio [12]. Por sua vez, ao produzir um hidrato ocorre a redu¸c˜ao da quantidade de energia liberada no processo de dissolu¸c˜ao em ´agua, resultando ent˜ao no aumento da velocidade de dissolu¸c˜ao de um f´armaco [13]. A figura 2 ilustra a jun¸c˜ao entre os componentes, ou seja, a estrutura cristalina ´e composta pela mol´ecula do f´armaco mais a mol´ecula de solvente.
Figura 2 – Forma¸c˜ao de solvatos de compostos farmacˆeuticos.
1.3.3 Sais
sal, como ilustra a figura 3. Ou seja, os sais s˜ao formados via transferˆencia de cargas entre um ´acido ou base onde ocorre liga¸c˜ao eletrost´atica entre ´ıons de cargas opostas [12]. A forma¸c˜ao de sal farmacˆeutico ´e desej´avel principalmente para f´armacos com problemas de cristaliza¸c˜ao, de solubilidade, de baixos pontos de fus˜ao, com altos ´ındices de ocorrˆencia de polimorfismo, etc.
Figura 3 – F´armaco carregado mais ´ıon reagente, formando sais farmacˆeuticos.
1.3.4 Co-cristais
Figura 4 – F´armaco mais mol´ecula neutra, formando co-cristais farmaˆeuticos.
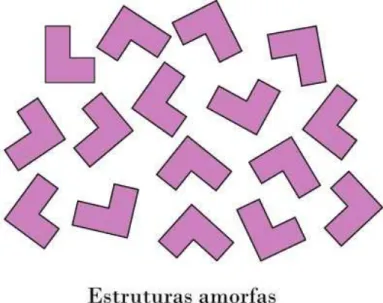
1.3.5 Amorfo
Estado amorfo, ´e outra subfase s´olida comumente encontrada. S´olidos amorfos apresentam caracter´ısticas interessantes tais como, maior solubilidade, maior velocidade de dissolu¸c˜ao, `as vezes melhor compressibilidade em rela¸c˜ao aos seus correspondentes cristalinos, por´em podem apresentar uma menor estabilidade termodinˆamica [15]. Dessa forma, sua aplica¸c˜ao n˜ao supera a dos s´olidos cristalinos, uma vez que, geralmente, apre-sentam baixa estabilidade qu´ımica e tem consider´avel tendˆencia de cristaliza¸c˜ao [6].
Figura 5 – Mol´eculas de APIs distribu´ıdas de formas aleat´orias, caracterizando um ma-terial amorfo.
ponto de vista estrutural, verifica-se que a inclus˜ao de certas mol´eculas ”convidadas”, tais como as mol´eculas de ´agua ou de solvente, pode ajudar a construir estruturas cristalinas mais est´aveis, atrav´es da forma¸c˜ao de redes de intera¸c˜ao intermolecular fortes ou preen-chimento de algumas ”lacunas”nas redes cristalinas de certos compostos farmacˆeuticos [16].
2 M´ETODOS EXPERIMENTAIS
Neste cap´ıtulo iremos tratar de todas as t´ecnicas empregadas na caracteriza¸c˜ao dos compostos farmacˆeuticos estudados neste trabalho.
2.1 Difra¸c˜ao de Raio X
2.1.1 Difra¸c˜ao de Raio X de P´o (DRXP)
Sabemos que a repeti¸c˜ao uniforme de celas unit´arias, define um cristal. O que se conhece por cristalito tamb´em ´e um monocristal, por´em n˜ao tem tamanho sufici-ente para ser usado para determina¸c˜ao de estrutura pelo m´etodo de monocristal. Muitos cristalitos juntos, espalhados de maneira aleat´oria, formam o policristal ou apenas p´o. A difra¸c˜ao de raios X a partir de amostras policristalinas ocorre quando v´arios cristalitos s˜ao irradiados simultaneamente por um feixe incidente. Na difra¸c˜ao de p´o, em consequˆencia da distribui¸c˜ao estat´ıstica das diferentes orienta¸c˜oes assumidas por um dado plano crista-lino, apenas uma parte dos cristalitos est´a corretamente orientada para difratar, ou seja, somente essa parte estar´a orientada de modo a satisfazer a condi¸c˜ao imposta pela lei de Bragg [19]. A identifica¸c˜ao de um composto pelo padr˜ao de difra¸c˜ao de p´o ´e uma t´ecnica pr´atica e conveniente para identifica¸c˜ao qualitativa de composto cristalinos, uma vez que cada substˆancia possui um padr˜ao de difra¸c˜ao ´unico.
A t´ecnica de difra¸c˜ao de raios X de p´o ´e usualmente empregada devido sua simplicidade e rapidez, al´em de fornecer informa¸c˜oes acerca do grau de cristalinidade dos compostos, ind´ıcios de forma¸c˜ao de complexos, atrav´es da compara¸c˜ao entre os difrato-gramas e verifica¸c˜ao de altera¸c˜oes na fase cristalina [20].
Dessa forma, o controle cristalino, atualmente recomendado para o estudo de f´armacos, faz com que o perfil difratom´etrico constitua uma importante ferramenta a ser aplicada na ind´ustria farmacˆeutica.
No presente trabalho foi utilizado um difratˆometro de p´o (DRXP) convencional D8 Advanced da Bruker AXS, equipado com um goniˆometro theta/theta, acoplado na geometria de reflex˜ao com porta amostra fixo e fonte de radia¸c˜ao Cu Kα (0,15419 nm) e um detector LynxEye. A tens˜ao e a corrente el´etrica aplicada foi de 40 kV e 40 mA, respectivamente. A abertura da fenda utilizado para o feixe incidente sobre a amostra foi de 0.2 mm. Foi feito uma varredura da amostra dentro do intervalo de 5o
a 45o
(2θ), com um tamanho de passo de 0.02o
2.1.2 Difra¸c˜ao de Raios X de Monocristal (DRXM)
A determina¸c˜ao estrutural de uma mol´ecula ´e uma etapa indispens´avel quando se pretende estudar um f´armaco, pois existe uma boa rela¸c˜ao entre a estrutura desses materiais com suas propriedades f´ısico-qu´ımicas. Dentre algumas ferramentas existentes para a elucida¸c˜ao da estrutura de um composto, a difra¸c˜ao de raios X em monocristal configura a mais poderosa t´ecnica para este fim, oferecendo informa¸c˜oes precisas a respeito da mol´ecula em an´alise. Atrav´es dos m´etodos cristalogr´aficos ´e poss´ıvel determinar as posi¸c˜oes relativas de todos os ´atomos que constituem a mol´ecula e a posi¸c˜ao relativa de todas as mol´eculas na cela unit´aria do cristal, ou seja, podemos saber como a estrutura molecular est´a arranjada no espa¸co. Al´em disso, outras informa¸c˜oes importantes podem ser obtidas, como por exemplo, ˆangulos e distˆancias dentro da estrutura cristalina, as distˆancias entre ´atomos de diferentes mol´eculas, bem como, as liga¸c˜oes de hidrogˆenio, for¸cas intermoleculares e intramoleculares.
A elucida¸c˜ao da estrutura cristalina do ricobendazol foi feita em parceria com o grupo de engenharia de cristais da universidade de Limerick (Irlanda). No qual foram selecionados monocristais utilizando-se um microsc´opio ´optico e demais an´alises foram re-alizadas em um difratˆometro de monocristal Enraf-Nonius Kappa-CCD, utilizando fonte de molibdˆenio acoplada a um monocromador de grafite (Kα= 0,71073 ˚A) a temperatura de 100K. As medidas foram registradas em varreduras phi e ˆomega com exposi¸c˜oes de 30s por quadro utilizando software APEX2 (BRUKER, 2005a). A estrutura foi resolvida usando o sofware olex2 (Dolomanov, Bourhis, Gildea, Howard, e Puschmann, 2009) jun-tamente com o software de resolu¸c˜ao de estruturas ShelXT (Sheldrick, 2015) utilizando m´etodos diretos. Em seguida a estrutura foi refinada com o software ShelXL (Sheldrick, 2008), aplicando o m´etodo dos m´ınimos quadrados. Para aquisi¸c˜ao, indexa¸c˜ao, integra¸c˜ao e dimensionamento das reflex˜oes de Bragg, tamb´em foi utilizado o APEX 2. As dimens˜oes da cela unit´aria foram adquiridas por meio de todas as reflex˜oes.
2.2 An´alise T´ermica
2.2.1 Termogravimetria e Calorimetria Explorat´oria Diferencial
A an´alise termogravim´etrica apresenta grande utilidade no estudo de f´armacos por permitir conhecer as altera¸c˜oes que o aquecimento pode causar na massa dos materiais [22]. Al´em de possibilitar a determina¸c˜ao de pureza, umidade, a identifica¸c˜ao de demais fases s´olidas e a temperatura em que os materiais come¸cam a se decompor, portanto, a verifica¸c˜ao da estabilidade t´ermica, caracter´ıstica de grande relevˆancia nesse estudo.
A calorimetria explorat´oria diferencial (do inglˆes differential scanning calori-metry, DSC) ´e a t´ecnica que mede a diferen¸ca no fluxo de calor entre a amostra e um material de referˆencia em fun¸c˜ao da temperatura, enquanto as duas est˜ao submetidas a um programa de temperatura controlada [21].
Esta t´ecnica ´e utilizada quando se pretende verificar informa¸c˜oes como ponto de fus˜ao, transi¸c˜oes v´ıtreas ou, de estado s´olido, n´ıvel de cristalinidade, dentre outros [9]. Na ind´ustria farmacˆeutica seu uso ocorre na an´alise de pureza, de estabilidade, de identifica¸c˜ao de isˆomeros ´opticos e ocorrˆencia de polimorfismo, porque cada transi¸c˜ao polim´orfica ocorre com a mudan¸ca de energia. Nos medicamentos, pequenas quantidades de impurezas podem diminuir a sua efic´acia ou causar efeitos colaterais [57]. ´E poss´ıvel verificar a pureza de um f´armaco atrav´es da endoterma de fus˜ao. Pois sabe-se que quanto maior a concentra¸c˜ao de impurezas menor a temperatura de fus˜ao [9].
Neste trabalho, as curvas de DSC foram obtidas em um aparelho de medidas de fluxo de calor da Netzsch, modelo 204 F1 Phoenix. Tamb´em realizamos medida em um instrumento da Netzsch de an´alise t´ermica simultˆanea TG/DSC, modelo STA 449 F3 J´upiter, usando-se um cadinho de alum´ınio (para referˆencia e amostra), mantidas em uma atmosfera de g´as inerte (nitrogˆenio) sobre fluxo de 50 mL.min-1, medindo em uma faixa de 30 a 300 o
C com taxa de aquecimento de 5 K/min. Al´em de an´alises feitas a baixa temperatura, desde a temperatura ambiente at´e -170o
C, a uma taxa de 10 K/min, em atmosfera de nitrogˆenio.
2.3 Espectroscopia Vibracional
A espectroscopia de absor¸c˜ao no infravermelho por transformada de Fourier ´e usada com sucesso na explora¸c˜ao das diferen¸cas na conforma¸c˜ao molecular, no empacota-mento e nos arranjos das liga¸c˜oes de hidrogˆenio dos cristais de compostos orgˆanicos. Va-ria¸c˜oes espectrais s˜ao originadas a partir de altera¸c˜oes nas liga¸c˜oes que exibem frequˆencias vibracionais caracter´ısticas, levando a deslocamentos nas frequˆencias e separa¸c˜oes das bandas de absor¸c˜ao. Essa an´alise qualitativa possibilita evidenciar a presen¸ca de v´arios grupos funcionais, uma vez que essa radia¸c˜ao causa o aumento da amplitude de vibra¸c˜ao das liga¸c˜oes covalentes entre ´atomos e grupos de ´atomos de compostos orgˆanicos. Como os grupos funcionais de mol´eculas orgˆanicas incluem ´atomos ligados por arranjos espec´ıficos, a absor¸c˜ao dessa radia¸c˜ao por uma mol´ecula orgˆanica ocorrer´a de modo caracter´ıstico dos tipos de liga¸c˜ao e de ´atomos presentes nos grupos funcionais espec´ıficos daquela mol´ecula. Em um espectro de infravermelho a frequˆencia de uma dada vibra¸c˜ao de estiramento pode estar relacionada a dois fatores: as massas dos ´atomos ligados e a rigidez relativa da liga¸c˜ao. Os ´atomos leves vibram com frequˆencias maiores do que os mais pesados e as liga¸c˜oes triplas vibram em frequˆencias maiores que as liga¸c˜oes duplas que vibram em frequˆencias maiores que as liga¸c˜oes simples. Para que ocorra uma vibra¸c˜ao com absor¸c˜ao da radia¸c˜ao de infravermelho, o momento de dipolo deve variar durante a vibra¸c˜ao. A possibilidade de dois compostos diferentes apresentarem o mesmo espectro de IR ´e extre-mamente pequena. Por isso o espectro IR ´e chamado de “impress˜ao digital” da mol´ecula [24, 24].
A espectroscopia Raman foi empregada como m´etodo complementar, pois per-mite, devido `as diferen¸cas nas regras de sele¸c˜ao, que sejam observadas as bandas de baixa intensidade que n˜ao poderiam ser exibidas na espectroscopia de absor¸c˜ao no infraverme-lho.
Para caracteriza¸c˜ao dos s´olidos via espectroscopia de infravermelho utilizamos um espectrˆometro de transformada de Fourier VERTEX 70V da Bruker Optics, com detector DTGS, atrav´es de um acess´orio de Refletˆancia Total Atenuada (FTIR-ATR), com cristal de diamante. Os espectros foram obtidos na faixa de 4000 a 400 cm−1, com
uma m´edia de 128 varreduras e resolu¸c˜ao de 2cm−1.
A caracteriza¸c˜ao dessas amostras via espectroscopia Raman foi realizada em um espectrˆometro Raman com Transformada de Fourier (FT-Raman) modelo M´odulo RAM II (laser Nd :YAG -1064 nm) da Bruker Optics.
focalizado nas amostras atrav´es de lentes objetivas com aumento de 10x e 20x. Todos os espectros foram registrados na janela espectral de 200 a 1800cm−1. Uma placa aquecedora
FTIR600 (Linkan Scientific instruments) foi utilizada para an´alises in-situ sob varia¸c˜ao de temperatura das amostras.
2.4 Microscopia ´Optica
Na t´ecnica de microscopia ´optica, a an´alise do material ocorre pela transmiss˜ao ou reflex˜ao do feixe de luz vis´ıvel incidente na superf´ıcie da amostra. Na ind´ustria far-macˆeutica, o estudo da morfologia externa das part´ıculas ´e a principal aplica¸c˜ao desta t´ecnica.
Foi utilizado nesse trabalho um microsc´opio de luz polarizada Leica (Modelo DM, 2500P), o que possibilitou a verifica¸c˜ao do h´abito cristalino do composto.
Tamb´em fizemos an´alise com a termomicroscopia (Hot-Stage microscopy- HSM). Em particular, HSM permite a observa¸c˜ao direta de uma amostra durante o aqueci-mento, arrefecimento ou sob condi¸c˜oes isot´ermicas. Tais investiga¸c˜oes fornecem evidˆencia confi´avel em primeira m˜ao sobre os processos que ocorrem [31].
2.5 Ativa¸c˜ao Mecanoqu´ımica
Moagem, tamb´em conhecida como ativa¸c˜ao mecanoqu´ımica, ´e um processo comum para a busca de novas formas s´olidas, tais como, polimorfos, sais e co-cristais, sendo nessa t´ecnica avaliada a predisposi¸c˜ao de um API de mudar de forma ou torna-se amorfo. Algumas das vantagens da t´ecnica s˜ao fornecer os resultados de forma imediata, ser de f´acil reprodu¸c˜ao e necessitar de pouco ou nenhum solvente para realiza¸c˜ao. O processo de s´ıntese consiste de um moinho de bolas que permite amplas condi¸c˜oes de moagem variando-se apenas o tempo e a frequˆencia. Para este trabalho usamos um moinho de bolas da Retsch, modelo MM400, e um vazo cil´ındrico de volume 5mL, onde em seu interior foram colocadas duas esferas de mesmo material com diˆametro de 5mm, o que possibilita, portanto, a moagem. Dessa forma, com uma transferˆencia de energia cin´etica e o atrito entre a esfera e a amostra induz uma poss´ıvel produ¸c˜ao de uma nova fase.
´
E poss´ıvel utilizar essa t´ecnica de duas formas, primeira, moagem pura, onde ambos os componentes s˜ao adicionados no moinho e misturados. Segunda, moagem com gotas de solvente (tamb´em conhecido como moagem l´ıquida assistida ou com moagem ´
3 RICOBENDAZOL
Os f´armacos benzimidaz´olicos s˜ao amplamente utilizadas em medicamentos para a preven¸c˜ao e tratamento de doen¸cas parasit´arias. A baixa toxicidade e um amplo espectro de atividade tˆem contribu´ıdo para seu sucesso como agente anti-helm´ıntico. Os derivados contendo enxofre (fenbendazol, Oxfendazol e albendazol) s˜ao f´armacos impor-tantes nesta classe, devido sua alta efic´acia. No entanto, sua baixa solubilidade aquosa (6 mg / mL) limitaram a sua administra¸c˜ao oral. Com isso buscou-se uma maneira de obter uma formula¸c˜ao mais vi´avel. Levando ent˜ao a estudos farmacocin´eticos utilizando uma forma injet´avel, conhecida como metabolito ativo do albendazol ou sulf´oxido de al-bendazol. Onde verificou-se que ap´os administra¸c˜ao oral do ABZ, as concentra¸c˜oes do mesmo s˜ao muito baixas (0,05mg/mL) e muitas vezes n˜ao detect´avel [17]. E que a ativi-dade sistˆemica se devia ao metabolito ativo, ou seja, ao sulf´oxido de albendazol. Assim, a formula¸c˜ao de RBZ como uma solu¸c˜ao para inje¸c˜ao foi poss´ıvel devido `a sua maior solubilidade aquosa em solu¸c˜oes ´acidas em compara¸c˜ao com ABZ. No qual se tem uma solubilidade de 67 mg/mL para RBZ e 0,53 mg /mL para ABZ [25]. Nesse contexto, o ricobendazol (RBZ) ´e relatado como o metabolito ativo de ABZ ap´os administra¸c˜ao oral do mesmo. Entendemos como metabolismo o processo pelo qual o f´armaco ´e alterado por rea¸c˜oes bioqu´ımicas no organismo.
Ricobendazol (RBZ) ou sulf´oxido de albendazol, segundo a IUPAC carbamato de metil N-(6-propilsulfinil-bensimidazol-2-il), com f´ormula molecularC12H15N3O3S, ´e um f´armaco benzimidaz´olico prescrito para o tratamento de verminoses. Este ´e um f´armaco amplamente utilizado em medicina veterin´aria para a preven¸c˜ao e tratamento de doen¸cas parasit´arias, estando entre os agentes anti-helm´ınticos mais eficazes [26]. O ricobendazol ´e praticamente insol´uvel em ´agua, pertencendo `a classe II dos sistemas de classifica¸c˜ao biofarmacˆeutica (BCS), ou seja, baixa solubilidade e alta permeabilidade, onde a velo-cidade de absor¸c˜ao ´e maior do que a de dissolu¸c˜ao, sendo esta ´ultima a que controla a biodisponibilidade [27].
A solubilidade ´e um parˆametro termodinˆamico definido como a quantidade m´axima de soluto que se dissolve em um determinado solvente ou solu¸c˜ao `a temperatura e press˜ao constantes e especificadas. De acordo com o BCS a solubilidade de um f´armaco ´e alta quando a maior dose existente do f´armaco se dissolve em 250 mL de uma solu¸c˜ao aquosa de pH entre 1 e 7,5, e ´e baixa quando ocorrer o oposto [9].
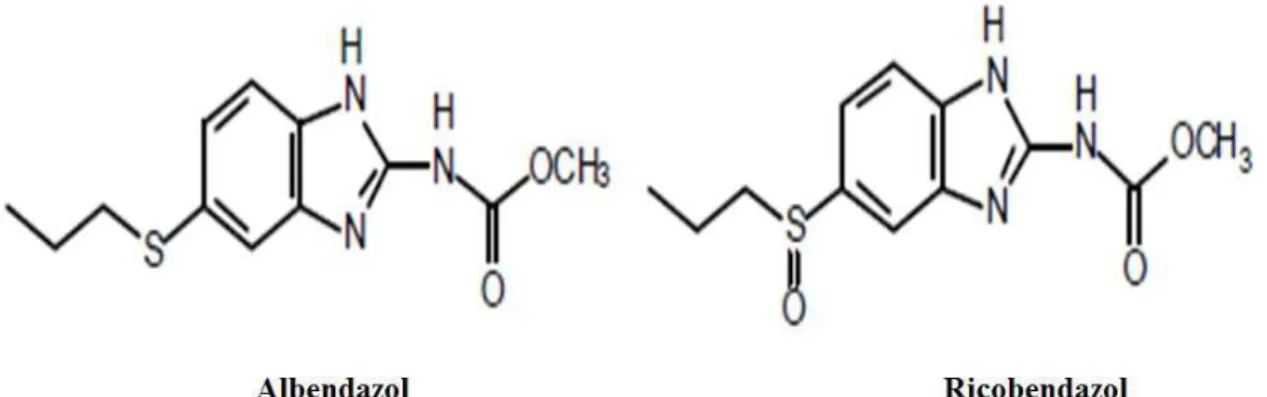
haema-tobium) e cest´odeos (Taenia saginata, Taenia solium), sendo assim um medicamento de amplo uso da medicina veterin´aria [28].
Figura 6 – Estrutura molecular do albendazol e do sulf´oxido de albendazol.
Como descrito anteriormente, a estrutura cristalina de um f´armaco pode afe-tar em algumas propriedades f´ısico-qu´ımicas, tais como estabilidade e solubilidade, o que pode comprometer a qualidade dos produtos disponibilizados, acarretando em falhas te-rapˆeuticas ou at´e mesmo toxicidade. Portanto, o conhecimento estrutural, como o empa-cotamento e conforma¸c˜ao das mol´eculas, as intera¸c˜oes intramoleculares e intermoleculares ´e extremamente relevante. Nesse contexto, o objetivo do presente cap´ıtulo consiste em descrever a determina¸c˜ao da estrutura cristalina do ricobendazol, uma vez que a mesma n˜ao se encontra reportada na literatura, bem como sua caracteriza¸c˜ao e descri¸c˜ao de suas propriedades f´ısico-qu´ımicas relevantes.
A estrutura cristalina do ricobendazol foi elucidada por difra¸c˜ao de raios x de monocristal. E a caracteriza¸c˜ao adicional foi realizada por espectroscopia de infra-vermelho, difra¸c˜ao de raios x em p´o e an´alise t´ermica (termogravimetria e calorimetria diferencial explorat´oria).
3.1 Processo de cristaliza¸c˜ao
O cristal de ricobendazol foi obtido pelo m´etodo convencional de cristaliza¸c˜ao, conhecida como evapora¸c˜ao lenta de solvente. O cristal foi obtido a partir da recrista-liza¸c˜ao do f´armaco em uma solu¸c˜ao hidroalc´oolica (´agua: metanol, 50:50, v/v), a 25 o
C. Nestas condi¸c˜oes obteve-se cristais com h´abito cristalino planar com dimens˜oes adequadas para as an´alises em difratˆometro de raios X de monocristal.
3.2 Descri¸c˜ao da Estrutura Cristalina
(Z=4), acomodando uma mol´ecula na unidade assim´etrica (Z’ =1), conforme pode ser observado na figura 7. A estrutura possui os seguintes parˆametros de rede: a = 7.5960(16) ˚
A, b = 9.3047(18) ˚A, c= 18.726(4) ˚A e β = 82,198(5)o
. Dados cristalogr´aficos adicionais encontram-se na Tabela 2.
Figura 7 – Representa¸c˜ao da cela unit´aria do Ricobendazol. Formando, assim, agregados moleculares ao longo da rede.
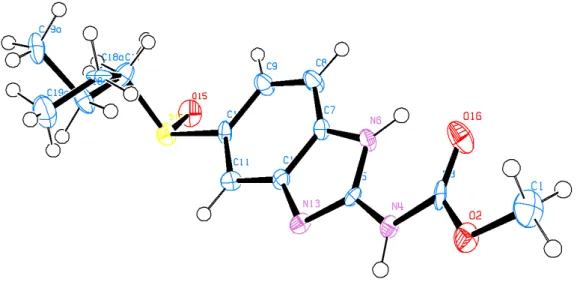
A representa¸c˜ao das elipsoides t´ermicas (ORTEP, do inglˆes Oak Ridge Ther-mal–Ellipsoid Plot Program) da unidade assim´etrica do ricobendazol ´e apresentada na Figura 8.
Tabela 1: Parˆametros cristalogr´aficos do RBZ
F´ormula Emp´ırica C12H14N303S
Peso molecular 283,33
Temperatura/K 122
Sistema cristalino monocl´ınico
Grupo espacial P21/c
a (˚A) 7,5960(16)
b (˚A) 9,3047(18)
c (˚A) 18,726(4)
β/o
82,198(5) Volume (˚A3
) 1311,3 (5)
Z/Z’ 4/1
Pcalc (g/cm
3
) 1,420
Coeficiente de absor¸c˜ao (mm−1) 0,255
F (000) 588
Tamanho do cristal (mm3
) 0,10 x 0,5 x 0,5 Radia¸c˜ao, λ (˚A) MoKa (0.71073) ´Indices R finais [I > 2σ(1)] 9.07
Tabela 2: Liga¸c˜oes de hidrogˆenio que contribuem para o arrajamento supramolecular Intera¸c˜ao D—H···˚A D—H˚A H···A(˚A) D···A(˚A) D—H···A(
o ) Intermolecular N4—H4···N13 0,88 2,04 2,89(7) 162
Intermolecular N6—H6···O16 0,88 2,04 2,740(7) 115
Intermolecular N6—H6···O15 0,88 2,04 2,758(7) 139
Intermolecular C8—H8···O15 0,95 2,55 3,178(8) 124
Intermolecular C17—H17A···O16 0,99 2,49 3,381(8) 149 C´odigo de simetria: 1 =−x,1−y,1−z 5 = 1−x,−1/2 +y,1/2−z 4 = 1−x,1/2 +y,1/2−z
O ˆangulo de tors˜ao entre o grupo alif´atico e a por¸c˜ao de carbamato de benzi-midazol demonstra que eles apresentam um grau de desordem. Dentro da cela unit´aria as mol´eculas s˜ao mantidas juntas por meio das intera¸c˜oes de hidrogˆenio (onde “D” e “A” s˜ao, respectivamente, o ´atomo doador e receptor da liga¸c˜ao de hidrogˆenio), podemos observar isso na tabela 2.
Para a intera¸c˜ao 2 e 3 que s˜ao liga¸c˜oes de hidrogˆenio convencionais do tipo N-H...O, os ˆangulos e distˆancias entre doador aceptor est˜ao dentro dos padr˜oes convencionais cuja a distˆancia entre doador e aceptor varia entre 2,8 e 3,2 ˚A e os ˆangulos variam dentro das normalidades. As intera¸c˜oes 4 e 5 s˜ao liga¸c˜oes de hidrogˆenio n˜ao convencionais do tipo C-H...O que tamb´em est˜ao dentro dos padr˜oes tabelados. Apesar das distˆancias entre doador e aceptor dessas intera¸c˜oes serem um pouco maiores do que nas intera¸c˜oes 2 e 3, estas ainda contribuem fortemente para a estabiliza¸c˜ao do arranjo molecular como representado na Figura 9.
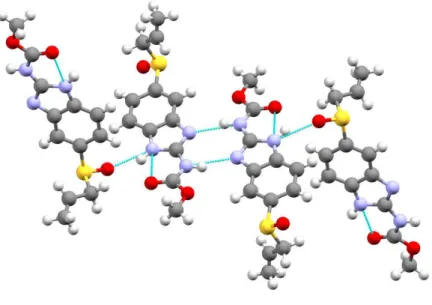
Como citado acima as mol´eculas de ricobendazol est˜ao organizadas como d´ımeros ligados por NH···N, liga¸c˜oes a partir de por¸c˜oes de carbamato de benzimidazol. Estes
d´ımeros s˜ao conectados por outra liga¸c˜ao de hidrogˆenio NH···O entre o benzimidazol e o
grupo sulf´oxido, tamb´em representado na Figura 9:
J´a vimos que as intera¸c˜oes intermoleculares da estrutura se mant´em devido ao padr˜ao de liga¸c˜oes de hidrogˆenio cl´assicas envolvendo ´atomos de oxigˆenio e nitrogˆenio, desempenhando um papel decisivo nas suas caracter´ısticas conformacionais.
Frequentemente surgem problemas durante o refinamento de uma estrutura, tal como problemas de desordem. A estrutura cristalogr´afica ´e a m´edia espacial de todas as mol´eculas sobre o volume de um cristal em um determinado momento. Em muitos casos, 23 partes da mol´ecula s˜ao encontradas em mais de uma orienta¸c˜ao cristalogr´afica. Essa situa¸c˜ao pode ser ocasionada pela existˆencia de mais de uma mol´ecula na unidade assim´etrica, a ocorrˆencia de gemina¸c˜ao ou ainda de desordem. Mol´eculas desordena-das possuem fragmentos que apresentam duas ou mais orienta¸c˜oes, ou seja, dois ou mais conjuntos de coordenadas para cada ´atomo. No caso do RBZ existe uma desordem na ori-enta¸c˜ao da cauda alif´atica de s´ıtio para s´ıtio. Ou seja, existe 50% de chance de achar uma dessas orienta¸c˜oes em cada s´ıtio ocupado pela mol´ecula. Entretanto, essas condi¸c˜oes n˜ao interferem nos resultados at´e aqui discutidos sendo portanto resultados representativos da mol´ecula.
3.3 Caracteriza¸c˜ao em estado s´olido do Ricobendazol 3.3.1 Difra¸c˜ao de Raio X de P´o
A Figura 10 mostra a compara¸c˜ao entre o padr˜ao de difra¸c˜ao de raios X experi-mental e calculado do RBZ. O objetivo foi verificar se o cristal utilizado para elucida¸c˜ao da estrutura ´e representativo quando comparado com a amostra obtida experimentalmente. Podemos verificar ent˜ao que os padr˜oes de difra¸c˜ao apresentam os mesmos picos de Bragg e as reflex˜oes de maior intensidade aparecem em 11o
; 18; 24 e 26o .
De acordo com a Farmacopeia Americana (USP, 2011), a diferencia¸c˜ao entre amostras teste e a amostra referˆencia ´e estabelecida por difra¸c˜ao de raios X de p´o se os ˆangulos de espalhamento das reflex˜oes mais intensas obtidas a partir do material de referˆencia variam em mais ou menos 0,10o
Figura 10 – Difratogramas referentes `as amostras de RBZ: (a) padr˜ao experimental e em (b) padr˜ao calculado.
3.3.2 Calorimetria Explorat´oria Diferencial e Termogravimetria
A fim de proporcionar uma vis˜ao completa do composto foi realizada a an´alise t´ermica do mesmo. Cujo esse comportamento t´ermico pode ser observado nas curvas de DSC / TG apresentados na Figura 11. A curva de DSC mostra um evento endot´ermico bem definido em 220o
Figura 11 – Comportamento t´ermico do RBZ recristalizado em metanol.
3.3.3 Espectroscopia Vibracional Raman e Infravermelho (IR)
As an´alises espectrosc´opicas forneceram informa¸c˜oes complementares no to-cante `as intera¸c˜oes intermoleculares da estrutura cristalina do ricobendazol. O espectro do infravermelho apresenta as bandas de absor¸c˜ao caracter´ısticas do f´armaco, tais como, uma banda intensa e estreita entre 1600 – 1800cm−1 que corresponde a vibra¸c˜ao de
esti-ramento do grupo carbonila. Nas regi˜oes entre 1000-1200 cm−1 pode ser observado uma
banda m´edia associada a vibra¸c˜ao do grupo sulf´oxido.como ilustra o espectro da figura 12. Al´em de uma banda fraca e larga entre 3300 a 3500 cm−1 correspondentes as vibra¸c˜oes
Figura 12 – Espectro de IR do ricobendazol.
T´ecnicas espectrosc´opicas vibracionais tˆem sido utilizadas com sucesso para a identifica¸c˜ao de fases cristalinas. A figura 13 mostra os espectros de FT-Raman e FT-IR, obtidos a partir da recristaliza¸c˜ao do ricobendazol. O espectro Raman apresenta bandas correspondetes ao grupo carbonila em torno de 1640 e ao estiramento NH em 1600cm−1.
3.3.4 Microscopia ´Optica e Microscopia Eletrˆonica de Varredura
As imagens referentes aos h´abitos cristalinos de RBZ gerados pela recrista-liza¸c˜ao em metanol e ´agua encontram-se ilustrados nas figuras 14 e 15. O cristal de RBZ obtido a partir dessa solu¸c˜ao demonstrou uma morfologia planar.
Figura 14 – Imagens referentes ao cristal de RBZ via microscopia ´optica.
As fotomicrografias mostradas na figura 15 tamb´em revelaram h´abito planar, al´em de mostrar uma distribui¸c˜ao heterogˆenea de tamanho de part´ıcula e a presen¸ca de aglomerados, revelando que ele cresce como sobreposi¸c˜ao de planos.
Figura 15 – Fotomicrografias obtidas por MEV referentes `a amostra RBZ.
´
E sabido que a morfologia cristalina desempenha um importante papel no processamento e desenvolvimento de um produto farmacˆeutico, uma vez que este impacta nas propriedades f´ısicas, como orienta¸c˜ao da part´ıcula, taxa de dissolu¸c˜ao, compacta¸c˜ao e compressibilidade, e fluxo de p´o, al´em do processo de mistura dos componentes da formula¸c˜ao [29].
4 POLIMORFISMO DO ALBENDAZOL
Como descrito na se¸c˜ao (1.3.1) o polimorfismo ´e a propriedade de uma substˆancia possuir duas ou mais estruturas cristalinas. Entre os f´armacos descritos na literatura que apresentam esta propriedade est´a o albendazol. O albendazol, carbamato de me-til N-(5-propilsulfanil-3H-benzoimidazol-2-il) segundo a IUPAC, com f´ormula molecular C12H15N3O2S, ´e um f´armaco benzimidaz´olico que est´a entre os agentes anti-helm´ınticos mais eficazes, prescrito para o tratamento das infec¸c˜oes causadas por parasitas intesti-nais, como: ancilostom´ıase, ascarid´ıase, enterob´ıase, estrongiloid´ıase, giard´ıase, ten´ıase, tricocefal´ıase, neurocisticercose e larva migrans cutˆanea [30].
Figura 16 – Estrutura qu´ımica do Albendazol.
O albendazol ´e praticamente insol´uvel em ´agua, resultado j´a esperado por ser um benzimidazol e sol´uvel em ´acido f´ormico, ´acido ac´etico glacial e ´acido sulf´urico, pouco sol´uvel em clorof´ormio, muito pouco sol´uvel em acetato de etila, acetona, cloreto de metileno, etanol, ´eter et´ılico, metanol e tolueno, insol´uvel em n-hexano e tetracloreto de carbono, dentre outros [4].
De acordo com o Sistema de Classifica¸c˜ao Biofarmacˆeutica (SCB) o albendazol ´e classificado como f´armaco de classe II (baixa solubilidade e alta permeabilidade) ou classe IV (baixa solubilidade e baixa permeabilidade).
Umas das consequˆencias do polimorfismo na ´area farmacˆeutica s˜ao altera¸c˜oes que ele pode causar nas propriedades f´ısico-qu´ımicas dos f´armacos (ver se¸c˜ao 1.3.1), le-vando a formula¸c˜oes que n˜ao apresentam a efic´acia esperada. Como citado anterior-mente, essas altera¸c˜oes s˜ao oriundas das diferentes conforma¸c˜oes e/ou intera¸c˜oes intra e intermoleculares que modificam os empacotamentos cristalinos das mol´eculas nas formas polim´orficas.
em 2009 e uma comunica¸c˜ao privada feita por A. Alhalaweh et al em 2007. Bem como as estruturas cristalinas depositadas na base de dados Cambridge Structural Data base (CSD), distribu´ıda pela Cambridge Crystallographic Data Centre(CCDC). Apresentando, portanto, dados sobre o grupo espacial, cela unit´aria, posi¸c˜oes atˆomicas, dentre outras informa¸c˜oes. Dessa forma, considerando a importˆancia do polimorfismo na ind´ustria farmacˆeutica e avaliando a descri¸c˜ao dessas formas polim´orficas reportadas, o presente trabalho teve por finalidade investigar estes polimorfos, al´em da existˆencia de novas fases da amostra comercial do f´armaco.
A amostra de albendazol foi analisada por difra¸c˜ao de raios X de p´o, para a identifica¸c˜ao dos polimorfos. E t´ecnicas auxiliares como TG/DSC e FTIR foram utilizadas para complementa¸c˜ao dos resultados.
4.1 Classifica¸c˜ao dos Polimorfos
Os polimorfos podem ser classificados como enantiotr´opicos ou monotr´opicos. Para um sistema enantiotr´opico a transi¸c˜ao de uma forma cristalina para outra ´e de na-tureza revers´ıvel. Condi¸c˜oes que dependem do material em estudo e dos tratamentos t´ermicos que ser˜ao submetidos. Em contrapartida, um sistema ´e monotr´opico se a mu-dan¸ca da forma cristalina acontece de forma irrevers´ıvel [12]. Para dois polimorfos, por exemplo, a estabilidade relativa depende de suas energias livre de Gibbs, onde o polimorfo mais est´avel a uma determinada press˜ao e temperatura ´e aquele com menor energia.
Para um sistema enantiotr´opicos ´e poss´ıvel observar uma transi¸c˜ao revers´ıvel a uma temperatura de transi¸c˜ao definida, menor que a temperatura de fus˜ao de qualquer das duas fases, j´a para um sistema monotr´opico n˜ao ocorre esse tipo de transi¸c˜ao antes da fus˜ao. As transi¸c˜oes sempre acontecem da forma menos est´avel para uma mais est´avel, nos dois casos o polimorfo com menor energia livre de Gibbs, em determinadas condi¸c˜oes de press˜ao e temperatura, ser´a o polimorfo mais est´avel. Onde nem sempre essa ´e a forma mais vi´avel do ponto de vista farmacˆeutico, j´a que maior estabilidade implica em menor solubilidade e, portanto, menor biodisponibilidade [33].
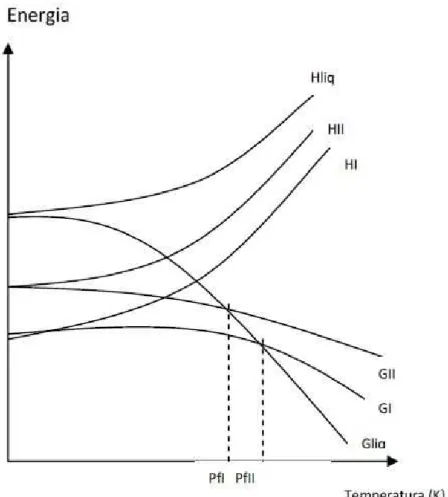
s´olida se encontram com a curva da fase l´ıquida. Ou seja, a curva Gliq representa a fase l´ıquida caracterizando o ponto de fus˜ao dos dois polimorfos. Verifica-se que a temperatura de transi¸c˜ao ´e menor que a temperatura de fus˜ao de qualquer das fases. Neste caso a forma I ´e a forma mais est´avel, j´a que tem menor energia livre em qualquer temperatura abaixo do ponto de transi¸c˜ao [33].
Figura 17 – Diagrama de Energia Livre versus Temperatura para um Sistema Enanti-otr´opico. G representa a energia livre de Gibbs e H ´e a entalpia. Adaptado de [12]
J´a o diagrama da figura 18 representa uma situa¸c˜ao para um sistema mo-notr´opico, onde n˜ao h´a ponto de transi¸c˜ao abaixo dos pontos de fus˜ao dos dois polimorfos. O que ´e representado pela ausˆencia do cruzamento das curvas GI e GII. Nestas condi¸c˜oes, para rela¸c˜ao termodinˆamica monotr´opica, os polimorfos I e II n˜ao se convertem entre si e a forma I ´e o polimorfo mais est´avel, a esta temperatura [33].
Figura 18 – Diagrama de Energia Livre versus Temperatura para um sistema Monotr´opico.
4.2 Descri¸c˜ao dos polimorfos do Albendazol
De acordo com a literatura temos uma forma cristalina descrita por [49], com grupo espacial C2/c e parˆametros de cela unit´aria a = 24,317(2)˚A, b = 5,413(0)˚A, c= 19,738(1)˚A, α = 90,00o
,β = 97,71(0)o
, γ= 90,00o
e V=2574,603 ˚A3 .
E uma segunda estrutura descrita por [32] denominada de forma II, com grupo espacial C2/c e parˆametros de cela unit´aria a = 23,934(5)˚A, b = 5,440(1)˚A, c= 19,586(6)˚A, β=99,29(1)o
, γ = 99,29o
e V=2516,640 ˚A3 .
Figura 19 – Unidade assim´etrica da forma descrita por [49].
Figura 20 – Unidade assim´etrica da forma II descrita por [32].
Os empacotamentos cristalinos de ambas as formas est˜ao ilustrados na Figura 21. Como podemos observar as arquiteturas de empacotamento das duas formas s˜ao muito semelhantes. Em ambas as fases, as mol´eculas do cristal encontram-se empacotadas em forma de zig-zag. Dentro as mol´eculas criam redes de liga¸c˜oes de hidrogˆenio. Embora estruturalmente as formas polim´orficas sejam muito semelhantes, elas diferem entre si em in´umeras propriedades f´ısicas.
No entanto, Pranzo e seus colaboradores, descrevem as duas formas polim´orficas do albendazol como forma I e II, onde a primeira ´e a forma comercialmente dispon´ıvel e a segunda ´e uma recristaliza¸c˜ao em metanol e dimetilformamida (DMF). A recristaliza¸c˜ao tanto a partir do metanol quanto do DMF proporcionou um polimorfo de forma est´avel (forma II) enantiotropicamente relacionada com a forma I, sendo esta ´ultima a forma metaest´avel `a temperatura ambiente.
Em suma, essas s˜ao as informa¸c˜oes reportadas na literatura a respeito do polimorfismo do albendazol. Visando explorar essa tem´atica em nosso trabalho, reunimos todas essas informa¸c˜oes e realizamos novos levantamentos, com isso chegamos a alguns resultados importantes e in´editos acerca do polimorfismo desse f´armaco.
Na figura 22 encontram-se os difratrogramas calculados a partir das estruturas SUTWIU em verde e BOGFUZ em marron, (denominadas formas II e III respectivamente, onde a denomina¸c˜ao forma III foi por n´os designada) e os ditratogramas referentes a mat´eria prima em vermelho (forma I) e a recristaliza¸c˜ao desta em metanol na cor azul. Indicando que a recristaliza¸c˜ao da forma I em metanol corresponde a forma III.
Figura 22 – Difratogramas das formas polim´orficas do albendazol.
Figura 23 – Formas polim´orficas do albendazol. Em a) forma II-experimental, em b) calculado e em c) forma I. Figura retirada de Pranzo et al, 2011.
Logo, de acordo com os difratogramas da figura 22 e tomando como referˆencia o difratograma retirado do artigo do Pranzo et al (figura 23), podemos observar que a forma I, referente `a nossa mat´eria prima (forma comercialmente distribu´ıda) pode ser recristalizada em metanol, obtendo a forma reportada por A. Alhalaweh et al. Enquanto Pranzo e seus colaboradores recristalizaram a forma I, obtendo a forma II, como mos-trados nas figuras 22 e 23. Assim podemos concluir que o albendazol possui trˆes formas polim´orficas. Onde a forma I, n˜ao tem estrutura cristalina elucidada, no entanto Pranzo realiza em seu trabalho an´alises por meio de difra¸c˜ao de raios-X em p´o e calorimetria diferencial explorat´oria (DSC). Por outro lado, a estrutura cristalina da forma II j´a est´a elucidada e caracterizada na literatura. Por sua vez, o albendazol na forma III tem sua estrutura cristalina determinada por A. Alhalaweh et al, (arquivo CIF BOGFUZ), mas sem nenhuma caracteriza¸c˜ao adicional, tal como an´alise t´ermica e espectroscopia de in-fravermelho, por exemplo.
as trˆes formas, visando, dessa forma, um estudo completo do acerca do polimorfismo do f´armaco em quest˜ao.
Entretanto n˜ao foi poss´ıvel realizar tal compara¸c˜ao da maneira como de-sej´avamos, j´a que n˜ao conseguimos a recristaliza¸c˜ao da forma II, uma vez que, todas as tentativas de recristaliza¸c˜ao a resultante era a forma III. Sendo assim, foi poss´ıvel fa-zer uma compara¸c˜ao direta entres as formas I e III e ao mesmo tempo com a forma II reportada por Pranzo e seus colaboradores.
4.3 Caracteriza¸c˜ao dos polimorfos do Albendazol
4.3.1 DSC/TG
De acordo com nossos resultados, podemos observar uma transi¸c˜ao de fase entre as formas I e III, na qual a forma III se transforma na forma I entre 150 a 160o
C, sendo, portanto, uma transi¸c˜ao irrevers´ıvel (figura 24). Desse modo, temos que a forma III ´e a forma metaest´avel e a forma I a forma mais est´avel termodinamicamente. Uma vez que, a forma de maior energia possui a tendˆencia de se transformar na forma de menor energia.
As figuras 24 e 25 mostram as curvas de DSC das formas polim´orficas I e III. Onde a figura 24 destaca a forma polim´orfica III (em vermelho) submetida primeiramente a uma taxa de temperatura controlada de 30 a 170o
C, em seguida apresenta o retorno para a temperatura ambiente, ou seja, de 170 a 30o
C (em preto) e por ´ultimo mais uma subida de 30 a 300o
C (em Azul), revelando claramente a transi¸c˜ao polim´orfica da forma III para a forma I, confirmando todas as informa¸c˜oes acima supracitadas.
J´a na figura 25, temos as curvas de DSC correspondentes aos polimorfos I e III (em vermelho e azul respectivamente). Sendo poss´ıvel realizar uma compara¸c˜ao entre ambas e notadamente comprovar a transi¸c˜ao demonstrada na figura 24. Ainda podemos destacar de acordo com a figura 25, os eventos endot´ermicos e exot´ermicos entre 150 a 170o
Figura 24 – Curvas de DSC que demonstram a transforma¸c˜ao polim´orfica da forma III para a forma I.
Figura 25 – Formas polim´orficas do albendazol. Forma I (Vermelha), no qual a mesma corresponde a nossa mat´eria prima e por sua vez a forma III (azul) ´e a recristaliza¸c˜ao em metanol.
Nas figuras 26 e 27 temos um paralelo entre as curvas de DSC/TG e a termo-microscopia, uma t´ecnica vers´atil que possibilita o acompanhamento em tempo real dos eventos t´ermicos. Assim, podemos observar que ap´os a mudan¸ca de fase do polimorfo III para o polimorfo I, que ocorre em torno de 150o
C, novos eventos endot´ermicos surgem a partir de 190o
uma vez que existe uma perda de massa, como mostra as curvas termogravim´etricas da figura 27.
Figura 26 – An´alise em microscopia de hot-state realizada na forma III mostrando que ocorre uma nova fus˜ao seguida de uma recristaliza¸c˜ao come¸cando em 190o
C, cujo o pro-cesso ´e dado em cima das seguintes temperaturas, em 190o
C in´ıcio da fus˜ao, em 216o C a recristaliza¸c˜ao total e em seguida come¸ca o processo de decomposi¸c˜ao do composto.
Figura 27 – Compara¸c˜ao das curvas de DSC/TG entre os dois polimorfos do albendazol, evidenciando a distin¸c˜ao entre ambas.
De maneira semelhante a figura 28 apresenta as an´alises de DSC de amostras recristalizadas em compara¸c˜ao com a ABZ original, ou seja, as formas I e II reportada por Pranzo et al. Uma das diferen¸cas mais not´aveis nos ensaios DSC corresponde a recristaliza¸c˜ao em metanol (ver Figura 28b), aparece como um efeito endo-exo claro em 143o
de 200o
C aparecem sobrepostos dificultando assim a sua interpreta¸c˜ao. Observou-se um comportamento an´alogo para outras amostras recristalizadas (28c). Este efeito endo-exo corresponde a uma transforma¸c˜ao polim´orfica de transi¸c˜ao s´olida-s´olida de ABZ obtida pela cristaliza¸c˜ao do ABZ. Estas duas formas polim´orficas foram isoladas com sucesso pelos autores acima citados, sendo caracterizado por ter uma rela¸c˜ao enantiotr´opica.
Figura 28 – Curvas de DSC das formas polim´orficas mostradas por Pranzo. Em a) forma I, em b) recristaliza¸c˜ao em DMF e em c) recristaliza¸c˜ao em metanol, ambas correspondentes `a forma II. Figura retirada de Pranzo, 2011.
Os espectros de infravermelho das amostras de albendazol podem ser observa-dos nas figuras 29 e 30. Algumas ´areas foram ampliadas, para melhor visualiza¸c˜ao das bandas e suas respectivas vibra¸c˜oes.
A figura 29 traz o espectro com bandas de vibra¸c˜ao caracter´ıstica para o alben-dazol, tais como a vibra¸c˜ao entre 1525-1630 cm−1 correspondendo ao grupamento N-H.
Em 599cm−1 temos a vibra¸c˜ao que corresponde a liga¸c˜ao (C-S). Em 1060cm−1,
encontra-se a liga¸c˜ao ´ester (C-O-C), j´a em 1589cm−1 a vibra¸c˜ao equivalente ao arom´atico (C=N).
Figura 29 – Espectro de FTIR das formas I e III do albendazol.
J´a a vibra¸c˜ao em 2958 cm−1 e uma banda larga em 2665cm−1 correspondem
Figura 30 – Espectro FTIR das formas I e III do albendazol. Regi˜ao ampliada, na faixa entre 2400 a 3500cm−1.
Nas Figuras 31, 32 e 33 observa-se que nas regi˜oes demarcadas existem dife-ren¸cas entre os espectros, indicando a presen¸ca de diferentes polimorfos. Fazendo uma compara¸c˜ao direta entre ambas, constata-se tais distin¸c˜oes em 1630 cm−1, onde
obser-vamos a duplica¸c˜ao da banda na forma I, j´a em 1400 cm−1 surge uma banda para o
polimorfo III, bem como diferen¸cas significativas entre 400 a 900cm−1 de acordo com o
Figura 33 – Espectro FTIR das formas I e III do albendazol. Regi˜ao ampliada, na faixa entre 2400 a 2450 cm−1.
A partir das an´alises realizadas neste trabalho, verificou-se que o albenda-zol apresenta trˆes formas polim´orficas (formas I, II e III). Em conformidade com as compara¸c˜oes entre os difratogramas experimentais das amostras e dados da literatura constatou-se que a forma I corresponde `a mat´eria prima, forma comercialmente dis-tribu´ıda, j´a a forma II corresponde ao arquivo SUTWIO depositada por Pranzo e seus colaboradores e por sua vez a forma III ´e correspondente `a recristaliza¸c˜ao da forma I em metanol o que condiz com o arquivo BOGFUS tamb´em depositado na base de dados da Cambridge Structural Data base (CSD).
Observou-se a partir das curvas de DSC que na faixa de temperatura en-tre 150o
C e 220o
C ocorreram dois eventos –endot´ermico e exot´ermico, correspondendo, respectivamente, `a fus˜ao da forma polim´orfica III seguida da recristaliza¸c˜ao na forma I, indicando que transi¸c˜ao entre ambas ´e irrevers´ıvel. Processo tamb´em evidenciado pela ter-momicroscopia. As curvas TG indicaram que a decomposi¸c˜ao t´ermica da amostra ocorreu a partir de 220o
C, fato revelado pela perda de massa nesta mesma faixa de temperatura. Nos espectros de FTIR foi poss´ıvel verificar diferen¸cas entre algumas bandas de absor¸c˜ao. Atribuindo vibra¸c˜oes em regi˜oes distintas. Caracterizando, portanto, diferentes formas polim´orficas.