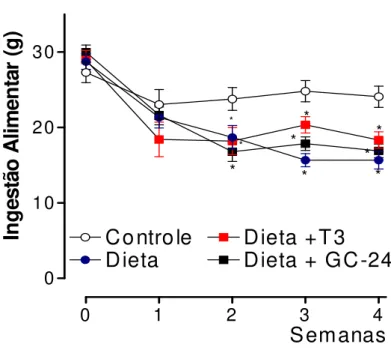
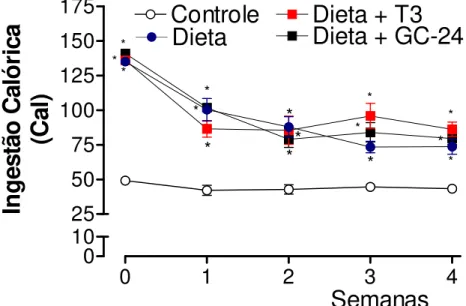
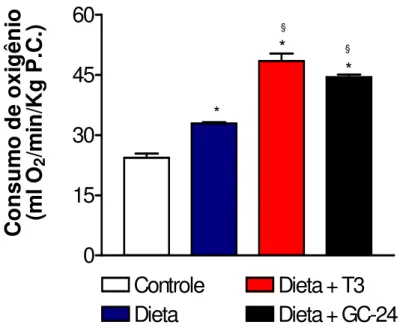
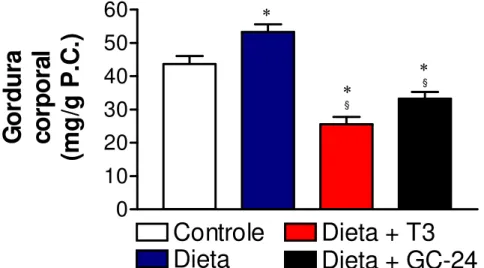
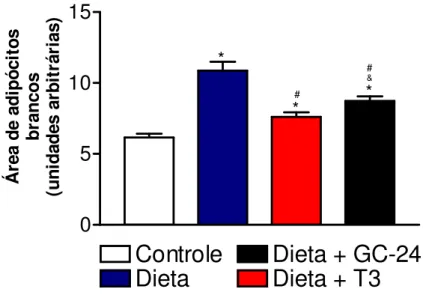
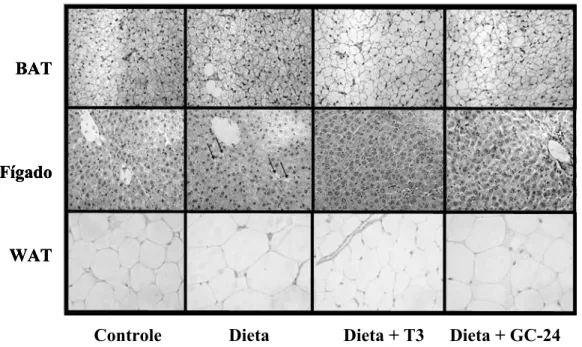
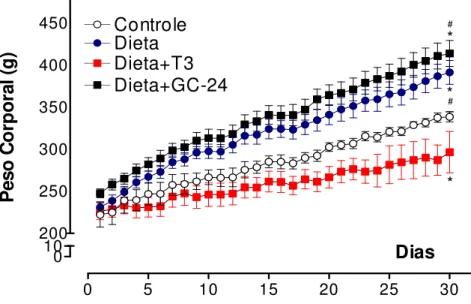
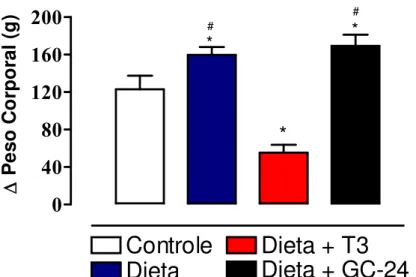
Papel do TR na termogênese induzida pela dieta
Texto
Imagem
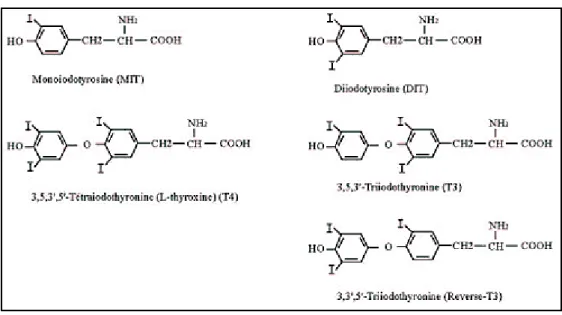
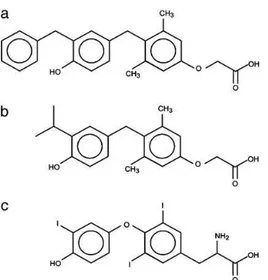
Outline
Documentos relacionados
Atualmente, segundo a Faculdade de Artes do Paraná, o Curso de Dança em seu currículo reformulado, parte do entendimento da dança como área de conhecimento, tendo
No que se refere à obtenção de uma envoltória espectral de fala, a técnica de suavização linear do espectro logarítmico generalizado (log-gen) pode ser compreendida com
(15) Exemplo: em Rio Grande o Governo mantém até hoje confiscado parte do terreno com (Tédio escolar - hoje construção nova, executada pelo Governo - da
Em Campinas, São Paulo, o Ambulatório de Violência contra Criança e Adolescentes (VCCA), localizado no Hospital das Clínicas (HC) da Universidade Estadual de
In line with these findings, this dissertation further explores the investigation and measure of effects of different visual representations concerning an e-commerce
Trabalhar com Blogs para auxiliar a aprendizagem de conteúdos matemáticos, ou desenvolver o pensamento geométrico com base nas técnicas de dobraduras não é algo
Este trabalho se justifica pelo fato de possíveis aportes de mercúrio oriundos desses materiais particulados utilizados no tratamento de água, resultando no lodo
Em relação ao art. 557 do CPC, muitos também afirmam a sua importância normativa para embasar este processo de aproximação entre os modelos de controle