Instituto de Biociências
Análise de SNPs nos genes
SLC6A3 e DRD2 em portadores de
gagueira desenvolvimental
persistente do Estado de São Paulo
Bianca Santos Domingues
Orientador: Prof. Dr. Danilo Moretti-Ferreira
Co-orientador: Msc. Carlos Eduardo Frigério Domingues
Monografia apresentada ao Departamento de Genética do Instituto de Biociências de Botucatu - UNESP, dentre os requisitos para obtenção do título de Bacharel em Ciências Biomédicas.
Botucatu–SP
FICHA CATALOGRÁFICA ELABORADA PELA SEÇÃO TÉC. AQUIS. TRATAMENTO DA INFORM. DIVISÃO DE BIBLIOTECA E DOCUMENTAÇÃO - CAMPUS DE BOTUCATU - UNESP
BIBLIOTECÁRIA RESPONSÁVEL: ROSEMEIRE APARECIDA VICENTE
Domingues, Bianca Santos.
Análise de SNPs nos genes SLC6A3 e DRD2 em portadores de gagueira desenvolvimental persistente do Estado de São Paulo / Bianca Santos Domingues. - Botucatu, 2010
Trabalho de conclusão de curso (bacharelado - Ciências Biomédicas) - Instituto de Biociências de Botucatu, Universidade Estadual Paulista, 2010
Orientador: Danilo Moretti-Ferreira
Co-Orientador: Carlos Eduardo Frigério Domingues Capes: 20205007
1. Distúrbios da fala. 2. Gagueira. 3. São Paulo (Estado).
Palavras-chave: Gagueira desenvolvimental; Gene SLC6A3; Gene DRD2; SNPs; PCR em tempo real.
Agradecimentos
À Universidade Estadual Júlio Mesquita Filho –UNESP- Campus Botucatu e de todo o
corpo docente e funcionários pelo aprendizado e infra-estrutura concedidos.
Ao Instituto de Biociências de Botucatu, sua direção, corpo docente e funcionários.
Ao Departamento de Genética por disponibilizar toda sua estrutura para a realização
desse trabalho.
Ao Serviço de Aconselhamento Genético–SAG e todos os seus funcionários.
À Fundação de Amparo à Pesquisa do Estado de São Paulo–FAPESP- pela Bolsa de
Iniciação Científica no período no período de abril de 2010 à dezembro de 2010 (Ref.
Proc. 2010/00501-1).
Ao Prof. Danilo Moretti-Ferreira, pela orientação, ensinamentos e auxílio.
Às famílias e controles integrantes deste estudo pela disponibilidade e compreensão
da importância do mesmo para outras famílias afetadas.
Agradecimentos Especiais
Aos meus pais, Hoover Domingues Júnior e Eliana Santos Domingues, que abdicaram
de tantas coisas para me fazerem feliz e proporcionar um futuro de grande sucesso. À
eles que sempre me apoiaram não importando minha escolha, me deram forças para
continuar quando eu achava que não conseguiria mais prosseguir e acreditaram em
mim mesmo em momentos que eu não acreditava.
Aos meus avôs que me apoiaram e rezavam para que eu conseguisse tudo que
desejei.
As minhas amigas, Fernanda Yamamoto, Isabela Romani e Thaís Isabela, que
conviveram comigo nestes quatro anos de faculdade fazendo com que mesmo os
momentos de mais difíceis ficassem suportáveis. À elas eu agradeço por terem me
proporcionado alguns dos melhores momentos da minha vida.
À minha vizinha e caloura, Niele, que se mostrou uma ótima amiga, me consolando ou
dando bronca quando achava necessário, mas, acima de tudo, me defendendo
quando fosse preciso.
Ao meu co-orientador, Carlos Eduardo, pela paciência e tempo despendidos para me
ensinar o cotidiano de um laboratório de genética molecular, além de proporcionar
uma amizade sincera.
Aos meus colegas de SAG, Gustavo Henrique Vieira, Bruno Gamba, Breila V. de
Oliveira, Deise Helena de Souza e Rosana Bicudo.
“Sonhe com aquilo que você quer ser, porque você possui apenas uma vida e nela só se tem uma chance de fazer aquilo que quer. Tenha felicidade bastante para fazê-la doce. Dificuldades para fazê-la forte. Tristeza para fazê-la humana. E esperança suficiente para fazê-la feliz. As pessoas mais felizes não tem as melhores coisas.
Elas sabem fazer o melhor das oportunidades que aparecem em seus caminhos. A felicidade aparece para aqueles que choram. Para aqueles que se machucam Para aqueles que buscam e tentam sempre. E para aqueles que reconhecem a importância das pessoas que passaram por suas vidas.”
Índice
1. INTRODUÇÃO...7
1.1. Definição...7
1.2. Classificação...8
1.3. Prevalência...10
1.4. Diagnóstico...10
1.5. Etiologia da doença...11
1.6. Aspectos biológicos da gagueira...13
2. JUSTIFICATIVAS E OBJETIVOS...17
3. MATERIAL E MÉTODOS...17
3.1. Casuística...17
3.1.1.Critérios fonoaudiológicos de inclusão...18
3.1.2.Critérios fonoaudiológicos de exclusão...18
3.1.3.Diagnóstico de gagueira e seleção...19
3.2. Aspectos éticos...19
3.3. Coleta e purificação de material biológico...20
3.4. Análise Molecular...21
4. RESULTADOS...25
4.1. Grupo amostral...25
4.2. Genotipagem...26
4.3. Análise Estatística...29
5. DISCUSSÃO...29
6. CONCLUSÃO...33
7. REFERÊNCIAS BIBLIOGRÁFICAS...34
8. ANEXOS...42
8.1. Aprovação do comitê de ética...42
8.2.Termo de Consentimento Livre e Esclarecido...43
1. INTRODUÇÃO
1.1. Definição
A linguagem é todo e qualquer sistema de signos que serve como meio de
comunicação de idéias ou sentimentos através de sinais convencionados, podendo ser
percebida pelos diversos órgãos dos sentidos (Almeida, 2005). Quando ocorrem
dificuldades nos processos de aquisição e desenvolvimento da linguagem oral, podem
ocorrer vários distúrbios e, entre eles, encontram-se os relacionados com a fluência
(Duarte et al., 2009).
Fluência é o aspecto da produção da fala que se refere a continuidade,
suavidade, velocidade e/ou esforço com as quais as unidades fonológicas, lexicais,
morfológicas e /ou sintáticas da linguagem são faladas (Andrade et al., 2001). A
disfluência é a fala espontânea que apresenta-se com pausas, prolongamentos,
repetições, substituições, deleções e inserções (Moniz et al., 2010).
Todos os indivíduos apresentam incertezas linguísticas devido a formulação de
frases (Perkins, 1990) caracterizando os momentos de disfluências típicas (Yairi et al.,
1992a; Bloodstein, 1995), no entanto existem também as repetição ao nível de
fonema; alongamento de sons; bloqueios na fonação; pausas silenciosas que
caracterizam as disfluências atípicas relacionadas ao comportamento dos indivíduos
gagos (Yairi et al., 1992a).
A gagueira é o mais comum e conhecido dos distúrbios da comunicação
relacionados a fluência. Segundo a Classificação Internacional de Doenças
(Organização Mundial de Saúde/CID-10) e o Manual Diagnóstico e Estatísco de
Doenças Mentais (DSM-IV,1994) a gagueira é definida como sendo “a fala que é
caracterizada pela frequência de repetições ou prolongamentos de sons, palavras ou
da fala”, bem como pela perturbação na fluência e padrão de tempo normal da fala
influenciando no rendimento escolar, profissional e/ou na comunicação social.
Os indivíduos gagos também podem apresentar determinados
comportamentos, chamados de “acessórios”, “secundários” ou “compensatórios”, que
envolvem um grupo de reações, estratégias, truques, comportamentos de evitação ou
fuga que são usados quando se gaguejam ou em antecipação ou medo de gaguejar
(Andrade et al., 2001). O surgimento de comportamentos como o medo e ansiedade
podem estar relacionados diretamente à incorporação da idéia de um distúrbio na fala
(Bloodstein, 1995), o que ocasionaria frustração em decorrência do tempo excessivo e
dos esforços dispensados na fala disfluente, embaraço, vergonha, culpa e até mesmo
hostilidade para com os companheiros de conversa seguidos aos episódios de
gagueira (Van Riper, 1982).
1.2.
Classificação
Segundo Andrade et al. (2001) a gagueira pode ser classificada em três tipos
de acordo com sua origem: a) neurogênica, que é iniciada ou mantida como um
resultado de injúria ou lesão neurológica específica e identificável (Helm-Estabrooks,
1993); b) psicogênica, refere-se a gagueira que é sintoma principal de alguma forma
de psicopatologia verificável (Roth et al., 1989); c) desenvolvimental, que é iniciada
durante o desenvolvimento cerebral dos indivíduos (0 à 18 anos) sem causas
neurogênicas ou psicogênicas associadas.
Quanto à gagueira desenvolvimental, esta foi subdividida por Yairi et al.
(1996b) dependendo do número de indivíduos afetados em uma família, em: familial,
presente em dois ou mais indivíduos da mesma família; ou isolada, apenas um caso
tempo de instauração da afecção: persistente, quando o indivíduo continua a
apresentar gagueira 36 meses ou mais após a instauração; recuperação tardia,
quando o indivíduo apresenta recuperação entre 18 e 36 meses após sua instauração;
e recuperação precoce, quando o indivíduo apresenta recuperação antes de 18 meses
após sua instauração. O organograma abaixo (figura 01) representa
esquematicamente todo o processo de classificação da gagueira.
Gagueira
Neurogênica Psicogênica Desenvolviment al
Familial
Persist ent e Recuperaçãot ardia Recuperação precoce
Isolada
Persist ent e Recuperaçãot ardia Recuperação precoce
Figura 01. Organograma de classificações da gagueira segundo Andrade et al.(2001) e Yairi et al. (1996b).
Desta forma, nossos estudos têm como alvo a gagueira desenvolvimental
persistente familial, que diferentemente das outras, ocorre à partir dos 6 anos de idade
(Bloodstein 1995), na fase de formação de palavras ou frases longas e sintaticamente
complexas (Karniol 1995; Natke et al, 2002) e de incorporação da idéia de disfluência
na fala fazendo com que nesse período se tornem mais pronunciados os sintomas
1.3.
Prevalência
A gagueira desenvolvimental persistente familial pode ocorrer em pessoas de
todas as etnias, nacionalidades e classes sociais. Acomete 5% das crianças com
média de idade entre os 4 anos, com maior prevalência do sexo masculino (2H:1M)
(Yairi et al., 1992b).
Os casos de recuperação espontânea implicam em uma redução da incidência
entre os adultos afetados à uma taxa que pode variar de 0,75% a 1% (Buchel et al.,
2004), a qual ocorre em crianças antes dos 6 anos, principalmente, em indivíduos do
sexo feminino (Ambrose et al.,1997) (4H:1M) (Yairi et al.,1996a; Drayna et al.,1999).
Tendo em vista as frequências de ocorrência da afecção na população mundial
estima-se que a prevalência da doença seja de 2,1%, 2,8% em crianças de 2 à 5 anos
e 3,4% em crianças de 6 à 10 anos (Craig et al., 2002). Entretanto, o grau de
parentesco é um fator que pode alterá-la: 18% em irmãos do mesmo sexo
(Andrews,1983) e 41,5% em parentes de primeiro grau (Lewis et al., 1993; Tallal et
al.,1989;Tomblin,1989).
1.4. Diagnóstico
Baseando-se no Manual de Diagnóstico e Estatística das Pertubações Mentais
(DSM-IV) (1994), os critérios para o diagnóstico da gagueira desenvolvimental
persistente são:
x Pertubação na fluência e padrão de tempo normal da fala ;
x Pertubação na fluência interferindo no rendimento escolar e profissional ou na
comunicação social;
x Presença de um déficit motor da fala, sensorial, as dificuldades na fala
1.5.
Etiologia da doença
A gagueira é considerada um distúrbio de caráter multifatorial que sofre
influência de fatores biológicos e ambientais (Andrade et al., 2001). Como fator
ambiental podemos destacar o emocional que pode afetar o desenvolvimento da
afecção ou sua severidade por meio de fatores pessoais e conflitos familiares (Brito
Pereira, 2002).
Dentre os fatores biológicos, os únicos que podem apresentar significância
quanto ao desenvolvimento da doença são: o histórico pré-natal, médico, de
desenvolvimento, lingaguem e genético (Cox et al., 1984; Buchel et al., 2004;
Felsenfeld et al., 2000). Apesar da contribuição genética para a gagueira não estar
totalmente esclarecida, têm-se referência à sua importância pelos estudos com
gêmeos monozigóticos e dizígóticos, estudos de adoção e o número de casos de
gagueira encaminhados as clínicas fonoaudiólogicas com quadros severos e histórico
familiar positivo para esta disfluência (Drayna, 1999).
1.5.1. Fatores genéticos
Diversos indicativos tem demonstrado uma possível relação de causalidade
entre a existência de fatores genéticos predisponentes e a manifestação da gagueira
(Yairi, 1998).
Entre os principais argumentos que fundamentam os fatores genéticos na
gagueira, são citados: 1) maior concordância entre gêmeos monozigóticos (62,5% a
90%) que em gêmeos dizigóticos (6,6% a 9%) (Howie, 1981; Felsenfeld et al., 2000;
Ooki et al., 2005; Dworzynski et al. , 2007), 2) a gagueira, é mais propensa a se
desenvolver em indivíduos consangüíneos do que nos casos em que os indivíduos
afetados não tenham essa relação (Andrews et al. 1991; Felsenfeld & Plomin, 1997,
entre gagos, como repetições, prolongamentos de sons e sílabas de palavras sem
estarem ligadas a diferenças de língua e cultura (Bloodstein, 1995, Wingate, 1964;
Felsenfeld e Plomin, 1997; Bloodstein, 1981) .
A busca de genes que influenciem características complexas tem sido muito
mais desafiadora do que os estudos genéticos de traços mendelianos (Botstein &
Risch, 2003). Existem vários fatores que contribuem para este problema, incluindo a
heterogeneidade etiológica e genética e, a necessidade de modelos genéticos
complexos com muitas variáveis para efeitos de lócus, interações gene e
gene-ambiente, o que justifica o uso de diversos métodos estatísticos. Um método
adequado de análise genética para a gagueira exige, uma combinação de passos para
a identificação de regiões cromossômicas, nas quais residem variações genéticas e
que caracterizam a etiologia complexa desta afecção (Wittke-Thompson, 2007).
O fato da contribuição genética para a gagueira não estar totalmente
esclarecido torna o conhecimento sobre sua etiologia complexo. No entanto o modelo
mais aceito é aquele em que um gene principal promove a susceptibilidade à doença,
e outros fatores (biológicos e ambientais) regulariam-no, o que explicaria, ao menos
em parte, as formas variáveis de gagueira: moderada e severa, bem como de sua
recuperação espontânea ou não (Yairi, 1998 e 1999), porém sem explicar as formas
de herança (Kidd,1977).
Viswanath et al. (2004) ao analisarem a segregação em 56 famílias com
gagueira persistente, firmaram a possibilidade da existência de um gene principal com
transmissão mendeliana dominante e salientaram que neste modelo a penetrância
desse gene dependeria do sexo e da existência ou não, de parentes gagos.
Contradizendo seus antecessores, Alm et al. (2006) sugeriram que talvez não existisse
um único modelo de transmissão, mas sim vários deles, mais frequentes para cada
Devido à possibilidade de existirem várias formas de susceptibilidade à doença,
variáveis para cada população, e sendo a população do Estado de São Paulo
miscigenada devido a uma história de continuas imigrações para o nosso país, torna a
abordagem da gagueira, quanto aos aspectos genéticos, significativamente relevante,
ao ponto de estabelecer-se como um marco comparativo em relação à outras
populações no estudo dessa doença complexa.
1.6.
Aspectos biológicos da gagueira
Na literatura não há casos de gagueira relacionados a alterações em estruturas
como: nariz; boca; faringe; e laringe, devido a tradução de uma proteína anômala,
causando a gagueira (Yaruss et al., 2003), no entanto em dezenas de estudos de
neuroimagem se observaram alterações estruturais e funcionais em indivíduos gagos,
não verificadas em pessoas fluentes (Foundas et al., 2001; Sommer et al., 2002).
Estudos de dosagens bioquímicas, tais como: variações nas concentrações de
cálcio; prolactina; estrógeno; e estudos dos receptores e transportadores
dopaminérgicos, bem como lesões neurológicas e dos níveis de ansiedade tem sido
relacionadas como possíveis fatores biológicos colaboradores no surgimento e/ou
agravamento da afecção (Wu et al., 1997; Maguire et al., 2004; Alm et al.,2006; Lan et
al., 2009).
As diferenças neurais entre indivíduos fluentes e disfluentes, tem sido
estudadas por meio de exames de eletroencefalograma (EEG), Tomografia por
Emissão de Positron (PETscan), Ressonância Magnética com Imagem Funcional
(fMRI) e Tensor de Difusão de Imagem (DTI), os quais têm embasado as teorias
fisiopatológicas em relação a gagueira.
Dentre as hipóteses, a de maior impacto no mundo científico é em relação a
de compensação pelo lado esquerdo anômalo nas áreas pré-motoras, motoras e
auditórias (Travis, 1978; Moore et al., 1980; Braun et al., 1997; Salmelin et al., 1998;
Fox et al., 1996 e 2000; Buchel et al., 2004).
Nudelman et al. (1992) demonstraram em seus trabalhos, a interação de quatro
sistemas neurais na produção do discurso fluente, três deles senso-motores e um
cognitivo, o qual foi separado em duas alças (loops): a) uma medial, que programa e
monitora os sons que estão sendo emitidos; b) uma lateral, que escolhe as palavras a
serem pronunciadas, sendo esta última preservada nos gagos e passível de ativação
através do canto; enquanto que a outra, estaria sob influência do neurotransmissor
dopamina, portanto permanecendo prejudicada.
Wu et al. (1995; 1997) por meio de PETscan com marcador 6-fluorodopa
analisaram as atividades dopaminérgicas pré-sinápticas no cérebro de indivíduos
gagos. Os resultados obtidos revelaram sinais de captação significativamente maior
em indivíduos disfluentes em relação aos controles, em diversas áreas, tais como:
córtex pré-frontal medial, córtex orbital profundo, córtex insular, amígdala extendida,
córtex auditório, núcleo caudado, límbico cortico ventral e em regiões subcorticais do
cérebro, além de uma diminuição do metabolismo de glicose nas áreas de Broca e
Wernicke e pólo frontal relacionadas ao processamento da fala e da linguagem
fonológica e semântica. Entretanto, Fox et al (1996) em seus trabalhos, revelaram que
a hiperatividade cerebral pré-motora encontrada em indivíduos gagos estaria
conectada tanto ao tálamo quanto ao gânglio basal.
Ludlow e Loucks (2003) ressaltam a função dos gânglios da base no apoio e
modulação da comunicação rápida entre as regiões de fala específicas, sugerindo que
a gagueira poderia refletir a instabilidade do controle motor da fala mais do que a
perda da função. Esta visão é apoiada devido a casos de surgimento de episódios de
implante do aparelho de estimulação cerebral profunda que é inserido próximo a área
do globo pálido interno (Allert et al., 2010; Nebel et al., 2009; Benke et al., 2000; Koller
et al., 1983; Burghaus et al., 2006).
Concomitante aos estudos de neuroimagem em indivíduos disfluentes,
realizavam-se estudos funcionais e moleculares em pacientes com Síndrome de
Tourette(ST). Os resultados obtidos sugeriram uma redução dos gânglios da base,
sendo estes atuantes na coordenação dos movimentos motores, e alteração de
gene(s) que auxiliam na metabolização de neurotransmissores, principalmente a
dopamina. Devido as semelhanças no esforço de produção da fala disfluente e os
tiques vocais apresentados por indivíduos afetados com ST, a hipótese de que ambas
afecções fossem ocasionadas pelas mesmas alterações foi levantada (Comings, et al.,
1990; Maguire, et al., 2004).
Em busca dos fatores genéticos que explicassem as alterações anatômicas
encontradas no sistema nervoso dos indivíduos gagos é que se iniciaram estudos
genéticos através de marcadores moleculares específicos em estudos de associação
e ligação. Shugart et al. (2004), foram os primeiros, à partir da análise de 68 famílias
norte-americanas e européias, que apontaram para diferenças significativas nos
marcadores do cromossomo 18 (análise de ligação não-paramétrica escore >5 em 18p
e >2,5 em 18q proximal), sugerindo a existência de um locus de predisposição à
doença.
Riaz et al. (2005) analisando o genoma de 56 famílias paquistanesas
consanguíneas com gagueira, revelaram evidências mais fortes de uma ligação
genética. À partir de análises de ligação não-paramétrica, observaram-se resultados
significativos na região cromossômica 12q.
Suresh et al.(2006), através da análise de ligação do genoma, pautado no
israelenses, obtiveram indícios de ligação no cromossomo 9 em indivíduos gagos,
persistentes e recuperados; e no cromossomo 15 nos gagos persistentes. Além disso,
foram observadas evidências de ligação sexo-específico no cromossomo 7 em
homens e no cromossomo 21 em mulheres.
Wittke-Thompson et al. (2007), em uma população de isolado consanguíneo,
huteritas (grupo consanguíneo norte europeu) foi possível identificar ligações
sugestivas nos cromossomos 3, 13 e 15.
Mais recentemente, Lan et al. (2009) estudaram e compararam, em indivíduos
gagos e fluentes, cinco SNP para os genes receptores (na região cromossômica
11q23) e transportadores dopaminérgicos (na região cromossômica 5p15.3). Deste
estudo verificaram-se que dos cinco SNPs testados o único que apresentou resultados
significantes foi um dos relacionados ao gene do receptor de dopamina, DRD2, no
qual a presença do alelo T no polimorfismo rs6277 foi tido como um fator protetor para
o aparecimento da gagueira e, conseqüentemente, o aumento do genótipo CC foi
considerado fator de risco para a afecção.
Em 2010, Kang et al. ao estudarem famílias paquistanesas e casos isolados de
gagueira da América do Norte, através da análise de ligação no braço longo do
cromossomo 12, observaram a recorrência de uma mutação (G3598A). Tal mutação
por alterar o tipo de aminoácido (substituição de um ácido glutâmico por uma lisina) na
enzima sintetizada pelo gene GNPTAB (N-acetylglucosamine-1-phosphate
transferase, alpha and beta subunits), implicou numa mudança em sua conformação
estrutural que impede a mesma de conduzir a enzima 6- fosfatomanose ao lisossomo.
Raza et al. (2010) estudaram famílias com diversos indivíduos afetados através
da análise de ligação paramétrica de 6090 SNP´s. Os resultados mostraram um LOD
escore de aproximadamente 4,92 para marcadores na região q do cromossomo 3 em
2. JUSTIFICATIVAS E OBJETIVOS
As descobertas dos fatores moleculares predisponentes da afecção
contribuiriam significativamente com a prevenção, diagnóstico, por meio de testes
moleculares, e o tratamento dos indivíduos portadores, evitando-se assim, possíveis
traumas em crianças submetidas sem necessidade a tratamentos intensivos, por
vezes tornando o que seria uma gagueira infantil recuperável em uma gagueira
psicogênica persistente. Desta forma, propomos de maneira inédita e pioneira na
população do Estado de São Paulo (Brasil) a realização deste trabalho que tem como
ojetivo principal:
x Avaliar e comparar, por meio de análises estatísticas e ferramentas de
bioinformática, o polimorfismo de cinco SNPs, já descritos na literatura,
presentes nos genes receptores e transportadores dopaminérgicos
(SLC6A3 e DRD2), em dois grupos: um de portadores de gagueira
desenvolvimental persistente familial do Estado de São Paulo e outro de
controles fluentes, do Estado de São Paulo, pareados por sexo.
3. MATERIAL E MÉTODOS
3.1.
Casuística
Este projeto contou com a participação de dois grandes núcleos institucionais
colaboradores, responsáveis pela triagem, diagnóstico e terapia dos pacientes e
familiares com gagueira desenvolvimental persistente familial, o Centro de Estudos da
Educação e da Saúde (CEES – Marília – Unesp) e o Departamento de
Fonoaudiologia, Fisioterapia e Terapia Ocupacional da Faculdade de Medicina da USP
(FOFITO – São Paulo – FMUSP), coordenados pelo Serviço de Aconselhamento
A casuística deste estudo foi composta por 100 indivíduos: a) grupo amostral,
com 50 probandos com gagueira persistente desenvolvimental familial, pertencentes à
famílias distintas, já selecionadas em estudos preliminares de Canhetti-Oliveira (2004),
Costa (2005), Domingues (2009), provenientes das clínicas escolas dos centros
supracitados e selecionados independente do número de membros da família, sem
distinção de sexo, raça, escolaridade e nível sócio-econômico-cultural, provenientes
do Estado de São Paulo; b) grupo controle, com 50 indivíduos fluentes (alunos de
graduação e pós-graduação) oriundos do Instituto de Biociências de Botucatu, sem
vínculos acadêmicos com o grupo responsável pela pesquisa, e pareados por sexo.
Após a avaliação fonológica dos indivíduos afetados, os pais, os próprios
indivíduos (adultos) ou a família receberam a devolutiva dos resultados da avaliação.
Informações sobre a gagueira foram oferecidas por meio de orientações e instruções
com o auxílio de um informe especialmente elaborado para esta finalidade. Os casos
que necessitaram de terapia foram mantidos nas clínicas dos centros colaboradores
supracitados para a intervenção fonoaudiológica.
3.1.1. Critérios fonoaudiológicos de inclusão
Os requisitos de inclusão dos indivíduos foram: ser falante nativo do português
brasileiro; ter idade acima de 6 anos; apresentar histórico familial positivo para a
gagueira, ou seja, apresentar no mínimo outro parente gago; e apresentar quadro de
gagueira há mais de seis meses, sem remissão.
3.1.2. Critérios fonoaudiológicos de exclusão
Os critérios de exclusão para o grupo de probandos foram: apresentar qualquer
distúrbio neurológico, genético ou não, nos probandos ou familiares, tais como
distonia, doenças extras piramidais, deficiência mental, epilepsia, transtorno do déficit
alterações de comunicação oral não compatíveis com a idade; apresentar perda
auditiva condutiva ou neurossensorial; e outras condições pertinentes que possam
gerar erros no diagnóstico.
3.1.3. Diagnóstico de gagueira e seleção
O diagnóstico de gagueira do participante foi estabelecido a partir da
metodologia de coleta da amostra de fala proposta por Andrade (2000) – fala
auto-expressiva obtida num mínimo de 200 sílabas expressas (fluentes), eliciada por
estímulo visual de figura (adaptada às diferentes faixas etárias).
A partir da análise da amostra de fala foram considerados participantes do
estudo aqueles que apresentaram no mínimo 3% de rupturas gagas (Yairi et al.,
1992b) e receberam 11 pontos ou mais (gravidade = leve) no Stuttering Severity
Instrument – 3 (SSI-3) (Riley, 1994). Em cada centro colaborador, foi solicitado o
parecer de dois profissionais com experiência no diagnóstico e na intervenção
fonouadiológica dos distúrbios da fluência de modo a garantir a confiabilidade do
diagnóstico. As análises das disfluências foram realizadas
a partir do registro audiovisual da fala dos candidatos à pesquisa (probando e seus
familiares).
3.2.
Aspectos éticos
Para a participação nos estudos prévios, todos os responsáveis presentes na
consulta fonoaudiológica foram informados sobre os objetivos da pesquisa e
esclarecidos sobre os procedimentos adotados para a anuência e assinatura do Termo
de Consentimento Livre e Esclarecido (TCLE). Com a concordância em participar da
pesquisa, foi solicitado, em cada instituição envolvida no projeto, o preenchimento do
TCLE específico e nos termos da Resolução CONEP/CNS196/1996, 340/2004 e
indivíduos, para o armazenamento de amostras de DNA em um banco, em freezer -
80°C, sob responsabilidade do Instituto de Biociências de Botucatu/UNESP, conforme
o protocolo 3440-2010, aprovado pelo Comitê de Ética da Faculdade de Medicina de
Botucatu (Anexo 8.1).
Desta forma foi constituído o Banco de DNA das 50 famílias, das quais os 50
probandos com gagueira desenvolvimental persistente foram analisados neste
presente estudo. A todos os indivíduos foi, solicitado novo TCLE, específico, nos
termos das resoluções do CONEP, supracitados (Anexo 8.2).
Para a constituição do grupo controle, realizou-se um convite aos alunos para
participar do projeto. Uma vez aceito, estes foram submetidos aos mesmos critérios de
inclusão e exclusão e, após assinatura de TCLE, foi realizado diagnóstico, a fim de
certificarmos de que se tratavam de apenas indivíduos fluentes. Isto posto, foram
coletadas amostras de material biológico para a construção de um banco de DNA de
indivíduos controles.
3.3.
Coleta e purificação de material biológico
De todos os indivíduos participantes deste projeto foram coletados 4 ml de
sangue periférico , armazenado em tubo contendo anticoagulante EDTA a 6% (frasco
Vacuette® EDTA 4 ml) os quais foram purificados com o kit comercial de extração
Wizard® Genomic DNA Purification Kit (Promega, Madison, WI - USA). Após seu
processamento as quantificações foram realizadas através de leitura em
espectrofotometria UV - plataforma ND-1000 Spectrophotometer da NanoDropTM
(Thermo Fisher Scientific Inc.- Wilmington, Delaware - USA) a partir de 1 l de solução
As amostras tiveram sua concentração final ajustada para 20ng/ l as quais
foram quantificadas em triplicata, visando minimizar possíveis erros de pipetagem e
garantir a sua reprodutibilidade nos ensaios.
3.4.
Análise Molecular
3.4.1. Técnica de PCR em tempo real
A técnica de PCR (reação em cadeia de polimerase) permite a amplificação de
regiões específicas do genoma milhares de vezes. A técnica do PCR em tempo real,
também conhecida como PCR cinético, permite além da amplificação, a quantificação
de uma determina molécula de DNA presente em uma reação de PCR. Existem dois
tipos de PCR em tempo real: os baseados em sondas (TaqMan) e em agentes
intercalantes (SyberGreen). Ambos os métodos requerem um termociclador especial
equipado com uma câmera sensível que monitora a fluorescência em cada poço da
placa em intervalos freqüentes durante a reação de PCR.
O sistema TaqMan® utiliza uma sonda que consiste de dois fluoróforos
(quencher e repórter), enquanto a sonda encontra-se integra e ligada a fita de DNA
molde, o quencher reduz a fluorescência do corante repórter. Durante o processo de
PCR a sonda TaqMan ® e os iniciadores se anelam ao DNA, enquanto a Taq
polimerase inicia a criação de uma cadeia complementar a fita de DNA molde. Ao
adicionar os nucleotídeos, a Taq polimerase remove a sonda Taqman®, separando o
quencher e o repórter e permitindo que o mesmo emita sua energia que será
quantificada pelo programa específico para a interpretação do sinal de fluorescência.
3.4.2. Genotipagem
A genotipagem foi realizada através da PCR em tempo real e sistema
reação (Saiki et al., 1985), para tal duas sondas foram inseridas em cada reação o que
permitiu avaliar duas variantes para cada um dos polimorfismos de nucleotídeo único
estudados. O corante VIC se anelou a extremidade 5´do alelo 1 e o corante FAM, à
extremidade 5´do alelo 2.
As reações foram realizadas em um termociclador ABI StepOne™ Real-Time
PCR System (Applied Biosystems) de acordo com o protocolo da empresa, porém
uma versão otimizada. O programa StepOne™v2.1 foi utilizado na captação, análise e
caracterização dos genótipos.
Neste projeto foram genotipados três SNP´s presentes no gene SLC6A3 e dois
presentes no gene DRD2 . A escolha destes polimorfismos foi realizada a partir do
trabalho de Lan et al. (2009), através do banco de dados dbSNP
(http://www.ncbi.nlm.nih.gov/projects/SNP/) e do programa ABI SNPbrowser™ v 4.0
(Applied Biosystems) os quais já apresentavam esses ensaios disponíveis (tabela 01).
Tabela 01. Caracterização dos SNPs selecionados. Região
cromossômica Gene Éxon RefSNP ID
Troca de alelo
Tipo de mutação
Alteração de aa
5p15.3 DRD2
2 rs2617604 124C>T Não-sinônima Leu42Phe
13
rs28364998 1692C>T Sinônima Ile564Ile
rs28364997 1676CC>T Não-sinônima Ala559Val
11q23 SLC6A3 7
rs6277 957C>T Sinônima Pro319Pro
rs6275 939T>C Sinônima His313His
De acordo com a base de dados dbSNP
(http://www.ncbi.nlm.nih.gov/projects/SNP/) e o HapMap
gene DRD2 (rs6275 e rs6277) está bem caracterizada apresentando-se polimórfica
nas mais diferentes populações, porém quanto ao gene SLC6A3 (rs2617604,
rs28364998 e rs28364997) estes têm-se apresentado não informativos (não
polimórficos) ou mesmo sem caracterização quanto as suas frequências alélicas
(tabela 02 e 03).
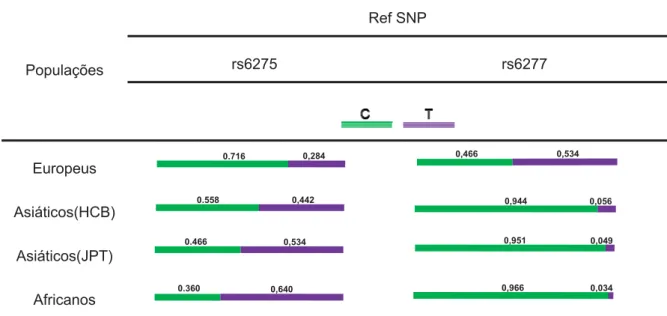
Tabela 02. Frequência alélica para SNPs rs6275 e rs6277 no gene SLC6A3
Populações
Ref SNP
rs6275 rs6277
Europeus
Asiáticos(HCB)
Asiáticos(JPT)
Africanos
0.716 0,284 0,466 0,534
0.558 0,442 0,944 0,056
0.466 0,534 0,951 0,049
Tabela03. Frequência alélica para SNPs rs2617604, rs28364997 e rs28364998 no gene DRD2
Populações
Ref SNP
rs2617604 rs28364997 rs28364998
Europeus N/A N/A
Asiáticos(HCB)
1,000
N/A N/A
Asiáticos(JPT)
1,000
N/A N/A
Africanos
1,000
N/A N/A
1,000
As reações de PCR em Tempo Real e genotipagem foram compostas por:
TaqMan® SNP Genotyping Master Mix (Applied Biosystems); TaqMan® Genotyping
Assay Mix (Applied Biosystems); água livre de RNAse e DNA à 20ng/μl. As reações
foram preparadas conforme as especificações do fabricante e posteriormente
otimizadas a um volume final de reação menor (tabela 04).
Tabela 04. Componentes da reação de PCR.
Reagentes Concentração (reação) Volume (μl)
TaqMan® Genotyping Master Mix (2X) 1X 5,0
SNP Genotyping Assay Mix (20X) 1X 0,5
DNA molde diluído em água (20ng/ μl) 3,3 ng/μl 1,0
Água estéril (RNAse free) 3,5
Volume Final
Em cada ensaio realizado, além das amostras de DNA foram aplicados dois
controles negativos, a fim de garantir de que não havia qualquer tipo de contaminação
passível de interferência nas análises.
3.4.3. Procedimentos Analíticos
As freqüências alélicas dos SNPs, bem como o estudo de associação dos
fenótipos (gago e fluente) em relação aos marcadores, utilizando-se do teste do
Qui-quadrado, pautado no equilíbrio de Hardy-Weinberg foram estimadas usando o
programa Haploview (Broad Institute – Cambridge – MA - USA) disponível
gratuitamente em (http://www.broadinstitute.org/haploview).
4. RESULTADOS
4.1. Casuística
A partir de 50 famílias com gagueira desenvolvimental persistente, foram
obtidos os 50 probandos, os quais foram pareados por sexo, a 50 indivíduos controles.
Dos 50 indivíduos com gagueira desenvolvimental persistente familial selecionados,
86% foram do sexo masculino e 14% do feminino, implicando em uma razão sexual de
6,14M:1F, semelhante as obtidas em outros trabalhos (tabela 05).
Tabela 05. Distribuição dos grupos amostral e controle
Sexo Grupos
Amostral Controle
Masculino 43 43
Feminino 07 07
4.2. Genotipagem
Dos cinco SNPs inicialmente proposto para a genotipagem (rs6275, rs6277,
rs2617604, rs28364998 e rs28364997) apenas dois (rs6275 e rs6277) relacionados ao
gene DRD2 tiveram sucesso quanto ao processo de genotipagem. Os três marcadores
restantes (rs2617604, rs28364998 e rs28364997) relacionados ao gene SLC6A3,
apesar do sucesso das reações o processo de genotipagem foi comprometido, uma
vez que o software StepOne™ v2.1, utilizado para a determinação dos genótipos,
processa as informações a partir da análise e comparação de três clusters bem
definidos (homozigose: alelo 1, homozigose: alelo 2 e heterozigose: alelos 1 e 2).
Assim, devido à ausência de um ou dois destes clusters, ou seja, de heterozigose, não
houve parâmetros suficientes para o processamento e genotipagem dessas
informações. A tabela 06, apresenta os genótipos obtidos para os marcadores rs6275
Tabela 06. Alelos obtidos pela genotipagem do grupos amostral e controle.
Indivíduos Sexo SNP 6275 SNP 6277 Indivíduos Sexo SNP 6275 SNP 6277 Indivíduos Sexo SNP 6275 SNP 6277
Alelo 1 Alelo 2 Alelo 1 Alelo 2 Alelo 1 Alelo 2 Alelo 1 Alelo 2 Alelo 1 Alelo 2 Alelo 1 Alelo 2
1.1 M A G G G 22.1 M A G A G 44.1 F A A G G
2.1 M A G G G 23.1 M G G A G 45.1 M A G A G
3.1 M A G G G 24.1 F A G A G 46.1 M A G A G
4.1 M A G A G 25.1 M A A G G 47.1 F G G A G
5.1 M G G A G 26.1 M A A G G 48.1 M G G A A
6.1 F A G A G 27.1 M A G G G 49.1 M G G A G
7.1 M G G A A 28.1 M A A G G 50.1 M G G A G
8.1 M A G A G 29.1 M G G A G 51.1 M A G A G
9.1 M G G A A 30.1 M A G A G 52.1 M A A G G
10.1 M A G A G 31.1 M A A G G 53.1 F G G G G
11.1 M G G A A 32.1 M A G A G BRCO0001 F A G A G
12.1 F G G A G 33.1 M G G A A BRCO0005 F G G G G
13.1 M A G G G 34.1 M A G A G BRCO0006 F G G A A
14.1 M G G A A 37.1 M A A G G BRCO0007 F A G A G
15.1 F A G G G 38.1 M G G A A BRCO0008 F A G A G
16.1 M G G G G 39.1 M A G G G BRCO0013 M A A G G
17.1 M A A G G 40.1 M G G A A BRCO0015 M G G A G
19.1 M A G A G 41.1 M G G A G BRCO0017 M A A G G
20.1 M G G A A 42.1 M A G A G BRCO0018 M A G A G
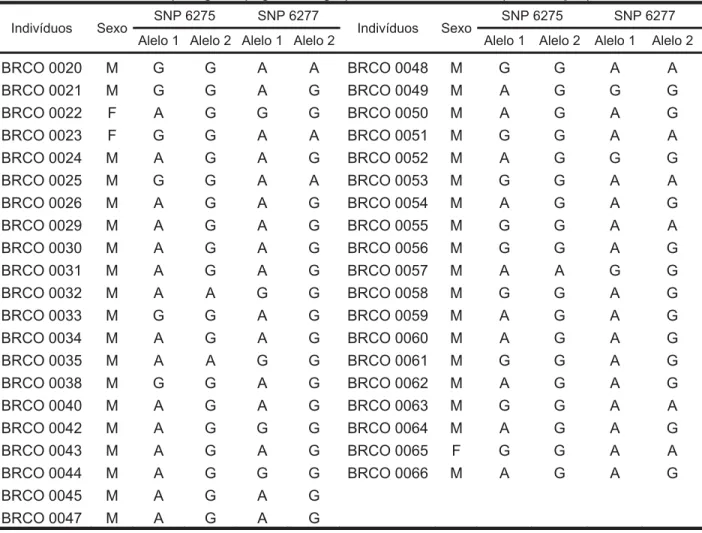
Tabela 06. Alelos obtidos pela genotipagem dos grupos amostral e controle(continuação).
Indivíduos Sexo SNP 6275 SNP 6277 Indivíduos Sexo SNP 6275 SNP 6277
Alelo 1 Alelo 2 Alelo 1 Alelo 2 Alelo 1 Alelo 2 Alelo 1 Alelo 2
BRCO 0020 M G G A A BRCO 0048 M G G A A
BRCO 0021 M G G A G BRCO 0049 M A G G G
BRCO 0022 F A G G G BRCO 0050 M A G A G
BRCO 0023 F G G A A BRCO 0051 M G G A A
BRCO 0024 M A G A G BRCO 0052 M A G G G
BRCO 0025 M G G A A BRCO 0053 M G G A A
BRCO 0026 M A G A G BRCO 0054 M A G A G
BRCO 0029 M A G A G BRCO 0055 M G G A A
BRCO 0030 M A G A G BRCO 0056 M G G A G
BRCO 0031 M A G A G BRCO 0057 M A A G G
BRCO 0032 M A A G G BRCO 0058 M G G A G
BRCO 0033 M G G A G BRCO 0059 M A G A G
BRCO 0034 M A G A G BRCO 0060 M A G A G
BRCO 0035 M A A G G BRCO 0061 M G G A G
BRCO 0038 M G G A G BRCO 0062 M A G A G
BRCO 0040 M A G A G BRCO 0063 M G G A A
BRCO 0042 M A G G G BRCO 0064 M A G A G
BRCO 0043 M A G A G BRCO 0065 F G G A A
BRCO 0044 M A G G G BRCO 0066 M A G A G
BRCO 0045 M A G A G
4.3. Análise Estatística
Os genótipos obtidos com os marcadores rs6275 e rs6277 para as 100
amostras foram tabulados e utilizados para gerar arquivos de entrada do programa
Haploview (Broad Institute – Cambridge – MA - USA) para o cálculo das freqüências
alélicas e de simples associação dos fenótipos (gago e fluente), utilizando-se do teste
do qui-quadrado, pautado no equilíbrio de Hardy-Weinberg (tabela 07).
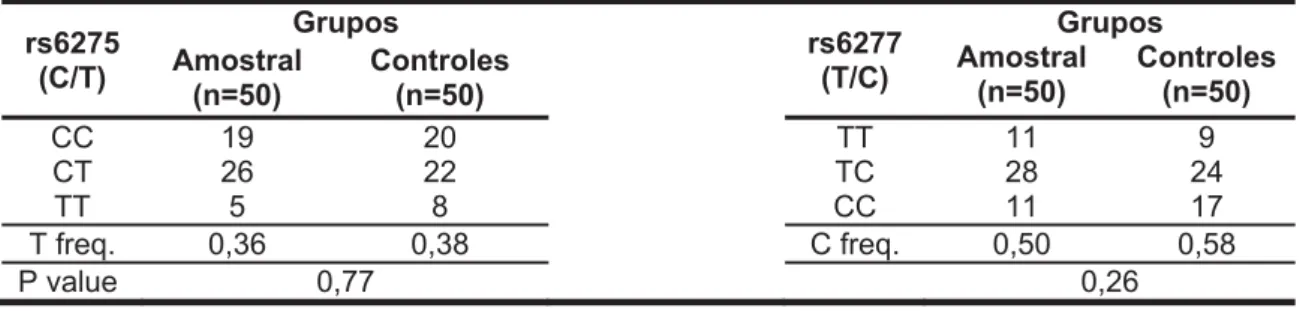
Tabela 07. Frequência alélica e associação alélica para dois SNPs no gene DRD2 nos grupos amostral e controle.
rs6275 (C/T) Grupos rs6277 (T/C) Grupos Amostral (n=50) Controles (n=50) Amostral (n=50) Controles (n=50)
CC 19 20 TT 11 9
CT 26 22 TC 28 24
TT 5 8 CC 11 17
T freq. 0,36 0,38 C freq. 0,50 0,58
P value 0,77 0,26
5. DISCUSSÃO
Os gânglios da base (GB) são as maiores estruturas subcorticais do
prosencéfalo e podem influenciar o comportamento motor, emotivo e cognitivo
(Graybiel, 2000). Eles consistem de um conjunto de núcleos interligados, sendo o
estriado e o globo pálido alguns destes núcleos. A substância negra compacta é
importante junto aos gânglios da base, uma vez que apresenta duas vias que podem
gerar comportamentos motores distintos: a via direta, que têm receptores excitatórios
D1, e promovem a desinibição motora e comportamental generalizada; e a indireta,
que têm receptores inibitórios D2, e conduzem a uma inibição geral de movimentos e
Cunnington et al. (1996) sugeriram que a área motora suplementar (AMS),
envolvida em movimentos auto-iniciados, bem aprendidos, complexos e seqüenciais,
depende mais do sincronismo dos movimentos do que da programação espacial
propriamente dita, o que sugere sua importância na produção das falas espontâneas.
Além disso, os gânglios da base, através da AMS, proveriam dicas para facilitar o
sincronismo interno dando início aos submovimentos em uma sequência motora bem
aprendida.
A execução de uma seqüência motora complexa exige o controle do padrão
espacial de ativação muscular e do tempo exato de cada movimento. Em indivíduos
gagos, o tempo “interno”, possivelmente é modificado devido a alterações nos gânglios
da base, gerando interrupções no ritmo continuo da fala. Durante o canto, isso não
acontece, pois, o ritmo do som da melodia proporciona ao cérebro uma representação
“interna” do tempo, cadenciando a pronuncia das sílabas. Jeffries, Fritz e Braun (2003)
ao compararem indivíduos gagos em dois momentos, ao cantar e ao falar
espontaneamente, a partir de estudos de neuroimagem (PETscan) observaram
aumento da atividade do putâmen esquerdo dorsal (circuito motor dos gânglios basais)
somente durante o canto.
Estudos têm demonstrado que os neurônios, em diferentes partes do globo
pálido (GP) produzem um pulso elétrico intenso ao final de um submovimento motor
conhecido, o que sugere tratar-se de uma sinalização interna, gerada pelos gânglios
da base, para marcar o fim em uma sequência de movimentos. Desta forma, este sinal
serviria como um gatilho à AMS, sinalizando a mudança para o próximo componente
da sequência do movimento (Brotchie, Iansek & Horne, 1991; Mushiake & Strick,
1995). Assim, a partir deste modelo, acredita-se que o movimento, ou frase seriam
iniciados por outras estruturas, que não os gânglios basais (Mink, 1996), porém, no
final deste primeiro estágio e, portanto, a ausência desta sinalização resultaria em
repetições de palavras, caracterizando a gagueira.
Os neurônios presentes nos gânglios da base são dependentes de
interneurônios, chamados “neurônios tonicamente ativos'' (TAN) capazes de modular
respostas comportamentais através de sinais temporalmente coordenados pelo núcleo
estriado (Graybiel et al.,1994; Blazquez et al., 2002), sincronizando assim os
movimentos. Além disso, suas respostas são mais intensas e definidas após a
repetição de determinados comportamentos (Brotchie et al, 1991;Graybiel et al, 1994).
Uma vez a gagueira estando relacionada a modificação do tempo “interno” promovida
por alteração nestes neurônios é esperado que a disfluência diminua após a prática de
uma sequência de fala, a qual já foi comprovada em indivíduos gagos que ao
empregarem palavras bem conhecidas do vocabulário ou ler o mesmo texto diversas
vezes apresentaram redução das difluências (Bloodstein, 1995; Dayalu et al. , 2002).
Estudos envolvendo neuroimagem funcional têm apontado para indícios de que
os gânglios da base e a secreção do neurotransmissor, dopamina, estão envolvidos
diretamente ao longo de todo o processo de aprendizagem, através do reforço (Mink,
1996; Reynolds, Hyland, & Wickens, 2001) o que permite o núcleo estriado reagir de
determinadas maneiras a padrões de ativação cortical.
Na década de 1950, iniciaram-se testes com medicamentos para o tratamento
da gagueira, principalmente, bloqueadores de dopamina, como o haloperidol, o qual a
princípio parecia atuar mais no que tange, a intensidade do que em relação a
manifestação da gagueira. O haloperidol exerce seu efeito na redução da ativação do
centro motor durante a gagueira, e não na redução do número de interrupções ao
longo do processo de fala. Desta forma, levando-se em conta a importância funcional
dos ganglios basais para o desenvolvimento da gagueira e a diminuição dos sintomas
sido sugerido que uma das formas de ação no combate a gagueira envolva os
receptores de dopamina D2, que por estarem localizados principalmente nos
neurônios estriais constituindo a via indireta, estariam reforçando a inibição difusa da
atividade motora.
Visando compreender melhor o papel da dopamina, Wu et al. (1997)
realizaram estudo de PETscan usando o 6-FDOPA (6-[18F]-fluorodopa) (análoga à
L-DOPA endógena) como um marcador dopaminérgico pré-sinaptico o qual, foi utilizado
para quantificar a taxa de síntese de dopamina no cérebro (Barrio, Huang & Phelps,
1997). Em indivíduos gagos, houve uma captação de 6-FDOPA três vezes maior em
diversas partes do cérebro, em comparação aos controles, o que pode ser associada
à superatividade do sistema dopaminérgico pré-sináptico em regiões que modulam a
verbalização.
Assim, baseando-se em evidências da possível relação da hiperatividade
dopaminérgica no cérebro de indivíduos gagos Lan et al. (2009), a partir dos genes
SLC6A3 e e DRD2, responsáveis, respectivamente, pela sintese de transportadores e
receptores dopaminérgicos, foram avaliados cinco possíveis e pontuais polimorfismos
(SNP) dessas duas regiões. Das estimativas de associação realizadas, foi observado
que a presença, em indivíduos disfluentes, do alelo C, (rs6277 - DRD2) quando
compado aos fluentes apresentaram-se significativamente associados (p=0,001)
sugerindo que a presença deste alelo pode ser considerada como um fator de risco
para o aparecimento da afecção.
Desta maneira, visando verificar esta possível associação na população
brasileira foram realizadas, análises semelhantes, e que não apresentaram
associação positiva (p 0,05) no SNP rs6277 em relação à gagueira desenvolvimental
persistente familial. Entretando, trabalhos realizados por Kang et al. (2010) mostraram
de outra região contendo o gene DRD3, pertencente a mesma família dos receptores
dopaminérgico DRD2, fundamentando e relacionando ainda o papel da dopamina no
processo de desenvolvimento da gagueira em algumas populações.
A substituição do alelo timina pela citosina, carcteriza uma mutação do tipo
silenciosa, pois não implica na troca efetiva do aminoácido, estudos tem revelado
recentemente que esse tipo de mutação pode interferir nas proteínas sintetizadas
uma vez que estariam alterando os níveis de afinidade
receptor/transportador/substrato, os quais desequilibrados, poderiam influenciar nos
processos fisiológicos (Chamary e Hurst, 2009) . Além disso, a possível associação
observada nas demais populações, para o marcados rs6277 (Lan et al., 2009), bem
como nos estudos recentes (Kang et al., 2010) no gene DRD3, em uma análise mais
refinada podem apontar para regiões distintas dentro destes genes, porém ligadas
aos marcadores até o momento apresentados, e que não foram descobertas até o
momento.
6. CONCLUSÃO
Apesar de nossos resultados não demonstrarem uma correlação positiva entre
a presença do alelo C nos SNP rs6275 e rs6277 e a gagueira, acreditamos que tal fato
possa estar relacionado a dois principais motivos: primeiro, de que não exista esta
associação de fato, na população composta por indivíduos com gagueira
desenvolvimental persistente familial, bem caracterizada em nosso grupo amostral, ao
contrário do grupo estudado por Lan et al. (2009); segundo, de que não exista esta
associação devido ao reduzido número de indivíduos analisados, contribuindo com
redução poder estatístico das análises. Acreditamos que a combinação de uma boa
caracterização do grupo amostral, como tem sido feito por nosso grupo, associado ao
ao ponto de comprovar ou refutar os achados chineses em relação à população
brasileira.
7. REFERÊNCIAS BIBLIOGRÁFICAS
ALLERT, N. et al. Stuttering induced by thalamic deep stimulation for dystonia. J.
Neural Transm. v. 117, p. 617-620, 2010.
ALM, P.A.; RISBERG, J. Stuttering in adults: The acoustic startle response,
temperamental traits, and biological factors. Journal Communication Disorders,
v. 5358, p.41, April, 2006.
ALMEIDA, N. M. Gramática metódica da língua portuguesa. São Paulo (SP, Brasil):
Saraiva, 2005.
AMBROSE, N.; COX, N.; YAIRI, E. The Genetic Basis of Persistence and Recovery in
Stuttering. Journal of Speech Language and Hearing Research, v.40,
p.567-580,1997.
ANDRADE, C. R.F, de; SASSI, F.C.; CAMLANATTI-OSTIZ, H. Terminologia: fluência e
desordens da fluência. Pró-fono, Carapicuíba, v.13, n.1, p.107-113, 2001.
ANDRADE, C.R.F., FLUÊNCIA. IN: ANDRADE, C.R.F., BÉFI-LOPES, D.M.,
FERNANDES, F.D.M.; WERTZNER, H.F. (EDS). ABFW - Teste de linguagem
infantil nas áreas de fonologia, vocabulário, fluência e pragmática. Carapicuiba SP: Pró-Fono, 2000.
ANDREWS, G., et al. Stuttering: A review of research findings and theories circa 1982.
Journal of Speech and Hearing Disorders, v.48, p.226-246, 1983.
ANDREWS, G.; MORRIS, Y.A.; HOWIE, P.; MARTIN, N.G. Genetic factors in stuttering
confirmed. Arch Gen Psychiatry, v.48, p.1034-5, 1991.
ASSOCIAÇÃO AMERICANA DE PSIQUIATRIA. Manual Diagnóstico e Estatístico
BARRIO, J.R., et al. Biological imaging and the molecular basis of dopaminergic
disease. Biochemical Pharmacology. v.54, p.341-348, 1997.
BENKE, T. et al. Repetitive speech phenomena in Parkinson’s disease. J. Neurol.
Neurosurg. Psychiatry. v. 69, p. 319-324, 2000.
BLAZQUEZ, P. M., et al. A network representation of response probability in the
striatum. Neuron. v. 33, p. 973-982, 2002.
BLOODSTEIN, O. A handbook on stuttering. 5 ed. Chicago: National Easter Seal
Society, 1995.
BOTSTEIN, D.; RISCH, N. Discovering genotypes underlying human phenotypes: Past
successes for mendelian disesse, future approaches for complex disease. Nature
Genetics, v. 33 (supl.), p. 228-237, 2003.
BRAUN, A.R., et al. Altered patterns of cerebral activity during speech and language
production in developmental stuttering/ An H215O positron emission tomography
study. Oxford University Press,1997
BRITO PEREIRA, M.M. A gagueira infantil como resultado da interação dos
fatores sociais e emocionais. Tratando Gagueira: diferentes abordagens. São Paulo, Cortez, p. 41, 2002
BROTCHIE, P., et al. Motor function of the monkey globus pallidus. 2 Cognitive
aspects of movement and phasic neuronal activity. Brain. v114, p.1685-1702.
BÜCHEL, C.; SOMMER, M. What cause stuttering? Plos Biol, v.2, 2004.
BURGHAUS, L. et al. Deep brain stimulation of the subthalamic nucleus reversibly
deteriorates stuttering in advanced Parkinson’s disease. J. Neural. Transm. v.
113, p. 625-631, 2006.
CANHETTI-OLIVEIRA, C.M.C. Gagueira Familial: Aspectos fonoaudiológicos e
CHAMARY, J. V. e HURST, L. D. O custo das mutações silenciosas. Scientific American Brasil., p.34-41, 2009.
COMINGS, D.E. Tourette Syndrome and Human Behavior. Duarte,CA:Hope Press,
p. 1-828, 1990.
COSTA, F.L. Análise de ligação da região 18p11.32-11 em portadores de gagueira
familial. Monografia apresentada ao Instituto de Biociências da Universidade Estadual Paulista/Botucatu. Botucatu, 2005.
COX, N.J.; SEIDER, R.A.; KIDD, K.K. Some environmental factors and hypotheses for
stuttering in families with several stutterers. J. Speech Hear. Res., v.27, p.543-548, 1984.
CRAIG, A., et al. Epidemiology of stuttering in the community across the entire life
span. Journal of Speech, Language and Hearing Research, v.45(6),
p.1097-1105, Dez 2002.
CUNNINGTON, R. et al. The role of supplementary motor area in the control of
voluntary movement. Human Moviment Science. v. 15, p. 627-647, 1996.
DAYALU, V. N., et al. Stuttering frequency on content and function words in adults who
stutter: a concept revisited. J Speech Lang Hear Res. v. 45, p. 871-8, 2002.
dbSNP. National Institute of Health. Disponível em:
<http://www.ncbi.nlm.nih.gov/projects/SNP/> Acesso em: 10/02/2010.
DE NIL, L. F. et al. A pósitron emission tomography study of silent and oral single Word
reading in stuttering and nonstuttering adults. J. of Speech, Language and
Hearing Research. v. 43, p. 1038-1053, 2000.
DOMINGUES, C.E.F. Estudos moleculares das regiões cromossômicas 18p e 18q
proximal em portadores de gagueira persistente familial. 2009. Mestrado em Genética- Instituto de Biociências -Universidade Estadual Paulista “Júlio de
DRAYNA D, KILSHAW J, KELLY J. The sex ratio in familial persistent stuttering. Am J Hum Genet. v.65, p.1473-1475, 1999.
DUARTE, T. F.; CRENITTE, P. A. P.; LOPES-HERRERA, S. A. Characterization of
individuals with fluency disorders at the Speech Language Pathology and
Audiology Clinic USP – Bauru. Rev. CEFAC. vol.11 no.3, 2009
FELSENFELD, S., et al. A study of the genetic and environmental etiology of stuttering
in a select twin sample. Behav Genet. v.30, n.5, p. 359-366, 2000.
FOUNDAS, M.D. et al. Aberrant auditory processing and atypical planum temporale in
developmental stuttering. American Academy of Neurology, v.63, n.9,
p.1640-1646, 2001.
FOX, P.T., et al. A PET study of the neural systems of stuttering. Nature, v.382, p.158-162, 11 jul 1996.
FOX, P.T. et al. Brain correlates of stuttering and syllable production. A PET
performance-correlation analysis. Brain. v. 123, p.1985-2004, 2000.
GRAYBIEL, A. M., et al. The basal ganglia and adaptive motor control. Science. v.
265, p. 1826-31, 1994.
GRAYBIEL, A. M. The basal ganglia. Curr Biol. v.10,p.509-11, 2000.
HANAKAWA, T., H. Fukuyama, et al. Enhanced lateral pre motor activity during
paradoxical gait in Parkinson's disease. Ann Neurol. v. 45, p.329-36, 1999 .
HAPMAP. National Institute of Health. Disponível: <hapmap.ncbi.nlm.nih.gov>Acesso
em: 07/12/2010.
HELM-ESTABROOKS, N. Stuttering, associated with acquired neurological
disorders. In R.F. CURLEE (Ed.), Stuttering and related disorders of fluency (p.205-219). New York: Thieme Medical Publishers,1993.
JEFFRIES, K. J., et al. Words in melody: an H(2)15O PET study of brain activation
KANG, C. et al. Mutations in lysosomal enzyme-targeting pathway and persistent
stuttering. New England of Journal Medicine. v. 362, p. 677-685, 2010.
KARNIOL, R. Stuttering, language, and cognition: A review and a model of stuttering
as suprasegmental sentence plan alignment (SPA). Psychological Bulletin,
v.117(1), p.104-124, Jan 1995.
KIDD, K. A genetic perspective on stuttering. J. Fluency Disord., v.2, p.259-269,1977.
KIDD, K.K.; KIDD, J.R.; RECORDS, M.A The possible causes of the sex ratio in
stuttering and its implications. J. Fluency Disord., v.3, p.13-23, 1978.
KOLLER, W.C. Dysfluency (stuttering) in extrapyramidal disease. Arch Neurol. v.40,
p.175-177, 1983.
LAN, J., et al. Association between dopaminergic genes (SLC6A3 and DRD2) and
stuttering among Han Chinese. J. Human Genetics, p.1-4, 2009.
LEWIS, B.A.; COX, N.J.; BYARD, P.J. Segregation Analysis of Speech and Language
Disorders. Behavior Genetics, v.23, n.3, 1993.
LUDLOW, C.L. and LOUCKS, T. Stuttering: a dynamic motor control disorder. J.
Fluency Disord. v. 28, p. 273-295, 2003.
MAGUIRE, G.A; et al. Alleviating stuttering with pharmacological interventions. Exp.
Opin. Pharmacother, v.5, p.1565-1571, 2004.
MINK, J. W. The basal ganglia: Focused selection and inhibition of competing motor
programs. Progress in Neurobiology. v. 50, p. 381-425, 1996.
MONIZ, H; TRANCOSO, I.; MATA, A. I. Disfluencies and the Perspective of Prosodic
Fluency. Lecture Notes in Computer Science, v.5967, p. 382-396, 2010.
MOORE, W.H.; HAYNES, W.O. Alpha Hemispheric Asymmetry and Stuttering/ Some
support for a segmentation dysfunction hypothesis. Journal of Speech and
MUSHIAKE, H., STRICK, P. L. Pallidal neuron activity during sequential arm
movements. Journal of Neurophysicology. v.74, p. 2754-2758, 1995.
NATKE, U.; GROSSER, J.; SANDRIESER, P.; KALVERAM, K.T. The duration
component of the stress effect in stuttering. Journal of Fluency Disorders,
v.27(4), p.305-318, 2002.
NEBEL, A. et al. Acquired stuttering after pallidal deep brain stimulation for dystonia. J. Neural Transm., v. 116, p. 167-169, 2009.
NUDELMAN, H.B., et al. A model of the phonatory response time of stutterers and
fluent speakers to frequency-modulated tones. J. Acoust. Soc. Am., v.92 (4 Pt 1),
p. 1882-1888, 1992.
ORGANIZAÇÃO MUNDIAL DE SAÚDE. Classificação Estatística Internacional de
Doenças e Problemas Relacionados à Saúde (CID-10), v.1. 10ª ed. Editora da Universidade de São Paulo, 2003
PERKINS, W.H. What is stuttering? J. Speech Hear. Disord., v.55, p. 370-382, 1990.
HAPLOVIEW. Responsabilidade Broad Institute. Disponível em:
<http://www.broadinstitute.org/haploview> Acesso em: 07/12/2010.
RAZA, M. H., et al. Identification of an autossomal recessive stuttering lócus on
chromosome 3q13.2-3q13.33. Human Genetic. 2010.
REYNOLDS, J. N., et al. A cellular mechanism of reward-related learning. Nature, v.
413, p. 67-70, 2001.
RIAZ, N.; STEINBERG, S.; AHMAD, J. ET AL. Genomewide Significant Linkage to
Stuttering on Chromosome 12. American Journal of Medical Genetics. v.76,
p.647-651, 2005.
RILEY, G.D. Stuttering Severity Instrument for Children and Adults. Austin: Pro
RINGO, C.C.; DIETRICH, S. Neurogenic stuttering: An analysis and critique. Journal of Medical Speech-Language Pathology, v.3, p.111-122, 1995.
ROTH, C.R.; ARONSON, A.E; DAVIS, L.J. Clinical studies in psychogenic stuttering of
adult onset. Journal of Speech and Hearing Disorders, v.54, p. 634-646, 1989.
SAIKI, R. K., et al. Enzymatic amplification of -globin genomic sequences and
restriction site analysis for diagnosis of sickle cell anemia. Science, v. 230, p.
1350-54, 1985.
SALMELIN, R. et al. Functional organization of the auditory cortex is different in
stutterers and fluent speakers. Neuroreport., v. 9, p. 2225-2229, 1998.
SHUGART, Y.Y.; MUNDORFF, J.; KILSHAW, J.; DOHENY, K.; DOAN, B.; WANYEE,J.
GREE, E.D.; DRAYNA, E. Results of a genome-wide linkage scan for stuttering.
Amer. J. Med. Genet., v.124A, p.133-135, 2004.
SOMMER, M.; KOCH, M.A.; PAULUS, W.; WEILLER, C.; BUCHEL, C. Disconnection
of speech-relevant brain areas in persistent developmental stuttering. Lancet,
v.360, p.380-383, 2002.
SURESH, R., et al. New complexities in the genetics of stuttering: significant
sex-specific linkage signals. Am J Hum Genet., nº78, v.4, p.554-63, 2006.
TALLAL, P.;ROSS, R.; CURTISS, S. Familial Aggregation in specific language
impairment. J. Speech Hear Disord., v.54, p. 167-173, 1989.
TOMBLIN, J.B. Familial concentration of developmental language impairment.
J.Speech Hear. Disord., v.54, p.287-295, 1989.
TRAVIS, L. E. The cerebral dominance theory of stuttering. Journal of Speech and
Hearing Disorders, v. 43, p. 278-281, 1978.
VAN RIPER, C. The nature of stuttering. 2 ed. Englewood Cliffs, NJ: Prentice-Hall,
VISWANATH, N.; LEE, H.S.; CHAKRABORTY, R. Evidence for a Major Gene on
Persistent Developmental Stuttering. Human Biology, v.76, n.3, p.401-412, Jun
2004.
WINGATE, M.E. A standard definition of stuttering. J Speech Hearing Disord., v.29,
p.484-489, 1964.
WITTKE-THOMPSON, J.K. et al. Genetic studied of stuttering in a founder
population.Journal of Fluency Disorders, v. 32, p.33-50, 2007.
WU, J.C., et al. A positron emission tomography [18F] deoxyglucose study of
developmental stuttering. Neuroport., v.6, p.501-505, 1995.
WU, J.C., et al. Increased dopamine activity associated with stuttering. Neuroreport.,
v.8(3), p.767-770, 10 Fev 1997.
YAIRI, E.; AMBROSE, N.G. A longitudinal study of stuttering in children: a preliminary
report. J. Speech Hear. Res., v. 35, p. 755-760, 1992a.
YAIRI, E.; AMBROSE, N.G. Onset of stuttering in preschool children: select factors.
J.Speech Hear. Res., v.35, p.782-788, 1992b.
YAIRI, E., AMBROSE, N., COX, n. Genetics of stuttering : A critical review. Journal of
Speech Language and Hearing Research, v. 39, p.771-784, 1996a.
YAIRI, E., et al. Predictive factors of persistence and recovery: Pathways of childhood
stuttering. J. Commun. Disord., v. 29, p. 53–77, 1996b.
YAIRI, E. Is the basis of stuttering genetic? ASHA., v. 40, n. 1, p. 29-32, 1998.
YAIRI, E.; AMBROSE, N.G. Early childhood stuttering. J Speech Lang and Hearing
Research, v.42, p.1097-1112, 1999.
YARUSS, J.S.; QUESAL, R.W. Stuttering and the International Classification of
Functioning, Disability, and Health (ICF): An update. J. of Communication
8. ANEXOS
8.2.Termo de Consentimento Livre e Esclarecido