Universidade de Trás-os-Montes e Alto Douro
ATIVAÇÃO ALCALINA DE RESÍDUOS INDUSTRIAIS NA
ESTABILIZAÇÃO DE SOLOS RESIDUAIS GRANÍTICOS
DISSERTAÇÃO APRESENTADA À ESCOLA DE CIÊNCIA E TECNOLOGIA DA UNIVERSIDADE DE
TRÁS-OS-MONTES E ALTO DOURO PARA A OBTENÇÃO DE GRAU DE MESTRE EM
ENGENHARIA CIVIL
AUTOR
E
RNESTOP
AULOF
ERNANDESL
UCASORIENTADORES
N
UNOM
IGUELC
ORDEIROC
RISTELOPROFESSOR AUXILIAR DA UNIVERSIDADE DE TRÁS-OS-MONTES E ALTO DOURO
P
EDROM
ANUEL DEM
ELOB
ANDEIRAT
AVARESPROFESSOR ASSOCIADO DA UNIVERSIDADE DE TRÁS-OS-MONTES E ALTO DOURO
Universidade de Trás-os-Montes e Alto Douro
ATIVAÇÃO ALCALINA DE RESÍDUOS INDUSTRIAIS NA
ESTABILIZAÇÃO DE SOLOS RESIDUAIS GRANÍTICOS
DISSERTAÇÃO APRESENTADA À ESCOLA DE CIÊNCIA E TECNOLOGIA DA UNIVERSIDADE DE
TRÁS-OS-MONTES E ALTO DOURO PARA A OBTENÇÃO DE GRAU DE MESTRE EM
ENGENHARIA CIVIL
AUTOR
E
RNESTOP
AULOF
ERNANDESL
UCASORIENTADORES
N
UNOM
IGUELC
ORDEIROC
RISTELOPROFESSOR AUXILIAR DA UNIVERSIDADE DE TRÁS-OS-MONTES E ALTO DOURO
P
EDROM
ANUEL DEM
ELOB
ANDEIRAT
AVARESPROFESSOR ASSOCIADO DA UNIVERSIDADE DE TRÁS-OS-MONTES E ALTO DOURO
Composição do júri:
___________________________________________________
___________________________________________________
___________________________________________________
Universidade de Trás-os-Montes e Alto Douro
ATIVAÇÃO ALCALINA DE RESÍDUOS INDUSTRIAIS NA
ESTABILIZAÇÃO DE SOLOS RESIDUAIS GRANÍTICOS
Ernesto Paulo Fernandes Lucas
Dissertação apresentada à Universidade de Trás-os-Montes e Alto Douro para obtenção do grau de Mestre em Engenharia Civil, realizada sob a orientação científica Professor Doutor Nuno Miguel Cordeiro Cristelo, docente do Departamento de Engenharia Civil da Escola de Ciências e Tecnologia da Universidade de Trás-os-Montes e Alto Douro e co-orientação científica do Professor Doutor Pedro Manuel de Melo Bandeira Tavares, docente do Departamento de Química da Escola de Ciências da Vida e do Ambiente da Universidade de Trás-os-Montes e Alto Douro.
AGRADECIMENTOS
O autor deseja agradecer a todas as pessoas e instituições que de alguma forma contribuíram para a elaboração deste trabalho e, em particular:
Ao Professor Nuno Cristelo, na qualidade de meu orientador, pelo permanente incentivo e inesgotável paciência com que orientou este trabalho. A aprendizagem de saber foi intensa e abundante e cuja amizade tanto contribuiu para o empenho e prazer com que o elaborei; Ao Professor Pedro Tavares, meu coorientador, pela sua disponibilidade, profissionalismo e ajuda prestada sempre que necessária ao longo deste trabalho. Acima de tudo, incansável, na reta final do trabalho. A sua orientação científica foi determinante e bastante esclarecedora; À minha colega e amiga Mestre em Engenharia Civil, Mónica Dias. A sua amizade e carácter foram motivadores para fomentar uma atitude de competência perante os desafios;
Ao meu colega e amigo Mestre em Engenharia Civil, Edgar Soares pelo seu legado de esforço e empenho constantes;
À Mariana Fernandes, pelo exemplo de conduta e hábitos laboratoriais;
A todos os colegas de Engenharia Civil da Universidade de Trás-os-Montes e Alto Douro, pelo apoio e amizade com que sempre me brindaram;
A todos os meus amigos e colegas em geral que de alguma forma me ajudaram e incentivaram para a conclusão desta etapa;
Ao Laboratório de Materiais e Solos da Universidade de Trás-os-Montes e Alto Douro, que me disponibilizou o equipamento para a realização da parte prática experimental;
Ao Departamento de Química da Universidade de Trás-os-Montes e Alto Douro, pelo equipamento e recursos disponibilizados de uma forma permanente, para a realização da metodologia experimental;
À Unidade de Microscopia Eletrónica da Universidade de Trás-os-Montes e Alto Douro, por ter efetuado as análises e caracterizações químicas dos materiais em estudo;
Ao Departamento de Mecânica da Universidade de Trás-os-Montes e Alto Douro, que me disponibilizou o equipamento necessário para a realização dos muitos ensaios que foram levados a cabo neste trabalho;
Ao Departamento de Geologia da Universidade de Trás-os-Montes e Alto Douro e, em especial, ao Sr. Tito pela disponibilidade e ajuda sempre que solicitada;
Ao Departamento de Engenharia Civil da Universidade do Minho pela disponibilidade das matérias-primas necessárias para a elaboração deste trabalho;
À minha família, em particular à minha mãe, que nunca deixaram de acreditar em mim; A todas estas pessoas, e a outras que eventualmente não mencionei mas que contribuíram para a realização deste trabalho, o meu sincero agradecimento, desejando um dia puder retribuir toda a atenção dispensada.
RESUMO
As crescentes exigências relacionadas com a indústria da construção conduzem, na maioria dos casos, à necessidade de melhorar as características dos solos existentes.
Urge encontrar soluções às alternativas tradicionais (cimento Portland), devido aos enormes custos que apresentam, e às preocupações ambientais, quer na utilização e quer na produção, que acarretam.
A produção massiva de resíduos provenientes de grandes centrais de produção é um problema para o meio ambiente. Normalmente têm um valor comercial muito reduzido, tornando-se um problema para as próprias empresas. Uma solução passa por associar diversos resíduos, quer para fins construtivos quer para a beneficiação de solos, através da ativação alcalina, numa técnica também designada por geopolimerização. Os geopolímeros são materiais à base de aluminosilicatos que apresentam excelentes propriedades físicas e químicas e uma variada gama de aplicações.
Neste trabalho, no sentido de melhorar as características de um solo residual granítico, foi investigada a ativação alcalina de cinzas F, dois slag e lamas provenientes de uma ETA. Foram analisadas as dissoluções das cinzas em soluções de hidróxido de sódio, variando os seguintes parâmetros: tempo de reação, tempo de moagem, velocidade de rotação, concentração de NaOH e temperatura. Foram também determinadas as dissoluções dos outros resíduos, um à base de alumínio (lamas ETA) e outro à base de cálcio (slag).
Relativamente às cinzas verificou-se que a maior parte da solubilidade à temperatura de 23°C ocorre nos primeiros 14 dias, com uma solubilidade limite de 37.5%. A cinética da dissolução foi ajustada a um modelo de Avrami modificado revelando um expoente de
Avrami de m=0.4555, e uma constante cinética de k = 0.0113 min-0.4555. A energia de ativação
calculada para o processo de dissolução das cinzas foi de EA = 39104 J/mol. Isto resulta em
ganhos significativos da quantidade de cinza dissolvida podendo superar os 70% se a dissolução ocorrer a 80°C. A moagem das cinzas também é eficaz no aumento da taxa de dissolução, em particular até aos 60 minutos de moagem. Um dos elementos existente nas cinzas que é dissolvido em maior extensão é o alumínio. Análises feitas à solução filtrada
mostram que o valor limite para a dissolução da alumina (Al2O3) é de 61.8%. A razão entre o
teor de alumínio e de silício solubilizados, a tempo infinito, à temperatura de 23°C, foi de 2.43. Este valor indica que a quantidade de sílica solúvel é demasiado baixa para uma geopolimerização eficaz, justificando a necessidade da adição de silicato de sódio no ativador, como meio de introduzir sílica solúvel no meio alcalino.
A taxa de dissolução nas lamas ETA secas está na ordem dos 60%, valor afetado pela existência de um teor elevado de matéria orgânica. A temperatura de calcinação de 950°C das lamas ETA foi demasiado elevada, o que diminuiu drasticamente as taxas de dissolução da alumina.
O slag preto e o slag branco são maioritariamente constituídos por cálcio, apresentando taxas de dissolução à temperatura ambiente muito superiores às da cinza. As dissoluções do slag branco são maiores do que as dissoluções do slag preto. Para ambos os slag, há um incremento de dissolução com o tempo de moagem, até aos 30 minutos, estabilizando depois.
Foram levados a cabo ensaios de compressão uniaxial em provetes de caldas cimentícias ativadas com solo. Os provetes foram fabricados de acordo com os mesmos parâmetros das dissoluções. No entanto, constatou-se que as condições de cura aplicadas, nomeadamente uma humidade relativa de 85% à temperatura de 21°C, não foram as mais indicadas para a ativação alcalina das cinzas e das lamas ETA, com baixas resistências à compressão axial (<3 MPa).
Os melhores resultados obtidos à compressão uniaxial foram nas misturas que continham slag preto após moagem, apresentando valores de 4.8MPa ao fim do 28°dia, com este valor estável até ao 90°dia.
Palavras-chave: melhoria de solos, ativação alcalina, cinzas volantes, dissolução,
ABSTRACT
The increasing demands related to the construction industry in most cases lead to improve the performance of existing soils.
Is urgent to find alternatives for the traditional solutions (Portland cement), due to the enormous costs they present and environmental concerns, either in use or in production. The massive production of waste from large power plants, is a problem for the environment and usually these have a very low commercial value, making it a problem for the companies themselves. One solution is to associate these wastes for constructive purposes, particularly for the soil improvement, through the technique of alkaline activation. Very often, this technique is associated with the formation of geopolymers. The geopolymers are aluminosilicate materials which have excellent physical and chemical properties and a wide range of applications.
In this work, in order to improve the characteristics of a residual granite soil, fly ash F alkali activated was investigated as also two slag and mud from a water treatment plant (ETA). Fly ash dissolutions in sodium hydroxide solutions were analyzed by varying the following parameters: reaction time, grinding time, rotation speed, temperature and concentration of NaOH. Dissolutions of other residues were also determined, one aluminum-based (ETA sludge) and other calcium-based (slag).
For the ash it was found that most of the solubility at 23 °C occurs within the first 14 days, with a solubility limit of 37.5%. The kinetics of dissolution was adjusted to a modified Avrami model revealing a Avrami exponent m = 0.4555, and a kinetic constant of k = 0.0113 min 0.4555. The activation energy calculated for the fly ash dissolution process was EA = 39104 J / mol. This leads in dissolved fly ash amount significant improvements which can exceed 70% when the dissolution occurs at 80 °C. The grinding of the ash is also effective in increasing the dissolution rate, in particular until to 60 minutes of grinding. One of the existing elements in the ash which is dissolved at a greater extent is the aluminum. Analyses carried out on the filtered solution shows that the limit value for the alumina dissolution
time, at a temperature of 23 ° C was 2.43. This value indicates that the amount of soluble silica is too low for effective geopolymerization, which justifies the need of the addition of the sodium silicate activator as a mean of introducing soluble silica in alkaline medium. The dissolution rate in the dry ETA sludge is in the order of 60%, affected by the existence of a high content of organic matter. The ETA sludge calcination temperature of 950 °C was too high, which drastically reduced the alumina dissolution rates.
The black slag and white slag are mainly composed of calcium, with dissolution rates at room temperature much higher than the fly ash. The white slag dissolutions are greater than the black slag dissolutions. For both slag, there is a dissolution increase with grinding time up to 30 minutes and leveling after.
Uniaxial compression tests were carried out on cement grout samples activated with soil. The specimens were fabricated according to the same parameters of the dissolutions. However, it was found that the curing conditions applied, including a relative humidity of 85% at 21 ° C, were not the more suitable for the fly ash and ETA sludge alkaline activation with low resistance to axial compression (<3 MPa).
The better uniaxial compression results were in the mixtures containing black slag after grinding, with 4.8MPa values after the 28th day, with this value stable until the 90th day.
ÍNDICE DE TEXTO
AGRADECIMENTOS ... i
RESUMO ... iii
ABSTRACT ... v
ÍNDICE DE TEXTO ... vii
ÍNDICE DE FIGURAS ... xi
ÍNDICE DE QUADROS ... xv
ÍNDICE DE GRÁFICOS ... xvii
SIMBOLOGIA ... xix ABREVIATURAS ... xxi 1 - INTRODUÇÃO ... 1 1.1 - ENQUADRAMENTO ... 1 1.2 - OBJECTIVOS ... 4 1.3 - ORGANIZAÇÃO DA DISSERTAÇÃO ... 6 2 - REVISÃO BIBLIOGRÁFICA ... 9 2.1 - INTRODUÇÃO ... 9 2.2 - ATIVAÇÃO ALCALINA ... 11 2.2.1 - MEIO ALCALINO ... 11 2.2.2 - O ATIVADOR ALCALINO ... 14 2.3 - GEOPOLÍMEROS ... 15
2.3.1 - PROPRIEDADES DOS ÓXIDOS AO LONGO DE UM PERÍODO ... 16
2.3.2 - NOMENCLATURA E PROPRIEDADES DAS LIGAÇÕES IÓNICAS E MOLECULARES ... 18
2.3.3 - O PROCESSO DA GEOPOLIMERIZAÇÃO ... 24
2.4 - CARACTARÍSTICAS QUÍMICAS ... 25
2.4.1 - OS METAIS ALCALINOS NO PROCESSO QUÍMICO DA GEOPOLIMERIZAÇÃO ... 28
2.5 - FATORES QUE AFETAM A RESISTÊNCIA MECÂNICA ... 32
2.6 - A IMPORTÂNCIA DAS TÉCNICAS ANALÍTICAS ... 35
2.6.1 - DIFRAÇÃO POR RAIO-X ... 36
2.6.2 - MICROSCOPIA ELETRÓNICA DE VARRIMENTO ... 38
3 - MATERIAIS UTILIZADOS ... 41
3.1 - SOLO RESISUAL GRANÍTICO ... 41
3.1.1 - PRECEDÊNCIA SOBRE A ESCOLHA ... 41
3.1.2 - CONSIDERAÇÕES GERAIS ... 43
3.1.3 - ENSAIOS DE CARATERIZAÇÃO E IDENTIFICAÇÃO DO SOLO ... 45
3.1.3.1 - Composição química ... 45
3.1.4 - CONSIDERAÇÕES FINAIS ... 47
3.2 - CINZAS VOLANTES ... 48
3.2.1 - PRECEDÊNCIA SOBRE A ESCOLHA ... 49
3.2.2 - CONSIDERAÇÕES GERAIS ... 50
3.2.3 - CARATERIZAÇÃO DAS CINZAS VOLANTES ... 52
3.2.3.1 - Estrutura e dimensões ... 52
3.2.3.2 - Composição química ... 54
3.3 - LAMAS ETA ... 55
3.3.1 - PRECEDÊNCIAS SOBRE A ESCOLHA ... 56
3.3.2 - CALCINAÇÃO DAS LAMAS ETA ... 57
3.3.3 - CONSIDERAÇÕES GERAIS ... 60
3.3.4 - CARATERIZAÇÃO E IDENTIFICAÇÃO DAS LAMAS ETA ... 62
3.3.4.1 - Estrutura e dimensões ... 62
3.3.4.2 - Composição química ... 62
3.4 - SLAG ... 64
3.4.1 - PRECEDÊNCIA SOBRE A ESCOLHA ... 65
3.4.2 - CONSIDERAÇÕES GERAIS ... 66
3.4.3 - CARATERIZAÇÃO E IDENTIFICAÇÃO DO SLAG ... 66
3.4.3.1 - Estrutura e dimensões ... 66
3.4.3.2 - Composição química ... 67
3.5 - HIDRÓXIDO DE SÓDIO ... 69
3.6 - SILICATO DE SÓDIO ... 70
4 - METODOLOGIA ... 73
4.1 - PREPARAÇÃO PRÉVIA DOS MATERIAIS UTILIZADOS ... 73
4.1.1 - SOLO RESIDUAL GRANÍTICO ... 74
4.1.2 - CINZAS VOLANTES ... 75
4.1.2.1 - Moagem ... 75
4.1.3 - LAMAS ETA ... 78
4.1.3.2 - Calcinação ... 80 4.1.3.3 - Trituração ... 81 4.1.3.4 - Moagem ... 83 4.1.4 - SLAG ... 83 4.1.4.1 - Trituração ... 84 4.1.4.2 - Moagem ... 85
4.2 - METODOLOGIA – PARTE QUÍMICA ... 86
4.2.1 - DISSOLUÇÃO COM DIFERENTES TEMPERATURAS ... 89
4.3 - METODOLOGIA – PARTE MECÂNICA ... 91
4.3.1 - PROGRAMA DE ENSAIOS ... 99 Parte Química 5 - RESULTADOS E DISCUSSÃO ... 107 5.1 - CINZA ...107 5.1.1 - DISSOLUÇÃO E REATIVIDADE ...107 5.1.1.1 - Tempo de reação ... 107 5.1.1.2 - Temperatura ... 111 5.1.1.3 - Concentração NaOH ... 113 5.1.1.4 - Tempo de moagem ... 114 5.1.1.5 - Velocidade de rotação ... 118
5.1.2 - QUANTIFICAÇÃO DO ALUMÍNIO E SÍLICA DISSOLVIDOS ...120
5.2 - LAMAS ETA ...128 5.2.1 - DISSOLUÇÃO/REATIVIDADE ...128 5.3 - SLAG ...130 5.3.1 - DISSOLUÇÃO/REATIVIDADE ...131 Parte Mecânica 5.4 - TEMPO DE CURA ...139 5.5 - TEMPO DE MOAGEM ...147 5.6 - VELOCIDADE DE ROTAÇÃO ...149 5.7 - CONCENTRAÇÃO DE NaOH...150 6 - CONCLUSÃO ... 153 6.1 - CONCLUSÕES GERAIS ...153 6.2 - TRABALHOS FUTUROS ...156 7 - BIBLIOGRAFIA E WEBGRAFIA ... 161 7.1 - BIBLIOGRAFIA ...161
ÍNDICE DE FIGURAS
Figura 2.1 – (a) polisilano; (b) polietileno (Davidovits, 1988) ... 19
Figura 2.2 – Três tipos de silicones e a estrutura química do quartzo (Davidovits, 1988) ... 19
Figura 2.3 – Configuração tetraédrica do sialato Si-O-Al-O, conceito iónico (Davidovits 1988; adaptado de Davidovits, 1976) ... 20
Figura 2.4 – Tipos de polisialatos (Davidovits, 1988) ... 21
Figura 2.5 – Ligação trivalente e tetravalente do átomo Al (Davidovits, 1988) ... 22
Figura 2.6 – Representação iónica e covalente de silicatos/siloxanatos e grupos sialato (Davidovits, 1988) .. 23
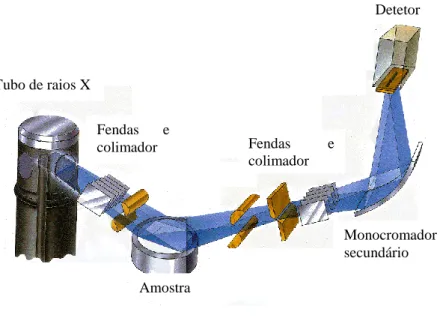
Figura 2.7 – Esquema representativo da geometria de Bragg-Brentano (Correia 2011) ... 37
Figura 2.8 – Representação esquemática do funcionamento de um aparelho de difração de raio X ... 37
Figura 3.1 –Solo residual granítico ... 41
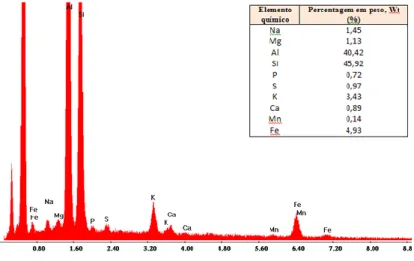
Figura 3.2 – Espectro de EDS do solo natural (Fernandes 2012) ... 46
Figura 3.3 – Imagens de SEM do solo natural obtidas por microscópio de varrimento (Fernandes 2012) ... 46
Figura 3.4 – Cinzas volantes da classe F ... 5319
Figura 3.5 – Cinzas volantes da classe F, com moagem de 60 min a 300 RPM ... 54
Figura 3.6 –Imagem de cinza volante da classe F obtidasatravés de SEM (Soares 2013) ... 5719
Figura 3.7 – Medição de esferas das cinzas volantes de classe F (Soares 2013)... 57
Figura 3.8 – Espectro da composição química referente a cinzas volantes de classe F (Soares 2013) ... 58
Figura 3.9 – Lamas ETA no seu estado natural ... 59
Figura 3.10 – Lamas ETA calcinadas a 950 °C ... 62
Figura 3.11 – Aspeto das lamas ETA em estado natural (à esquerda) e em estado seco (à direita) ... 63
Figura 3.12 –Aspeto das lamas ETA secas (à esquerda) e calcinadas a 950 °C (à direita) ... 63
Figura 3.13 – Imagens obtidas através de SEM das lamas ETA: (a) no seu estado original natural; (b) secas a 120 °C; (c) calcinadas a 950 °C. Barra de escala de 200 µm.) ... 66
Figura 3.14 –Espectro da composição química referente às lamas ETA em estado natural ... 67
Figura 3.15 –Espectro da composição química referente às lamas ETA secas em estufa a 120 °C ... 67
Figura 3.17 – Aspeto geral do slag branco (à esquerda) e do slag preto (à direita) ... 69
Figura 3.18 – Imagens obtidas através de SEM (a) slag preto, escala de 200 μm; (b) slag branco, escala de500 μm ... 71
Figura 3.19 – Espectro da composição químicareferente ao slag preto ... 72
Figura 3.20 – Espectro da composição química referente ao slag branco ... 72
Figura 3.21 – Hidróxido de sódio em estado sólido ... 73
Figura 3.22 – Hidróxido de sódioem forma de solução de concentração 12,5 molal ... 73
Figura 3.23 – Silicato de sódio ... 74
Figura 4.1 – Efeito do processo de destorroamento promovido ao solo (a) solo original; (b) solo destorroado ... 78
Figura 4.2 – Solo colocado num tabuleiro para se proceder À sua secagem na câmara climática ... 78
Figura 4.3 – Moinho utilizado (à esquerda), recipiente e esferas utilizadas (à direita) ... 19
Figura 4.4 – Separação manual das esferas com o auxílio de uma colher... 81
Figura 4.5 – a) cinza no seu estado original; b)cinza com período de moagem de 60 min a 300 RPM ... 81
Figura 4.6 – Cinza com diferentes tempos de moagem, à velocidade de 300 RPM (da esquerda para direita, cinza no seu estado original, cinza moída 15min, cinza moída 30min, cinza moída 60min, cinza moída 120min, cinza moída 240min) ... 81
Figura 4.7 – Lamas ETA no seu estado natural em forma de torrão ... 82
Figura 4.8 – Sequência do processo de desagregação: a) início da desagregação; b) decurso do processo; c) fase final... 83
Figura 4.9 – Secagem das lamas ETA na câmara climática ... 83
Figura 4.10 – Aspeto final das lamas ETA depois da sua secagem em estufa ... 84
Figura 4.11 – Mufla utilizada para a calcinação das lamas ETA ... 84
Figura 4.12 – Sequência do processo de calcinação: a) lamas ETA originais no tabuleiro; b) tabuleiro no interior da mufla ... 85
Figura 4.13 – Remoção manual do tabuleiro em condições de segurança ... 85
Figura 4.14 – Equipamento utilizado para a trituração ... 86
Figura 4.15 – Sequência do processo de trituração: a) colocação da rede; b) introdução manual das lamas ETA no funil do moinho ... 86
Figura 4.17 – Slag preto na sua forma original ... 88
Figura 4.18 – Sequência da pré-trituração do slag preto: a) início do processo com o auxílio de um martelo; b) aspeto final ... 89
Figura 4.19 – a) slag preto original; b) slag preto após trituração ... 89
Figura 4.20 – Sequência do processo de dissolução: a) pesagem de uma amostra de cinza na balança analítica, b) introdução da solução de NaOH no copo, c) dissolução no agitador magnético ... 90
Figura 4.21 – Filtro de vidro utilizado nas filtragens a vácuo ... 91
Figura 4.22 – Sistema de filtragem a vácuo ... 91
Figura 4.23 – Coloração do papel indicador universal de pH mostrando que a solução ainda está alcalina ... 92
Figura 4.24 – Sistema utilizado para a dissolução com diferentes temperaturas ... 94
Figura 4.25 – Execução da base dos moldes: a) início do processo; b) decurso do processo; c) molde final ... 95
Figura 4.26 – Sequência do processo de fabrico da mistura: a) pesagem do solo; b) pesagem da cinza no mesmo recipiente; c) pesagem do ativador; d) adição do ativador na mistura... 96
Figura 4.27 – Aspeto de uma mistura final de calda em cinza ... 97
Figura 4.28 – Calda de cinzas ativadas a ser vertida para os moldes... 97
Figura 4.29 – Desmolde dos provetes cilíndricos: a) colocação do provete com o molde em cima do cilindro; b) colocação da alonga; c) provete completamente desmoldado ... 98
Figura 4.30 – a) provete de cinza ainda no interior do molde; b) aspeto de um provete de cinzas ativadas depois de efectuado o desmolde; c) pormenor da base de um provete de cinza ... 98
Figura 4.31 – Provetes envolvidos em película aderente ... 99
Figura 4.32 – Aspeto do excedente húmido na base superior de um provete de cinza) ...100
Figura 4.33 – Processo de retificação das extremidades dos provetes ...100
Figura 4.34 – a) aspeto final de um provete com cinza após retificação das extermidades: b) pormenor da base de um provete em cinza após retificação ...100
Figura 4.35 – Aspeto geral dos provetes: a) cinza original; b) lamas ETA secas; c) lamas ETA calcinadas; d) slag branco; e) slag preto ...101
Figura 4.36 – Aspecto de provetes em cinza: a) original; b) moagem 15min a 300RPM; c) moagem 30min a 300RPM, d) moagem 60min a 300RPM, e) moagem 120min a 300RPM, f) moagem 240min a 300RPM ...102
Figura 4.37 – Aspeto de provetes: a) lamas ETA calcinadas sem moagem; b) lamas ETA calcinadas com moagem 60min a 300RPM; c) slag branco sem moagem; d) slag branco com moagem 60min a
300RPM; e) slag preto sem moagem; f) slag preto com moagem 60min a 300RPM ... 102
Figura 4.38 – Equipamento da marca ISTROM ® utilizado para realizar os ensaios à compressão ... 103
Figura 5.1 – Fotografia SEM de uma esfera de cinza parcialmente fraturada (tempo de moagem 60minutos a 300 RPM) ... 116
Figura 5.2 – Fotografias SEM e distribuição de tamanhas de partículas que mostram o efeito do tempo de moagem sobre a microestrutura das cinzas (300 RPM) ... 117
Figura 5.3 – Esquema de montagem para um ensaio de compressão uniaxial ... 138
Figura 5.4 – Exemplo de rotura de um provete ... 138
ÍNDICE DE QUADROS
Quadro 3.1 – Composição química do solo natural obtida por EDS. ... 46
Quadro 3.2 – Quadro resumo das propriedades do solo (Soares 2013) ... 50
Quadro 3.3 – Resultados da medição das dimensões da cinza volante de classe F (Soares 2013) ... 58
Quadro 3.4 – Composição química das cinzas obtida por EDS ... 59
Quadro 3.5 – Composição química das lamas ETA obtida por EDS ... 68
Quadro 3.6 – Composição química dos slag obtida por EDS ... 72
Quadro 5.1 – Valores estatísticos obtidos na medição das partículas de cinza a partir das imagens de SEM 118 Quadro 5.2 – Composição química em % (p/p) da cinza original e aos diferentes tempos de dissolução ...120
Quadro 5.3 – Teor de alumínio presente no filtrado determinado por AAS ...121
Quadro 5.4 – Composição química das cinzas, expressa em óxidos ...122
Quadro 5.5 – Percentagem de alumínio dissolvido em cada dissolução ...122
Quadro 5.6 – Quadro resumo das análises EDS aos sais da solução filtrada ...125
Quadro 5.7 – Composição química das lamas ETA calcinadas a 950 °C ...129
Quadro 5.8 – Composição química dos slag branco e preto ...131
Quadro 5.9 – Identificação das misturas fabricadas ...135
Quadro 5.10 – Controlo da densidade média dos provetes ensaiados para cada uma das misturas ...136
ÍNDICE DE GRÁFICOS
Gráfico 5.1 – Evolução da quantidade de cinza dissolvida ao longo do tempo ...107 Gráfico 5.2 – Representação de Avrami para a dissolução com NaOH ...109 Gráfico 5.3 – Ajuste da dissolução de cinzas com NaOH ao modelo assintótico da eq [32] ...110 Gráfico 5.4 – Representação da equação de Avrami modificada para a dissolução de cinza com NaOH ...110 Gráfico 5.5 – Evolução da percentagem de dissolução com a temperatura ...111 Gráfico 5.6 – Representação de Arrhenius para obtenção da energia de ativação do processo de dissolução da cinzas com NaOH ...113 Gráfico 5.7 – Evolução da quantidade dissolvida às 16 horas com o aumento da concentração de NaOH
(moagem por 60 minutos às 300 RPM, 23 °C) ...114 Gráfico 5.8 – Evolução da quantidade dissolvida às 16 horas com o tempo de moagem da cinza (300 RPM,
15,5 molal, 23 °C) ...115 Gráfico 5.9 – Representação gráfica dos valores estatísticos obtidos na medição das partículas de cinza
apartir das imagens de SEM ...118 Gráfico 5.10 – Evolução da quantidade dissolvida às 16 horas com a velocidade de rotação de moagem na
cinza (1 hora de moagem, 12,5 molal 23 °C) ...119 Gráfico 5.11 – Percentagem de Al2O3 dissolvido ao longo do tempo; ajuste a uma função assintótica para
determinação de x∞ ...123
Gráfico 5.12 – Aplicação do modelo de Avrami modificado à dissolução do alumínio ...124 Gráfico 5.13 – Evolução da presença de alumínio dissolvido ao longo do tempo ...126 Gráfico 5.14 – Evolução da presença de silício dissolvido ao longo do tempo ...127 Gráfico 5.15 – Percentagem de dissolução obtida nas lamas ETA secas e lamas ETA calcinadas ...128 Gráfico 5.16 – Percentagem de dissolução obtida nas lamas ETA calcinadas e cinza ...129 Gráfico 5.17 – Evolução da dissolução obtida no slag banco e no slag preto ...131 Gráfico 5.18 – Percentagem de dissolução obtida no slag branco, no slag preto e cinza ...132 Gráfico 5.19 – Variação da resistência à compressão uniaxial ao longo do tempo...140 Gráfico 5.20 – Evolução da resistência a 90 dias com o tempo de moagem na cinza ...147 Gráfico 5.21 – Evolução da resistência a 90 dias, com o incremento da velocidade de rotação na moagems 149 Gráfico 5.22 – Evolução da resistência a 90 dias com o incremento da concentração de NaOH ...150
SIMBOLOGIA
Al Alumínio
Al2O3 Óxido de Alumínio
At Peso atómico
Ba(OH2 hidróxido de bário
Ca Cálcio
Ca(OH)2 Hidróxido de cálcio
CaO Óxido de cálcio
Cl Cloro
cm Centímetros
CO2 Dióxido de carbono
Cr Crómio
C-S-H Silicato de cálcio hidratado
Cu Cobre Cu Coeficiente de uniformidade Fe Ferro Fe2O3 Óxido de ferro g Grama h Horas K Potássio Kg Quilograma kN Quilo Newton
KOH Hidróxido de Potássio
K2O Óxido de Potássio
Li Lítio
m Metros
Mg Magnésio
MgO Óxido de Magnésio
min Minutos
Mn Manganês
mm Milímetros
molal Concentração de molalidade expressa em peso
MPa Mega Pascal
N Newton
Na Sódio
NaOH Hidróxido de sódio
Na2O Óxido de Sódio
Na2SiO3 Silicato de sódio
pH Potencial de hidrogénio P2O5 Pentóxido de Fósforo PVC Policloreto de Vinilo s Segundos S Enxofre Si Silício
SiO2 Dióxido de Silício
Ti Titânio
TiO2 Dióxido de Titânio
μm Micrómetro
WP Limite de plasticidade
WL Limite de liquidez
ABREVIATURAS
ASTM American Society for Testing and Materials
AdTMAD Águas de Trás-os-Montes e Alto Douro
EN Norma Europeia
ETA Estação de tratamento de água EUA Estados Unidos da América
EDS Espectrometria de dispersão de energia (do inglês: Energy dispersive spectroscopy) LVDT Transformador diferencial variável linear (do ingles: Linear variable differential
transformer)
RPM Rotações por minuto
SEM Microscopia eletrónica de varrimento (do inglês: Scanning electron microscopy) UCS Ensaio de compressão uniaxial (unconfined compression strength)
1 - INTRODUÇÃO
1.1 - ENQUADRAMENTO
Tendo em conta a expansão, quer social, quer industrial dos últimos tempos, desencadeou-se um aumento da procura das matérias-primas necessárias, para responder a uma sociedade cada vez mais exigente. As grandes fábricas e centrais de produção e o seu consumo de imensas quantidades de carvão e outras matérias-primas, deu origem a problemas de formação de resíduos resultantes da confeção e manufaturação das matérias-primas. Estes resíduos industriais normalmente têm um valor comercial muito reduzido ou mesmo nulo, tornando-se um problema para as próprias empresas. Na sua generalidade, o volume de resíduos gerado é muito grande e, como tal, as próprias empresas têm de despender muito dinheiro para lhes dar um destino conveniente, num aterro ou num tratamento próprio. Acresce ainda que estes resíduos em muitos dos casos são considerados poluentes, pois originam posteriormente efeitos negativos na natureza. A libertação de resíduos ou produtos “não-necessários” da indústria para o ambiente, sem qualquer tipo de tratamento, pode causar a poluição do ar e do solo, contaminando consequentemente as águas superficiais e os lençóis freáticos (Torgal, 2010).
A enorme diversificação das indústrias e dos processos por elas utilizados, origina resíduos de toda a espécie. Estes materiais impõem determinadas necessidades no que diz respeito à sua deposição em locais indicados para o efeito. Este facto, para além de acarretar despesas por parte da entidade que os produz, traduz-se também em manifestações muito prejudiciais para o meio ambiente. Devido ao crescimento destes resíduos ambientais, começam a procurar-se novas soluções sobre a utilização e reutilização de resíduos. Com uma seleção criteriosa e evitando misturar resíduos na mesma unidade fabril, muitos destes podem ser reutilizados ou reaproveitados.
A indústria da construção surge como uma solução viável para a utilização destes resíduos provenientes das indústrias. Não só porque o volume de material gasto para a construção é suficientemente grande, mas também porque a área da construção tem sido pioneira no avanço científico e tecnológico e também porque gasta muita matéria-prima e gera resíduos.
De entre todas as técnicas de construção que mais sofrem processos evolutivos, são de destacar as técnicas de melhoramento e reforço de solos, pois estas possibilitam a ocupação de novas áreas de solo, caracterizadas por fracas propriedades geotécnicas (baixa resistência e elevada deformabilidade). A estabilização dos solos é um processo recente, que tem como finalidade obter dos solos um melhor comportamento mecânico, uma melhor coesão, reduzir a porosidade, aumentando a impermeabilidade e reduzir a erosão provocada pelo vento e chuva (Fonseca, 1988). A beneficiação dos solos de fundação, tem como objetivo, conferir melhores características de base, otimizando o uso do espaço onde eles se inserem.
É possível referir que a melhoria das características mecânicas de um solo pode ser conseguida através de técnicas de estabilização mecânica, estabilização física e estabilização química. Esta última (através do processo da ativação alcalina) foi a escolhida para tema deste trabalho, pois acredita-se que seja aquela que melhores garantias dá ao nível do aproveitamento de resíduos, e também aquela que poderá ser utilizada em todos os tipos de solos. Muito frequentemente, a técnica da ativação alcalina está associada com a formação de geopolímeros (Davidovits, 1994).
O mecanismo exato que traduz a reação destes geopolímeros obtidos pela ativação alcalina ainda não está completamente compreendido, embora a maioria dos autores concorde que esta consiste num processo de três etapas distintas e contínuas, designadamente a dissolução, a orientação e o endurecimento (Xu, 2001).
Nas últimas décadas, têm-se verificado alterações significativas no mundo e na vida dos seus habitantes. O aparecimento de novas tecnologias, o aumento do número de indústrias, o crescimento populacional e a diversificação do consumo de bens e serviços, levou a um aumento significativo na produção de resíduos. Devido à dificuldade e escassez de áreas para deposição de resíduos, aos elevados custos de gestão e aos problemas de contaminação ambiental, os resíduos são atualmente um problema de difícil resolução. Assim, nos últimos anos as preocupações ambientais assumiram um papel fundamental na vida quotidiana em geral, de muitos cidadãos, sendo um tema prioritário na política na maioria dos países desenvolvidos, exigindo-se uma política de intervenção e atuação sérias e eficazes por forma a reduzir esta problemática.
A gestão de resíduos está regulamentada, em cada País da Comunidade Europeia, por legislação própria. Em Portugal, é o Decreto-Lei no 17812006 de 5 de Setembro de 2006 que atualmente regulamenta a gestão de resíduos. Este decreto define que a gestão de qualquer resíduo é da responsabilidade do produtor e deve obedecer ao princípio da hierarquia das operações de gestão de resíduos:
Prevenção e/ou redução;
Reutilização e/ou reciclagem e/ou valorização; Eliminação.
Neste contexto, privilegia-se a reutilização, a reciclagem e a valorização, visto que na maioria das indústrias torna-se difícil a prevenção ou a redução de resíduos. A reutilização, a reciclagem e a valorização de resíduos, além de serem operações ambientalmente corretas face à operação de eliminação, apresentam várias vantagens, nomeadamente a redução de áreas de deposição de resíduos, a diminuição do consumo de matérias-primas e a redução dos custos de eliminação, visto que estas operações de gestão de resíduos são normalmente mais económicas do que a eliminação (Torgal, 2010)
A metodologia de estudo para a valorização de um resíduo varia de acordo com as características do resíduo e com os requisitos necessários para as diferentes aplicações. A seleção de alternativas de valorização compreende a comparação das características físico-químicas dos resíduos com os requisitos necessários para as várias aplicações, seguida da seleção das alternativas mais viáveis em termos de desempenho técnico, impacte ambiental e viabilidade de mercado. As melhores alternativas são aquelas em que: i) o resíduo pode ser utilizado diretamente (sem recorrer a nenhum tratamento ou beneficiação); ii) há diminuição dos custos inerentes ao transporte do resíduo; iii) resulta um novo produto com vantagens competitivas (técnicas e/ou económicas) sobre os existentes no mercado (Van Deventer et al, 2007).
O objetivo deste trabalho de investigação passou por um estudo químico detalhado da etapa da dissolução da ativação alcalina, com o intuito de perceber a sua influência nas reações químicas. Foi elaborado um protocolo de quantificação da dissolução da matéria-prima (cinza volante classe F) em estado original, alterada mecanicamente com vários tipos de moagem. Foram também investigadas dissoluções com concentrações diferentes de
solução de NaOH e a várias temperaturas. Foram também experimentadas dissoluções de outros materiais, considerados como resíduos, mas com potencial alcalino, como lamas de uma ETA e um slag, sendo este último, sub-produto proveniente da indústria siderúrgica e da fundição de minérios.
Ao combinar a técnica da estabilização dos solos com a reutilização de resíduos industriais, através da ativação alcalina, não são apenas as questões de estabilidade e segurança que estão em estudo ao longo deste trabalho, mas também as questões ambientais e de sustentabilidade que dão forma à busca de materiais classificados como resíduos para reutilização nos processos construtivos. Com esta reutilização torna-se possível a redução de impactos negativos no meio ambiente, mas também se conseguem obter aplicações para os resíduos produzidos por outro tipo de indústrias.
Na sequência de trabalhos anteriores (Soares, 2013), foi elaborado um estudo com o intuito de perceber a influência dos diversos intervenientes da ativação alcalina, como o processo de estabilização química, num solo residual granítico. Foi necessário um procedimento prévio de otimização e caracterização das misturas. A quantidade dos percursores alcalinos (ativador e cinzas) foi suficiente para garantir que a mistura final tinha um comportamento tipicamente fluido e, portanto, podia ser vertido em moldes, sem qualquer necessidade de compactação, apenas com alguma necessidade de vibração, num processo semelhante ao da moldagem de betão.
1.2 - OBJECTIVOS
Esta Dissertação de Mestrado tem como objetivo contribuir para um melhor conhecimento e compreensão da técnica da ativação alcalina, particularizando esta técnica com a estabilização de solos, nomeadamente de um solo residual granítico. Numa primeira parte, no âmbito da química, estudou-se a dissolução nas cinzas volantes e também noutros resíduos (lamas ETA e slag), por forma a quantificar o material solúvel em soluções de NaOH e, deste modo, compreender o efeito dos diversos fatores sobre a ativação alcalina. Efetuaram-se alterações mecânicas ao material residual e alterações de concentração e temperatura por forma a comparar as quantificações das dissoluções. Numa segunda parte, no âmbito do comportamento mecânico, teve-se oportunidade de medir as propriedades mecânicas de
provetes em caldas ativadas, e de comparar os resultados com os obtidos na parte química. As diferentes condições dos resíduos (cinzas volantes, lamas ETA e slag) assim como as várias condições do ativador foram as mesmas verificadas na primeira parte química. Através de ensaios laboratoriais, pretendeu-se quantificar os benefícios alcançados com a adição de cinzas ativadas (e outros resíduos) e otimizar o processo de estabilização de solos residuais. Fabricaram-se caldas ativadas de base alcalina para melhorar o solo granítico em termos de resistência mecânica e durabilidade.
Para o efeito da primeira parte química, o trabalho que se apresenta visa a caraterização da dissolução em NaOH, em resíduos com potencial alcalino, bem como a caraterização dos vários fatores que influenciam o processo de dissolução. Assim sendo, os principais objetivos podem definir-se como:
Caraterização morfológica e química dos materiais residuais com recurso a SEM/EDS;
Efeito do tempo na dissolução no material residual; Efeito da concentração de NaOH na dissolução; Efeito do tempo de moagem na dissolução; Efeito da velocidade de rotação na dissolução; Efeito da temperatura na dissolução;
Identificação e quantificação das espécies solúveis.
Para o efeito da segunda parte mecânica e para que tal análise seja passível de ser efetuada, têm de ser ponderados diversos fatores que poderão ter interferência nos resultados finais de resistência à compressão simples, entre os quais:
Evolução da resistência mecânica dos diferentes resíduos com o tempo de cura (idades de cura de 7, 14, 28, 60 e 90 dias);
Efeito na resistência mecânica em cinzas com o tempo de moagem; Efeito na resistência mecânica em cinzas com a velocidade de rotação;
Efeito na resistência mecânica em cinzas com a concentração de NaOH presente no ativador;
Caraterização do módulo de deformabilidade (idade de cura de 28 dias).
1.3 - ORGANIZAÇÃO DA DISSERTAÇÃO
Neste ponto será abordada a forma como está organizada esta dissertação. Foi definido um programa experimental, constituído por duas partes. Uma primeira parte em que foi feita uma caracterização morfológica e química aos materiais residuais em estudo, através de Microscopia Eletrónica de Varrimento (SEM), acompanhada por Espectrometria de Dispersão de Energia (EDS). Estas técnicas permitem obter imagens com a microestrutura do material e fazer a identificação qualitativa e semiquantitativa dos elementos químicos presentes no mesmo. Posteriormente realizaram-se várias dissoluções por forma a identificar o material solúvel e sua análise quantitativa.
Numa segunda parte, que se carateriza por um extenso programa de ensaios, requereu uma preparação prévia dos resíduos, para que estes pudessem estar disponíveis para o fabrico de provetes. No estudo das diversas misturas em calda com os diferentes resíduos é colocado em prática o processo de estabilização do solo residual, sendo aqui descritas todas as técnicas de moldagem e cura das amostras, bem como os ensaios de compressão simples, utilizados para avaliar a resistência mecânica.
Como tal, a presente dissertação está organizada em 6 Capítulos, sendo o primeiro dos quais constituídos pela presente introdução.
A revisão bibliográfica, que incorpora o Capitulo 2, apresenta a descrição da técnica da ativação alcalina. É descrito detalhadamente todo o processo da geopolimerização, os fatores que a influenciam, bem como alguns conceitos inerentes ao assunto em estudo e sua envolvente.
No Capítulo 3 caracterizam-se os materiais utilizados nos processos de melhoria de solo, mais concretamente o solo objeto de melhoria, a cinza, lamas ETA e slag utilizados e as soluções que dão origem ao ativador. São ainda expostos neste capítulo uma caracterização química de todos dos materiais residuais utilizados, assim como a sua proveniência.
O Capítulo 4 diz respeito à metodologia laboratorial da primeira parte química e segunda parte mecânica, onde é descrito todo o procedimento experimental. É apresentado aqui também toda a preparação prévia dos materiais residuais utilizados e os ensaios executados nas misturas realizadas e estudadas, e os ensaios de compressão uniaxial.
No Capítulo 5 são apresentados e discutidos todos os resultados do trabalho experimental. Este capítulo está dividido em duas partes. Uma parte química e uma parte mecânica. Na parte química são realizadas várias representações gráficas para avaliar a evolução das diversas dissoluções e caracterização analítica da sílica e do alumínio dissolvidos. Na parte mecânica estão expostos gráficos e observações da resistência à compressão simples em função dos parâmetros estudados na parte química
As conclusões deste trabalho são expostas no Capítulo 6, onde também são apresentadas algumas propostas para trabalhos futuros, no sentido de otimizar os processos de análise de materiais residuais com potencial alcalino. Serão também apresentadas algumas propostas de continuidade e de desenvolvimento do trabalho efetuado.
2 - REVISÃO BIBLIOGRÁFICA
2.1 - INTRODUÇÃO
O solo natural apresenta grande utilidade para construção, por se tratar de um material abrangente e por apresentar baixo custo, sendo a sua disponibilidade praticamente ilimitada. O solo é frequentemente usado nas construções em terra e nas fundações (onde são transmitidas as solicitações das construções), sendo por exemplo nas fundações onde é exigida uma estabilização do solo. A estabilização de solos visa assim, a melhoria das características e das propriedades do solo (resistência mecânica, deformabilidade, permeabilidade, etc.).
Contudo, o solo é um material complexo e variável de acordo com a sua localização. Pode portanto não cumprir os requisitos necessários na sua aplicabilidade. De acordo com Cristelo 2001, quando tal acontece, tem de se adotar a solução mais indicada para cada caso:
Aceitar o solo original e ajustar o projeto às restrições por ele impostas; Remover o solo original e substituí-lo por um material de qualidade superior; Alterar as propriedades do solo existente de forma a criar um material capaz de
responder às necessidades da tarefa prevista (estabilização de solo).
Uma das principais técnicas normalmente utilizadas para superar os problemas criados pelo baixo desempenho dos solos é a sua beneficiação com um ligante de base cimentícia. Tradicionalmente, estes ligantes são cimento e/ou cal, que agregam as partículas do solo num esqueleto pétreo através de reações químicas.
O cimento é o principal material de construção usado como ligante. No entanto, a produção do cimento levanta muitas questões ambientais e de sustentabilidade energética e económica que, desta forma, encorajam o desenvolvimento de novos ligantes para a construção.
A crescente procura das matérias-primas associadas à produção do cimento, aliada ao facto do aumento exponencial dos resíduos resultantes do seu fabrico, veio trazer um novo impulso
à questão de valorização dos resíduos. Esta valorização, como o próprio nome indica, pretende reutilizar os resíduos que de outra forma teriam como destino um aterro.
O uso de resíduos na indústria da construção é uma importante contribuição para a redução no consumo de cimento. Um bom exemplo disso, são as cinzas volantes. Resultam da combustão do carvão nas centrais termoelétricas, e consistem na matéria inorgânica que não arde durante o processo.
As razões para investigar o uso de ligantes alternativos para a construção e estabilização de solos não são apenas técnicas e de conhecimento prático (haverá sempre boas razões para melhorar o desempenho de todo e qualquer material de construção), mas também do meio
ambiente, devido aos altos níveis de CO2 libertados durante a produção de cimento (Torgal,
2010).
Os geopolímeros são um bom exemplo como ligantes alternativos. São cadeias ou redes de minerais agrupados com ligações covalentes, formando-se assim um novo material. As propriedades e usos dos geopolímeros estão a ser explorados em muitas áreas científicas e industriais: química inorgânica moderna, química-física, química coloidal, mineralogia, geologia e em outros tipos de tecnologias de transformação de engenharia, nomeadamente aplicações para engenharia civil (www.geopolymer.org).
Os geopolímeros podem ser obtidos através da técnica da ativação alcalina. As primeiras investigações para a elaboração de ligantes, com o propósito de serem utilizados na área da construção civil através da ativação alcalina, remontam à década de 50 (Davidovits, 1991).
As pesquisas no domínio dos ligantes obtidos por ativação alcalina, sofreram um incremento exponencial a partir das descobertas efetuadas pelo investigador francês Joseph Davidovits que desenvolveu e patenteou ligantes obtidos por ativação alcalina de caulino e metacaulino (Silva et al, 1999).
O domínio dos ligantes obtidos através de ativação alcalina tem sofrido sucessivos avanços ao longo dos tempos. Com efeito, não só as cinzas volantes apresentam potencial para a ativação alcalina. Davidovits verificou que era possível produzir aglutinantes, tirando partido da reação de um líquido alcalino com silício (Si) e alumínio (Al), com origens geológicas ou
resultantes de subprodutos de outros materiais, de que são exemplo as cinzas volantes e escórias (Davidovits, 1994). Assim sendo, vários outros resíduos apresentam potencial para utilização de ligantes em ativação alcalina, tais como escórias, subprodutos siderúrgicos, lamas, etc.
2.2 - ATIVAÇÃO ALCALINA
Para Palomo et al. (1999) a ativação alcalina é uma reação de polimerização de compostos alumino-siliciosos que ocorre em meio alcalino, na presença de determinadas soluções, como por exemplo hidróxido de potássio ou de sódio e silicato de potássio ou de sódio. Trata-se assim de um processo químico que permite a transformação de determinadas estruturas parcial ou totalmente amorfas, em estruturas cristalinas com propriedades cimentícias.
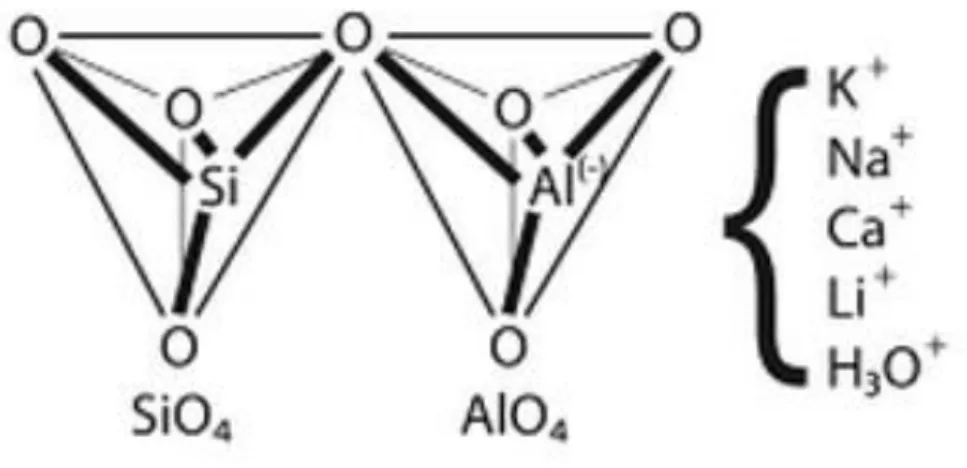
Para Vargas et al. (2006) a ativação alcalina transforma as estruturas amorfas, vítreas (parcial ou totalmente amorfas) em compostos cristalinos bem compactos. No entanto, para que esse processo ocorra é necessário um meio fortemente alcalino, o que é conseguido utilizando-se soluções de NaOH, ou outras soluções alcalinas. Desta forma, é possível dissolver parcialmente a sílica e a alumina, bem como hidrolisar (decompor uma molécula pela ação da água) a superfície das partículas das matérias-primas. Na ativação alcalina, a
sílica (SiO2) e a alumina (Al2O3), constituintes dos alumino-silicatos, reagem entre si em
ambiente fortemente alcalino, organizando-se tridimensionalmente pela partilha dos átomos
de oxigénio. Os iões alcalinos (K+ e Na+) atuam como agentes formadores da estrutura,
compensando o excesso de cargas negativas decorrente da alteração da coordenação do alumínio com o oxigénio, e são os componentes que determinam as propriedades ligantes. Obtém-se então um novo tipo de materiais, com elevada resistência mecânica, estabilidade térmica e dureza elevada, onde o cálcio está praticamente ausente (designados por geopolímeros).
2.2.1 - MEIO ALCALINO
De acordo com Raymond Chang, uma base pode ser descrita como uma substância que
cede iões hidróxido (OH−) quando dissolvida em água. Ou seja, as bases ionizam-se em água
Svante Arrhenius para classificar substâncias cujas propriedades em solução aquosa eram bem conhecidas.
Alguns exemplos são: hidróxido de sódio (NaOH), hidróxido de potássio (KOH),
hidróxido de bário [Ba(OH)2].
Algumas das características das bases são:
As bases têm sabor amargo;
As bases são escorregadias ao toque, devido à saponificação das matérias gordas à superfície da pele. Por exemplo, os sabões que contêm bases apresentam esta característica;
As soluções concentradas são cáusticas (causam queimaduras químicas);
As bases causam mudança de cor nos corantes vegetais, por exemplo, causam uma alteração na cor do tornesol de vermelho para azul;
As soluções aquosas de bases conduzem eletricidade;
As bases são normalmente solúveis em água, embora algumas, como o carbonato de bário, sejam apenas solúveis quando reagem com uma solução aquosa ácida. A definição de base, segundo Arrhenius, é limitada pois aplicam-se apenas a soluções aquosas. Definições mais gerais foram propostas pelo químico dinamarquês Joannes Bronsted em 1932. Uma base de Bronsted é um aceitador de protões. Note-se que as definições de Bronsted não obrigam a que as bases se encontrem em soluções aquosas.
O hidróxido de sódio e o hidróxido de bário, por exemplo, são eletrólitos fortes. Isto significa que se ionizam completamente em solução [1] e [2]:
O ião OH− pode aceitar um protão [3]:
Portanto, o OH− é uma base de Brosnsted.
A base forte mais comum usada em laboratório é o hidróxido de sódio. É barata e solúvel (todos os hidróxidos de metais alcalinos são solúveis). Todos os elementos do Grupo 2 da
Tabela Periódica formam hidróxidos do tipo M(OH)2, onde M representa um metal
alcalino-terroso.
Atendendo que as concentrações de H+ e OH− em soluções aquosas são frequentemente
números muito pequenos e, portanto, inconvenientes de lidar, Soren Sorensen, em 1909, propôs uma medida mais prática designada por pH. O pH de uma solução define-se como o co-logaritmo da concentração do ião hidrogénio (em mol/L) [4]:
O sinal negativo dá-nos um número positivo para o pH que, de outro modo, seria negativo
devido ao baixo valor de [H+]. Além disso, o termo [H+] diz respeito apenas à parte numérica
da expressão para a concentração do ião hidrogénio, visto que não se pode aplicar logaritmos a unidades. Assim, o pH de uma solução é uma quantidade adimensional.
Uma vez que o pH é simplesmente um modo de exprimir a concentração hidrogeniónica, as soluções ácidas e básicas a 25ºC podem-se distinguir pelos seus valores de pH como se segue [5], [6], [7]:
Note-se que o pH aumenta quando [H+] diminui. Em laboratório, o pH de uma solução é
2.2.2 - O ATIVADOR ALCALINO
Na sua generalidade, os ativadores usados em ativação alcalina, são fabricados com base em hidróxido de sódio e silicato de sódio. Assim, é possível dizer que os ativadores são reagentes que têm de ser preparados quimicamente, pois não se encontram disponíveis na Natureza. No processo da ativação alcalina, podem-se utilizar ativadores de dois tipos:
Os simples, constituídos por uma base alcalina (geralmente hidróxido de sódio ou de potássio);
Os compostos, formados pela associação de uma base alcalina com um silicato de sódio ou de potássio.
O hidróxido de sódio está disponível em cristais e/ou cristais granulados, bastando promover a sua dissolução em água de acordo com a concentração pretendida. Este hidróxido de sódio irá atuar de forma a propiciar o processo de dissolução das matérias-primas, enquanto o silicato de sódio vai ter o papel de um ligante ao promover a reorganização da estrutura (Yang et al., 2008).
Palomo et al. (1999) chegaram à conclusão de que quando a solução alcalina contém silicatos solúveis, de sódio ou de potássio, as reações ocorrem em taxas maiores do que quando são apenas utilizados hidróxidos como ativadores.
Xu e Van Denventer (2000) observaram que a utilização da combinação entre silicato de sódio e o hidróxido de sódio como solução alcalina melhora a reação entre o material de origem e a solução. Em complemento, após o estudo da geopolimerização de dezasseis minerais naturais de Al−Si, foi verificado que em geral, a solução de NaOH causa uma maior amplitude de dissolução de minerais do que a solução de KOH.
Puertas et al. (2000) efetuaram um estudo sobre a ativação alcalina de pastas cimentícias, utilizando misturas contendo apenas escória ou cinzas volantes, ativadas com NaOH em solução de 2 molal e 10 molal. Concluiu-se que para a situação de utilização de um ativador com maior concentração (10 molal), a resistência mecânica para diferentes tempos de cura aumenta com o correspondente aumento da percentagem de escórias no aglomerado (até esta atingir os 100%).
Hardjito e Rangan, (2005), ao estudarem o efeito da concentração da solução de hidróxido de sódio na resistência à compressão, concluíram que uma maior concentração da solução de NaOH resultou numa maior resistência à compressão, para dois rácios diferentes de silicato de sódio / hidróxido de sódio.
2.3 - GEOPOLÍMEROS
Victor Glukhovsky, desenvolveu nos anos 50 na Ucrânia, sistemas com ativação alcalina que continham silicato de cálcio hidratado (CSH) e fases com alumino-silicatos. Estes sistemas de ativação alcalina foram usados para construir um edifício na Rússia. Glukhovsky foi o primeiro autor que constatou que todo o processo geológico de transformação de algumas rochas vulcânicas em zeólitos toma lugar durante a formação das rochas sedimentares a baixas pressões e temperaturas. Este processo pode ser utilizado em sistemas cimentícios. Na fase de formação destes sistemas cimentícios, em meio alcalino, é originada uma rede cristalina formada à base de alumínio e silício. Esta rede cristalina apresenta uma enorme durabilidade. A utilidade destes sistemas oferece um potencial muito grande, devido ao enorme campo de aplicação das propriedades das estruturas cristalinas dos zeólitos (Glukhovsky, 1965).
Em 1972 Davidovits designou de “geopolímeros” as malhas cristalinas tridimensionais de alumino-silicatos que se formam naturalmente, a baixas temperaturas e em curtos períodos de tempo (Davidovits 1988).
Depois de 1970 vários projetos foram implementados para provar a teoria de Davidovits, segundo a qual as pirâmides no Egito foram construídas através de blocos de pedra fabricada
in situ e deixados repousar no próprio local, desenvolvendo assim uma rocha zeolítica
artificial (Davidovits 1994).
Entre 1979 e 1995, muitos trabalhos foram publicados e emitidas patentes pelo Davidovits e a sua equipa em geopolimerização. Estas patentes incluem o desenvolvimento de um polímero mineral constituído por alumino-silicatos, o qual é formado a temperaturas de até cerca de 120ºC, como uma solução sólida. Este é o método para a obtenção de um aglutinante geopolimérico (Davidovits, 1994), bem como para a produção de um totalmente hidratado alumino-silicato geopolimérico.
Hoje em dia, a aplicação da ativação alcalina está presente em muitas áreas (ligações cerâmicas alcalinas, hidrocerâmicos, sistemas cimentícios ativados alcalinamente, etc), sendo que a abundância de todos estes novos materiais é elevada. Assim sendo, os geopolímeros podem ser definidos como polímeros inorgânicos.
Segundo Davidovits (Davidovits 1988) a reação de geopolimerização realiza-se em condições altamente alcalinas entre um pó de alumino-silicato e uma solução ativadora (baseada numa mistura molar de hidróxido de sódio e um silicato alcalino, por exemplo sódio ou potássio), em condições ambientais.
Um alumino-silicato é um mineral que contém óxido de alumínio (Al2O3) e sílica (SiO2).
Podem-se considerar como derivados dos silicatos, devido à substituição dos iões Si4+ pelos
iões Al3+, os quais devido à carga negativa que possuem, requerem catiões adicionais com a
finalidade de conseguirem neutralizar a carga elétrica.
O processo de polimerização ocorre quando se coloca um material pozolânico (alumino−silicato) em contacto com a solução do ativador alcalino, cujo resultado é a formação de cadeias de polímeros, depois dos iões em solução terem sido reorganizados. Estas cadeias de polímeros podem ser consideradas como o resultado da policondensação de iões de ortosialato. Uma vez que o mecanismo exato desta reação ainda não foi completamente determinado, normalmente assume-se que a sua síntese é levada a cabo por intermédio de oligómeros os quais provêm das estruturas unitárias da rede macromolecular tridimensional.
2.3.1 - PROPRIEDADES DOS ÓXIDOS AO LONGO DE UM PERÍODO
Uma maneira de comparar as propriedades dos elementos representativos ao longo de um período é examinar as propriedades de uma série de compostos semelhantes. Como o oxigénio se combina com quase todos os elementos, pode-se fazer uma comparação das propriedades de óxidos dos elementos do terceiro período para ver em que é que os metais diferem dos semimetais e dos não-metais. Alguns elementos do terceiro período (P, S e Cl) formam vários tipos de óxidos, mas para simplificar, considera-se apenas os óxidos em que os elementos têm o número de oxidação mais alto (Raymond Chang).
O ião oxigénio tem tendência para formar o ião óxido. Esta tendência é grandemente favorecida quando o oxigénio se combina com os metais que têm energias de ionização
baixas, nomeadamente os dos Grupos 1 e 2 e o alumínio. Ao longo da série Na2O, MgO,
Al2O3 e SiO2 o caráter iónico vai diminuindo. Assim, o Na2O é considerado um composto
100% iónico, enquanto o SiO2 é 100% covalente. Todos têm estruturas tridimensionais
extensas nas quais cada catião está rodeado de um número específico de aniões e vice-versa. As ligações são fortes, apresentando todos estes compostos um ponto de fusão elevado.
Os óxidos de fósforo, de enxofre e de cloro são compostos moleculares constituídos por unidades pequenas e discretas. As fracas atrações entre estas moléculas resulta em pontos de fusão e de ebulição relativamente baixos.
A maior parte dos óxidos pode ser classificada em acídicos ou básicos dependendo de produzirem ácidos ou bases quando dissolvidos em água ou se reagem como ácidos ou bases em certos processos. Alguns óxidos são anfotéricos, o que significa que apresentam propriedades ácidas quando reagem com bases e propriedades básicas quando reagem com ácidos. É o caso do óxido de alumínio que não reage com a água. Contudo, mostra propriedades básicas ao reagir com ácidos [8]:
Também exibe propriedades ácidas ao reagir com bases [9]:
Repare-se que esta neutralização ácido-base apenas produz um sal (contendo iões Na+ e
Al(OH−)4), mas nenhuma água. O Al2O3 é classificado com um óxido anfotérico.
O óxido de silício também não reage com a água. Tem, contudo, propriedades ácidas pois reage com bases muito concentradas [10]:
Por isso, as soluções aquosas concentradas de bases como NaOH (aq) não devem ser
Os óxidos metálicos são em geral básicos e a maioria dos óxidos de não-metais são ácidos. Os óxidos metálicos básicos reagem com a água para dar hidróxidos metálicos [11]:
2.3.2 - NOMENCLATURA E PROPRIEDADES DAS LIGAÇÕES IÓNICAS E MOLECULARES
Em 1988 Davidovits propôs a seguinte nomenclatura para os processos geopoliméricos (Davidovits, 1988):
siloxo, poli(siloxo): unidade −Si−O− envolta numa macromolécula de poli(siloxo) (−Si−O−Si−O−);
siloxano: unidade siloxo alcalina-terrosa, sendo o metal alcalino o sódio, ou potássio, ou lítio ou cálcio. A Figura 2.2 mostra algumas estruturas moleculares de poli(siloxanatos);
silanol: grupos −Si−OH intermédios ou de final incluídos nas macromoléculas poli (siloxo);
sialato: é uma forma abreviada para silico-oxo-aluminato alcalinos, sendo o metal alcalino, o sódio ou potássio ou lítio ou cálcio e o termo poli (sialato) abrange todos os geopolímeros contendo, pelo menos, uma unidade de (Na, K, Li, Ca) (Si−O−Al), (Na, K, Li, Ca)−sialato.
Há analogias estruturais diretas entre moléculas de silicatos, aluminosilicatos e poli(metilsiloxanos). Existem numerosas estruturas de silicatos alcalinos solúveis. O que é importante aqui é a identidade exacta em forma e estrutura entre as moléculas à base de siloxonatos (silicatos alcalinos) e silicones. Esta é outra prova da existência, de um modo geral, de uma ligação covalente de Si−O−Si−O em minerais.
Os átomos de carbono e silício são ambos tetravalentes. Numa fase muito inicial da química de polímeros foi levantada a questão sobre a capacidade do silício para produzir cadeias de átomos que contêm átomos de hidrogénio análogos aos compostos alifáticos de carbono. Em teoria, a cadeia de polisilano Figura 2.1a seria equivalente à cadeia de polietileno da Figura 2.1b.
Figura 2.1 – (a) polisilano; (b) polietileno (Davidovits, 1988)
Contudo, na prática, estes polisilanos, eram compostos muito perigosos e instáveis. No entanto, pode ser preparado um composto de silício, envolvendo a formação de um grupo siloxano muito importante (também designado de siloxo), Si−O−Si. Este grupo siloxano resulta da reação de condensação de dois grupos silanol de acordo com [12]:
A reação do grupo siloxano, originou a produção de polímeros minerais orgânicos, conhecidos como silicones. Pouco tempo depois, logo após esta descoberta notável, tornou-se evidente que a ponte de siloxano tinha algo em comum com a estrutura atómica básica do quartzo. Considerando que no quartzo 4 átomos de oxigénio estão ligados a um átomo de silício, nos silicones, apenas pode haver um ou dois ou três átomos de oxigénio por átomo de silício. Os oxigénios em falta ser substituídos por um grupo orgânico R (Figura 2.2).