U IVERSIDADE FEDERAL DE UBERLÂ DIA
ESTUDOS SI TÉTICOS PARA A PREPARAÇÃO DO
ÁCIDO 5 AMI O 4 OXOPE TA ÓICO
DOUGLAS EDUARDO SOARES PEREIRA
UBERLÂ DIA – MG
DOUGLAS EDUARDO SOARES PEREIRA
ESTUDOS SI TÉTICOS PARA A PREPARAÇÃO DO
ÁCIDO 5 AMI O 4 OXOPE TA ÓICO
Dissertação apresentada ao Programa de Mestrado em Química da Universidade Federal de Uberlândia, para a obtenção do título de mestre em química.
Orientador: Prof. Dr. Luis Antônio
Ortellado Gómez Zelada
#
Dedico
!
"
#
$
!%
!
#
AGRADECIME TOS
$ %&' ' () )*)' *+, - . / 0 0 () %&' ( 1 %' 2* (
-' - ( 0 3 %&' ' 0 ( ) ) 4'5
' ' ( 4' - ' ( 1' 1 , )' )+6 -' - ' 78 -' 9 :; <
'' ' 0 6 %' , )' ((' ) 1=( ( * '8 , - ) 1' <
0 - ) %&' '- ) 9 0 ( ;/ 0 ' ( , () ' -' - 5
' '65 5 >* ( )' ' ) ' 7, 3 ? 0 ' ) %&'/ 0' '
0 - 0 , ) 0 '( -' 4 - , )'( ) (, ) '( * ) 3 %&' ' ) 4'5
' '/ 0 ' 6' - , )' 8 ) (/ 0 ( @ ( ( 0A 0 8 , 3 5
' )=- -' , / 0 -' ' %&' ' 6' - , )' :* 0 , )'( ' )7 '5
$ 1 ( . ( (/ 0 '( (0 -) '( ((' - 8 =)
-*- 5
, *( - '( -' 8 ( ' )7 '/ ' # / 0 -' ' %&' , 3 5
#
ESTUDOS SI TÉTICOS PARA A PREPARAÇÃO DO ÁCIDO 5 AMI O 4 OXOPE TA ÓICO
*)' C '*8 ( * ' ' (
) ' C '65 5 >* ( )' ' ) ' ', 3 ?
() )*)' *+, - 1 ( .
DE5F!!5G! / /
Resumo
' 0 ( ) ) 4' 6' , ()* '( 8* ( ,=)' '( ' ) %&' ' @- ' H
, ' F 'B'0 ) 7 -' 9 > ; 8* ( ( *( 1 '(/ :* 0* (( , 0 , )
(* 6@- 0 0 %&' , '((' , '5 ' 2 ) 1' 0 , ) ( ' *(' () ( ,
()* '( (* ( 0 '0 ( 6')' , - ( 0' 0 ) '*) ' 8 *0' 0 (:* ( '
:* () ,'( (('- '( () ) 0' ) 4'5 .' , ( - ' ( 0 ' 0 ( )
()* ' ') ( (+ ) ( :* 6'(( , - ((+1 ( <( -' %I ( (0' +1 ( , '((' , '
:* 0 , ) (( , *, 6@- @0 0 0 %&' '( 1 '( ' > 0 '0'()'(5 ,
'( ' 2 ) 1'( / - *( 1 / -' )' ' *(' 0 ((I ( - , ),'(6= - * )
) 0 6 *%&'/ :* ' 8 ' *(' *, )' 5 , 0 '- , )' ) )*
()* ' - , ) / :* 1' 1 *%&' -', 3 -' , )@ -' ,'() '*
0'*-( ) 1 / ' ( 1 ' ( *%&' '*) '( 8 *0'( 6* - ' ( =, :*
( 2 '5 ( 1' 1 , )' *, 0 '- , )' 0 '0'()' 1' 1 ' ' *('
)@ ( (6 J - . ( 7 ' >+:* ' 0 , ) * 0 0 %&' *, '(
1 '( ( 2 '( ' > ) 1=( *, 0 '- , )' 1 )'5
0 '- , )' 1' 1 (* ) 0 6 *%&' ' 0 -* (' ' > 6' , '/
*) 3 ' ( *, - ) ( ' 0 @ ' (*0' ) ' (' - ' ' *, 0 4'
4 '8 %&' -' () *+ ' ' ' )7 ' :* 6* - ' 1 (' 0 ((&' ),'(6= - 5
) ) )'/ ' 1 ' (( , ( ) ) 3 ' 6' ' ) ' 6' , , ()* 1 '
#
Synthetic studies for preparing the 5 amino 4 oxopentanoic acid
*)4' C '*8 ( * ' ' (
*0 1 ( C '65 5 >* ( )' ' ) ' ', 3 ?
() )*)' *+, - 1 ( .
DE5F!!5G! / /
Abstract
)4 ( K' L ) K ( ()* (', , )4' ( 6' ' ) 8 )4 H , ' F
'B'0 ) ' - - 9 > ; (', '6 )( 1 ) ( )4 ) -'* 'K )( (M
0 0 ) ' 5 4 ( 0* 0'( K'* 'K )4 *( '6 )4 ( 1 ) ( )4 ()* ( '6 )(
04')' M , - 0 '0 ) ( M ')4 8 '*0 '6 ( -4 K4 -4 K 2' )' )4 (
L '6 K' L5 4 K ( -) 6' )4 ( ()* M/ 0 )4( '6 (M )4 ( ( K4 -4 -'*
-- (( )' )4 1 -' ) ' ( '* 1 ' , ) -'* 'K (M
:* -L 0 0 ) ' '6 )4 > 1 ) ( 0 '0'( 5 ')4 , K ( )' )* '* )4
*( 0 ((* ( '1 )4 ),'(04 - ' ( * 8 )4 6 () 0 '6 *-) ' )4 )
, ( )4 *( -)' 5 ) )* 0 '- 8 0 1 '*( M ()* )4 ) 1' 1 )4
*-) ' '6 , ) - 3 - 4 ( (4'K )) ( -) 1 )M/ ' ( 1 8 )4 *-) ' '6 ')4
6* -) ' 8 '*0( ( ( )4'( ( 5 4 1 '0, ) '6 )4 ) 0 '- 8
1' 1 8 )4 *( '6 )4 ) M( ( (6 '6 ' > :* 4 ( 'K )4
0 0 ) ' '6 ' '6 )4 > K ) 1 ) ( )4 '*84 -) :* -L 0 '- 85
*-4 0 '- 8 1' 1 )( 6 () 0 )4 *-) ' '6 )4 0 , M 6' ,
> / *( 8 0 *, - ) M3 (*00' ) M - ' 4M '8 ) 8
:* 0, ) * ) )4 )4 ) K' L * ),'(04 - 0 ((* 5 1 )4 ((/ )4
1 ) (' (M )4 ( 3 K ( ' ) ( , B)* 6' , * )' )4 66 -* ) ( 6'*
N
Í DICE
@85
RELAÇÃO DE FIGURAS __________________________________________ N
RELAÇÃO DAS EQUAÇÕES QUÍMICAS____________________________ N
RELAÇÃO DOS ESQUEMAS____________________________________________ N
SÍMBOLOS E ABREVEAÇÕES_____________________________________ N #
CAPÍTULO 1 – I TRODUÇÃO E OBJETIVOS
1.1 Introdução ____________________________________________________________ "
1.1.1 Terapia Fotodinâmica (TFD) ____________________________________________ 1.1.2 Ácido 5 aminolevulínico (ALA) __________________________________________ D
1.1.3 Metodologias de síntese do ácido 5 amino 4 oxopentanóico (ALA) e derivados_______ H
1.2 Objetivo ______________________________________________________________ G
CAPÍTULO 2 – PREPARAÇÃO DO ÁCIDO 5 AMI O 4 OXOPE TA ÓICO (ALA)
2.1 Introdução ___________________________________________________________ ""
2.2 Síntese do anidrido succínico (1)____________________________________ ""
2.3 Síntese do ácido 4 metóxi 4 oxobutanóico (2)_______________________________ "
2.4 Síntese do 4 ciano 4 oxobutanoato de metila (4)________________________ "
2.5 Tentativa de obtenção do 5 (etanoilamino) 4 oxopentanoato
de metila (10)____________________________________________________"D
2.6 Análise final_____________________________________________________"F 2.7 Conclusões______________________________________________________ "O
PARTE EXPERIME TAL_____________________________________________ "P
'- , )'( ,=)' '(QQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQ "P
:* 0 , )'( ,0 8 '(QQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQ "P
5" + ) ( ' ' (*--+ -' 9";QQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQ "E
5 + ) ( ' R- ' F , )7B F 'B' *) 7 -' 9 ;QQQQQQQQQQQQQQQQQQQQQQQQQ "E
5D + ) ( F - ' ' F 'B' *) ' )' , ) 9D;QQQQQQQQQQQQQQQQQQQQQQQQQQ "G
5F + ) ( ' - )' -' 9 * ;QQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQ "G
N
5O ) ) 1 ' ) %&' ' H 9 ) ' , '; F 'B'0 ) ' )'
, ) 9"!;QQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQ "
CAPÍTULO 3 –PROCEDIME TO EXPERIME TAL ELABORADO PARA A PREPARAÇÃO DO ÁCIDO(ETA OILAMI O) 4 OXO
PE TA ÓICO UTILIZA DO CATÁLISE DE TRA SFE RÊ CIA DE FASE
3.1 Introdução __________________________________________________________ H
3.2 Preparação dos sais 4 ciano 4 oxobutanoato de benziltrietilamônio (15 a) e 4 ciano 4 oxobutanoato de potássio (15 b) por
CTF SL________________________________________________________ P
3.3 Preparação do ácido 5 etanoilamino 4 oxopentanóico (17)_____________ P
3.4 Análise final____________________________________________________ G
3.5 Conclusões_____________________________________________________ D!
PARTE EXPERIME TAL_____________________________________________ D"
'- , )'( ,=)' '(QQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQ D"
D5" 0 %&' '( ( ( F - ' F 'B' *) ' )' 3 ) ) ,S '
9"H ; F - ' F 'B' *) ' )' 3 ) ) ,S ' 9"H ; 0'
. >QQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQ D"
D5 0 %&' ' @- ' H ) ' , ' F 'B'0 ) 7 -' 9"P;QQQQQQQQQQQQQQQ D"
CAPÍTULO 4 –PROCEDIME TO EXPERIME TAL ELABORADO PARA A PREPARAÇÃO DO ÁCIDO 5 (ETA OILAMI O) 4 OXO PE TA ÓICO UTILIZA DO CATALIZADOR Pd/C
4.1 Introdução __________________________________________________________ DF
4.2 Preparação dos sais 4 ciano 4 oxobutanoato de benziltrietilamônio (15 a) e 4 ciano 4 oxobutanoato de potássio (15 b) por
CTF SL________________________________________________________ DH
4.3 Preparação do ácido 5 etanoilamino 4 oxopentanóico (17)_____________ DO
4.3.1 Construção do aparelho de hidrogenação catalítica________________________ DO
4.3.2 Preparação do ácido 5 etanoilamino 4 oxopentanóico (17)____________ DG
N
4.5 Conclusões_____________________________________________________ F"
PARTE EXPERIME TAL_____________________________________________ FD
'- , )'( ,=)' '(QQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQ FD
F5" 0 %&' '( ( ( F - ' F 'B' *) ' )' 3 ) ) ,S '
9"H ; F - ' F 'B' *) ' )' 3 ) ) ,S ' 9"H ; 0'
. >QQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQ FD
F5 + ) ( ' - ) ( ' 0 @ ' (' - ' ' QQQQQQQQQQQQQQQQQQQQQQQQQQ FD
F5D 0 %&' ' @- ' H ) ' , ' F 'B'0 ) 7 -' 9"P;QQQQQQQQQQQQQQQQ FF
CAPÍTULO 5 – PREPARAÇÃO DO ÁCIDO 5 AMI O 4 OXOPE TA ÓICO (ALA)
5.1 Introdução ___________________________________________________________ FO
5.2 Síntese do Ácido 4 metóxi 4 oxobutanóico (2)_______________________________ FP
5.3 Síntese do 4 ciano 4 oxobutanoato de metila (4)________________________ FP
5.4 Preparação do ácido 5 etanoilamino 4 oxopentanóico (17)_____________ FE
5.5 Análise final_____________________________________________________FG 5.6 Conclusões______________________________________________________ FG
PARTE EXPERIME TAL_____________________________________________ H"
'- , )'( ,=)' '(QQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQ H"
H5" + ) ( ' R- ' F , )7B F 'B' *) 7 -' 9 ;QQQQQQQQQQQQQQQQQQQQQQQQQ H"
H5 + ) ( F - ' ' F 'B' *) ' )' , ) 9D;QQQQQQQQQQQQQQQQQQQQQQQQQQ H
H5D + ) ( ' F - ' F 'B' *) ' )' , ) 9F;QQQQQQQQQQQQQQQQQQQQQQQ H
H5F + ) ( ' - ) ( ' 0 @ ' (' - ' ' QQQQQQQQQQQQQQQQQQQQQQQQQ HD
H5H 0 %&' ' @- ' H ) ' , ' F 'B'0 ) 7 -' 9"P;QQQQQQQQQQQQQQQ HD
REFERÊ CIAS BIBLIOGRÁFICAS_________________________________ HH
A EXO I: RELAÇÃO DAS ESTRUTURAS EMPREGADAS___________ HE
A EXO II: ESPECTRO DE ALGU S COMPOSTOS PREPARADOS
ESTE TRABALHO____________________________________ O"
(0 -) '( 6 1 , 4'QQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQ O
N
RELAÇÃO DAS FIGURAS
@85
Figura 1: () *)* ' @- ' H , ' F 'B'0 ) 7 -'5 QQQQQQQQQQQQQQQQQQQ D
Figura 2: () *)* ,' -* 0 ')'0' 6 N5QQQQQQQQQQQQQQQQQQQQQQQQ D
Figura 3: '((+1 ( 8 *0'( (* () )* ) ( ' 0 7)' ' 8 *0' - 'B '
> - ) %&' ' 8 *0' , '5QQQQQQQQQQQQQQQQQQQQQQQQQQQQ G
Figura 4: ' *)' *) ' ' )' ) , ) ' ) ' ' 6 0'((
1 (+ ) ( '(10)5QQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQ"O
Figura 5: - (,' B) ) 1' ) L( 0 - )@ ( ) (6
J - 6 ( +:* ' +:* '5QQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQ O
Figura 6: ( '%' ' 0 4' 4 '8 %&' - ) +) - *) 3 '
@8* 5QQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQ DO
Figura 7: ( '%' ' () , 4 '8 %&' - ) +) - *) 3 '
1 ' # 5QQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQ DE
Figura 8: ( '%' ' 0 4' 4 '8 %&' - ) +) - *) 3 '
N
RELAÇÃO DAS EQUAÇÕES QUÍMICAS
@85
Equação 1: (+ ) ( ' @- ' F , )7B F 'B' *) 7 -'QQQQQQQQQQQQQQQQQQQQQQQQ O
Equação 2: (+ ) ( ' @- ' H , ' F 'B'0 ) 7 -' 4 '- ' '(5)QQQQQQQQQQ O
Equação 3: (+ ) ( ' H , ' F 'B'0 ) ' )' ) - *) (6)QQQQQQQQQQQQQQ P
Equação 4: + ) ( ' F - ' F 'B' *) ' )' , ) (4)__________________ E
Equação 5: (+ ) ( ' H 9 ) ' , '; F 'B'0 ) ' )' , ) (10)QQQQQQQQQ E
Equação 6: (+ ) ( ' @- ' H , ' F 'B'0 ) 7 -' 4 '- ' '(5)QQQQQQQQQ E
Equação 7: (+ ) ( ' ' (*--+ -'QQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQQ "
Equação 8: s+ ) ( ' @- ' F , )7B F 'B' *) 7 -'QQQQQQQQQQQQQQQQQQQQQQ "
Equação 9: (+ ) ( ' F - ' ' F 'B' *) ' )' , ) (3)QQQQQQQQQQQQQQQQQQ "
Equação 10: %&' 6' , %&' ' - )' -' QQQQQQQQQQQQQQQQQQQQQQQ "D
Equação 11:(+ ) ( ' F - ' F 'B' *) ' )' , ) 9F;QQQQQQQQQQQQQQQQ "D
Equação 12: (+ ) ( ' H 9 ) ' , '; F 'B'0 ) ' )' , ) (10)QQQQQQ "F
Equação 13: %&' 6' , %&' ' 0 - 0 ) ' - )' 0 ) QQQQQQQQQQQQQ !
Equação 14: s+ ) ( ' @- ' F , )7B F 'B' *) 7 -'QQQQQQQQQQQQQQQQQQQQQ FP
N #
Equação 16: (+ ) ( ' F - ' F 'B' *) ' )' , ) (4)QQQQQQQQQQQQQQQQ FP
N#
RELAÇÃO DOS ESQUEMAS
Esquema 1:*, '( 0 , '( 0 '- (('( 0 (+ ) ( ' > QQQQQQQQQQQQQQQQQ H
Esquema 2: (+ ) ( ' F - ' F 'B' *) ' )' , ) (4)QQQQQQQQQQQQQQQQQQQ O
Esquema 3: ') ( )=) - ' > 1' 1 ' 8 ) ( , '( )7B -'(QQQQQQQQQ P
Esquema 4: 0 0 %&' 0' . > '( ( ( (15 a) (15 b)QQQQQQQQQQQQQQQQQ P
Esquema 5: 0 0 %&' ' @- ' H ) ' , ' F 'B'0 ) 7 -'(17)QQQQQQQQQ E
Esquema 6: 0 0 %&' 0' . > '( ( ( (15 a) (15 b)QQQQQQQQQQQQQQQQQ DH
Esquema 7: 0 0 %&' ' @- ' H ) ' , ' F 'B'0 )
N#
SÍMBOLOS E ABREVEAÇÕES
ALA –R- ' H , ' F'B'0 ) 7 -'5
Å – * 8() ', 9"!O-,;5
AcO – @- ' ) 7 -'5
Ac2O ' -=) -'5
BTS –
cat - ) ( '
CDCl3 - ' '67 , ' *) '
cm1 1 ( ' - )+, ) '/ * U, ' ' 'IV5
13
C RM – (0 -) ', ) ((' - , 8 =) - *- - ' ' "D5
CTF – - )@ ( ) (6 J - 6 (
CTF SL – - )@ ( ) (6 J - 6 ( (7 ' +:* '
Ed. )'
ed. %&'
) ( 6 - / 'IV5
) ( ,* )' 6 - / 'IV5
) ( 6' ) / 'IV5
N#
g 8 , / * , (( 5
h – 4' / * ) ,0'5
1
H RM – (0 -) ', ) ((' - , 8 =) - *- 0 7)' (5
Hz – A )3/ 6 :VJ - / , - - '( 0' ( 8* '5
IV – (0 -) '(-'0 8 &' ' 6 1 , 4'5
KBr – ', )' 0')@(( '5
L – ) '/ * 1' *, 5
LDL 0'0 ') + ( B ( 5
m – ,* ) 0 )'/ 5
) ( ,= / 'IV5
mg – , 8 , / * , (( 5 MHz – , 8 4 )35
mL – , ) '(/ * 1' *, 5
mmHg – , +, ) '( , -U '5
mTorr – , =( , 0 ) *, )' 5
ν ν ν
N#
pf 0' )' 6*(&'5
pe 0' )' * %&'5
pH 0') - 4 '8 S -'5
PP IX 0 ')'0' 6 N
Pd/C - ) ( ' 0 @ ' (' - ' '5
R – 8 *0' (* () )* ) 8 = -'5
RM – (0 -) ', ) ((' - , 8 =) - 5
s – ( 8 )'/ RM 5
t – ) 0 )'/ RM 5
TFD –) 0 6')' ,
Capítulo 1
I TRODUÇÃO E OBJETIVOS
1.1 Introdução
! "
#
$
%" "&" ' ( ) *
" )
+ ) , "
"
-- - ) "
,
1.1.1 Terapia fotodinâmica (TFD)
- % . / 0 - "
, - "
1
' - "
$ $ - ' ()+)* 2
-3 45+ "
-
-' ( * - "
" %" $
( ) *
45+
45+ ) - $ 6 "
- "
7 8 9 $ )
- : "
$ , # ; -3
- ) $
- - "
- # & <
#
' "
, ' 7 ' 45+
= > 3
' "
9 %
"
"
#
1.1.2 Ácido 5 amino 4 oxopentanóico (ALA)
= - %" "&" ' .( ) *
9 "
Figura 1: %" "&" '
"
- " ) "
?@ (<<"?@*
$ 3 <<"?@ - "
"
( ' * 8 ' , ( "
* ( '
* ' .
7 ) - 4 5 (45+*
Figura 2: ?@
&
) - "
$ - 7
9 "
$
+ ) "
/
6
•4 6
02 22 C $
-• 6 -
-( *
.2 C $ , & : "
9
•D 3 6
$ ( * E
) 9
9 9
$
# & 3 ; "
, # :
) - " 9 ,
< - "
-
-3 F - "
+ $
-$ )
%
) 9
(5+ * 7 "
! : $ 0 B G , B
> H ( B>?H * 22 "
B>?H D7 I #/. I
%#% 2 %2/1J2 "1/ 2& 22 "
) - H - ) K LM
%#% %2/& J 22." 2 - I 10 + !
. 2 22. 1
; ) 3
:
$ , :
-, N O
' 8 1
1.1.3 – Metodologias de síntese do ácido 5 amino 4 oxopentanóico (ALA) e deri
vados
$ %" $ 2 "
- :
$ P - 9 " )
Esquema 1: $ )
B
- Q"
$ ) - "
.
, ! R
P %" P "&" ' (5) "
) P %" "&" ' "
- (6) ) 9 $ $ "
: : : "
R 8 $ &" ' "&"
' - (2) $ (1) - "
(1%C* ' (1) 22I; #9 S (2) (1%C*
Equação 1: $ &" ' "&" '
-D (2) - " $
&" "&" ' - (3)
-8 - " &" "&" ' - (4) "
(2)
S H ; '
#%I; %9 /2I; .9
(4) (3)
;A#;B
S ; ;B
..
Esquema 2: $ &" "&" ' - (4)
B F, %" P "&" ' (5) "
(4) < J; %
(4) < J; A; ".= % 09 (5) .. (01C* S A ( *
/
(5) ) -
-(01C* J " "
%" P "&" ' "- (6) "
Q
" AH &
(5) (6) (%0C*
Equação 3: $ %" P "&" ' "- (6)
$
- )
) "
- (6)
> $ -
' "
# B
Esquema 3: ) '
< T # - $
%" "&" ' $
) H "
& (4) - "
3 (9) (8) (7) (3) (1) .. .. .. .. .. .. S A;
A;( *( B*
A < J; ;A#B J "G K
4A5 B ;A# B BA B 4A5 ; ;A# H ;
;A# A
0
(4) (3)
;A#;B
; ;B
; S ;B..
(/2C " 02C* S ; ;
Equação 4: $ &" "&" ' - (4)
B
-'
%"( *"&" ' (10)
%" "&" '
#
(0#C* %
(0#C*
S (;A#; *U
..
&2I; BA
(10) S U ( *S ;A#; A
; B
(4)
..
Equação 5: $ %"( *"&" ' (10)
- F 9 (10) $ "
(5)
#
(1%C* .
Equação 6: $ V %" "&" ' 9 (5)
?
) K L & - $
$ ) +
(11 a i) (R1) - - 9 ,
- ' (R2) - &
#
BA
A; 22I;
A BA# ;
(10) (5)
.. S ;A#; A
1
R1 O R2
H O
O
R1 R2
H H
a
b H C H3
H
c C2H 5
C2H 5
d H
H e
O
i C2H 5
C2H 5 h
g
H
R1 R2
O H O O O f
1 1 a i
Figura 3: $ - 9 , - ' )
- $ )
- .
R - "
9 '
B 9 $ "
- % - 9
$
'
< T # 9 "
$
< $
) 9 $
-- 9
1.2 Objetivos do presente trabalho
H -3 - 9 $ %"
$ ( ) * $ "
2
H $ 9 "
3 '
H - ) $
: 3
8
7 - ' $ )
: - '
) , "
-; 9 $ $
)
$ <
$ ) 3
: -
% < "
Capítulo 2
PREPARAÇÃO DO ÁCIDO 5 AMI O 4 OXOPE TA ÓICO
(ALA)
2.1 Introdução
< %" "&" ' ( ) *
9 R
< T # 7 9 8 : - 9
- -
-- 9 - " $ "
9 $
- )
: - " $ 3 <
R
< T # 9 $"
+ $ )
$ 8 "
$ $ $
-2.2 Síntese do anidrido succínico (1)
$ #2 (1)
A
AS S A
(12) (13) (1) (14)
D '
(01 #C*
Equação 7: $ $
- $ $
$ R F, $ &"
' "&" ' - (2).
2.3 Síntese do Ácido 4 metóxi 4 oxobutanóico (2)
$ " (2) R
$ (1) Q
- - ' (
0* $
Equação 8: $ V &" ' "&" '
-2.4 Síntese do 4 ciano 4 oxobutanoato de metila (4)
< 9 8 $ (4)
&" "&" ' - (3) (H ; *
- (2) 1
(1/ #C*
(2)
22I; #9
(1)
#
(3) #%I; %9
'
S H ;
(2)
S H S A;
Equação 9: $ &" "&" ' - (3)
< F, $ (4) "
- ? (; ;B* $ - 7 "
A R G - %
2
; H &S K;B S B AH #S A ; ;B S #B AH &
Equação 10: - ?
; 1%C ; ;B - $
$ (4) R
D " (3) - (; ;B* ( ;B* /2I; .
9 - (4).
/2I; .9
(4) (3)
;A#;B S ; ;B
..
( / #C*
Equação 11: $ &" "&" ' - (4).
2.5 – Tentativa de obtenção do 5 (etanoilamino) 4 oxopentanoato de metila (10)
< (10) "
< T #
' 9
- $
D " - (4) &2I; 9
&
(%/ 0C*
S (;A#; * U
..
&2I; BA
(10) S U ( *S ;A#; A
;B
(4)
..
Equação 12: $ %"( *"&" ' (10)
- $ "
'
- B 9
$ - "
$ - (10)
7 " "
- - $ $
9 - $
-(10) B $ , - : 9 "
"%2I; 9 '
2.6 – Análise final
a) Síntese do anidrido succínico (1)
$ (1) - ' "
- " > $
IV
b) Síntese do Ácido 4 metóxi 4 oxobutanóico (2)
$ (2) 9 "
IV "
%
c) Síntese do 4 ciano 4 oxobutanoato de metila (4)
B $ (4) "
(H ; * $ - (; ;B*
-$ (3) H ; - "
- 9 , "
' #%I; R $ ; ;B
- 9
:
-- $ $ (4)
- "
;
$ F, - (4)
d) Tentativa de obtenção do 5 (etanoilamino) 4 oxopentanoato de metila (10)
(10) #
$ '
- B 9 "
$ :
- 9 ' "
"
B
-, : $ (10)
-- 9
-- IV
R - (10)
.
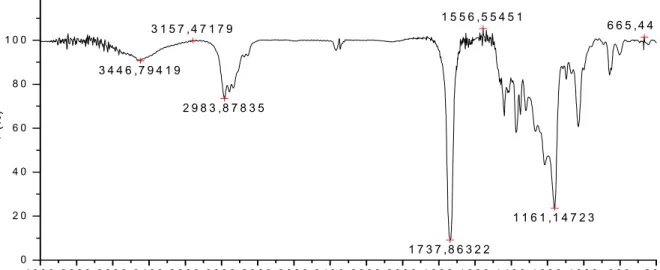
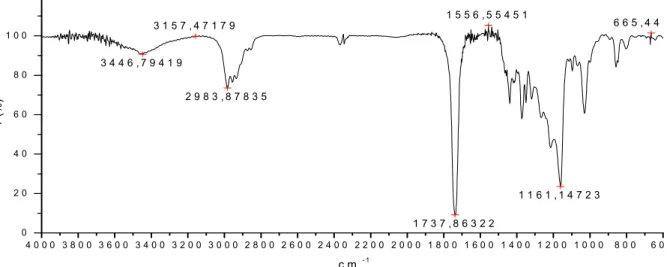
$ - (10) IV 1H RM 13C RM "
- 9 '
&
Figura 4: - - $ (10)
2.7 – Conclusões:
; - " $ (1),
(2) e (4) - 9
-3 :
$ (10) ' - 9
- '
(10) "
9 $ 9 ' "
&2I; 9 8
9
' $
- " "
9 "
-/ Procedimentos e métodos
5 $ "
- W
#2 4 :
' - P
" 9 "
P "
G4H - - "
9 ' (K A* & X
"
$ $ : "
" 9
$ (> Y".2*
' - ' 8 "
: 9 - 9
-Equipamento empregado
9 , - " #
- 9 G L > B;7 +D@ 22 ( 22 =A * G "
L > B;7 +D@ &22 ( &22 =A * ? W $ ! 5
= Y $ 9
( * - " # (δ Z 2*
9 ,
9 - P
H9 ?D< [ ? W $ !
5 !- $ - 3
B ; $ "
9 KG - : ' Q ( "*
- "
0
A
(2)
2 Preparação do ácido 5 Amino 4 oxopentanóico (ALA)
2.1 Síntese do anidrido succínico (1)
" - "
%22 ) ' B
"
-( [ * ; " - 2# % (2 0/ *
$ (12) .. ) (13) " 2I;
9 9 ,"
D " 2I; 9
" - - P
- ) , :
&2 ) $ - P <
- - " - /0 #/
(01 #C* $ (1) \ 1I;J ] ^) #2 1" 2IJ _
12C`
IV ( 9 KG *6ν( "* Z 1/2 # (ν;"A* 0./ # (ν;Z [ I* /0
(ν;Z [ I* & (ν;" ";* 2%0 1 (ν;"
; " "; ";* 1 . (ν;Z $ *
2.2 Síntese do ácido 4 metóxi 4 oxobutanóico (2)
7 - , - % )
&2 2 $ (2 ## * % )
' B
" - (
[ * " - 9
-, 9 " 22" 2I; + ' "
-"
Q 5 - % %& (1/ .C*
1
\2 #1 ] & " ' "&" ' - (2) \ %&"%%I;] ^) %.I;J _
1%C`
IV ( 9 KG *6ν( "* Z #&%2 " %22 (ν" A - '$ * 1%. 0 (ν;"A*
/# (ν;Z * /22 (ν;Z - '$ *
� 0 (ν;" "A* /. % \ν;"(;Z *" ]
2.3 – Síntese 4 cloro 4 oxobutanoato de metila (3)
? 12 )
- 0% ) 7
%1 ) - ,
- % %& (2 #1 * & " ' "&" ' - (2) "
'
a ) %
) B ; JB ; # + ' " - , 9 #%I;
- 9 9 , (A; *
a B ; JB ; # -
-- P
-, - #22 )
- H ;
- - - " $ ; $ -"
$ 9 "
" - &" "&" ' - (3)
2.4 – Síntese do cianeto de cobre (CuC )
$ ; ;B 9 "
F, ) A R
G - . 3 %
5 , : : $ 6
• - "9 # ( % * 022
) A &%I;
2
• 2 ( % * 22 ) A
/2I;
• - .% 2# (2 . * 22 ) A
%%I;
7 , : GF 9
.2I; ) , :
) - .2I; 2
- GF 9
-%22 ) ( * - "
" 2/ 2 (1% .C* 22I; \) / &/&I;J _
/2"1/C] < ; ;B "
2 2 11 2
? # 2 2 ; ;B 2 )
- % ) " % ) - "
- #
; ;B S B # ;B S ; B #
Equação 13:
- ;B $
; ;B $ ; ;B
-2.5 – Síntese do 4 ciano 4 oxobutanoato de metila (4)
7 - , - $ (3) "
- #% 2
(2 #1 * ; ;B - P
-'
-P 5 ; ;B "
- / ) - "
" P - "
/2I; - 9 + ' "
-;B
"
-%2 ) 7
-
-- " - 2 )
- $
-P - $ - 2 2
" 2 "
-$ $
' - " $ ( % 0. *
/ .% $
-8 02I; - $ 7 $
- 8 - & 0/ (2
* \ / #C] &" "&" '
-(4) \) .0C]
Produto (4)
IV ( *6 ν( "* Z 10% 0 (ν;"A* #/ & (ν;≡B* /#/ 0 (ν;Z *
. \ν;"(;Z *" ]
Sólido
IV ( 9 KG *6ν( "* Z ##22 " %22 (ν" A - '$ * 10% 0 (ν;"A*
/#/ 0 (ν;Z * / 2 (ν;Z - '$ *
2.6 – Tentativa de obtenção do 5 (etanoilamino) 4 oxopentanoato de metila (10)
$ (10)
< T # 7
"
<
- , - % ) " "
P ; " - P 2
H - "
-BA
P # 2 (2 2 * $ &" "&" '
-(4) & ) & )
&2I; 9 - P + ' " "
- - - P "
- 9 "
%2 2 $ Y".2 $
%2 ) "
:
9 $
3 : - % )
- $ B
-$ 2 ) ' "
(%I;* 9 ' "
- " $ % #
$ (10) D "
- ,
-%22 )
Q ; " &/ &0
H - " 0/ (2 20& *
$ &" "&" ' - (4) 0 %
" % 9 - P &2I; + ' " "
- - -
-P # : #2 ) "
&2I;
- $
-' (%I;* 9
- 5 $
#2 2 $ .2 $
6# 9 " : %2 )
%C
/%C ' : % 9 "
: . 9
; " : % : . $
#
- $
: . - - "
- 9 :
1% 2 1%
-( % # * "
$ 9 , "
= " , : $ " % ) 7
- 9 $ 8 "%2I; 3 N
O ; 9 " 2I;
9 9 ' "
- 9 $ 8 "%2I; "
- 7 " 9 8 "#2I;
$
-- - P <
' - $
-- - - , :
$ - 5 "
= $
-IV
Fração 1
IV ( *6 ν( "* Z 10# 0 (ν;"A* #.. . (ν;≡B* /#/ 0 (ν;Z *
. \ν;"(;Z *" ]
Fração 2
IV ( *6ν( "* Z 10# 0 (ν;"A* /#/ 0 (ν;Z * . \ν;"(;Z *" ]
Fração 3
IV ( *6ν( "* Z 10# 0 (ν;"A* /#/ 0 (ν;Z * . \ν;"(;Z *" ]
IV - , : - "
- 3 $
&
( 10I;* $ (10).
() # % "%#I;J _ 0#C*
-IV ( 9 KG *6ν( "* Z 10# 0 (ν;"A* / & # (ν;Z * 2 \ν;"
(;Z *" ]
1
H RM (&22 =A ;+;#*6δ ( * Z #1 [ /% ( #A* . / ( &A* # .0%
( #A* & ##"& % ( A*
13
C RM (&22 =A ;+;#*6 δ ( * Z # /&% ( ;* 0 &./" 0 //2 ( ;*
% #22 ( ;* .2 2& ( ;* / 021"
/ ##1 ( ;*
-( ' - * , : /2 )
- " 2 2 - 7 ' "
#2 " "
- - " 1 # 7
- IV - '
IV ( 9 KG *6 ν( "* Z #& / % (νB"A * #.. . (ν;≡B* . 2 (ν
%
Capítulo 3
Procedimento experimental elaborado para a preparação do ácido
5 (etanoilamino) 4 oxopentanóico utilizando catálise de transfe
rência de fase
3.1 Introdução
$ %"( *"&" ' (17)
, - 9 Q
(17)
, (;45*
-7
P $ ' $
- + "
- /6
• "
• J
•
•
$ ,
.
' b" "
- F 8 P
P %
D " b S WS@" D " @ S WSb"
B b S WS@" B @ S WSb"
Interface
Fase aquosa Fase orgânica
Figura 5: ' H L , $ " $
, $ " $ (;45"))* "
9 ;45 " $ (;45"H)* " $ (;45"Y)*
;45"H) P "
$ 8 ;45"))
0
6
P "
H L 0 ,
- P
$ 6
-- P (47G 47G "G * 9 9 ' 9
" "- P 9 ' - P (4 G*
, - 9 "
" $ (;45"H)* , "
- P (47G * 7 9 $"
- $
-
-- -3
- -
-- B
/
5 &" "&" ' - - "
P (15 a) &" "&" ' - - P (15 b)
, " $ B F, 9 "
$ #
3.2 – Preparação dos sais 4 ciano 4 oxobutanoato de benziltrietilamônio (15 a) e 4
ciano 4 oxobutanoato de potássio (15 b) por CTF SL
D " $ (1)
2 2 $ c - P (47"
G * - P &
(15 a) (15 b) - ;45"H) WS
- - P
Esquema 4: ;45"H) (15 a) (15 b)
- "
(15 a) (15 b) ; $ 9
F,
3.3 – Preparação do ácido 5 etanoilamino 4 oxopentanóico (17)
B $ (17) " 9 "
< T #
c W - 8 0C
-;A; Fase Orgânica Fase sólida ;B " KS ;B " WS
WS;B" S S K;B S WS;B"
Interface WS;B" S K; WS;" S K;B
(1) (15 a) (15 b)
.. ..
0
; 9 $ ; $"
- 9 - %" "&"
' (17) :
-! " 9
9 , "
- > $
D " (15 a) (15 b)
' &2I; 9 B F, "
$ - - - "
$ %
$ (17)
S U ( *S A
&2I;
(15 a/b) (16) ..
B;
"WSJ KS B.. "WSJ KS
A A; 2C B A A ..
WS;" S K; S
(17)
Esquema 5: %" "&" ' (17)
$ "
- F, "
- " - (17)
IV
- - "
$ - -"
1
9 $
(17)
3.4 – Análise final
a) Preparação dos sais 4 ciano 4 oxobutanoato de benziltrietilamônio (15 a) e 4
ciano 4 oxobutanoato de potássio (15 b) por CTF SL
(15 a) (15 b)
-- 9 Q
-- " ;45"H) (15 a) (15 b)
- Q 3
$ "
< 9 - "
$ ; (15
a) (15 b) $ "
b) Preparação do ácido 5 etanoilamino 4 oxopentanóico (17)
: $ (17)
- $ 9
- H "
-3 3 "
< IV -
-- ' - '$ - - "
(17) B " - -
-( * (15 a) (15 b) 9 "
? "
8 9 9
7 "
#2
R -
-- $ IV B
- - ' - '$
-- - - "
$
3.5 – Conclusões:
; - " (15 a) (15 b)
" ;45"H) 3 "
" $ - Q
$ ? IV
;45 "
9
B - "
$ (17) - "
$ - :
-8 ;45
-# Procedimentos e métodos
' - 9
- : ' 9 8
' ; $ $ - 9 $ 8
5 - $ "
#2 4
9 - : "
< 7'
; $
3.1 Preparação dos sais 4 ciano 4 oxobutanoato de benziltrietilamônio (15 a) e 4
ciano 4 oxobutanoato de potássio (15 b) por CTF SL
B - , - % )
- # (2 2
* %C
- P (47G * 2 / (2 22# *
(&2 * &2I;
-P 7 - P " .2 ) "
- 2 (2 2 * $
8 - 9 7 "
; $ $"
9 (15 a) (15
b)
-3.2 Preparação do ácido 5 etanoilamino 4 oxopentanóico (17)
B - , - $ (15
a) (15 b) - P & )
& ) "
8 - #2
#
$ "
- P 7 - "
, - (- * % )
# 2 (2 2& * U - "
P " % ) "
$ - , - - "
P - 2
P "
12 &2I; - - P
- "
( 22 4 * B
- # ) ( 2C*
$ 2 2 #2 "
- .2 )
- $ .2 $ &2 )
$ 9 - %2 ) "
2 " 2 "
-
-(#2 4 * " - "
2 ) ( *
%I; % 9 5 " -
-- - - P
-- (&2 4 * - " 2
IV ( 9 KG *6ν( " * Z #& % % (νB"A* ##22 " %22 (ν" A - '$ *
1 1 (ν;"A* #/2 % (ν;≡B* / 1 (ν;Z
- '$ * /2. / (ν;Z * .%0 / (ν;Z
* .2/ % (ν;"B * & # 2 (ν;" "A
##
2 ) "
" 2 9 " %I; A
-- - P "
(&2 4 * - " 2 .% ( 0" #2I;J *
IV ( 9 KG *6ν( " * Z #&&. / (νB"A* ##22 " %22 (ν" A - '$ *
1#2 (ν;"A* #. / (ν;≡B* / % % (ν;Z
- '$ * .1 # (ν;Z * ./ (ν;Z
* .2& / (ν;"B * & % # (ν;" "A "
- '$ *
- , - (- *
%2 ) " % $ -
-P (&2 4 * - " ( 0 "
0#I;J *
IV ( 9 KG *6ν( " * Z #&2& # (νB"A* ##22 " %22 (ν" A - '$ *
1#. 1 (ν;"A* #.& / (ν;≡B* / 0 % (ν;Z
- '$ * %.2 & (ν;"B * &22 # (ν;" "A
#&
Capítulo 4
Procedimento experimental elaborado para a preparação do ácido
5 (etanoilamino) 4 oxopentanóico utilizando
catalizador Pd/C
4.1 Introdução
7 - - 9
' , $ # B "
, " $ (;45"H)*
- "
# B :
8
9 $ < T # 3 - "
, 7 9
- - (< J;* - H "
, 9 9 "
$ - - 9
9 9 $
' -
-9 - $ P - - 9
- 9
9 9 - 9
#%
Y #2 3
9 9 $
- 9
9 $ - -3 - - (17)
' 9
4.2 – Preparação dos sais 4 ciano 4 oxobutanoato de benziltrietilamônio (15 a) e 4
ciano 4 oxobutanoato de potássio (15 b) por CTF SL
(15 a) e (15 b) 9
; $ # : "
D " $ (1)
2 2# $ - P (47"
G * - P .
(15 a) (15 b) - ;45"H) WS
- - P
Esquema 6: ;45"H) (15 a) (15 b)
+ ' " - ( *
(15 a) (15 b)
- < J; 9 "
; - 9 "
9 F, 8 ;A; Fase Orgânica Fase sólida ;B " KS ;B " WS
WS;B" S S K;B S WS;B"
Interface WS;B" S K; WS;" S K;B
(1) (15 a) (15 b)
.. ..
#.
4.3 – Preparação do ácido 5 etanoilamino 4 oxopentanóico (17)
< $ (17)
9 9 $ :
- :
4.3.1 Construção do aparelho de hidrogenação catalítica
; : $ ) "
9 $ 9 "
- % 9 8
? - 9 Y "
1
9 , 022
) - "
9 ,
-. 9 9 9 2 2#
9
- " 9 - - 9 "
9 , Q
-9 ' ? $
E
B
F C A
H2(g)
Reservatório contendo
H2O
Balão Reacional Ar(g)
H2SO4 (conc)
D
G
Reservatório de H2(g)
...
Tubo secador contendo
KOH(s)
#/
9 9 $ 9
Q 9 '
9 "
, 9 "
-- "
9 $ 9 9 "
9 9 A ; $
/ 9 9
- 9 # #%
1 % B - - 9
- $ - 9
( * "
- 5 9
-9 , - - '
B
( * 9 , - F ' "
"
9 , - 9 "
, , "
"
$ 9
-(<>;* 3 % "
- B
- - ' - "
- ?
9 ,
A
' 9 ( * - - <>;
#0
H 9
/ - 4
-A ; $ <>;
Tubo de Hidrogenação Catalítica (parte externa)
Tubo de Hidrogenação Catalítica (parte interna)
H2(g)
Ar(g)
Frasco Reator Reservatório
de H2(g) Pistão Pressurizador
Pesos de Chumbo
Figura 7: - H 9 $ <>;
B 9 9 9 $ "
$ - 9 : ;
8
-- $ ? 9 "
9 $
9 $
9 (;A#;B*
-- < J;* 9 8
9 0
#1
9 9
- (17) < J;
E Tubo secador contendo KOH(s) B F
D C A
H2(g) Reservatório contendo óleo mineral Balão Reacional Ar(g) Reservatório de H2(g)
Figura 8: - 9 9 $
4.3.2 – Preparação do ácido 5 etanoilamino 4 oxopentanóico (17)
; 9 9 $ "
(17) $ < J; ;
$ - 9 < J;
'
-$ - "
1
< J;
- - ;45"H)
- < J; - P
-9 9 $ - "
%I; - 9 / 9
-(18)
-$ 2C 4 "
&2
Esquema 7: %" "&" ' (17) < J;
$ - "
" - "
$ (17) IV RM
- " 9 $ 9
9 $ "
- 9 , ' < "
- - 9 "
%I; '
-- 9 ,
4.4 – Análise final
a) Preparação dos sais 4 ciano 4 oxobutanoato de benziltrietilamônio (15 a) e 4
ciano 4 oxobutanoato de potássio (15 b) por CTF SL
; (15 a) (15 b) 3 9 ; "
$ # ' , 9
? 3 9 ;45"H)
- - 9 "
B $ (15 a) (15 b) 9
"
(17) (16)
WS;"S K; S B.. A
A
A; ( 2C*
B "WSJ KS
A
..
B;
"
WSJ KS
..
(15 a/b) (18)
%I; < J; J ;A;
S A ( * AB
"
&
' 9
9 - " (15 a) (15 b) 9
9
-b) Preparação do ácido 5 etanoilamino 4 oxopentanóico (17)
; $ $
-IV RM $ - "
(17) - - "
$ (17) IV
- '$
- 9 "
$
- 13C
RM e 1H RM - ! 5 = Y (!5=Y*
- 3 !
' : - "
$
"
13
C RM e 1H RM 3 "
9 "
$
< - ,
- ; ;45"H)
$ 9
9
4.5 – Conclusões:
7 9 ;45"H) -
& :
-- '
(17) IV RM
9 9
-9 < J;
&# Procedimentos e métodos
' - 9
- : ' 9 8
' ; $ $ - 9 $ 8
5 - $ "
#2 4 Q
8
9 - : "
< 7'
; $ A +
4.1 Preparação dos sais 4 ciano 4 oxobutanoato de benziltrietilamônio (15 a) e 4
ciano 4 oxobutanoato de potássio (15 b) por CTF SL
B - , - % )
- &
(2 2# * # C
- P (47G * 2 % (2 2221 * "
(&2 4 * &2I; - "
P 7 - P " %2 ) "
- # # (2 2# * $
8 - 9
-- P
; $ $ 9
(15 a) (15 b)
-4.2 Síntese do catalisador de paládio sobre carbono
? $ "
; " 2 (2 2 * # 2 (# %0 *
$ - %2 ) &2
&&
) " '
- " " 9 < ;
20 /% ) (&#% _ &% * 7
22 ) 8 9 2 %
-- - (&2 4 * &2I; "
P " % ) -
-- " / )
< ; $ 9
-- - P
-( *
-(d %2 )* " A A e / 2
(&2 4 * &2I; - " 2 % % "
< J;
4.3 Preparação do ácido 5 etanoilamino 4 oxopentanóico (17)
B - 22
) < J;
-P 8 (15
a) (15 b) - ;45"H)
- : 2 ) H
-- 9 - 9 %I;
" 9 9 9 $ ( /*
/ 9 - - P"
- % ) "
& 20 (2 2& *
9 (#2 4 * - - "
" & ) ( 2C* $ "
2 2 - #2 4 "
-$ % ) " #2 ) $
- "
- 22 ) (d 2 *
$ (#2 4 * - "
- 2 %2 ( /0" 02I;J * R
B A
A
&%
(#2 4 * - " # 1& ( /%" 02I;J *
- & && " /. 1C
Sólido da fase orgânica
IV ( 9 KG *6ν( " * Z ##22 " %22 (ν" A - '$ * 1# 0 (ν;"A*
/2 (ν;Z - '$ * & 0 . (ν;" "A
- '$ *
1
H RM (&22 =A ;+;#*6δ( * Z %2/" .&2 ( #A* & /21 ( A*
13C RM (&22 =A ;+;
#*6 δ ( * Z # 1. ( ;* 0 & &" 1 2 ( &;*
. 0.# ( ;* /% .2 ( ;* /. 1# (
;*
Sólido da fase aquosa
IV ( 9 KG *6 ν( "* Z ##22 " %22 (ν" A - '$ * 1# 0 (ν;"A*
/# % (ν;Z * / % 1 (ν;Z - '$ "
* .1/ # (ν;Z * & / . (ν;" "A "
- '$ *
1
H RM (&22 =A ;+;#*6δ( * Z %/0 ( A* & /21 ( A*
13
C RM (&22 =A ;+;#*6 δ( * Z 0 1. ( ;* 0 & 0" 0 1 . ( #;* &. ..%
&.
Capítulo 5
Preparação do ácido 5 (etanoilamino) 4 oxopentanóico (17) uti
lizando procedimento da literatura
21e o aparelho de hidrogenação
catalítica
5.1 Introdução
7
-(17) - H
" R "
- - 9 "
< J; 9 9 $
"
- 9
< J; 9 9 $ $ 7
- 9 - "
&/
S ; ; 5.2 Síntese do ácido 4 metóxi 4 oxobutanóico (2)
" (2) R
$ D "
- ' - (2) - & $
(2) 22I; #9 (1) ' S (1%C*
Equação 14: $ &" ' "&" '
-5.3 Síntese do 4 ciano 4 oxobutanoato de metila (4)
$ (4) (3)
- &" "&" ' - (3)
(H ; * - (2) %
(2)
S H ; ' S H ( *S A;( *
#%I; %9
(3)
Equação 15: $ &" "&" ' - (3)
; - 3 9 " (3)
; ;B /2I; . 9 .
/2I; .9
(4) (3)
;A#;B S ; ;B
..
&0
- - P " "
" - "
$ (4)
$ $
5.4 Preparação do ácido 5 etanoilamino 4 oxopentanóico (17)
(4)
-- P
-< J; - 9 9 - "
- - P "
- 9 9
- " $ "
" "
0 $ (17)
Esquema 8: $ %" "&" ' (17)
f - (%I;* -"
" -
-P IV
RM
AB
S A ( *
< J; J ;A; %I;
(4) (18) ..
..
B
A
A; ( 2C*
B A
A
..
(17) (16)
B;
S
&1 5.5 – Análise final
a) Síntese do Ácido 4 metóxi 4 oxobutanóico (2)
$ (2) 9
3
; $ ' ,
IV $ 3
b) Síntese do 4 ciano 4 oxobutanoato de metila (4)
- $ $ (4) "
$ "
7 $
-; $ ; $
$ 9
-c) Preparação do ácido 5 etanoilamino 4 oxopentanóico (17)
D - $
- (17) - IV
RM B IV - "
-- '$ (17)
13
C RM e 1H RM - 9 , "
9 , ,
; $ " (17) 9
3
-5.6 – Conclusões:
; - " "
' Q
%2
7 "
< J; 9 9 $
(17)
-$ ? - ,
9 9 9 "
$ $ 3 , < J;
< - "
- %" "&" '
% Procedimentos e métodos
' - 9
- : ' 9 8
' ; $ $ - 9 $ 8
5 - $ "
(#2 4 * &2I;
9 - : "
< 7'
; $ A +
5.1 Síntese do Ácido 4 metóxi 4 oxobutanóico (2)
7 - , - % ) &2 2
$ (2 ## * %2 )
-' B "
-( * " - "
, 9 " 22" 2I; + ' "
-Q 5 - %2 #% (1% #C*
\2 #0 ] & " ' "&" ' - (2) \ %&I;] ^) %.I;J _
1%C`
IV ( 9 KG *6 ν( "* Z 1%. 0 (ν;"A* / 0 (ν;Z * /2 / (ν;Z
- '$ * &#% 1 (ν;" "A* /. % \ν;"
% 5.2 – Síntese 4 cloro 4 oxobutanoato de metila (3)
? 02 )
- /% ) 7
% ) - ,
- % 2 (2 2# * & " ' "&" ' - (2) "
'
a ) %
) B ; JB ; #
+ ' " - 9 #%I; "
- 9 9 , (A; * a
B ; JB ; #
- - "
- P - , - #22 ) "
- H ;
- " $ "
$
; $ - $ 9
" - &" "&" ' - (3)
5.3 – Síntese do 4 ciano 4 oxobutanoato de metila (4)
B - , - $ (3)
- # (2 2#
* ; ;B - P - "
' - "
5 / )
3 ; ;B
" P - "
/2I; - % 9 + ' "
-" (#22 4 * 12I;
- %2 ) " 2 "
$ - - P
- ; $ $ "
(3)
;B
%#
9 " "
(4).
5.4 Síntese do catalisador de paládio sob carbono
; < ; $ 3 9
< 7' ; $ & " - "
22 ) 8 9 "
2 % - (&2 "
4 * &2I; P " % )
-- - "
/ ) < ; $ 9 "
- - - P
- ( * - "
(d %2 )* "
A A e / 2 (&2 4 * &2I; - "
" 2 % % < J;
5.5 Preparação do ácido 5 etanoilamino 4 oxopentanóico (17)
B - 22
) < J;
-P $ &"
"&" ' - (4) - "
- : 2 ) H -
-9 - 9 %I; " 9 "
9 9 $ ( /* .
- - P
% ) " & 20 (2 2& *
- 9 "
(&% 4 * - - " &2 )
" - " % "
"
B A
A
%&
- $
% 2 " "
- " $ $
" 2 ) ' %I; "
- " "
- P - (%2 "
* - " 2 ( 2C* \ %" .I;]
IV ( 9 KG *6ν( " * Z #&&2 / (νB"A* ##22 " %22 (ν" A - '$ *
1%. 0 (ν;"A* /# 2 (ν;Z - '$ *
/2 % (ν;Z * .00 / (ν;Z *
.2/ % (ν;"B * &&# 2 (ν;" "A - '$ "
*
1
H RM (&22 =A ;+;#*6δ( * Z .. [ ./. ( %A* # .## [ # /&0 ( &A*
0 /0& ( A*
13
C RM (&22 =A ;+;#*6 δ ( * Z 0 .2 [ 0 0/ ( ;* % 1%1 ( ;*
%%
REFERÊ CIAS BIBLIOGRÁFICAS
+ ; < ; < 7 R G 9 ) G g = !9 9 R = < 9
+ D H < 7 G + 7 g g 5 4 a g H < a D H 5
! " 86 #/#"#02 ( 10#*
D H 5 + D H ) G g g 5 4 a g 7 = R D = 9 < 7
G g H < a < ; < G 9 7 R ! 67 %%" .& ( 11 *
# B b 9 9 B 4 = L b K a 9 b = L 4 A 9
# 50 .%"/. ( 22&*
& K L R A T G = R $64 11&" 222 ( 11.*
% 7 H Ba < A Aa 28, /# ( 22&*
. 7 5 Y + L D ) Y a D A < ! $48 1#1 ( 22#*
/ ? R = + 4 R + 9 " " $5(2), 2% ( 22 *
0 = ; H > < R $ 8(3), /# ( 22.*
1 b B K D Y a 7 $66, 2. ( 22 *
2 H = 9 H ! H 9 "7 9 % & ' $ 44, %& ( 22#*
4 K _ b 9 < H ) T B R 4 9 a 9 a
a "$150 2. " 2.1 ( 22&*
+ D 5 H _ 4 ; _ ) D 5 > _ < = G D _ ) B _ = 9
R = _ D R ; Y _ G a = > ) G ? L %"
9 a 9 a !
%.
# U ) L ? 7 R = R = B W < ( " %)$
* " + " " * , #
- .. ! . $ 169 ##"#1 ( 22 *
& D 5 + a_ < R < = = ) = + g %
" . " %)
" "$3 12" 2 ( 22.*
% H ) = _ = a g D <9 a 9 a a
(* & ( $7 (2) # 0"## ( 22 *
. 9 6JJTTT a - J 'h J< .&1 9 - 221
/ 9 6JJTTT J J- J J h 9 "
- 221
0 / 0 + $
9 6JJTTT J J J J '
221
1 9 6JJTTT - - J 3 " J 0&/J " " "% "
" " ( 6 #J J 221*
2 + < 4 9 a ; & ! 24 %%."%%/ ( 1%0*
= H K K + = K R H R A R # 28 " # ( 22%*
) ) A "5 R b "Y g < ) ! % 2/#2 & 7 Bi # ( 22%*
# < H ? K K = 9 . ! # <
T . 25 B 0 1//" 102 ( 10&*
& R K L G = R > A T $64 11&" 222 ( 11.*
% D > a 5 H 9 R G Y g > g D B ) R "
%/
. A R G - ! 1 /1 ( 1&#*
/ 7 + 9 T > _ + 9 T H H _ ! " >A; < - 9 B T
b L # ( 11#*
0 ; H L = _ ) ; ) _ A = _ ! " ;9 j
A B T b L ( 11&*
1 ) Y _ . " & ! "$ ) #/."#/0
( 1&#*
#2 > ?_ 2 & 3 4 $% = R H < ( 1/ *
%0
Anexo I
RELAÇÃO DE ESTRUTURAS
%1 (1)
A
(14) (2)
(3)
(4)
..
(5)
B
;A# B ..
(7)
B
;A# ..
(8)
A B
;A#
(9)
(10)
BA.. (6)
D B D
A
(11 a i)
A
A
.2 ;B
"WS
(15 a)
;B "KS
(15 b)
B A
A ..
(17) B;
"
WSJ KS
(15 a/b)
B "WSJ KS
A
.
Anexo II
ESPECTROS DE ALGU S
COMPOSTOS
.
.#
Espectros de Infravermelho
.&
Figura A.1: IV $ (1)
.%
Figura A.3: IV &" "&" ' - (4)
..
Figura A.5: IV - fração 1 - %"
( *"&" ' (10)
./
Figura A.7: IV - fração 3 - (10)
Figura A.8: IV - $ #2I;
.0
-.1
Espectros de Infravermelho
/2
Figura B.1: IV - 2
-(17)
Figura B.2: IV - 2 .%
-(17)
! " "#
/ Figura B.3: IV
-- (17)
/
Espectros de Infravermelho
/# Figura C.1: IV
-- (17)
Figura C.2: IV
-- (17)
! " "#
/&
Espectros de Infravermelho
/%
Figura D.1: IV &" ' "&" ' - (2)
Figura D.2: IV - - "
/.
//
Espectros de RM
/0
Figura E.1: H RM &22 =A $ #2I; -"
(10) ;+;#
Figura E.2: #C RM &22 =A $ #2I; -"
/1
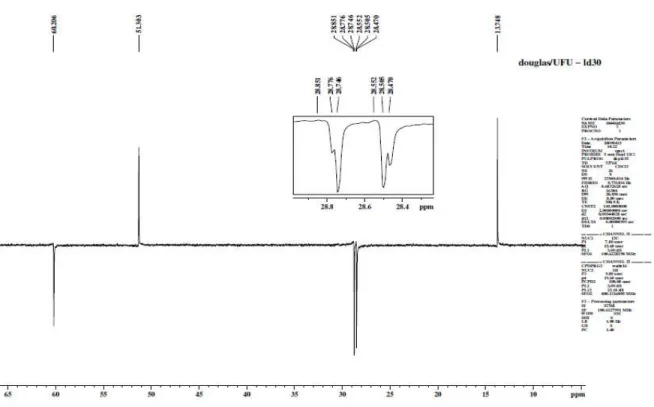
Figura E.3: #C RM +7<4 &22 =A $ #2I; "
02
Espectros de RM
0
Figura F.1: H RM &22 =A
-- (17) ;+;#
Figura F.2: #C RM &22 =A
-- (17) ;+;#
0
Figura F.3: H RM &22 =A
-- (17) +
Figura F.2: #C RM &22 =A
0#
Espectros de RM
0& Figura G.1: H RM &22 =A
-- (17) ;+;#
Figura G.2: #C RM &22 =A