AUTOR: Alysson Antônio Borges
ORIENTADOR: Prof. Dr. José Aurélio Medeiros da Luz
A minha mãe pela de dedicação e exemplo;
Aos familiares pela força:
A Dagmar pelo amor;
Aos amigos pela motivação;
Aos amigos do mestrado pelo companheirismo;
Ao grande professor José Aurélio Medeiros da Luz pelo incentivo, pela confiança, pela
orientação;
Aos professores do programa de pós Graduação em Engenharia Mineral da UFOP pelos
ensinamentos
A todos os funcionários do laboratório de Tratamento de Minérios do departamento
Engenharia de Minas da UFOP pelo apoio;
Ao Departamento de Engenharia de Minas e ao Programa de Pós Graduação em
Engenharia Mineral da UFOP pela oportunidade;
Ao Departamento de Engenharia Geológica da UFOP pelas análises realizadas no
À Fertilizantes Fosfatados S.A. pelo tema de trabalho;
%
& &
" '( "
) ' ' )
)*& +,-!. ! /0! 123 1,/ 1 )
)*&*& /4 5 /6 )
)*&*" 61-/7123 ! 23 )
)*&*) ! - 8/1 9
)*&*: '!+!;/6/1+!0 <
)*" 4 61 16 ! =4 /614 ! 1,-/612>!4 1 +180! / 1 &&
)*"*& 4 +/0! 1/4 , 1 !4 !-!+!0 ! &&
)*"*" 44=?!/4 1,-/612>!4 1 +180! / 1 &" )*"*"*& ! 23 +/0@ / ! ;! !+ 1- ; 0 &" :
:*& 1,14 1 61 16 ! /7123 !60 -58/61 "#
:*&*& 0A-/4! 10 - +@ /61 "#
:*&*" /; 123 ! 1/ 4 B "&
:*&*) /6 46 ,/1 /61 ""
:*&*: /6 46 ,/1 -! C0/61 ! 1 ! 1 ")
:*&*9 4,!6 46 ,/1 D44 1 ! "9
:*" 4 4 ! 06!0 123 "<
:*"*& !,1 123 180@ /61 "<
9*&*) /; 1 +! /1 ! 1/ 4 B ):
9*&*: 4,!6 46 ,/1 D44 1 ! ):
9*&*9 /6 46 ,/1 /61 )9
9*&*$ /6 46 ,/1 -! C0/61 ! 1 ! 1 :&
9*" 4 4 ! 06!0 123 9G
9*"*& 041/ 4 ! !,1 123 180@ /61 9G
9*"*" 041/ 4 ! - 123 9<
9*"*) 041/ ! /./?/123 6/ 1 $)
$ E $$
G E ' $<
< ' ' G&
/4 1 ! /8
14
/8 1 )*&I 1,1 ! - 61-/7123 +,-!. ! /0! 123 1,/ 1 :
/8 1 )*"I !, 4/23 6 06!0 1 +180@ /6 01 16/1 ! !J!/ 4 &&
/8 1 :*&I 4 23 !44 010 !I 14! ! !;!/ D44 1 ! "$
/8 1 :*"I 4K !+1 ! ; 06/ 01+!0 ! + !4,!6 C+! D44 1 ! * "$
/8 1 9*&I /4 / /23 8 10 - +@ /61 F )"
/8 1 9*"I 4,!6 D44 1 ! F )9
/8 1 9*:I 3 =,/6 +1 ! /1- !+ !4 )$
/8 1 9*9I !8/3 6!0 1- 1 ,1 =6 -1 1, !4!0 1 1 01 /8 1 9*: )G
/8 1 9*$I 3 +1 ! /1- !+ !4 , 1 /61+!0 ! +1 / /71 )<
/8 1 9*GI +/6 8 1;/1 1, !4!0 10 +180! / 1L 1 M!+1 / 1 ! 1 /-+!0/ 1* )H
/8 1 9*HI +/6 8 1;/1 1, !4!0 10 /-+!0/ 1 ! +180! / 1 :#
/8 1 9*&#I -@ 0 +/6 8 1;/1 ! ,1 =6 -1 =,/61 4/4 !+1 !+ !4 :" /8 1 9*&&I 4,!6 ! 1/ 4 B 8! 1- 1 ,1 =6 -1 1, !4!0 1 1 01 /8 1 9*&# :) /8 1 9*&"I 4,!6 ! 1/ 4 B 1 !8/3 6!0 1- 1 ,1 =6 -1 1, !4!0 1 1 01
/8 1 9*&# ::
/8 1 9*&9I 4,!6 ! 1/ 4 B 1 1 ) 1 ,1 =6 -1 1, !4!0 1 1 01 /8 1 9*&# :G
/8 1 9*&$I 4,!6 ! 1/ 4 B 1 1 : 1 ,1 =6 -1 1, !4!0 1 1 01 /8 1 9*&# :<
/8 1 9*&GI -@ 0 +/6 8 1;/1 ! ,1 =6 -1 4/4 !+1 !+ !4 :H
/8 1 9*&<I +,-/123 1 N !8/3 6!0 1-O 1 /8 1 9*&G 9#
/8 1 9*&HI 4,!6 ! 1 ;14! !46 1 1 ,1 =6 -1 1, !4!0 1 1 01 /8 1 9*&< 9&
/8 1 9*"#I 4,!6 ! 1/ 4 B 1 ;14! 6-1 1 1 ,1 =6 -1 1, !4!0 1 1 01 /8 1
9*&< 9"
/8 1 9*"&I +,-/123 1 1 4 ,! / / !/ 1 1 ,1 =6 -1 1, !4!0 1 1 01
/8 1 9*&G 9)
/8 1 9*""I 4,!6 ! 1/ 4 B 1 1 4 ,! / / !/ 1 1 ,1 =6 -1 1, !4!0 1 1
01 /8 1 9*&G 9:
/8 1 9*")I -@ 0 +/6 8 1;/1 6 + !4 1K ! A , !4!021 ! /-+!0/ 1 99
/8 1 9*":I 4,!6 1 1 / !/ 1 /0;! / 1 ,1 =6 -1 1, !4!0 1 1 01 /8 1
9*") 9$
/8 1 9*"9I /4 / /23 8 10 - +@ /61 , +180@ /6 9<
/8 1 9*"$* /4 / /2>!4 8 10 - +@ /614 ,54 + 18!+ 9H
/8 1 9*"GI !6 ,! 12>!4 +A44/614 ! +! 1-P 8/614 4 !041/ 4 6 + $&
/8 1 9*"<I 0A-/4! " 90 $"
/8 1 9*"HI !6 ,! 12>!4 +A44/614 ! +! 1-P 8/614 4 !041/ 4 6 + F $"
/4 1 ! 1 !-14
1 !-1 )*&* Q +, 4/23 +/0@ / ; 4;A /6 ! 1,/ 1 <
1 !-1 )*"I 4,!6/;/612>!4 ! +/0@ / 4 ! ;! ,1 1 4/ ! 8/1 &"
1 !-1 )*)I 04 + 61- =;/6 01 ,!- /7123 &$
1 !-1 :*&* 0 /2>!4 4 !041/ 4 ! ;- 123 )#
1 !-1 9*&I 0A-/4! 8 10 - K =+/61 F ))
1 !-1 9*"I 5 /8 14 -R+/014* )9
1 !-1 9*)I ! ? - +@ /6 !4 /+1 :&
1 !-1 9*:I 0A-/4! K =+/61 8! 1- 1 ,1 =6 -1 1, !4!0 1 1 01 /8 1 9*&# :"
1 !-1 9*9I 0A-/4! K =+/61 1 !8/3 6!0 1- 1 ,1 =6 -1 1, !4!0 1 1 01 /8 1 9*&# ::
1 !-1 9*$I 0A-/4! K =+/61 1 1 & 1 ,1 =6 -1 1, !4!0 1 1 01 /8 1 9*&# :9
1 !-1 9*GI 0A-/4! K =+/61 1 1 " 1 ,1 =6 -1 1, !4!0 1 1 01 /8 1 9*&# :$
1 !-1 9*<I 0A-/4! K =+/61 1 1 ) 1 ,1 =6 -1 1, !4!0 1 1 01 /8 1 9*&# :G
1 !-1 9*HI 0A-/4! K =+/61 1 1 : 1 ,1 =6 -1 1, !4!0 1 1 01 /8 1 9*&# :<
1 !-1 9*&#I 0A-/4! K =+/61 1 ;14! !46 1 1 ,1 =6 -1 1, !4!0 1 1 01 /8 1 9*&< 9&
1 !-1 9*&"I 0A-/4! K =+/61 1 ,1 =6 -1 1, !4!0 1 1 01 /8 1 9*&G 9:
1 !-1 9*&)I 0A-/4! K =+/61 1 1 / !/ 1 /0;! / 1 ,1 =6 -1 1, !4!0 1 1 01 /8 1
9*")* 99
1 !-1 9*&:I '1-102 ! +1441 ! +! 1-P 8/6 !041/ ! 4!,1 123 +180@ /61 9G
1 !-1 9*&9I !4 - 1 4 4 !041/ 4 ! ;- 123 $#
1 !-1 9*&$I !4 - 1 4 1 -/./?/123 A6/ 1* $9
A caracterização tecnológica de minérios é uma ferramenta de alta importância no
aproveitamento de um recurso mineral de forma otimizada, sendo recomendada nas fases
de exploração e explotação de um bem mineral. O presente trabalho vem apresentar a
caracterização do produto magnético proveniente do beneficiamento do minério de fosfato
do Complexo Mineração de Tapira, Tapira – MG. Foram determinadas as principais
características físicas, químicas e mineralógicas, bem como as respostas desse material a
ensaios em escala de bancada de separação magnética, flotação e lixiviação ácida. O
trabalho foi dividido de duas etapas: a primeira envolveu a caracterização mineralógica do
produto magnético (análise granuloquímica, difratometria de raios X, espectroscopia
Mössbauer, microscopia ótica e microscopia eletrônica de varredura); a segunda etapa
envolveu a realização ensaios de concentração (separação magnética, flotação e lixiviação
ácida). O material portador de ferro é composto predominantemente por magnetita, sendo
que esta magnetita apresenta processo de martitização (transformação magnetita para
hematita). Ilmenita ocorre intercrescida nos grãos de magnetita. O elemento P presente é
proveniente da apatita, isto é, não esta associado estruturalmente ao elemento Fe.
Separação magnética de baixa intensidade e a úmido resultou em recuperação metalúrgica
acima de 95%, o que sugere um estudo mais aprofundado no sentido de uma possível
implementação de mais uma etapa de separação magnética no processo de concentração da
apatita. Com relação ao processo flotação destacaIse o melhor desempenho do hidrocol
frente a amina como coletores de silicatos e apatitas, sendo o elemento P o contaminante
mais deletério no processo siderúrgico. Não foi possível detectar influência positiva quanto
'
The technological ore characterization is a tool of high importance in the exploitation of a
mineral resource of optimized form, being recommended in the phases of exploration and
miniing. The present work comes to present the characterization of the magnetic product of
the Complex Mining of Tapira, Tapira I MG. had been determined the main physical,
chemical and mineralogical characteristics, as well as the answers of this material the
assays in benches scale. The work was divided of two stages: the first involved the
mineralogical characterization of the magnetic product (particle size distribution, XIray
diffraction, Mössbauer spectroscopy, optics microscopy and scanning electron
microscopy); the second stage involved the concentration assays (magnetic separation,
flotation and acid leaching). The carrying material of iron is composed predominantly for
magnetite, being that this magnetite presents in process of transformation for hematite.
Ilmenite occurs in the magnetite grains. Present element P is proceeding from the apatite,
that is, not this associate structurally to the Fe element. Magnetic separation of low
intensity and the humid resulted in metallurgic recovery above of 95%, what it more
suggests a deepened study in the direction of a possible implementation of plus a stage of
magnetic separation in the process of concentration of the apatite. With regard to the
process flotation optimum performance of hidrocol is distinguished front to amine as
collecting of silicates and apatites, being element P the contaminante most deleterious in
the siderurgical process. It was not possible to detect positive influence how much to the
scrub process. Acid leaching assays of the carrying phase of the match had been effected
using acid ascetic and acid chloride. The results of this leaching show that acid ascetic
extracted only 0,41% and the acid chloride leached 64,88% of element P present in the
material The objective of assays was of if indicating a possible way of concentration of
& Q
A caracterização tecnológica de minérios é uma ferramenta de alta importância no
aproveitamento de um recurso mineral de forma otimizada, sendo recomendada nas fases
de exploração e explotação de um bem mineral.
Apesar de várias informações serem obtidas por um trabalho de caracterização bem
executado, esta é pouco aplicada aos rejeitos das usinas de beneficiamento de minérios,
sendo este descartado sem qualquer prévio conhecimento de suas características físicas,
químicas e mineralógicas.
Nos últimos anos isto vem mudando, não só pelas maiores cobranças com relação às
questões ambientais, como também, em alguns casos, devido à escassez do minério e
também com o próprio desenvolvimento tecnológico do beneficiamento de minérios.
Com o conhecimento deste rejeito é possível estudar a possibilidade de seu posterior
aproveitamento na própria usina onde foi gerado ou então que possa ser colocado como um
subproduto para um outro segmento industrial na forma em que se encontra. Com isso se
diminui o volume de rejeito que é descartado diariamente nas bacias, minimizando o
problema ambiental e também possibilitando a geração de capital com o seu posterior
aproveitamento.
Dessa forma o presente trabalho vem apresentar a caracterização do concentrado magnético
" Q '(
O presente trabalho foi desenvolvido com o principal objetivo de se executar a
caracterização tecnológica do concentrado magnético que é gerado no processo de
beneficiamento do minério fosfático no Complexo de Mineração Tapira e é descartado em
bacia de rejeito. Portanto para se levantar suas principais características físicas, químicas e
mineralógicas foram empregadas as técnicas de caracterização tecnológica de minérios:
análise granuloquímica, difração de raiosIx, microscopia ótica, microscopia eletrônica,
espectroscopia Mössbauer.
Paralelamente aos trabalhos de caracterização tecnológica foram realizados ensaios de
concentração com o intuito de indicar um possível caminho de separação entre fases
minerais distintas, minérios de ferro e apatita nas condições e proporções em que se
apresentam no material em estudo. Para tal foram feitos ensaios em escala de bancada de
separação magnética, flotação em célula e lixiviação ácida.
Assim o trabalho justificaIse no fato de que com o conhecimento deste rejeito tornaIse
possível analisar possibilidades de reaproveitamento no setor mineroImetalúrgico, que vem
associado á diminuição do impacto ambiental no que se refere ás bacias de contenção de tal
) Q ' '
)*& Q +,-!. /0! 123 1,/ 1
)*&*& Q /4 5 /6
Almeida (2001) relata que a Fosfértil I Fertilizantes Fosfatados S.A – iniciou suas
atividades em 1977 como uma empresa do governo federal com o intuito de promover a
pesquisa, lavra, beneficiamento e comercialização da rocha fosfática da jazida de Patos de
Minas – MG. No início da década de 80 a Fosfértil incorporou a Valep (empresa de
mineração de fosfato de Tapira) e também a Valefértil (complexo químico de fertilizantes
de Uberaba). Posteriormente, através do Programa Nacional de Desestatização, e também
por compras diretas de acionistas, a Fosfértil adquiriu 99,9% das ações da Utrafértil S.A e
também da Goiás Fertilizantes S.A. Hoje a Fosfértil é uma empresa com atribuições de uma
holding e de uma empresa de produtora de adubos fosfatados com as seguintes unidades de
produção.
• Complexo de Mineração Tapira
• Complexo de Mineração de Catalão
• Complexo Industrial de Uberaba
• Unidade II de Granulação de Uberaba
beneficiamento, mineroduto e instalações de suporte. A Figura 3.1 traz a localização do
Complexo de Mineração Tapira
Figura 3.1: Mapa de localização do Complexo de Mineração Tapira (Melo, 1997)
De Acordo com Almeida (2001) o Complexo de Mineração Tapira produz concentrado de
“rocha fosfática” (apatítico), obtido a partir da concentração do minério de fosfato com teor
inicial de aproximadamente de 8% P2O5, e é obtido um concentrado com teor final de
35,5% de P2O5. Este concentrado é transferido para o Complexo Industrial de Uberaba
(CIU), via mineroduto, onde é produzido o ácido fosfórico, base para a fabricação de
fertilizantes.
)*&*) Q ! - 8/1
Melo (1997) conceitua geologicamente o complexo alcalinoIcarbonatítico de Tapira como
uma chaminé ultramáficaIalcalina, de forma ovalada, com cerca de 35 km2, distribuídos em
aproximadamente 6,5 km na direção NS e a 5,5 km na direção EW. A chaminé ultramáficaI
alcalina está relacionada ao evento magmático, que afetou a plataforma brasileira, de idade
Cretácea, com aproximadamente 70 milhões de anos, e é intrusiva em rochas préI
cambrianas do Grupo Canastra.
Ainda de acordo com Melo 1997 o complexo de Tapira é composto principalmente por
rochas ultrabásicas, com predomínio do piroxenito (provavelmente maior que 80%), sobre
os peridotitos e dunitos.
Piroxenitos: Variam desde rochas praticamente monominerálicas a outros tipos litológicos,
onde a apatita, biotita ou flogopita, perovskita e titanomagnetita se tornam minerais
essenciais.
Dunitos: Rochas, cinzento escuras, de granulação fina a média, constituída por olivina
fosterítica e acessórios, de apatita, perovskita, magnetita e melanita.
Peridotitos: Tipos intermediários entre os dunitos e piroxenitos. Apatita, perovskita,
Carbonatitos: Formados essencialmente por calcita e minerais acessórios tais como:
flogopita, biotita, calcita e magnetitaIilmenita; ocorrendo nas porções centrais do
complexo.
Finalmente Melo (1997) define o modelo geológico de Tapira como o de complexos
carbonatíticos, onde os depósitos de fosfato, titânio e nióbio, são formados por
enriquecimento superficial, e os fatores gerais que regularam a formação destes depósitos
são: a composição original da rocha matriz; as condições de clima e relevo favoráveis; a
velocidade da erosão controlada e finalmente os aspectos estruturais da região.
Almeida (2001) coloca em seu trabalho que em função dos estudos realizados durante a
fase de pesquisa mineral o manto de intemperismo foi subdividido em 5 (cinco) zonas:
zona de estéril, zona de mineralização em titânio, zona de mineralização em fosfato com
titânio, zona de mineralização em fosfato e zona de mineralização em nióbio.
• Zona de estéril
Ocorre entre as cotas superiores e apresenta espessura média de 30 m. Os teores de P2O5
solúvel são menores que 5% os e teores de TiO2 estão abaixo de 10%. Este material é
constituído de pequenos fragmentos de rocha silificada, nódulos milimétricos de limonita e
raríssimas palhetas de vermiculita.
• Zona de mineralização em Titânio
È a zona imediatamente abaixo da zona de estéril. Os teores de TiO2 estão acima de 10% e
o de P2O5 é menor que 5%. A composição desta zona é similar à zona de estéril, mas já
aparece alguma perovskita, e o anatásio tornaIse mais abundante.
Em geral ocorre logo abaixo da zona de mineralização em titânio, numa transição para a
zona de mineralização em fosfato. O anatásio é o mineral de titânio mais freqüente, sendo
os teores de titânio nesta zona semelhante à anterior. O fosfato é predominantemente
apatítico, implicando na elevação dos teores de P2O5.
• Zona de Mineralização em Fosfato
Ocorre abaixo da zona de mineralização em fosfato com titânio e vai até atingir a rocha sã.
Os teores de P2O5 solúvel são superiores a 5% e o TiO2 são menores que 10%. Há uma
tendência em se encontrar teores mais elevados de P2O5 de acordo com o aumento da
profundidade. A magnetita já apresentaIse nesta zona e entre as micas a vermiculita é o
mineral freqüente.
• Zona de mineralização em Nióbio
Ocupa a parte mais central do corpo intrusivo e não apresenta aproveitamento econômico.
Há uma associação de titânio e terras raras com algum titânio e apatita. O titânio ocorre nas
partes mais próximas da superfície e a apatita aparece abaixo da zona de nióbio, em geral
com teores baixos.
Na Tabela 3.1 estão apresentadas as composições mineralógicas típicas do minério friável,
Tabela 3.1. – Composição do minério fosfático de Tapira (Almeida, 2001).
Composição típica do minério de fosfato (%)
TIPO DE MINÉRIO
Minerais Friável (75%) Granulado (25%) R.O.M
Apatita 21 16 20
Magnetita 22 19 21
Calcita/Dolomita 2 21 7
Mica 22 6 18
Quartzo 10 21 13
Diopsídio 5 5 5
Perovskita/ Anatásio 12 10 12
Opacos/ Outros 6 2 5
TOTAL 100 100 100
)*&*: Q '!0!;/6/1+!0
Almeida (2001) faz em seu trabalho a descrição do beneficiamento do minério do
Complexo de Mineração de Tapira, onde inicialmente o minério lavrado é transportado até
a unidade de britagem primária, onde se reduz o tamanho do minério de 762 mm para 127
mm. Após a britagem primária o material é homogeneizado e empilhado simultaneamente,
formando duas pilhas paralelas.
A etapa seguinte envolve a retomada do minério, que é enviado por meio de um sistema de
primeiro é denominado de minério granulado e apresenta granulometria teórica entre 7,1 e
28 mm e o segundo tipo de minério é chamado de minério friável e possui granulometria
abaixo de 7,1mm.
Esta subdivisão do processo de beneficiamento resulta em dois circuitos principais e
independentes: circuito granulado e circuito friável. Em ambos os circuitos as operações
unitárias empregadas para a concentração do minério são: moagem, separação magnética,
deslamagem e flotação. O Anexo 1 traz os fluxograma do circuito friável e o Anexo 2 traz o
fluxograma do circuito granulado..
De uma maneira geral, o que ocorre nos circuitos granulado e friável é o seguinte:
Circuito Granulado
O minério passa inicialmente por uma moagem em barras em dois moinhos paralelos. O
produto desta moagem alimenta a etapa de separação magnética de baixa intensidade,
executada em separadores tipo tambor. A fração magnética, objeto de estudo do presente
trabalho, é descartada, e a fração não magnética segue para uma etapa de adequação da
granulometria, passando por um moinho de bolas e subsequentes operações de deslamagem
em ciclones. A etapa seguinte consiste da flotação em células mecânicas nos estágios
rougher, scavenger, cleaner e recleaner. Assim, o flotado da etapa recleaner constitui o
concentrado granulado, e o afundado da etapa scavenger, o rejeito grosso granulado.
circuitos: um denominado de circuito grosso friável, onde é gerado um concentrado grosso
friável, que é obtido por etapas de flotação em células mecânicas (rougher, scavenger,
cleaner e recleaner); e o segundo, circuito ultrafino, onde se emprega colunas de flotação
nas etapas rougher, cleaner e célula mecânica na etapa scavenger, gerando o concentrado
ultrafino.
Finalmente, o produto final do circuito granulado se junta ao concentrado grosso friável, e
são remoídos para a adequação da granulometria, isto para o transporte no mineroduto. O
concentrado ultrafino segue para um espessador em seguida é filtrado e estocado para a
expedição por transporte rodoviário.
A taxa média de alimentação da usina de concentração é de 1680 t/h (base seca), sendo que
a partição de produtos da usina em média é: 14% de concentrado fosfático, 21% de lamas,
13% de rejeito magnético e 52% de rejeitos de flotação.
Como o processo industrial do Complexo de Mineração Tapira gera rejeitos da ordem de
85% da massa alimentada na usina de concentração, foi necessária a construção de duas
grandes barragens, sendo uma para contenção de lamas e outra para rejeitos grossos. A
Figura 3.2 mostra a deposição do concentrado magnético.
Há de se destacar, que no presente trabalho foi estudado somente o produto magnético do
Figura 3.2: Deposição concentrado magnético na bacia de rejeitos (Luzivotto, 2003)
)*" Q 4 1 16 ! =4 /614 ! ,-/612>!4 1 180! / 1
)*"*& Q 4 +/0! 1/4 , 1 !4 !-!+!0 !
Dana (1981) traz que o elemento ferro como um dos mais abundantes da litosfera, onde
entra na proporção de 4,2% em massa. Embora seus compostos sejam numerosos,
apresentamIse em grandes concentrações sob a forma de óxidos.
Betjtin (s.d.) cita que os minérios de ferro podem resultar de segregações magmáticas,
como é o caso dos depósitos de magnetitas relacionados com rochas intrusivas, ou, então,
de deposição química que é a origem mais freqüente.
Vários são os minerais portadores do elemento ferro, Dana (1981) traz em seu trabalho
várias informações sobre cada um destes minerais, sendo os de expressiva importância
apresentados a seguir:
Hematita: A composição química da hematita é Fe2O3,com conteúdo teórico em ferro de 70
%, e é o mineral de ferro mais comum e abundante da natureza. É a principal fonte de ferro
para a fabricação de ferro gusa. A martita ou hematita porosa, é um mineral secundário que
é formado a partir do intemperismo das magnetitas primárias. Existem várias discussões
sobre os processos de oxidação magnetita formando hematita.
Goethita: Sua composição química é FeO(OH), com conteúdo teórico de 62,9% de Fe. É
um dos minerais de ferro mais comuns e formaIse de modo típico, sob condições de
oxidação, como produto de intemperismo dos minerais de ferro.
Pirita: A fórmula química da pirita é FeS2, contendo teoricamente 53% do elemento Fe. O
mineral de pirita é muitas vezes explorado devido ao ouro ou cobre associado. Devido a
grande quantidade de enxofre presente no mineral, este é empregado como minério de ferro
nos países onde não se dispõe de óxidos de ferro. É principalmente empregada para
fornecer enxofre, matéria prima para a fabricação de ácido sulfúrico.
Magnetita: A composição química da magnetita é Fe3O4 ou FeO.Fe2O3, com conteúdo
teórico em ferro de 72,4 %, e tem como característica marcante seu forte magnetismo.
EncontraIse distribuída, sob forma de um mineral acessório, em muitas rochas magmáticas.
Em certos tipos de rochas, através da segregação magmática, tornaIse um dos principais
constituintes e pode assim formar grandes corpos de minério. Estes corpos são muitas vezes
altamente titaníferos.
Ilmenita: A fórmula química da ilmenita é FeO.TiO2, com conteúdo teórico de 36,8% de Fe
)*"*" 44=?!/4 ,-/612>!4 1 180! / 1
)*"*"*& Q ! 23 +/0@ / ! ;! !+ 1- ; 0
Vários autores como Dana (1981), Lisboa (1967) e outros, citam a magnetita (Fe3O4) como
matériaIprima para obtenção de ferroIgusa, mas atualmente o que se tem na indústria
siderúrgica é a obtenção de ferro primário através da redução da hematita (Fe2O3), e a
seqüência evolutiva de redução deste minério que ocorre no altoIforno é a Série
determinada por Moisson (1880) apresentada a seguir:
!" ) ⇒⇒⇒⇒ !) : ⇒⇒⇒⇒ ! ⇒⇒⇒⇒ !
Analisando a seqüência acima, se é induzido a pensar que seria mais vantajoso começar o
processo de redução pela magnetita. De acordo com Vieira (2002) ao se partir da hematita,
se tem a vantagem decorrente da mudança de densidade ao se mudar de fase
cristaloquímica. O sistema de cristalização da hematita é romboédrico (classe hexagonal),
ao passo que o sistema de simetria da magnetita é isométrico I assim como da wustita
(FeO) e do ferro elementar (Fe) I os quais são cúbico. Portanto no processo de obtenção do
ferro metálico a partir da carga de hematita é que ocorre um aumento na porosidade,
facilitando a percolação dos gases redutores. Por esse motivo, o uso da carga somente de
magnetita para obtenção do ferro tornaIse um problema em termos de redutibilidade,
Tabela 3.2: Especificações de minérios de ferro para siderurgia (Silva,1988)
10 -1 /0 ! ;!! !-! ;!!
Fe > 65 > 63 > 64
SiO2 < 2 1,5 a 6 1,5 a 7
Al2O3 < 1,5 > 1,7 > 1,7
P < 0,07 < 0,07 < 0,07
O é um produto da indústria mineral especialmente preparado para a
sinterização e possui características físicas e químicas adequadas a obtenção de um
aglomerado, denominado sínter, utilizado em altos fornos.
Oliveira (2003) traz o conceito de sinterização como a técnica empregada na aglomeração
de finos de minério de ferro, que surgiu com o principal objetivo de se aproveitar as frações
de minérios de ferro com granulometria inferior a 6 mm e superior a 0,150 mm, pois estas
não podem ser utilizadas diretamente nos altosIfornos por diminuírem a permeabilidade da
carga afetando consideravelmente o desempenho do equipamento.
No Brasil, praticamente todo o sinter é produzido a partir de minério hematítico, não se
tendo conhecimento, em nosso país, da produção de sínteres a partir de concentrados de
magnetita. Mas na China, segundo Yang e colaboradores (1997), os concentrados
domésticos de magnetita representam o minério dominante em muitas plantas de
sinterização.
Yang e colaboradores (1997) e Cloud e colaboradores (2003) apresentaram em seus estudos
comparações entre os sínteres produzidos pelos chineses a partir de concentrados de
magnetita com sínteres produzidos a partir de minérios hematíticos. Ambos concluíram que
o ideal seria uma mistura de ambos concentrados para se obter um sínter de mesma
Lundh (1989) e Chanda (1994) executaram testes de sinterização em escala piloto e
observaram ganhos termais provenientes da oxidação da magnetita (reação exotérmica), em
misturas de minérios hematíticos contendo concentrado de magnetita.
Assim como a produção de um aparece como uma opção, para posterior
sinterização, com já mencionado a possível produção de pellet feed aparece também como
alternativa para aproveitamento do material em estudo.
O é um produto da indústria mineral que explora minério de ferro e que surgiu
com o intuito de se aproveitar as frações de minério com granulometria abaixo de 0,150
mm. A pelotização é o processo de aglomeração destes finos de minério de ferro. Os
aglomerados produzidos por este processo denominamIse pelotas e podem ser utilizados
em todos os reatores de redução de minério de ferro (altosIfornos, processo Midrex,
processo Hyl e processos de redução direta), ao passo que o sínte é somente utilizado em
altos fornos e em fornos elétricos.
A pelota é um aglomerado esférico que é formado através do rolamento da mistura
finamente moída e adequadamente umedecida em discos ou tambores de pelotização. A
pelota pode ser posteriormente queimada ou não. Na grande maioria das instalações
industriais são produzidas pelotas queimadas, e esta queima ocorre em temperaturas da
ordem de 1250 a 1320 ºC.
O processo de endurecimento a quente (cocção), ou queima das pelotas, visa conferir as
pelotas alta resistência mecânica e propriedades metalúrgicas adequadas ao uso posterior
Tabela 3.3: Consumo calorífico na pelotização (Araújo, 1997).
/0@ / 04 + 61- =;/6
S (T ! ,!- 14U
0! 8/1 -@ /61
SVWMT ! ,!- 14U
Magnetita natural 240 –400 23 I 27
Misturas de
magnetita e hematita
540 – 830 25 – 30
Hematita 960 – 1100 28 – 33
Limonita 1250 – 1880 35 – 40
Conforme pode ser observado acima, o consumo calorífico é menor para minérios contendo
somente magnetita ou uma mistura de magnetita e hematita, isto é justificável porque
durante a queima das pelotas a magnetita se oxida para hematita, em uma reação
exotérmica, liberando cerca de 460 kJ por quilo de magnetita. Esta energia adicional é
obviamente favorável ao processo de endurecimento das pelotas.
Portanto, duas principais vantagens na utilização da magnetita na pelotização de finos de
minério de ferro. A primeira relaciona a economia de energia no processo de queima das
pelotas e a segunda relacionaIse à oxidação da magnetita para hematita contribuindo para
melhoria da qualidade das pelotas.
Colocada as possibilidades de aproveitamento da magnetita na siderurgia ainda há de se
destacar que o material em estudo ainda possui muitas impurezas e necessita passar por
processos de concentração que possibilitem a melhoria de qualidade.
Assim segundo Meyer (1980) ( Sá, 2003), podeIse citar como contaminantes
indesejáveis em minérios magnetíticos o titânio, principalmente na forma de ilmenita
Ainda em se tratando da qualidade dos minérios de ferro para redução em alto forno,
Araújo (1997) destaca em seu trabalho alguns dos principais elementos ou compostos
presentes nos minérios de ferro que podem tornarIse indesejáveis durante o processo de
redução, a saber:
Silício: O silício sob a forma de sílica (SiO2), representa o maior componente de ganga no
minério. Como o calor de redução da sílica é elevado ela é considerada um óxido
dificilmente reduzível. Nas temperaturas acima de 1200 ºC, grande parte da sílica combinaI
se com o CaO e o MgO para formar silicatos, que passam para a escória.
Fósforo: É talvez, o único elemento que passa totalmente para o gusa, ao serem reduzidos
com seus componentes carregados no alto forno. O fósforo é altamente indesejável porque
é o responsável pela fragilidade a do aço, isto é, baixo resistência ao choque à temperatura
ambiente.
Enxofre: O coque é o principal contribuinte para o elemento enxofre no ferroIgusa. Pode
chegar também ao altoIforno nos minérios sulfurosos. Forma com o elemento ferro um
sulfeto (FeS) e se localiza nos contornos dos grãos. Devido ao baixo ponto de fusão do FeS,
este irá fundirIse nas temperaturas correspondentes às operações de forjamento e
laminação, diminuindo a tenacidade do aço, chegando às vezes a causar sua desintegração
pela formação de fissuras durante a ação do martelo de forja ou cilindros laminadores.
Titânio: A redução do TiO2 no alto forno causa a formação sucessiva de Ti3O5, Ti2O3 e
líquido também são afetadas, resultando em cascões excessivos nas panelas do gusa
: Q
O presente trabalho foi desenvolvido junto ao Departamento de Engenharia de Minas da
Escola de Minas da Universidade Federal de Ouro Preto, com apoio de outros
departamentos da Universidade Federal de Ouro Preto e também com o apoio
daFertilizantes Fosfatados S.A – Fosfertil.
O trabalho constou de duas etapas; a primeira envolveu a caracterização mineralógica do
concentrado magnético; a segunda envolveu a realização de ensaios de separação
magnética, flotação e lixiviação ácida.
1,1 ! + 8!0!/7123 ! F 1 !1+!0
Inicialmente foi retirada amostra do concentrado magnético no circuito industrial da
Fosfértil logo após etapa de separação magnética, esta foi enviada para Ouro Preto e a partir
daí seguiuIse para etapa de homogeneização de 112 kg do material, que foi inicialmente
homogeneizada através de pilha cônica, e em seguida partiuIse para a formação de uma
pilha longitudinal de aproximadamente 2,5 m. Concluída a formação da pilha longitudinal
o material foi sendo recolhido novamente em balde e outra pilha longitudinal foi sendo
formada. Este procedimento foi repetido por três vezes para se garantir a completa
homogeneização da amostra. Ao final deste procedimento a pilha foi dividida
transversalmente e longitudinalmente e assim foram obtidas 7 amostras de 14,5 kg e uma
de 10 kg. De posse de uma destas oito alíquotas partiuIse para execução de sucessivas
:*& Q 1,14 ! 1 16 ! /7123 !60 -58/61
:*&*& 0A-/4! 10 - +@ /61
Salum (1988) traz a análise granulométrica como uma tarefa de grande importância nos
trabalhos de laboratório, esta pode fornecer informações tais como qualidade de uma
moagem, e avaliar o estabelecimento do grau de liberação, entre outras. Vários são os
métodos de análise granulométrica, sendo que cada qual é recomendado para uma faixa de
tamanho.
O peneiramento aplicaIse a uma ampla faixa de tamanho (1.000.000 m a 37 m). Consiste
na passagem de partículas em uma série de peneiras cujas aberturas são sucessivamente
menores.
As peneiras para análise granulométrica são padronizadas, sendo a série da ABNT a mais
utilizada. Tem como base uma peneira de abertura de 74 m, com as aberturas variando em
uma relação da raiz quadrada de dois.
O peneiramento pode ser a úmido, a seco e combinado, sendo que a escolha do método
depende de alguns fatores tais com teor de umidade e percentagem de finos. O tempo de
peneiramento na prática fica em torno de 10 minutos.
Assim, a amostra de concentrado magnético foi analisada granulometricamente utilizandoI
se a série da ABNT de peneiras 35 a 400 malhas. O peneiramento foi realizado a seco, com
pesagem das massas retidas em cada peneira. A massa inicial da amostra foi de 300 g com
tempo de peneiramento de 10 min. Uma alíquota de cada faixa granulométrica foi retirada
:*&*" /; 123 ! 1/ 4 B
A difração de raios X é uma técnica básica na caracterização tecnológica de minérios, com
vistas à identificação mineral, Gomes (1984) traz em seu trabalho o princípio desta técnica
sendo apresentado a seguir:
A difração de raios X pelos cristais resulta de um processo em que os raios X são dispersos
pelos elétrons dos átomos sem mudança no comprimento de onda (dispersão coerente ou de
Bragg). Um feixe difratado é produzido por dispersão só quando algumas condições
geométricas expressas pela lei de Bragg são satisfeitas. As difrações resultantes de um
cristal, compreendendo posições e intensidades das linhas de difração, é uma propriedade
física fundamental da estrutura cristalina da substância servindo não só à identificação
como também ao estudo de sua estrutura.
Conforme mencionado, a base teórica da técnica é dada pele lei de Bragg, que é expressa
por:
θ
λ
=
⋅
⋅
⋅
2
Onde:
λ: comprimento de onda da fonte de raiosIX;
ordem de difração, que também é conhecido. Portanto é o único valor desconhecido e
cada mineral possui um conjunto de distâncias interplanares características, sendo que essas
distâncias estão tabuladas em diversas referências.
A determinação mineralógica foi efetuada por difratometria de raios X onde uma alíquota
da amostra cabeça foi pulverizada e analisada em difratômetro de raiosIX, modelo XRDI
6000 XIRay Difractometer, com filtro de ferro e tubo de cobalto, de fabricação do
Shimadzu, pertencente ao Departamento de Química da Universidade Federal de Ouro
Preto. A varredura da amostra foi feita de 20I70° com velocidade angular 2 ° por minuto.
:*&*) Q /6 46 ,/1 /61
De acordo com Craig (1981) três tipos principais de propriedades qualitativas de
identificação mineral, a saber:
properiedades óticas: cor, reflectância, birreflectância e pleocloísmo, anisotropismo e
reflexões internas;
propriedades dependentes da dureza: dureza de risco, dureza de polimento e dureza de
microreentrância;
propriedades dependentes da estrutura e morfologia das fases: forma do cristal, geminação,
clivagem e partição.
A microscopia ótica é o método mais tradicional empregado na identificação mineral.
Trabalha na faixa de radiação visível e permite uma série de funções, tais como: estudar a
textura do minério, identificar as fases presentes e suas distribuições e determinar a forma,
tamanho de partículas e grãos e o grau de liberação do minério.
das seções delgadas, estas propriedades são qualitativas e podem não ser suficientes para
identificação sem equívocos.
Contudo é importante ressaltar que existe uma dependência muito forte entre as
propriedades, e a identificação é feita através da avaliação de vários grãos, tendo como base
todas as propriedades acima mencionadas.
Portanto a microscopia ótica auxiliou na identificação dos minerais presentes e também foi
executado um trabalho de contagem com o intuito de se determinar ao teor volumétrico dos
minerais de ferro e titânio presentes na amostra. Todo o trabalho de microscopia foi
executado em um microscópio ótico do Departamento de Engenharia de Minas, da
Universidade Federal de Ouro Preto, de responsabilidade da Prof. Rosa Malena Fernandes
Lima.
:*&*: /6 46 ,/1 -! C0/61 ! 1 ! 1 ! /6 44 0 1 -! C0/61
A microscopia eletrônica de varredura é um sistema da análise EDS geralmente utilizada
na caracterização mineralógica para estudar detalhadamente a morfologia das partículas
com dimensões ínfimas, elucidando dúvidas geradas na microscopia ótica. A possibilidade
de se analisar microestruturas e a tipologia da amostra é o maior indicativo para a
aplicação dessas técnica de análise instrumental. Essa técnica baseiaIse na interação da
matéria com os elétrons excitados e destinados à produção de imagens com aumentos de até
5000 vezes. Os elétrons são produzidos em uma fonte que pode ser um filamento de
tungstênio aquecido, e focalizados na amostra por meio de um sistema de lentes
Quando o feixe de elétrons atinge a amostra são muitas as interações com a superfície
varrida, ocorrendo várias emissões a saber: elétrons retroespalhados, elétrons transmitidos,
elétrons secundários, elétrons Auger, raiosX carcterísticos e luz.
Elétrons secundários, retroespalhados e transmitidos, usualmente, são utilizados para a
visualização da amostra no MEV.
Para se obter informações sobre a composição das amostras observadas, utilizamIse raios X
característicos, elétrons Auger e catodoluminescência. Assim sendo, a microssonda
eletrônica é baseada na medida desses raios X característicos. As linhas de raios X
característicos são específicas do número atômico da amostra e da energia, podendo
identificar o elemento que está emitindo a radiação.
Dois tipos de espectroscopia de raios X podem ser utilizadas, por dispersão de energia
(EDS) e por dispersão do comprimento de onda (WDS).
Os sitemas EDS e WDS são complementares. O EDS possibilita a observação do espectro
inteiro dos raios X de modo simultâneo, o que permite uma análise semiIquantitativa rápida
dos principais constituintes, enquanto o WDS deve ser varrido mecanicamente na faixa de
comprimento de onda, sendo necessária a troca de vários cristais para cobrir a mesma
faixa de enregia como o EDS, o que é uma operação bastante demorada. Para análises de
elementos leves, tanto o WDS como o EDS tem condições de detectar raios X até de
elementos de número atômico tão baixo quanto 5. Após uma análise qualitativa de uma
amostra com EDS, geralmente é necessário utilizar o WDS para determinar se alguns picos
dos constituintes menores ou traços, de interesse que estão contidos nas vizinhanças dos
constitintes principais (Bento, 2000).
• permite a análise semiIquantitativa da composição química dos campos amostrais com
diâmetro da ordem de poucos micrômetros;
• o material pode ser visualisado ao tempo de análise, o que ganha destaque quando
certos materiais, sob o impacto do feixe de elétrons, emitem luz visível;
• material é analisado podendo ser observado a luz transmitida, polarizada ou
refletida;
• é uma técnica muito eficiente, considerando o número de informações em função do
tempo de análises.
Desta forma, as análises em MEVIEDS foram executadas no laboratório de Microscopia e
Microanálise do Departamento de Engenharia Geológica, da Universidade Federal de Ouro
Preto.
:*&*9 Q 4,!6 46 ,/1 D44 1 !
Sá e outros (1999) mostra em seu trabalho um comparativo entre várias técnicas de
caracterização para minérios de ferro e as espectroscopia Mössbauer é uma delas. De Grave
e outros (1998) conceituam a espectroscopia de Mössbauer como uma técnica não
destrutiva que utiliza a absorção ressonante da radiaçãoγsem recuo. O processo ressonante
consiste na emissão de radiação por um núcleo excitado e na absorção dessa radiação por
um outro núcleo idêntico, sem perda de energia pelo recuo dos núcleos, se o emissor ou o
absorvedor estiver incorporado a uma matriz sólida. A Figura 4.1 mostra a absorção
Figura 4.1: Absorção ressonante: base de efeito Mössbauer
Para usar a fonte de Mössbauer como instrumento espectroscópico é necessário fazer variar
a sua energia num dado intervalo. Isso é alcançado através do efeito de Doppler, usando o
movimento relativo entre a fonte e absorvedor. A fonte radioativa é fixada na ponta de um
eixo ligado a um transdutor que executa um movimento oscilatório longitudinal. Quando
esse fóton atinge a amostra contendo o elemento com núcleo idêntico ao emissor, ela pode
ser absorvida ou não, dependendo das condições da ressonância. Quando o fóton não é
absorvido, o fóton atravessa a amostra e atinge o detector. Quando ele é absorvido, o fóton
é reIemitido não necessariamente na direção do detector. Assim quando há ressonância, a
taxa de contagem de fótons lida pelo detector é sensivelmente menor do que o observado
quando a amostra não absorve os fótons. Assim um espectro de Mössbauer é um gráfico de
transmissão dos raiosγversus a velocidade da fonte de radiação.
A espectroscopia de Mössbauer de compostos contendo Fe é baseada no fenômeno de
emissão dos raios γ pelo Fe57, produto do decaimento do Co57, e absorção pelo Fe57 em
sólidos.
A partir de um espectro Mössbauer podemIse obter os seguintes parâmetros:
FatorIf e o Deslocamento Doppler de 2ª ordem: parâmetros relacionados com a dinâmica de
vibração do reticulo cristalino;
Deslocamento Isomérico: parâmetro relacionado com o estado de oxidação ou valência dos
átomos que compõe a amostra;
Desdobramento Quadrupolar: parâmetro relacionado com o potencial eletrostático local dos
átomos;
Campo Hiperfino: parâmetro relacionado com os momentos magnéticos dos átomos
envolvidos na ressonância.
Mitra (1992) cita em seus estudos que desde a descoberta da espectroscopia de Mössbauer,
esta técnica tem várias aplicações na mineralogia, tais como:
•Identificar fases minerais;
•Caractererizar o estado oxidação do ferro (Fe2+ou Fe3+);
•Determinar a coordenação dos átomos de ferro (octaédrico, tetraédrico, plana, etc) e a
natureza das distorções dos sítios simétricos (tetragonal ou trigonal, comprimida ou
estendida, etc);
Assim, a espectroscopia de Mössbauer forneceu o teor dos óxidos de ferro na amostra e os
estados de oxidação do ferro. As análises foram executadas no Laboratório de
Espectroscopia Mössbauer, do Departamento de Química da Universidade Federal de Ouro
Preto.
:*" Q 4 4 ! 06!0 123
:*"*& Q !,1 123 180@ /61
Apesar do material em estudo ser produto de uma etapa de separação magnética em escala
industrial, optouIse por realizar uma nova etapa de separação magnética, em escala de
bancada, sendo empregado para tanto, um separador magnético tipo tambor de baixa
intensidade com amperagem 2 amperes, tratandoIse polpa com 20 % de sólidos, em
massa. Esta etapa do trabalho foi executada no Laboratório de Tratamento de Minérios do
Departamento de Engenharia de Minas da Universidade Federal de Ouro Preto.
Estes ensaios de separação magnética, logicamente, geraram dois produtos, um nãoI
magnético e um magnético, sendo a porção magnética a de maior interesse no presente
estudo e denominada FSM (produto magnético pósIseparação magnética). Deste FSM foi
feita a análise granulométrica, análise química por faixa granulométrica e também foi
empregado em ensaios de flotação em célula.
:*"*"Q - 123
A fim de se concentrar os minerais de Fe foram executados ensaios de flotação em célula
reversa de minério de ferro e o hidrocol, óleo vegetal ligeiramente hidrogenado (Oliveira
2005), na flotação de apatita. Ainda foi trabalhada a questão da atrição da polpa antes o
condicionamento da mesma, por um tempo de 10 minutos, sendo que para esta a polpa
estava com uma concentração de 60% de sólidos e para a flotação propriamente dita este
valor foi de 35% de sólidos. O tempo de condicionamento para o amido foi de 5 minutos e
para os coletores foi de 1 minuto. O pH de flotação ficou entre 10 e 10,5. Foram
empregados os materiais FTQ e FSM. A Tabela 4.1 traz de que forma os ensaios de
flotação. Os ensaios foram realizados em duplicata, isto é: #&X #"Y #) X #:Y #9 X
#$Y #G X #<Y #H X &#Y && X &"Y &)X &:Y &9 X &$
Tabela 4.1.Condições dos ensaios de flotação
! 4 ! 4 1 ! /1 - /2 3 / 6 - + /0 1
E 0 1 F S M X
E 0 2 F S M X
E 0 3 F S M X X
E 0 4 F S M X X
E 0 5 F T Q X
E 0 6 F T Q X
E 0 7 F T Q X X
E 0 8 F T Q X X
E 0 9 F S M X
E 1 0 F S M X
E 1 1 F S M X X
E 1 2 F S M X X
0 4 1 / 4 ! - 1 2 3
Ante ensaios de flotação propriamente ditos foi necessário a adequação granulométrica do
FTQ e do FSM ao processo de flotação, onde para minérios de ferro esta é recomendada
100% abaixo de 0,210 mm (65#). Assim para tanto esta preparação da granulometria foi
feita através da moagem em um moinho de bolas, em um tempo de 45 minutos, em uma
polpa com 70% de sólidos e com um fator de enchimento de 50%. Assim desta moagem
foram obtidos os produtos FTQ moído e FSM moído.
:*"*) /./?/123 6/ 1
Uma outra forma de se concentrar os minerais de ferro no material em estudo, ou melhor,
de se extrair o elemento P de tal amostra, foi analisada através de testes de lixiviação ácida,
onde se utilizou o ácido acético e o ácido clorídrico, isto é um ácido “fraco” e um ácido
“forte”, ambos concentrados em solução a 5% em volume.
A metodologia de execução do teste foi de se fazer passar pelo material as soluções de
ácido acético e ácido clorídrico, uma de cada vez, cada qual com uma alíquota do material.
Isto foi feito por meio de um tubo de acrílico colocado na posição vertical, sendo que na
extremidade inferior deste tubo foi colocado um funil com papel de filtro para reter o
material e filtrar a solução. Assim inicialmente se colocou a amostra do material no tubo e
depois a solução ácida foi adicionada sobre a amostra. Desta forma foi iniciada a
percolação da solução pela amostra, sendo que a cada determinado volume de solução
percolado pela amostra, foi sendo coletado e posteriormente foi determinada a concentração
do elemento P para cada um desses volumes de solução, possibilitando determinar quanto
de tal elemento foi extraído da amostra por cada tipo de ácido.
solução pelo minério são referentes ao papel e se descontar tal valor na determinação da
9 Q
9*& Q 1 16 ! /7123 !60 -58/61
9*&*& 0A-/4! 10 - +@ /61
Neste tópico do trabalho é apresentada na Figura 5.1 a distribuição granulométrica do FTQ
(friável tal qual), realizada por peneiramento a seco, onde se verifica que o d80= 0,42 mm,
isto é, 80 % da amostra encontraIse abaixo de 420 m.
/4 / /23 10 - +@ /61 F
# "# :# $# <# &##
&# &## &### ! 1 +/6 C+!
Z
,
1
44
1
0
!
Figura 5.1: Distribuição granulométrica do FTQ
9*&*" Q 0A-/4! F =+/61
Para melhor conhecimento do FTQ a análise química foi feita por faixa granulométrica,
sendo que a análise química foi executada pela Fertilizantes Fosfatados S.A e estão
Tabela 5.1: Análise granuloquímica do FTQ
! 1
++ Z ! 4/+,-!4 ! 8 1 / " -" ) / "
0,420 20,00 0,68 74,40 2,27 2,20 11,23 1,02 3,46
0,210 27,50 0,96 73,06 2,03 3,07 10,38 0,85 3,55
0,149 13,83 0,94 77,37 1,76 2,94 9,36 0,61 2,65
0,074 23,33 0,77 79,59 1,66 2,27 8,61 0,64 2,63
0,037 11,00 0,69 78,90 1,67 2,12 7,98 0,67 2,41
I0,037 4,33 0,67 80,63 1,68 2,12 7,83 0,83 2,57
0A-/4! 10 - K =+/61 F
É visto ao se avaliar a tabela acima alguns tópicos interessantes, tais como, o elevado teor
do elemento Fe, que tende a se concentrar nas frações mais finas e que a princípio conduz a
um pensamento de aplicação deste na indústria siderúrgica, mas que em contrapartida a este
raciocínio se tem a presença de P2O5,que quando comparada a especificação de minério de
ferro (P < 0,040%), são exorbitantes, mas isto já era esperado, pois trataIse de um “rejeito”
de um processo de concentração de minério essencialmente apatítico.
Outro ponto a se destacar é a presença de Ti, na forma de TiO2. A influência do elemento
Ti em minérios de ferro é que este contribui com a melhora da qualidade do aço inox, mas
para aplicação em processo de fabricação de aço em fornos elétricos o elemento Ti
influência negativamente na economia de energia e aumenta o consumo de refratários.
Com relação aos outros compostos presentes (SiO2, MgO e CaO) estes estão em proporções
mais bem mais próximas às especificações de mercado de minérios de ferro para a
detectado na analise química é proveniente da magnetita e da hematita e o elemento Ti da
ilmenita..
9*&*: 4,!6 +! /1 D44 1 !
Através da Espectometria Mössbauer foi possível determinar quanto do FeT presente
corresponde a cada uma das três fases minerais presentes portadoras de tal elemento, isto é,
possibilitou a quantificação das fases minerais portadores do Fe, e sendo assim distribuída:
• Magnetita I 69%
• Hematita I 23%
• Ilmenita I 6%
9*&*9 /6 46 ,/1 /61
Os estudos de microscopia ótica foram realizados com principal foco nos minerais
portadores do elemento Fe, através da identificação desses em face à técnica, onde
praticamente se trabalhou com luz refletida. Para tal, foram confeccionadas seções polidas
delgadas por faixa granulométrica. A codificação das lâminas está mostrada na Tabela 5.2
Tabela 5.2: Código das lâminas.
Código
[ ++
35 0,42 LAM183
65 0,21 LAM184
100 0,149 LAM185
200 0,074 LAM186
400 0,037 LAM187
I400 I0,037 LAM188
Retido
Através da aplicação da microscopia possível identificar a magnetita, que apresenta aspecto
caracteristicamente cor rosa, esta encontraIse em processo de martitização, processo pelo
qual a magnetita transformaIse pseudomorfologicamente em hematita, o qual evolui das
bordas para o centro do grão. Também é vista a ilmenita, na maioria das vezes lamelar e
intercrescida nos grãos da magnetita, fator que vem a dificultar expressivamente ou a até
impossibilitar uma possível concentração dos dois minerais distintamente em escala
industrial. A seguir são apresentadas algumas figuras que possibilitam a visualização
Figura 5.4: Grão típico do material em estudo
Acima na Figura 5.4 apresenta um grão típico do sistema em estudo, este está na fração
acima de 420gm sendo a que foi a análise em microscopia ótica foi feita com luz refletida
polarizada, com nicóis descruzados e foi possível identificar a magnetita que tem como
característica marcante a sua cor rosada e a mesma apresentaIse em processo de
martitização, que caracteristicamente ocorre das bordas para o centro do grão. Na Figura
5.5 a seguir é mostrado em detalhe a região central da mesma partícula apresentada e fica
Figura 5.5: Região central da partícula apresentada na Figura 5.4
Na Figura 5.5 fica mais evidente a magnetita (rosa) e o processo de martitização onde a
martita apresenta coloração cinza e o processo de martitização sendo as condições de
Figura 5.6: Grão do material em estudo praticamente todo martitizado.
Na Figura 5.6 é apresentada a fotomicrografia de uma partícula praticamente toda
martitizada, sendo que a análise desta foi feita com luz polarizada refletida, nicóis
descruzados, a partícula mostrada esta na faixa granulométrica acima de 420gm. Em
análise da partícula para efeito de cálculo de teor volumétrico esta apresenta em torno de
Figura 5.7: Fotomicrografia apresentando magnetita, a hematita e a ilmenita.
A Figura 5.7 mostra a presença da ilmenita que tem como característica sua forma lamelar,
a sua identificação é feita sob nicóis cruzados e com o giro da lâmina, a mesma muda de
intensidade de cor ao se girar a lâmina, este grão esta na faixa granulométrica acima de
420gm. Para efeito de contagem de pontos magnetita fica na faixa de 45%, a hematita 50%
Figura 5.9: Fotomicrografia apresentando ilmenita e magnetita
Na Figura 5.9 é apresentado um grão com a presença clara de ilmenita lamelar, magnetita e
processo de martitização. A análise deste grão foi feita sob luz polarizada refletida, com
nicóis descruzados. Para efeito de tratamento de minérios dificilmente se consegue separar
esta ilmenita da magnetita, talvez somente por processos hidrometalúrgicos.
Assim através da microscopia ficou evidenciado a presença da magnetita, das ilmenita e da
hematita. Também com a microscopia ótica foi feita a estimativa do teor volumétrico para
quatro faixas granulométricas, para tanto se adotou a metodologia de se tomar
espaçamentos transversais e longitudinais constantes no decorrer da lâmina.
Tabela 5.3: Teor volumétrico estimado.
123 [ 4 6 0 1 4 4 180! / 1 1 / 1 -+!0/ 1 ! M/ 1
35 150 11,24 58,20 20,66 7,19 2,68
65 140 8,36 60,34 28,34 4,43 0,04
100 170 5,60 62,61 25,68 3,60 0,37
200 200 4,25 67,15 23,99 3,25 0,70
I400 200 1,08 68,71 24,05 2,63 3,45
! - +@ /6 4 /+1
Z 4 +/0! 1/4
Portanto, através desta técnica, assim como na análise granuloquímica notaIse que há uma
concentração dos minerais de Fe nas frações mais finas. RessaltaIse que esta técnica
aplicada sofre grande influência direta do operador no resultado, mas não foge muito á
realidade.
9*&*$ /6 46 ,/1 -! C0/61 ! 1 ! 1 6 + /4 !+1 ! 0A-/4!
A microscopia eletrônica foi feita com o objetivo de se detectar elemento P, e se esse está
associado à estrutura dos minerais portadores do elemento Fe, ou então adsorvido nesses.
A seguir estão apresentadas de eletronImicrografias do material em estudo com os
respectivos espectros e as percentagens dos elementos e compostos presentes no ponto
analisado.
Figura 5.10: ElétronImicrografia de partícula típica do sistema em estudo.
Figura 5.11: Espectro de raios X geral da partícula apresentada na Figura 5.10
Tabela 5.4: Análise química geral da partícula apresentada na Figura 5.10
3041 5.55 11.66 CO2 20.33
7021 39.67 62.59 III
459 0.62 0.65 MgO 1.03
447 0.42 0.40 Al2O3 0.80
! 568 0.42 0.38 SiO2 0.91
Figura 5.12: Espectro de raios X da região central da partícula apresentada na Figura 5.10
Tabela 5.5: Análise química da região central da partícula apresentada na Figura 5.10
1765 3.42 7.78 CO2 12.53
6138 36.20 61.79 III
443 0.65 0.73 MgO 1.07
387 0.39 0.40 Al2O3 0.74
" 4005 3.71 2.12 TiO2 6.19
304 0.48 0.24 MnO 0.62
33069 55.15 26.96 FeO.Fe2O3 78.84
Figura 5.13: Espectro de raios X da borda 1 da partícula apresentada na Figura 5.10
Tabela 5.6: Análise química da borda 1 da partícula apresentada na Figura 5.10
#
2544 4.58 9.97 CO2 16.80
6490 38.11 62.20 III
472 0.63 0.68 MgO 1.05
625 0.58 0.56 Al2O3 1.10
! 321 0.24 0.22 SiO2 0.51
Figura 5.14: Espectro de raios X da borda 2 da partícula apresentada na Figura 5.10
Tabela 5.7: Análise química da borda 2 da partícula apresentada na Figura 5.10
#
3041 5.55 11.66 CO2 20.33
7021 39.67 62.59 III
459 0.62 0.65 MgO 1.03
447 0.42 0.40 Al2O3 0.80
! 568 0.42 0.38 SiO2 0.91
" 3295 2.97 1.57 TiO2 4.95
31112 50.34 22.76 FeO.Fe2O3 71.98
Figura 5.15: Espectro de raios X da borda 3 da partícula apresentada na Figura 5.10
Tabela 5.8: Análise química da borda 3 da partícula apresentada na Figura 5.10
#
1927 3.70 8.35 CO2 13.57
6548 36.55 61.87 III
395 0.57 0.64 MgO 0.95
308 0.31 0.31 Al2O3 0.59
177 0.11 0.10 P2O5 0.25
Figura 5.16: Espectro de raios X da borda 4 da partícula apresentada na Figura 5.10
Tabela 5.9: Análise química da borda 4 da partícula apresentada na Figura 5.10
#
2968 4.85 10.53 CO2 17.76
2607 38.05S 62.06 III
274 0.34 0.36 MgO 0.56
295 0.25 0.24 Al2O3 0.48
! 557 0.37 0.35 SiO2 0.80
" 2277 1.83 0.99 TiO2 3.04
4479 4.20 2.11 Cr2O3 6.14
32923 47.37 22.13 FeO.Fe2O3 67.72
$ 1323 2.75 1.22 NiO 3.50
Portanto pelos resultados apresentados é visto que se trata de uma partícula composta basicamente de Fe e Ti.
Figura 5.17: ElétronImicrografia de partícula do sistema em estudo
Figura 5.18: Ampliação da “região central” da Figura 5.17.
Figura 5.19: Espectro de da fase escura da partícula apresentada na Figura 5.18
Tabela 5.10: Análise química da fase escura da partícula apresentada na Figura 5.18.
#
10915 24.96 52.45 III
291 0.58 0.80 MgO 0.96
276 0.38 0.47 Al2O3 0.72
! 1801 1.93 2.31 SiO2 4.12
560 0.48 0.52 P2O5 1.11
261 0.23 0.20 CaO 0.33
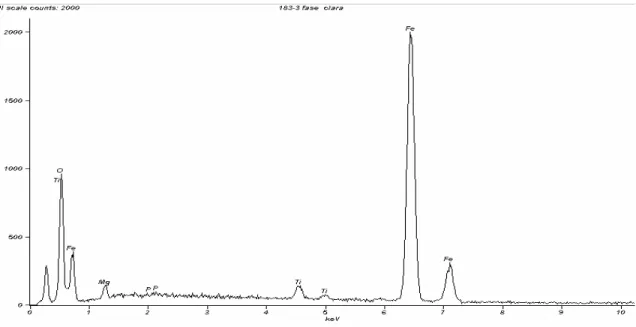
Figura 5.20: Espectro de raios X da fase clara da partícula apresentada na Figura 5.18
Tabela 5.11: Análise química da fase clara da partícula apresentada na Figura 5.18
Assim frente aos resultados obtidos é dito que a fase clara é a martita e fase escura a magnetita.
#
6655 23.25 50.61 III
779 1.64 2.36 MgO 2.73
57 0.05 0.06 P2O5 0.12
" 1303 1.57 1.14 TiO2 2.62
33781 73.49 45.83 FeO 94.54
Figura 5.21: Ampliação da borda superior direita da partícula apresentada na Figura 5.17
A Figura 5.21 mostra a ampliação da borda superior direita da partícula apresentada na
Figura 5.17 e o que se destaca nesta partícula é a presença de elementos de terras raras,
como pode ser observado através da análise do espectro de raios X apresentado na Figura
5.22, e confirmado através da análise química apresentada na Tabela 5.13 que traz as
Figura 5.22: Espectro de raios X da borda superior direita da partícula apresentada na Figura 5.17
Tabela 5.12: Análise química da partícula apresentada na Figura 5.17
#
6449 34.08 65.46 III
294 0.50 0.57 Al2O3 0.94
16319 18.01 17.87 P2O5 41.27
5453 6.92 5.31 CaO 9.68
1862 5.66 3.11 FeO 7.28
% 8629 17.81 3.94 La2O3 20.89
6480 17.02 3.73 Ce2O3 19.94
Figura 5.23: ElétronImicrografia com destaque á presença de ilmenita
Figura 5.24: Espectro da borda direita inferior da partícula apresentada na Figura 5.23
Tabela 5.13: Análise química da borda direita inferior da partícula apresentada na Figura 5.23.
#
2281 33.70 57.55 III
358 2.30 3.31 F 2.30
5820 8.18 9.19 MgO 13.56
" 27421 31.70 18.08 TiO2 52.87
& 307 0.42 0.22 V2O5 0.75
2196 4.34 2.16 MnO 5.60
9348 19.37 9.48 FeO 24.92
Através da análise química é visto que a região analisada tem alta concentração de titânio o
que indica ser a presença de ilmenita, o que associado á forma lamelar, como pode ser
observado na região em destaque na Figura 5.23, reforça tal afirmação.
Assim a microscopia eletrônica e as análises químicas pontuais das partículas do sistema
em estudo confirmaram quais os minerais e elementos presentes, mostraram que o elemento
P não está estruturalmente associado aos minerais portadores do Fe, e trouxe como
novidade a presença dos elementos de terras raras.
9*" Q 041/ 4 ! 06!0 123
9*"*& Q !,1 123 180@ /61
Apesar do material em estudo ser a porção magnética de uma separação magnética
industrial (rejeito), foi feito uma nova separação magnética de baixa intensidade em escala
de bancada, onde se utilizou um separador magnético de tambor, trabalhandoIse com 2A e
polpa com 20% de sólidos. A seguir são apresentados na Tabela 5.18 os resultados deste
ensaio.
Tabela 5.14: Balanço de massa e metalúrgico do ensaio de separação magnética
1441 S8U " 9 !
Alimentação 1050,00 1,62 78,86
Fração Magnética 140,60 10,10 20,53
Fração Magnética 881,00 0,61 87,02
" 9SZU ! SZU
! !4 SZU
implementação de mais uma etapa de separação magnética no processo de concentração da
apatita.
Após o ensaio de separação magnética foi feita análise granulométrica do produto
magnético (FSM), via peneiramento a seco e o resultado apresentado na Figura 5.25, onde
também é novamente apresentada a distribuição granulométrica do material original (FTQ),
e é visto que o FSM apresenta uma granulometria menor.
/4 / /23 8 10 - +@ /61 F !
# "# :# $# <# &##
&# &## &###
! 1 +/6 C+!
Z , 1 44 1 0 ! FTQ FSM
Figura 5.25: Distribuição granulométrica do produto magnético
9*"*" Q 041/ 4 ! - 123
Para realização dos ensaios de flotação foi primeiramente necessário adequar a
granulometria das alimentações, isto foi obtido através de moagem, portanto são
apresentadas as análises granulométricas do FTQ e do FSM após moagem. As distribuições
granulométricas são apresentadas na Figura 5.26. As tabelas com as distribuições
.
/4 / /23 8 10 - +@ /61 ,54 + 18!+
# "# :# $# <# &##
&# &## &###
! / 1 !+ +/6 +! 4
Z , 1 44 1 0 ! / F /
Figura 5.26. Distribuições granulométricas pósImoagem.
Assim apresentaIse que o material esta 100% abaixo de 210 gm, atendendo ás
especificações granulométricas ao processo de flotação reversa de minério de ferro.
Como já colocado os ensaios de flotação foram realizados trabalhandoIse com algumas
variações, quais sejam elas: o tipo de material (FSM, FTQ); o tipo de coletor para apatita
(hidrocol e amina); e também quanto ao processo de atrição da polpa antes do
condicionamento da mesma. RessaltaIse que os ensaios foram realizados em duplicata, isto
é, ensaio#"foi realizado sob as mesmas condições que o ensaio#&(E 01 = E 02); (E 03= E
04); assim por diante. Os resultados dos ensaios de flotação são apresentados na Tabela
Tabela 5.15: Resultados dos ensaios de flotação
041/ /, ! 6!44 144/61 !
1-+1 ! /1- ! 1 /23 / 6 - +/01 " 9 ! SZU SZU
E 01 FSM X Conc 0,50 88,89 46,12 79,62
Rejeito 0,89 83,91
E 02 FSM X Conc 0,42 88,33 48,65 90,31
Rejeito 0,89 82,69
E 03 FSM X X Conc 0,42 88,01 60,88 96,70
Rejeito 1,14 80,76
E 04 FSM X X Conc 0,47 88,79 59,89 87,23
Rejeito 1,14 81,25
E 05 FTQ X Conc 0,64 82,21 86,43 94,41
Rejeito 7,99 51,00
E 06 FTQ X Conc 0,50 84,89 85,85 86,92
Rejeito 7,99 55,87
E 07 FTQ X X Conc 0,59 83,40 88,30 92,48
Rejeito 9,80 50,42
E 08 FTQ X X Conc 0,55 85,43 88,04 87,93
Rejeito 10,56 52,77
E 09 FSM X Conc 0,67 90,38 97,81 90,37
Rejeito 1,44 68,92
E 10 FSM X Conc 0,63 88,32 97,88 97,83
Rejeito 1,48 67,96
E 11 FSM X X Conc 0,65 88,89 97,74 96,20
Rejeito 1,78 66,39
E 12 FSM X X Conc 0,78 89,34 97,02 93,79
Rejeito 1,60 69,15
E 13 FTQ X Conc 1,69 81,02 92,13 92,59
Rejeito 2,76 64,31
E 14 FTQ X Conc 1,69 81,04 92,99 95,79
Rejeito 3,64 55,37
E 15 FTQ X X Conc 1,78 82,26 92,82 91,29
Rejeito 3,03 58,76
E 16 FTQ X X Conc 1,68 82,99 93,83 88,96
Rejeito 3,24 59,33
Sob o ponto de vista da resposta dos minerais de ferro frente aos ensaios realizados destacaI
se a seguir as Figuras 5.27 e 5.28 em que se tem plotadas recuperações mássicas e
metalúrgicas do FeT obtidas nos ensaios. Os resultados foram plotados separadamente por
tipo de material. Na Figura 5.34 se tem os resultados dos ensaios E 01, E 02, E 03, E 04, E
09, E 10, E 11e E12 versus recuperações, ensaios realizados com o FSM
041/ 4 6 +
# "# :# $# <# &##
#& #" #) #: #H &# && &"
041/ 4 !6 , ! 1 23 SZ U 144/61 ! 1-P 8/61
Figura 5.27: Recuperações mássicas e metalúrgicas dos ensaios com o FSM
A primeira analogia que se faz é em relação ao tipo de coletor utilizado, pois nos ensaios
E01, E 02, E 03, E 04 se empregou o hidrocol como coletor e nos demais (E 09, E 10, E 11,
E12), a amina. Analisando a Figura 5.27 éIse induzido a concluir que o melhor resultado
foi obtido com a amina, mas ao se analisar a Figura 5.28,a seguir, onde se tem plotado
Ensaios versus Teores de P2O5no Concentrado, observaIse que o hidrocol foi mais seletivo,