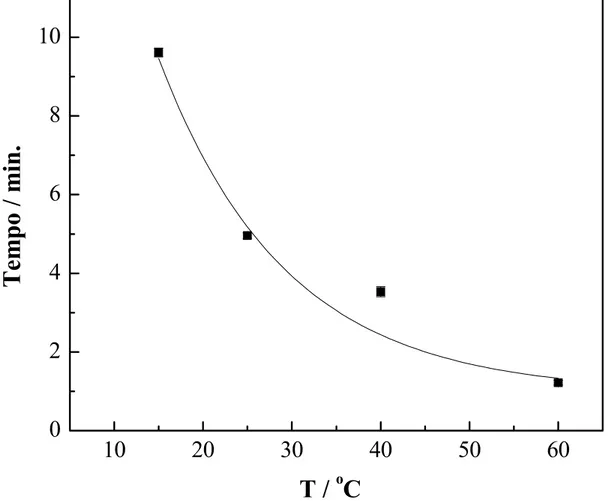
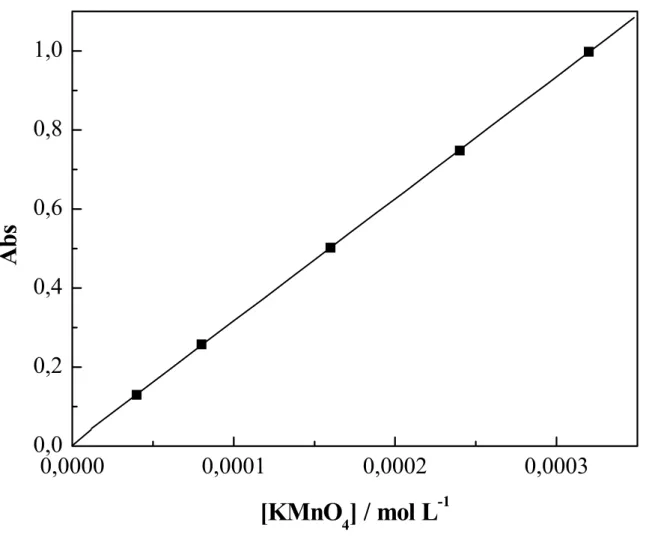
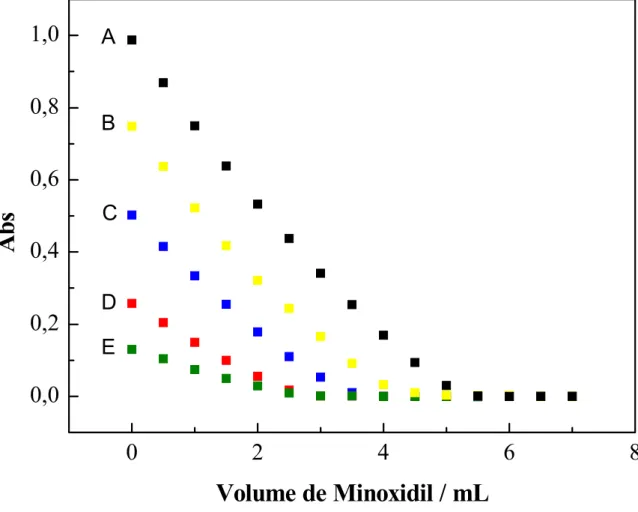
Estratégias para a determinação de Minoxidil.
Texto
Imagem
![Tabela 2: Classificação clínica quanto ao nível da pressão arterial (PA) [5]](https://thumb-eu.123doks.com/thumbv2/123dok_br/18608420.383183/28.892.128.807.125.419/tabela-classificação-clínica-quanto-nível-pressão-arterial-pa.webp)
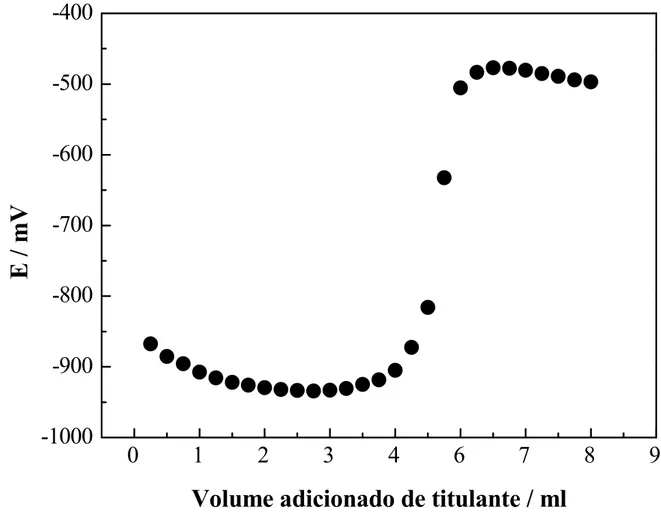


Documentos relacionados
• Participar dos Encontros de Formação Inicial e Continuada promovido pela Coordenação Geral do Projeto. • Organizar as fichas de matrícula dos alunos por turma e
45 Figure 18 - Study of the extract concentration in the phycobiliproteins extraction and purification using the mixture point composed of 10 wt% Tergitol 15-S-7 + 0.3
Avaliação do impacto do processo de envelhecimento sobre a capacidade funcional de adultos mais velhos fisicamente ativos.. ConScientiae
O tratamento com resveratrol diminuiu de maneira significativa o número de células totais e de eosinófilos no tecido pulmonar dos camundongos controles e obesos, não
• The definition of the concept of the project’s area of indirect influence should consider the area affected by changes in economic, social and environmental dynamics induced
O Artigo 68 do Código Florestal, que prevê que os proprietários ou possuidores de imóveis rurais que realizaram supressão de vegetação nativa, respeitando os limites impostos pela
O Diretor do campus avançado Ubá agradeceu a Pró-reitoria de Ensino deste IF pelo apoio
• A teoria da comunicação é uma teoria que explica como os métodos de comunicação, a questão sutil de comunicação e os processos de influenciar pessoas através da