PRISCILLA MARIA PEREIRA MACIEL
EFEITO DA FRAÇÃO AQUOSA DE
Cissampelos sympodialis
Eichl.
EM ARTÉRIA PULMONAR DE RATO COM HIPERTENSÃO
PULMONAR INDUZIDA POR MONOCROTALINA
JOÃO PESSOA - PB 2015
PRISCILLA MARIA PEREIRA MACIEL
EFEITO DA FRAÇÃO AQUOSA DE
Cissampelos sympodialis
Eichl.
EM ARTÉRIA PULMONAR DE RATO COM HIPERTENSÃO
PULMONAR INDUZIDA POR MONOCROTALINA
Dissertação apresentada ao Programa
de Pós-Graduação em Produtos Naturais e Sintéticos Bioativos da Universidade Federal da Paraíba, como parte dos requisitos para a obtenção do
título de Mestre. Área de Concentração:
Farmacologia.
Orientador: Prof. Dr. Isac Almeida de Medeiros
PRISCILLA MARIA PEREIRA MACIEL
EFEITO DA FRAÇÃO AQUOSA DE
Cissampelos sympodialis
Eichl.
EM ARTÉRIA PULMONAR DE RATO COM HIPERTENSÃO
PULMONAR INDUZIDA POR MONOCROTALINA
Data da aprovação: 27/ 02 / 2015
Banca examinadora
Prof. Dr. Isac Almeida de Medeiros (Orientador)
Prof. Dr. Evandro Leite de Souza (Examinador externo)
Aos meus pais, meus maiores incentivadores. Obrigada pelo
eterno amor e estímulo em todos os momentos da minha
vida, pela bondade, dedicação. Obrigada pela abdicação de
tantos sonhos para que os meus pudessem ser realizados.
Aos meus irmãos Patrícia, Panmella e Antônio Filho pelo
Agradeço inicialmente a Deus, por iluminar e preencher de bênçãos a minha vida, e por me por diante de pessoas maravilhosas que me incentivam e me fazem ser uma pessoa melhor a cada dia.
Aos meus pais, avos, tias e irmãos por todo o carinho, estímulo e oportunidades oferecidas para realização desse sonho.
Ao meu orientador, Prof. Dr. Isac Almeida de Medeiros, com todo respeito, admiração e carinho, pela confiança depositada, incentivo e conhecimentos transmitidos
Ao primeiro orientador, Prof. Dr Robson Veras, pela oportunidade que me proporcionou em ingressar na iniciação científica, por todo incentivo, conhecimentos transmitidos e disponibilidade dispensada sempre quando surgiam dúvidas.
À Thais Porto, que me acompanhou ao longo do mestrado contribuindo para o desenvolvimento deste trabalho, por toda atenção, paciência e carinho que tem comigo.
À Kívia Sales, Maria do Carmo de Alustau, Natalia Tabosa, e Rayanne Araújo, grandes amigas, pelo carinho, companheirismo, conhecimento compartilhado, por estarem sempre dispostas a ajudar, mesmo estando atarefadas, fazendo com que cada dia fosse divertido e enriquecedor.
À Anais Gusmão, aluna de iniciação científica, por todo carinho, amizade e dedicação no desenvolvimento deste trabalho
Aos alunos de iniciação científica, Tays Amanda, Mayara Pessoa, Hassler Cavalcanti, Pablo Ferreira e Arthur Pontes, pela ajuda e amizade
Aos meus amigos do Laboratório de Farmacologia Cardiovascular: Fátima Assunção, George Albuquerque, Lisandra Fernandes, Luara Monteira, Manuelle Jardins, Mônica Almeida, Suênia Maria, Mathânia, Tereza Raquel, Thandy, Valéria Lopes, Walma Vasconcelos.
À minha turma de mestrado, Camila, Ayala, Paula, Vivianne, Tatiana, Tatiane Mota,
Diego, Rayssa, Luciano, Iara, Ináciopelo incentivo e momentos compartilhados.
A Matheus Monteiro e José Crispim Duarte pela amizade, pela força e pela disposição de estar sempre pronto a ajudar.
Aos professores do Programa de Pós-Graduação em Produtos Naturais e Sintéticos Bioativos pelos ensinamentos.
RESUMO
Efeito da Fração Aquosa de Cissampelos sympodialis Eichl. em Artéria Pulmonar de Rato com Hipertensão Pulmonar Induzida por Monocrotalina
MACIEL, P.M.P
Pós-Graduação em Produtos Naturais e Sintéticos Bioativos,
Dissertação de Mestrado,CCS/UFPB (2015)
A hipertensão pulmonar (HP) é caracterizada pelo aumento crônico da pressão arterial pulmonar, remodelamento vascular e hipertrofia do ventrículo direito. O estresse oxidativo é uma das desordens comum na HP. Cissampelos sympodialis
Eichl. é frequentemente utilizada na medicina popular para o tratamento de doenças do aparelho respiratório, reumatismos e artrites. Além disso, muitas dessas atividades têm sido cientificamente comprovadas tornando essa planta um alvo de pesquisa bastante promissor. Nesse contexto, o trabalho teve como objetivo avaliar
o efeito agudo de fração aquosa de Cissampelos sympodialis Eichl. (FAFCS) em
artéria pulmonar de rato saudável, bem como avaliar o potencial da FAFCS em prevenir e/ou melhorar disfunção vascular pulmonar promovida pelo modelo de HP induzido pela monocrotalina (MCT). Em anéis de artéria pulmonar isolada de rato
normotenso, pré-contraídos com fenilefrina (FEN) (1μM), FAFCS (10-γ000μg/mL)
induziu vasorrelaxamento, dependente de concentração, na presença (Emáx=98±2%;
CE50=599μg/mL) e ausência (Emáx=102±2%; CE50 =700μg/mL) do endotélio,
demonstrando que FAFCS produz efeito vasorrelaxante independente dos fatores endoteliais. A HP foi induzida pela injeção subcutânea de MCT (60mg/kg, dose única). Os animais receberam FAFCS via oral (50 ou 100mg/kg/dia), sildenafil ou salina durante 28 dias. O grupo MCT apresentou aumento na PAP (63±5 mmHg) e HVD (0,52±0,03g) em comparação ao grupo controle (PAP=29±2mmHg; HVD=0,28±0,02g). O tratamento com FAFCS 50mg/kg (PAP=46±3mmHg; HVD=0,36±0,04g) e 100mg/kg (30±5mmHg; HVD=0,37±0,05g) ou sildenafil 50mg/kg (32±2mmHg; HVD=0,35±0,03g) apresentaram redução significativa da pressão e hipertrofia ventricular direita em comparação ao grupo MCT. Nos ensaios de reatividade vascular, os animais MCT apresentaram redução da resposta à FEN
(∆contração=0,γ7±0,04g) e diminuição das respostas vasorrelaxantes à ACh e NPS
(Emáx=45±6%) em relação ao grupo controle (FEN, ∆contração=0,86±0,09 g; NPS,
Emáx=96±6%). O tratamento com FAFCS ou sildenafil não reverteu à disfunção
endotelial causada pela exposição a MCT. Entretanto, a resposta à FEN e ao NPS
foram restauradas com o tratamento com FAFCS 50mg/kg (FEN, ∆contração
=0,63±0,04g; Emáx=79±γ%), FAFCS 100mg/kg (FEN, ∆contração=0,77±0,06g; NPS,
Emáx= 85±5 %) e sildenafil (FEN, ∆contração = 0,8±0,08g; NPS, Emáx=72±2%). Além
disso, o tratamento com FAFCS reduziu significativamente os níveis de espécies reativas de oxigênio em cortes de artéria pulmonar, detectado pela fluorescência
emitida pela oxidação do DHE por ânions O2●-. Em conclusão, estes resultados
sugerem que FAFCS promove efeito relaxante independente de endotélio em artéria pulmonar de rato normal. No modelo de HP adotado, o tratamento com FAFCS reduz o estresse oxidativo e restaura a resposta muscular lisa em artéria pulmonar de rato, prevenindo a HP e hipertrofia ventricular direita.
Palavras-chave: Cissampelos sympodiales Eichl. Hipertensão pulmonar. Reatividade
ABSTRACT
Effect of aqueous fraction cissampelos sympodialis Eichl. in rat pulmonary artery with pulmonary hypertension monocrotaline-induced MACIEL, P.M.P
Graduate and Synthetic Bioactive Natural Products, Master-Thesis, CCS / UFPB (2015)
The pulmonary hypertension (PH) is caracterized for the increase chronic pulmonary arterial pressure, vascular remodeling and ventricle right hypertrophy. The oxidative stress is a common disorders in the PH. Cissampelos sympodialis Eichl. is frequently
used in the popular medicine for the treatement of deseases of the tract respiratory, rheumatism and arthritis. Furthermore many of these activites it has been proved scientifically making this plant an promising target. In this context this study had with aim to evaluate the acute effect of aqueous fraction of Cissampelos sympodialis Eichl
(FAFCS) in pulmonary artery of normotensives rats and to avaluate the FAFCS potential in to prevent and/or to improve the pulmonary vascular dysfunction induced for the monocrotaline PH (MCT). In pulmonary artery rings precontracted with phenilefrine (PHE) (1uM) isolated of normotensive rats, FAFCS (10-3000ug/mL) induzed vasorelaxation, concentration dependent, with (MR=98±2%;
EC50=599μg/mL) or without of endothelium (MR=102±2%; EC50 =700μg/mL),
demostrate that FAFCS produces vasorelaxation independent of the endothelial factors. The PH was induced for the subcutaneous injection of MCT (60mg/kg, single dose). The animals receive FAFCS oral via (50 ou 100mg/kg/day), sildenafil or saline during 28 days. The MCT group presented increase of PAP (63±5 mmHg) and HVD (0,52±0,03g) in comparing to the control group (PAP=29±2mmHg; HVD=0,28±0,02g). The treatment with FAFCS 50mg/kg (PAP=46±3mmHg; HVD=0,36±0,04g) and 100mg/kg (30±5mmHg; HVD=0,37±0,05g) or sildenafil 50mg/kg (32±2mmHg; HVD=0,35±0,03g) showed a significant reduction in pressure and right ventricular hypertrophy compared to the MCT group. In the tests of vascular reactivity the MCT
animals showed reduction of the response to PHE (∆ contraction=0,γ7±0,04g) and
decrease of the reponse vasorelaxation to ACh and NPS (MR=45±6%) in relation to
the control group (PHE, ∆ contraction=0,86±0,09 g; NPS, MR=96±6%). The
treatment with FAFCS or sildenafil not reversed to endothelial dysfunction caused for the exposition to MCT. However the effect to PHE and the NPS were restored with
FAFCS 50mg/kg (PHE, ∆contraction =0,6γ±0,04g; MR=79±γ%), FAFCS 100mg/kg (PHE, ∆contraction=0,77±0,06g; NPS, MR= 85±5 %) e sildenafil (PHE, ∆contraction
= 0,8±0,08g; NPS, MR=72±2%). Furthermore FAFCS reduced significantly the levels of reactive oxygen species in the DHE staining in pulmonary artery. In conclusion these results suggests that FAFCS promotes relaxant effect endothelium independent in pulmonary artery of normotensive rats. In PH monocrotaline-induced the treatment with FAFCS reduced the oxidative stress and restore the damage on smooth muscle in pulmonary artery of rat and hypertrophy right ventricle induced by monocrotaline.
Keywords: Cissampelos sympodialis Eichl, pulmonary hipertension; vascular
LISTA DE FIGURAS
Figura 1: Foto da espécie Cissampelos sympodialis Eichl... 26
Figura 2: Representação esquemática da cuba para órgãos isolados. ... 35
Figura 3: Foto do sistema para banho de órgãos isolados ... 35
Figura 4: Representação do protocolo de verificação da viabilidade do tecido muscular e da integridade do endotélio vascular. ... 36
Figura 5: Representação esquemática do protocolo experimental para avaliação do
efeito da FAFCS (10 – γ000 μg/mL) em anéis de artéria extrapulmonar de rato
saudável, pré-contraídos com FEN (1 μM). ... 37
Figura 6: Representação esquemática dos grupos experimentais e esquema de tratamento dos animais ... 39
Figura 7: Sistema de aquisição de dados para medida de PAP em ratos anestesiados. ... 40
Figura 8: Representação esquemática do protocolo da resposta contracturante ao agonista, FEN em anéis de artéria extrapulmonares, isoladas de ratos. ... 41
Figura 9: Representação esquemática dos protocolos de resposta relaxante aos agonistas, ACh ou NPS, em anéis de artéria extrapulmonares isoladas de ratos pré-contraídas com FEN. ... 42
Figuras 10: Registros originais representativos das respostas relaxantes a FAFCS
(10 – 3000 μg/mL) em anéis pré-contraídos com FEN (1 μM), na presença, E + (A)
ou ausência, E - (B) do endotélio vascular. ... 45
Figura 11: Registro original representativo da PAP no dia 28º seguinte à injeção subcutânea de monocrotalina ou salina. ... 47
Figura 12: Registro original representativo da curva concentração-resposta para a
FEN (10-10– 10-5 M) em anéis de artéria extrapulmonar isolada de rato, após 28 dias
da injeção subcutânea de MCT ou salina. ... 49
Figura 13: Registro original representativo da curva concentração-resposta para a
ACh (10-10 – 10-5 M) em anéis de artéria extrapulmonar isolada de rato, pré-
Figura 14: Registro original representativo da curva concentração-resposta para o
NPS (10-10– 10-5 M) em anéis de artéria extrapulmonar isolada de rato, após 28 dias
LISTA DE GRÁFICOS
Gráfico 1: Curvas concentração-resposta para o efeito relaxante induzido pela
FAFCS (10 –γ000 μg/mL) em anéis de artéria extrapulmonares isolada de ratos, na
presença (●) ou ausência (○) do endotélio, pré-contraídos com FEN (1 μM) (n = 7 e
6, respectivamente). ... 46
Gráfico 2: FAFCS previne o desenvolvimento da hipertensão pulmonar. Representação gráfica da pressão arterial pulmonar (PAP) 28º dia, seguinte à injeção de salina (grupo controle) ou MCT, para os grupos MCT, MCT + FAFACS 50
mg/kg, MCT + FAFCS 100 mg/kg e sildenafil 50 mg/kg. ... 47
Gráfico 3: FAFCS previne a hipertrofia ventricular direita (HVD) em ratos com hipertensão pulmonar. A HVD foi determinada pela razão entre o peso do ventrículo direito e peso do ventrículo esquerdo mais septo (VD/DE+S) 28º dia, seguinte a injeção de salina (grupo controle) ou MCT, para os grupos MCT, MCT + FAFACS 50
mg/kg, MCT + FAFCS 100 mg/kg e sildenafil 50 mg/kg. ... 48
Gráfico 4: Efeito do tratamento com FAFCS sobre a reatividade vascular de artéria
pulmonar. Curva concentração-resposta para a FEN (10-10 – 10-5 M) em anéis de
artéria extrapulmonares de ratos, no 28º dia, após a indução da HP com MCT (60
mg/kg). ... 50
Gráfico 5: Efeito do tratamento com FAFCS sobre a reatividade vascular de artéria
pulmonar. Curva concentração-resposta para a ACh (10-10 – 10-5 M) em anéis de
artéria extrapulmonares de ratos 28 dias após a indução da HP com MCT (60
mg/kg). ... 52
Gráfico 6: Efeito do tratamento com FAFCS sobre a reatividade vascular de artéria
artéria extrapulmonares de ratos 28 dias após a indução da HP com MCT (60
mg/kg). ... 54
Gráfico 7: O tratamento com FAFCS previne o aumento da produção de ROS em
LISTA DE ABREVIATURAS
ACh: Acetilcolina
AP: Artéria pulmonar
ATII: Angiotensina II
cAMP: monofosfato de adenosina cíclico
cGMP: monofosfato de guanosina cíclico
CE50: Concentração responsável por 50% do efeito máximo
CML: Célula muscular lisa
DHE: Di-hidroetídeo
DMSO: Dimetilfulfóxido
EDHF: Fator hiperpolarizante derivado do endotélio
Emáx: Efeito máximo
eNOS: sintase do óxido nítrico endotelial
NPS: Nitroprussiato de sódio
Erk: Cinase ativada por sinal extracelular
ET-1: Endotelina 1
FAFCS: Fração aquosa do extrato etanólico das folhas de Cissampelos sympodialis
FEN: Fenilefrina
HP: Hipertensão pulmonar
HVD: Hipertrofia ventricular direita
IFN- : Interferon gama
IgE: Imunoglogulina E
IL: Interleucina
MAPK: Proteína cinase ativada por mitógeno
MCT: Monocrotalina
MMP: Metaloproteinase
NADPH oxidase: Nicotinamida adenina dinucleotídeo fosfato-oxidase
NO: Óxido nítrico
PAP: Pressão arterial pulmonar
PBS: Solução tampão fosfato
PDGF: Fator de crescimento derivados de plaquetas
PGI2: Prostaciclina
PKA: Proteina cinase dependente de cAMP
PKG: Proteína cinase dependente de cGMP
PSVD: Pressão sistólica do ventrículo direito
ROS: Espécies reativas de oxigênio
RVP: Resistência vascular pulmonar
sGC: Ciclase de guanilil solúvel
VD: Ventrículo direito
VE + S: Ventrículo esquerdo mais septo
TGF-β: Fator de crescimento de transformação
TNF-α: Fator de necrose tumoral α
SUMÁRIO
1 INTRODUÇÃO ... 19
1.1. CONSIDERAÇÕES SOBRE AHIPERTENSÃO PULMONAR ... 19
1.2. MODELO DE HP INDUZIDO PELA MONOCROTALINA ... 21
1.3 TRATAMENTOS UTILIZADOS NA HP ... 24
1.4. Cissampelos sympodialis Eichl. ... 25
2 OBJETIVO ... 30
2.1 OBJETIVO GERAL ... 30
2.2 OBJETIVOS ESPECÍFICOS ... 30
3 MATERIAL E MÉTODOS ... 32
3.1 ANIMAIS ... 32
3.2 SUBSTÂNCIA TESTE ... 32
3.3 SUBSTÂNCIAS E MEIOS UTILIZADOS ... 32
3.4 SOLUÇÕES NUTRITIVAS ... 33
4 MÉTODOS ... 34
4.1 Triagem farmacológica inicial de FAFCS em artéria pulmonar de ratos normotensos ... 34
4.1.1 Avaliação do efeito vasorrelaxante da FAFCS em anéis de artéria pulmonar pré-contraídas com FEN ... 36
4.2 ENSAIOS FARMACOLÓGICOS IN VIVO ... 37
4.2.1 Modelo experimental de HP ... 37
4.2.2 Grupos experimentais e protocolo de tratamento ... 38
4.2.3 Avaliação dos efeitos de FAFCS no modelo de HP induzida por MCT ... 39
4.2.3.1 Medida direta da PAP em ratos ... 39
4.2.3.2 Medida da hipertrofia do ventrículo direito ... 40
4.3 ENSAIOS FARMACOLÓGICOS IN VITRO ... 40
4.3.1 Ensaios farmacológicos de reatividade vascular utilizando anéis de artéria pulmonar isolada de ratos com HP induzida por monocrotalina ... 40
4.3.1.2 Avaliação da resposta relaxante dos anéis de artéria pulmonar, isolada de
rato, à ACh e ao NPS ... 42
4.4 AVALIAÇÃO DA PRODUÇÃO DE ÂNIONS SUPERÓXIDO (O2●-) EM VASOS PULMONARES POR MICROSCOPIA DE FLUORESCÊNCIA ... 42
4.5 ANÁLISE ESTATÍTICA ... 43
5 RESULTADOS ... 45
5.1 ESTUDOS FARMACOLÓGICOS IN VITRO ... 45
5.1 Triagem farmacológica de FAFCS em artéria pulmonar de ratos normotensos .. 45
5.1.1 Influencia do endotélio sobre o efeito vasorrelaxante induzido pela FAFCS .... 45
5.2 ESTUDOS FARMACOLÓGICOS IN VIVO ... 46
5.2.1 Efeito da FAFCS sobre a PAP de ratos com HP induzida por MCT ... 46
5.2.1 Efeito da FAFCS sobre hipertrofia do ventrículo direito de ratos com HP induzida por MCT ... 48
5.2.2 Efeito do tratamento com FAFCS sobre a reatividade vascular em anéis de artéria pulmonar de ratos com HP induzida por MCT ... 49
5.2.2.1 Avaliação da resposta contrátil à FEN em anéis de artéria pulmonar ... 49
5.2.2.2 Avaliação da resposta relaxante à ACh em anéis de artéria pulmonar frente a contração com FEN ... 51
5.2.2.3 Avaliação da resposta relaxante ao NPS em anéis de artéria pulmonar frente à contração com FEN ... 52
5.3 EFEITO DE FAFCS SOBRE O ESTRESSE OXIDATIVO INDUZIDO PELO MODELO DE HIPERTENSÃO PULMONAR INDUZIDO POR MONOCROTALINA 54 6 DISCUSSÃO ... 57
7 CONCLUSÃO ... 65
8 PERSPECTIVAS... 67
Efeito da fração aquosa de Cissampelos sympodialis Eichl. em artéria pulmonar de rato com hipertensão pulmonar induzida por monocrotalina 19
1 INTRODUÇÃO
1.1. CONSIDERAÇÕES SOBRE AHIPERTENSÃO PULMONAR
A hipertensão pulmonar (HP) é uma doença progressiva das artérias pulmonares, caracterizada por um aumento sustentado da pressão arterial pulmonar (PAP) seguido de remodelamento vascular. Apresenta-se como uma condição clínica de etiologia variada, com elevação dos níveis da PAP média maior ou igual a 25 mmHg no repouso (ARCHER;WEIR ;WILKINS, 2010; GROTH et al., 2014).
Dada a multiplicidade das causas da HP, informações sobre incidência, prevalência, história natural e prognóstico da doença ainda são escassos. Em um estudo realizado na França, demonstrou-se uma estimativa da prevalência e incidência de 15 casos/milhão de habitantes e 2,4 casos/milhão de habitantes anualmente, respectivamente (HUMBERT et al., 2006). Outro estudo realizado em oito centros de HP no Reino Unido e Irlanda revelaram uma incidência estimada de 1,1 casos/ milhão por ano e prevalência de 6,6 casos por milhão de habitantes no período de 2001 a 2009 (LING et al., 2012). No Brasil, não existem dados disponíveis sobre a prevalência da HP (ROMANO, 2010).
A HP pode ocorrer associada a uma variedade de condições médicas subjacentes, caracterizando-se como uma doença que afeta exclusivamente a circulação pulmonar. O sistema de classificação atual, proposto em 2013, durante o V Simpósio Mundial de Hipertensão Pulmonar, realizado em Nice na França, agrupa as diferentes formas de hipertensão pulmonar baseado nas similaridades entre sua fisiopatologia, características hemodinâmicas e resposta ao tratamento (SIMONNEAU et al., 2009; SIMONNEAU et al., 2013). Atualmente, cinco grupos principais de hipertensão pulmonar são reconhecidos: (1) hipertensão arterial pulmonar (HAP); (2) hipertensão pulmonar devido à doença do coração esquerdo; (3) hipertensão pulmonar devido à doença pulmonar crônica e/ou hipóxia; (4) hipertensão pulmonar tromboembólica crônica; e (5) hipertensão pulmonar devido a mecanismos multifatoriais não esclarecidos (SIMONNEAU et al., 2013).
Efeito da fração aquosa de Cissampelos sympodialis Eichl. em artéria pulmonar de rato com hipertensão pulmonar induzida por monocrotalina 20
hiperplasia e proliferação das células musculares lisas, levando ao seu espessamento e aumento do tônus vascular pulmonar. Esses processos conduzem a um estado de vasoconstrição sustentada, resultando em aumento da resistência vascular pulmonar (RVP) e elevação da PAP, bem como diminuição da complacência vascular (ABMAN ;IVY, 2011; O'CALLAGHAN ;HUMBERT, 2012; DUONG-QUY et al., 2013).
A elevação dos níveis pressóricos na circulação pulmonar culmina em aumento da pós-carga sobre o ventrículo direito (VD), resultando em hipertrofia ventricular direita (HVD) com posterior disfunção cardíaca direita, evidenciada pela redução do débito cardíaco (ABMAN ;IVY, 2011; O'CALLAGHAN ;HUMBERT, 2012; DUONG-QUY et al., 2013). A redução progressiva do débito cardíaco resulta em intolerância ao exercício, falta de ar, edema periférico, fadiga, fraqueza, angina, distensão abdominal podendo levar o paciente a óbito (GALIÈ et al., 2009; TABIMA;FRIZZELL ;GLADWIN, 2012).
O desenvolvimento da HP resulta da interação de processos complexos e heterogêneos de múltiplas anomalias genéticas, moleculares e humorais, apresentando uma manifestação final de remodelamento vascular, no qual as células endoteliais, musculares lisas e os fibroblastos desempenham um papel fundamental (MANDEGAR et al., 2004; ZAPATA-SUDO et al., 2012). Os fatores que contribuem para essas alterações estruturais e hemodinâmicas da HP estão relacionados ao desequilíbrio na produção e/ ou sinalização anormal de mediadores vasoconstritores e vasodilatadores, oxidantes e antioxidantes, ativadores e inibidores do crescimento e migração celular, mediadores pró-inflamatórios, anti-inflamatórios e pró-trombóticos (STENMARK ;FRID, 2011).
Efeito da fração aquosa de Cissampelos sympodialis Eichl. em artéria pulmonar de rato com hipertensão pulmonar induzida por monocrotalina 21
1.2. MODELO DE HP INDUZIDO PELA MONOCROTALINA
A MCT é um alcaloide pirrolizidínico tóxico, encontrado em plantas do gênero Crotalaria. O modelo de HP por MCT foi introduzido há mais de 50 anos, quando se
observou que a ingestão oral repetida de sementes de Crotolaria spectabilis ou MCT
causava o desenvolvimento progressivo da HP em ratos de laboratório (LALICH ;MERKOW, 1961; KAY;HARRIS ;HEATH, 1967).
Atualmente, é utilizada uma única injeção de MCT, via intraperitoneal ou subcutânea, a qual é suficiente para induzir rapidamente à doença vascular pulmonar na ausência de doenças cardíaca e pulmonar intrínsecas, sugerindo, assim, o seu valor como um modelo animal de HP. A MTC é biotransformada no fígado a um metabólito ativo, a dihidromonocrotalina (DHM), que é inteiramente responsável pelo efeito citotóxico pulmonar, tendo como alvo diversas proteínas e peptídeos do endotélio vascular (HUXTABLE, 1990; ZAPATA-SUDO et al., 2012).
Apesar de ser um modelo experimental utilizado desde 1961 (WILSON et al., 1992), o mecanismo exato pelo qual a MCT provoca a HP ainda não é totalmente esclarecido. Estudos demonstram que a exposição à MCT induz, inicialmente, danos sobre a vasculatura pulmonar em um intervalo de 24 a 48 horas da sua administração. Estes danos são caracterizados pelo aumento da permeabilidade capilar, edema intersticial e alveolar, acúmulo de células inflamatórias e modificações dos pneumócitos. Em resposta a essas mudanças, ocorre degeneração endotelial, hiperplasia e hipertrofia da musculatura lisa medial e edema da adventícia. Isto leva ao aumento da resistência vascular e sobrecarga de pressão ventricular direita, com consequente desenvolvimento da HP e hipertrofia do ventrículo direito (HUXTABLE, 1990; SCHULTZE et al., 1994; GOMEZ-ARROYO et al., 2012).
Essas alterações são mediadas por modificações que podem ocorrer tanto em nível de plaquetas, com elevação da produção e libertação de serotonina, como em nível de diferentes estruturas da parede arterial, como a camada de células endoteliais, musculares e adventícia (SUBIAS et. al., 2010).
No endotélio, observa-se uma redução da síntese de substâncias
Efeito da fração aquosa de Cissampelos sympodialis Eichl. em artéria pulmonar de rato com hipertensão pulmonar induzida por monocrotalina 22
que ocorre uma elevação de elementos vasoconstrictores como o tromboxano A2
(TxA2) e endotelina-1 (ET-1) (BUDHIRAJA;TUDER ;HASSOUN, 2004; WHARTON et
al., 2005; TABIMA;FRIZZELL ;GLADWIN, 2012; WILKINS, 2012).
Entre os fatores vasoativos, o NO é o principal mediador envolvido na regulação do tônus vascular e inibição da proliferação das células musculares lisas na circulação pulmonar (BUDHIRAJA;TUDER ;HASSOUN, 2004; WHARTON et al., 2005; TABIMA;FRIZZELL ;GLADWIN, 2012; WILKINS, 2012). O NO é sintetizado no endotélio pela ação catalítica da isoforma endotelial da enzima NO sintase (eNOS). O NO age, nas células do músculo liso vascular, ativando a enzima ciclase de
guanilil solúvel (sGC), a qual catalisa a formação do γ’,5’- monofosfato cíclico de ganosina (cGMP) (KRUUSE et al., 2001). Uma vez produzido, o cGMP atua em diversos alvos, tais como a proteínas cinases dependentes de cGMP (PKG). Esta, após ser ativada, atua fosforilando proteínas-alvo no músculo liso, mediando o
relaxamento vascular (KLEMENSKA; BERĘSEWICZ, β009; FRANCIS; BUSCH;
CORBIN, 2010).
As alterações induzidas pela ação da MCT nas células musculares da camada média, por sua vez, envolvem a diminuição da expressão dos canais de potássio dependentes da voltagem, bem como um aumento da expressão e atividade da fosfodiesterase 5 (PDE-5) e redução da expressão da sGC e PKG (CHUNG et al., 2010).
Na camada adventícia ocorre um aumento na síntese de citocinas pró-inflamatórias e de proteínas da matriz extracelular (colágeno, elastina, tenascina-C e fibronectina), demonstrando uma hiperatividade de elastases e metaloproteases (MMP). Estas enzimas podem degradar diversos componentes da matriz extracelular, e conduzir a uma proliferação de células musculares lisas que conduzem ao remodelamento vascular (SUBIAS;MIR ;SUBERVIOLA, 2010).
O dano vascular provocado pela exposição à MCT gera uma resposta inflamatória induzindo a liberação de citocinas e fatores de crescimento, tais como: fator de crescimento de transformação beta (TGF- ); fator de crescimento derivado
de plaquetas (PDGF); interleucina 6 (IL-6); e fator de necrose tumoral alfa (TNF-α
Efeito da fração aquosa de Cissampelos sympodialis Eichl. em artéria pulmonar de rato com hipertensão pulmonar induzida por monocrotalina 23
superóxido (O2●-), via aumento da expressão e atividade da enzima NADPH oxidase
(TOUYZ, 2004; VEIT et al., 2013).
O aumento da bioatividade dos ânions O2●- leva à disfunção endotelial;
migração e crescimento das células musculares lisas; infiltração de células inflamatórias; e aumento da deposição de proteínas da matriz extracelular, importantes fatores relacionados à injúria vascular na HP (TOUYZ, 2004; VEIT et al., 2013). Um mecanismo proposto para o aumento da migração celular está relacionado à expressão aumentada de MMP via a ativação de MAPK (Erk1/2)-dependente de espécies reativas de oxigênio (ROS) (VEIT et al., 2013).
O aumento de ROS também pode diminuir os efeitos vasodilatadores e antiproliferativos da via NO/cGMP. A inativação do NO ocorre pela reação com
ânions O2●-, desacoplamento da eNOS, redução da expressão e atividade da sCG, e
aumento da expressão e atividade da PDE-5 nos vasos pulmonares (FARROW FARROW et al., 2012; KLINGER;ABMAN ;GLADWIN, 2013). No músculo liso
vascular, os ânions O2●- tem como alvos as enzimas sCG e PDE-5. O sítio ativo da
sGC pode ser modificado pelo estresse oxidativo, reduzindo a resposta ao NO (WOLIN;AHMAD ;GUPTE, 2005; FARROW et al., 2010). Estas alterações contribuem para o aumento da resistência vascular pulmonar e remodelamento patológico dos vasos pulmonares durante o desenvolvimento da HP.
Estudos demonstram que a elevação dos níveis intracelulares de ânions O2●
-aumenta a atividade e expressão da PDE-5 em células musculares lisas de artéria pulmonar (FARROW et al., 2008; FARROW et al., 2012). A enzima PDE-5 hidrolisa especificamente o cGMP, fato que contribui para o aumento da resistência vascular pulmonar e remodelamento patológico dos vasos pulmonares durante o desenvolvimento da HP (SCHERMULY et al., 2004).
Evidencias experimentais indicam que os processos moleculares associados às mudanças estruturais dos vasos pulmonares, no modelo HP induzido por MCT, refletem em alterações funcionais na responsividade a agentes vasodilatadores e contracturantes durante a evolução da doença.
Efeito da fração aquosa de Cissampelos sympodialis Eichl. em artéria pulmonar de rato com hipertensão pulmonar induzida por monocrotalina 24
contratilidade de artérias pulmonares (extra e intrapulmonares) aos agentes contracturantes, angiotensina II (ATII), cloreto de potássio e noradrenalina, além da redução do relaxamento dependente e independente de endotélio, mediado pela acetilcolina (ACh) e isoproterenol, respectivamente. Observações semelhantes foram feitas por Mam (2010), que avaliou a responsividade à fenilefrina, acetilcolina e nitroprussiato de sódio (NPS) em vasos mesentéricos e pulmonares após 4 semanas da exposição a MCT, mostrando que as respostas contráteis e relaxantes também foram reduzidas apenas nos vasos pulmonares.
1.3 TRATAMENTOS UTILIZADOS NA HP
Atualmente, os fármacos utilizados para o tratamento da HP têm como alvo vias de sinalização específicas, que no processo da doença estão desreguladas como as vias do NO, prostaciclinas e endotelinas (O'CALLAGHAN et al., 2011).
No Brasil, de acordo com a Portaria nº 35, de 2014, que estabelece os protocolos clínicos e diretrizes terapêuticas da HP, quatro classes farmacológicas estão disponíveis para o tratamento específico da HP, os bloqueadores de canais de cálcio, inibidores de PDE-5, análogos das prostaciclinas e os antagonistas dos receptores de endotelina. A instituição do tratamento é fundamentada em alguns fatores como conhecimento sobre o fármaco, resposta terapêutica e perfil de efeitos adversos (BRASIL, 2014).
Entre os fármacos utilizados para tratar a HP, os inibidores de canais de cálcio são predominantemente usados, a exemplo do nifedipino e anlodipino. Este grupo compõe o tratamento de escolha para pacientes com resposta positiva ao teste de vasorreatividade pulmonar (resposta ao teste vasodilatador verificado na avaliação hemodinâmica). Nos casos em que os objetivos para o tratamento da HP não foram atingidos deve ser indicado o uso de iloprosta ou sildenafil, ou os antagonistas dos receptores de endotelina (bosetana e ambrisentana) (BRASIL, 2014).
Efeito da fração aquosa de Cissampelos sympodialis Eichl. em artéria pulmonar de rato com hipertensão pulmonar induzida por monocrotalina 25
Estudos que avaliaram a eficácia do sildenafil em paciente com HP evidenciaram que além da melhora dos parâmetros hemodinâmicos também foi observado o aumenta da tolerância ao exercício e da qualidade de vida dos mesmos (BHARANI et al., 2003; SASTRY et al., 2004; SINGH et al., 2006; PEPKE-ZABA et al., 2008; RUBIN et al., 2011).
Apesar das alternativas terapêuticas, a HP continua sendo uma doença progressiva, crônica e incurável, uma vez que até o momento não existe uma droga que seja completamente eficaz na reversão dos efeitos deletérios da doença. Sendo assim, substâncias que promovam a prevenção ou reversão dos mecanismos que desencadeiam à HP são de grande importância para a sociedade.
Os benefícios à saúde de diferentes compostos naturais têm sido associados às suas ações como antioxidantes e inibidores de reações de peroxidação (STOCLET;SCHINI-KERTH, 2011). Diversos produtos naturais têm sido intensivamente estudados quanto à sua influência para a ação benéfica sobre o sistema cardiovascular, incluindo os efeitos diretos nas células vasculares (SCHINI-KERTH et al., 2011). Estudos envolvendo modelos animais de HP vêm sendo realizados no Laboratório de Farmacologia Cardiovascular. Anteriormente, foi
demonstrado que o extrato de C. sympodialis reduziu de forma significante a
hipertensão pulmonar induzida por MCT de maneira semelhante ao sildenafil, droga padrão utilizada para o tratamento da HP. Neste mesmo trabalho, também foi
demonstrado que a terapia combinada com extrato de C. sympodialis e sildenafil não
produziu efeito adicional na melhora da HP, quando comparados com o uso de C.
sympodialis ou sildenafil isoladamente (MAGALHÃES, 2010).
1.4. Cissampelos sympodialis Eichl.
A espécie C. sympodialis Eichl, tem sido estudada há mais de vinte anos no
Programa de Pós-graduação em Produtos Naturais e Sintético Bioativos (PgPNSB),
devido as suas propriedades medicinais. A C. sympodialis é encontrada apenas na
América do Sul, especificamente no Brasil, ocorrendo principalmente em áreas de semiárido (RHODES, 1970; SEMWAL et al., 2014) (Figura 1). Conhecida
Efeito da fração aquosa de Cissampelos sympodialis Eichl. em artéria pulmonar de rato com hipertensão pulmonar induzida por monocrotalina 26
raízes são empregadas na medicina popular e indígena para o tratamento de doenças do aparelho respiratório (asma, bronquite, gripe), reumatismos e artrites (BARBOSA FILHO;AGRA ;THOMAS, 1997; AGRA;FREITAS ;BARBOSA-FILHO, 2007).
Figura 1: Foto da espécie Cissampelos sympodialis Eichl.
Fonte: CAVALCANTI (2014)
Estudos fitoquímicos demonstraram que essa espécie é rica em alcaloides.
Alguns desses compostos foram isolados e identificados: warifteína (DE F CǑRTES
et al., 1995), metilwarifteina (BARBOSA FILHO;AGRA ;THOMAS, 1997), laurifolina, simpodialina (ALENCAR, 1994), milonina (DE FREITAS et al., 1995), roraimina, liriodenina (DE LIRA et al., 2002) e desmetilroraimina (MARINHO, 2011).
Estudos com o extrato hidroalcoólico das folhas de C. sympodialis
identificaram a presença de compostos fenólicos (taninos e flavonoides) e alcaloides (CAVALCANTI, 2014). Os alcaloides foram identificados como compostos majoritários, sendo a warifteína a principal substância bioativa (THOMAS et al., 1997b; ARAGÃO;FILHO ;MACÊDO, 2001; OLIVEIRA JÚNIOR et al., 2011). Além da warifteína, outros alcaloides bioativos foram isolados nesse extrato como a metilwarifteína e milonina. Recentemente, publicou-se um registro de patente do
processo para produção do extrato etanólico de C. sympodialis com concentração
Efeito da fração aquosa de Cissampelos sympodialis Eichl. em artéria pulmonar de rato com hipertensão pulmonar induzida por monocrotalina 27
farmacêuticas e uso de composições obtidas. O produto deste processo resulta em um extrato padronizado, com atividade anti-inflamatória e atividade farmacológica em doenças do aparelho respiratório (INPI, 2015).
Estudos com extratos ou frações, bem como para os compostos isolados de
C. sympodialis, têm caracterizado uma variedade de atividades farmacológicas,
como: atividade espasmolítica (DE FREITAS et al., 1996), antidepressiva (ALMEIDA et al., 1998), broncodilatadora (THOMAS et al., 1997a), antidiarreica (SALES, 2014), analgésica (OLIVEIRA JÚNIOR et al., 2011), anti-inflamatória, antialérgica (BEZERRA-SANTOS et al., 2006; BEZERRA-SANTOS et al., 2012) e atividade relaxante em corpo cavernoso de rato (ALVES, 2012).
Avaliações toxicológicas utilizando a fração aquosa do extrato hidroalcoólico de C sympodialis (FAFCS) indicam a baixa toxicidade dessa forma utilizada em
ensaios biológicos. Ensaios de toxicidade aguda em camundongos, ratos e cães utilizando a FAFCS, demonstraram que a administração oral de doses de até 5000 mg/kg não resultou em mortes dos animais (DINIZ, 2000). Ensaios de toxicidade subaguda em cães, utilizando uma dose de 45 mg/kg/dia (5 vezes a dose utilizada pelos seres humanos) durante 4 semanas, não mostrou qualquer efeito sobre os parâmetros bioquímicos e hematológicos (hemograma e plaquetas) (DINIZ et al., 2002). Nos ensaios de toxicidade crônica em ratos, a administração das doses 9 mg/kg, 45 mg/kg e 225 mg/kg não alterou os parâmetros hematológicos. Entretanto, foi observado o aumento das enzimas hepáticas (ALT e AST) nos grupos tratados com as doses de 45 mg/kg e 225 mg/kg, a qual foi revertida após 15 e 30 dias da suspensão do tratamento (DINIZ, 2000).
Outro estudo, envolvendo ratas prenhas demonstrou que o tratamento com FAFCS nas doses de 9 mg/kg/dia (baseada no uso popular); 45 mg/kg/dia e 225 mg/kg/dia durante o período gestacional não alterou a fertilidade ou teve efeitos teratogênicos ao nascimento e desenvolvimento dos filhotes. Estes achados confirmam a segurança da administração de FAFCS em doses terapêuticas por via oral durante o período gestacional de ratas (MAIOR et al., 2003).
Efeito da fração aquosa de Cissampelos sympodialis Eichl. em artéria pulmonar de rato com hipertensão pulmonar induzida por monocrotalina 28
níveis de IL-10 e IFN-y (interferon- ) em células de baço de camundongo alérgico e
elevação dos níveis apenas de IL-10 em culturas de macrófagos (PIUVEZAM et al., 1999; BEZERRA-SANTOS et al., 2004).
BEZERRA-SANTOS et al. (2012) também demonstraram que C. sympodialis
e seu composto isolado, a warifteina inibem a hiperreatividade das vias aéreas e o remodelamento pulmonar causados pela asma por um mecanismo dependente de IL-13. Além disso, também foi demonstrado que a fração aquosa do extrato hidroalcoólico (FAFCS) inibiu a degranulação de neutrófilos humanos, associada a um aumento na atividade da proteína cinase A dependente de cAMP (PKA) nessas células (THOMAS;SELAK ;HENSON, 1999).
Ensaios in vitro demonstraram que FAFCS inibe o tônus espontâneo de
traquéia de cobaia, e que este efeito é potencializado na presença do inibidor de PDE (3-isobutil-l-metilxantina). Entretanto, não têm sua resposta alterada na presença dos inibidores da eNOS (L-NAME) ou sGC (azul de metileno) (THOMAS et al., 1997a). Estudos subsequentes, que melhor caracterizaram este efeito, demonstraram que a inibição do tônus espontâneo de traquéia é mediado por meio da inibição de PDE específicas para os nucleotídeos cíclicos, cAMP e cGMP. Nesse mesmo estudo, foi mostrado que a FAFCS aumenta os níveis de cGMP e cAMP em cultura de células de músculo liso de traquéia (THOMAS et al., 1997b).
Recentemente, foi demonstrado que FAFCS induz o relaxamento em tiras de corpos cavernosos de ratos, e que este efeito não é alterado na presença do inibidor da eNOS (L-NAME), entretanto é reduzido na presença do inibidor da sGG (ODQ) e PKG (KT-5823). Além disso, FAFCS induziu o aumento dos níveis de cGMP nesse órgão, demonstrando que seu efeito relaxante parece ser mediado pela ativação da via GC/cGMP/PKG. No mesmo estudo, FAFCS também demonstrou melhorar a função erétil de ratos em modelo de disfunção erétil induzido por estreptozotocina (ALVES, 2012).
Efeito da fração aquosa de Cissampelos sympodialis Eichl. em artéria pulmonar de rato com hipertensão pulmonar induzida por monocrotalina 29
Efeito da Fração Aquosa de Cissampelos sympodialis EICH. em Artéria Pulmonar de Rato com Hipertensão Pulmonar Induzida por Monocrotalina 30
2 OBJETIVOS
2.1 OBJETIVO GERAL
Avaliar o efeito da fração aquosa do extrato etanólico de Cissampelos
sympodialis Eichl. (FAFCS) sobre a disfunção vascular associada ao modelo
experimental de hipertensão pulmonar induzido por monocrotalina.
2.2 OBJETIVOS ESPECÍFICOS
Avaliar o potencial de FAFCS em prevenir a instalação da hipertensão
pulmonar induzida por monocrotalina.
Investigar o efeito de FAFCS sobre as alterações da função vascular,
relacionadas a HP por meio da:
Respostas vasoconstritoras à fenilefrina em artéria pulmonar de ratos;
Respostas relaxante dependente e independente de endotélio vascular;
Determinação do potencial anti- oxidante, por meio da medida de
Efeito da Fração Aquosa de Cissampelos sympodialis Eichl. em Artéria Pulmonar de Rato com Hipertensão Pulmonar Induzida por Monocrotalina 32
3 MATERIAL E MÉTODOS
3.1 ANIMAIS
Foram utilizados, neste trabalho, ratos normotensos da linhagem Wistar (Rattus novergicus albinus), com idade de 12 semanas (250- 270 g) e de 8 a 9
semanas (190-220 g) para os protocolos de indução da HP. Os animais foram
fornecidos pelo biotério “Prof. George Thomas” do CBiotec, da Universidade Federal
da Paraíba. Os animais foram mantidos em gaiolas sob condições controladas de temperatura, umidade e ciclo claro-escuro de 12 horas, tendo livre acesso a água e ração. Todos os experimentos desenvolvidos neste estudo foram aprovados pelo Comitê de Ética em Uso Animal (CEUA) da UFPB, com certidão nº 0103/14.
3.2 SUBSTÂNCIA TESTE
A FAFCS foi cedida pelo Prof. Dr. José Maria Barbosa Filho, do Programa de Pós-Graduação em Produtos Naturais e Sintéticos Bioativos-UFPB.
Para a realização dos ensaios farmacológicos in vitro, a FAFCS foi
solubilizada em cremofor e diluída em água destilada. Para a obtenção das concentrações desejadas e realização dos protocolos experimentais, a concentração
de cremofor não ultrapassou 0,03% v/v. Já para os protocolos in vivo, a FAFCS foi
solubilizada em cremofor e diluída em solução salina. O veículo não promoveu efeito sobre os parâmetros avaliados (dados obtidos em experimentos anteriores em nosso laboratório). Apesar da solubilidade da fração em água, a dissolução com o agente emulsificante ocorre de modo mais homogêneo, evitando a formação de qualquer precipitado.
3.3 SUBSTÂNCIAS E MEIOS UTILIZADOS
Efeito da Fração Aquosa de Cissampelos sympodialis Eichl. em Artéria Pulmonar de Rato com Hipertensão Pulmonar Induzida por Monocrotalina 33
sódio (NPS) e monocrotaliana (crotalina). Todos as substâncias foram obtidos da Sigma-Aldrich Brasil Ltda (São Paulo-SP, Brasil).
As substâncias foram dissolvidas em água destilada, exceto a monocrotalina, que foi dissolvida em HCl 1 M e o DHE que foi dissolvido em DMSO e diluído em água destilada. As soluções foram mantidas a -20°C e, retiradas imediatamente antes dos experimentos.
3.4 SOLUÇÕES NUTRITIVAS
Para a preparação das soluções nutritivas foram utilizadas as seguintes substâncias: cloreto de sódio (NaCl), cloreto de potássio (KCl), cloreto de cálcio
(CaCl2), sulfato de magnésio (MgSO4), glicose (C6H12O6) bicarbonato de sódio
(NaHCO3) e fosfato de potássio (NaH2PO4). Todos estes sais foram obtidos da
VETEC. Para o preparo da solução de Krebs 80 mM de KCl, foi realizada uma
substituição equimolar do Na+ pelo K+, ajustando isosmoticamente a solução (Tabela
1).
Tabela 1: Composição da solução de Krebs-Henseleit e Krebs-Henseleit com KCl 80 mM para artéria pulmonar
Krebs-Henseleit Krebs-Henseleit - KCl 80 mM
Sais Concentração (mM) Concentração (mM)
NaCl 118,4 43.1
KCl 4,7 80
CaCl2 2,5 2,5
MgSO4 1,2 1,2
C6H12O6 11,1 11,1
NaHCO3 25 25
KH2PO4 1,2 1,2
Fonte: (RODAT-DESPOIX et al., 2007)
Para a preparação da solução de PBS foram utilizados os seguintes sais:
cloreto de sódio, fosfato de sódio monobásico (NaH2PO4) e fosfato de sódio dibásico
Efeito da Fração Aquosa de Cissampelos sympodialis Eichl. em Artéria Pulmonar de Rato com Hipertensão Pulmonar Induzida por Monocrotalina 34
Tabela 2:Composição da solução salina tamponada (PBS).
Componentes Quantidade
NaCl 8,76 g
NaH2PO4 H2O 0,255 g
Na2H2PO4 2,249 g
Água destilada qsp 1000 mL
4 MÉTODOS
4.1 Triagem farmacológica inicial de FAFCS em artéria pulmonar de ratos normotensos
Os animais foram sacrificados por decapitação em guilhotina, de acordo com as recomendações do CEUA-UFPB. Imediatamente após a eutanásia dos animais, os pulmões e coração foram retirados intactos da cavidade torácica e lavados com
uma solução gelada de Krebs-Henseleit (RODAT-DESPOIX et al., 2007).
Os ramos extrapulmonares das artérias foram isolados e dissecados de todo tecido perivascular em solução de Krebs-Henseleit gelado gaseificado com uma
mistura de 5% de CO2 e 95% de O2. As preparações de artéria pulmonar foram
seccionadas em anéis de 1-2 mm de comprimento, e imersas em cubas para banho de órgãos isolados contendo 10 mL de solução Krebs-Henseleit, a temperatura de
37 ºC, pH 7,4 e gaseificadas continuamente com mistura carbogênica (95% de O2 e
5% de CO2) (PAUVERT et al., 2004). Os anéis de artéria pulmonar foram suspensos
Efeito da Fração Aquosa de Cissampelos sympodialis Eichl. em Artéria Pulmonar de Rato com Hipertensão Pulmonar Induzida por Monocrotalina 35
Figura 2: Representação esquemática da cuba para órgãos isolados.
Fonte: MACHADO-TABOSA; ASSIS; FURTADO, 2013
O transdutor, por sua vez, foi acoplado a um sistema de aquisição (ML870/P com LabChart versão 7.0, ADInstruments, Austrália) para o registro das tensões isométricas (Figura 3). Os anéis de artéria pulmonar foram submetidos a uma tensão constante de 1 g por um período de estabilização de 60 minutos. Durante esse período a solução de Krebs-Henseleit foi trocada em intervalos de 15 minutos, para prevenir a interferência de metabólitos indesejáveis (ALTURA ;ALTURA, 1970).
Figura 3: Foto do sistema para banho de órgãos isolados
Efeito da Fração Aquosa de Cissampelos sympodialis Eichl. em Artéria Pulmonar de Rato com Hipertensão Pulmonar Induzida por Monocrotalina 36
4.1.1 Avaliação do efeito vasorrelaxante da FAFCS em anéis de artéria pulmonar pré-contraídas com FEN
Para a realização de todos os protocolos experimentais, após o período de
estabilização de 60 minutos, foi obtida uma contração com FEN (10 μM), um agonista dos receptores α1-adrenérgicos (BYLUND, 1992; BÜSCHER et al., 1999)
encontrados no músculo liso vascular, com a finalidade de verificar a viabilidade do
tecido. No componente tônico desta contração, ACh (10 μM), um agonista dos
receptores muscarínicos, expressos no endotélio vascular, foi adicionada à cuba com o intuito de avaliar a integridade destas células (FURCHGOTT; ZAWADZKI, 1980). Os anéis que apresentaram relaxamento de 80-100% sobre a pré-contração com FEN foram considerados anéis com endotélio funcional. Já os anéis com relaxamento inferior a 10% foram considerados anéis sem endotélio vascular (Figura 4) (PAUVERT et al., 2004).
Figura 4: Representação do protocolo de verificação da viabilidade do tecido muscular e da integridade do endotélio vascular.
a) Presença do endotélio e b) Ausência do endotélio funcional.
Após a verificação da viabilidade do órgão e da presença ou ausência do endotélio (Item 4.1.1) as preparações foram submetidas a trocas do meio nutritivo até que a tensão do órgão retornasse aos valores de base (1 g). Logo após este período, foi induzida uma segunda contração com a concentração submáxima de
FEN (1 μM). No componente tônico desta segunda contração, concentrações
crescentes de FAFCS (10 - γ000 μg/mL) foram adicionadas à preparação, de
Efeito da Fração Aquosa de Cissampelos sympodialis Eichl. em Artéria Pulmonar de Rato com Hipertensão Pulmonar Induzida por Monocrotalina 37
vasorrelaxante do composto foi avaliado em anéis com o endotélio intacto e anéis desprovidos de endotélio funcional (Figura 5).
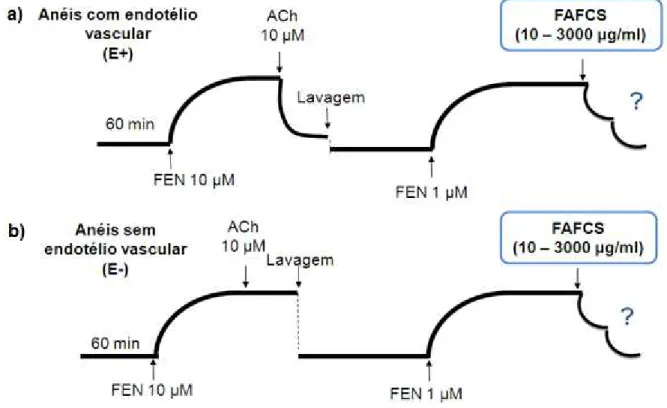
Figura 5: Representação esquemática do protocolo experimental para avaliação do efeito da FAFCS (10 – 3000 μg/mL) em anéis de artéria
extrapulmonar de rato saudável, pré-contraídos com FEN (1 μM).
a) Anéis com endotélio vascular; b) Anéis sem endotélio vascular.
4.2 ENSAIOS FARMACOLÓGICOS IN VIVO
4.2.1 Modelo experimental de HP
Para a indução da hipertensão pulmonar, os animais receberam uma dose
única subcutânea (sc) de MCT (Sigma- Aldrich), 60 mg/kg de peso corpóreo. A MCT
foi dissolvida em HCl 1 N e o volume da solução foi ajustada com solução salina
para alcançar uma concentração de 30 mg/mL. OpH foi neutralizado com NaOH 1 N
Efeito da Fração Aquosa de Cissampelos sympodialis Eichl. em Artéria Pulmonar de Rato com Hipertensão Pulmonar Induzida por Monocrotalina 38
4.2.2 Grupos experimentais e protocolo de tratamento
Os animais foram divididos aleatoriamente em 5 grupos experimentais, um grupo controle saudável (Controle), cujos animais receberam uma única injeção subcutânea de salina 0,9% (2 mL/kg) e quatro grupos testes MCT (salina, FAFCS 50, FAFCS 100, Sildenafil), cujos animais receberam uma única dose subcutânea de MCT. Após 24 horas da injeção de MCT ou salina, os animais receberam seus respectivos tratamentos (figura 6):
I. Controle saudável (Controle): os animais receberam salina via oral ao longo de todo o protocolo experimental;
II. Controle hipertenso (MCT): os animais com HP receberam salina via oral ao longo de todo o protocolo experimental;
III. MCT + FAFCS 50 mg/kg: os animais com HP receberam a fração na dose de 50 mg/kg ao longo de todo o protocolo experimental;
IV. MCT + FAFCS 100 mg/kg: os animais com HP receberam a fração na dose de 100 mg/kg ao longo de todo o protocolo experimental;
V. MCT + Sildenafil: os animais com HP receberam sildenafil na dose de 50 mg/kg ao longo de todo o protocolo experimental.
Efeito da Fração Aquosa de Cissampelos sympodialis Eichl. em Artéria Pulmonar de Rato com Hipertensão Pulmonar Induzida por Monocrotalina 39
Figura 6: Representação esquemática dos grupos experimentais e esquema de tratamento dos animais
4.2.3 Avaliação dos efeitos de FAFCS no modelo de HP induzida por MCT
4.2.3.1 Medida direta da PAP em ratos
A medida da pressão sistólica ventricular direita (PSVD) foi utilizada como um indicador da pressão arterial pulmonar (PAP). Após 28 dias da indução da HP pela MCT, os animais foram anestesiados por meio de uma injeção intraperitoneal de cetamina (50 mg/kg) e xilazina (10 mg/kg). Foi realizada a tricotomia do tórax do animal e o mesmo colocado sobre manta térmica (37 ºC) e entubado via endotraqueal para ventilação mecânica (ventilador mecânico, Ugo Basile 7025) com ar ambiente, volume corrente de 10 mL/kg e frequência de 60 ciclos/min (SCHERMULY et al., 2004).
Efeito da Fração Aquosa de Cissampelos sympodialis Eichl. em Artéria Pulmonar de Rato com Hipertensão Pulmonar Induzida por Monocrotalina 40
(PowerLab, ADInstruments) e analisados pelo programa LabChart Reader (Version
7.0, ADInstruments) (Figura 7).
Figura 7: Sistema de aquisição de dados para medida de PAP em ratos anestesiados.
Fonte: Fotografia da autora
4.2.3.2 Medida da hipertrofia do ventrículo direito
Após a medida de pressão, os animais ainda anestesiados foram sacrificados por decapitação em guilhotina. O tórax foi aberto e os órgãos extraídos. O coração foi rapidamente retirado e os átrios separados dos ventrículos. O ventrículo direito (VD) e o ventrículo esquerdo mais septo (VE+S) foram dissecados e pesados em balança analítica. O índice de hipertrofia foi calculado pela razão do peso do VD (g) e do peso do (VE+S) (STEINER et al., 2009; PANKEY et al., 2012).
4.3 Ensaios farmacológicos “in vitro”
4.3.1 Ensaios farmacológicos de reatividade vascular utilizando anéis de artéria pulmonar isolada de ratos com HP induzida por monocrotalina
Efeito da Fração Aquosa de Cissampelos sympodialis Eichl. em Artéria Pulmonar de Rato com Hipertensão Pulmonar Induzida por Monocrotalina 41
artérias extrapulmonares foram isoladas e dissecadas, para obtenção dos anéis, como descrito anteriormente (Item 4.1).
Após a montagem do anel de artéria na cuba, foi induzida mecanicamente uma tensão de 1 g, a qual foi mantida durante todo o experimento. Os anéis permaneceram por um período de 60 minutos de estabilização e, em seguida foram estimulados com solução despolarizante de potássio (KCl 80 mM) para verificar a viabilidade do tecido. Os anéis foram lavados com solução de Krebs-Henseleit até o retorno da tensão inicial (de repouso/basal). Em seguida, foram traçadas curvas concentração-efeito para fenilefrina (FEN), acetilcolina (ACh) ou nitroprussiato de sódio (NPS).
4.3.1.1 Avaliação da resposta contrátil dos anéis de artéria pulmonar isolada de ratos à FEN
Após o procedimento de verificação da viabilidade do tecido muscular liso, as preparações foram lavadas. Em seguida, concentrações crescentes e cumulativas
de FEN (10-10 – 10-5 M) foram adicionadas ao banho, e as respostas obtidas após a
adição do agonista foram utilizadas para a obtenção de uma curva concentração-resposta (Figura 8).
Efeito da Fração Aquosa de Cissampelos sympodialis Eichl. em Artéria Pulmonar de Rato com Hipertensão Pulmonar Induzida por Monocrotalina 42
4.3.1.2 Avaliação da resposta relaxante dos anéis de artéria pulmonar, isolada de rato, à ACh e ao NPS
Em cada anel foi obtida uma contração com FEN (10-5 M). No componente
tônico desta contração, concentrações crescentes e cumulativas de ACh (10-10– 10-5
M) ou NPS (10-10 - 10-5 M) foram adicionadas ao banho, com intervalos de
aproximadamente três minutos entre cada concentração (Figura 9). As respostas obtidas foram utilizadas para a obtenção de uma curva concentração-resposta.
Figura 9: Representação esquemática dos protocolos de resposta relaxante aos agonistas, ACh ou NPS, em anéis de artéria extrapulmonares isoladas de
ratos pré-contraídas com FEN.
4.4 AVALIAÇÃO DA PRODUÇÃO DE ÂNIONS SUPERÓXIDO (O2●-) EM VASOS
PULMONARES POR MICROSCOPIA DE FLUORESCÊNCIA
A sonda DHE foi utilizada para avaliar a produção in situ de ânions O2●-, nos
seguimentos de artéria extrapulmonares de ratos nos grupos controle, MCT, MCT + FAFCS (50 e 100 mg/kg) e MCT + sildenafil. O DHE é amplamente utilizado para
detecção de ânions O2●- citosólico devido à sua capacidade de difusão passiva para
o interior das células e alta reatividade. No interior da célula, o DHE é oxidado pelos
ânions O2●-, formando um produto intermediário, o 2-hidroxietídio (2-OHEt+) que
intercala com o DNA, o que leva à exibição de uma fluorescência vermelha. O
2-OHEt+ é excitado em 500 nm e tem um espectro de emissão a 580 nm (WOJTALA
Efeito da Fração Aquosa de Cissampelos sympodialis Eichl. em Artéria Pulmonar de Rato com Hipertensão Pulmonar Induzida por Monocrotalina 43
Após o isolamento das artérias extrapulmonares, as mesmas foram cortadas em anéis de 2-3 mm de comprimento (item 4.1.1) e incluídas em meio de inclusão
para amostras frescas, Tissue Tek Compound (OCT) e imediatamente congeladas
em nitrogênio líquido e estocadas a -80 ºC até as análises. A microtomia do tecido foi realizada a -20ºC em criostato (Cryostat Leica, Nussloc, Alemanha), com uma espessura de 14 µm. Os cortes obtidos fixados em lâminas apropriadas.
Para a realização da medida dos ânions O2●-, as lâminas com os segmentos
de artéria foram lavadas com solução salina tamponada (PBS) e, em seguida,
incubadas com o DHE 10 μM durante γ0 min à temperatura de γ7º C em câmara
úmida, ao abrigo da luz (GROBE et al., 2006; WOJTALA et al., 2013). Em seguida, os cortes foram lavados com PBS para remoção do excesso de sonda fluorescente, e levadas imediatamente ao microscópio de fluorescência (NIKON Eclipse Ti-E, NIKON, Japão) para análise. A intensidade de fluorescência foi utilizada para mensurar a produção de ânions superóxidos nos diferentes grupos.
Os dados foram expressos na forma de Δ de porcentagem de fluorescência,
normalizados pela fluorescência emitida pelo DHE do grupo controle. A fluorescência obtida para os diferentes grupos de tratamento foi determinada de
acordo com a seguinte equação: Δ% Fluorescência = (TRATADA – CONTROLE) x 100/ CONTROLE.
4.5 ANÁLISE ESTATÍTICA
Os resultados foram expressos como média ± erro padrão da média (e.p.m.). As comparações estatísticas entre duas variáveis foram realizadas por meio da
utilização do teste t de Student não pareado. Para as análises de mais de duas
variáveis foi utilizado o teste ANOVA one way, seguido pelo pós-teste de Bonferroni.
A diferença entre as médias foi considerada significativa quando p<0,05.
As curvas concentração-resposta e os valores de Emáx (efeito máximo em
porcentagem de relaxamento) e CE50 (concentração de uma substância que induz
50% do efeito máximo) foram obtidos por regressão não linear. Os dados foram
analisados e plotados em gráficos por meio do programa GraphPad Prism® versão
Efeito da Fração Aquosa de Cissampelos sympodialis Eichl. em Artéria Pulmonar de Rato com Hipertensão Pulmonar Induzida por Monocrotalina 45
5 RESULTADOS
5.1 ESTUDOS FARMACOLÓGICOS IN VITRO
5.1 Triagem farmacológica de FAFCS em artéria pulmonar de ratos normotensos
5.1.1 Influencia do endotélio sobre o efeito vasorrelaxante induzido pela FAFCS
Após o período de estabilização (60 minutos) da contração de FEN (1 μM),
foram adicionadas concentrações crescentes da FAFCS, de maneira cumulativa (10
– 3000 μg/mL). A fração promoveu um efeito relaxante, dependente de
concentração, em anéis de artéria extrapulmonar isolada de rato e com endotélio
intacto (Emáx = 98 ± 2%; CE50 = 599 μg/mL, n = 7). A remoção mecânica do endotélio
vascular não alterou a resposta relaxante induzida pela FAFCS (Emáx = 102 ± 2%;
CE50= 700 μg/mL, n = 6) (Figura 10 e Gráfico 1).
Figura 10: Registros originais representativos das respostas relaxantes a FAFCS (10 – 3000 μg/mL) em anéis pré-contraídos com FEN (1 μM), na
Efeito da Fração Aquosa de Cissampelos sympodialis Eichl. em Artéria Pulmonar de Rato com Hipertensão Pulmonar Induzida por Monocrotalina 46
Gráfico 1: Curvas concentração-resposta para o efeito relaxante induzido pela FAFCS (10 –3000 μg/mL) em anéis de artéria extrapulmonares isolada de
ratos, na presença (●) ou ausência (○) do endotélio, pré-contraídos com FEN (1
μM) (n = 7 e 6, respectivamente).
Os dados estão representados como média ± e.p.m.
5.2 ESTUDOS FARMACOLÓGICOS IN VIVO
5.2.1 Efeito da FAFCS sobre a PAP de ratos com HP induzida por MCT
Em nosso estudo, a HP induzida por MCT em ratos foi evidenciada 28 dias após a injeção de MCT (60 mg/kg, subcutâneo) devido ao aumento acentuado da PAP. Os ratos tratados com MCT subcutânea apresentaram um aumento significativo da PAP (63 ± 5 mmHg, n = 6) ao final de quatro semanas em relação àqueles que foram injetados com igual volume de salina (29 ± 2 mmHg, n = 7)
(Figura 11 e Gráfico2).
Efeito da Fração Aquosa de Cissampelos sympodialis Eichl. em Artéria Pulmonar de Rato com Hipertensão Pulmonar Induzida por Monocrotalina 47
Figura 11: Registro original representativo da pressão arterial pulmonar (PAP) no dia 28º seguinte à injeção subcutânea de monocrotalina (MCT) ou salina.
a) controle, normotenso não tratado; b) hipertenso não tratado; c) hipertenso tratado com FAFCS na dose de 50 mg/kg/dia; d) hipertenso tratado com FAFCS na dose de 100 mg/kg/dia; e) hipertenso
tratado com sildenafil na dose de 50 mg/kg/dia
Gráfico 2: FAFCS previne o aumento da pressão arterial pulmonar (PAP) em ratos com hipertensão pulmonar.
Representação gráfica da PAP no 28º dia, seguinte à injeção de salina (grupo controle) ou MCT e MCT + FAFCS 50 mg/kg, MCT + FAFCS 100 mg/kg e MCT + sildenafil 50 mg/kg. Os dados estão representados como média ± e.p.m. (n = 5-8), p ˂ 0,05 # vs grupo controle, vs grupo MCT, ϕvs
Efeito da Fração Aquosa de Cissampelos sympodialis Eichl. em Artéria Pulmonar de Rato com Hipertensão Pulmonar Induzida por Monocrotalina 48
5.2.1 Efeito da FAFCS sobre hipertrofia do ventrículo direito de ratos com HP induzida por MCT
Os animais tratados com MCT subcutânea apresentaram um aumento significativo da relação VD/VE+S (0,52 ± 0,03 g; n = 6), quando comparados aos animais do grupo controle (VD/VE+S = 0,28 ± 0,02 g; n = 7, p< 0,05). O tratamento com FAFCS (doses 50 e 100 mg/kg) e sildenafil reduziram significativamente a relação VD/VE+S (0,36 ± 0,04 g; 0,37± 0,05 g; 0,35 ± 0,03 g, respectivamente) em relação ao grupo tratado com MCT. Não foram observadas diferenças significativas entre os grupos tratados com FAFCS e sildanafil ou em relação ao grupo controle (Gráfico 3).
Gráfico 3: FAFCS previne a hipertrofia ventricular direita (HVD) em ratos com hipertensão pulmonar.
A HVD foi determinada pela razão entre o peso do ventrículo direito e peso do ventrículo esquerdo mais septo (VD/DE+S) 28º dia, seguinte a injeção de salina (grupo controle) ou MCT, para os grupos
Efeito da Fração Aquosa de Cissampelos sympodialis Eichl. em Artéria Pulmonar de Rato com Hipertensão Pulmonar Induzida por Monocrotalina 49
5.2.2 Efeito do tratamento com FAFCS sobre a reatividade vascular em anéis de artéria pulmonar de ratos com HP induzida por MCT
5.2.2.1 Avaliação da resposta contrátil à FEN em anéis de artéria pulmonar
A adição cumulativa de FEN (10-10 – 10-5 M), um agonista α
1-adrenérgico,
induziu contração, dependente de concentração, em anéis de artéria pulmonar isolada de ratos no grupo controle saudável (CTL). O efeito contracturante máximo
foi observado na concentração de 10-5 M (Figura 12a). A resposta contracturante foi
significativamente diminuída no grupo MCT (∆ contração = 0,37 ± 0,04 g; n = 7),
quando comparado ao grupo controle (CTL) (∆ contração = 0,86 ± 0,09 g; n = 9, p< 0,05) (Figura 12b e gráfico 4).
Figura 12: Registro original representativo da curva concentração-resposta para a FEN (10-10 – 10-5 M) em anéis de artéria extrapulmonar isolada de rato,
após 28 dias da injeção subcutânea de MCT ou salina.