Universidade Federal de Ouro Preto
Programa de Pós-Graduação em Ecologia de Biomas Tropicais
INFLUÊNCIA DE FATORES AMBIENTAIS SOBRE A OCORRÊNCIA E DIVERSIDADE DE MAMÍFEROS DE MÉDIO E GRANDE PORTE EM UNIDADES
DE CONSERVAÇÃO DA SERRA DO ESPINHAÇO MERIDIONAL
Fernando Ferreira de Pinho
Universidade Federal de Ouro Preto
Programa de Pós-Graduação em Ecologia de Biomas Tropicais
INFLUÊNCIA DE FATORES AMBIENTAIS SOBRE A OCORRÊNCIA E
DIVERSIDADE DE MAMÍFEROS DE MÉDIO E GRANDE PORTE EM UNIDADES DE CONSERVAÇÃO DA SERRA DO ESPINHAÇO MERIDIONAL
Fernando Ferreira de Pinho
Dissertação apresentada ao Programa de Pós-Graduação em Ecologia de Biomas Tropicais da Universidade Federal de Ouro Preto como parte dos requisitos para a obtenção do título de mestre em Ecologia de Biomas Tropicais
Orientador: Dr. Adriano Pereira Paglia
Agradecimentos
Ao Instituto Biotrópicos pela oportunidade de desenvolver esta pesquisa e por todos as oportunidades, ensinamentos e condições de realizar pesquisa em ecologia desde os primeiros anos da minha formação em Ciências Biológicas;
À Rede ComCerrado e ao núcleo Biotrópicos/UFVJM da rede pela oportunidade de fazer parte desse projeto e contribuir para o conhecimento da mastofauna do bioma Cerrado; Ao CNPQ (programa SISBIOTA, processo 563134/2010-0 e programa PPBIO, processo 457434/2012-0) pelo financiamento que viabilizou o desenvolvimento dessa pesquisa; À FAPEMIG pela bolsa concedida que permitiu a minha dedicação ao desenvolvimento desse projeto;
Ao meu orientador Adriano Paglia pelo auxílio desde o planejamento da amostragem até a redação final da dissertação;
Ao Guilherme Ferreira pela confiança para desenvolver a pesquisa e pela disponibilidade para ensinar e ajudar em todas as etapas deste projeto, assim como já ocorreu em diversas oportunidades anteriores;
Aos docentes do Programa de Ecologia de Biomas Tropicais, da UFOP, pelos ensinamentos; Ao IEF-MG pela licença para a amostragem no Parque Estadual do Rio Preto;
Ao gerente o Parque Estadual do Rio Preto, Tonhão, pelas caronas de São Gonçalo do Rio Preto até a o parque e por toda a prestatividade que tornaram possível a amostragem no ano de 2013;
A todos os funcionários do Parque Estadual do Rio Preto pela receptividade e pelo auxílio nas atividades de campo;
Ao ICMBio pela licença de coleta no Parque Nacional das Sempre-Vivas;
Aos analistas ambientais do Parque Nacional das Sempre-Vivas pelos auxílios logísticos, pela disponibilização de dados referentes ao parque e pela prestatividade sempre que solicitados;
Aos vigias do Parque Nacional das Sempre-Vivas pela receptividade durante as atividades de campo;
Ao Marcelo Juliano Oliveira e ao Flávio Rodrigues pelo auxílio na identificação de espécies de alguns vídeos mais “problemáticos”;
A todos os colegas de mestrado pela amizade, momentos de descontração, conselhos e incentivos durante este período;
A todos os meus amigos que de uma forma ou de outra me deram forças completar mais esta etapa;
Índice
Índice de Tabelas ... i
Índice de figuras ... ii
Apresentação ... 1
Área de estudo ... 1
Amostragem ... 3
Referências Bibliográficas ... 6
Capitulo 1- ESTIMATIVAS DE OCUPAÇÃO DE MAMÍFEROS DE MÉDIO E GRANDE PORTE NA SERRA DO ESPINHAÇO ... 8
Resumo ... 8
Introdução ... 9
Metodologia ... 11
Resultados ... 14
Discussão ... 21
Referências Bibliográficas ... 28
Capítulo 2 - RIQUEZA E USO DO HABITAT POR MAMÍFEROS DE MÉDIO E GRANDE PORTE EM DUAS UNIDADES DE CONSERVAÇÃO DA SERRA DO ESPINHAÇO ... 37
Resumo ... 37
Introdução ... 38
Metodologia ... 41
Resultados ... 43
Discussão ... 49
Implicações para conservação ... 55
i
Índice de Tabelas
ii
Índice de figuras
1
Apresentação
Este estudo é parte dos estudos desenvolvidos pela Rede ComCerrado, uma rede de
pesquisas que visa o preenchimento de lacunas no conhecimento sobre o bioma Cerrado,
através de uma interação de estudos do meio biótico e abiótico com metodologias
patronizadas em diversas partes do bioma. Um dos objetivos da rede é mapear a
biodiversidade do Cerrado e estudar os fatores ambientais que determinam o atual estado de
conservação do bioma.
Utilizamos nesse estudo protocolos padronizados de armadilhamento fotográfico que
vem sendo utilizados em diversas partes do mundo e, recentemente, têm sido implantados
em algumas localidades do Cerrado. O uso desses protocolos padronizados permite uma
ampla gama de opções de estudos integrados para o melhor entendimento dos processos que
influenciam a distribuição de mamíferos de médio e grande porte no Cerrado.
Aqui dividimos o estudo em dois capítulos, visando futuras publicações. No primeiro
capítulo demos ênfase à ecologia de populações por meio das estimativas de ocupação de
cada espécie de mamífero e aos fatores ambientais que podem influenciar essa ocupação no
Parque Estadual do Rio Preto e no Parque Nacional das Sempre-Vivas. No segundo capítulos
avaliamos a riqueza e estrutura da comunidade nas duas Unidades de Conservação e os
fatores que as influenciam.
Área de estudo
A cadeia montanhosa da Serra do Espinhaço representa uma das mais importantes
regiões biogeográficas do Brasil, pois além de estar inserida na Caatinga, no Cerrado e na
2
como hostspots para conservação da biodiversidade (MYERSet al. 2000, MITTERMIERet al.
2005). A Serra do Espinhaço é um dos maiores centros de endemismo de espécies de animais
e plantas da América do Sul, sendo que várias espécies de diferentes grupos taxonômicos
têm sido recentemente descritas.
Tal importância biológica tem sido destacada em muitos estudos de priorização de áreas
para a conservação da biodiversidade (e. g. DRUMOND et al.2005,MMA/PROBIO 2007,SILVA
et al. 2008). Em sua parte meridional, a Serra do Espinhaço compreende o Mosaico de
Unidades de Conservação do Espinhaço: Alto Jequitinhonha – Serra do Cabral, onde estão
localizadas sete Unidades de Conservação de Proteção Integral e cinco Áreas de Proteção
Ambiental (Uso Sustentável), sob os domínios do Cerrado, em sua maior extensão, e da Mata
Atlântica, ao extremo leste. A área do mosaico é considerada prioritária para conservação da
biodiversidade pelos critérios de complementaridade e insubstituibilidade (SILVA et al.
2008).
Este estudo foi realizado em duas das Unidades de Conservação de Proteção Integral
do Mosaico de Unidades de Conservação: Alto Jequitinhonha – Serra do Cabral, totalmente
inseridas dentro dos domínios do Cerrado: Parque Estadual do Rio Preto (PERP) e Parque
Nacional das Sempre-Vivas (PNSV).
O PERP foi criado em 1994 e possui uma área de 12.185 hectares. A unidade apresenta
formações vegetacionais abertas e florestadas, compondo um mosaico de vegetação,
incluindo áreas de campo rupestre, cerrado (stricto sensu) e matas ciliares ao longo das
margens do Rio Preto. O parque apresenta um gradiente altitudinal de mais de 1000 metros,
variando de aproximadamente 750 metros até mais de 1800 metros de altitude. Devido ao
3 de fatores antrópicos recentes sobre a mastofauna no PERP pode ser considerado desprezível.
Uma Reserva Particular de Patrimônio Natural (RPPN Raiz), adjacente ao PERP em sua
porção à noroeste, com características de relevo e vegetação semelhantes ao do parque,
também foi amostrada durante o estudo.
O PNSV foi criado em 2002 e possui uma área de 124.154 hectares. A unidade
apresenta um domínio de formações campestres, principalmente campo rupestre, além de
áreas de campo limpo, cerrado (stricto sensu), veredas, matas-secas e matas ciliares. A
unidade tem uma altitude mínima de aproximadamente 650 metros e altitude máxima de
1.525 metros. Este estudo, no entanto, por questões logísticas, aconteceu somente na parte
sul do parque, em um intervalo de altitude entre aproximadamente 1000 e 1400 metros,
caracterizado por fitofisionomias primariamente campestres, com campos rupestres e campos
limpos, além de formações de cerrado, matas ciliares e capões de mata. Ao contrário de
PERP, o PNSV ainda possui diversas situações fundiárias pendentes e alguns impactos
antrópicos ainda são consideráveis dentro dos limites da unidade. A incidência de fogo é
considerada uma ameaça de alta significância (ÁVILA 2014).
Amostragem
Foram seguidos protocolos internacionais de armadilhamento fotográfico já bem
estabelecidos (TEAM NETWORK 2008, O’BRIEN 2010), que são adotados pela Rede
ComCerrado com algumas modificações. As armadilhas fotográficas foram distribuídas
sistematicamente a uma densidade de uma armadilha fotográfica a cada 200 ha,
representando espaçamento de 1,5 km entre as armadilhas. A definição dos pontos foi feita
utilizando um programa de geoprocessamento, sobrepondo-se blocos quadriculados, de 1,5
4 blocos quadriculados. Os pontos pré-definidos foram inseridos em um GPS, que auxiliou nas
atividades de instalação das armadilhas fotográficas. Em campo as armadilhas fotográficas
foram instaladas dentro de um raio de 150 m do ponto previamente definido, priorizando o
local que aparentemente era mais adequado para registrar diversas espécies de mamíferos de
médio e grande porte. No entanto, quatro pontos no PERP e dois no PNSV foram deslocados
além do raio pré-estabelecido devido às dificuldades de acesso, não ultrapassando em
nenhum dos casos um raio de 250 m do ponto previamente definido. Dois pontos extras (além
dos pontos pré-estabelecidos) foram incluídos nos limites do PERP, mas respeitando uma
distância de no mínimo 1,2 km entre os pontos. A amostragem destes pontos extras teve como
objetivo preencher lacunas de amostragem na UC, causadas pela inacessibilidade de alguns
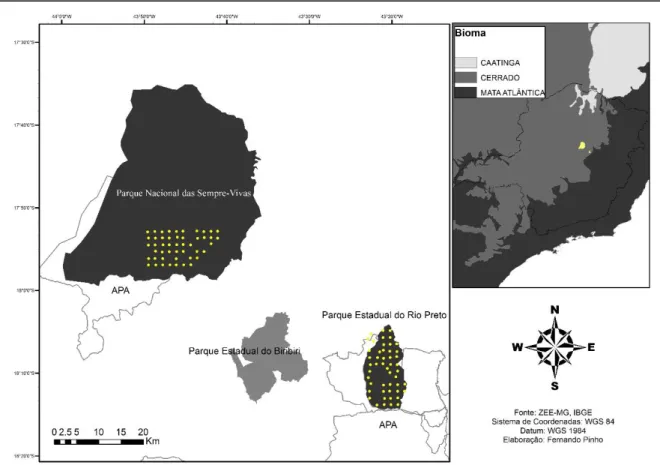
dos pontos pré-estabelecidos. No total, foram instaladas 51 armadilhas fotográficas no PERP
(incluindo três pontos na RPPN Raiz) e 55 pontos no PNSV. Devido a falhas nos
equipamentos, no entanto, a amostragem real foi de 49 pontos no PERP e 48 no PNSV (figura
5 Figura 1 - Mapa da amostragem de mamíferos de médio e grande porte do Parque Estadual do Rio Preto (2013) e Parque Nacional das Sempre-Vivas (2014) por armadilhas fotográficas.
As amostragens ocorreram exclusivamente na estação seca, entre junho e setembro de
2013 no PERP e entre maio e junho de 2014 no PNSV. Cada armadilha ficou em campo por
no mínimo 30 dias, embora algumas tenham parado de funcionar antes de completar este
tempo. No PERP, os pontos válidos foram amostrados de 7 a 108 dias, com média de 57,18
dias/câmera. Já no PNSV, os pontos válidos foram amostrados de 9 a 50 dias, com média de
6
Referências Bibliográficas
ÁVILA,G.C.2014.MOSAICO DE ÁREAS PROTEGIDAS DO ESPINHAÇO:ALTO JEQUITINHONHA
-SERRA DO CABRAL,MINAS GERAIS E OS DESAFIOS PARA SUA EFETIVIDADE.DISSERTAÇÃO
DE MESTRADO.UNIVERSIDADE FEDERAL DE MINAS GERAIS,INSTITUTO DE GEOCIÊNCIAS.
AZEVEDO,A.A.&F.A.SILVEIRA.2005.TWO NEW SPECIES OF CENTRIS (TRACHINA)KLUG,
1807 (HYMENOPTERA: APIDAE) FROM THE STATE OF MINAS GERAIS, BRAZIL, WITH A
NOTE ON CENTRISPACHYSOMACOCKERELL,1919.LUNDIANA 6(SUPPLEMENT):41-48.
BARATA, I. M., SANTOS, M. T., LETITE, F. S. & GARCIA, P. C. 2013.A NEW SPECIES OF
CROSSODACTYLODES(ANURA:LEPTODACTYLIDAE) FROM MINAS GERAIS,BRAZIL: FIRST
RECORD OF GENUS WITHIN THE ESPINHAÇO MOUNTAIN RANGE.ZOOTAXA 3731(4):552– 560.
DRUMOND,G.M.;MARTINS,C.S.;MACHADO,A.B.M.;SEBAIO,F.A;ANTONINI,Y.
BIODIVERSIDADE EM MINAS GERAIS: UM ATLAS PARA SUA CONSERVAÇÃO.BELO
HORIZONTE:FUNDAÇÃO BIODIVERSITAS,2005.222 P.
FREITAS,G.H., CHAVES,A. V.,COSTA,L. M.,SANTOS,F. R.&RODRIGUES,M..A NEW
SPECIES OF CINCLODES FROM THE ESPINHAÇO RANGE, SOUTHEASTERN BRAZIL: INSIGHTS
INTO THE BIOGEOGRAPHICAL HISTORY OF THE SOUTH AMERICAN HIGHLANDS. THE INTERNATIONAL JOURNAL OF AVIAN SCIENCE.X:1-18.
MINISTÉRIO DO MEIO AMBIENTE.2007.PROJETO DE CONSERVAÇÃO E USO SUSTENTÁVEL DA
7 MITTERMEIER,R.A.,GIL,R.P.,HOFFMAN,M.,PILGRIM,J.,BROOKS,T.,MITTERMEIER,C.
G., LAMOREUX, J., FONSECA, G. A. B. 2005. HOTSPOTS REVISITED: EARTH'S
BIOLOGICALLY RICHEST AND MOST ENDANGERED TERRESTRIAL ECOREGIONS.BOSTON: UNIVERSITY OF CHICAGO PRESS.392 P.
MYERS,N.,R.A.MITTERMEIER,C.G.MITTERMEIER,G.A.B. DA FONSECA &J.KENT.2000.
BIODIVERSITY HOTSPOTS FOR CONSERVATION PRIORITIES.NATURE,403:853-858.
O’BRIEN,T.2010.WILDLIFE PICTURE INDEX:IMPLEMENTATION MANUAL VERSION 1.0.WCS
WORKING PAPERS NO.39,JUNE.
OLIVEIRA,R.S.&SANO,P.T.2009.TWO NEW SPECIES HABRANTHUS (AMARYLLIDACEAE)
FROM THE ESPINHAÇO RANGE,BRAZIL.KEW BULLETIN, VOL 64:537-541.
PARDIÑAS,U.F.,LESSA,G.,TETA,P.,SALAZAR-BRAVO,J.,CÂMARA,E.M.A NEW GENUS OF
SIGMODONTINE RODENT FROM EASTERN BRAZIL AND THE ORIGIN OF THE TRIBE PHYLLOTINI.JOURNAL OF MAMMALOGY 95(2):201-215.
SILVA,J.A.,MACHADO,R.B.,AZEVEDO,A.A.,DRUMOND,G.M.,FONSECA,R.L.,GOULART,
M.F.,JÚNIOR,E.A.M.,MARTINS,C.C.,NETO,M.B.R.2008.IDENTIFICAÇÃO DE ÁREAS
INSUBSTITUÍVEIS PARA CONSERVAÇÃO DA CADEIA DO ESPINHAÇO, ESTADOS DE MINAS GERAIS E BAHIA,BRASIL.MEGADIVESIDADE,4(1-2):248–269.
TEAMNETWORK.2008.TERRESTRIAL VERTEBRATE PROTOCOL IMPLEMENTATION MANUAL,
V.3.0. TROPICAL ECOLOGY, ASSESSMENT AND MONITORING NETWORK, CENTER FOR APPLIED BIODIVERSITY SCIENCE, CONSERVATION INTERNATIONAL, ARLINGTON, VA,
8
Capitulo 1- ESTIMATIVAS DE OCUPAÇÃO DE MAMÍFEROS DE MÉDIO E GRANDE PORTE NA SERRA DO ESPINHAÇO
Resumo
Mamíferos de médio e grande porte são essenciais para a funcionalidade do ecossistema
e entender como estas espécies se distribuem ao longo no ambiente e quais são os fatores que
influenciam nessa distribuição é fundamental para medidas efetivas de manejo e conservação
da vida silvestre. Neste estudo procuramos descrever a riqueza e composição de espécies em
duas Unidades de Conservação (UC) de Proteção Integral na Serra do Espinhaço, estimar a
ocupação espécies e avaliar os fatores que influenciam a distribuição dessas espécies.
Seguimos protocolos internacionais de armadilhamento fotográfico e amostramos 49 pontos
no Parque Estadual do Rio Preto (PERP) e 48 pontos no Parque Nacional das Sempre-Vivas
(PNSV). Avaliamos a detectabilidade (p) das espécies registradas em cada UC e realizamos
as análises com modelos mais complexos para todas que apresentaram p>0.1. A proporção
da área ocupada (Ψ) foi calculada através do modelo nulo da estimativa de ocupação
single-season e o efeito dos fatores ambientais avaliados foi medido através do ranking de modelos
(AIC). Registramos 23 espécies, sendo 19 no PERP e 18 no PNSV. As maiores taxas de
ocupação foram do cachorro-do-mato e lobo-guará no PERP e tamanduá-bandeira e anta no
PNSV. Houve uma grande variação dos fatores ambientais que influenciam a distribuição
entre as espécies e entre as UC’s. As relações mais claras encontradas foram da ocupação de
Leopardus tigrinus em áreas de menor altitude no PERP, e Myrmecophaga tridactyla com a
locais com maior densidade de focos de calor no PNSV e Cuniculus paca com habitats
florestais no PNSV. Essas diferentes respostas refletem adaptações morfológicas,
9 indicam que, mesmo em áreas próximas e com fitofisionomias semelhantes, populações de
uma mesma espécie podem variar suas respostas aos fatores ambientais, muitas vezes em
função de ações antrópicas.
Introdução
O conhecimento da distribuição das espécies e o uso de habitats pelos animais são
elementos chave para ecologia e pré-requisitos básicos para o manejo efetivo da vida silvestre
(SUNQUIST et al. 1999, LINKIE et al. 2007). Por este motivo, a maior parte das análises de
perda de biodiversidade, incluindo análises de comunidades de mamíferos, tem se baseado
na distribuição de espécies e inferências quanto ao uso do habitat (CEBALLOS et al. 2005,
CEBALLOS & EHRLICH 2006, HOFFMANN et al. 2011, RONDININI et al. 2011). De fato, a
extinção de algumas espécies de grandes mamíferos pode desencadear cascatas tróficas com
importantes consequências ambientais (CROOKS & SOULÉ 1999, TERBORGH et al. 2001,
MORENOet al. 2006), devido a direta relação do grupo com dispersão de sementes, controle
de herbívoros e ciclagem de nutrientes (BRODIE &GIBBS 2009,JANSENet al. 2010). Além do
mais, entender como as variáveis ambientais influenciam a comunidade de grandes
mamíferos permite a construção de modelos preditivos de ocorrência de espécies baseado na
relação entre animais e habitats (SUNARTO et al. 2012), informação crucial, especialmente
em regiões de alta biodiversidade e pouco estudadas.
Diversos estudos têm avaliado a influência de fatores bióticos e abióticos sobre a
ocupação de mamíferos médios e grandes. Kinnaird & O’Brien (2012) verificaram que ambientes com maior grau de restrição às atividades antrópicas apresentam maiores taxas de
ocupação de mamíferos de médio e grande porte no Quênia. Linkie et al. (2007), no entanto,
10 Rica, Ahumada et al. (2013) avaliou como fatores ambientais, como altitude e altura do
dossel, influenciam a ocupação e a dinâmica de populações de mamíferos e observou uma
variedade de respostas entre as espécies avaliadas. Sunarto et al. (2012) estudou populações
de tigres em Sumatra e demonstrou que a cobertura vegetal é determinante para a ocupação
da espécie.
Entretanto, avaliar esses padrões e tendências em comunidades de grandes mamíferos
é um desafio, especialmente no Cerrado, uma vez que geralmente, estas espécies possuem
hábitos noturnos, ocorrem em baixas densidades, são bastante esquivas e difíceis de detectar.
Collen et al. (2011), mostrou que existe uma grande falta de dados a respeito de tendência de
populações de mamíferos na América do Sul, que só poderá ser superada com informações
locais sobre estas espécies. O uso de armadilhas fotográficas é uma técnica com grande
potencial para ajudar a preencher esta lacuna no conhecimento, uma vez que necessita de
relativamente pouco esforço de campo para gerar dados de considerável cobertura espacial e
temporal (i. e. algumas centenas de km2 e várias semanas).
O uso de armadilhas fotográficas tem sido bem-sucedido na determinação de
abundâncias absolutas (KARANTH & NICHOLS 1998, KAWANISHI & SUNQUIST 2004). A
técnica foi bem desenvolvida dentro de uma estatística robusta com dados de captura e
recaptura quando é aplicável a identificação de indivíduos dentro das populações estudadas
(POLLOCK 1982). Para a maioria dos grandes mamíferos, no entanto, os animais não podem
ser individualizados com confiança. A estimativa de ocupação é uma alternativa a este
método, já que leva em conta a detecção ou não de uma espécie em um local particular,
11 Rovero & Marchal (2009) destacam que a ocupação é muitas vezes um substituto útil
para abundâncias absolutas. Para isso, se assume que a distribuição de ocorrência de espécies
tenha uma relação positiva com a abundância. Segundo Gaston et al. (2000) essa relação é
verdadeira, uma vez que o declínio na abundância de uma espécie tende a mostrar também
um declínio de áreas que ela ocupa, enquanto o aumento da abundância tende a aumentar a
ocupação. A técnica minimiza ainda os efeitos da falsa ausência, ou seja, quando a espécie
não é registrada em um local onde, na verdade, ela ocorre. Isto é importante em estudos
ecológicos, já que as falsas ausências podem levar a inferências incorretas (MCCARTHYet al.
2013).
O objetivo deste estudo foi descrever a composição de espécies de duas unidades de
conservação de proteção integral na Serra do Espinhaço, em Minas Gerais, estimar a
ocupação das espécies mais detectáveis e avaliar quais são os fatores que influenciam a
estimativa de ocupação destas espécies. Acreditamos que as UC’s avaliadas comportem uma
importante parcela da riqueza de espécies conhecida para a Serra do Espinhaço e para o
Cerrado, que as taxas de ocupação das espécies sejam semelhantes entre as duas UC’s devido
à proximidade e similaridade das fitofisionomias que apresentam, e que as respostas aos
fatores avaliados variem entre as espécies, em virtude de suas variações morfológicas,
fisiológicas e comportamentais.
Metodologia
Análise de dados
Estimamos a ocupação (ψ) e a probabilidade de detecção (p) para cada espécie de
mamífero de médio ou grande porte registrada usando a análise de ocupação de única estação
12
software livre R (RDEVELOPMENT CORE TEAM 2010). Consideramos para os dois casos cada
7 dias como uma ocasião de amostragem. Primeiramente realizamos uma análise exploratória do modelo nulo (sem covariáveis influenciando ψ ou p). Consideramos aqui apenas as
espécies com p>0,1, já que detectabilidades muito baixas superestimam os valores de ocupação. Os valores de ψ do modelo nulo foram consideradas como a proporção da área
ocupada por cada espécie na área de estudo. As análises com modelos envolvendo
covariáveis de ψ e p, foram realizadas para todas as espécies com p>0,1.
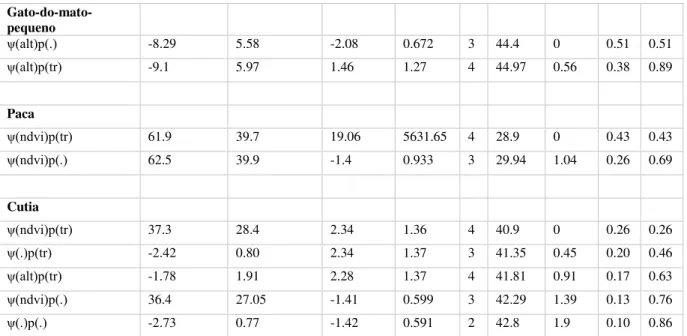
Para os modelos com covariáveis, incluímos altitude (exclusivamente para o PERP),
densidade de focos de calor (exclusivamente para o PNSV), fitofisionomia e índice de cobertura de vegetação (NDVI) como covariáveis de ψ (tabela 1). A opção por utilizar
altitude como covariável apenas para o PERP foi devido à baixa variação de altitude entre os
pontos no PNSV (1041 a 1369 m enquanto no PERP a variação foi de 797 a 1751 m).
Consideramos ainda que a incidência de fogo não é um fator importante no PERP, que não
tem ocorrência de grandes queimadas na última década, enquanto o problema ainda é muito
constante no PNSV. A posição das armadilhas fotográficas (em trilhas ou não) foi utilizada
13 Tabela 1 - Descrição das covariáveis de ocupação e detectabilidade utilizadas nas análises dos dados.
Covariável Classificação PERP PNSV
Altitude Medida através de um GPS GarminEtrex em cada ponto
de instalação de armadilhas fotográficas. X
Foco de calor A partir de dados de focos de calor entre os anos de 1999
e 2012 foi produzido um mapa de Kernel na área do estudo. É uma técnica de interpolação que leva em conta a densidade de pontos para geração de valores. Os valores foram coletados no pixel em que se encontrava o ponto amostrado por armadilha fotográfica, indicando uma provável relação com a intensidade de incêndios no período de 1999 a 2012. Os focos de calor foram fornecidos pelo INPE (2015). A técnica foi realizada através do software ArcGis 10. A medida foi considerada como a frequência em que as áreas amostradas foram queimadas ao longo do período que precede a amostragem deste estudo.
X
Fitofisionomia Classificada para cada ponto em quatro categorias possíveis: mata (matas ciliares, de galeria e capões de mata), cerrado (incluindo cerradão e cerrado stricto sensu), campo aberto (campo cerrado, campos limpos e
sujos) ou ambiente rupestre (campo rupestre e afloramentos rochosos sem ou com muito pouca vegetação). Essa classificação foi pontual, considerando o habitat predominante no entorno do ponto de instalação das armadilhas fotográficas.
X X
NDVI Índice com valores possíveis de -1 a 1, onde -1 indica sem
cobertura vegetal e 1 cobertura vegetal máxima. Foram utilizadas imagens de satélite Landsat 8 de datas próximas à metade da amostragem em cada Unidade de Conservação, obtidas através da USGS. A medida foi feita pela média dos valores obtidos em cada pixel em um buffer de 250 metros de cada ponto de amostragem utilizando o software ArcGis 10.
X X
Trilhas Classificado de acordo com a localização da instalação
das câmeras, podendo assumir apenas duas categorias: trilha ou fora de trilha.
14 Utilizamos os valores do Critério de Informação de Akaike (AIC) para fazer o ranking de modelos e apresentamos apenas os modelos com ΔAIC ≤ 2.0. O teste goodness-of-fit (GoF)
foi realizado para avaliar a sobre-dispersão, utilizando abordagem desenvolvida para
modelos de ocupação (MACKENZIE & BAILEY 2004), utilizando o pacote AICmodavg
(MAZEROLLE 2015) no programa R. O teste foi aplicado ao modelo melhor suportado para
cada espécie e foi definido o nível de significância de 0.1, abaixo do qual consideramos que
houve sobre-dispersão. Nestes casos utilizamos os valores de quase-AIC (QAIC) para
construir o ranking de modelos e a raiz quadrada do fator de inflação da variância (c-hat)
para ajustar os erros padrões das estimativas dos modelos obtidos, conforme recomendações
de Mackenzie & Bailey (2004). Foram eliminados das análises as espécies que apresentaram
sobre-dispersão (p<0.1) e valor de c-hat maior ou igual a 4.
Resultados
Foram registradas 23 espécies de mamíferos de médio e grande porte nas duas áreas
amostradas, das quais sete são classificadas como “Vulneráveis” (lobo-guará,
raposinha-do-campo, onça-parda, gato-mourisco, tatu-canastra e ante) e uma “Em Perigo”
(gato-do-mato-pequeno) de acordo com a lista de espécies da fauna ameaçadas de extinção no Brasil (MMA
2014), com um total de 19 espécies registradas no PERP em 2865 dias/câmera, e 18 espécies
no PNSV em 2010 dias/câmera (tabela 2). Cinco espécies foram registradas exclusivamente
no PERP enquanto outras três foram registradas apenas no PNSV. De todas as espécies
registradas, 12 apresentaram detectabilidade >0.1, sendo oito no PERP e nove no PNSV.
Dentre estas espécies o tamanduá-bandeira (Myrmecophaga tridactyla) e o veado-catingueiro
(Mazama gouazoubira), ambas no PERP, apresentaram sobre-dispersão e valor de c-hat
15 Tabela 2 - Registros de mamíferos de médio e grande porte no Parque Estadual do Rio Preto (2013) e Parque Nacional das Sempre-Vivas (2014)
GRUPO TAXONÔMICO NOME POPULAR PERP PNSV
N P N P
Pilosa
Myrmecophagidae
Tamandua tetradactyla Tamanduá-mirim 2 0.01 5 0.111
Myrmecophaga tridactyla Tamanduá-bandeira 59 0.22 34 0.141
Cingulata
Dasypodidae
Dasypus sp Tatu-galinha 2 0.01 5 0.09
Cabassous unicinctus Tatu-do-rabo-mole 3 0.01 - -
Euphractus sexcinctus Tatu-peba 1 >0.01 2 0.01
Priodontes maximus Tatu-canastra 14 0.131 5 0.561
Carnivora
Canidae
Cerdocyon thous Cachorro-do-mato 31 0.161 - -
Chrysocyon brachyurus Lobo-guará 22 0.221 7 0.07
Lycalopex vetulus Raposinha-do-campo - - 15 0.661
Mephitidae
Conepatus semistriatus Jaritataca 3 0.01 5 0.02
Mustelidae
Eira Barbara Irara 6 0.08 3 0.281
Felidae
Puma yagouaroundi Gato-mourisco 3 >0.01 4 0.01
Leopardus pardalis Jaguatirica 4 0.02 5 0.02
Leopardus tigrinus Gato-do-mato-pequeno 10 0.101 3 0.141
Puma concolor Onça-parda 17 0.08 - -
Procionidae
Procyon cancrivorus Mão-pelada 1 >0.01 - -
Nasua nasua Quati 1 >0.01 1 >0.01
Perissodactyla
Tapiridae
Tapirus terrestres Anta - - 19 0.191
Artiodactyla
Cervidae
Mazama gouazoubira Veado-catingueiro 10 0.152 16 0.281
Tayassuidae
Pecari tajacu Catitu - - 3 >0.01
16
Cuniculidae
Cuniculus paca Paca 6 0.191 26 0.331
Dasyproctidae Dasyprocta sp
Caviidae Cutia 7 0.21 - -
Hydrochoerus hydrochaeris Capivara
- - 1 >0.01
N – Número de registros, p – detectabilidade
1 - p>0.1 e c-hat<4 – espécies que foram consideradas para as análises de ocupação 2– p>0.1 e c-hat>4 – espécies não avaliadas por apresentar sobre-dispersão
Nas duas UC’s, na maioria dos casos espécies de maior porte apresentaram maiores
taxas de ocupação. As maiores taxas de ocupação estimadas foram: cachorro-do-mato
(Cerdocyon thous) e lobo-guará (Chrysocyon brachyurus) no PERP e tamanduá-bandeira
(Myrmecophaga tridactyla) e anta (Tapirus terrestris) no PNSV (figura 2). Das espécies que
tiveram sua ocupação estimada nas duas UC’s, tatu-canastra, gato-do-mato-pequeno e paca
apresentaram variações importantes (figura 2).
Figura 2 - Estimativas de ocupação das espécies com detectabilidade maior que 0.1 no PERP e no PNSV
0.37 0.21 0.06 0.06 0.13 0.19 0.74 0.26 0.16 0.15 0.14 0.08 0.04 0.03 0.02
17 Os fatores ambientais selecionados influenciam a ocupação da maioria das espécies
avaliadas, porém foi observada uma grande variedade de respostas, ou seja, um mesmo fator
pode afetar de uma forma determinada espécie e ter efeito contrário ou inexistente em outra.
Em apenas cinco das 15 populações avaliadas (seis no PERP e nove no PNSV) o modelo nulo para ψ foi o mais forte. A cobertura vegetal (NDVI) representou o modelo mais forte
para cinco populações (muito suportado especialmente para paca no PERP e
veado-catingueiro no PNSV), a intensidade de fogo para três (principalmente tamanduá-bandeira
no PNSV), o habitat para uma (paca no PNSV) e altitude para uma (gato-do-mato-pequeno
no PERP). O fator “trilha”, por sua vez, foi importante para as probabilidades de detecção de
quase 60%, estando mais frequente nos modelos melhor suportados no PERP (cinco dos seis
avaliados) em relação ao PNSV (dois dos nove avaliados) (tabela 3, tabela 4).
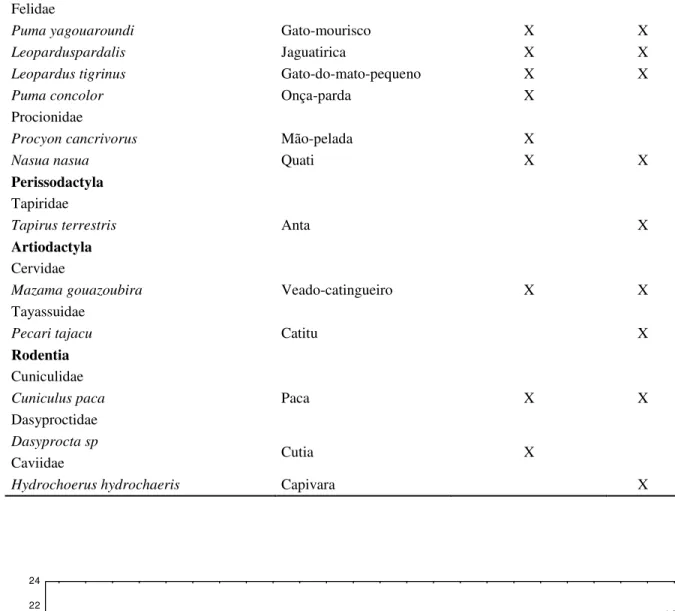
Tabela 3- Seleção de modelos de ocupação para oito espécies de maior detectabilidade no Parque Estadual do Rio Preto.
Ocupação Detectabilidade
Modelo Ψ SE Ψ SE K AIC ΔAIC W Wi
Tatu-canastra
ψ(ndvi)p(tr) 35.54 28.79 13.3 213 4 65.12 0 0.38 0.38
ψ(.)p(tr) -0.359 0.77 9.57 35.6 3 65.57 0.45 0.30 0.68
ψ(hab)p(tr) 10.07(Ma); 8.84(Cer); 2.96 (Rup); 9.84 (Ca) 50.3 (Ma); 50.3 (Cer); 287.7 (Rup); 50.3 (Ca)
-1.92 0.561 6 67 1.88 0.15 0.83
Cachorro-do-mato
ψ(.)p(tr) 0.293 0.68 2.03 0.715 3 133.71 0 0.52 0.52
ψ(alt)p(tr) 0.294 1.13 2.08 0.72 4 135.63 1.92 0.20 0.71
ψ(ndvi)p(tr) -2.17 16.18 2.03 0.715 4 135.69 1.98 0.19 0.91
Lobo-guará
ψ(.)p(tr) -0.119 0.57 10.2 32.8 3 99.59 0 0.46 0.46
ψ(alt)p(tr) -0.725 0.86 9.96 31.3 4 100.84 1.26 0.25 0.71
ψ(ndvi)p(tr) 13.7 19.25 20 3954 4 100.98 1.39 0.23 0.94
18
Gato-do-mato-pequeno
ψ(alt)p(.) -8.29 5.58 -2.08 0.672 3 44.4 0 0.51 0.51
ψ(alt)p(tr) -9.1 5.97 1.46 1.27 4 44.97 0.56 0.38 0.89
Paca
ψ(ndvi)p(tr) 61.9 39.7 19.06 5631.65 4 28.9 0 0.43 0.43
ψ(ndvi)p(.) 62.5 39.9 -1.4 0.933 3 29.94 1.04 0.26 0.69
Cutia
ψ(ndvi)p(tr) 37.3 28.4 2.34 1.36 4 40.9 0 0.26 0.26
ψ(.)p(tr) -2.42 0.80 2.34 1.37 3 41.35 0.45 0.20 0.46
ψ(alt)p(tr) -1.78 1.91 2.28 1.37 4 41.81 0.91 0.17 0.63
ψ(ndvi)p(.) 36.4 27.05 -1.41 0.599 3 42.29 1.39 0.13 0.76
ψ(.)p(.) -2.73 0.77 -1.42 0.591 2 42.8 1.9 0.10 0.86
Ψ – Estimativa de ocupação; SE – erro padrão (logit); p – detectabilidade, K -número de parâmetros; AIC - Critério de Inforção de Akaike; ΔAIC – Variação em relação ao menor AIC; w – peso do modelo; wi– peso acumulado dos modelos (.) – modelo nulo; hab – habitat; alt – altitude; ndvi – Índice de Cobertura Vegetal
Cer: Cerrado; Ma: Mata; Ca: Campo aberto; Rup: Ambiente rupestre
Tabela 4 - Seleção de modelos de ocupação para oito espécies de maior detectabilidade no Parque Nacional das Sempre-Vivas.
Ocupação Detectabilidade
Modelo Ψ SE Ψ SE K AIC ΔAIC W wi
Tamanduá-bandeira
ψ(fc)p(tr) 66.3 68.7 1.31 0.45 4 167.47 0 0.84 0.84
ψ(.)p(tr) 5.21 28.1 1.18 0.44 3 171.9 4.43 0.09 0.93
Tamanduá-mirim
ψ(.)p(.) -1.85 1 -2.07 1 2 42.59 0 0.21 0.21
ψ(hab)p(.) 9.16 (Rup);
7.87 (Cer); 2.97 (Ma); -9.40 (Ca)
42.4 (Rup); 42.4 (Cer); 228.1 (Ma); 42.4 (Ca)
-2.09 1 5 43.15 0.57 0.16 0.37
ψ(fc)p(.) -0.9 0.933 -2.05 1 3 43.36 0.77 0.14 0.51
ψ(.)p(tr) -1.61 1.04 -7.7 48.7 3 43.4 0.81 0.14 0.65
ψ(hab)p(tr) 9.94 (Rup);
8.70 (Cer); 2.95 (Ma); -9.8 (Ca)
56 (Rup); 56 (Cer); 295 (Ma); 56 (Ca)
-9.29 96.65 6 43.64 1.05 0.12 0.77
ψ(fc)p(tr) -1.04 1.04 -7.99 54.15 4 44.06 1.48 0.10 0.87
ψ(ndvi)p(.) -8.715 27.67 -2.08 1.01 3 44.49 1.9 0.08 0.95
19 psi(.)p(.) -3.81 1.78 0.25 1.38 3 12.18 0 0.29 0.29 psi(.)p(tr) -1.9 1.90 10.6 60.48 4 12.99 0.81 0.19 0.48 psi(fc)p(tr) 12.2 92.05 10.9 100.16 5 13.08 0.90 0.18 0.67 psi(fc)p(.) 22.9 58.89 -0.81 1.06 4 13.18 1.00 0.17 0.84 psi(ndvi)p(.) -47.35 125.55 0.24 1.38 4 13.95 1.77 0.12 0.96
Raposinha-do-campo
ψ(.)p(.) -3.11 0.72 0.67 0.72 2 32.01 0 0.27 0.27
ψ(ndvi)p(.) -43.68 49.24 0.65 0.72 3 32.87 0.87 0.18 0.45
ψ(fc)p(.) 0.59 0.58 0.67 0.72 3 33.08 1.08 0.16 0.61
ψ(.)p(tr) -2.92 0.72 -9.30 49.51 3 33.26 1.25 0.14 0.75
Gato-do-mato-pequeno
ψ(.)p(.) -2.47 0.99 -1.82 1.01 2 32.95 0 0.35 0.35
ψ(fc)p(.) 0.331 0.67 -1.83 1.02 3 34.71 1.77 0.14 0.49
ψ(.)p(tr) -2.66 1.02 -0.57 1.84 3 34.86 1.91 0.13 0.63
Irara*
psi(.)p(.) 1.71 3.36 -0.93 1.68 3 12.62 0 0.43 0.43 psi(ndvi)p(.) 53.41 104.68 -0.91 1.70 4 14.18 1.56 0.20 0.63 psi(.)p(tr) 1.71 3.36 -7.5 91.67 4 14.48 1.85 0.17 0.80
Veado
ψ(ndvi)p(tr) 39.79 21.9 -9.11 49.59 4 80.73 0 0.36 0.36
ψ(ndvi)p(.) 32.56 18.23 -0.94 0.44 3 81.9 1.17 0.20 0.56
0.58
Anta
ψ(ndvi)p(.) 25.11 17.28 0.04 0.87 3 97.72 0 0.32 0.32
ψ(.)p(.) -1.07 0.518 -1.44 0.46 2 98.2 0.48 0.25 0.57
Paca
psi(hab)p(.) 14.84 (Ma); -1.33 (Rup); -1.33 (Cer); -8.14 (Ca) 23.25 (Ma); 70.55 (Rup); 65.90 (Cer); 27.58 (Ca)
-1.11 0.31 6 36.71 0 0.27 0.27
psi(hab)p(tr) 12.39 (Ma); -2.91 (Rup); -3.06 (Cer); -11.55 (Ca) 141.11 (Ma); 756.85 (Rup); 760.06 (Cer); 141.11 (Ca)
-1.136 1.17 7 37.17 0.45 0.22 0.49
psi(ndvi)p(.) -0.44 0.86 -0.705 0.39 4 37.28 0.57 0.20 0.69
Ψ – Estimativa de ocupação; SE – erro padrão (logit); p – detectabilidade, K -número de parâmetros; AIC - Critério de Inforção de Akaike; ΔAIC – Variação em relação ao menor AIC; w – peso do modelo; wi– peso acumulado dos modelos (.) – modelo nulo; hab – habitat; fc – foco de calor; ndvi – Índice de Cobertura Vegetal
Cer: Cerrado; Ma: Mata; Ca: Campo aberto; Rup: Ambiente rupestre
20 Os efeitos mais consistentes de covariávies sobre ocupação observados no PERP foram
da altitude para o gato-do-mato-pequeno (Leopardus tigrinus) e do NDVI para a paca
(Cuniculus paca). O gato-do-mato-pequeno apresentou maior taxa de ocupação em áreas
baixas do parque. Avaliando os dados brutos, de fato esta espécie não foi registrada na parte alta do parque, chamada de “Chapada” e caracterizada por ambiente predominantemente
campestre. A ocupação da paca apresentou uma relação positiva com o índice de cobertura
vegetal, ou seja, a distribuição da espécie está associada às áreas com maior cobertura.
No PNSV a densidade de focos de calor foi importante para o tamanduá bandeira, o
NDVI foi importante para o veado catingueiro, o habitat foi importante para a paca. O
tamanduá-bandeira apresentou uma forte associação com áreas com maior densidade de
focos de calor, o veado-catingueiro ocupou áreas com maior cobertura vegetal e a paca
apresentou uma associação muito forte, com a ocupação estimada de 99,99%, em áreas de
mata, próximo a 5% para áreas de cerrado e ambiente rupestre e menos de 0.01% em habitats
de campo aberto. Avaliando os dados brutos, a paca foi registrada em cerca de 67% dos
pontos em áreas de mata e nenhum registro foi obtido em outros tipos de habitat.
Nossos resultados não permitem avaliações mais conclusivas sobre os efeitos dos
fatores ambientais para as demais populações avaliadas. Para cachorro-do-mato e lobo-guará
no PERP e tamanduá-mirim (Tamandua tetradactyla), raposinha-do-campo (Lycalopex
vetulus) e gato-do-mato-pequeno no PNSV o modelo nulo para ocupação foi o mais
consistente. Tatu-canastra (Priodontes maximus) e cutia (Dasyprocta sp.) no PERP e
21 variação de AIC entre os modelos mais fortes, indicando uma falta de tendência a resposta
aos fatores avaliados.
Dentre três espécies que foram avaliadas nas duas UC’s, verificamos que uma mesma
espécie pode apresentar variações quanto à resposta aos fatores que mais afetam sua
ocupação em função da UC. Por exemplo, o gato-do-mato-pequeno apresentou associação
com áreas mais baixas no PERP enquanto no PNSV não foi afetado pelos fatores avaliados.
O tatu-canastra, no PERP não apresentou uma clara relação com nenhum fator, embora o
modelo mais bem suportado tenha sido com a covariável de cobertura vegetal (NDVI),
enquanto no PNSV o modelo nulo foi mais bem suportado. A paca também variou a resposta
aos fatores avaliados entre as UC’s tendo sua ocupação associada à maior cobertura vegetal
(NDVI) no PERP e à habitats de “mata” no PNSV.
Discussão
O número de espécies registradas representa 69,7% das espécies de mamíferos de
médio e grande porte na Cadeia do Espinhaço (LESSAet al. 2008) e 54,8% das espécies do
Cerrado (MARINHO-FILHO et al. 2002). A maior parte das espécies registradas, no entanto,
apresentou baixos valores de detectabilidade, impedindo que análises mais robustas e
complexas fossem feitas para estas. Para a maioria destas espécies, as baixas detectabilidades
encontradas devem ser reflexo de baixas abundâncias das espécies nas áreas avaliadas.
Estudos demonstram que a abundância das espécies focais está diretamente relacionada com
a probabilidade de detecção (MCCARTHYet al. 2013). Em populações mais abundantes mais
indivíduos estão disponíveis para serem detectados, levando a probabilidades de detecção
22
O tatu-canastra apresentou taxas baixas de ocupação nas duas UC’s. Embora a espécie
tenha uma ampla distribuição por uma grande variedade de ambientes, autores indicam que
em todos os locais em que ocorre eles são raros (NOSSet al. 2004, SILVEIRAet al. 2009). No
PNSV, no entanto, sua ocupação foi cerca de 6 vezes menor em relação ao PERP. O fato do
PNSV ser uma UC mais recente e ainda com pressões antrópicas mais evidentes pode
contribuir com essa grande variação. No PERP, embora a cobertura vegetal tenha estado no
modelo com mais suporte, o peso do modelo nulo é muito próximo ao modelo mais
suportado, indicando que pode ser precipitado assumir a cobertura vegetal como um fator
determinante para a ocupação da espécie. No PNSV o modelo nulo foi mais bem suportado,
indicando que os fatores avaliados não são determinantes para a ocupação da espécie. A
existência de uma preferência por habitats pela espécie ainda é controversa na literatura
(ANACLETO 1997, SILVEIRAet al. 2009)
O gato-do-mato-pequeno apresentou maior taxa de ocupação no PERP em relação ao
PNSV. Os dois modelos mais fortes no PERP indicam uma forte tendência de aumento da
ocupação da espécie com a diminuição da altitude. Fato similar já foi observado para outros
felinos (AHUMADAet al. 2013, SUNARTOet al. 2012). No PERP, a maior complexidade dos
ambientes de menor altitude e aparente suporte a maior abundância de presas nesses locais
pode ser o fator determinante dessa associação. No PNSV o efeito da altitude não foi avaliado
devido à baixa variação de altitude entre os pontos, mas a área avaliada como um todo está
em altitude aproximada a parte alta do PERP, o que deve explicar a baixa taxa de ocupação na UC. Em nenhuma das UC’s a espécie apresentou preferência por trilhas, o que pode
indicar um comportamento de evitar o encontro com carnívoros de maior porte que
23 GOULARTet al. 2009). Este comportamento de fuga foi observado para outros carnívoros de
porte menor que seus competidores (DURANT 1998, CREEL &CREEL 2002, OLIVEIRAet al.
2010).
A paca apresentou taxa de ocupação quase três vezes maior no PNSV em relação ao
PERP. A aparente maior abundância de predadores, especialmente a onça-parda, no PERP
pode explicar esta variação. Enquanto no PNSV a onça-parda sequer foi registrada, no PERP,
embora não tenha sido possível realizar análises de ocupação devido à baixa detectabilidade,
a espécie apresentou uma taxa relativamente alta de registros em pontos variados. No PERP
o NDVI foi a variável que mais afetou a ocupação da paca, enquanto no PNSV foi o habitat.
Em ambos os casos a resposta da espécie condiz com o que é conhecido de sua história
natural, já que as pacas estão geralmente associadas a ambientes de maior cobertura vegetal,
como as matas de galeria (SMYTHE 1983; COLLETT 1981, MARINHO-FILHO et al. 2002;
GOULART et al. 2009). O fato da espécie responder em uma escala maior da paisagem no
PERP (o índice de cobertura vegetal foi calculado pela média dos NDVI dos pixels em um
buffer de 250 metros a partir do ponto da instalação da câmera), enquanto respondeu em um
nível pontual no PNSV provavelmente é devido a configuração da paisagem. Enquanto no
PERP observamos uma transição de mata para o cerrado mais imperceptível, em geral, no
PNSV as matas estão restritas a capões com mudanças abruptas de fisionomia para campos
abertos, o que pode restringir a movimentação da espécie apenas aos capões e matas ciliares.
Entre as espécies que foram avaliadas apenas no PERP, cachorro-do-mato e lobo-guará
não apresentaram relação com as covariáveis de ocupação e foram predominantemente
registradas em trilhas. No PNSV, o lobo-guará teve uma detectabilidade muito baixa e
24 PNSV, enquanto a raposinha-do-campo, o outro canídeo de menor porte de ocorrência no
Cerrado, foi registrado apenas no PNSV. Para esta espécie o modelo nulo tanto para ocupação
como para detectabilidade foi o mais forte. Entre os canídeos, portanto, nenhuma das
variáveis analisadas foi determinante. Destaca-se, no entanto, a presença de apenas um dos
canídeos de menor porte com distribuição para a região ser registrado em cada UC. Estudos
indicam que relações interespecíficas podem ser importantes para determinar a distribuição
de canídeos (MITCHELL &BANKS 2005,TANNERFELDTet al. 2002). Para o cachorro-do-mato
e a raposinha-do-campo, no entanto, embora seja relatada uma sobreposição de uso de habitat
e dieta em áreas onde coexistem (JÁCOMOet al. 2004, MARINHO-FILHO 2002), estudos das
relações ecológicas entre as espécies ainda são incomuns. É indicado uma análise mais
profunda para entender essa relação.
A cutia foi registrada apenas no PERP e com uma ocupação muito baixa. Essa baixa
frequência vai contra o que parece ser um padrão em diversos biomas brasileiros, onde
geralmente a cutia é abundante. Ahumada et al. (2011) encontrou altas taxas de ocupação
para cutias em três florestas tropicais. No Cerrado, Ferreira et al. (submetido) também
verificou uma alta estimativa de ocupação para a espécie. Diferente da UC avaliada por
Ferreira et al. (submetido) no entanto, as UC’s avaliadas nesse estudo são
predominantemente campestres. É provável que ambientes campestres não favoreçam a
ocorrência de espécies. De fato, o modelo mais forte para cutia indicou uma preferência por
maior cobertura vegetal. A seleção de modelos, no entanto, indica uma variação muito
pequena entre os pesos dos modelos avaliados, o que indica que a relação com a cobertura
25 Entre as espécies avaliadas apenas no PNSV, o modelo nulo foi o mais bem suportado
para a irara. Além da raposinha-do-campo, o tamanduá-mirim também não apresentou
tendências em relação a nenhuma variável de ocupação nem de detectabilidade. Da mesma
forma, a anta apresentou somente uma relação fraca com a cobertura vegetal, e não podemos
chegar a resultados mais conclusivos a respeito da influência desta variável sobre a espécie.
Entretanto, diversos estudos mostram a associação da anta com habitats ripários (PADILLA &
DOWLER 1994, SALVADORet al. 2011), o que apoia a relação da espécie com maior cobertura
vegetal.
O tamanduá-bandeira obteve no PNSV a maior taxa de ocupação encontrada dentre todas as espécies avaliadas nas duas UC’s. Este fato já havia sido observado no Parque
Estadual Veredas do Peruaçu, no Cerrado do norte de Minas Gerais (FERREIRA et al.
submetido). A associação da espécie com áreas com alta incidência de fogo no PNSV deve
ser explicada pela disponibilidade de recursos alimentares. A ocorrência e a abundância do
tamanduá-bandeira estão diretamente ligadas a abundância de seus recursos alimentares, que
consiste principalmente de formigas e cupins (EISENBERG, 1989). Diversos estudos têm
mostrado que a ocorrência de fogo pode aumentar a abundância de formigas e cupins em savanas (N’Dri et al. 2011; ANDERSEN, 1991; ANDERSEN &MULLER, 2000). Além disso,
uma frequência alta da incidência de fogo deve ser responsável pela conversão de habitats
com vegetação mais densa em habitats com menos densidade de vegetação, o que pode
facilitar a locomoção e a percepção dos recursos alimentares (cupinzeiros e formigueiros)
pela espécie, dessa forma se tornando um ambiente mais atrativo para a espécie.
O veado-catingueiro apresentou uma taxa de ocupação razoavelmente alta no PNSV. A
onça-26 parda sequer foi registrada durante a amostragem, embora estudos anteriores e relatos
indiquem a presença da espécie na UC (FERREIRA et al. 2011, LESSAet al. 2008). A ausência
de registros do predador no PNSV pode ser reflexo de uma baixa densidade de sua população
local, refletindo em uma pressão menor sobre a população de presas na UC, refletindo em
um aumento de suas populações e consequentemente de sua distribuição, como relatado em
outros estudos (CROOKS &SOULÉ 1999). A cobertura vegetal foi o fator mais determinante
para a ocupação da espécie, que ocorreu preferencialmente em áreas com maior cobertura
vegetal. O veado-catingueiro tem ampla distribuição e ocorre em variados ambientes, desde
habitats campestres até habitats florestais, embora ocorra preferencialmente em áreas
savânicas e florestais em detrimento de áreas campestres (MARINHO-FILHO et al. 2002).
Destaca-se ainda que a espécie teve uma relação negativa com o uso de trilhas, o que pode
ser um comportamento para evitar o encontro com o predador. Ahumada et al. (2013) avaliou
a influência de diversos fatores ambientais sobre a ocupação da Mazama temana na Costa
Rica e observou que as taxas de ocupação da espécie aumentam em maiores alturas de dossel,
que provavelmente deve ter correlação com o índice de cobertura vegetal avaliado nesse
estudo, além de observar ainda um aumento desta taxa em altitudes maiores.
Houve uma variação importante do efeito da trilha sobre a detectabilidade entre as duas UC’s. O uso de trilhas por mamíferos de médio e grande porte é comumente relatado na
literatura e é justificado pela facilitação do deslocamento nessas áreas. No entanto são poucos
os estudos que avaliam o uso das trilhas pelo grupo (HARMSENet al. 2010; SRBECK-ARAÚJO
&CHIARELLO 2013,WEARN et al. 2013). Acreditamos que as características da vegetação
das áreas amostradas em cada UC justificam a variação encontrada. No PNSV, praticamente
27 heterogeneidade ambiental, com maior parcel de fitofisionomias savânicas e florestais.
Portanto, é provável que a maior complexidade da vegetação no PERP faça com que a
maioria dos mamíferos de médio e grande porte priorize trilhas para o deslocamento nesta
UC. Enquanto na área amostrada no PNSV, com predominância de vegetação mais baixa, o
deslocamento através da vegetação ocorre mais facilmente, minimizando a importância das
trilhas nesta região.
É esperado que espécies diferentes respondam de formas diferentes ao ambiente, como
resultado de um processo evolutivo que maximiza a eficiência da espécie na sua relação com
o meio e minimiza os efeitos negativos das relações interespecíficas. Para isso ocorrem
adaptações morfológicas (DAYANet al., 1992), comportamentais (BOYDSTONet al., 2003) e
ecológicas (SCHUETTEet al. 2013), que, consequentemente, modificam a relação das espécies
com o ambiente (FEDRIANIet al. 2000, KARANTH &SUNQUIST 1995,KITCHENet al. 1999,
OWEN-SMITH &MILLS 2008,SINCLAIRet al. 2003).
Entender a distribuição e o uso do habitat em comunidades silvestres é um grande
desafio para ecólogos. Nosso estudo mostrou que mesmo em áreas próximas e com paisagens
semelhantes populações diferentes de uma mesma espécie podem responder de formas
diferentes aos fatores ambientais locais. São vários os fatores que influenciam a ocupação
das espécies silvestres, e por muitas vezes é impossível controlar todos eles. Aqui, avaliamos
alguns dos fatores ambientais locais mais facilmente perceptíveis e encontramos importantes
relações de uso do habitat. O entendimento mais aprofundado da relação dos mamíferos com
os fatores que influenciam sua abundância tem importância prática na conservação, uma vez
28 favoráveis a um maior número de espécies são mais úteis e tem maiores chances de serem
bem-sucedidas.
Referências Bibliográficas
AHUMADA,J.A.,HURTADO J.,LIZCANO,D.2013.MONITORING THE STATUS AND TRENDS OF
TROPICAL FOREST TERRESTRIAL VERTEBRATE COMMUNITIES FROM CAMERA TRAP
DATA:ATOOL FOR CONSERVATION.PLOSONE8(9): E73707.
AHUMADA,J.A.,SILVA,C.E.F.,GAJAPERSAD,K., HALLAM,C.,HURTADO,J.,MARTIN,E.,
MCWILLIAN,A.,MUGERWA,B.,O’BRIEN,T.,ROVERO,F.,SHEIL,D.,SPIRONELLO,W.R.,
WINARNI, N., ANDELMAN, S.J. (2011). COMMUNITY STRUCTURE AND DIVERSITY OF
TROPICAL FOREST MAMMALS: DATA FROM A GLOBAL CAMERA TRAP NETWORK. PHILOSOPHICAL TRANSACTIONS OF THE ROYAL SOCIETY B366,2703-2711.
ANACLETO,T.C.1997.DIETA E UTILIZAÇÃO DE HÁBITAT DO TATU-CANASTRA NUMA ÁREA DE
CERRADO DO BRASIL CENTRAL. MSC DISSERTATION, ECOLOGY DEPARTMENT, UNIVERSITY OF BRASILIA,BRASILIA,BRAZIL.
ANDERSEN A. N. & MÜLLER W. J.2000. ARTHROPOD RESPONSES TO EXPERIMENTAL FIRE
REGIMES IN AN AUSTRALIAN TROPICAL SAVANNAH: ORDINAL-LEVEL ANALYSIS.AUST.J. ECOL.25,199–209
ANDERSEN, A.N. 1991. RESPONSES OF GROUND-FORAGING ANT COMMUNITIES TO THREE
29 BOYDSTON,E.E.,K.M.KAPHEIM,H.E.WALTS,M.SZYKMAN,AND K.E.HOLEKAMP.2003.
ALTERED BEHAVIOR IN A LARGE AFRICAN CARNIVORE ASSOCIATED WITH INCREASED
HUMAN ACTIVITY.ANIMAL CONSERVATION 6:207-219.
BRODIE,J.F.&GIBBS,H.2009BUSHMEAT HUNTING AS CLIMATE THREAT.SCIENCE 326:364–
365.
CEBALLOS, G. & EHRLICH, P. R. 2006. GLOBAL MAMMAL DISTRIBUTIONS, BIODIVERSITY
HOTSPOTS, AND CONSERVATION.PROC.NATL ACAD.SCI.103(19):374–19379.
CEBALLOS, G., EHRLICH, P., SOBERON,J., SALAZAR, I. & FAY, J.2005 GLOBAL MAMMAL
CONSERVATION: WHAT MUST WE MANAGE?SCIENCE 309:603–607.
COLLEN,B.,MCRAE,L.,DEINET,S.,DE PALMA,A.,CARRANZA,T.,COOPER,N.,LOH,J.,
BAILLIE,J.E.M.2011.PREDICTING HOW POPULATIONS DECLINE TO EXTINCTION. PHIL.
TRANS.R.SOC.B 366,2577–2586
COLLETT, S. F. 1981. POPULATION CHARACTERISTICS OF AGOUTI PACA (RODENTIA) IN
COLOMBIA. PUBLICATIONS OF THE MUSEUM, BIOLOGICAL SERIES 5, PP. 485-602.
MICHIGAN STATE UNIVERSITY,LANSING,MICHIGAN
CREEL,S., AND N. M. CREEL. 2002.THE AFRICAN WILD DOG: BEHAVIOR, ECOLOGY AND
CONSERVATION.PRINCETON UNIVSERSITY PRESS,PRINCETON,NEW JERSEY,USA.
CROOKS,K.R.,SOULÉ,M.E.,1999.MESOPREDATOR RELEASE AND AVIFAUNAL EXTINCTIONS
IN A FRAGMENTED SYSTEM.NATURE 400,563–566.
DAYAN, T., SIMBERLOFF, D., TCHERNOV, E., YOM-TOV, Y., 1992. CANINE CARNASSIALS:
30 DURANT, S.M., 1998. COMPETITION REFUGES AND COEXISTENCE: AN EXAMPLE FROM
SERENGETI CARNIVORES.J.ANIM.ECOL.67,370–386.
EISENBERG,J.F. 1989.MAMMALS OF THE NEOTROPICS: THE NORTHERN NEOTROPICS.THE
UNIVERSITY OF CHICAGO PRESS,CHICAGO,ILLINOIS
FEDRIANI, J.M., FULLER, T.K., SAUVAJOT, R.M., YORK, E.C., 2000. COMPETITION AND
INTRAGUILD PREDATION AMONG THREE SYMPATRIC CARNIVORES.OECOLOGIA 125,258– 270.
FERREIRA, G. B., BARATA, I. M., MAFIA, P. O., PINHEIRO, M. S. 2011. INVENTÁRIO DE
VERTEBRADOS NO PARQUE NACIONAL DAS SEMPRE-VIVAS, SERRA DO ESPINHAÇO, MINAS GERAIS.RELATÓRIO NÃO PUBLICADO.INSTITUTO BIOTRÓPICOS.
FISKE,I.,CHANDLER,R.2010.UNMARKED: MODELS FOR DATA FROM UNMARKED ANIMALS.R
PACKAGE VERSION 0.8-7. DISPONÍVEL EM: HTTP://CRAN.R
-PROJECT.ORG/WEB/PACKAGES/UNMARKED/.
GASTON,K. J.; BLACKBURN, T. M.; GREENWOOD, J. D.;GREGORY,R. D.;QUINN,R. M.;
LAWTON, J. H.. 2000. ABUNDANCE OCCUPANCY RELATIONSHIPS. 2000. JOURNAL OF
APPLIED ECOLOGY 37(1):39-59
GOULART, F.V.B., CÁCERES, N., GRAIPEL, M.E., TORTATO, M.A., GHIZONI JR, I.R &
OLIVEIRA-SANTOS, L.G.R. 2009. HABITAT SELECTION BY LARGE MAMMALS IN A
SOUTHERN BRAZILIAN ATLANTIC FOREST.MAMM.BIOL.74:182-190.
HARMSEN B.J.,FOSTER R.J.,SILVER S.,OSTRO L.,DONCASTER C.P.2010. DIFFERENTIAL
USE OF TRAILS BY FOREST MAMMALS AND THE IMPLICATIONS FOR CAMERA TRAP STUDIES:
31 HOFFMANN,M.,BELANT,J.L.,CHANSON,J.S.,COX,N.A.,LAMOREUX,J.,RODRIGUES,A.S.
L.,SCHIPPER,J.&STUART,S.N.2011THE CHANGING FATES OF THE WORLD’S MAMMALS.
PHIL.TRANS.R.SOC.B366:2598–2610.
INPE-INSTITUTO NACIONAL DE PESQUISAS ESPACIAIS,2015.PORTAL DO MONITORAMENTO
DE QUEIMADAS E INCÊNDIOS.DISPONÍVEL EM HTTP://WWW.INPE.BR/QUEIMADAS.
JÁCOMO,A.T.A.,SILVEIRA,L.,&DINIZ,J.A.F.(2004).NICHE SEPARATION BETWEEN THE
MANED WOLF (CHRYSOCYON BRACHYURUS), THE CRAB-EATING FOX (DUSICYON THOUS)
AND THE HOARY FOX (DUSICYON VETULUS) IN CENTRAL BRAZIL.JOURNAL OF ZOOLOGY, 262,99-106.
JANSEN,P.,MULLER-LANDAU,H.C.&WRIGHT,S.2010BUSHMEAT HUNTING AND CLIMATE:
AN INDIRECT LINK.SCIENCE 327:30.
KARANTH, K.U., NICHOLS, J.D., 1998. ESTIMATION OF TIGER DENSITIES IN INDIA USING
PHOTOGRAPHIC CAPTURES AND RECAPTURES.ECOLOGY 79:2852–2862.
KARANTH,K.U.,SUNQUIST,M.E.,1995.PREY SELECTION BY TIGER, LEOPARD AND DHOLE IN
TROPICAL FORESTS.J.ANIM.ECOL.,439–450.
KAWANISHI,K. &SUNQUIST,M.E. 2004.CONSERVATION STATUS OF TIGERS IN A PRIMARY
RAINFOREST OF PENINSULAR MALAYSIA.BIOLOGICAL CONSERVATION 120:329–344.
KINNAIRD, M.F. & O’BRIEN, T.G. 2012. EFFECTS OF PRIVATE-LAND USE, LIVESTOCK MANAGEMENT, AND HUMAN TOLERANCE ON DIVERSITY, DISTRIBUTION, AND
ABUNDANCE OF LARGE AFRICAN MAMMALS.CONSERVATION BIOLOGY 26 (6):
32 KITCHEN, A.M., GESE, E.M., SCHAUSTER,E.R., 1999. RESOURCE PARTITIONING BETWEEN
COYOTES AND SWIFT FOXES: SPACE, TIME, AND DIET.CAN.J.ZOOL.77,1645–1656.
LESSA,LG;COSTA,BMA; ROSSONI,DM;TAVARES,VC;DIAS,LG;JÚNIOR,EAM;SILVA,
JA.2008.MAMÍFEROS DA CADEIA DO ESPINHAÇO: RIQUEZA, AMEAÇAS E ESTRATÉGIAS
PARA CONSERVAÇÃO.MEGADIVERSIDADE.V:4 N1-2.
LINKIE,M.;DINATA,Y.;NUGROHO,A.;HAIDIR,I.A. 2007.ESTIMATING OCCUPANCY OF A
DATA DEFICIENT MAMMALIAN SPECIES LIVING IN TROPICAL RAINFORESTS:SUN BEARS IN
THE KERINCI SEBLAT REGION,SUMATRA.BIOLOGICAL CONSERVATION 137:20-27
MACKENZIE,D.I.&L.L.BAILEY. 2004.ASSESSING THE FIT OF SITE-OCCUPANCY MODELS.J.
AGRIC.BIOL.ENVIRON.STAT.9:300–318.
MACKENZIE D.I.;NICHOLS,J.D.;ROYLE,J.A.;POLLOCK,K.H.; BAILEY,L.L.; HINES,J.E.
2006. OCCUPANCY ESTIMATING AND MODELLING – INFERRING PATTERNS AND
DYNAMICS OF SPECIES OCCURENCE. ELSEVIER ACADEMIC PRESS.
MACKENZIE, D.I., NICHOLS,J.D., LACHMAN,G.B., DROEGE, S., ROYLE,J.A., LANGTIMM,
C.A.,2002.ESTIMATING SITE OCCUPANCY RATES WHEN DETECTION PROBABILITIES ARE
LESS THAN ONE.ECOLOGY 83:2248–2255.
MARINHO-FILHO,J., F.H.G. RODRIGUES &K.M. JUAREZ.2002.THE CERRADO MAMMALS:
DIVERSITY, ECOLOGY, AND NATURAL HISTORY.IN:P.S.OLIVEIRA &R.J.MARQUIS (EDS.). THE CERRADOS OF BRAZIL: ECOLOGY AND NATURAL HISTORY OF A NEOTROPICAL
33 MAZEROLLE,MARK J.2015.AICCMODAVG:MODEL SELECTION AND MULTIMODEL INFERENCE
BASED ON (Q)AIC(C). R PACKAGE VERSION 2.0-3. HTTP
://CRAN.R-PROJECT.ORG/PACKAGE=AICCMODAVG
MCCARTHY,M.A.;MOORE,J.L.;MORRIS,W.K.;PARRIS,K.M.;GARRARD,G.E.;VESK,P.
A.;RUMPFF,L.;GILJOHANN,K.M.;CAMAC,J.S.;BAU,S.;FRIEND,T.;HARRISON,B.;
YUE,B.2013THE INFLUENCE OF ABUNDANCE ON DETECTABILITY.OIKOS 122:717–726.
MITCHELL, B. D. & BANKS, P. B. 2005. DO WILD DOGS EXCLUDE FOXES? EVIDENCE FOR
COMPETITION FROM DIETARY AND SPATIAL OVERLAPS.AUSTRAL ECOLOGY 30:581-591.
MMA(MINISTÉRIO DO MEIO AMBIENTE).2014.PORTARIA Nº 444, DE 17 DE DEZEMBRO DE
2014-LISTA NACIONAL OFICIAL DE ESPÉCIES DA FAUNA AMEAÇADAS DE EXTINÇÃO.
MORENO, R., KAYS, R. & SAMUDIO JR., R. 2006. COMPETITIVE RELEASE IN THE DIET OF
OCELOTS (LEOPARDUS PARDALIS) AND PUMA (PUMA CONCOLOR) AFTER JAGUAR
(PANTHERA ONCA) DECLINE.J. OF MAMMAL.87(4):808-816.
N’DRI,A.B.,GIGNOUX,J.,KONATÉ,S,,DEMBÉLÉ,A.,AIDARA,D.2011.ORIGIN OF TRUNK
DAMAGE IN WEST AFRICAN SAVANNA TREES: THE INTERACTION OF FIRE AND TERMITES.J TROP ECOL 27:269–278
NOSS,A.,R.PEÑA AND D.I.RUMIZ.2004.CAMERA TRAPPING PRIODONTES MAXIMUS IN THE
DRY FORESTS OF SANTA CRUZ,BOLIVIA.ENDANGERED SPECIES UPDATE 21:43–52.
OLIVEIRA,T.G.;M.A.TORTATO;L.SILVEIRA;C.B.KASPER; F.D.MAZIM;M.LUCHERINI;
A.T.JÁCOMO;J.B.G.SOARES;R.V.MARQUES &M.SUNQUIST.2010.OCELOT ECOLOGY
34 IN:D.MACDONALD &A.LOVERIDGE (EDS).THE BIOLOGY AND CONSERVATION OF WILD
FELID.OXFORD,OXFORD UNIVERSITY,762P.
OWEN-SMITH, N., MILLS, M.G.L., 2008. PREDATOR–PREY SIZE RELATIONSHIPS IN AN
AFRICAN LARGE-MAMMAL FOOD WEB.J.ANIM.ECOL.77,173–183.
PADILLA,M.&R.C.DOWLER. 1994. Tapirus terrestris. Mammalian species 481: 1-8.
POLLOCK,K.H.,1982.A CAPTURE–RECAPTURE DESIGN ROBUST TO UNEQUAL PROBABILITY OF
CAPTURE.JOURNAL OF WILDLIFE MANAGEMENT 46:757–760.
RDEVELOPMENT CORE TEAM.(2010).R: A LANGUAGE AND ENVIRONMENT FOR STATISTICAL
COMPUTING. R FOUNDATION FOR STATISTICAL COMPUTING. DISPONÍVEL EM:
HTTP://WWW.R-PROJECT.ORG.
RONDININI, C., RODRIGUES, A. S. L. & BOITANI, L. 2011. THE KEY ELEMENTS OF A
COMPREHENSIVE GLOBAL MAMMAL CONSERVATION STRATEGY.PHIL.TRANS.R.SOC.B 366:2591–2597.
ROVERO,F.,MARSHALL,A.(2009).CAMERA TRAPPING PHOTOGRAPHIC RATE AS AN INDEX OF
DENSITY IN FOREST UNGULATES.JOURNAL OF APPLIED ECOLOGY 46,1011–1017.
ROYLE,J.A.&NICHOLS,J.D.,2003.ESTIMATING ABUNDANCE FROM REPEATED PRESENCE–
ABSENCE DATA OR POINT COUNTS.ECOLOGY,84:777–790.
SALVADOR,S.,M.CLAVERO AND R.L. PITMAN.2011.LARGE MAMMAL SPECIES RICHNESS
35 SCHUETTE,P.,WAGNER,A.P.,WAGNER,M.E.,CREEL,S.2013.OCCUPANCY PATTERNS AND
NICHE PARTITIONING WITHIN A DIVERSE CARNIVORE COMMUNITY EXPOSED TO
ANTHROPOGENIC PRESSURES.BIOLOGICAL CONSERVATION 158(2013)301–312.
SILVEIRA, L., A. T. A. JACOMO, M. M.FURTADO, N. M.TORRES, R.SOLLMANN, AND C.
VYNNE. 2009. ECOLOGY OF THE GIANT ARMADILLO (PRIODONTES MAXIMUS) IN THE
GRASSLANDS OF CENTRAL BRAZIL.EDENTATA 8–9:25–34
SILVEIRA, L., JACOMO, A. T., DINIZ-FILHO,J. A. F. 2003. CAMERA TRAP, LINE TRANSECT
CENSUS AND TRACK SURVEYS: A COMPARATIVE EVALUATION. BIOLOGICAL CONSERVATION, 114(3),351-355.
SINCLAIR,A.R.E.,MDUMA,S.A.R.,BRASHARES,J.S.2003.PATTERNS OF PREDATION IN A
DIVERSE PREDATOR–PREY SYSTEM.NATURE 425,288–290.
SMYTHE,N.1983.DASYPROCTA PUNCTATA AND AGOUTI PACA.IN D.H.JANZEN (ED.).COSTA
RICAN NATURAL HISTORY, PP.463-465.UNIVERSITY OF CHICAGO,CHICAGO,ILLINOIS.
SRBEK-ARAUJO,A.C.,CHIARELLO,A.G.2005.IS CAMERA-TRAPPING AN EFFICIENT METHOD
FOR SURVEYING MAMMALS IN NEOTROPICAL FORESTS?A CASE STUDY IN SOUTH-EASTERN BRAZIL. JOURNAL OF TROPICAL ECOLOGY, 21(1),121-125.
SUNARTO,S.;KELLY,M.J.;PARAKKASI,K.;KLENZENDORF,S.;SEPTAYUDA,E.;KURNIAWAN,
H. 2012. TIGER NEED COVER: MULTI-SCALE OCCUPANCY STUDY OF THE BIG CAT IN
SUMATRAN FOREST AND PLANTATION LANDSCAPES.PLOS ONE 7(1):1-14
SUNQUIST M.,KARANTH K.U.,SUNQUIST F.1999.ECOLOGY, BEHAVIOUR AND RESILIENCE OF
36
EDS. RIDING THE TIGER: TIGER CONSERVATION IN HUMAN-DOMINATED LANDSCAPES. CAMBRIDGE:CAMBRIDGE UNIVERSITY PRESS. PP 5–18.
TANNERFELDT,M., ELMHAGEN, B., ANGERBJORN, A. 2002. EXCLUSION BY INTERFERENCE
COMPETITION? THE RELATIONSHIP BETWEEN RED AND ARTIC FOXES. OECOLOGIA 132:213-220.
TERBORGH, J., ET AL. 2001. ECOLOGICAL MELTDOWN IN PREDATOR-FREE FOREST
FRAGMENTS.SCIENCE 294:1923-1925.
TROLLE,M.&KERRY,M.(2005):CAMERA-TRAP STUDY OF OCELOT AND OTHER SECRETIVE
MAMMALS IN THE NORTHERN PANTANAL.–MAMMALIA,69:405–412
WEARN, O.R., ROWCLIFFE, M.J., CARBONE, C., BERNARD, H. AND EWERS, R.M. (2013)
ASSESSING THE STATUS OF WILD FELIDS IN A HIGHLY-DISTURBED COMMERCIAL FOREST
37
Capítulo 2 - RIQUEZA E USO DO HABITAT POR MAMÍFEROS DE
MÉDIO E GRANDE PORTE EM DUAS UNIDADES DE CONSERVAÇÃO
DA SERRA DO ESPINHAÇO
Resumo
O bioma Cerrado compreende uma elevada riqueza de mamíferos de médio e grande porte,
com grandes variações de massa corporal e ecologia entre as espécies. Diversos estudos têm
procurado entender os fatores que influenciam a riqueza e a distribuição de espécies. O nosso
objetivo foi avaliar a riqueza de espécies de mamíferos de médio e grande porte em duas
Unidades de Conservação de Proteção Integral localizadas na parte Meridional da Serra do
Espinhaço e entender os fatores que influenciam a riqueza e a taxa de registros. As
amostragens ocorreram nas estações secas dos anos de 2013 e 2014 no Parque Estadual do
Rio Preto (PERP) e Parque Nacional das Sempre-Vivas (PNSV), respectivamente. Foram
amostrados 49 pontos no PERP e 48 no PNSV. Estimamos a riqueza de espécies com
intervalo de confiança de 95% e construímos a curva do coletor para cada UC. Para avaliar
o uso do habitat obtivemos a riqueza de espécies em cada fitofisionomia de cada UC, em
duas faixas altitudinais no PERP, e a riqueza média por ponto no PNSV para correlacionar
com a densidade de focos de calor. Observamos que as duas UC’s compreendem uma
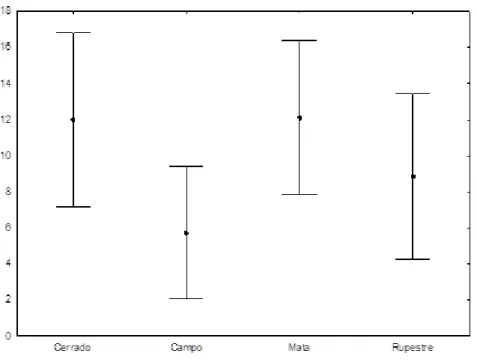
importante parcela da riqueza de espécies da Serra do Espinhaço (69,7%) e do Cerrado (54,8%) ainda que nem todas as espécies tenham sido registradas. Os ambientes de “mata” e “cerrado” compreendem uma maior riqueza de espécies em relação aos ambientes
campestres. Embora a em valores absolutos a riqueza espécies em cotas mais baixas de
altitudes no PERP tenha sido consideravelmente mais alta, esta diferença não foi
significativa, e, no PNSV, não houve uma relação entre a riqueza de espécies e a intensidade
38
Introdução
Entender os fatores que a influenciam a riqueza de espécies é um desafio constante para
ecólogos. A gama de recursos ofertados pelo ambiente, o grau de especialização das espécies
presentes aptas a utilizar os mais diversificados recursos e a capacidade das espécies
coexistirem com outras espécies que utilizam os mesmos recursos são essenciais para a
determinação da riqueza local de espécies (MACARTHUR 1972). Em geral, habitats mais
heterogêneos sustentam esses fatores mais determinantes. Tews et al. (2004) compilaram
pesquisas das últimas décadas e observaram que 85% dos estudos encontraram uma
correlação positiva entre a heterogeneidade ambiental e a riqueza de espécies para diversos
grupos da fauna. Uma parte desproporcional desses estudos, no entanto, se concentra em
respostas de aves a heterogeneidade (TEWS et al. 2004), mas essa correlação foi observada
também para mamíferos (SOUTHWELLet al. 1999; WILLIAMSet al. 2002). August (1983) por
sua vez, encontrou uma relação positiva entre a riqueza de mamíferos e a complexidade do
habitat, definida como variação vertical do habitat (quantidade de estratos da vegetação), mas
não encontrou essa correlação com a heterogeneidade do habitat, definida como variação
horizontal das fitofisionomias.
A heterogeneidade de habitats é também um fator importante para a coexistência de
espécies potencialmente competidoras e pode minimizar a extinção por competição
interespecífica, favorecendo, portanto, um incremento na riqueza local de espécies. Schuette
et al. (2013) observou no Vale do Rift, no Quênia, que espécies de carnívoros respondem de
formas distintas aos diferentes fatores ambientais e essas variações nas respostas devem
promover a diversidade local de carnívoros. Scognamillo et al. (2003) observaram na