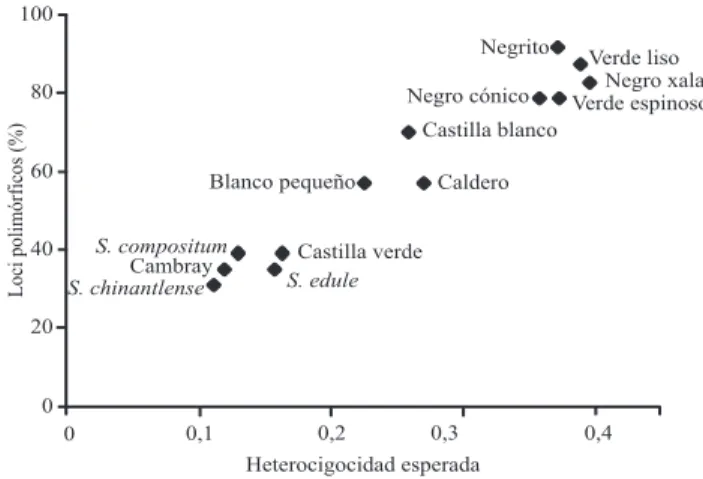
Genetic variation of an infraspecific chayote complex evaluated by isoenzimatic systems
Texto
Imagem

Documentos relacionados
Los pacientes fueron divididos en 2 grupos para tra- queotomía precoz y tardía, de acuerdo con el tiempo de intubación endotraqueal antes de la traqueotomía percutánea..
Las familias con mayor número de individuos en este estudio fueron Araneidae, Tetragnathidae, Saliticidae y Theridiidae; por lo general en otros estudios, las familias
Los resultados mostraron que las categorías sobre los sentimientos o reacciones maternas con connotación negativa o connotación positiva y la comunicación con el equipo de salud
Para identiicar diferencias entre grupos con relación a las variables de este estudio, fueron efectuadas análisis. de variancia (ANOVA) y testes t de Student
Con respecto a la concordancia entre los conceptos y las imágenes, la mayor concordancia fue del tipo 5 en cuanto que el de menor correspondencia para los médicos fueron los tipos 6
estos, 60 ancianos fueron clasificados como dependientes para las actividades básicas de la vida.. diaria y fueron descritos de acuerdo con la Clasificación Internacional
Fueron seleccionados como casos los pacientes consecutivos con diagnóstico de labio y/o paladar hendido que fueron inscritos en la clínica de labio y/o paladar hendido entre Marzo
La Figura 1 muestra los promedios horarios de PA, durante las 24 horas, en los grupos de mujeres mayores con HABB y normotensas. En los dos grupos, los promedios de PAS y PAD fueron