Capítulo 2
2.1 – RADIAÇÃO ELETROMAGNÉTICA
Tipo de energia que se transmite no espaço a uma enorme velocidade e que possui simultaneamente propriedades ondulatórias e corpusculares.
⇓
Comportamento dualístico ⇒ partícula / onda
ªModelo ondulatório ⇒ emprega parâmetros típicos, tais como: velocidade, freqüência, amplitude e comprimento de onda
⇓
explicar fenômenos tais como reflexão, refração, interferência, difração, dispersão, etc.
ªModelo corpuscular ⇒ radiação formada por partículas discretas de energia ⇓
fótons
explicar o efeito fotoelétrico e as interações entre a radiação e o meio material
• Dois modelos ⎯→ complementares ⎯→ descrição dos fenômenos associados à radiação eletromagnética e às partículas elementares
2.1.1 – PROPRIEDADES ONDULATÓRIAS:
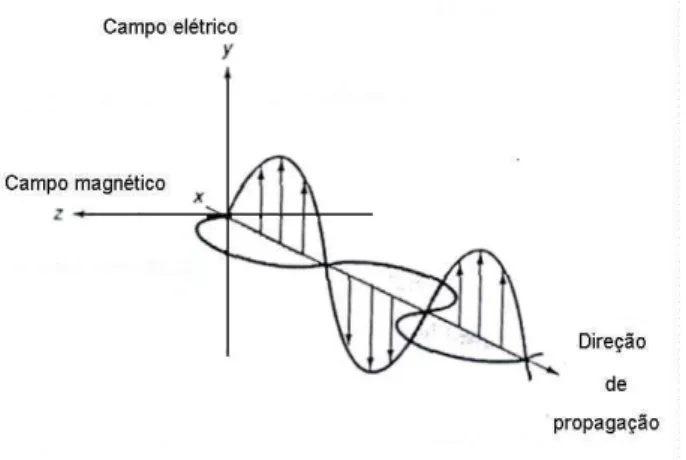
A radiação eletromagnética é um campo elétrico alternado no espaço, tendo associado um campo magnético. Esses campos são perpendiculares entre si e à direção de propagação.
• Interação entre radiação eletromagnética e o meio material apenas o componente elétrico é ativo ⎯→ restringir o estudo a este componente
Figura 2.2 – Representação bidimensional do vetor elétrico.
2.1.1.1 – Parâmetros importantes:
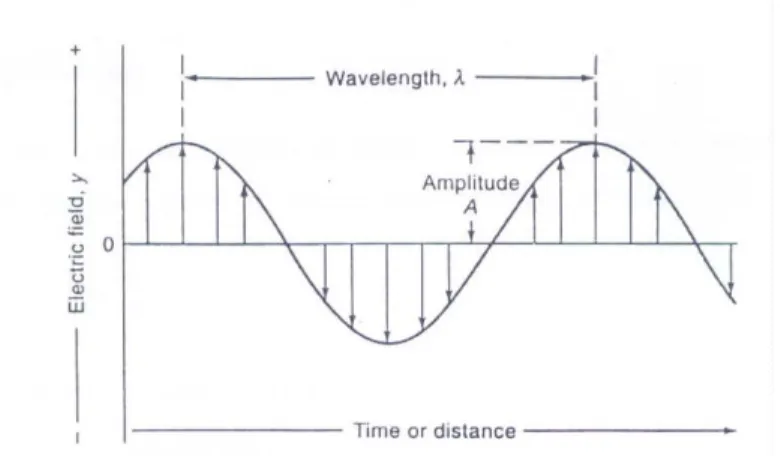
¾ Amplitude (A):
Comprimento do vetor elétrico no ponto máximo da onda.
¾ Comprimento de onda (λ):
É a distância linear entre os máximos de duas ondas sucessivas.
Unidades: Å (ângstrom) = 10-8 cm ou 10-10 m
nm (nanômetro) = 10-7 cm ou 10-9 m
µm (micrômetro) = 10-4 cm ou 10-6 m
¾ Período (τ):
Corresponde ao tempo necessário para a passagem de dois máximos sucessivos por um ponto fixo.
¾ Freqüência (ν):
Corresponde ao número de ciclos ou ondas completas que passam por um ponto fixo na unidade de tempo. É o inverso do período.
τ
ν
=
1
Unidades: ciclos / s (s-1) Hertz (Hz)
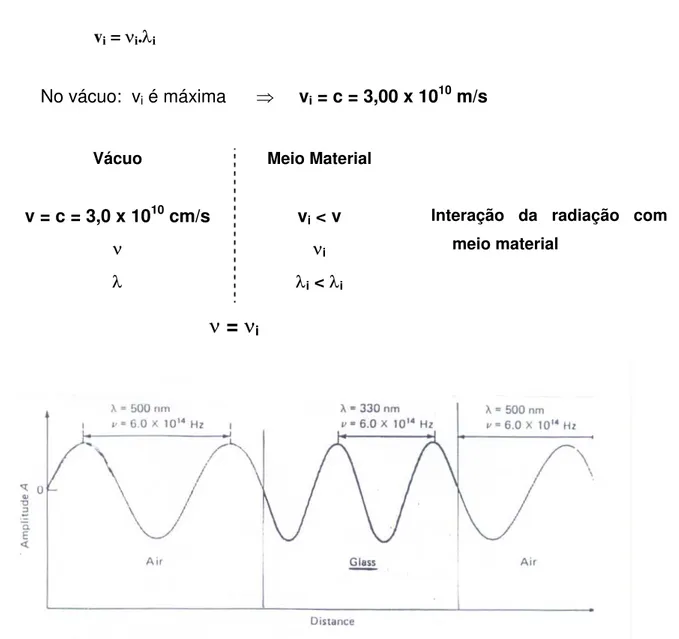
OBS: A freqüência depende apenas da fonte de radiação e permanece constante, independentemente do meio no qual a radiação se propaga.
¾ Velocidade de propagação (v):
É igual ao produto da freqüência pelo comprimento de onda. Depende do meio no qual a radiação se propaga.
vi = νi.λi
No vácuo: vi é máxima ⇒ vi = c = 3,00 x 1010 m/s
Vácuo Meio Material
v = c = 3,0 x 1010 cm/s
ν λ
vi < v
νi
λi < λi
Interação da radiação com o meio material
ν = ν
iTabela 2.1 - Diferentes regiões do espectro eletromagnético e a natureza das alterações provocadas pela radiação correspondente
Tipo de transição
quântica Nuclear
Elétrons das camadas
internas
Elétrons de valência Vibrações moleculares: alongamento,
deformação
Rotação molecular
Orientação de spin no campo magnético
elétrons núcleos
Tipo de
espectroscopia Emissão
de raios γ
Absorção, emissão,
fluores-cência e difração de raios X
Absorção no
UV vácuo Absorção, emissão e fluorescência no UV/VIS
Absorção molecular no IV e espalhamento Raman
Absorção de
microon-das
RSE RMN
Região do espectro Raios γ Raios X UV vácuo UV
próximo Visível IV próximo fundamental IV Microondas Ondas rádio de
Faixa de λ 0,005-1,4
(Å) 0,1 – 100 (Å) 10-180 nm 180-380 nm 380-780 nm 0,78 – 300 µm 0,75-3,75 mm 3 cm 0,6 – 10 m
¾ Número de onda (ν):
É o inverso do comprimento de onda em cm.
ν
ν
=
1
(cm-1)¾Potência radiante (P):
É a energia do feixe que alcança uma dada área por segundo.
P ∝ A2
OBS: Intensidade (I) é a potência por unidade de ângulo sólido.
2.1.1.2 – Espectro eletromagnético:
¾Regiões espectrais de interesse
• Raios γ • Raios X • UV/VIS • IV
¾ Radiação Policromática ⎯→ feixe comporta radiações com vários comprimentos de onda
¾ Radiação Monocromática ⎯→ feixe envolve radiação com um único comprimento de onda
¾Percepção da cor ⎯→ absorção seletiva de certos comprimentos de onda da radiação incidente pelos objetos. Os demais comprimentos de onda são transmitidos ou
refletidos e percebidos como a cor do objeto.
Faixa de λ (nm) Cor (observada) Cor complementar (absorvida)
< 380 Ultravioleta -
380-435 Violeta Verde-amarelado
435-480 Azul Amarelo 480-490 Azul-esverdeado Alaranjado 490-500 Verde-azulado Vermelho 500-560 Verde Púrpura 560-580 Verde-amarelado Violeta 580-595 Amarelo Azul
595-650 Alaranjado Azul-esverdeado
650-780 Vermelho Verde-azulado
> 780 Infravermelho -
OBS:
Objeto branco ⎯→reflete todos os comprimentos de onda Objeto negro ⎯→absorve todos os comprimentos de onda
Cor complementar + cor do objeto = luz branca
2.1.1.3 – Descrição matemática da onda:
y = A sen (
ω
t +
φ
)
sendo: ω = freqüência angular = 2 πν φ = ângulo de fase
2.1.1.4 – Sobreposição de ondas:
Princípio da sobreposição ⎯→ quando duas ou mais ondas atravessam o mesmo espaço, provocam uma perturbação que é a soma das perturbações de cada onda individualmente.
Para n ondas:
y = A
1sen (2
πν
1t +
φ
1) + A
2sen (2
πν
2t +
φ
2) + ...+ A
nsen (2
πν
nt +
φ
n)
Ex: A1 < A2 e ν1=ν2
φ1-φ2 = -20o ⇒ A > A1 ou A2 φ1-φ2 = -200o ⇒ A < A1 ou A2
Quando:
• φ1 - φ2 = 0, 360, 720, .... ⇒ ondas “em fase” ⇒ interferência construtiva máxima
•φ1 - φ2 = 180, 540, .... ⇒ ondas “fora de fase” ⇒ interferência destrutiva máxima
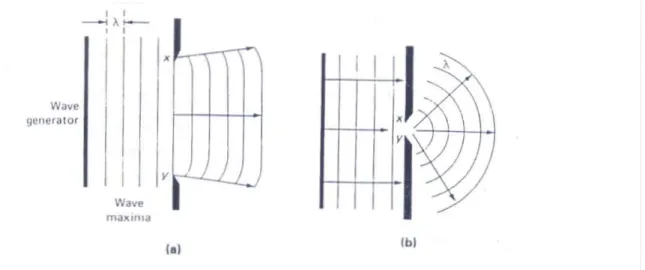
2.1.1.5 – Difração da radiação:
Figura 2.4 – Propagação de ondas através de uma fenda (a) xy >> λ ; (b) xy ≈λ
 Difração ⇒ conseqüência da interferência entre as ondas
OE >>>BC ⇒ BD // OD //CD CBF = θ
 Banda central E intensa ⎯→ sombra do material opaco que separa as fendas ⇒ Interferência construtiva entre os feixes difratados pelas duas fendas ⎯→ BE = CE
 Bandas laterais ⇒ condições de interferência construtiva
Da Figura 5(c)
CF = BC sen
θ
Como:
BC <<< OE
⇒FD
≈
BD
Então ⇒ CF ≈ diferença entre os percursos dos dois feixes (BD e CD)
Para que os feixes BC e CD estejam “em fase”
λ
= CF = BC sen
θ
Condição de reforço ocorre quando a diferença entre os percursos dos feixes for múltipla inteira de λ, sendo assim:
n
λ
= BC sen
θ
(expressão geral para as bandas laterais)sendo: n = ordem de interferência
A distância entre os feixes difratados no plano XY (DE, por exemplo), depende de OE e de BC
DE = OD sen
θ
˜
Substituindo na expressão geral
)
OD
(
)
DE
).(
BC
(
n
λ
=
) OE ( ) DE ).( BC ( ≅
2.1.1.6 – Transmissão da radiação:
vi < c ⇒ interação da radiação com o meio material sem que haja transferência
¾ Transmissão da radiação
Interação da radiação com o meio material é atribuída à polarização periódica sofrida por átomos e moléculas que constituem o meio
Radiação + Meio Material ⇒ Deformação temporária das nuvens eletrônicas (10-14–10-15s)
↓
Reemissão da radiação sem alteração no meio material (não há absorção) ↓
Freqüência da radiação não se altera, mas a velocidade de propagação diminui
¾Índice de refração(η) ⇒ uma medida da interação do meio material com a radiação
i i
v
c
=
η
Ex: líquidos ⇒ ηi = 1,3 – 1,8 sólidos ⇒ ηi = 1,3 – 2,5
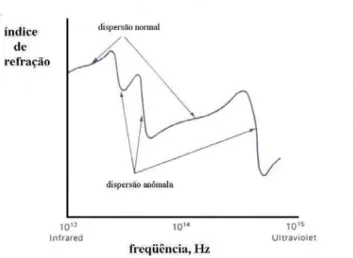
¾ Curvas de dispersão
Representação da a variação do índice de refração da substância com o comprimento de onda da radiação incidente
Figura 2.6 - Curva de dispersão típica
 Importante para escolha do material para componentes óticos dos equipamentos • Dispersão normal ⇒ lentes ⇒ ηi constante e elevado
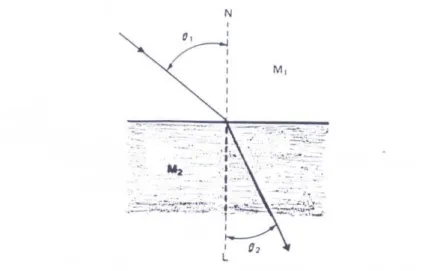
2.1.1.7 - Refração:
Corresponde à mudança na direção de propagação de um feixe luminoso que atravessa a interface entre dois meios com densidades diferentes.
Figura 2.7 - Refração da luz que passa de um meio menos denso (M1) para um mais denso (M2)
A extensão da refração é dada pela Lei de Snell
2 1 2 1
v
v
sen
sen
1 2=
=
η
η
θ
θ
Se M1 = vácuo ⇒ v1 = c e η1 = 1
Então 2 1 2
sen
)
(sen
vácuoθ
θ
η
=
Por conveniência, η é medido e reportado em relação ao ar
2 1 2
sen
)
(sen
arθ
θ
η
=
η
vácuo= 1,00027
η
ar2.1.1.8 - Reflexão:
Quando a radiação atravessa a interface entre meios com índices de refração diferentes, também ocorre reflexão.
2 1 2 2 1 2
)
(
)
(
I
I
0 rη
η
η
η
+
−
2.1.2 – PROPRIEDADES CORPUSCULARES
Quando a radiação eletromagnética é emitida ou absorvida ocorre uma transferência permanente de energia entre o objeto emissor e o meio absorvente. Para explicar esta interação admite-se que a radiação seja formada por partículas discretas de energia chamadas fótons. A energia do fóton depende da freqüência da radiação e é
dada por:
ν
=
h
.
E
ouλ
=
h
.
c
E
sendo: E = energia (erg)
h = constante de Planck (6,6 x 10-23 erg/s) ν = freqüência
λ = comprimento de onda c = 3,0 x 1010 cm/s
Nota-se que:
Fóton com alta energia alta freqüência
baixo comprimento de onda Fóton com baixa energia baixa freqüência
comprimento de onda elevado
E ↑ ν ↑ λ ↓
P ∝ número de fótons propagados por segundo
2.1.2.1 – Absorção da radiação eletromagnética
Corresponde a um tipo de interação entre a radiação eletromagnética e o meio material. Depende da estrutura das espécies atômicas ou moleculares envolvidas no processo:
Feixe Incidente Feixe Emergente
Houve absorção de radiação com freqüência ν3 pelo meio material
Energia E = h.ν3 é transferida para os átomos ou moléculas do meio material
ESTADO FUNDAMENTAL ESTADO EXCITADO
• Átomos e moléculas ⇒ número limitado de níveis energéticos, todos com energia definida ⇒ Níveis energéticos são quantizados
⇓
só fótons com energias bem definidas (E = ∆E1 ou ∆E2) podem ser absorvidos, originando
um átomo ou molécula excitada
ESTADO
FUNDAMENTAL
ESTADO EXCITADO (vida breve)
10-8 s
ESTADO FUNDAMENTAL
¾Absorção Atômica
Absorção de energia por átomos isolados
• Radiação UV/VIS ⇒ transições elétrons de valência • Raios X ⇒ transições elétrons internos
fóton
E = h.
ν
Liberação de energia:
- calor
- energia cinética
- luz
- reação
h.ν∆E1 = E1 – E0 ∆E2 = E2 – E0
Ex:
Absorção radiação UV/VIS por átomos de Na
11Na = 1s2 2s2 2p6 3s1 3p 3d ...
5p ____________________ 4f ____________________ 5s ____________________ 4p ____________________ 3d ______________________ 4s ____________________ 3p ____________________ 3s ____________________
Característica dos espectros atômicos
⇓
linhas ou raias em λ bem definidos
¾ Absorção Molecular
Absorção de radiação por moléculas no estado gasoso, líquido ou sólido.
Processo complexo:
E total = E rotacional + E vibracional + E eletrônica
sendo:
E rotacional = associada à rotação da molécula em torno de seu centro de gravidade
3s → 3p ⎯→
∆E = 2,10 eV (1eV = 1,602 x 10-12 erg)
λ
=
−−12
6
,
6
x
10
27x
3
x
10
1010
x
602
,
1
x
10
,
2
λ = 588,6 nm
3s → 5p ⎯→
∆E = 4,34 eV (1eV = 1,602 x 10-12 erg)
λ
=
−−12 27
3
x
10
10x
10
x
6
,
6
10
x
602
,
1
x
34
,
4
λ = 285 nm
λ (nm)
E vibracional = associada à vibração dos átomos dentro da molécula (estiramento,
torção, etc)
E eletrônica = estados eletrônicos dos elétrons ligantes
Todos os três componentes são quantizados (só podem assumir valores bem definidos) e além disso:
∆E
eletrônicas>>>> ∆E
vibracionais>>>> ∆E
rotacionaisUV/VIS IV microondas
Ex: Seja a absorção da radiação UV/VIS por moléculas ⇒ transições eletrônicas
∆E1=(E1+v0+r0) – (E0+v0+r0)
∆E2=(E1+v1+r2) – (E0+v0+r0)
∆E3=(E1+v2+r0) – (E0+v1+r0)
• Observa-se que o número de transições eletrônicas possíveis entre os níveis 1 e 2 é muito grande, todas eles com energias muito próximas
Características dos espectros de absorção molecular na região UV/VIS
⇓
Bandas de absorção largas abrangendo vários comprimentos de onda
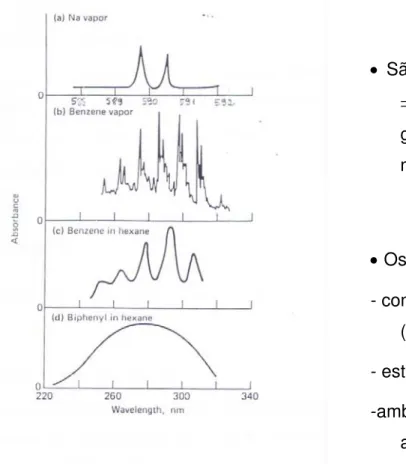
¾ Espectros de Absorção
Representação da variação da absorvância em função do comprimento de onda da radiação incidente.
Figura 2.8 - Espectros de absorção no UV-VIS
• São específicos da espécie absorvente ⇒ identificação desta espécie ou de grupos funcionais presentes na molécula.
• Os espectros de absorção dependem:
- complexidade da partícula absorvente (átomos, moléculas, íons)
- estado físico
-ambiente que envolve a partícula absorvente
OBS:
• Amostras sólidas, líquidas ou em presença de solvente ⎯→ alargamento maior das bandas ⎯→ espectro contínuo
• Transições vibracionais ⇒ radiação IV
- espectro ⎯→ picos ou bandas estreitas ⎯→ transição entre os vários níveis vibracionais de um mesmo nível eletrônico (fundamental)
2.1.2.2 - Processos de relaxação
Retorno ⇒ ESTADO EXCITADO ⎯→ ESTADO FUNDAMENTAL
¾ Relaxação não radiativa
Liberação da energia ocorre numa série de pequenas etapas.
energia de excitação ⇒ energia cinética (colisões entre moléculas) ↓
pequeno aumento em T
¾ Relaxação por fluorescência ou por fosforescência
• Fluorescência ⇒ t ≈ 10-5 s
∗ Fluorescência de ressonância
- processo no qual a radiação emitida tem freqüência idêntica à da radiação que promoveu a excitação (radiação absorvida)
- átomos no estado gasoso
∗ Fluorescência não ressonante
- moléculas em solução ou em fase gasosa ⇒ tempo de vida estados vibracionais excitados (10-15 s) <<< tempo de vida dos estados eletrônicos excitados (10-8 s)
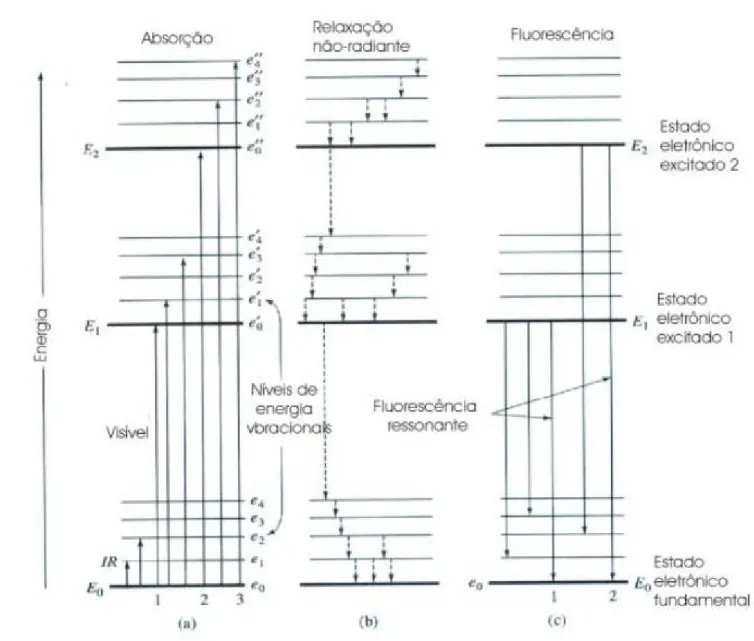
relaxação vibracional ocorre antes da relaxação eletrônica ↓
energia emitida é menor que a absorvida ↓
Figura 2.9- Diagrama parcial dos níveis de energia de uma molécula orgânica fluorescente
• Fosforescência ⇒t > 10-5 s
- ocorre quando a molécula excitada relaxa para um estado eletrônico metaestável, no qual o tempo de vida é maior que 10-5 s. Isso ocorre devido a inversão do spin
do elétron.
2.1.2.3 - Emissão de radiação
Ocorre quando partículas excitadas (átomos, moléculas ou íons) retornam a estados de energia menores emitindo fótons.
¾ Fontes de excitação
• Bombardeamento com elétrons ou outras partículas elementares ⇒ emissão de raios X
• Exposição a corrente elétrica (centelha) ou ao calor de chama, forno ou arco elétrico ⇒ emissão UV/VIS, IV
• Irradiação com feixe de radiação eletromagnética ⇒ emissão radiação fluorescente
¾ Espectro de emissão
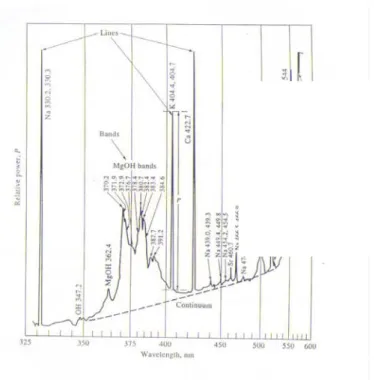
Figura 2.10 –Espectro de emissão de salmoura obtido com chama O2/H2
• Três tipos de espectro:
- Linhas
- Bandas
• Espectro de linhas
∗ UV/VIS ⇒ emissão por átomos em fase gasosa
• Espectro de bandas
- emissão por radicais ou moléculas pequenas
•Espectro contínuo
- Sólidos aquecidos até a incandescência espectro contínuo característico da temperatura do corpo emissor (Radiação do corpo negro)
Figura 2.12 – Curvas de radiação características do corpo negro
2.2 - ASPECTOS QUANTITATIVOS DAS MEDIDAS ESPECTROSCÓPICAS
2.2.1 - MÉTODOS ESPECTROQUÍMICOS
Classe Potência medida Relação com a
concentração Tipo de método
Emissão Pe (emitida) Pe = kC Emissão atômica
Luminescência Pl (luminescente) Pl = kC
Fluorescência, fosforescência e quimiluminescência atômica e molecular
Espalhamento Ps (espalhada) Ps = kC Turbidimetria, nefelometria
Absorção P0 (incidente), P (transmitida) kC P
P log
0 =
− Absorção atômica e molecular
¾ Medidas de potência radiante
Detetores ⇒ energia radiante ⎯⎯→ sinal elétrico
 Emissão, luminescência, espalhamento
P = kC
eS = kP + k
d⇒
S = k’C + k
dsendo: k’ ⎯→ determinado com auxílio de padrões
 Absorção
λ
Duas grandezas são definidas ⇒ Transmitância e Absorvância:
(a) Transmitância (T)
0
P
P
T
=
oux
100
P
P
(%)
T
0=
(b) Absorvância ou Absorbância (A)
P
P
log
)
T
log(
P
P
log
A
0 0=
−
=
−
=
A ∝ C ⇒ Lei de Beer
Exercícios
1) Calcular a freqüência em Hertz, a energia em Joules and a energia em elétron-volts de um fóton de raio X com comprimento de onda de 2,70Å.
2) Calcular a velocidade, freqüência e o comprimento de onda da linha D do sódio (λ=589nm) quando ela atravessa uma célula ótica cujo índice de refração (nD) é 1,43.
3) Quando alinha D do sódio atravessa uma interface ar/diamante com um ângulo de incidência de 30o ela sofre difração num ângulo de 11,9o . Qual o índice de refração do diamante ?
4) Qual o comprimento de onda do fóton que tem três vezes mais energia que um fóton com comprimento de onda 500nm ?
5) A energia de ligação do iodeto de prata é aproximadamente igual a 255kJ/mol. Qual o maior comprimento de onda de luz capaz de quebrar a ligação do iodeto de prata ?
6) O césio metálico é extensivamente usado em fotocélulas e câmeras de televisão devido à sua baixa energia de ionização (a menor entre os elementos químicos estáveis). Qual a energia cinética máxima de um fotoelétron ejetado da superfície do metal quando sobre esta incide luz com comprimento de onda de 500nm ? Considerar que o maior comprimento de onda capaz de arrancar elétrons da superfície do césio é 660nm.
7) Calcular o comprimento de onda:
(a) da linda D do sódio (λ=589nm) em uma solução aquosa com índice de refração de 1,35. (b) da linha de emissão de um laser de rubi (λ=694,3nm) quando ela passa através de uma
peça de quartzo com índice de refração igual a 1,55.
8) Calcular a perda por reflexão (expressar em % da intensidade do feixe incidente) quando um feixe de radiação passa através de uma placa de quartzo. Admitir que o índice de refração do quartzo é 1,55.
9) Converter as absorvâncias abaixo em transmitâncias percentuais. (a) 0,375 (b) 1,325 (c) 0,012
10) Dadas as transmitâncias abaixo, calcular as absorvâncias correspondentes. (a) 33,6% (b) 92,1% (c) 1,75%
11) Calcular as transmitâncias percentuais das soluções cujas absorvâncias são iguais à metade das absorvâncias do problema 9.
12) Calcular as absorvâncias das soluções cujas transmitâncias são a metade daquelas do problema 10.
Respostas
1) ν=1,111x1018 Hz E=7,333x10-16 J E=4,576x103 eV 2) 411,9 nm
3) 2,425 4) 166,7 nm 5) 466nm 6) 9,6x10-20 J
7) (a) 436,3 nm (b)447,9 nm 8) perda total = 9,08%
9) (a) 42,17% (b) 4,73% (c) 97,27% 10) (a) 0,4737 (b) 0,0357 (c) 1,757