UNIVERSIDADE FEDERAL DA PARAÍBA CENTRO DE CIÊNCIAS DA SAÚDE
PROGRAMA DE PÓS-GRADUAÇÃO EM ODONTOLOGIA
DANIELLE BEZERRA ALMEIDA
CONCENTRAÇÕES DE FLÚOR EM SALIVA E URINA DE CRIANÇAS
APÓS USO DE PRODUTOS FLUORETADOS
Dissertação apresentada ao Programa de Pós-Graduação em Odontologia da Universidade Federal da Paraíba (UFPB), em cumprimento às exigências para obtenção do título de Mestre em Odontologia, Área de concentração Preventiva e Infantil.
Orientador: Prof. Dr. Fábio Correia Sampaio Co-orientador: Profa. Dra. Andressa Feitosa Bezerra de Oliveira
JOÃO PESSOA-PB
FOLHA DE APROVAÇÃO
DANIELLE BEZERRA ALMEIDA
CONCENTRAÇÕES DE FLÚOR EM SALIVA E URINA DE CRIANÇAS
APÓS USO DE PRODUTOS FLUORETADOS
Dissertação apresentada ao Programa de Pós-Graduação em Odontologia da Universidade Federal da Paraíba (UFPB) para obtenção do título de Mestre em Odontologia, Área de concentração Preventiva e Infantil.
Aprovada em ____/____/____
BANCA EXAMINADORA
__________________________________ Prof. Dr. Fábio Correia Sampaio
Universidade Federal da Paraíba Orientador
__________________________________ Prof. Dr. Saul Martins de Paiva Universidade Federal de Minas Gerais
Membro efetivo
__________________________________ Prof. Dr Franklin Delano Soares Forte
AGRADECIMENTOS
Aos voluntários que participaram desta pesquisa, pelo senso de cooperação,
desprendimento e dedicação.
Ao Prof. Dr. Fábio Correia Sampaio, por ter sido um orientador atencioso nos
momentos da realização desta dissertação, onde pude aprimorar meus conhecimentos através deste trabalho científico, meu eterno agradecimento.
A Profa. Dra. Andressa Feitosa Bezerra de Oliveira, por ter me aceitado como
orientanda no processo de seleção do mestrado.
Aos meus queridos amigos, em especial Kalyne, Janine, Marianne, Jean, Juliana, Phelipe, Marcos Jr e Giovanni por terem paciência comigo nestes dois anos de dedicação ao curso e nos períodos de ausência, principalmente neste momento final de conclusão de redação.
Aos amigos de laboratório, em especial Andréa, Fabíola e Aninha, pela ajuda, conversas, desabafos e por compartilhar momentos de alegrias e amizade.
As minhas colegas de Mestrado de Preventiva e Infantil, especialmente a amiga Calina, e aos meus colegas de Pós-Graduação, pelos bons momentos passados.
Aos queridos colegas Anselmo, Maria Regina e Calina por me ajudarem a controlar o tempo de coletas de saliva.
AGRADECIMENTOS ESPECIAIS
Ao Prof. Dr. Franklin Delano Soares Forte, como meu “eterno” orientador que
acompanhou de perto, na clínica de Cariologia da UFPB, o início deste estudo. Obrigada pela amizade, apoio e incentivo nos momentos de fraqueza.
Aos meus irmãos, Cintia e Hélio Júnior pelo apoio e incentivo constante.
Ao Juliano, pelo amor, dedicação, companheirismo e paciência.
Dona Rita pelo abraço carinhoso!
RESUMO
ALMEIDA, D.B. Concentrações de flúor em saliva e urina de crianças após uso de produtos fluoretados. 2009. 80f. Dissertação (Mestrado em Odontologia — Área de Concentração em Odontologia Preventiva Infantil) — Programa de Pós-Graduação em Odontologia, Universidade Federal da Paraíba, João Pessoa, PB, 2009.
O objetivo desse estudo foi de mensurar a concentração de flúor em saliva e na urina de crianças expostas a fluoretos tópicos de uso profissional. O delineamento desse estudo é clínico, aleatório e cruzado. Participaram 17 crianças com idades entre 6 e 12 anos, de ambos os sexos, com manchas brancas ativas em superfícies lisas, necessitando de fluorterapia. Escovas e dentifrícios foram fornecidos aos voluntários, onde n= 11 receberam dentifrício de 1.100 ppm e n= 6 dentifrício sem flúor. Os produtos fluoretados utilizados foram: gel neutro (9.000 ppm), espuma neutra (12.300 ppm) e verniz (22.600 ppm). As aplicações do gel (5g) e a espuma (1,5g) foram em moldeiras por 1 minuto e o verniz (0,5g) com pincel, cobrindo toda a superfície vestibular do dentes. As coletas de saliva foram feitas no dia da aplicação dos produtos fluoretados nos seguintes tempos: 0, 3, 6, 9, 15, 30, 45 e 60 minutos. As coletas de urina foram feitas por 24 horas. Sendo, 24 horas dividida em dois períodos: diurno ou 11horas (coleta das 7:00 h às 18:00 h) e período noturno ou de 13 horas (coleta das 18:00 h às 7:00 h). Nas análises das amostras de saliva e urina utilizou-se um eletrodo combinado íon-específico da ORION (9409BN) com eletrodo de referência (900200), ambos acoplados a um potenciômetro 720 A (ThermoOrion). Os dados foram digitados no SPSS v. 13.0, submetidos a testes estatísticos e considerados significativos com p< 0,05. Os resultados indicaram uma maior concentração de flúor na saliva após 3 minutos de uso do verniz, gel e espuma, os valores (ppmF) foram de 99,33 ± 59,8; 95,02 ± 82,2 e 75,51 ± 41,0, respectivamente. A excreção de flúor na urina foi maior para verniz, espuma e gel com valores (ppmF) de 1,1± 7,1; 0,6 ± 0,3 e 0,6± 0,6, respectivamente. Pode-se concluir que os valores mais elevados de flúor na saliva independentemente do tempo de medição foram obtidos com o verniz. Para a excreção do flúor seguiu uma tendência semelhante, apresentando valores mais elevados para o verniz e sugerindo que este produto pode produzir uma elevada ingestão de flúor.
ABSTRACT
ALMEIDA, D.B. Fluoride concentrations in saliva and urine of children after use of fluoride products. 2009. 80f. Dissertation (Master´s Program in Dentistry — Area of concentration Preventive Dentistry and Pedodontics) — Post-Graduation Program in Dentistry, Federal University of Paraiba, João Pessoa, PB, 2009.
The aim of this study was to measure the bioavailability of fluoride in saliva and to observe the pattern of urinary fluoride excretion in children exposed to topical fluoride products of professional use. Seventeen children of 6- 12-years-old, both genders with active white spots on smooth surfaces, no cavities and needing fluoride treatment were included in the study. All volunteers (n=17) received toothbrushes and fluoridated toothpaste (1,100 ppm, 11 volunteers) and no fluoride (6 volunteers) eight days before fluoride a application. A wash-out period of 7 days was established before and after the exposure of neutral gel fluoride (9,000 ppm), foam (12,300 ppm) and varnish (22,600 ppm). Except for the varnish, the fluoridated gel (5g) and foam (1.5g) were applied in trays. /the products were applied for one minute covering all buccal surfaces. Saliva was collected in the following times: 0, 3, 6, 9, 15, 30, 45 and 60 minutes. Urine was collected covering the 24 hours of baseline and after application of the products covering 11 and 13 hours of collection to cover day and night periods as (7:00-18:00 h) and (18:00-7:00 h). Fluoride was measured with the aid of ion specific electrode ORION (9409BN) coupled to a potenciometer (720 A,ThermoOrion). Data statistical analyses were performed in SPSS v. 13.0 applying p< 0.05. The results indicated a higher concentration of fluoride in saliva after 3 minutes of using varnish, foam and gel, the values are 95.02 ± 82.2 ppmF, ppmF 41.0 ± 75.51 and 99.33 ± 59, 8 ppm F, respectively. The excretion of fluoride in urine was higher for varnish, foam and gel, the values are 1.1 ± 7.1 ppm F, 0.6 ± 0.3 ppm F and 0.6 ± 0.6 ppm F, respectively. It can be concluded that the highest values of salivary fluoride regardless the time of measurement were achieved by the fluoride varnish. For the urinary fluoride followed a similar trend showing higher values for the varnish and suggesting that this product can produce a high ingestion of fluoride.
LISTA DE GRÁFICOS
GRÁFICO 1: Médias das concentrações de flúor em saliva ao longo de 60 minutos após aplicação do gel. João Pessoa, PB, Brasil, 2009...48
GRÁFICO 2: Médias das concentrações de flúor em saliva ao longo de 60 minutos após aplicação da espuma. João Pessoa, PB, Brasil, 2009...49
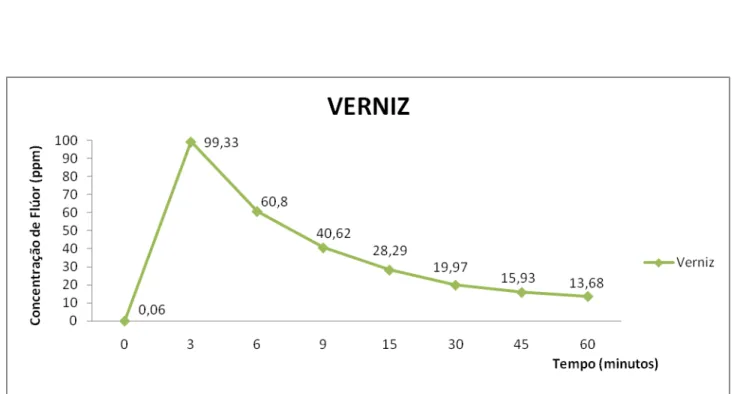
GRÁFICO 3: Médias das concentrações de flúor em saliva ao longo de 60 minutos após aplicação do verniz. João Pessoa, PB, Brasil, 2009...50
LISTA DE TABELAS
TABELA 1: Cálculos dos volumes de urina e das concentrações de flúor no período diurno (7:00 às 18:00 h). João Pessoa, PB, Brasil, 2009...43
TABELA 2: Detalhamento das concentrações de flúor nos produtos, nas amostras e estimativas de exposição ao flúor pelos voluntários. João Pessoa, PB, Brasil, 2009...47
TABELA 3: Médias e desvio padrão (DP) das concentrações de flúor em saliva ao longo de 60 minutos após aplicação do gel. João Pessoa, PB, Brasil, 2009...48
TABELA 4: Médias e desvio padrão (DP) das concentrações de flúor em saliva ao longo de 60 minutos após aplicação da espuma. João Pessoa, PB, Brasil, 2009...49
TABELA 5: Médias e desvio padrão (DP) das concentrações de flúor em saliva ao longo de 60 minutos após aplicação do verniz. João Pessoa, PB, Brasil, 2009...50
TABELA 6: Médias e desvio padrão (DP) das concentrações de flúor em ppmF na saliva ao longo de 60 minutos após aplicação dos produtos fluoretados. João Pessoa, PB, Brasil, 2009...51
TABELA 7: Variáveis relacionadas com a excreção urinária e concentrações de flúor na urina no baseline diurno (11:00 h). João Pessoa, PB, Brasil, 2009...52
TABELA 8: Variáveis relacionadas com a excreção urinária e concentrações de flúor na urina no período diurno (11:00 h), após aplicação dos produtos fluoretados. João Pessoa, PB, Brasil, 2009...53
TABELA 9: Variáveis relacionadas com a excreção urinária e concentrações de flúor na urina no baseline noturno (13:00 h). João Pessoa, PB, Brasil, 2009....54
TABELA 10: Variáveis relacionadas com a excreção urinária e concentrações de flúor na urina no período noturno (13:00 h), após aplicação dos produtos fluoretados. João Pessoa, PB, Brasil, 2009...55
TABELA 11: Variáveis relacionadas com a excreção urinária e concentrações de flúor na urina no baseline de 24:00 h. João Pessoa, PB, Brasil, 2009...56
LISTA DE QUADRO
LISTA DE FIGURA
FIGURA 1: Representação esquemática do desenho do estudo...32
FIGURA 2: Produtos fluoretados utilizados na pesquisa...34
FIGURA 3: Tubos de ensaios e funis utilizados para as coletas de saliva...37
FIGURA 4: Tubos de microcentrífugas com amostras de saliva... ...37
FIGURA 5: Micro-centrífuga com micro-tubos, TISAB III, ponteiras e pipetas...38
FIGURA 6: Potenciômetro, soluções padrões de pH 4.0 e 7.0, eletrodo para medir pH e amostras de urina...40
FIGURA 7: Garrafas para as coletas de urina por período...42
LISTA DE ABREVIATURAS
F- íon flúor
pH potencial hidrogeniônico CaF2 fluoreto de cálcio
% porcentagem
[F] concentração de flúor
ppmF parte por milhão de fluoreto mg miligrama
PAIHAP produto de atividade iônica em relação à hidroxiapatita KPSHAP produto de solubilidade da hidroxiapatita
M Molar
mL mililitro
CEP comitê de ética em pesquisa
g grama
oC grau Celsius
LABIAL laboratório de biologia bucal
TISAB tampão de ajuste de força iônica total mV milivoltagem
h hora
min minuto
L litro
Kg kilograma
μg microgramas
SPSS Statistical Package for Social Sciences UFPB Universidade Federal da Paraíba NaOH hidróxido de sódio
FT flúor total
FI flúor iônico solúvel FST flúor solúvel total
SUMÁRIO
1 INTRODUÇÃO...15
2 REVISÃO DE LITERATURA...17
2.1GENERALIDADES E HISTÓRICO DO FLÚOR...17
2.2 MECANISMO DE AÇÃO DO FLÚOR...18
2.3METABOLISMO DO FLÚOR...20
2.3.1 Saliva...21
2.3.1 Urina ...23
2.4 MÉTODOS PROFISSIONAIS DE APLICAÇÃO TÓPICA DE FLÚOR...25
2.4.1 Gel...25
2.4.2 Espuma ...26
2.4.3 Verniz...27
3 OBJETIVOS...29
4 MATERIAL E MÉTODO...30
4.1 TIPO DE ESTUDO...30
4.2 AMOSTRA ...33
4.3 OBTENÇÃO DO BASELINE...33
4.4PRODUTOS UTILIZADOS...34
4. 5 FORMAS E TEMPOS DE APLICAÇÃO DOS PRODUTOS...35
4.6 COLETA DE SALIVA...36
4.6.1 ANÁLISE DE FLÚOR...37
4.7 ESTUDO 2 - COLETA DE URINA...39
4.7.1 ANÁLISE DE pH...40
4.7.2 ANÁLISE DE FLÚOR...40
4.8 DOSAGEM DE FLÚOR NOS PRODUTOS...44
4.9 ANÁLISE ESTATÍSTICA...46
5 RESULTADOS...47
6 DISCUSSÃO...58
7 CONCLUSÃO...64
REFERÊNCIAS...65
APÊNDICES...73
1 INTRODUÇÃO
A prevalência da cárie dentária, embora esteja em declínio em vários países, é ainda considerado problema de saúde pública, pois envolve um grande número de indivíduos, causando sofrimento, perda dentária, sérias conseqüências estéticas e problemas mastigatórios. Além do mais, sabe-se que através da adequação de hábitos alimentares e de higiene, associado ao efetivo controle do biofilme e a ações preventivas, pode-se controlar a doença cárie (TENUTA; CURY, 2005).
O flúor exerce papel importante no declínio da cárie dentária, quer seja através de seu uso em sistemas de abastecimento de água, dentifrícios, associado aos métodos mecânicos de remoção ou desorganização do biofilme dental, como também utilizado nos fluoretos tópicos de uso profissional.
É importante que se estude a excreção dos fluoretos, pois a mesma pode ser um bom indicador de exposição em crianças e adultos. Principalmente nos indivíduos na primeira infância, que estão susceptíveis ao desenvolvimento de fluorose dentária (MARTHALER, 1999; MARTHALER et al., 2000). Estima-se que dos fluoretos ingeridos, em torno de 50% são excretados via urina durante as 24 horas seguintes a sua ingestão e a maior parte fica associado aos tecidos calcificados (WHITFORD, 1990; WHITFORD, 1996).
Além da urina, o monitoramento da exposição dos indivíduos aos fluoretos pode ser feito através da determinação de seus níveis no plasma, biofilme dental, fluido do biofilme, unhas, cabelos e saliva (WHITFORD, 1990; SAMPAIO, 2000). A concentração e excreção dos fluoretos na urina não dependente apenas dos níveis no plasma, mas também são influenciados pelo fluxo urinário, pH e outros fatores (WHITFORD, 1996; MARTHALER, 1996).
Acredita-se que o flúor presente na boca na forma lábil seja mais benéfico durante desafio carioso (FUKUSHIMA et al., 2000; ten CATE, 2004).
A concentração de flúor na saliva após aplicações de produtos fluoretados serve como um reservatório bucal de flúor, ficando retidos, por exemplo: na língua, mucosa bucal e biofilme. O flúor é liberado de forma gradual (SJÖGREN; BIRKHED, 2004). Diferentes formulações de flúor, a concentração do fluoreto e o tempo de aplicação são importantes para influenciar o nível de flúor na cavidade bucal (ZERO et al., 1992).
2 REVISÃO DE LITERATURA
2.1 GENERALIDADES E HISTÓRICO DO FLÚOR
O elemento mais eletronegativo da tabela periódica é o flúor. E deve-se ao seu pequeno raio atômico. É o 13º elemento mais abundante na natureza, apresentando cor amarelo-pálido, odor característico, propriedades tóxicas e em temperatura ambiente é um elemento gasoso e naturalmente compõe a biosfera (NARVAI, 2000). Devido a sua elevada reatividade, raramente o encontramos em seu estado rudimentar, é encontrado mais comumente na combinação na forma iônica F- e na forma eletrovalente ou covalente (FEJERSKOV; KIDD, 2005). Pertence a família VIIA ou grupo 17 da tabela periódica e tem como símbolo a letra F, número atômico 9 e peso atômico 19. O flúor tem grande afinidade por elementos metais alcalinos e alcalinos terrosos, particularmente pelo cálcio, sódio e magnésio. Com estes elementos forma composto iônicos de elevada importância.
O flúor é amplamente estudado na Odontologia. Nas primeiras décadas do século XX, McKay e Black relacionaram os dentes mosqueados e marrons aos altos teores de flúor nas águas de abastecimento público na cidade de Colorado Springs (EUA) (BLACK; MCKAY, 1916). Esses dentes mosqueados e marrons também foram observados em outras cidades dos EUA bem como nos países Inglaterra e Itália (HUNSTRABRATEN, 1982). Entre 1933 e 1945, Henry Trendley Dean realizou vários
estudos epidemiológicos, conhecido como ―Estudo das 21 Cidades‖. Nestes estudos
Desde então, o flúor vem sendo utilizado na odontologia e sua ação terapêutica para o declínio da cárie dentária é comprovada, melhorando significativamente a saúde bucal da população. Apesar de haver um consenso na relação existente entre o uso do flúor e a redução da cárie dentária. O flúor pode ser uma substância tóxica capaz de causar efeitos colaterais quando são ingeridas em altas doses (toxicidade aguda) ou
quando em baixas doses (≥ 1 ppmF) são ingeridas diariamente (toxicidade crônica).
2.2 MECANISMOS DE AÇÃO DO FLÚOR
Os microorganismos presentes no biofilme dental após metabolizar carboidratos, principalmente a sacarose, produzem ácidos que diminuem o pH no meio bucal, fazendo com que a camada inicial de fosfato de cálcio do esmalte dentário dissolva, formando lesão cariosa. Essa lesão pode variar de acordo com o grau de desmineralização, de uma mancha branca até completa destruição da coroa dentária (STEPHAN, 1940; GUSTAFSSON et al., 1954).
Existem três teorias que se destacam para explicar o mecanismo de ação do flúor. As teorias: formação do esmalte, formação do fluoreto de cálcio e antibacteriano (CURY, 2001; FEJERSKOV; KIDD, 2005).
A incorporação do flúor no momento de formação dos prismas de esmalte é importante, substituindo a hidroxiapatita por fluorapatita (CHAVES, 1977). Viegas (1989) acreditava que uma vez exposto ao flúor o indivíduo estaria permanentemente protegido da cárie dentária, mas tal evento não é verdadeiro. A presença constante do flúor é importante, mesmo que em pequenas concentrações, nos sucessivos episódios de desmineralização e mineralização superficial, pois o mesmo será incorporado na forma de flúor-hidroxiapatita e confere maior resistência a superfície dentária, pois este é menos solúvel aos ácidos presentes no processo carioso. Apesar de haver a formação de fluorapatita durante a mineralização do esmalte dentário, o processo que confere maior resistência a superfície do dente ocorre durante toda a vida.
(FA), ou F fortemente ligado e 2. reservatórios tipo fluoreto de cálcio (CaF2), ou F fracamente ligado (SAXEGAARD; RÖLLA, 1988).
Por muito tempo acreditou-se que o efeito anti-cárie dos métodos de aplicação tópica de F era resultado do aumento da FA no esmalte, enquanto o reservatório fluoreto de cálcio seria consumido rapidamente em contato com a saliva (BRUDEVOLD et al., 1967). Atualmente considera-se que o efeito do F na inibição do desenvolvimento de cárie é basicamente tópico, quando presente no biofilme dental para atuar na diminuição da desmineralização e ativação da remineralização do esmalte (ten CATE, 1999). Devido à deposição de uma camada de fosfato sobre os glóbulos de fluoreto de cálcio diminui-se a solubilidade desse composto na saliva (RÖLLA; ÖGAARD, 1986; SAXEGAARD; LAGERLÖF; RÖLLA, 1988; ÖGAARD et al., 1990). Com a diminuição do pH do biofilme dental a camada de fosfato dissolve-se, liberando F para atuar no processo de remineralização. Quando ocorrem desafios cariogênicos (paciente de alto risco) com elevada freqüência é sugerido aplicações profissionais de produtos fluoretados para repor flúor perdido e aumentar a formação de CaF2.
Para que haja um equilíbrio no meio bucal e não ocorra perda mineral do dente é necessário que o produto de atividade iônica em relação à hidroxiapatita (PAIHAP) e o produto de solubilidade da hidroxiapatita (KPSHAP) sejam iguais, havendo homeostase. O PAIHAP depende da concentração de íons livres na saliva, como Ca+2, PO4-3 e OH-, enquanto que o KPSHAP é uma constante pré-definida de quanto de íons livres precisa para formar a HAP. Quando o PAIHAP é maior do que KPSHAP, significa que há mais íons disponíveis/livre no meio bucal e assim ocorrerá a remineralização dos tecidos dentais (BUZALAF et al., 2008).
A outra teoria de ação do flúor é quando os microorganismos da cavidade bucal absorvem o flúor topicamente disponível. Causando interferência no mecanismo de transporte de açúcar pela bactéria através da inibição da atividade enzimática e no controle do pH intracelular, reduzindo conseqüentemente a produção de ácidos (SHELLIS; DUCKWORTH, 1994). No entanto, para que esta ação antimicrobiana do flúor seja de fato considerada, há necessidade de haver uma situação de elevada concentração de flúor no biofilme e por certo período de tempo (LOVEREN, 2004).
2.3 METABOLISMO DO FLÚOR
Fluorterapia é definida como sendo o uso de fluoretos para o tratamento de alterações minerais provocadas pela doença cárie que decorrem da presença de biofilme dental e desafio cariogênico, manifestadas por meio de perdas mineras progressivas, as quais no início são clinicamente invisíveis e quando esta desmineralização não é revertida, atingem o estágio de mancha branca e progridem para a cavitação (CURY, 1991). Medeiros e Souza (1994) afirmam que os fluoretos são eficazes para interferir em tais perdas, por meio da paralisação e/ou reversão das lesões de cárie incipientes.
O destino dos fluoretos no corpo pode ser diferente de acordo com sua forma de administração:
Tópica, através de dentifrício, verniz, gel, espuma, bochecho, entre outros, o flúor é incorporado ao esmalte na forma de glóbulos de CaF2, que vão funcionar de
reservatório de fluoreto e serão disponibilizados durante a baixa de pH após o consumo de alimentos cariogênicos.
mecanismo dependente do pH urinário. Retorna a cavidade bucal através da saliva e como já citado anteriormente substituindo parte da apatita, em função disso denomina-se de apatita fluoretada ou fluorapatita. De certa forma essa característica confere uma resistência nos períodos de desmineralização (WHITFORD, 1996).
2.3.1 Saliva
A saliva é composta por vários eletrólitos, incluindo sódio, potássio, cálcio, magnésio, bicarbonato e fosfatos. Também são encontrados na saliva imunoglobulinas, proteínas, enzimas, mucinas, e produtos nitrogenados, como uréia e amônia. Estes componentes interagem em funções relacionadas nas seguintes áreas gerais: (1) bicarbonatos, fosfatos, uréia e agem para modular o pH e a capacidade tampão da saliva (2); macromoléculas protéicas e mucinas servem para limpar, agregar, e / ou anexar microrganismos orais e contribuir para o metabolismo do biofilme; (3) cálcio, fosfato e proteínas trabalham juntos como fator modular da desmineralização e remineralização; e (4) imunoglobulinas, proteínas e enzimas fornecem ação antibacteriana (HUMPHREY; WILLIAMSON, 2001). Entre os constituintes da saliva está o flúor que pode ser proveniente do metabolismo do flúor no organismo como também pelo contato com produtos fluoretados de uso caseiro ou profissional.
A permanência e a eliminação do flúor pela saliva é um processo referido
usualmente pelo termo ―clearence‖ que será influenciado por fatores fisiológicos
individuais e pelo grau de exposição do flúor à cavidade bucal. Durante o uso regular de dentifrícios fluoretados, há um aumento desse íon na saliva. Portanto, os estudos de clearence salivar refletem a situação in vivo diretamente, proporcionando desta maneira uma medida mais apropriada de biodisponibilidade do flúor após tratamentos tópicos; ao contrário dos dados obtidos em estudo in vitro (DUCKWORTTH; MORGAN;
As baixas concentrações de íons flúor (> 0,04 ppmF) na cavidade bucal desempenham um papel importante na eficácia da prevenção da cárie dentária (FEJERSKOV; THYLSTRUP; LARSEN, 1981; MARGOLIS; MORENO, 1990). Após a aplicação tópica de produtos fluoretados, os níveis de flúor aumentam na saliva e tornam-se disponíveis para a interação com a superfície do dente em um determinado tempo (OLIVEBY; EKSTRAND; LAGERLOF, 1987). A concentração de flúor presente nos fluídos bucais após a aplicação de flúor é influenciada pela concentração do produto fluoretado, tempo desde a última exposição e o método de aplicação. E esses influenciam o clearance e a retenção de flúor. Em um estudo determinou que o bochecho com NaF 0,05% produziu um rápido aumento no nível de flúor salivar que volta a concentração inicial após 2 a 4 horas (ZERO et al., 1988).
O clearance salivar de fluoreto tem sido estudado. O estudo mais amplo na depuração de flúor salivar foi relatado por Bruun et al. (1982), que acompanhou a concentração de flúor na saliva após diferentes tratamentos com flúor tópico e encontraram três distintamente diferentes curvas de fluoreto: (i) curva a curto prazo após a eliminação do uso de flúor, contendo creme dental, comprimidos, ou goma de mascar, (ii) curva de eliminação de longo prazo após a aplicação tópica de F 1,23% ou 2%, solução de NaF; e (iii) curva de eliminação intermediária decorrentes de bochechos com solução de NaF 0,2%. No primeiro grupo, os níveis iniciais de flúor na saliva variaram de 1352- 4472 µmol/L, mas voltou aos níveis normais em 1 a 2 horas. Depois da aplicação de 1,23 % F ou 2% NaF, os níveis de flúor na saliva foram cerca de 520 µmol /L após uma 1 h e permaneceram elevados até 11h de após o tratamento. E com enxaguatório de 0,2% NaF resultou em níveis elevados de flúor com duração de aproximadamente 3 horas.
No estudo clínico de cárie de Leverett et al. (1993a e 1993b) mostrou que teores de flúor na saliva acima de 0,04 ppmF relaciona-se com menor risco da progressão da doença. Além disso, teores de flúor de acima de 0,08 ppm na saliva foram relacionados a baixa progressão de cárie em um subseqüente estudo longitudinal de avaliação de risco (SHIELDS et al., 1997).
precipitado dissolve-se, liberando lentamente uma baixa concentração de íon flúor livre na saliva. O fluoreto de cálcio precipitado é armazenado na superfície do dente e em outros sítios inespecíficos, com o passar do tempo mantém a concentração mínima na saliva, garantindo uma remineralização. Estes produtos com alta concentração de flúor não necessita ser aplicado diariamente (JACOBSEN; YOUNG, 2003).
2.3.2 Urina
É importante que se estude a excreção dos fluoretos, pois a mesma pode ser um bom indicador de exposição em crianças e adultos; principalmente nos indivíduos na primeira infância, que estão susceptíveis ao desenvolvimento de fluorose dentária (MARTHALER, 1999; MARTHALER et al., 2000). Estima-se que dos fluoretos ingeridos, em torno de 50% são excretados via urina durante as 24 horas seguintes a sua ingestão; e a maior parte fica associado aos tecidos calcificados (WHITFORD, 1990; WHITFORD, 1996).
A excreção está associada ao pH urinário. Desta forma, existe ainda a possibilidade de reabsorção (redifusão) do fluoreto em função do pH, sendo essa semelhante ao que acontece no estômago, que envolve a difusão do ácido fluorídrico no epitélio, já que o íon flúor é impermeável (WHITFORD, 1990; WHITFORD, 1994).
Quando a urina está relativamente alcalina, quase todo o fluoreto que se encontra no interior do túbulo renal, encontra-se na forma iônica e, devido o seu tamanho e carga, permanece no interior do túbulo renal para ser excretado. Quando a urina encontra-se relativamente ácida, há uma maior formação de ácido fluorídrico, e é reabsorvido o líquido intersticial. (WHITFORD, 1990; WHITFORD, 1999)
Alguns fatores podem alterar o pH urinário, entre eles, destacam-se: composição da dieta, certos medicamentos (diuréticos), doenças metabólicas, como, diabetes
mellitus e acidose tubular renal.
no nível de flúor na urina pode ser causado não apenas pela água fluoretada, mas pela inalação de partículas fluoretadas e pela dieta.
No estudo de Forte et al. (2008) após avaliar a excreção de fluoreto na urina de crianças de 2 a 7 anos de idade expostos a água com diferentes concentrações de fluoreto na cidade de Catolé do Rocha, PB, Brasil. Observou-se que o dentifrício de fluoreto (1.510 ppm) não promoveu aumento da excreção urinária de fluoreto. Houve uma tendência, embora não significativa, como para o aumento da concentração de fluoreto na urina em relação às concentrações de fluoreto na água.
A medição da taxa de excreção urinário do flúor foi recomendada como um método adequado para monitorar a ingestão de flúor em crianças consumindo ou sal fluoretado ou água fluoretada (MARTHALER et al., 1995), e há um relatório sobre coleta de urina em 24 h, para estimar a ingestão de flúor entre crianças de 4 anos do Sri Lanka e Inglaterra (RUGG-GUNN et al. 1993).
As taxas de excreção urinária de F estão sendo usadas atualmente para controlar vários programas de fluoretação (VILLA et al. 1997; WANG; BIAN; PHILLIPS, 1997). Para esse controle teria que relacionar a ingestão de flúor consumida diariamente pelas crianças.
Uma alternativa a coleta de urina de 24 horas seria relacionando a excreção de flúor, através da creatinina como observamos no estudo de Zohouri et al. (2006) com 7 crianças, idade média de 32 meses (intervalo: 16-36 meses), saudáveis que residiam em uma área com água fluoretada. Amostras de alimentos e bebidas foram analisadas quanto ao teor de flúor. Ingestão de flúor a partir de pasta de dentes também foi medida. Amostras de urina de 24 h e de manhã foram coletadas de cada criança. A média de ingestão diária total de flúor foi de 0,71 (±0,41 mg) ou 0,05 (±0,02) mg / kg de peso corporal, dos quais 37% eram provenientes da dieta, sendo o restante da ingestão de creme dental. Nenhuma das crianças usava outras fontes de flúor, tais como comprimidos de flúor ou sal fluoretado. A média de F / Cr foi de 1,49 (±0,63) mg F / g de creatinina. A relação entre o F / Cr de uma amostra de urina matinal podem ser usados para estimativa média da excreção urinária de flúor de 24 horas. Estimativa da excreção de flúor urinário em 24 horas pode ser usada para medir exposição ao flúor.
uma menor excreção fracionária de fluoreto pelas crianças quando comparadas com adultos, devido nas crianças apresentarem mais ―sítios‖ de deposição de flúor nos tecidos duros.
2.4 MÉTODOS PROFISSIONAIS DE APLICAÇÃO TÓPICA DE FLÚOR
Os métodos de uso do flúor podem ser divididos didaticamente em dois grupos: tópicos e sistêmicos ou profissional e caseiro. As concentrações de flúor nos produtos de uso caseiro são: de 1 ppmF em água fluoretada, 225 ppmF em enxaguatórios de uso diário, 900 ppmF em enxaguatórios semanais, 1.000- 1.500 ppmF em cremes dentais e 5.000 ppmF em géis e cremes dentais quanto prescritos. E nos de aplicação profissional variam de 4.000- 12.300 ppmF em géis e espuma ou mousses e de 22.600 ppmF em verniz (JACOBSEN; YOUNG, 2003).
Entre os fluoretos tópico de uso profissional, destacamos: gel, espuma e verniz.
2.4.1 Gel
técnica, além de não provocar manchamento nos dentes e restaurações (CURY, 2001; FEJERSKOV; KIDD, 2005).
Em geral aplica-se o gel com o auxílio de moldeiras pré-fabricadas, pois permite que o produto tenha um contato mais efetivo com as áreas interproximais.
2.4.2 Espuma
As espumas ou mousses fluoretados surgiram como veículo mais recentemente e são indicados especialmente para crianças inclusive bebês. Tem composição parecida com a do gel de FFA, mas devido a sua menor densidade, uma menor quantidade de fluoreto é utilizada por aplicação, tornando-o mais seguro no aspecto de toxicidade. (BUZALAF, 2008). As pesquisas mostram que a quantidade de fluoreto utilizada na moldeira é aproximadamente 4 a 5 vezes menos quando comparada com o gel, apresentando a mesma concentração (WEI; CHIK, 1990; WHITFORD et al., 1995). Basicamente a técnica de aplicação é similar a forma de aplicação do gel que é feito com auxílio de moldeiras.
No estudo de Jiang (2005) de aplicação de espuma bi-anual mostrou-se significativamente eficaz na redução do incremento de cárie proximais superfícies, mas não significativo na superfície oclusal. Esse dado foi semelhante com os achados de Seppä et al. (1995), que mostrou que a aplicação tópica de flúor pode garantir a prevenção de superfícies lisas, mas teve efeito limitado sobre fossas e fissuras em dentes.
concentração de flúor na saliva. Portanto, recomendou-se a aplicação tópica de flúor na forma de espuma, com base na menor probabilidade de toxicidade durante seu uso.
2.4.3 Verniz
Desenvolvidos na Europa há mais de 30 anos (ELLWOOD; FEJERSKOV, 2005), o verniz fluoretado é um veículo de aplicação tópica com alta concentração de flúor, tendo uma resina natural como base e surgiu com o objetivo principal de aumentar os efeitos preventivos e terapêuticos das formulações tópicas de flúor. Apresenta características como maior concentração de flúor, poder de retenção nas superfícies dentárias aplicadas proporcionando um aumento no tempo de exposição aos fluoretos e conseqüente aumento da formação de fluoreto de cálcio na superfície dentária e prolonga a ação remineralizadora das lesões de cárie (BELTRÁN-AGUILAR et al., 2000; SEPPÄ, 1991). Ele contém 5% de fluoreto de sódio (equivalente a 2,26% de flúor) em uma base de colofônia natural, apresentado como um material viscoso amarelado que, ao tomar presa, torna-se uma cobertura de cor marrom-amarelada sobre o dente.
Quando aplicado sobre a superfície dentária o verniz fluoretado forma uma capa aderente que pode permanecer aproximadamente 24 horas. Durante este período o paciente recebe orientações para não escovar sobre o verniz. Tal situação promove a formação de fluoreto de cálcio (CaF2) na superfície aplicada liberando, lentamente e em altas concentrações, íons flúor que participam ativamente no processo de remineralização do esmalte dental (OGAARD; SEPPA; ROLLA, 1994; SËPPA; PÖLLANEN; HAUSEN, 1994; ten CATE, 1997; ten CATE, 2004).
prevalência de cárie (HAWKINS et al., 2004; CURY, 2001; OGAARD; SEPPA; ROLLA, 1994; SËPPA; PÖLLANEN; HAUSEN, 1994).
Outras vantagens deste produto seriam a facilidade de aplicação, diminuição do tempo de trabalho, alta margem de segurança, além de não exigir do paciente elevada cooperação (DI NICOLÓ et al., 1997). Como desvantagem Warren, Henson e Chan (2000) citaram a descoloração temporária dos dentes no dia da aplicação. Um fato notório é a disparidade de preço entre os produtos fluoretados, o verniz chega a ser 14 vezes mais caro que o gel, em âmbito nacional.
Hawkins et al.(2004), comparou os custos e aceitabilidade de crianças de alto risco de cárie da região de York e da cidade de Hamilton, Ontário, Canadá, que tinham sido identificadas com necessitando de fluorterapias (n = 256) à aplicação tópica de dois métodos (espuma e verniz). As crianças receberam espuma em moldeiras ou verniz fluoretado pincelados nas superfícies dentárias. O tempo de aplicação do verniz (5,81 min.) foi significativamente menor em comparação com espuma (7,86 minutos). Os sinais de engasgos foram observados em uma menor proporção de participantes que receberam verniz (3,8%) quando comparados a espuma (15,1%), e esta diferença foi maior para as crianças 3-6 anos de 2,6% e 29,7%, respectivamente para verniz e espuma. Portanto, o uso de flúor verniz em programas de prevenção da cárie foi indicado, especialmente para crianças mais novas.
3 OBJETIVOS:
3.1: Mensurar a concentração de flúor presente na saliva de crianças em função do tempo depois da aplicação dos produtos fluoretados gel, espuma e verniz.
4 MATERIAL E MÉTODO
O protocolo de pesquisa referente à este trabalho foi apreciado e aprovado pela Comissão de Avaliação de Projetos do Programa de Pós-Graduação em Odontologia da UFPB e pelo Comitê de Ética em Pesquisa em Seres Humanos do Centro de Ciências da Saúde da Universidade Federal da Paraíba.(ANEXO1)
4.1 TIPO DE ESTUDO
Este estudo é do tipo clínico, aleatório e cruzado. Este desenho de estudo minimiza variações individuais, visto que todos os voluntários usaram todos os produtos fluoretados (ALMEIDA FILHO e ROUQUAYROL, 2006). Nesta pesquisa utilizou-se os produtos: gel, espuma e verniz (especificação no Quadro 1).
O protocolo de aplicações e coleta de amostras está detalhado na Figura 1. Os dentifrícios usados nesta pesquisa foram:
- Dentifrícios utilizados: 11 voluntários utilizaram como dentifrício padrão o Tandy® (1.100 ppm) e 6 o dentifrício Phillips®.
- Aplicação dos produtos fluoretados: para cada voluntário sorteou-se a ordem de qual produto seria aplicado a cada semana.
- Os Kits (escova + dentifrício padrão) foram entregues aos voluntários 8 dias antes da aplicação. Para o período de wash-out (7 dias escovando com o dentifrício para padronização do meio bucal). O período de wash-out foi em três momentos: antes de aplicar o primeiro produto e no intervalo da aplicação dos outros dois.
- Coletas de saliva: No dia da aplicação as coletas foram feitas nos seguintes tempos: 0, 3, 6, 9, 15, 30, 45 e 60 minutos.
* 1ª Coleta (Urina-baseline): No dia anterior a aplicação dos produtos fluoretados.
4.2 AMOSTRA
Nesta pesquisa foram incluídas 17 crianças com idades entre 6 e 12 anos, de ambos os sexos, que tinham manchas brancas ativas em superfícies lisas, necessitando de fluorterapia, sem lesões cavitadas nos dentes decíduos ou permanentes. As mesmas residiam em João Pessoa, onde não existe a fluoretação de água pública (ALVES; SAMPAIO, 2004).
Foram incluídos os voluntários, cujos responsáveis assinaram o termo de consentimento livre e esclarecido conforme a Resolução 196 do CEP (APÊNDICE 1), e através dos relatos dos responsáveis as crianças selecionadas eram: sadias, não tomavam medicamentos, suplementos a base de flúor e produtos que podia alterar o fluxo salivar. Não participaram deste estudo crianças usuárias de aparelhos ortodônticos, com deficiências físicas, irradiadas, desnutridas e imunodeprimidas.
Inicialmente foram agendas reuniões com as mães e ou responsáveis pelas crianças explicando os objetivos do projeto e a metodologia empregada, para que o protocolo fosse seguido, deixando claro que a qualquer momento o voluntário poderia desistir de participar do experimento e que a identidade dos participantes são confidenciais. Nesta etapa foi apresentado o Termo de Consentimento Livre e Esclarecido para cada pai e ou responsável pelas crianças, quando receberam os insumos de higiene bucal (escova de dentes e o dentifrício fluoretado Tandy® (1.100 ppmF ) ou Phillips®(sem flúor), além de serem ressaltadas as medidas de manutenção caseira das condições de saúde bucal.
4.3 OBTENÇÃO DO BASELINE:
crianças foram convidadas a participarem do presente estudo. Alguns voluntários utilizaram os dentifrícios fluoretados Tandy® (1.100 ppmF, a base de sílica- Colgate-Palmolive, Osasco-SP, Brasil) e outros o Phillips (sem flúor- GlaxoSmithKline Brasil Ltda., Rio de Janeiro -RJ, Brasil) fornecidos pela pesquisadora por um período mínimo de sete dias, antes de serem feitas as aplicações com os produtos fluoretados de uso tópico.
4.4 PRODUTOS UTILIZADOS:
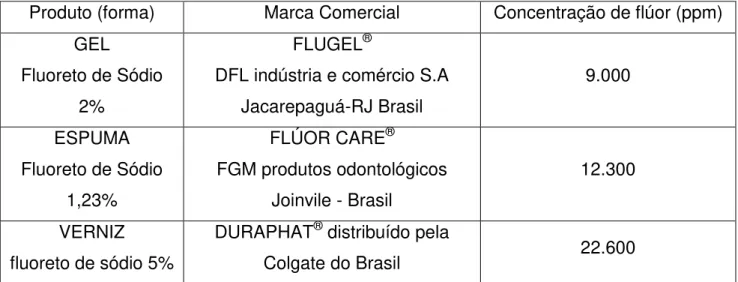
Os produtos utilizados foram os seguintes:
Produto (forma) Marca Comercial Concentração de flúor (ppm) GEL
Fluoreto de Sódio 2%
FLUGEL®
DFL indústria e comércio S.A Jacarepaguá-RJ Brasil
9.000
ESPUMA Fluoreto de Sódio
1,23%
FLÚOR CARE®
FGM produtos odontológicos Joinvile - Brasil
12.300
VERNIZ fluoreto de sódio 5%
DURAPHAT® distribuído pela
Colgate do Brasil 22.600
Quadro 1: Especificação dos produtos fluoretados da pesquisa.
Fonte: Dados da pesquisa
Todos os produtos selecionados para esta pesquisa são agentes tópicos de uso profissional e utilizados na Clínica para controle de manchas brancas ativas. Sendo assim, os produtos foram sorteados antes da aplicação tópica, de forma que os voluntários usaram todos os produtos. Após a pesquisa foi dada continuidade ao tratamento dentário das crianças.
4.5 FORMAS E TEMPOS DE APLICAÇÃO DOS PRODUTOS:
Foi realizado isolamento relativo com algodão e com sugador. Em seguida foram aplicados os produtos, no caso do gel e da espuma foram aplicado com auxílio de moldeira, por um tempo de 1 minuto, onde usamos 5g e 0,75g, respectivamente. Já com o verniz a aplicação foi feita através de pincel usando 0,50g do produto. O tempo de aplicação entre cada produto foi de 7 dias (período de wash-out). E nesse período o voluntário usou apenas o dentifrício fornecido na pesquisa. Os produtos foram pesados previamente à aplicação, em balança de precisão Scout TM Pro (OHAUS®,New Jersey, USA). O gel e a espuma foram pesados nas moldeiras e o verniz nos casulos, antes de pesar os produtos, a balança foi zerada para desconsiderar o peso das moldeiras e do casulo.
As aplicações dos produtos seguiram o protocolo de atendimento da Clínica de Cariologia-UFPB. Sendo assim:
Para o Gel acidulado e espuma:
Medidas preventivas antes: explicou-se ao responsável e a criança o procedimento que seria realizado e preparou-se o material a ser utilizado.
- Foi feita a profilaxia dos dentes com pedra pomes e água, com auxílio da escova de Robinson;
- Preparou-se previamente a cavidade bucal com rolinhos de algodão e posicionou-se o sugador,
- O gel e a espuma foram pesados antes das aplicações, nas próprias moldeiras, em balança de precisão;
- Posicionou-se o paciente sentado na cadeira odontológica com o apoio das costas na vertical, evitando a deglutição do produto;
- Secou-se previamente os elementos dentários Medidas durante a aplicação:
- Foi controlada a saliva com o sugador e foi dada atenção ao paciente. Procedimentos depois da aplicação:
- recomendações: não podiam se alimentar nos 60 minutos subseqüentes a aplicação e cuspiam 2 vezes após a aplicação do produto, eliminando o excesso, para assim começar a contar o tempo com o cronômetro e serem coletada a saliva nos tempos determinados.
Para o verniz fluoretado:
Procedimentos antes: explicou-se ao responsável e para a criança o procedimento realizado, foi feita a profilaxia dos dentes com pedra pomes e água, com auxílio da escova de Robinson, isolou-se com rolinhos de algodão, posicionou-se o sugador e preparou-se o material a ser utilizado;
Durante: aplicou-se com pincéis descartáveis posicionados em cabos específicos disponíveis na clínica, pincelando nos dentes.
Depois: orientou-se para não remover o verniz dos dentes, alimentação pastosa a líquida nas 12 horas subseqüentes a aplicação, bem como não escovar os dentes.
4.6 COLETA DE SALIVA:
Utilizou-se a técnica da saliva não estimulada, a qual foi realizada sempre no período da manhã e por um único operador, a pesquisadora. Antes do início da coleta foi realizada uma explicação verbal para as crianças de forma individual do que seria realizado.
identificados com o código do voluntário, tempo, produto utilizado. Os tempos de coleta de saliva foram 0 (baseline), 3, 6, 9, 15, 30, 45 e 60 minutos após a aplicação do produto fluoretado. Durante este período os voluntários permaneceram sentados e não ingeriram comida ou bebida alguma.
Após essa fase as salivas foram centrifugadas, pipetadas e armazenadas tubo microcentrífuga 2,0mL graduado, tampa com trava (Axygen, Califórnia,USA) e mantidas sob refrigeração 4oC. Cada voluntário tinha um funil para cada tempo de coleta. Todos os tubos e funis foram previamente e posteriormente lavados com água destilada e deionizada.
O local de coletas das salivas foi realizado na clínica de Cariologia da Universidade Federal da Paraíba e sua análise foi realizada no Laboratório de Biologia Bucal (LABIAL).
Fonte: Dados da pesquisa Fonte: Dados da pesquisa
FIGURA 3: Tubos de ensaios e funis FIGURA 4: Tubos de microcentrífuga utilizados para as coletas de saliva. com amostras de saliva.
4.6.1 ANÁLISE DE FLÚOR
O flúor iônico e ionizável presente nos padrões e nas amostras foram determinados após calibração do eletrodo específico para flúor (ORION 9409BN) associado a um eletrodo de referência (900200) e ambos acoplados a um potenciômetro 720A (ThermoOrion, MA, USA). A concentração de flúor nas amostras foi calculada a partir da regressão linear das curvas de calibração, obtidas por padrões com concentrações de flúor variando de 0,05; 0,1; 0,2; 0,4; 0,8; 1,6; 3,2; 6,4; 12,8; 25,6 e 51,2 ppm F em água deionizada, feitas a partir de padrão de 100 ppm F (ORION).
No total foram 360 amostras de salivas analisadas. A exatidão das leituras foi avaliada por testes com soluções de concentrações conhecidas de flúor. O volume de 0,5 mL de saliva foi pipetado ao qual adicionou 0,05 mL de TISAB III (Total Ionic Strength Adjustment Buffer) e foram feitas as leituras em milivolts (mV), em duplicata para cada padrão, que foram registrados. Os potenciais de milivoltagens foram convertidos em ppmF utilizando-se para isso uma curva padrão com coeficiente de regressão r2 ≥0.99. As médias das leituras dos padrões foram inseridas em planilha do Excel® e então calculadas a porcentagem de variação entre a quantidade mensurada e a esperada nos padrões conhecidos. Somente curvas de calibração com porcentagem de variação de até 10% foram consideradas.
Fonte: Dados da pesquisa
4.7 ESTUDO 2 - COLETA DA URINA
Essa metodologia foi baseada na publicação de Marthaler (1999) - o monitoramento da excreção renal em comunidades de programas preventivos de saúde bucal da Organização Mundial de Saúde (1999). As mães foram treinadas para a coleta da urina em 24 horas (Marthaler, 1999), adaptado por Villa et al.(2008). Dividiu-se a coleta de urina de 24 horas em dois períodos: diurno e noturno, que começavam às 7h às 18h e das 18h às 07h, respectivamente.
A urina foi coletada 24 horas antecedentes à aplicação dos produtos na Clínica, nos turnos pré-estabelecidos. Os voluntários foram orientados a coletarem a urina em recipientes plásticos com capacidade de 1 L fornecidos pela pesquisadora, que foram previamente rotulados e identificados. Sendo assim, o recipiente 1 continha o volume de urina de 11 horas e o recipiente 2 tinha o volume de urina de 13 horas antes da aplicação do produto. O recipientes 3 e 4 continha o volume de urina de 11 e 13 horas, respectivamente, após a aplicação do produto fluoretado, totalizando 24 horas de urina. Todos os recipientes foram fechados com as tampas próprias do recipiente plástico evitando a evaporação.
Após a medição do volume de urina excretado pelo voluntário nos períodos de 11 e 13 horas foram retirados 15 mL e coletados em tubos plásticos (Cral®, São Paulo -SP, Brasil), previamente identificados com o número e nome da criança. Com o auxílio de uma proveta era medido o volume restante, ao qual era somada os 15mL colocados no tubo; todas essas informações eram anotadas em fichas próprias.
4.7.1 ANÁLISE DE pH
Para análise de pH utilizou-se um eletrodo de pH em vidro 420A(Orion, Massachusetts, USA) acoplado a um potenciômetro 290A+ (Orion, Massachusetts, USA). Para calibração foram utilizadas as soluções padrões de pH 4,01 e 7,0 com slope superior a 90%.
Fonte: Dados da pesquisa
FIGURA 6: Potenciômetro, soluções padrões de pH 4,0 e 7,0, eletrodo para medir pH e amostras de urina.
4.7.2 ANÁLISE DE FLÚOR
ppmF utilizando-se para isso uma curva padrão com coeficiente de regressão r2 ≥0.99.
As médias das leituras dos padrões foram inseridas em planilha do Excel® e então calculadas a porcentagem de variação entre a quantidade mensurada e a esperada nos padrões conhecidos. Somente curvas de calibração com porcentagem de variação de até 10% foram consideradas.
Os dados foram analisados e anotados em ficha de Marthaler et al. (1999), adaptado por Villa et al. (2008).
Tabela 1 - (Para 11 horas de coleta- período diurno) A- Dados pessoais e exposição a fluoretos:
(1) Número do sujeito na pesquisa, (2) nome, (3) gênero, (4) idade (anos), (5) data de nascimento, (6) peso em (kg).
B- Dados laboratoriais:
7- o tempo inicial da coleta de urina (horas e minutos); 8- o tempo final da coleta de urina (horas e minutos); 9- volume (mL) da urina;
10- concentrações de fluoretos em ppm; C- Dados preliminares:
11- duração da coleta (horas, decimais);
12- quantidade de fluoreto na urina em microgramas (μg) foi obtida multiplicando o valor em mL da urina com a concentração de fluoreto em ppm (o valor do número 9 multiplicando com o 10);
13- fator de correção para exatas 11h foi obtido dividindo 11 pela duração da coleta (11 divido pelo valor da coluna 11);
D- Resultados ajustados a 11 horas:
14- fator de correção do volume de urina em 11h é obtido multiplicando o volume em mL pelo fator de correção para exatas 11h (o valor da coluna 9 multiplicando o da coluna 13);
E- 11 horas resultados por 1 hora:
16- fluxo urinário (mL/horas) (valor da coluna 14 dividido por 11);
17- fator de excreção de fluoretos urinária em hora/hora (valor da coluna 15 dividido por 11);
F- Resultados por Kg e horas:
18- volume em 11 horas por Kg /peso/altura, foi obtido dividindo o valor do peso corporal pela correção do volume urinário em mL (valor da coluna 14 dividido pela coluna 6);
19- excreção urinária de fluoretos por peso corporal, foi obtido dividindo o valor da excreção de fluoretos em 11h (μg) pelo peso corporal (Kg) (valor da coluna 15 dividido pela coluna 6)
Foram feitas as mesmas tabelas de cálculos para as coletas de 13h e 24h. Para a tabela de 24h, os volumes e concentrações de 11h e 13h foram somados para dar o volume total e concentrações totais de 24h, respectivamente. Ainda no cálculo das variáveis de 24h considerou-se os valores brutos de 11h e 13h para obtenção das médias.
Fonte: Dados da pesquisa Fonte: Dados da pesquisa
FIGURA 7: Garrafas para as coletas de urina FIGURA 8: Eletrodo específico para
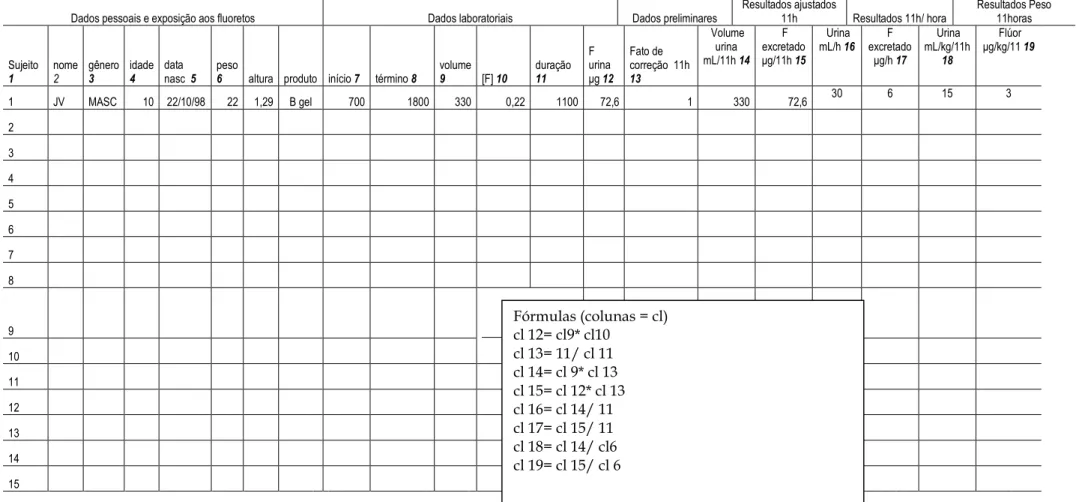
Tabela 1 –Planilha para o banco de dados da Pesquisa ― Concentrações de flúor em saliva e urina de
crianças após uso de produtos fluoretados‖ para período diurno de 11 horas (7:00 às 18:00)
Dados pessoais e exposição aos fluoretos Dados laboratoriais Dados preliminares
Resultados ajustados
11h Resultados 11h/ hora
Resultados Peso 11horas Sujeito 1 nome 2 gênero 3 idade 4 data nasc 5
peso
6 altura produto início 7 término 8
volume
9 [F] 10
duração
11
F urina
μg 12
Fato de correção 11h
13
Volume urina mL/11h 14
F excretado
μg/11h 15
Urina mL/h 16
F excretado
μg/h 17
Urina mL/kg/11h
18
Flúor
μg/kg/11 19
1 JV MASC 10 22/10/98 22 1,29 B gel 700 1800 330 0,22 1100 72,6 1 330 72,6 30 6 15 3
2
3
4
5
6
7
8
9
10
11
12
13
14
15
Fórmulas (colunas = cl) cl 12= cl9* cl10
4.8 DOSAGEM DE FLÚOR NOS PRODUTOS:
4.8.1 DENTIFRÍCIOS
Pesou-se 100 mg de dentifrício e colocou-se em um tubo plástico graduado para centrífuga. E adicionou-se 10 mL de água destilada e deionizada e homogeneizou-se em um agitador de tubos MA-162 (MARCONI- Piracicaba-SP, Brasil), para obtenção de uma suspensão homogênea. Para dosagem de flúor total (FT), retirou-se 0,25 mL da suspensão e transferiu-se a um tubo de ensaio plástico e acrescentou-se 0,25 mL de HCl 2M. Esta solução permaneceu em agitação durante 1h a 45ª C. Após esse tempo, foram adicionados 0,5 mL de NaOH 1M e 1mL de TISAB II sendo a amostra levada para dosagem de FT. Para dosagem de flúor solúvel total (FST) e flúor iônico solúvel (FI), a suspensão do dentifrício foi submetida à centrifugação de 3.000 rpm durante 10 minutos. Para análise do FST retirou-se 0,25 mL do sobrenadante e transferiu-se para tubo de ensaio plástico e adicionou-se 0,25 mL de HCl 2M. Após agitação por 1h a 45º C foram adicionados ao tubo 0,5 mL de NaOH 1M e 1 mL de TISAB II. Para análise de FI pipetou-se 0,25 mL do sobrenadante e acrescentou-se 0,25 mL de NaOH 1M e 1mL de TISAB II (a leitura feita imediatamente).
4.8.2 GEL E ESPUMA
4.8.3 VERNIZ
Pesou-se 1 gota de verniz (0,08 g) e em seguida colocou-se 50mL de água destilada e deionizada, em um erlenmeyer e manteve por 5 minutos em 100º C. Em seguida a solução foi colocada em um balão volumétrico e completou-se o volume até 100mL. Para análise, pipetou-se 1 mL desta solução e 1mL de TISAB II.
PREPARO DOS PADRÕES PARA CURVA DE CALIBRAÇÃO
Previamente às leituras das amostras, foram feitas leitura da curva de calibração com soluções padrões de íons flúor contendo de 0,5 a 8 ppmF em HCl 0,25M, NaOH 0,25M e TISAB II a 50%. As leituras de todas as amostras e padrões foram feitas em triplicata, sob agitação magnética, utilizando-se agitador magnético e barras magnéticas. As médias das leituras dos padrões foram inseridas em planilha do Excel® e então calculadas a porcentagem de variação entre a quantidade mensurada e a esperada nos padrões conhecidos. Somente curvas de calibração com porcentagem de variação de até 10% foram consideradas.
CÁLCULOS DAS CONCENTRAÇÕES DE FLÚOR NOS PRODUTOS UTILIZADOS
DENTIFRÍCIOS: O cálculo final de flúor foi obtido pela fórmula: μgF calculado x (diluição) /peso. Para cálculo do flúor ionizável (MFP) partiu-se da dosagem do FST e subtraiu-se o valor encontrado de FI (MFP= FST- FI). No cálculo do flúor insolúvel (Fins), partiu-se da dosagem do FT e subtraiu-se o valor encontrado de FST (Fins.= FT- FST).
Comprovou-se que o dentifrício Tandy® tinha acima de 1.000 ppmF e o Phillips® não apresentava flúor.
GEL e ESPUMA: multiplicou-se o a média da concentração de flúor por 2.000. VERNIZ: multiplicou-se o a média da concentração de flúor por 3.000.
4.9 ANÁLISE ESTATÍSTICA
Os dados foram digitados e tratados no pacote estatístico SPSS v. 13.0.
5 RESULTADOS
Os resultados a seguir são apresentados na forma de tabelas e gráficos.
TABELA 2 – Detalhamento das concentrações de flúor nos produtos, nas amostras e estimativas de exposição ao flúor pelos voluntários. João Pessoa, PB, Brasil, 2009.
PRODUTO CONCENTRAÇÃO DE FLÚOR [F] ESTIMATIVA DA [F] NA AMOSTRA APLICADA
INFORMADO
(ppm) DETERMINADO (ppm) QUANTIDADE DE PRODUTO APLICADO (mg)
[F]
(mg) MÉDIA DE PESO VOLUNTÁRIOS (Kg) (SD)
DOSE ESTIMADA
(mg/Kg)
GEL 9.000 8.740 5.000 43,70
31,3 (7,6)
1,39
ESPUMA 12.300 11.260 1.500 16,89 0,53
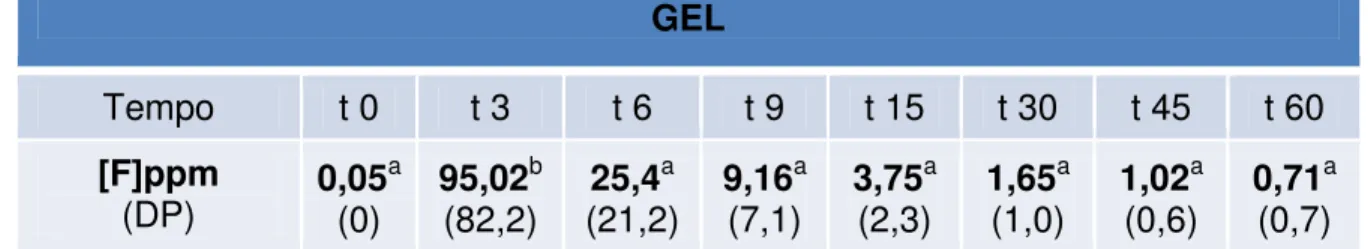
Tabela 3. Médias e desvio padrão (DP) das concentrações de flúor em saliva ao longo de 60 minutos após aplicação do gel. João Pessoa, PB, Brasil, 2009.
GEL
Tempo t 0 t 3 t 6 t 9 t 15 t 30 t 45 t 60
[F]ppm
(DP) 0,05
a
(0) 95,02 b
(82,2) 25,4 a
(21,2) 9,16 a
(7,1) 3,75 a
(2,3) 1,65 a
(1,0) 1,02 a
(0,6) 0,71 a (0,7)
* Médias seguidas de letras sobrescritas distintas (linha) indicam diferença estatística entre os tempos (p<0.05)
Tabela 4. Médias e desvio padrão (DP) das concentrações de flúor em saliva ao longo de 60 minutos após aplicação da espuma. João Pessoa, PB, Brasil, 2009.
ESPUMA
Tempo t 0 t 3 t 6 t 9 t 15 t 30 t 45 t 60
[F]ppm
(DP) 0,05
a
(0) 75,51 b
(41,0) 23,02 a
(14,1) 9,57 a
(5,8) 4,44 a
(2,7) 2,15 a
(1,3) 1,39 a
(0,9) 0,98 a (0,6)
* Médias seguidas de letras sobrescritas distintas (linha) indicam diferença estatística entre os tempos (p<0.05)
Tabela 5. Médias e desvio padrão (DP) das concentrações de flúor em saliva ao longo de 60 minutos após aplicação do verniz. João Pessoa, PB, Brasil, 2009.
VERNIZ
Tempo t 0 t 3 t 6 t 9 t 15 t 30 t 45 t 60
[F]ppm (DP) 0,06
a
(0) 99,33 b
(59,8) 60,8 c
(35,7) 40,62 c,d
(21,5) 28,29 a,d
(13,3) 19,97 a,d
(11,6) 15,93 a,d
(7,8) 13,68 a,d (6,7)
* Médias seguidas de letras sobrescritas distintas (linha) indicam diferença estatística entre os tempos (p<0.05)
Tabela 6. Médias e desvio padrão (DP) das concentrações de flúor em ppmF na saliva ao longo de 60 minutos após aplicação dos produtos fluoretados. João Pessoa, PB, Brasil, 2009.
t 0 t 3 t 6 t 9 t 15 t 30 t 45 t 60
GEL 0,05A
(0) 95,02 A
(82,2) 25,4 A
(21,2) 9,16 A
(7,1) 3,75 A
(2,3) 1,65 A
(1,0) 1,02 A
(0,6) 0,71 A (0,7) ESPUMA 0,05A
(0) 75,51 A
(41,0) 23,02 A
(14,1) 9,57 A
(5,8) 4,44 A
(2,7) 2,15 A
(1,3) 1,39 A
(0,9) 0,98 A (0,6) VERNIZ 0,06A
(0) 99,33 A
(59,8) 60,8 B
(35,7) 40,62 B
(21,5) 28,29 A
(13,3) 19,97 A
(11,6) 15,93 A
(7,8) 13,68 A (6,7) Médias seguidas de letras sobrescritas distintas (colunas) indicam diferença estatística entre os mesmos tempos dos produtos (p<0.05)
TABELA 7 - Variáveis relacionadas com a excreção urinária e concentrações de flúor na urina no baseline diurno
(11:00 h). João Pessoa, PB, Brasil, 2009.
BASELINE DIURNO (11horas)
mL μg F mL/h μg F/h mL/kg μgF/kg
GEL MÉDIA DP 95% 395,8a 176,1 305,3-486,4 97,1a 37,6 77,7-116,4 35,6a 15,9 27,4-43,8 8,2a 3,4 6,5-10,0 12,5a 5,6 9,6-15,4 2,8a 1,9 1,8-3,9
ESPUMA MÉDIA DP 95% 263,8a 196,2 162,9-364,7 82,8a 44,3 60,0-105,6 23,5a 17,8 14,3-32,7 7,0a 4,0 4,9-9,1 8,5a 6,6 5,1-11,9 2,4a 2,0 1,3-3,4
VERNIZ MÉDIA DP 95% 236,4a 94,7 187,7-285,1 96,8a 73,5 59,0-134,6 21,1a 8,7 16,5-25,6 8,2a 6,7 4,8-11,7 7,5a 3,6 5,6-9,4 2,8a 2,6 1,4-4,2
TABELA 8- Variáveis relacionadas com a excreção urinária e concentrações de flúor na urina no período diurno (11:00 h), após aplicação dos produtos fluoretados. João Pessoa, PB, Brasil, 2009.
PERÍODO DIURNO (11horas)
mL μgF mL/h μgF/h mL/kg μgF/kg
GEL MÉDIA DP 95% 189,7a 117,8 129,1-250,2 109,1a 71,3 72,4-145,8 16,6a 10,6 11,1-22,1 9,4a 6,5 6,1-12,8 5,4a 2,6 4,0-6,7 3,1a 2,4 1,9-4,4 ESPUMA MÉDIA DP
95% 206,7a 61,8 174,9-238,5 171,7a 109,7 115,3-228,2 18,3a 5,6 15,4-21,2 15,1a 9,9 10,0-20,2 6,5a 2,8 5,0-7,9 5,3a 4,4 3,0-7,6 VERNIZ MÉDIA DP
95% 223,5a 125,7 158,8-288,1 264,3a 219,6 151,4-377,24 20,0a 11,2 14,2-25,7
23,4 a 20,0 13,1-33,7 6,8a 4,1 4,7-9,0 8,2a 7,8 4,2-12,3 * Médias seguidas de letras sobrescritas distintas (colunas) indicam diferença estatística entre os grupos (p<0.05)
Comparando-se as Tabelas 7 e 8 observamos diferenças estatisticamente significantes (p<0,05) na seguinte variável:
TABELA 9- Variáveis relacionadas com a excreção urinária e concentrações de flúor na urina no baseline
noturno (13:00 h). João Pessoa, PB, Brasil, 2009.
BASELINE NOTURNO (13horas)
mL μgF ml/h μgF/h mL/kg μgF/kg
GEL MÉDIA DP 95% 355,5a 172,9 266,6-444,5 115,2a 71,2 78,5-151,8 26,8a 13,3 20,0-33,7 8,4a 5,5 5,5-11,2 11,2a 6,2 8,0-14,4 3,5a 3,2 1,8-5,2
ESPUMA MÉDIA DP 95% 354,1a 170,9 266,2-442,0 111,9a 62,4 79,9-144,0 26,8a 13,3 20,0-33,5 8,1a 4,7 5,7-10,6 11,2a 5,9 8,2-14,2 3,2a 2,6 1,9-4,6
TABELA 10- Variáveis relacionadas com a excreção urinária e concentrações de flúor na urina no período noturno (13:00 h), após aplicação dos produtos fluoretados. João Pessoa, PB, Brasil, 2009.
PERÍODO NOTURNO (13horas)
mL μg ml/h μg/h mL/kg μg/kg
GEL MÉDIA DP 95% 356,1a 188,4 259,3-453,0 218,5a 367,3 29,6-407,4 27,0a 14,3 19,6-34,3 16,2a 28,2 1,7-30,8 10,8a 5,9 7,8-13,9 6,9a 13,3 0,0-13,7 ESPUMA MÉDIA DP
95% 350,8a 172,0 261,9-439,7 113,4a 55,8 84,7-142,2 26,5a 13,3 19,6-33,3 8,1a 4,2 5,9-10,3 10,8a 4,6 8,4-13,3 3,4a 2,0 2,3-4,4