U
NIVERSIDADEF
EDERAL DAP
ARAÍBA– UFPB
D
EPARTAMENTO DEQ
UÍMICA– DQ/CCEN
FÍSICO-QUÍMICA EXPERIMENTAL
M
ANUAL DEP
RÁTICASC
OMPLETOCONTEÚDO:
UTILIZAÇÃO DESTE MANUAL
P
ARTE1: T
ERMODINÂMICAQ
UÍMICAI
PRÁTICA N° 1: LEI DE BOYLE
PRÁTICA N° 2: LEI DE CHARLES E GAY-LUSSAC PRÁTICA N° 3: LEI DE GRAHAM
PRÁTICA N° 4: CALOR ESPECÍFICO DE UM SÓLIDO
PRÁTICA N° 5: CALOR DE NEUTRALIZAÇÃO, DISSOLUÇÃO E DILUIÇÃO PRÁTICA N° 6: FUNÇÕES TERMODINÂMICAS E SOLUBILIDADE
PRÁTICA N° 7: ENTROPIA DE UM PROCESSO IRREVERSÍVEL
PRÁTICA N° 8: CONSTANTE DE EQUILÍBRIO POR FOTOCOLORIMETRIA PRÁTICA N° 9: CONSTANTE DE EQUILÍBRIO POR TITULOMETRIA
1-18;19-47;103;104;105
P
ARTE2: T
ERMODINÂMICAQ
UÍMICAII
PRÁTICA N° 1: VOLUME MOLAR PARCIAL PRÁTICA N° 2: TENSÃO SUPERFICIAL
PRÁTICA N° 3: VISCOSIDADE DE UM LÍQUIDO PRÁTICA N° 4: EQUILÍBRIO SÓLIDO-LÍQUIDO
PRÁTICA N° 5: DISTRIBUIÇÃO DE SOLUTO ENTRE SOLV. IMISCÍVEIS PRÁTICA N° 6: SOLUBILIDADE LÍQUIDOS (SISTEMA BINÁRIO)
PRÁTICA N° 7: SOLUBILIDADE LÍQUIDOS (SISTEMA TERNÁRIO) PRÁTICA N° 8: CONDUTIVIDADE MOLAR
PRÁTICA N° 9: CONSTANTE DE FARADAY E NÚMERO DE AVOGADRO
1-18;48-72;103;104;106
P
ARTE3: C
INÉTICAQ
UÍMICAPRÁTICA N° 1: PARÂMETROS CINÉTICOS PELO MÉTODO DO ISOLAMENTO PRÁTICA N° 2: ORDEM DE REAÇÃO PELO MÉTODO DAS VELOC. INICIAIS PRÁTICA N° 3: CONSTANTE DE VELOC. POR CONDUTIVIMETRIA
PRÁTICA N° 4: PARÂMETROS CINÉTICOS POR FOTOCOLORIMETRIA PRÁTICA N° 5: CONSTANTE DE VELOC. POR TITULOMETRIA
PRÁTICA N° 6: CONSTANTE DE VELOC. POR POLARIMETRIA PRÁTICA N° 7: CATÁLISE ENZIMÁTICA VIA FOTOCOLORIMETRIA PRÁTICA N° 8: ISOTERMA DE ADSORÇÃO VIA TITULOMETRIA
1-18;73-102;103;104;107
F
ÍSICO-Q
UÍMICAE
XPERIMENTAL: P
RÁTICASS
UGERIDASPRÁTICAS N°: 1.4, 1.5, 1.7, 2.1, 2.2, 2.3, 3.2, 3.3, 3.4
1-18;19;29-31;32-35;38-40;48;49-50;51-53;54-56;73; 77-80;81-84;85-88;103;104;108
F
UNDAMENTOS DEF
ÍSICO-Q
UÍMICA: P
RÁTICASS
UGERIDASPRÁTICAS N°: 1.1, 1.2, 1.4, 1.5, 1.7, 3.2, 3.3, 3.4, 3.6
ORIENTAÇÕES INICIAIS:
ATITUDES SEGURAS NO LABORATÓRIO E TRATAMENTO DE DADOS
O
BSERVAÇÕESI
NICIAIS1. Segurança no Laboratório: A participação nas aulas práticas só será permitida se o aluno estiver portando o seu caderno de laboratório e vestido adequadamente (calça, sapato e bata). É de suma importância que cada aluno se esforce para manter o laboratório limpo e organizado, de forma a permitir o seu uso posterior.
2. Tempo da Atividade: Em todas as aulas práticas os alunos devem trazer seus cadernos de laboratório devidamente organizados, contendo o pré-relatório e as tabelas a serem preenchidas com os dados dos experimentos. A critério do professor, a realização da atividade prática poderá ser suspensa caso o caderno de laboratório pré-organizado não seja apresentado no início da atividade.
3. Avaliação da Prática: O caderno de laboratório também deve conter o tratamento de dados referente a cada prática, cuja cópia deve ser entregue ao professor no início da aula prática seguinte. Este procedimento deve ser feito antes da elaboração do relatório final da atividade prática.
T
RATAMENTO DED
ADOSALGARISMOS SIGNIFICATIVOS
Em matemática 10 é igual a 10,0. Entretanto, nas ciências experimentais esses números não são necessariamente iguais. Por exemplo, quando se expressa a massa de uma amostra como sendo 10 g significa dizer que a quantidade pesada está entre 11 g e 12 g, enquanto que 10,0 g significa algo entre 9,9 g e 10,1 g.
Os algarismos necessários para expressar o resultado de um experimento, com a mesma precisão que as medidas efetuadas, são chamados algarismos significativos. Por exemplo, ao se escrever que a distância entre dois pontos é de 12,00 cm, a medida está sendo representada por quatro algarismos significativos. Escrevendo que a distância é de 0,1200 m ou 0,0001200 km tem-se tem-sempre quatro algarismos significativos. Note-tem-se que os zeros que precedem o algarismo 1 não fazem parte dos algarismos significativos, porque servem apenas para indicar a posição da vírgula. Os dois zeros seguintes aos algarismos 1 e 2 são significativos, porque indicam que a medida foi feita com precisão da ordem de um décimo de milímetro.
O experimentador deve registrar os resultados de tal modo que o último algarismo significativo, e apenas ele, seja incerto. A soma algébrica de um algarismo incerto com algarismos exatos é um algarismo incerto. Por exemplo:
104,65 + 0,2248 ---104,87
.
Neste caso o algarismo incerto é o 7, de modo que o resultado deve ser expresso como 104,87. Na multiplicação e na divisão o raciocínio é análogo. Por exemplo:
12,4 x2,54 496 620 248 ---31, 496
,
de modo que o resultado deve ser representado na forma de 31,5.
PRECISÃO & EXATIDÃO
Os termos precisão e exatidão são usados para dar informações sobre a qualidade das medidas e a confiança que se pode depositar nelas. Por exemplo, pesou-se uma amostra sobre duas balanças, de modo que a primeira pesagem indicou 1,25±0,02 g e a segunda 1,2500±0,0002 g. O resultado apresentado pela segunda balança é mais preciso que o da primeira, mas não se tem certeza de qual resultado é o mais exato, visto que uma das balanças pode apresentar um erro sistemático.
Fala-se de precisão quando se considera o número de algarismos significativos e a reprodutibilidade dos resultados, enquanto a exatidão representa a diferença entre a medida e o seu valor real. Assim, uma medida pode ser muito precisa e pouco exata, mas se a medida for muito exata é provável que seja muito precisa. A precisão depende dos erros acidentais (devidos ao operador; esses erros são variáveis em grandeza e sinal, e se compensam quando o número de medidas é grande), enquanto a exatidão depende dos erros sistemáticos (independentes do operador; esses erros são constantes em grandeza e sinal e nunca se compensam).
A determinação da precisão é feita pela percentagem de erro da medida. Por exemplo, duas medidas deram 1,25±0,02 g e 1,2500±0,0002 g, de modo que a precisão das medidas é:
1ª Medida: 0,02
1,25 = 0,016 = 1,6 %
2ª Medida: 0,0002
1,2500 = 0,00016 = 0,016%
.
ERRO ABSOLUTO & ERRO RELATIVO
Em uma medida expressa na forma 7,25±0,03 cm, a quantidade 7,25 cm representa o valor absoluto da medida, enquanto que ±0,03 cm representa o erro absoluto, que é independente do valor da medida. O erro relativo é a fração do erro cometido na medida e depende do valor absoluto. Por exemplo, duas medidas deram 7,25±0,03 cm e 72,50±0,03 cm, de modo que os erros absolutos são os mesmos, mas os erros relativos são:
1ª Medida: 0,03
7,25 = 0,004 = 0,4%
2ª Medida: 0,03
72,50 = 0,0004 = 0,04%
.
A análise de erro descrita acima diz respeito a precisão da medida. No entanto, outra análise de erro a ser considerada é feita com base na exatidão, para a qual é necessário um valor de referência (geralmente um valor tabelado em handbooks ou determinado através de um trabalho científico meticuloso). Para este tipo de análise, o erro absoluto é determinado pela expressão:
Erro =
|
Medida−Referência|
,e o erro relativo:
%Erro =
|
Medida−Referência Referência|
.FONTES DE DADOS ADICIONAIS
Todos os dados adicionais, necessários para a realização de tratamentos de dados ou determinações de erros experimentais, tais como densidade, tensão superficial e viscosidade em diferentes temperaturas, devem ser obtidos em manuais de constantes físicas e químicas ou em artigos científicos (muitos dos quais são recomendados neste manual, ao final de cada prática).
R
EFERÊNCIAS1. Bueno, W. A.; Degrève, L.; Manual de Laboratório de Físico-Química, São Paulo, McGraw-Hill, 1980.
2. Silva, R. R.; Bocchi, N.; Rocha Filho, R. C.; Introdução à Química Experimental, São Paulo, McGraw-Hill, 1990.
ELABORAÇÃO DE PRÉ-RELATÓRIOS:
DOCUMENTAÇÃO ANTERIOR A REALIZAÇÃO DAS PRÁTICAS
O
BSERVAÇÕESI
NICIAIS1.
Cada aluno deve preparar um pré-relatório manuscrito em seu caderno de laboratório. O objetivo do pré-relatório é o de permitir que o aluno tome conhecimento dos detalhes do experimento antes de sua ida ao laboratório, bem como possibilitar a execução rápida e eficiente da atividade prática. É de suma importância a preparação antecipada do pré-relatório para a compreensão das bases teóricas e do roteiro da prática para o bom aproveitamento acadêmico.2. A realização da prática dependerá, a critério do professor responsável, da apresentação do pré-relatório no início das atividades no laboratório.
C
OMPONENTES DOP
RÉ-R
ELATÓRIOEste material deve conter os seguintes itens: 1. MATERIAIS:
Lista completa de todos os equipamentos e reagentes a serem utilizados.
2. PROCEDIMENTO:
Descrição resumida do procedimento da prática. Deve-se evitar a simples cópia do roteiro da prática.
3. QUESTÕES:
Discussão sobre as questões sugeridas no manual do laboratório. 4. DADOS:
Quando for necessária a preparação de soluções, todos os cálculos relativos a massas e volumes a serem medidos devem constar neste item. Deve-se reservar um espaço para o registro das massas e volumes a serem efetivamente medidos na atividade prática. Quando necessário, tabelas (devidamente legendadas) para o registro dos dados a serem medidos devem ser preparadas e incluídas nesta seção. Deve-se tomar cuidado com o registro correto dos algarismos significativos e unidades de medida.
Materiais: 2 Béqueres de 250 mL;
2 Pipetas Volumétricas de 50±0,1 mL; 2 Termômetros Digitais (0-100 °C±0,1 °C);
100 mL de Ácido Clorídrico (HCl) 1,0 M; 100 mL de Hidróxido de Sódio (NaOH) 1,0 M; ...
Procedimento: Resumido, mas facilmente compreensível...
Questões: Devidamente respondidas...
Dados: 100 mL HCl 1,0 M.
MHCl = 36,46 g/mol, pHCl = 38 %, ρHCl(Conc.) = 1,181 g/mL
mHCl = cHClMHClVsol/p
VHCl = mHCl/ρHCl =cHClMHClVsol/pρHCl
VHCl= (1,0 mol/L)(36,66 g/mol)(0,100 L)/(0,38)(1,181 g/mL) VHCl= 8,12 mL
100 mL NaOH 1,0 M.
MNaOH = 40,00 g/mol, pNaOH = 99 %
mNaOH = cNaOHMNaOHVNaOH/p
mNaOH = (1,0 mol/L)(40,00 g/mol)(0,100 L)/(0,99) mNaOH = 4,04 g
VHCl: ±0,1 mL
mNaOH: ±0,0001 g
Reação entre HCl 1,0 M (50±0,1 mL) e NaOH 1,0 M (50±0,1 mL).
Tempo (s) THCl (°C) TNaOH (°C) Tcalorímetro (°C)
10
...
ELABORAÇÃO DE RELATÓRIOS:
DOCUMENTAÇÃO POSTERIOR A REALIZAÇÃO DAS PRÁTICAS
O
BSERVAÇÕESI
NICIAIS1.
O relatório deve ser, preferencialmente, impresso em papel tamanho A4, com fonte Times 12, Arial 11 ou Verdana 11, espaçamento 1,5 e títulos/subtítulos em negrito e letras maiúsculas.2.
O relatório deve ser bem organizado e conciso, sem sacrificar a clareza. Atenção especial deve ser dada ao estilo literário científico compatível ao esperado para a disciplina. Ortografia e regras gramaticais não devem ser negligenciadas e serão penalizadas, a critério do professor responsável, caso não atendam a níveis adequados.3.
Equações matemáticas devem ser acompanhadas de material verbal suficiente para deixar claro os significados dos termos empregados. Gráficos e tabelas devem ser adequadamente legendadas, com especial atenção a algarismos significativos e unidades de medida.4.
O relatório elaborado deve ser, acima de tudo, um material original. Objetiva-se, com isto, o desenvolvimento da habilidade de escrever de forma concisa e eloquente, obedecendo a padrões rígidos impostos a argumentação científica.5. O material deve ser elaborado no formato de “relatório completo” ou “relatório curto”, a critério do professor responsável.
R
ELATÓRIOC
OMPLETOEste formato deve conter os seguintes componentes: 1. CAPA:
Título e número da prática, identificação do(s) aluno(s) e da turma(s) (ex.: Bacharelado em Química), data da realização do experimento e nome do professor responsável.
2. RESUMO:
Texto contendo entre 5 e 10 linhas resumindo todo o relatório (objetivos, procedimentos e resultados).
3. OBJETIVOS:
Com verbo no infinitivo, indicando o(s) objetivo(s) da prática. 4. INTRODUÇÃO:
Teoria necessária para o entendimento da prática e fundamentação da discussão dos resultados, devendo estar referenciada com numeração sequencial, evitando-se cópia de textos da bibliografia consultada.
5. MATERIAIS E MÉTODOS:
5.1.Equipamentos: Informar, na forma de itens, todos os materiais e equipamentos utilizados. Ex.:
◦ Chapa Elétrica Aquecedora (ou Bico de Bunsen + Tripé de Ferro); ◦ Termômetro (0-100 °C±0,5 °C).
5.2.Reagentes: Informar, na forma de itens, todos os reagentes utilizados, com formulação e concentração. Ex.:
◦ Ácido clorídrico concentrado (HCl);
◦ Solução aquosa de ácido clorídrico (HCl) 0,50 mol/L.
5.3.Procedimento: Descrever o procedimento experimental realizado, com detalhes, levando-se em conta as possíveis diferenças do roteiro da prática. Os verbos devem estar no passado e de forma impessoal. Ex.: “colocou-se...” ou “foram colocados...”.
6. RESULTADOS E DISCUSSÃO:
Colocar todos os resultados alcançados na ordem em que foram adquiridos, apresentado-os com clareza e organização.
◦ Fazer uso de quadros, tabelas, gráficos e figuras, quando conveniente, devendo ser numerados e mencionados no texto antes de suas colocações no documento. Quadros apresentam as laterais fechadas e as tabelas apresentam as laterais abertas. Figuras facilitam a ilustração de um esquema ou montagem experimental, e gráficos facilitam a ilustração de uma tendência, devendo ser priorizados se os resultados o permitirem. Gráficos devem conter escalas coerentes aos valores mínimos e máximos dos pontos, com eixos rotulados com o símbolo da grandeza ou palavras que a definam, com as unidades indicadas entre parênteses. Em todos os casos deve-se utilizar legendas autoexplicativas, posicionadas na parte superior em tabelas, e na parte inferior em quadros, figuras e gráficos.
◦ Todos os dados numéricos obtidos através de medidas devem apresentar unidades, fazendo-se o uso correto de algarismos significativos. Deve-se informar nesta seção os erros absolutos e relativos (erros relacionados a precisão das medidas). Todos os cálculos relativos ao tratamento de dados devem ser apresentados neste item, atentando-se rigorosamente as regras operacionais de análise dimensional. No caso de cálculos repetitivos, apenas um deve ser realizado em detalhes, e os demais devem ser apresentados em uma tabela. Quando um valor de referência estiver disponível a partir de dados da literatura, deve-se informar nesta seção os erros absolutos e relativos obtidos (erros relacionados a exatidão dos resultados).
7. CONCLUSÕES:
Apresentar as conclusões de forma clara e resumida a partir dos resultados obtidos. Deve-se indicar os conceitos mais relevantes apreendidos durante a execução do experimento ou durante a elaboração do relatório.
8. QUESTÕES:
Discussão das questões sugeridas no roteiro da prática.
9. REFERÊNCIAS:
Listar as referências consultadas para a realização do relatório de acordo com a ABNT (Associação Brasileira de Normas técnicas), com a numeração adequada. Ex.:
1. SOBRENOME, Iniciais; Título do Livro, Nº da Edição, Local da Publicação, Editora, Páginas Consultadas, Ano.
2. ATKINS, P.W.; Físico-Química, 7ª Ed., RJ, Ed. LTC, p. 84, 2004.
3. CORSARO, G. Colorimetric Chemical Kinetics Experiment. J. Chem. Educ., v. 41, n. 1, p. 48, 1964.
R
ELATÓRIOC
URTOEste formato deve conter os seguintes componentes: 1. CAPA:
Título e número da prática, identificação do(s) aluno(s) e da turma(s), data da realização do experimento e nome do professor responsável.
2. DADOS:
Colocar todos os resultados alcançados na ordem em que foram adquiridos, apresentado-os com clareza e organização.(*)
3. TRATAMENTO DE DADOS:
Todos os cálculos relativos ao tratamento de dados devem ser apresentados neste item.(*)
4. ANÁLISE DE ERROS:
Deve-se informar nesta seção os erros absolutos e relativos (relacionados a precisão e exatidão das medidas).(*)
5. CONCLUSÕES:
Apresentar as conclusões de forma clara e resumida a partir dos resultados obtidos.
6. QUESTÕES:
Discussão das questões sugeridas no roteiro da prática. 7. REFERÊNCIAS:
Listar as referências consultadas para a realização do relatório de acordo com a ABNT, com a numeração adequada.(**)
*(*) Vide recomendações para “Resultados e Discussão” do Relatório Completo.
M
ODELO DER
ELATÓRIOUNIVERSIDADE FEDERALDA PARAÍBA – UFPB
Departamento de Química – DQ/CCEN
Prática Nº 1: Determinação do
Calor de Neutralização
Grupo: Fulano de Andrade Sicrano de Bezerra
Turma: Bacharelado em Química
Data: 27 de agosto de 2014
R
ESUMONeste experimento, utilizou-se um calorímetro adiabático (constituído de uma garrafa térmica e um termômetro digital) para a determinação do calor liberado em uma reação de neutralização entre o ácido clorídrico (HCl 0,1 M) e hidróxido de sódio (NaOH 0,1 M) concentrados. Os resultados obtidos indicam que, apesar da simplicidade da montagem experimental, é possível obter uma boa concordância com resultados tabelados.
O
BJETIVOSDeterminar o calor de neutralização em uma reação ácido-base a partir de um simples experimento de calibração de um calorímetro.
I
NTRODUÇÃOA calorimetria permite determinar a troca de calor envolvida em um processo químico ou físico. O conhecimento deste tipo de dado pe muito importante em diversas áreas, como a indústria química (calor liberado ou absorvido em um processo) e alimentícia (onde se determina o “teor calórico” de alimentos). Um calorímetro é um aparelho simples, termicamente isolado, que possibilita medir a quantidade de calor envolvida em um processo a partir da determinação da variação de temperatura medida em seu interior. Conhecendo-se a capacidade calorífica Ccal do calorímetro é possível determinar
a quantidade de calor qproc envolvida no processo a partir da determinação da
variação de temperatura ΔT medida no calorímetro e da aplicação da 1ª Lei da Termodinâmica, segundo a qual:
Calor do Processo
= −
Calor do Calorímetro
⇒
q
proc= −C
calΔ
T
.(...)
M
ATERIAIS& M
ÉTODOSEQUIPAMENTOS
• 01 Garrafa Térmica de 500 mL;
• 01 Béquer de 200 mL;
• 01 Proveta de 100 mL;
• 01 Chapa Elétrica Aquecedora;
• 02 Termômetros Digitais (0-100 °C±0,1 °C).
REAGENTES
• HCl 1,0 mol/L;
PROCEDIMENTO
Inicialmente, procedeu-se a calibração do calorímetro, constituído de uma garrafa térmica e 100 mL de água destilada. Colocou-se 100 mL de água destilada, sob temperatura ambiente, no interior da garrafa térmica (recipiente calorimétrico) e anotou-se a temperatura (T1(1)) de equilíbrio. Em seguida,
aqueceu-se 100 mL de água destilada em um béquer de 200 mL até ~80 °C. Transferiu-se 50 mL da água aquecida para uma proveta de 100 mL e devolveu-se a água ao béquer. Repetiu-devolveu-se este procedimento 3 vezes de modo que a proveta entrasse em equilíbrio térmico com a água aquecida. Finalmente, coletou-se 50 mL da água aquecida com a proveta, anotou-se a temperatura (T2(1)) e transferiu-se a água aquecida para o interior do calorímetro. Esperou-se
o equilíbrio térmico ser alcançado e anotou-se a temperatura de equilíbrio (Tf(1)).
Em seguida, esvaziou-se o calorímetro, que foi lavado com bastante água da torneira e depois com água destilada. Com o calorímetro lavado, colocou-se 50 mL de uma solução de NaOH 1,0 mol/L em seu interior e anotou-se a temperatura (Ti(2)). Pegou-se 50 mL de uma solução de HCl 1,0 mol/L, sob a
mesma temperatura do interior do calorímetro (Ti(2)), e colocou-se esta solução
sobre a solução de hidróxido de sódio do calorímetro. Esta última etapa restaurou o volume inicial do calorímetro. Agitou-se suavemente a mistura e anotou-se a temperatura de equilíbrio (Tf(2)).
R
ESULTADOS ED
ISCUSSÃODADOS
VHCl = 8,1 mL (±0,1 mL)
cHCl = VHClpρHCl/MHClVsol
= (8,1 mL)(0,38)(1,181 g/mL)/(36,66 g/mol)(0,100 L) = 0,9916 mol/L
Vsol(1) = 50,0 mL (±0,1 mL)
s(VHCl) = 0,1/8,1 = 1,2 % [Erro Relativo (Precisão)]
mNaOH = 4,0381 g (±0,0001 g) [s(mNaOH) = 0,1/8,1 = 1,2 %]
cNaOH = mNaOHp/MnaOHVsol
= (4,0381 g)(0,99)/(40,00 g/mol)(0,100 L) = 0,9949 mol/L
Vsol(2) = 50,0 mL (±0,1 mL)
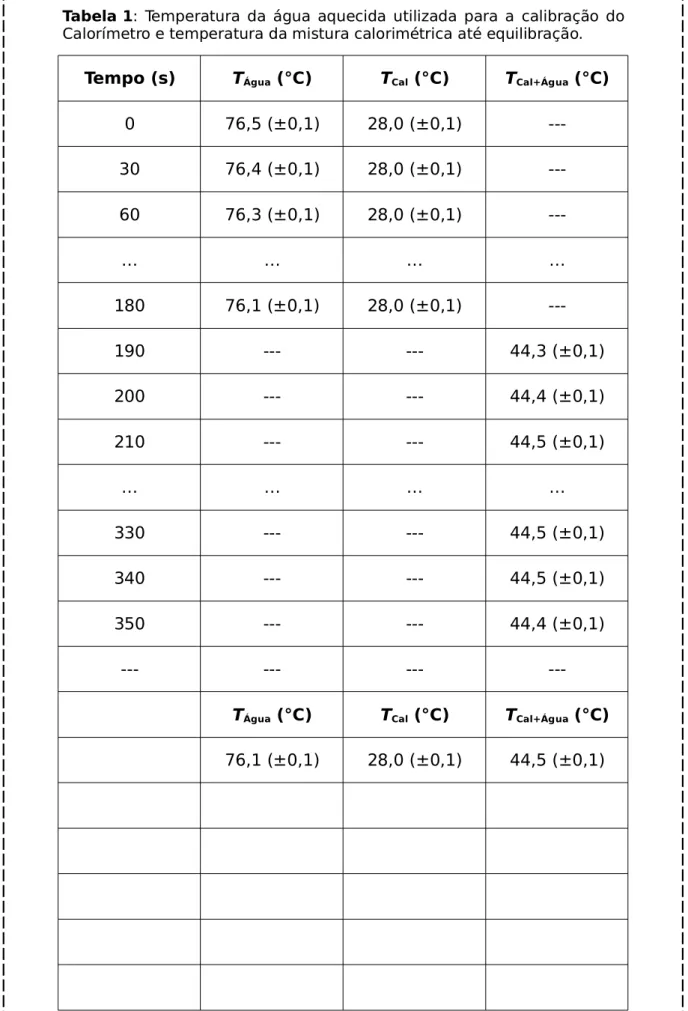
Tabela 1: Temperatura da água aquecida utilizada para a calibração do Calorímetro e temperatura da mistura calorimétrica até equilibração.
Tempo (s) TÁgua (°C) TCal (°C) TCal+Água (°C)
0 76,5 (±0,1) 28,0 (±0,1)
---30 76,4 (±0,1) 28,0 (±0,1)
---60 76,3 (±0,1) 28,0 (±0,1)
---… … … …
180 76,1 (±0,1) 28,0 (±0,1)
---190 --- --- 44,3 (±0,1)
200 --- --- 44,4 (±0,1)
210 --- --- 44,5 (±0,1)
… … … …
330 --- --- 44,5 (±0,1)
340 --- --- 44,5 (±0,1)
350 --- --- 44,4 (±0,1)
--- --- ---
---TÁgua (°C) TCal (°C) TCal+Água (°C)
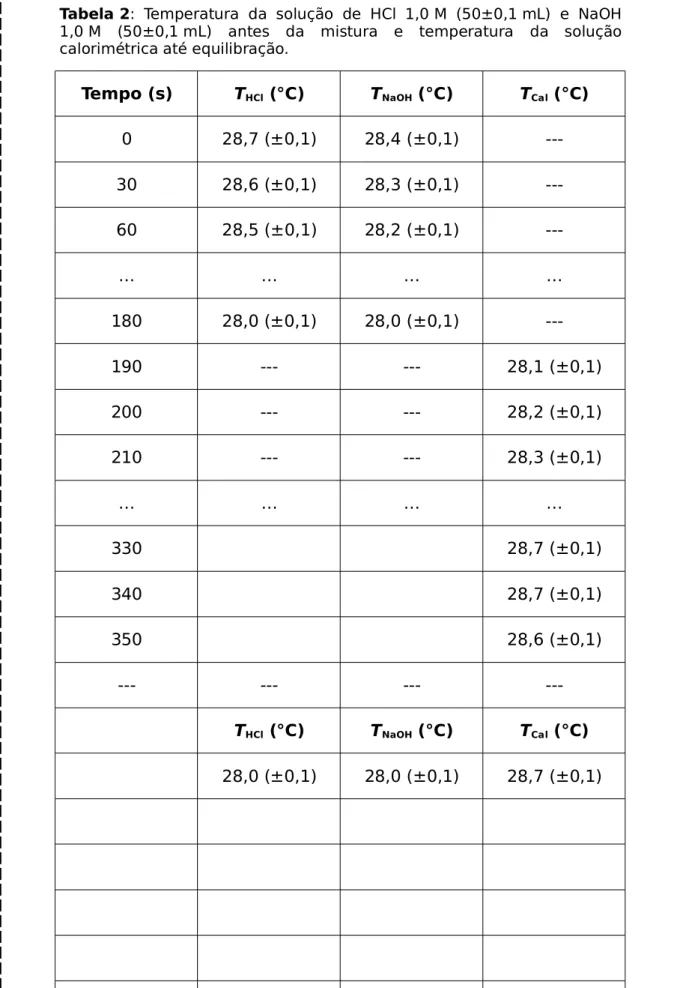
Tabela 2: Temperatura da solução de HCl 1,0 M (50±0,1 mL) e NaOH 1,0 M (50±0,1 mL) antes da mistura e temperatura da solução calorimétrica até equilibração.
Tempo (s) THCl (°C) TNaOH (°C) TCal (°C)
0 28,7 (±0,1) 28,4 (±0,1)
---30 28,6 (±0,1) 28,3 (±0,1)
---60 28,5 (±0,1) 28,2 (±0,1)
---… … … …
180 28,0 (±0,1) 28,0 (±0,1)
---190 --- --- 28,1 (±0,1)
200 --- --- 28,2 (±0,1)
210 --- --- 28,3 (±0,1)
… … … …
330 28,7 (±0,1)
340 28,7 (±0,1)
350 28,6 (±0,1)
--- --- ---
---THCl (°C) TNaOH (°C) TCal (°C)
TRATAMENTO DE DADOS
Capacidade Calorífica do Calorímetro:
cÁgua = 4,201±0,002 J/g°C[1]
ρÁgua = 9,9568±0,0022 g/mL (a 30 °C)[1]
VÁgua = 50,0±0,1 mL
ΔTÁgua = 44,5-76,1 °C = -31,6 °C ± s(ΔT)[*]
ΔTCal(1) = 44,5-28,0 °C = +16,5 °C ± s(ΔT)[*]
Ccal = -ρÁguaVÁguacÁguaΔTÁgua/ΔTCal(1)
= -(4,201 J/g°C)(9,9568 g/mL)(50,0 mL)(-31,6 °C)/ = -(+16,5 °C)
= -4.005,397 J/°C = 4,01 kJ/°C ± s(Ccal)[**]
s(ΔT) = √[(0,1 °C)²+(0,1 °C)²] = 0,1 °C
sr(Ccal) = √[(0,0022/9,9568)²+(0,1/50,0)²+(0,002/4,201)²+
= √(0,1/31,6)2+(0,1/16,5)2] = 0,007
s(Ccal) = Ccal×sr(Ccal)
= 4.005,397 J/°C × 0,007
= 28,0 J/°C → Ccal = 4.005±28 J/°C
[*] Diferença: → desvio padrão absoluto (s)
[**] Produto: → desvio padrão relativo (sr) → (s)
Entalpia de Neutralização Molar:
nHCl = cHClVsol(1)
= (0,9916 mol/L)(0,050 mL) = 0,0495 mol ± s(nHCl)
nNaOH = cNaOHVsol(2)
= (0,9949 mol/L)(0,050 mL) = 0,0497 mol ± s(nNaOH)
nNeu = 0,0495 mol ± s(nNeu) [Menor valor]
ΔTCal(2) = 23,7-23,0 °C = +0,7 °C ± s(ΔT)
ΔHNeu(Exp) = -CCalΔTCal(2)/nNeu
= -(4.005 J/°C)(+0,7 °C)/(0,0495 mol) = -56,636 kJ/mol ± s(ΔHNeu)
ΔHNeu(Ref) = -57,300 kJ/mol ± 0,012[2-3]
DISCUSSÃO
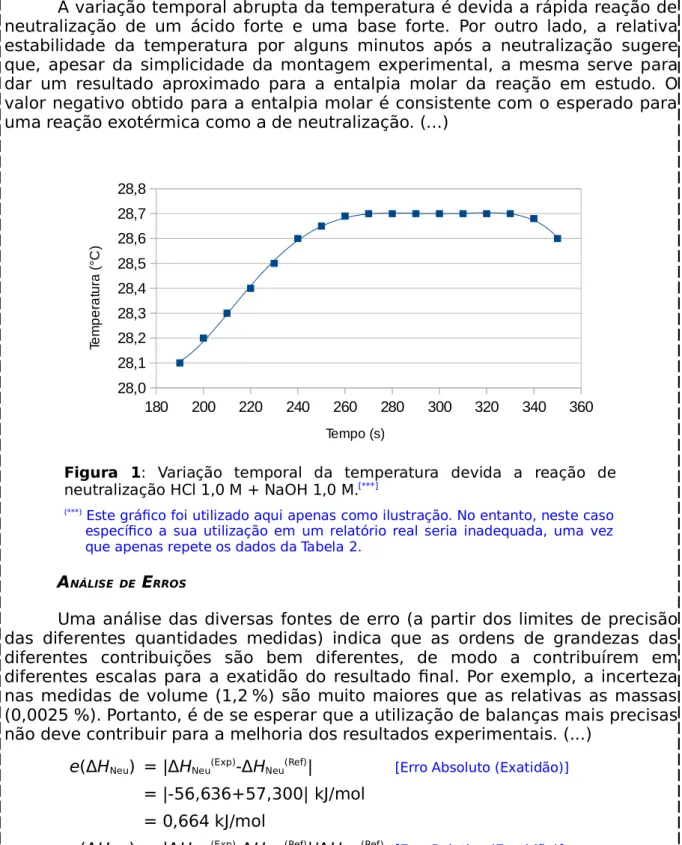
A variação temporal abrupta da temperatura é devida a rápida reação de neutralização de um ácido forte e uma base forte. Por outro lado, a relativa estabilidade da temperatura por alguns minutos após a neutralização sugere que, apesar da simplicidade da montagem experimental, a mesma serve para dar um resultado aproximado para a entalpia molar da reação em estudo. O valor negativo obtido para a entalpia molar é consistente com o esperado para uma reação exotérmica como a de neutralização. (...)
Figura 1: Variação temporal da temperatura devida a reação de neutralização HCl 1,0 M + NaOH 1,0 M.[***]
(***) Este gráfico foi utilizado aqui apenas como ilustração. No entanto, neste caso
específico a sua utilização em um relatório real seria inadequada, uma vez que apenas repete os dados da Tabela 2.
ANÁLISE DE ERROS
Uma análise das diversas fontes de erro (a partir dos limites de precisão das diferentes quantidades medidas) indica que as ordens de grandezas das diferentes contribuições são bem diferentes, de modo a contribuírem em diferentes escalas para a exatidão do resultado final. Por exemplo, a incerteza nas medidas de volume (1,2 %) são muito maiores que as relativas as massas (0,0025 %). Portanto, é de se esperar que a utilização de balanças mais precisas não deve contribuir para a melhoria dos resultados experimentais. (...)
e(ΔHNeu) = |ΔHNeu(Exp)-ΔHNeu(Ref)| [Erro Absoluto (Exatidão)]
= |-56,636+57,300| kJ/mol = 0,664 kJ/mol
er(ΔHNeu) = |ΔHNeu(Exp)-ΔHNeu(Ref)|/ΔHNeu(Ref) [Erro Relativo (Exatidão)]
= (0,664)/(57,300) = 0,0116 = 1,16 %
180 200 220 240 260 280 300 320 340 360
28,0 28,1 28,2 28,3 28,4 28,5 28,6 28,7 28,8
Tempo (s)
Te
m
p
e
ra
tu
ra
(
°C
Q
UESTÕES1. Os resultados obtidos são satisfatórios?
Razoáveis, uma vez que o erro obtido para a entalpia molar de neutralização difere do valor de referência na ordem de, apenas, 1 %. (...)
R
EFERÊNCIAS1. LENNON, J.; Handbook of Chemistry and Physics, p. 321, 2001.
2. MCCARTNEY, P.; Thermochemical Experiment, J. Chem. Educ., 1(2), 34, 2002.
3. HARRISON, G.; Experimental Physical Chemistry, J. Chem. Educ., 5(6), 78, 2003.
PARTE 1
PRÁTICA N° 4:
DETERMINAÇÃO DO CALOR ESPECÍFICO DE UM SÓLIDO POR CALORIMETRIA
O
BJETIVODeterminar o calor específico de um sólido a partir de um simples experimento de calibração de um calorímetro.
I
NTRODUÇÃOCalor pode ser definido como uma quantidade que se transfere de um corpo a outro como consequência exclusiva de uma diferença de temperatura entre ambos. A experiência mostra que a quantidade de calor recebida por um sistema, sob pressão constante, é proporcional ao acréscimo de temperatura produzido, ou seja:
q = C ×(T2−T1) , (1)
onde T1 e T2 são as temperaturas inicial e final do sistema, respectivamente, e C
é uma constante de proporcionalidade, denominada capacidade calorífica média, a qual depende da natureza, do estado físico e do tamanho do sistema. Se dividirmos a capacidade calorífica pela massa do sistema, obtém-se a capacidade calorífica específica, ou simplesmente calor específico, do sistema, c:
c = C
m ⇔ C = mc . (2)
De acordo com a primeira lei da termodinâmica, quando dois sistemas interagem e trocam energia, um deles ganha e o outro perde a mesma quantidade de energia. Desta forma, se os sistemas estiverem em temperaturas diferentes, a quantidade de energia trocada pode ser representada da seguinte forma:
q1 = −q2 ⇔ q1 + q2 = 0 , (3)
onde q1 é a quantidade de energia perdida pelo corpo 1 e q2 a quantidade de
energia ganha pelo corpo 2. Se substituirmos q1 e q2, teremos:
C1×(Tf−T1) = −C2×(Tf−T2) , (4)
onde C1 e C2 são as capacidades caloríficas dos sistemas 1 e 2, T1 e T2 as
temperaturas iniciais dos sistemas 1 e 2 e Tf a temperatura final (de equilíbrio).
M
ATERIAIS: E
QUIPAMENTOS& R
EAGENTES01 Calorímetro adiabático de isopor; 01 Copo de alumínio.
01 Esfera de ferro metálico; 01 Esfera de chumbo metálico; 01 Proveta de 250 mL;
01 Chapa Elétrica Aquecedora (ou Bico de Bunsen + Tripé de Ferro); 01 Balança mecânica;
02 Termômetros (0-100 °C±0,5 °C).
P
ROCEDIMENTOPARTE A: CALIBRAÇÃO DO CALORÍMETRO
1. Coloque 200 mL de água destilada no interior do sistema calorimétrico e deixe-o alcançar o equilíbrio térmico. Anote a temperatura.
2. Pese uma quantidade de ferro metálico (c = 0,106 cal/g°C) em balança adequada (mecânica). Aqueça-a em água destilada até que esta entre em ebulição e anote a temperatura. Em seguida, transfira rapidamente o ferro metálico para o sistema calorimétrico, espere o equilíbrio térmico ser alcançado e anote a temperatura de equilíbrio.
3. Utilize estes dados para calcular a capacidade calorífica do sistema calorimétrico.
PARTE B: DETERMINAÇÃO DO CALOR ESPECÍFICO DE UM SÓLIDO
1. Esvazie e lave o calorímetro.
2. Repita o procedimento anterior, utilizando uma amostra de chumbo metálico.
T
RATAMENTO DED
ADOS2. Utilizando a equação (4), os dados da segunda parte e o resultado anterior, determine o calor específico do chumbo.
3. Compare seus resultados com os da literatura. Calcule o erro relativo e o absoluto e discuta sobre as diferenças.
Q
UESTÕES PARA OR
ELATÓRIO1. Os valores obtidos são satisfatórios?
2. Quais as possíveis fontes de erro ou limitações neste experimento? Para cada uma, tente dizer que efeito elas terão no resultado esperado dos experimentos.
B
IBLIOGRAFIA1. ATKINS, P.W.; Físico-Química, 7ª Ed., RJ, Ed. LTC, 2004.
PRÁTICA N° 5:
DETERMINAÇÃO DO CALOR DE NEUTRALIZAÇÃO, DISSOLUÇÃO E DILUIÇÃO
O
BJETIVODeterminar o calor de neutralização (em uma reação ácido-base) e dissolução (na solubilização de um soluto em água).
I
NTRODUÇÃOCalor pode ser definido como uma quantidade que se transfere de um corpo a outro como consequência exclusiva de uma diferença de temperatura entre ambos. A experiência mostra que a quantidade de calor recebida por um sistema, sob pressão constante, é proporcional ao acréscimo de temperatura produzido, ou seja:
q = C ×(Tf−Ti) , (1)
onde Ti e Tf são as temperaturas final e inicial do sistema, respectivamente, e C é
uma constante de proporcionalidade, denominada capacidade calorífica média, a qual depende da natureza, do estado físico e do tamanho do sistema. Se dividirmos a capacidade calorífica pela massa do sistema, obtém-se a capacidade calorífica específica, ou simplesmente calor específico, do sistema, c:
c = C
m ⇔ C = mc . (2)
De acordo com a primeira lei da termodinâmica, quando dois sistemas interagem e trocam energia, um deles ganha e o outro perde a mesma quantidade de energia. Desta forma, se os sistemas estiverem em temperaturas diferentes, a quantidade de energia trocada pode ser representada da seguinte forma:
q1 = −q2 ⇔ q1 + q2 = 0 , (3)
onde q1 é a quantidade de energia perdida pelo corpo 1 e q2 a quantidade de
energia ganha pelo corpo 2. Se substituirmos q1 e q2, teremos:
C1×(Tf−T1) = −C2×(Tf−T2) , (4)
onde C1 e C2 são as capacidades caloríficas dos sistemas 1 e 2, T1 e T2 as
temperaturas iniciais dos sistemas 1 e 2 e Tf a temperatura final (de equilíbrio).
A quantidade de calor trocada entre um sistema e o meio externo é medida por meio de um calorímetro, que é um reservatório de calor de capacidade calorífica conhecida, cujas variações de temperatura fornecem as quantidades de calor recebidas de um sistema ou transferidas para este.
H(+aq) + Cl
(aq)
- + Na
(aq)
+ + OH
(aq)
- → Na
(aq)
+ + Cl
(aq)
- + H
2O(ℓ) . (5)
Observa-se experimentalmente que reações entre soluções diluídas de ácidos fortes e bases fortes são sempre acompanhadas do mesmo efeito térmico, e este, por sua vez, é totalmente devido à formação da água. Porém, se um ácido fraco for neutralizado por uma base forte, ou vice-versa, o efeito térmico será completamente diferente. Isto ocorre devido a vários processos simultâneos: alguns são exotérmicos, como a neutralização, e outros endotérmicos, como a ionização do ácido e da base. O calor medido é a soma de todos os processos: neutralização, ionização, solvatação, diluição, entre outros.
Calor integral de dissolução é a variação de entalpia associada com a adição de certa quantidade de um soluto a uma determinada quantidade de solvente, à temperatura e pressão constantes. Exs.:
I: HCl(g) + 10H2O(ℓ) → HCl·10H2O(ℓ) ∆HI = -16,608 kcal.mol-1. (6)
II: HCl(g) + 25H2O(ℓ) → HCl·25H2O(ℓ) ∆HII = -17,272 kcal.mol-1. (7)
Os processos acima representam os calores integrais de dissolução do HCl na água, à 25 °C. A diferença entre os processos Ι e ΙΙ é a quantidade do solvente. Portanto, ∆HΙΙ - ∆HΙ representa o calor integral de diluição do HCl quando se
acrescentam 15 mols de água à solução de HCl do processo I.
A determinação do calor de neutralização e do calor integral de dissolução é feita a partir de um sistema calorimétrico, de acordo com:
ΔHr = qr
n , qr = −qcal = −CcalΔT ⇒ ΔHr =
−CcalΔT
n , (8)
onde ∆Hr e qr são a entalpia e o calor da reação (neutralização e dissolução),
respectivamente, n o número de mols neutralizados e Ccal a capacidade calorífica
do calorímetro.
M
ATERIAIS: E
QUIPAMENTOS& R
EAGENTES01 Frasco de Dewar (Garrafa Térmica/Calorímetro) de 500 mL; 01 Béquer de 200 mL + Proveta de 50 mL (ou 100 mL) + Funil; 01 Chapa Elétrica Aquecedora (ou Bico de Bunsen + Tripé de Ferro); 02 Termômetros (0-100 °C±0,5 °C);
HCl 1,0 mol/L + NaOH 1,0 mol/L (prepare-as se necessário); Nitrato de Sódio (NaNO3) ou Nitrato de Potássio (KNO3).
P
ROCEDIMENTOPARTE A: CALIBRAÇÃO DO CALORÍMETRO
100 mL de água a temperatura ambiente) constitui o calorímetro a ser utilizado em todas as demais etapas da prática.
2. Aqueça 100 mL de água destilada até ~80 °C. Coloque 50 mL da água aquecida em uma proveta e a devolva. Repita este procedimento 3 vezes de modo que a proveta entre em equilíbrio térmico com a água aquecida. Finalmente, colete 50 mL da água aquecida em uma proveta, anote a temperatura (T2) e a transfira para o interior do calorímetro.
3. Espere o equilíbrio térmico ser alcançado e anote a temperatura (Tf).
PARTE B: CALOR DE NEUTRALIZAÇÃO DE UM ÁCIDO FORTE POR UMA BASE FORTE
1. Esvazie o calorímetro e lave-o cuidadosamente (com bastante água da torneira e depois com água destilada). Em seguida, coloque 50 mL de uma solução de NaOH 1,0 mol/L no interior do calorímetro e anote a temperatura (Ti) quando esta estiver constante.
2. Pegue 50 mL de uma solução de HCl 1,0 mol/L, à temperatura conhecida e igual à do interior do calorímetro (Ti; caso as temperaturas não sejam
iguais, deve-se esperar que até que as temperaturas estabilizem até atingirem a temperatura ambiente), e coloque-a (com auxílio de um funil, se necessário) sobre a solução de hidróxido de sódio do calorímetro.
3. Agite suavemente a mistura e anote a temperatura de equilíbrio (Tf). Note
que os 100 mL de água no interior do calorímetro foram restaurados.
PARTE C: DETERMINAÇÃO DO CALOR INTEGRAL DE DISSOLUÇÃO(*)
1. Esvazie o calorímetro e lave-o cuidadosamente. Coloque 100 mL de água destilada no interior deste e anote a temperatura de equilíbrio.
2. Pese cerca de 2,5 g de NaNO3 (ou KNO3) e transfira para o interior do
calorímetro. Feche-o, homogeneíze a mistura e anote a temperatura de equilíbrio.
PARTE D: DETERMINAÇÃO DO CALOR INTEGRAL DE DILUIÇÃO(*)
1. Retire 50 mL da solução do interior do calorímetro e deixe esfriar até a temperatura inicial (ambiente). Descarte o restante da solução do calorímetro e lave-o cuidadosamente.
2. Devolva os 50 mL de solução para o calorímetro. Leia a temperatura de um em um minuto e anote a temperatura de equilíbrio.
3. Adicione 50 mL de água destilada à solução contida no calorímetro. A temperatura deve ser igual à da solução do interior do calorímetro.
4. Leia a temperatura a cada minuto e anote a temperatura de equilíbrio.
(*) Etapa opcional na disciplina de Fundamentos da Físico-Química Experimental.
T
RATAMENTO DED
ADOS2. Com os valores de temperatura obtidos na parte B e a capacidade calorífica do sistema calorimétrico, calcule o calor de neutralização (em J/mol) a partir da relação: ∆H = -Ccal∆Tcal/n, onde n é o número de mols
neutralizados.
3. Com os valores de temperatura obtidos na parte C e a capacidade calorífica do sistema calorimétrico, calcule o calor integral de dissolução do sal (NaNO3 ou KNO3).
4. Com os valores de temperatura obtidos na parte D e a capacidade calorífica do sistema calorimétrico, calcule o calor integral de diluição do sal.
5. Compare seus resultados com os da literatura. 6. Calcule o erro relativo em cada caso e discuta.
Q
UESTÕES PARA OR
ELATÓRIO1. Se a quantidade de massa de cada composto fosse reduzida à metade, o calor de dissolução também seria reduzido à metade?
2. Explique o que aconteceria, em relação ao calor de dissolução, se a quantidade de solvente fosse o dobro da que foi usada no experimento. 3. Os valores obtidos são satisfatórios?
4. Quais as possíveis fontes de erro ou limitações neste experimento? Para cada uma, tente dizer que efeito elas terão no resultado esperado dos experimentos.
B
IBLIOGRAFIA1. ATKINS, P.W.; Físico-Química, 7ª Ed., RJ, Ed. LTC, 2004.
PRÁTICA N° 7:
DETERMINAÇÃO DA ENTROPIA DE UM PROCESSO IRREVERSÍVEL
O
BJETIVOCalcular a variação de entropia para um processo irreversível.
I
NTRODUÇÃOA variação da entropia é definida por
dS ≥ dqrev
T , (1)
em que a igualdade vale para processos reversíveis e a desigualdade para processos irreversíveis. Para uma transformação finita, a variação de entropia é dada pela integral:
ΔS =
∫
1 2 dq
rev
T , (2)
que é a soma das variações de entropia para cada uma das etapas infinitesimais que compõem o processo irreversível. Sob pressão constante, o calor desenvolvido em cada etapa infinitesimal é:
dqrev = CpdT , (3)
onde dqrev é o calor trocado sob pressão constante, dT a variação de temperatura
e Cp a capacidade calorífica a pressão constante. Substituindo (3) em (2) tem-se:
ΔS =
∫
1 2 C
pdT
T = Cpln
(
T2
T1
)
, (4)que fornece a variação da entropia do processo.
O processo em estudo é a mistura de duas amostras de água a diferentes temperaturas em um calorímetro adiabático: em uma etapa procede-se o resfriamento de uma amostra de água quente, com aquecimento do conjunto calorimétrico; em uma segunda etapa promove-se o aquecimento de uma amostra de água fria, com resfriamento do conjunto calorimétrico. O calor absorvido ou cedido pelo calorímetro é dado por:
qcal = CΔT , (5)
onde C é a capacidade calorífica do sistema calorimétrico (equivalente d’água do calorímetro) e ΔT é a variação de temperatura. Devido à Primeira Lei:
M
ATERIAIS: E
QUIPAMENTOS& R
EAGENTES02 Béqueres de 200 mL; 02 Provetas de 50 mL; 02 Provetas de 100 mL;
01 Chapa Elétrica Aquecedora (ou Bico de Bunsen + Tripé de Ferro); 01 Frasco de Dewar (Garrafa Térmica/Calorímetro) de 500 mL;
02 Termômetros (0-100 °C±0,5 °C).
P
ROCEDIMENTOPARTE A: CALIBRAÇÃO DO CALORÍMETRO
1. Meça com uma proveta 100 mL de água destilada e a transfira para o calorímetro. Com um termômetro leia a temperatura da água no calorímetro a cada minuto até que esta estabilize.
2. Em um béquer de 200 mL aqueça ~100 mL de água destilada a ~90 °C. Encha uma proveta de 50 mL com a água quente e, em seguida, devolva-a para o béquer. Repita esta operação mais duas ou três vezes até que a temperatura da água na proveta atinja ~80 °C. Anote a temperatura e, em seguida, transfira os 50 mL da proveta para o calorímetro.
3. Tampe o calorímetro com uma tampa contendo um termômetro e meça a temperatura do sistema (calorímetro+água quente) a cada minuto até que esta estabilize.
PARTE B: COLETA DE DADOS
1. Esvazie o calorímetro. Novamente, meça com uma proveta 100 mL de água destilada e a transfira para o calorímetro. Com um termômetro leia a temperatura da água no calorímetro a cada minuto até que esta estabilize. 2. Em um béquer de 200 mL resfrie ~100 mL de água destilada a ~0 °C. Encha uma proveta de 50 mL com a água gelada e, em seguida, devolva-a para o béquer. Repita esta operação mais duas ou três vezes até que a temperatura da água na proveta atinja ~5 °C. Anote a temperatura e, em seguida, transfira os 50 mL da proveta para o calorímetro.
T
RATAMENTO DED
ADOS1. Procure no manual de constantes físicas e químicas a densidade e o calor específico da água a pressão constante na temperatura em que você trabalhou. A partir destes dados e da utilização da equação (6), determine a capacidade calorífica do calorímetro.
2. A partir da equação (4), encontre ∆S para o aquecimento da água fria, para o resfriamento da água quente e o ∆S total para o conjunto calorimétrico nas etapas de calibração e de coleta de dados (partes A e B do procedimento). Apresente seus resultados em unidades SI.
Q
UESTÕES PARA OR
ELATÓRIO1. Os processos de mistura (partes A e B) são espontâneos? Justifique. 2. Os valores obtidos são satisfatórios?
3. Quais as possíveis fontes de erro ou limitações neste experimento? Para cada uma, tente dizer que efeito elas terão no resultado esperado dos experimentos.
B
IBLIOGRAFIA1. ATKINS, P.W.; Físico-Química, 7ª Ed., RJ, Ed. LTC, 2004.
PARTE 2
PRÁTICA N° 1:
DETERMINAÇÃO DO VOLUME MOLAR PARCIAL
O
BJETIVODeterminar experimentalmente o volume molar parcial dos componentes de uma mistura binária.
I
NTRODUÇÃOO volume molar parcial de um constituinte em uma solução binária representa a variação de volume provocada pala adição à solução de 1 mol deste constituinte, mantendo-se constante a temperatura, a presssão e o número de mols do outro constituinte. Se o aumento do volume é pequeno em relação ao volume inicial V da solução, os volumes molales parciais V1 e V2 dos constituintes
1 e 2 são dados por:
V1 =
(
∂V∂n1
)
n2,p , Te V2 =
(
∂V
∂n2
)
n1,p , T, (1)
onde n1 e n2 são os números de mols dos constituintes 1 e 2, respectivamente. O
volume total da mistura é dado por:
V = n1V1 + n2V2 . (2)
M
ATERIAIS: E
QUIPAMENTOS& R
EAGENTES01 Balão de 10 mL (Picnômetro); 05 Balões de 25 mL;
05 Béqueres de 20 mL; 01 Balança;
NaCl puro.
P
ROCEDIMENTO1. Prepare cinco soluções de cloreto de sódio dissolvendo 0,550 g, 1,027 g, 1,612 g, 3,257 g e 4,407 g em exatamente 25,0 mL de água. Mantenha os balões volumétricos fechados para evitar evaporação.
2. Pese o picnômetro vazio e seco. Coloque água destilada pura no picnômetro até a marca do menisco. Coloque a tampa, enxugue o excesso do líquido e pese novamente. Anote a pesagem.
T
RATAMENTO DED
ADOS1. Corrija as massas obtidas para o NaCl no item 1 do procedimento (massa aparente, m) para o vácuo (massa no vácuo, m(v)), utilizando a equação:
mNacl
(v) = m
Nacl×
(
1 +ρar ρNaCl −
ρar
ρref
)
, (3)com ρar = 1,22×10-3 g/mL, ρref = 8,50 g/mL e ρNaCl = 2,17 g/mL, a 25 °C.
2. Calcule o volume do picnômetro a partir da massa de água obtida no item 2 do procedimento e da densidade da água, utilizando a equação:
Vpic = mágua
ρágua
. (4)
3. Determine a molalidade e a densidade de cada uma das 5 soluções de NaCl. As molalidades (bsol, em mol/kg: dados do item 1 do procedimento)
são calculadas pela expressão:
bsol = nNaCl
mágua =
mNaCl(v)
MNaClρáguaVágua , (5)
e as densidades (ρsol, em g/mL: dados do item 3 do procedimento):
ρsol = msol
Vpic . (6)
4. Faça um gráfico de volume de solução contendo 1.000 g (mil gramas) de solvente versus molalidade da solução e obtenha a expressão do ajuste (polinomial). O volume de solução é obtido da expressão:
Vsol = msol
ρsol , msol = mágua + mNaCl, mNaCl = MNaClmáguabsol
∴ Vsol = mágua
ρsol
(
1 + MNaClbsol)
. (7)A inclinação da tangente à curva em uma dada concentração fornece diretamente o valor de VNaCl (volume molar parcial do NaCl).(*)
(*) Nota: Isto ocorre porque, para 1.000 g de solvente, a quantidade química de sal é
numericamente igual à molalidade da solução, de modo que VNaCl = ∂Vsol/∂bsol = ∂Vsol/∂nNaCl. A inclinação é obtida da derivada da função de ajuste polinomial aos dados experimentais.
5. Determine VNaCl em várias concentrações, compare os valores e comente.
Q
UESTÕES PARA OR
ELATÓRIO1. Os valores obtidos são satisfatórios?
2. Quais as possíveis fontes de erro ou limitações neste experimento?
B
IBLIOGRAFIAPRÁTICA N° 2:
DETERMINAÇÃO DA TENSÃO SUPERFICIAL POR ASCENSÃO CAPILAR
O
BJETIVODeterminar a tensão superficial de um líquido a partir do método da ascensão capilar.
I
NTRODUÇÃOUma molécula no interior de um líquido está totalmente envolvida por outras moléculas do líquido, sendo atraída igualmente em todas as direções. Como consequência, a resultante média das forças de atração é nula. No entanto, na superfície a resultante das forças atrativas não é nula, de modo que as moléculas são puxadas para o interior do líquido, fazendo com a superfície se contraia e ocupe a menor área possível. Esta resultante de forças é a origem da tensão superficial, que tem o mesmo valor em cada ponto da superfície.
A tensão superficial, característica de cada líquido, é uma propriedade intensiva (medida no SI em N·m-1 ou kg·m·S-2m-1). É responsável pela resistência
a penetração da superfície, a forma aproximadamente esférica de gotas de água de chuva, a flutuação de lâminas metálicas sobre superfícies líquidas e a ascensão de líquidos em capilares. Há vários métodos disponíveis para a se obter a tensão superficial de um líquido, dentre os quais se destacam a balança de torsão (método de Nouy), o passo de gota (estalagmômetro de Traube), a pressão de bolha e a ascensão capilar.
Neste experimento será usado o método da ascensão capilar para a obtenção da tensão superficial de líquidos puros. Este método é baseado no fato de que muitos líquidos, quando postos em contacto com tubos capilares (geralmente de vidro), ascendem as paredes do tubo, apresentado uma superfície côncava dentro do capilar. Quando isto ocorre, diz-se que o líquido molha o tubo. Caso o líquido não molhe o tubo, como no caso do mercúrio, tem-se uma depressão capilar, com formação de uma superfície convexa.
Considere um capilar uniforme com raio interno r, imerso em um recipiente contendo um líquido de densidade ρ, que molha o vidro. Devido a tensão superficial o líquido ascende o capilar. A ascensão cessa quando a força devida à tensão superficial (para cima) se torna igual à força devida ao peso da coluna de líquido de altura h (para baixo). Da igualdade entre estas forças, conclui-se que a tensão superficial γ (gama) é dada por:
γ = 1
2ρg h r , (1)
onde g é a aceleração da gravidade.
M
ATERIAIS: E
QUIPAMENTOS& R
EAGENTES01 Régua;
01 Suporte de ferro e garra; 01 Pisseta com água destilada;
Líquidos para estudo: Água destilada, Álcool Etílico e Acetona.
P
ROCEDIMENTOPARTE A: DETERMINAÇÃO DO RAIO DO TUBO CAPILAR
1. Meça a temperatura da água. Em seguida, introduza o tubo capilar no furo da rolha de borracha existente no tubo de ensaio. Prenda o tubo de ensaio ao suporte de ferro através de uma garra.
2. Coloque água no tubo de ensaio preso ao suporte até que o nível da água esteja ~10 cm acima do traço zero do capilar (traço de referência).
3. Adapte uma seringa plástica a extremidade superior do capilar e aspire com uma pêra de borracha até encher ~2/3 da seringa. Retire a seringa e esvazie seu conteúdo. Repita o procedimento até que todo o capilar esteja limpo, o que é evidenciado por um brilho metálico.
4. Com o capilar limpo, acrescente ou retire água do tubo de ensaio até que o nível da superfície da água coincida com o traço zero do capilar.
5. Insira água com a seringa pela parte superior do capilar até que o mesmo atinja o nível mais alto do capilar. Depois, retire suavemente a seringa e observe a descida da água através do capilar. Anote o traço do capilar que mais se aproxime do nível da água dentro do capilar.
6. Retire suavemente o capilar e, com o auxílio de uma régua, meça a altura, que vai do zero do capilar até o traço anotado no item anterior.
7. Repita o procedimento de três a cinco vezes e obtenha o valor médio da altura da ascensão capilar.(*)
(*) Alternativa: caso ocorram dificuldades de leitura da ascensão capilar a partir do
procedimento descrito acima, utilize um outro capilar e um béquer contendo o líquido de estudo, tendo o cuidado de tomar a leitura a partir da superfície do líquido no béquer até o topo da coluna de líquido no capilar.
8. Utilize a equação (1) para calcular o raio interno do capilar. Considere tabela a seguir, referente à água:
Temperatura (°C)
Densidade
(kg·m-3) Tensão γ
(mN·m-1)
25 997,08 71,99
30 995,68 71,20
35 994,63 70,41
PARTE B: DETERMINAÇÃO DA TENSÃO SUPERFICIAL DE UM LÍQUIDO
T
RATAMENTO DED
ADOS1. Utilize a equação (1), com o valor médio da ascensão capilar obtido para a água na parte A, bem como os dados de densidade e tensão superficial na temperatura do experimento, para calcular o raio r do tubo capilar. Considere a aceleração da gravidade como 9,8 m·s-2.
2. Utilize a equação (1), com o raio r determinado anteriormente, bem como o valor médio da ascensão capilar determinado na parte B, para calcular a tensão superficial γ do líquido de estudo.
3. Compare os valores com os da literatura e comente.
Q
UESTÕES PARA OR
ELATÓRIO1. Os valores obtidos são satisfatórios?
2. Quais as possíveis fontes de erro ou limitações neste experimento? Para cada uma, tente dizer que efeito elas terão no resultado esperado dos experimentos.
B
IBLIOGRAFIA1. ATKINS, P.W.; Físico-Química, 7ª Ed., RJ, Ed. LTC, 2004.
PRÁTICA N° 3:
DETERMINAÇÃO DA VISCOSIDADE DE UM LÍQUIDO C/ VISCOSÍMETRO DE OSTWALD
O
BJETIVODeterminar a viscosidade relativa e a viscosidade absoluta de um líquido puro, usando um viscosímetro de Ostwald.
I
NTRODUÇÃOLíquidos e gases possuem uma propriedade conhecida como viscosidade, que pode ser concebida como a resistência ao escoamento. Esta resistência é devida ao atrito interno que surge devido ao movimento relativo de camadas adjacentes do fluído (gás ou líquido). Esta propriedade é expressa quantitativamente através de um índice chamado coeficiente de viscosidade ou simplesmente viscosidade, η (eta, medida no SI em poise ou g·cm-1s-1; lê-se
poási).
Há diversos métodos experimentais para se determinar a viscosidade de líquidos, tais como queda de esferas sólidas através de líquidos (viscosímetro de Hoppler) e escoamento através de tubos capilares (viscosímetro de Ostwald). Neste experimento, a viscosidade relativa de um líquido será encontrada através do uso de um viscosímetro de Ostwald. O princípio do método é baseado na equação de Poiseville, para o coeficiente de viscosidade absoluta de um fluído:
η = πp r
4t
8ℓ V , (1)
onde p é a pressão hidrostática exercida pelo fluido de volume V, que escoa em um tempo t através de um tubo capilar de raio interno r e comprimento ℓ.
Considerando-se um líquido de viscosidade conhecida como padrão (η1),
pode-se determinar a viscosidade de um líquido desejado (η2) a partir do tempo
de escoamento de um volume fixo de líquido através de um determinado capilar. De acordo com a equação de Poiseville, a razão entre as viscosidades dos dois líquidos (viscosidade relativa do líquido “2” em relação ao líquido “1”, η(2,1)) é
dada por:
η(2,1) =
η2
η1 =
(
πp2r4
t2 8ℓV
)(
8ℓV πp1r
4
t1
)
= p2t2
p1t1 = ρ2t2
ρ1t1 ⇒ η2 =
(
ρ2t2
ρ1t1
)
η1 , (2)esta última expressão sendo devida a proporcionalidade entre a pressão p e a densidade ρ dos líquidos. Portanto, conhecendo-se a viscosidade η1 de um líquido
padrão e as densidades ρ1 e ρ2 dos líquidos, a medida experimental dos tempos
de escoamento t1 e t2 de um volume fixo de líquido em um dado capilar permite
determinar a viscosidade η2 do fluido de interesse.
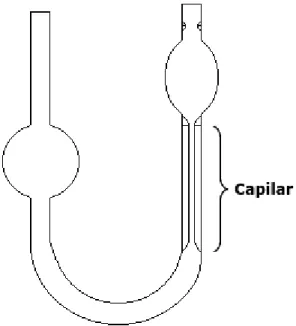
outro ramo é constituído por um tubo de diâmetro maior, tendo uma grande dilatação próxima a parte inferior.
Figura 1: Viscosímetro de Ostwald.
M
ATERIAIS: E
QUIPAMENTOS& R
EAGENTES01 Viscosimetro de Ostwald; 01 Suporte com garra; 01 Pêra de borracha; 01 Cronômetro; 01 Termômetro 01 Pipeta; 02 Béqueres; 01 Pisseta;
Líquidos para estudo: Água destilada, Álcool Etílico e Acetona.
P
ROCEDIMENTOPARTE A: DETERMINAÇÃO DO TEMPO DE ESCOAMENTO DO PADRÃO
1. Meça a temperatura de uma amostra de água destilada. Em seguida, introduza certo volume de água destilada no ramo não-capilar do viscosímetro, de modo que o tubo fique cheio até 1/3. O nível do líquido deverá ficar abaixo da extremidade inferior do capilar, contido no outro ramo do viscosímetro.
superior. Reproduza sempre esta mesma posição em todas as medidas subsequentes.
3. Observe a descida do líquido e inicie a contagem do tempo no momento em que a superfície livre da água passe pelo traço de referência superior. Esta observação deve ser realizada colocando-se a visão no plano horizontal do traço de referência. Da mesma forma, desligar o cronômetro quando a superfície livre da água atingir o traço de referência inferior. 4. Repetir a operação 3 vezes, anotando os tempos medidos. Se o aparelho
estiver convenientemente limpo, os tempos não devem diferir de mais do que 0,2 %. Calcule a média dos tempos de escoamento. Denomine esta média de t1 para o líquido padrão.
5. Meça novamente a temperatura do líquido em estudo. Encontrar a média aritmética entre as temperaturas inicial e final. Esta será considerada a temperatura do experimento.
PARTE B: DETERMINAÇÃO DO TEMPO DE ESCOAMENTO DO LÍQUIDO DE INTERESSE
1. Repita o procedimento anterior para o líquido de interesse e obtenha o tempo de escoamento médio t2.
T
RATAMENTO DED
ADOS1. Calcule a viscosidade relativa (η(2,1)) e absoluta (η2) do líquido de interesse
a partir da equação (2), considerando os tempos de escoamento médio t1 e
t2 determinados e a tabela a seguir, referente à água:
Temperatura (°C)
Densidade
(kg·m-3) Viscosidade η
(μPa·s)
25 997,08 890,3
30 995,68 797,5
35 994,63 719,5
2. Compare os valores com os da literatura e comente.
Q
UESTÕES PARA OR
ELATÓRIO1. Os valores obtidos são satisfatórios?
2. Quais as possíveis fontes de erro ou limitações neste experimento? Para cada uma, tente dizer que efeito elas terão no resultado esperado dos experimentos.
B
IBLIOGRAFIA1. ATKINS, P.W.; Físico-Química, 7ª Ed., RJ, Ed. LTC, 2004.
PARTE 3
PRÁTICA N° 2:
DETERMINAÇÃO DA ORDEM DE REAÇÃO PELO MÉTODO DAS VELOCIDADES INICIAIS
O
BJETIVODeterminar a ordem da reação de oxidação do iodeto de potássio pelo persulfato de potássio através do método das velocidades iniciais.
I
NTRODUÇÃONeste experimento será estudada a reação (qual a equação iônica?) do iodeto de potássio (KI) com o persulfato de potássio (K2S2O8):
2 KI(aq) + K2S2O8(aq) → I2(aq) + 2 K2SO4(aq). (1)
A velocidade inicial da reação pode ser medida trabalhando-se com uma concentração baixa (por que baixa?) e conhecida de íons tiossulfato (S2O32–), com
formação de íons tetrationato (S4O62–):
2 S2O32–(aq) + I2(aq) → 2I–(aq) + S4O62–(aq). (2)
Esta reação é muito mais rápida que a primeira, que prossegue consumindo o iodo gerado na reação (1) até que todo tiossulfato tenha sido convertido em tetrationato. Quando isto ocorre, a mínima quantidade de iodo adicional, gerada pela reação (1), na presença do iodeto que ainda não reagiu, leva à formação de I3–, que pode ser revelado através do indicador amido. O intervalo de tempo
decorrido entre o início da reação e a mudança na coloração da solução é uma medida da velocidade inicial da reação.
A lei de velocidade desta reação, à temperatura e força iônica constantes, pode ser escrita como:
v = −d[S2O8
2–]
dt = k[S2O8
2–
]m[I-]n , (3) onde m e n são as ordens de reação em relação ao persulfato (S2O82–) e ao iodeto
(I–), respectivamente. Nesta prática, utilizaremos o método da velocidade inicial
para encontrar m e n. Este método consiste na medição da velocidade de reação após um período de tempo curto o bastante para que a reação não tenha ocorrido apreciavelmente, mas longo o suficiente para que a velocidade não seja afetada pelo tempo de mistura dos reagentes. (Que complicações teríamos se esta reação fosse monitorada por um período de tempo mais longo?) Para um dado conjunto de condições iniciais, mede-se o intervalo de tempo (Δt) entre o início da reação e o aparecimento de uma coloração azul característica, correspondente à formação pela reação (1) de uma quantidade fixa de iodo (Δ[I2]), que é determinada pela quantidade de tiossulfato utilizada na reação (2).
A taxa de formação do iodo é igual à taxa de consumo do perssulfato e, portanto, à velocidade da reação.